Sintesis Nanotube Karbon melalui Reaksi Dekomposisi Katalitik
Metana dengan Katalis Fe/Mo/MgO pada Reaktor Katalitik
Terstruktur
Widodo W. Purwanto*, Praswasti PDK Wulan, Bernadet Valentine
Departemen Teknik Kimia, Universitas Indonesia, Depok, Indonesia *E-mail: widodo@che.ui.ac.id
A B S T R A K
Sintesis nanotube karbon jenis Single Walled Nanotube Carbon (SWNT) dan Few Walled
Nanotube Carbon (FWNT) masih sulit untuk dilakukan. Salah satu penyebab utama
adalah katalis yang kurang tepat. Penelitian ini menggunakan katalis Fe/Mo/MgO untuk menghasilkan SWNT atau FWNT (diameter luar nanotube karbon kurang dari 10 nm). Katalis Fe/Mo/MgO dipreparasi dengan metode sol gel/spray coating. Nanokarbon akan dihasilkan melalui reaksi dekomposisi katalitik metana pada suhu 850oC. Hasil penelitian menunjukkan konversi metana tertinggi mencapai 97,64% dan yield karbon sebesar 1,48 gC/gkat. Nanokarbon kemudian dikarakterisasi dengan Transmission
Electron Microscope (TEM). Nanokarbon yang dihasilkan terdiri atas nanotube karbon
jenis FWNT (diameter luar 4,5 nm – 10 nm) dan Multi Walled Nanotube Carbon (MWN) dengan diameter luar 10 nm – 89,5 nm, carbon nanofiber, coil nanotube, dan
bamboo-shaped carbon juga telah dihasilkan. Jenis nanokarbon yang dihasilkan bukan hanya
jenis nanotube karbon disebabkan oleh waktu reaksi yang terlalu panjang serta diameter partikel katalis 20 nm hingga 100 nm yang terdeteksi dari hasil X-Ray
Diffraction (XRD) dan Field Emmision Scanning Electron Microscope (FE SEM).
Kata kunci: FWNT, katalis Fe/Mo/MgO, MWNT, sol gel/spray coating, reaksi
dekomposisi katalitik metana
1. Pendahuluan
Aplikasi nanotube karbon di berbagai bidang seperti listrik dan elektronik, material komposit maupun polimer, kesehatan, serta energi terbarukan seperti penyimpanan gas hidrogen telah menarik banyak perhatian industri global untuk memproduksi nanotube karbon pada skala industri [1]. Berdasarkan prediksi yang dilakukan oleh Freedonia [2], total permintaan nanotube karbon jenis Single-walled nanotubes
(SWNT) maupun Multi-walled nanotubes (MWNT) dapat mencapai US$ 1.070 juta di tahun 2014. Kedua jenis nanotube karbon tersebut juga sangat mendominasi permintaan industri [3]. Oleh
karena itu, produksi SWNT maupun FWNT untuk produksi skala pilot sangat menjanjikan untuk dikembangkan.
Penelitian mengenai produksi nanotube karbon skala pilot melalui reaksi dekomposisi katalitik metana telah dikembangkan oleh Departemen Teknik Kimia Universitas Indonesia (DTK UI) sejak tahun 2009. Namun, beberapa penelitian yang telah dilakukan belum berhasil menghasilkan nanotube karbon jenis SWNT atau FWNT (berdiameter kurang dari 10 nm). Hal ini disebabkan pemilihan serta preparasi katalis yang kurang tepat. Penelitian di DTK UI menggunakan katalis Ni/Cu/Al2O3 [4] tetapi rekonstruksi katalis
MN-09
204 ISBN 978-979-98300-2-9
terjadi saat bereaksi dengan reaktan metana di suhu 700oC sehingga katalis tidak bekerja dengan optimal [5]. Sedangkan, penelitian Manggiasih [6] menggunakan katalis Fe/MgO belum berhasil menghasilkan SWNT maupun MWNT karena perilaku reduksi yang terlalu lama menyebabkan aglomerasi partikel Fe [7]. Oleh karena itu, kedua katalis tadi tidak lagi digunakan.
Berdasarkan beberapa penelitian tentang sintesis nanotube karbon, katalis Fe/Mo/MgO merupakan katalis yang sangat baik dalam mensintesis nanotube karbon jenis SWNT atau FWNT. Salah satu penelitian yang berhasil membentuk nanotube karbon seperti SWNT dengan diameter di bawah 3 nm adalah penelitian Qian et al [8]. Hal ini disebabkan dispersi Fe nanopartikel (NPs) di dalam katalis sangat merata akibat penambahan logam Mo sehingga mencegah partikel Fe mengalami aglomerasi di suhu tinggi [8-9]. Selain itu, kombinasi katalis FeMo dapat membentuk diameter partikel katalis kurang dari 5 nm sehingga pembentukan MWNT dapat dihindari [8]. Penggunaan Mo juga membantu memudahkan aromatisasi karbon dalam membentuk nanotube karbon dengan membentuk prekursor intermediet [9]. Maka, katalis Fe/Mo/MgO digunakan pada penelitian ini.
Selain pemilihan katalis, preparasi katalis meliputi temperatur kalsinasi, perilaku reduksi, serta temperatur reaksi juga memengaruhi diameter katalis yang terbentuk. Temperatur reaksi yang digunakan adalah 850oC. Hal ini disebabkan temperatur ini merupakan temperatur yang sangat baik untuk katalis Fe/Mo/MgO dapat menghasilkan SWNT melalui reaksi dekomposisi katalitik metana [9]. Perilaku reduksi dilakukan untuk menghasilkan partikel Fe np sebagai inti aktif untuk menghasilkan nanotube karbon [10].
Penelitian terhadap perilaku reduksi serta kalsinasi dilakukan pada penelitian ini karena perubahan ukuran partikel katalis yang akan memengaruhi ukuran nanokarbon yang dihasilkan. Selain itu, jenis dan diameter ukuran diameter luar nanokarbon juga diamati melalui
karakterisasi yang dilakukan. Penelitian ini diharapkan menghasilkan nanotube karbon sejenis FWNT atau SWNT.
2. Metode Penelitian
2.1 Preparasi Katalis Fe/Mo/MgO
Metode sintesis katalis yang dilakukan menggunakan metode sol gel untuk katalis Fe/Mo/MgO dengan komposisi molar 1/0,1/13 [11]. Prekursor Fe(NO3)3.9H2O, (NH4)6Mo7O24.4H2O, Mg(NO3)2.H2O, asam sitrat, dilarutkan dalam deionized water dengan komposisi berat 1,23:0,07:10:5,84:5. Larutan diaduk hingga menjadi gel pada suhu 90oC. Kemudian katalis dikalsinasi pada suhu 550oC selama 1 jam.
2.2 Persiapan Wiremesh SS 316 dan Pelapisan Katalis Fe/Mo/MgO
Wiremesh yang akan digunakan disonikasi
selama 10 menit terlebih dahulu dengan aseton untuk menghilangkan pengotor. Kemudian, dibilas dengan deionized water. Selanjutnya, wiremesh SS 316 direndam dengan asam (%v/v asam nitrat 2 M : asam klorida 2 M = 1 : 2) selama 1 jam). Wiremesh kemudian dibilas dengan deionized
water sekali lagi dan ditimbang pada keadaan
kering (Wo).
Pelapisan katalis pada wiremesh dilakukan dengan metode spray coating [12]. Katalis Fe/Mo/MgO dilarutkan dalam isopropanol dengan konsentrasi 0,15 g/ml. Larutan katalis disemprotkan ke penyangga wiremesh yang telah dipanaskan pada suhu 350oC selama 1 jam. Pelapisan dilakukan berulang-ulang hingga
loading katalis dapat tercapai.
2.3 Set up reaktor
Peralatan yang digunakan untuk reaksi dekomposisi katalitik metana terdiri atas tabung gas metana, mass flow controller, check valve,
needle valve, pressure gauge, quartz reaktor,
bubble soap, GC TCD dan GC FID, serta fiber glass
filter dengan filter holder 47 mm (Pall
Corporation) dihubungkan seperti pada Gambar 1.
205 ISBN 978-979-98300-2-9
GC TCD CH4 Pressure Regulator Bubble Soap To vent Needle Valve Needle Valve Needle Valve MFC Filter Reaktor katalis terstruktur Tube Furnace
Gambar 1. Skema rangkaian peralatan 2.4 Kalsinasi, Reduksi, dan Reaksi Dekomposisi Katalitik Metana
Katalis yang telah dilapiskan pada
wiremesh kemudian dikalsinasi kembali dalam
furnace pada suhu 850oC. Kemudian, wiremesh
dimasukkan ke dalam reaktor katalitik terstruktur. Reaktor dipanaskan hingga suhu 850oC. Kemudian, gas hidrogen dialirkan dengan laju 30 L/jam selama 10 menit untuk reduksi. Setelah itu, gas hidrogen diganti dengan gas metana yang dialirkan dengan laju 160 L/jam selama 70 menit.
Setelah reaksi dekomposisi katalitik metana selesai, suhu reaktor diturunkan hingga suhu ruangan. Kemudian, jumlah karbon yang terdeposit di atas wiremesh setelah reaksi selesai dihitung menggunakan persamaan (1).
ܿܽݎܾ݊ݕ݈݅݁݀ ൌ ೌೝି್
್ೝ (1)
Dimana mar merupakan massa wiremesh setelah
reaksi, mb massa katalis dengan wiremesh
sebelum reaksi, dan mbr massa fresh katalis yang
dimasukkan ke reaktor.
Sedangkan, konversi metana pada waktu tertentu (sesaat) dihitung dengan menggunakan rumus berikut.
Ψ݇݊ݒ݁ݎݏ݅ ൌுరିுరೠ
ுర ൈ ͳͲͲΨ (2)
Dimana V merupakan laju alir metana dalam L/jam.
2.5 Karakterisasi Katalis Fe/Mo/MgO
Karakterisasi katalis Fe/Mo/MgO dilakukan dengan alat X-Ray Diffraction (XRD),
Shimadzu 7000, CuKα = 0,1541 nm). Untuk mengetahui ukuran kristal dari katalis dapat digunakan rumus Schrerrer pada persamaan 3.
ܦሺ݊݉ሻ ൌ௦ఏǡଽఒ (3)
Dimana B merupakan Full Width at Half Maximum
(FWHM) pada data XRD, ߣ merupakan panjang gelombang yang digunakan dalam nanometer, ߠ merupakan sudut pada peak oksida yang ditunjukkan pada gambar, dan D merupakan diameter kristal yang terhitung.
Karakterisasi SEM dilakukan di Laboratorium BATAN Serpong. Karakterisasi Field
Emission Scanning Electrone Microscope (FE SEM)
dilakukan dilakukan di Laboratorium Metalurgi UI Depok.
2.6 Karakterisasi Nanotube Karbon
Nanokarbon yang dihasilkan dikarakterisasi dengan XRD, FE SEM, dan
Transmission electron microcope (TEM) di
Universitas Gajah Mada Yogyakarta.
3. Hasil dan Pembahasan 3.1 Pengaruh Kalsinasi
Kalsinasi dapat mengubah struktur katalis dengan pembentukan oksida logam serta perubahan ukuran kristal. Hasil XRD katalis Fe/Mo/MgO ditunjukkan pada Gambar 2. Keberadaan oksida MgO berfungsi membantu dispersi inti aktif katalis dan oksida Fe3O4 juga yang merupakan sumber inti aktif Fe sebelum direduksi dengan hidrogen [8].
206 ISBN 978-979-98300-2-9
Gambar 2. Karakterisasi XRD Katalis Fe/Mo/MgO
Hasil XRD katalis setelah reduksi dengan hidrogen pada suhu 850oC pada Gambar 2 menunjukkan adanya puncak FeMoO4 bukan fasa logam Fe atau Mo. Hal ini disebabkan fasa FeMoO4 merupakan fasa yang sangat stabil sehingga sulit direduksi oleh gas H2 dalam waktu yang sangat singkat [8]. Fasa ini juga memungkinkan terbentuknya Fe NP sehingga diameter nanotube karbon yang kecil seperti SWNT atau FWNT lebih mudah terbentuk.
Berdasarkan hasil karakterisasi SEM pada Gambar 3(a), ukuran partikel dari katalis sebelum mengalami reduksi 18 nm hingga 56 nm. Hal ini menunjukkan bahwa diameter partikel katalis yang dihasilkan setelah kalsinasi memiliki ukuran yang bervariasi. Variasi ukuran ini terjadi karena adanya variasi ukuran kristal Fe3O4 dan MgO. Ukuran partikel katalis yang membesar ini disebabkan sintering partikel katalis membentuk ukuran yang lebih besar [13].
3.2 Pengaruh Reduksi
Pada Gambar 3 (b), ukuran partikel katalis Fe/Mo/MgO setelah direduksi justru mengalami perubahan diameter dari 20 nm hingga lebih dari 100 nm (mencapai lima kali dari semula). Hal serupa juga terjadi pada katalis Fe2O3/SiO2, dengan reduksi oleh gas hidrogen [14].
(a)
(b)
Gambar 3. Hasil SEM Katalis Fe/Mo/MgO metode A (a) setelah kalsinasi 850oC (b) sebelum
reduksi
Hal ini dapat terjadi karena adanya penggabungan katalis pada saat reduksi untuk membentuk partikel yang lebih besar terjadi karena adanya partikel katalis yang bergerak mendekati partikel katalis yang lain pada suhu tinggi (Gambar 4). Selanjutnya, partikel dapat berada dalam keadan meleleh sehingga sangat mudah melebur untuk membentuk partikel yang lebih besar. Hal ini dapat terjadi tergantung pada suhu yang digunakan. Reduksi partikel Fe pada sebelum reaksi dilakukan pada suhu 850oC (1123oK). Fenomena pada Gambar 3 (b) dapat dijelaskan melalui Gambar 4 (c) dimana partikel Fe cenderung mengalami penggabungan dengan partikel Fe lain dan membentuk partikel Fe dengan ukuran yang lebih besar .
207 ISBN 978-979-98300-2-9
Gambar 4. Pergerakan partikel Fe pada suhu (A) 500 K (B) 800 K (C) 1200 K (D) 1400K (E) 1460 K [15]
Fungsi promoter Mo dalam katalis Fe/Mo/MgO adalah dapat mencegah partikel Fe mengalami sintering untuk membentuk partikel katalis yang lebih besar [5] belum terlihat pada penelitian ini. Penyangga MgO yang dapat membantu dispersi katalis Fe dan Mo yang baik di dalam katalis Fe/Mo/MgO juga belum terlihat dengan baik [17]. Hal ini disebabkan dispersi katalis Fe/Mo/MgO kurang baik pada saat preparasi sehingga katalis tidak berada dalam keadaan yang optimal untuk menghasilkan nanotube karbon.
3.3 Hasil Nanokarbon yang terbentuk 3.3.1 Karakterisasi XRD
Hasil XRD yang dilakukan pada katalis yang telah ditumbuhi nanotube karbon ditunjukkan pada Gambar 5.
Gambar 5. Hasil XRD katalis Fe/Mo/MgO yang telah ditumbuhi nanotube karbon
Keberadaan nanotube karbon (C 0 0 2) ditunjukkan pada peak 2ߠ = 26,34o pada Gambar 6 [18]. Berdasarkan perhitungan rumus Scherer, diameter luar nanotube karbon yang terbentuk adalah 6,2 nm. Keberadaan peak Mo2C pada Gambar 5 menunjukkan fungsi Mo pada membantu aromatisasi metana dan Fe-Carbida menunjukkan bahwa Fe berperan dalam perengkahan katalitik metana [9].
3.3.2 Karakterisasi TEM
Hasil nanokarbon yang diperoleh dari karakterisasi TEM ditunjukkan pada Gambar 6 dan 7.
Gambar 6. Hasil TEM nanokarbon (skala 50 nm)
208 ISBN 978-979-98300-2-9
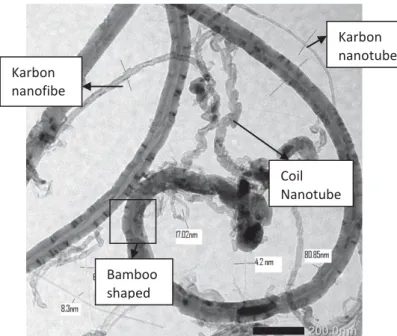
Hasil TEM pada Gambar 6 menunjukkan adanya nanotube karbon berukuran 4,5 nm hingga 89,5 nm. Tipe nanokarbon yang dihasilkan (Gambar 7), yaitu tipe bamboo shaped yang menyerupai nanokarbon, coil nanotube carbon, serta carbon
nanofiber.
Gambar 7. Hasil TEM nanokarbon (skala 200 nm)
Diameter nanotube karbon yang kecil (<10 nm) masih dapat teridentifikasi dalam hasil penelitian ini. Hal ini disebabkan keberadaan oksida FeMoO4 yang terdeteksi pada XRD saat katalis telah mengalami reduksi [8]. Oksida yang stabil ini dapat membuat katalis Fe maupun Mo dapat tereduksi perlahan-lahan saat bereaksi dengan metana [8]. Akibatnya, Fe akan sulit mengalami agregasi menjadi partikel yang besar sehingga diameter nanotube karbon yang dihasilkan akan menjadi kecil.
Nanotube karbon dengan diameter 10 nm hingga 90 nm memiliki porsi yang terbesar pada hasil penelitian ini. Hal ini disebabkan ukuran partikel katalis yang dihasilkan juga sebesar 20 hingga 100 nm. Fenomena ini sesuai dengan korelasi diameter nanotube karbon yang dihasilkan dengan diameter nanotube karbon yang dihasilkan. Karena, ukuran diameter partikel katalis yang dihasilkan pada penelitian ini juga sekitar 20 nm hingga 100 nm setelah reduksi dari
hasil karakterisasi ukuran partikel pada FE SEM dapat menghasilkan diameter nanotube karbon hingga mencapai 4 hingga 89,5 nm.
Salah satu parameter operasi yang juga berpengaruh terhadap jenis nanokarbon yang dihasilkan adalah waktu reaksi. Hasil nanotube karbon yang bervariasi pada penelitian ini berdasarkan pengamatan pada TEM juga disebabkan oleh pengaruh waktu reaksi yang terlalu lama, yaitu 70 menit. Berdasarkan penyelidikan terhadap pengaruh waktu reaksi [11] dengan katalis Fe/Mo/MgO pada suhu reaksi 850oC terhadap jenis nanotube karbon yang dihasilkan, waktu optimal untuk menghasilkan nanotube karbon berdiameter kurang dari 3 nm adalah 30 menit. Jika waktu reaksi melebihi 30 menit, hasil nanokarbon berupa nanofiber dan karbon amorf akan semakin meningkat sehingga nanotube karbon berdiameter seperti SWNT hanya sedikit yang dihasilkan. Hal ini disebabkan sisi aktif dari katalis telah tertutup tetapi reaksi dekomposisi metana tetap terjadi.
Berdasarkan Gambar 8, pertumbuhan nanotube karbon pada katalis mengikuti base
growth mechanism dimana nanotube karbon
tumbuh memanjang dari katalis [20]. Inti aktif memanjang mengikuti nanotube karbon yang tumbuh pada katalis.
Gambar 8. Hasil FE SEM pertumbuhan nanotube karbon pada katalis
3.3.3 Perhitungan yield karbon dan konversi metana sesaat Coil Nanotube Karbon nanofibe Bamboo shaped Karbon nanotube 209 ISBN 978-979-98300-2-9
Hasil konversi gas metana sesaat menjadi produk karbon (solid) dan gas hidrogen ditunjukkan pada Gambar 9.
Gambar 9. Konversi sesaat gas metana pada menit tertentu
Total karbon yang terdeposisi pada reaktor adalah 19,6 gram. Yield karbon yang dihasilkan pada katalis ini adalah sebesar 1,48 gC/gkat. Berdasarkan kurva vulcano pada reaksi dekomposisi katalitik metana, perbedaan yield
karbon yang signifikan dari katalis Ni/Cu/Al2O3 dengan katalis Fe/Mo/MgO atau katalis Fe/MgO terletak pada keaktifan katalis dalam reaksi dehidorgenasi. Katalis Ni jauh lebih aktif dibandingkan dengan katalis Fe maka katalis Ni akan menghasilkan yield karbon yang jauh lebih banyak. Konversi metana tertinggi yang dihasilkan mencapai 97,64%.
4. Kesimpulan
Reaksi dekomposi katalitik metana dengan katalis Fe/Mo/MgO menghasilkan diameter luar nanotube karbon yang ingin dicapai pada tujuan penelitian, yaitu nanotube karbon yang memiliki diameter luar kurang dari 10 nm (FWNT) tetapi hasil nanotube karbon tidak murni karena adanya MWNT (diameter luar di atas 10 nm hingga 90 nm), carbon nanofiber, coil
nanotube, dan nanokarbon berbentuk
bamboo-shaped. Hal ini terjadi disebabkan ukuran partikel
katalis setelah reduksi yang berkisar antara 20 nm hingga 100 nm hampir sama dengan ukuran diameter luar nanotube karbon yang terbentuk, yaitu 4 nm hingga 90 nm. Selain itu, waktu reaksi yang terlalu lama (70 menit) juga dapat menghasilkan nanokarbon berdiameter yang besar. Yield karbon yang dihasilkan pada penelitian ini sebesar 1,48 gc/gkat. Konversi metana tertinggi 97,64%.
Ucapan Terima Kasih
Kami ucapkan terima kasih pada Direktorat Riset dan Pengabdian Pada Masyarakat Universitas Indonesia yang telah mendanai penelitian ini melalui Hibah Madya UI 2012 Nomor: 2192/H2.R12/HKP.05.00/2012.
Daftar Referensi
[1] Daenen, J.M., Fouw, R., Hamers, B., Janssen, P. G.A., Schouteden, K., dan Veld, M.A.J, 2003, Wondrous world of carbon nanotubes,
http://students.chem.tue.nl/ifp03/default.h tm.
[2] Freedonia, 2009, World nanotubes to 2009 – Market research, market share, market size, market leaders, company profiles,
industry trends,
www.freedoniagroup.com/World-Nanotubes.html.
[3] Global Industry Analyst, Inc, 2007, Global
carbon nanotubes market to exceed US$ 1,9
billion by 2010,
www.prweb.com/releases/carbon_nanotub es/prweb540780.htm.
[4] Francy, 2009, Scale-up Reaktor Katalis Terstruktur Gauze Skala Pilot untuk Produksi Hidrogen dan Nanokarbon Melalui
Reaksi Dekomposisi Katalitik Metana,
Departemen Teknik Kimia - Universitas Indonesia, Depok.
[5] Li, D., Chen, J., dan Li, Yongdan, 2009, Evidence of composition deviation of metal particles of a Ni-Cu/Al2O3 catalyst during 0 20 40 60 80 100 120 Konv er si g as me tana se saa t (% ) Waktu (menit) 210 ISBN 978-979-98300-2-9
methane decomposition to Cox-free hydrogen, Int J. Hydrogen Energy, 34, 299 – 307.
[6] Manggiasih, A, 2011, Perbandingan Kinerja Katalis Terstruktur Fe dan Ni Berpenyangga MgO Untuk Sintesis Nanotube Karbon Melalui Reaksi Dekomposisi Katalitik
Metana, Departemen Teknik Kimia -
Universitas Indonesia, Depok.
[7] Ago, H., Uehara, N., Yoshihara, N., Tsuji, M., Yumura, M. Tomonaga, N., dan Setoguchi, T., 2006, Gas analysis of the CVD process for high yield growth of carbon nanotubes over metal-supported catalysts, Carbon, 44, 2912–2918.
[8] Qian, W., Weizhong, Q., dan Fei, W, 2008, Synthesis of single-walled carbon nanotubes with narrow diameter by calcination of a Mo-modified Fe/MgO catalyst, Chin J Catal., 29 (7), 617 – 623. [9] Ni, L., Keiji, K., Zhou, L., Ohta, K., Matsuishi,
K., dan Nakamura, J, 2009, Decomposition of metal carbides as an elementary step of carbon nanotubes synthesis, Carbon, 44, 3054 – 3062.
[10] Li, Y., Zhang, X., Shen, L., Luo, J., Tao, X., Liu, F., Xu, G., Wang, Y., dan Geishe, V. T. , 2006, Controlling the diameters in large-scale synthesis of single-walled carbon nanotubes by catalytic decomposition of
CH4, Chem Lett, 398, 276-282.
[11] Fang, Y. dan Niu, Z., 2004, Effects of synthesis time for synthesizing single-walled carbon nanotubes over Mo-Fe-MgO catalyst and suggested growth mechanism,
J Cryst Growth, 297, 228 – 233.
[12] Fang, M., 2003, Sintesis membran perovskite dengan menggunakan Katalis
La0,8NixFeyO1-x-y dengan metode
Impregnasi/Spray Coating, Departemen
Teknik Kimia - Universitas Indonesia, Depok.
[13] Richarson, J.T., 1989, Principles of catalyst
development, Plenum Press, New York.
[14] Moodley, P., Loos, J., Niemantsverdriet, J.W., dan Thu, P.C., 2009, Is there a correlation between catalyst particle size and CNT diameter? Carbon, 47, 2003-2012. [15] Ding, F., Rosen, A., dan Bolton, K., 2004,
Size dependence of the coalescence and melting of iron clusters: A molecular-dynamics study, Phys Rev B, 70, 075416. [16] Lamouroux, E.,Serp, P.,Klack, P., 2007,
Catalytic routes towards single wall carbon nanotubes, Catal Rev, 49, 341–405.
[17] Ning, Q., Wei, F., Wen, Q.,Luo, G., Wang, Y., dan Jin, Y, 2006, Improvement of Fe/MgO catalysts by calcination for the growth of single- and double- walled carbon nanotubes, J Phys Chem, B (110), 1201 – 1205.
[18] Xu, X., Huang, S., Yang, Z., Zhou, C., Jiang, J., Shang, Z., 2011, Controllable synthesis of carbon nanotubes by changing the Mo content in bimetallic Fe-Mo/MgO catalyst,
Mat Chem Phys, 127, 379 – 384.
[19] Coquay, P., Grave, D.E., Peigney, A., Vandenberghe, R.E., dan Laurent, C, 2002, Carbon nanotubes by a CVD method part I: Synthesis and characterization of the (Mg, Fe)O catalysts, J Phys Chem B, 106, 13186-13198.
[20] Chen, Y., Conway, M.J., FitzGerald, J.D., Williams, J.S., dan Chadderton, L.T., 2004, The nucleation and growth of carbon nanotubes in a mechano-thermal process.
Carbon, 42, 1543.
211 ISBN 978-979-98300-2-9