BAB 2
TINJAUAN PUSTAKA
2.1. Beras (Oriza sp)
Beras merupakan butir padi yang telah dibuang kulit luarnya (sekamnya)
yang menjadi dedak kasar. Beras adalah gabah yang bagian kulitnya sudah
dibuang dengan cara digiling dan disosoh menggunakan alat pengupas dan
penggiling serta alat penyosoh. Beras secara biologi adalah bagian biji padi yang
terdiri dari :
• aleuron, lapis terluar yang sering kali ikut terbuang dalam proses
pemisahan kulit.
• endospermia, tempat sebagian besar pati dan protein beras berada, dan
embrio, yang merupakan calon tanaman baru (dalam beras tidak dapat tumbuh
lagi, kecuali dengan bantuan teknik kultur jaringan). Dalam bahasa sehari-hari
embrio disebut dengan mata beras. (Astawan, 2004).
2.1.1. Komposisi Gizi Beras
Beras merupakan salah satu kebutuhan pokok bagi masyarakat Indonesia.
Beras sebagai bahan makanan mengandung nilai gizi cukup tinggi yaitu
kandungan karbohidrat sebesar 360 kalori, protein sebesar 6,8 gr, dan kandungan
mineral seperti kalsium dan zat besi masing-masing 6 dan 0,8 mg (Astawan,
2004). Bagian gabah yang dapat dimakan adalah kariopsis yang terdiri dari 75%
karbohidrat dan 8% protein pada kadar air 14%. Penyusun lainnya adalah lemak,
serat, dan abu yang terdapat dalam jumlah sedikit. Bagian endosperm atau bagian
gabah yang diperoleh setelah penggilingan yang kemudian disebut beras giling,
mengandung 78% karbohidrat dan 7% protein (Haryadi, 2006).
Sebagian terbesar karbohidrat dalam beras ialah pati dan hanya sebagian kecil
pentosan, selulosa, hemiselulosa, dan gula. Antara 85% hingga 90% dari berat
kering beras berupa pati. Kandungan pentosan berkisar 2,0 – 2,5% dan gula 0,6 –
fisikokimiawi beras terutama ditentukan oleh sifat-sifat patinya, karena penyusun
utamanya adalah pati (Haryadi, 2006).
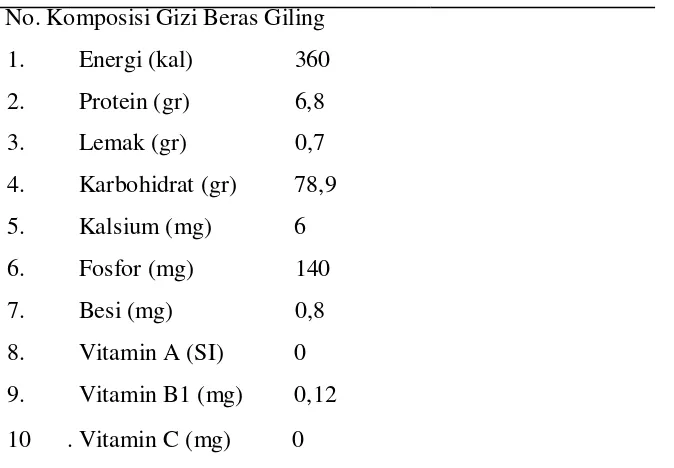
Tabel 2.1 Komposisi Gizi Beras Giling (dalam 100 gr bahan)
No. Komposisi Gizi Beras Giling
1. Energi (kal) 360
2. Protein (gr) 6,8
3. Lemak (gr) 0,7
4. Karbohidrat (gr) 78,9
5. Kalsium (mg) 6
6. Fosfor (mg) 140
7. Besi (mg) 0,8
8. Vitamin A (SI) 0
9. Vitamin B1 (mg) 0,12
10 . Vitamin C (mg) 0
Sumber : Departemen Kesehatan RI, 2005
2.1.2. Mutu Beras
Di Indonesia, tingkat mutu didasarkan antara lain pada kesepakatan oleh
sebagian besar pedagang beras. Tingkatan mutu yang berlaku di masyarakat
sangat beragam. Menurut Haryadi (2006), secara umum mutu beras dapat
dikelompokkan menjadi empat yaitu mutu giling, mutu rasa dan mutu tanak, mutu
gizi, mutu berdasar ketampakan dan kemurnian biji.
a. Mutu giling
Mutu giling merupakan salah satu faktor penting yang menentukan mutu
beras. Mutu giling mencakup berbagai ciri, yaitu rendemen beras giling,
rendemen beras kepala, persentase beras pecah dan derajat sosoh beras.
(Balittan Sukamandi, 1987 dalam Damardjati dan Endang Y. Purwani,
b. Mutu rasa dan mutu tanak
Di Indonesia, mutu tanak belum dijadikan syarat dalam menetapkan mutu
beras. Lain halnya dengan dunia internasional, khususnya di Amerika
Serikat, mutu tanak merupakan salah satu persyaratan terutama dalam
pengolahan beras. Ciri-ciri umum yang memengaruhi mutu tanak ialah
perkembangan volume, kemampuan mengikat air, stabilitas pengalengan
nasi parboiling, lama waktu penanakan dan sifat viskositas pati.
c. Mutu gizi
Beras pecah kulit hanya disenangi oleh sejumlah persentase kecil
konsumen meskipun beras pecah kulit mengandung protein, vitamin,
mineral, dan lipid lebih banyak daripada beras sosoh.
d. Mutu berdasar ketampakan dan kemurnian biji
Ketampakan biji pada umunya ditemukan berdasarkan keburaman
endosperm, yaitu bagian biji yang tampak putih buram, baik pada sisi
dorsal biji, sisi ventral, maupun tengah biji. Keburaman biji menentukan
mutu beras yang dalam persyaratan mutu dikenal sebagai butir mengapur.
2.2 Logam
Logam dapat dibagi menjadi dua bagian, yaitu logam esensial dan logam
nonesensial. Logam esensial adalah logam yang sangat membantu dalam proses
fisiologis makhluk hidup dengan jalan membantu kerja enzim atau pembentukan
organ dari makhluk yang bersangkutan, yang termasuk logam esensial adalah seng
(Zn), tembaga (Cu) dan selenium (Se). Logam nonesensial adalah arsen (As),
merkuri (Hg), Cadmium (Cd), Timbal (Pb), Kromium (Cr), dan Aluminium (Al),
tetapi beberapa jenis logam lain yang termasuk kelompok logam esensial dapat
pula bersifat racun bila keberadaannya telah melebihi dari kebutuhan pada proses
2.2.1 Logam Seng (Zn)
Seng adalah yang paling kurang beracun diantara mikro mineral.Tanda-tanda
kekurangan seng adalah gangguan pertumbuhan dan kematangan seksual. Fungsi
pencernaan terganggu, karena gangguan fungsi fankreas dan kerusakan
permukaan saluran cerna. Jaringan yang banyak mengandung seng adalah bagian
mata, kelenjar prostat, spermatozoa, kulit, rambut dan kuku. Kelebihan seng
disimpan di dalam hati dalam bentuk metalotionein. Lainnya dibawa ke pankreas
dan jaringan tubuh lain. Bentuk simpanan ini akan dibuang bersama sel-sel
dinding usus halus yang umurnya 2-5 hari . Logam seng berperan pula dalam
sintesis dan degradasi kalogen, pembentukan kulit, metabolisme jaringan ikat dan
penyembuhan luka, serta dalam pengembangan fungsi reproduksi laki-laki dan
pembentukan sperma, selain itu sebagai pengangkut sintesis vitamin A,
pembentukan antibodi sel, metabolisme tulang, transpor oksigen, pembentukan
struktur dan fungsi membran serta proses penggumpalan darah
(Almatsier,S.2001). Disamping itu dapat terjadi diare dan gangguan fungsi
kekebalan. Kekurangan seng kronis mengganggu pusat sistem saraf dan fungsi
otak.. Kekurangan seng juga mengganggu fungsi kelenjar tiroid dan laju
metabolisme, gangguan nafsu makan, penurunan ketajaman indra rasa serta
memperlambat penyembuhan luka. Walaupun seng sangat dibutuhkan oleh tubuh
namun konsumsi seng yang berlebihan juga dapat bersifat toksik. Maksimum asupan
harian iron yang diizinkan(Provosional maximum tolerable daily intake/PMDTI) adalah
0.3-1 mg/Kg berat badan. Kelebihan seng mempengaruhi metabolisme kolesterol,
mengubah nilai lipoprotein dan dapat mempercepat timbulnya aterosklerosis.
2.2.2 Logam Besi (Fe)
Zat besi adalah komponen hemoglobin di dalam sel darah merah (eritrosit) yang
tersedia untuk mentransportasikan oksigen ke seluruh tubuh dan dalam bentuk
mioglobin untuk penyimpanan dan penggunaan oksigen di otot. Oksigen dikeluarkan di
jaringan dalam bentuk hemoglobin digunakan untuk metabolime oksidatif. Hemoglobin
mengikat karbondioksida dalam jaringan dan membawanya ke paru-paru dimana dia
dalam serapan dari diet dan mentransfer ke dalam sirkulasi sistemik, transportasi di
seluruh tubuh dan penyimpanan pada jaringan, serta pengiriman ke situs fungsional
(Geissler dan Singh, 2011). Besi terjadi sebagai konstituen alami dari semua makanan
Besi telah dievaluasi oleh JECFA pada tahun 1983. Asupan maksimum
asupanharian iron yang diizinkan (Provosional maximum tolerable daily intake/PMDTI)
adalah 1-10 mg/Kg berat badan., PMDTI ini ditetapakan untuk mencegah
terjadinyapenimbunan besi dalam tubuh secara berlebihan.
Dosis mematikan besi rata-rata adalah 200-250 mg / kg berat badan, tetapikematian telah
terjadi setelah mengkonsumsi dosis serendah 40 mg / kg berat badan. Otopsi telah
menunjukkan nekrosis hemoragik dan pengelupasan daerah mukosa di perut dengan
ekstensi ke submukosa. Kronis hasil kelebihan zat besi terutama dari kelainan genetik
(hemokromatosis) ditandai dengan penyerapan zat besi meningkat dan penyakit yang
memerlukan transfusi sering. Dewasa sering mengambil suplemenzat besi untuk waktu
yang lama tanpa efek merusak, dan asupan 0,4-1 mg / kg berat badan per hari tidak
mungkin menyebabkan efek samping pada orang sehat (WHO,1996).
Dosis mematikan besi rata-rata adalah 200-250 mg / kg berat badan, tetapi kematian telah
terjadi setelah mengkonsumsi dosis serendah 40 mg / kg berat badan. Otopsi telah
menunjukkan nekrosis hemoragik dan pengelupasan daerah mukosa di perut dengan
ekstensi ke submukosa. Kronis hasil kelebihan zat besi terutama dari kelainan genetik
(hemokromatosis) ditandai dengan penyerapan zat besi meningkat dan penyakit yang
memerlukan transfusi sering. Dewasa sering mengambil suplemen zat besi untuk waktu
yang lama tanpa efek merusak, dan asupan 0,4-1 mg / kg berat badan per hari tidak
2.2.3 Logam Tembaga (Cu)
logam berat Cu digolongkan kedalam logam berat dipentingkan atau logam berat
esensial, artinya meskipun Cu merupakan logam berat beracun, unsur logam ini
sangat dibutuhkan tubuh meskipun dalam jumlah sedikit. Pada manusia Cu paling
banyak didapatkan dalam hati dan darah. Logam Cu dibutuhkan untuk sistem
enzim oksidatif seperti enzim askorbat oksidase, sistikrom oksidase, polyfenol
oksidase dan lain-lain. Cu juga dibutuhkan manusia sebagai kompleks Cu-protein
yang mempunyai fungsi tertentu dalam pembentukan hemoglobin, kolagen,
pembuluh darah dan myelin otak. Disamping itu, Cu juga terlibat dalam proses
pembentukan energi untuk metabolisme serta dalam aktifitas tirosin
(Heryando.1994)
Tembaga sebagai tembaga sulfat telah dievaluasi oleh JECFA pada tahun 1966,
1970, dan 1982. Maksimum asupan harian yang diizinkan (Provosional maximum
tolerable daily intake/PMDTI) adalah 0,05-0,5 mg / kg berat badan. Logam Cu akan
berbalik menjadi bahan racun untuk manusia bila masuk dalam jumlah berlebihan.
Bentuk Cu yang paling beracun adalah debu-debu Cu yang dapat mengakibatkan
kematian pada dosis 3,5 mg/kg. Sedangkan daya racun yang dimiliki oleh garam
klorida terhidrasi (CuCl2.2H2O) akan mengakibatkan kematian pada dosis 9,4
mg/kg. Untuk garam sulfat dalam bentuk terhidrasi (CuSO4.5H2O) daya racun
yang dimilikinya akan mengakibatkan kematian pada dosis 33 mg/kg .Pada
manusia, efek keracunan utama yang ditimbulkan akibat terpapar oleh debu atau
uap logam Cu adalah terjadinya gangguan pada jalur pernafasan sebelah
atas,terjadinya kerusakan atropik pada selaput lendir yang berhubungan dengan
hidung (Heryando.1994).
kaleng yang dilapisi seng . (Sunita.2002).Seng dalam jumlah yang banyak
dapat menyebabkan kematian. Dosis seng yang tinggi juga dapat menghambat
2.3 Perombakan Bahan Organik dan Biologis
Untuk menentukan kandungan mineral bahan makanan, bahan makanan
dihancurkan atau didekstruksi terlebih dahulu. Cara yang biasa dilakukan yaitu
dengan metode pengabuan kering (dry ashing) dan pengabuan basah (wet
digestion). Pemilihan metode pengabuan tersebut tergantung pada sifat zat
organik dalam bahan, sifat zat anorganik yang ada dalam bahan, mineral yang
akan dianalisa serta sensitivitas yang digunakan (Apriyanto,A.1989).
a. Dekstruksi Basah
Dekstruksi basah yaitu pemanasan sampel (organic atau biologis) dengan adanya
pengoksidasi kuat seperti asam-asam mineral baik tunggal maupun campuran.
Jika dalam sampel dimasukkan zat pengoksidasi, lalu dipanaskan pada
temperature yang cukup tinggi dan jika pemanasan dilakukan secara kontinu pada
waktu yang cukup lama, maka sampel akan teroksidasi sempurna sehingga
meninggalkan berbagai elemen-elemen pada larutan asam dalam bentuk senyawa
anorganik yang sesuai untuk dianalisis (Anderson,R.1987).
Dekstruksi basah pada prinsipnya adalah penggunaan asam nitrat untuk
mendekstruksi zat organik pada suhu rendah dengan maksud mengurangi
kehilangan mineral akibat penguapan. Pada tahap selanjutnya, proses seringkali
berlangsung sangat cepat akibat pengaruh asam perklorat atau hidrat peroksida.
Dekstruksi basah pada umumnya digunakan untuk menganalisa arsen, tembaga,
timah hitam, timah putih, dan seng.
Ada tiga macam cara kerja dekstruksi basah dapat dilakukan, yaitu :
1. Dekstruksi basah menggunakan HNO3 dan H2SO4
2. Dekstruksi basah menggunakan HNO3,H2SO4 dan HClO4
3. Dekstruksi basah menggunakan HNO3,H2SO4 dan H2O2(Apriyanto,A.1989)
b. Dekstruksi Kering
Dekstruksi kering merupakan yang paling umum digunakan dengan cara
membakar habis bagian organik dan meninggalkan residu anorganik sebagai abu
untuk analisis lebih lanjut. (Anderson,R.1987). Pengabuan kering dapat
diterapkan pada hampir semua analisa mineral, kecuali merkuri dan arsen. Cara
ini lebih membutuhkan sedikit ketelitian sehingga mampu menganalisa bahan
menganalisa kandungan Ca,P dan K akan tetapi kehilangan K dapat terjadi apabila
suhu yang digunakan terlalu tinggi. Oleh karena itu, untuk menganalisa K harus
dihindari pemakaian suhu lebih tinggi dari 480oC. Suhu 450oC tidak dapat
digunakan jika menganalisa kandungan seng (Zn), yang penggunaan suhu yang
terlalu tinggi juga menyebabkan beberapa mineral menjadi tidak larut (misal
timah putih) (Apriyanto,A.1989).
2.4. Kitosan
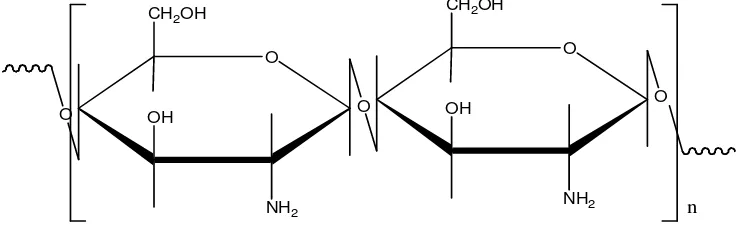
Kitosan adalah poli-(2-amino-2-deoksi-β(1-4)-D-glukopiranosa) dengan
rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin (Gambar
2.1). Kitosan juga dijumpai secara alamiah di beberapa organisme (Sugita,2009).
O
NH2 OH
CH2OH
O O
O
NH2 OH
CH2OH
O
n
Gambar 2.4. Struktur Kimia Kitosan
Kitosan merupakan suatu turunan utama dari kitin, dimana untuk
mendapatkan kitosan yang baik tergantung dari kitin yang diperoleh dan kekuatan
suatu alkali serta waktu yang digunakan dalam reaksi deasetilasi (Zakaria, 1995).
Kitosan mengandung unsur nitrogen yang tinggi (sekitar 70 %) dapat mengambil
ion logam yang tinggi. Elektron terpencil pada atom nitrogen dan oksigen pada
gugus amina dapat membentuk ikatan kovalen dengan ion logam berat dan ion
logam peralihan. Gugusan amina pada kitosan juga merupakan tempat pengkhelat
ionlogam perlaihan dan gugus ini bersifat stabil dalam NaOH 50 % walaupun
mencapai temperatur 160oC. Kitosan juga telah digunakan secara luas dalam
farmasi karena mempunyai kemampuan biodegredasi dan biocompatibility dan
rendah toksitasnya (Muzzarelli, 1977).
2.4.1. Kitosan pada Belangkas
Kitin dan kitosan banyak ditemukan pada arthropoda yaitu krustacea
(kerangka luar udang, kepiting, lobster, belangkas), insekta, arachnida, dan
sebagainya. Belangkas termasuk ordo Xiphosura, terdiri dari hanya empat spesies
yang masih tersisa yaitu Limulus polyphemus, Tachypleus gigas, T. tridentatus,
dan Carcinoscorpius rotundicauda. Belangkas memiliki panjang hingga 60cm,
berekor, sekali bertelur sekitar 20.000 yang diletakkan betina dalam
lubang-lubang pasir yang digalinya di pantai. Belangkas yang hidup di perairan air
tenggara adalah jenis tachypleus gigas.
Pada cangkang belangkas (berbeda dengan kepiting dan krustacea lainnya)
tidak memiliki komponen kalsium pada bahan kitin dan kitosannya. Penelitian
tentang kitin belangkas dilakukan oleh Rutherford dan Dunson (1984) mengenai
permeabilitas film kitin yang diisolasi dari cangkang belangkas Limulus. Isolasi
kitin yang didapatkan dari cangkang belangkas Tachypleus gigas sebanyak 30,2%
(Agusnar et al. 2013).
2.4.2. Sifat Fisika-Kimia Kitosan
Kitosan merupakan padatan amorf yang berwarna putih dengan rotasi
spesifik [α]D11 -3 hingga -10o (padatan konsentrasi asam asetat 2%). Kitosan larut
pada kebanyakan larutan asam organik, pada pH sekitar 4,0 tetapi tidak larut pada
pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alcohol dan aseton.
Dalam asam mineral HCl dan HNO3, kitosan larut pada konsentrasi 0,15-1,1%,
tetapi tidak larut pada konsentrasi 10%. Kitosan tidak larut dalam H2SO4 pada
berbagai, konsentrasi,sedangkan dalam H3PO4 tidak larut pada konsentrasi 1%
sementara pada konsentrasi 0,1% sedikit larut. Perlu kita ketahui, bahwa kelarutan
kitosan dipengaruhi oleh bobot molekul, derajat deasetilasi dan rotasi spesifiknya
yang beragam tergantung pada sumber dan metode isolasi serta transformasinya
Kitosan tidak larut dalam air, pelarut-pelarut organik, juga tidak larut
dalam alkali dan asam-asam mineral pada pH di atas 6,5. Dengan adanya
sejumlah asam, maka dapat larut dalam air - metanol, air - etanol, dan campuran
lainnya. Kitosan larut dalam asam formiat dan asam asetat dan menurut Peniston
dalam 20% asam sitrat juga dapat larut. Asam organik lainnya juga tidak dapat
melarutkan kitosan, asam-asam anorganik lainnya pada pH tertentu setelah distirer
dan dipanaskan dan asam sitrat juga dapat melarutkan kitosan.
Kitosan bersifat polikationik yang dapat mengikat lemak dan logam berat
pencemar. Kitosan yang mempunyai gugus amina yaitu adanya unsur N bersifat
sangat reaktif dan bersifat basa (Inoue, 1994 ).Kitosan mempunyai sifat spesifik
yaitu adanya sifat bioaktif, biokompatibel, pengkelat, anti bakteri dan dapat
terbiodegradasi. Kualitas kitosan dapat dilihat dari sifat intrinsiknya, yaitu
kemurniannya, massa molekul, dan derajat deasetilasi. Umumnya kitosan
mempunyai derajat deasetilasi 75-100%. Massa molekul kitosan dan distribusinya
berpengaruh terhadap sifat-sifat fisiko-kimia polisakarida. Derajat deasetilasi dan
massa molekul kitosan hasil deasetilasi kitin pada dasarnya dipengaruhi oleh
konsentrasi alkali/basa, rasio larutan terhadap padatan, suhu dan waktu reaksi,
lingkungan/kondisi reaksi selama deasetilasi. (Ramadhan,L.O.A.N, 2010).
Sedangkan sifat biologi kitosan antara lain (Kaban, 2009):
a. Bersifat biokompatibel (sebagai polimer alami sifatnya tidak mempunyai
akibat samping, tidak beracun, tidak dapat dicerna serta mudah diuraikan
oleh mikroba).
b. Dapat berikatan dengan sel mamalia dan mikroba secara agresif.
c. Mampu meningkatkan pembentukan yang berperan dalam pembentukan
tulang.
d. Bersifat hemostatik, fungistatik, spermisidal, antitumor, antikolesterol.
e. Bersifat sebagai depresan pada system saraf pusat.
2.4.3. Pelarut Kitosan
Pelarut yang digunakan dalam penelitian ini adalah pelarut asam asetat 1%
dan pelarut asam laktat 1%. Pelarut terbaik yang digunakan dalam
asamasetat. Pelarut yang umum digunakan untuk melarutkankitosan adalah asam
asetat dengan konsentrasi 1 – 2 % (Knorr, 1982). Asamasetat adalah cairan tidak
berwarna dengan karakteristik bau yang tajam,berasa asam, serta larut dalam air,
alkohol, dan gliserol. Rumus empirik asamasetat adalah C2H4O2 dan rumus
strukturnya CH3COOH. Asam asetatmempunyai berat molekul 60, titik didih 118
oC, titik beku 16,7 oC, dan dapat digunakaan sebagai penambahan rasa (Dillon,
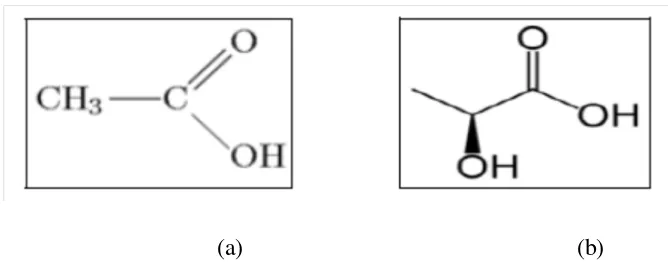
1992). Rumus struktur (a) asamasetat, (b) asam laktat dapat dilihat pada Gambar
2.
(a) (b)
Gambar 2. Rumus Struktur (a) Asam Asetat dan (b) Asam laktat
Asam laktat atau asam 2-hidroksi propionat merupakan senyawa
nonatsiridan tidak berbau yang diklasifikasikan ke dalam GRAS
(GenerallyRecognized As Safe) sebagai bahan aditif makanan. Asam laktat
mempunyaisifat larut dalam air dan pelarut organik polar tetapi tidak larut dalam
pelarutorganik lainnya.Dalam struktur kimianya, asam laktat merupakan salah
satu molekulterkecil yang memiliki sifat optis aktif yang mempunyai satu atom
karbonkiral sehingga memiliki dua bentuk enantiomer, yaitu L- dan D-laktat.
Sekitar85% kebutuhan asam laktat saat ini adalah untuk aplikasi di bidang
pangandan yang berhubungadengan pangan, antara lain sebagai pengasam
makanan(food acidulan, flavoring agent, pH buffering agent, dan antimicrobial
agent)(Koesnandar, 2004).
Molekul kitosan di dalam larutan asam encer berkekuatan ion
rendahbersifat lebih kompak bila dibandingkan dengan larutan polisakarida
lainnya.Hal ini disebabkan densitas muatan yang tinggi. Namun, dalam
molekul kitosan terganggu sehingga konformitas menjadi bentuk acak (random
coil).Sifat fleksibel molekul ini yang akan menjadikan kitosan dapat
membentukbaik konformitas kompak maupun memanjang (polisakarida
lainnyaumumnya berbentuk memanjang). Sifat fleksibel kitosan membantu
dayagunanya di dalam berbagai produk (Angka dan Suhartono, 2000).
Kitosan mempunyai gugus fungsionalyaitu gugus amina, sehingga
mempunyai derajat reaksi kimia yang tinggi(Johnson dan Peniston, 1982). Kitin
dan kitosan merupakan senyawa kimia yang mudahmenyesuaikan diri, hidrofilik,
memiliki reaktivitas kimia yang tinggi (karenamengandung gugus OH dan gugus
NH2) untuk ligan yang bervariasi (sebagaibahan pewarna dan penukar ion).
(Muzzarelli, 1997).
2.4.4. Kitosan sebagai Adsorben
Kitosan larut dalam pelarut organik, HCl encer, HNO3 encer, H3PO4 0,5%
dan CH3COOH 1%, tetapi tidak larut dalam basa kuat dan H2SO4. Dalam kondisi
asam berair, gugus amino (-NH2) kitosan akan menangkap H+ dari
lingkungannya, sehingga gugus aminonya terprotonasi menjadi –NH3+. Gugus –
NH3+ inilah yang menyebabkan kitosan bertindak sebagai garam, sehingga dapat
larut dalam air, analog dengan pelarutan garam dapur dalam air. Selain itu muatan
positif –NH3+ dapat dimanfaatkan untuk adsorpsi zat warna anionik (Sugita,2009).
Proses adsorpsi meliputi tiga tahap mekanisme yaitu :
1. Pergerakan molekul-molekul adsorbat menuju permukaan adsorben.
2. Penyebaran molekul-molekul adsorbat kedalam rongga-rongga adsorben.
3. Penarikan molekul-molekul adsorbat oleh permukaan aktif membentuk
ikatan, yang berlangsung sangat cepat (Metcalf, 1979).
Adsorben (untuk adsorpsi fisik) adalah bahan padat dengan luas permukaan yang
besar. Permukaan yang luas ini termasuk karena banyaknya pori yang halus pada
padatan tersebut. Tergantung pada tujuan penggunaannya adsorben dapat berupa
granulat (dengan ukuran butir sebesar beberapa mm) atau serbuk (khusus untuk
2.4.5. Penggunaan Kitosan Untuk Menurunkan Logam Berat
Metode yang selalu digunakan didalam penanggulangan limbah logam
berat dapat dilakukan antara lain dengan mengatur pH sehingga logam berat itu
mengendap, dengan pengkompleks, dengan melakukan penukar kationik, dan
juga dengan koagulasi dan flokulasi serta adsorbsi (Agusnar, 2010).
Kitosan merupakan biopolimer alam yang bersifat polielektrolit kationik yang
berpotensi tinggi untuk penyerapan logam dan mudah terbiodegredasi serta tidak
beracun (Muzzarelli.1997).
Perubahan pH akan mengakibatkan perubahan daya serap terhadap logam.
Dimana konsentrasi logam terserap makin tinggi dengan naiknya pH. Daya serap
juga semakin tinggi dengan pada larutan kitosan 10 ml sedangkan volume
dinaikkan daya serap menurun dimana pH yang digunakan untuk tiap-tiap
penambahan adalah sama yaitu pH 9, dimana pada kondisi ini kitosan mampu
menetralkan menjadi flok yang terbentuk secara sempurna dan pada akhirnya
bersamasama mengendap. Untuk mengetahui besarnya penyerapan kadar
logam-logam berat dilakukan dengan pengukuran adsorbsi larutan dengan menggunakan
Spektrofotometer serapan atom (SSA). Hasil serapan yang diperoleh kemudian
diolah dengan menggunakan metode least square, (Agusnar,2010)
2.5 Kitosan Nano Partikel
Nano kitosan yaitu kitosan yang memiliki pertikel yang berbentuk padat
denganukuran sekitar 10 – 1000 nm. Kitosan dalam bentuk nanopartikel ini pun
bersifatnetral, tidak toksik, dan memiliki stabilitas yang konstan. Nanopartikel
inidigunakan dalam berbagai aplikasi yang sangat tidak invasive. Dalam
sistempengantaran obat, nanopartikel berperan sebagai pembawa (carrier) dengan
caramelarutkan, menjebak, mengenkapsulasi, atau menempelkan obat di
dalammatriksnya. Baru-baru ini, nanopartikel yang berasal dari bahan
polimerdigunakan sebagai sistem pengantaran obat yang potensial karena
kemampuan penyebarannya di dalam organ tubuh selama waktu tertentu, dan
kemampuannyauntuk mengantarkan protein atau peptida (Mohanraj,
You Shan Szeto dan Zhigang Hu untuk menyiapkan nanopartikeldimana kitosan
dilarutkan dalam asam lemah kemudian ditambahkan larutan yang bersifat basa
seperti amoniak, natrium hidroksida atau kalium hidroksida kemudian distirer
dengan kecepatan 300 rpm sehingga diperoleh gel kitosan putih dan dibilas
dengan aquades sampai netral kemudian ditempatkan pada ultrasonicbath untuk
memecah partikel gel kitosan menjadi lebih kecil (Szeto, 2007).Sebagian ahli juga
mencoba metode lain untuk menyiapkan kitosan nanodengan menambahkan
larutan tripoliposfat kedalam larutan kitosan sehingga diperoleh emulsi kitosan
sambil distirer dengan kecepatan 1200 rpm kemudianemulsi di buat pH 3,5
dengan menambahkan asam asetat hasilnya akan berupasuspensi kitosan (Cheung,
2008).
2.6 Natrium Tripolifosfat
Na Tripolifosfat dengan rumus molekul Na5P3O10 dan memiliki bobot
molekul 368 g mol . Na tr polifosfat dibuat denganmemanaskan campuran
dinatrium fosfat (Na5P3O10) dan sesuai dengan persamaan berikut :
Na2HPO4+ NaH2PO4 → Na5P3O10 + H2O
Na-Tripolifosfat digunakan untuk surfaktan, larutan buffer, bahan pengemulsi
(emulsifier), dan hidrolisis lemak. Selain itu, na-tripolifospat juga sering
digunakan untuk peanut silang pada pembuatan membrane kitosan. Penggunaan
tripolifosfat sebagai ikat silang telah dilakukan oleh Hu et all, (2006) dalam
pembuatan nanopartikel kitosan tertaut silang (Sugita, 2009).
2.7 Ultrasonikasi
Spektum suara (sonic) yang memiliki frekuensi sangat tinggi disebut
ultrasonik, Rentang frekuensi ultrasonic yaitu 20 kHz-10 MHz. Ultrasonik dibagi
menadi tiga golongan utama: Frekuensi rendah (20-100 kHz). Frekuensi
menengah (100 kHz – 1 MHz), dan frekuensi tinggi (1-10 MHz). Ultrasonik
dengan frekuensi 20 kHz -1 MHz banyak digunakan dalam bidang kimia yang
Metode ultrasonik adalah metode yang menggunakan gelombang
ultrasonic yaitu gelombang akustik dengan frekuensi lebih besar dari 16-20kHz
(Suslick, 1988). Ultrasonik bersifat non-destructive dan non-invasive sehingga
dapat dengan mudah diadaptasikan keberbagai aplikasi (McClements, 1995.
Menutrut kuldiloke (2002), salah satu manfaat metode ekstraksi ultrasonik adalah
untuk mempercepat proses ektraksi. Dinding sel dari bahan dipecah dengan
getaran ultrasonik diatas 1 MHz banyak digunakan dalam bidang kedokteran
seperti pencitraan, analisis aliran darah, kedokteran gigi, sedot lemak, ablasi
tumor, dan penghancuran batu ginjal (Mason,1990).
Proses degradasi bergantung kepada berat molekoul, yaitu molekul dengan
rantai panjang lebih utama dihilangkan dan polidipersitas polimer berubah.
Dengan demikian degradasi dapat digunakan sebagai proses tambahan sebagai
parameter dalam mengontrol distribusi berat molekul, produk utama degradasi
diperoleh ketika bahan redikal yang timbul dari kerusakan ikatan homolitik
sepanjang rantai (Tabata,1980).
Degradasi (yang berarti pemutusan ikatan rantai panjang yang disebabkan
oleh pembelahan dan tidak tentu pada perubahan kimia) dari rantai polimer dalam
larutan yang memiliki intensitas tinggi. Proses degradasi lebih cepat dengan berat
molekul lebih rendah pada temperature yang lebih rendah dalam larutan dengan
pelarut yang memiliki volatilitas yang lebih rendah juga. Sonikasi pada suhu yang
lebih tinggi atau dalam pelarut yang mudah menguap menghasilkan uap lebih
banyak masuk kegelembung dan terjadi penurunan pelunakan sehingga tingkat
kekerasannya berkurang. Dalam larutan encer rantai polimer tidak terjerat dan
bebas untuk bergerak dalam daerah aliran sekitar gelembung. Degradasi lebih
efesien pada intensitas ultrasonic yang lebih tinggi karena semakin banyak jumlah
gelembung dengan jari-jari yang lebih besar (Suslick,1999).
2.8. Particle Size Analyzer (PSA)
Particle size analyzer (PSA) adalah alat yang mampu mengukur partikel
distribusi emulsi, supensi dan bubuk kering. Hal ini dapat dilakukan pada sebagai
Keunggulannya antara lain:
1. Akurasi dan reproduksibilitas beradah dalam ±1 %
2. Mampu mengukur partikel berkisar 0,02 mm nm sampai 2000 nm
3. Dapat digunakan untuk pengukuran distribusi ukuran partikel
emulsi, suspense, dan bubuk kering (Hossaen,2000).
2.9. Spektrofotometri Serapan Atom (SSA)
Spektrofotometri serapan atom adalah metoda pengukuran kuantitatif
suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya
pada panjang gelombang tertentu oleh atom – atom bentuk gas dalam keadaan
dasar. telah lama ahli kimia menggunakan pancaran radiasi oleh atom yang
dieksitasikan dalam suatu nyala sebagai alat analisi. fraksi atom – atom yang
tereksitasi berubah secara eksponensial dengan temperatur. tekni ini digunakan
untuk penetapan sejumlah unsur, kebanyakan logam dan sampel yang sangat
beraneka ragam (Walsh , 1955)
2.9.1 Prinsip dan Teori
Spektrofotometri serapan atom didasarkan pada bahwa atom – atom pada
suatu unsur dapat mengabsropsi energi sinar pada panjang gelombang tertentu.
banyak energi sinar yang di absropsi berbanding lurus dengan jumlah atom – atom
unsur yang mengabsropsi. Atom terdiri atas inti atom yang mengandung proton
bermuatan positif dan neutron berupa pertikel netral, dimana inti atom
dikelilingi oleh elektron –elektron bermuatan negatif pada tingkat energi yang
berbeda – beda. Jika energi diabsropsi oleh atom, maka elektron yang berada di
kulit terluar ( electron valensi ) akan tereksitasi dan bergerak dari keadaan dasar
atau tingkat energi yang terendah kekeadan tereksitasi dengan tingkat energi yang
terendah. Jumlah energi yang dibutuhkan untuk memindahkan elektron ke tingkat
energi tertentu dikenal sebagai potensial eksitasi untuk tingkat energi tersebut
2.9.2 Instrumentasi
Untuk keperluan analisis kuantitatif dengan spektrofotometer serapan
atom, maka sampel harus dalam bentuk larutan. Untuk menyiapkan larutan,
sampel harus diperlukan sedemikian rupa yang pelaksanaannya tergantung dari
macam dan jenis sampel. Yang penting untuk diingat adalah bahwa larutan yang
akan dianalisis haruslah sangat encer.
Ada beberapa cara untuk melarutkan sampel, yaitu:
• Langsung dilarutkan dengan pelarut yang sesuai
• Sampel dilarutkan dalam suatu asam
• Sampel dilarutkan dalam suatu basa atau dilebur dahulu dengan basa kemudian hasil leburan dilarutkan dengan pelarut yang sesuai
Metode pelarutan apapun yang akan dipilih untuk dilakukan analisis dengan
spektrofotometer serapan atom, yang terpenting adalah bahwa larutan yang
dihasilkan harus jernih, stabil dan tidak mengganggu zat-zat yang akan dianalisis.
Pelarutan juga dimaksudkan untuk destruksi sampel dimana sampel dimana
biasanya digunakan asam-asam seperti asam nitrat pekat (Rohman, 2007)
Komponen penting yang membentuk spektrofotomter serapan atom diperlihatkan
pada gambar 2.5 dibawah ini.
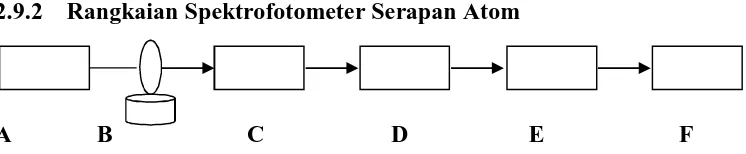
2.9.2 Rangkaian Spektrofotometer Serapan Atom
A B C D E F
Gambar 2.9.2. Rangkaian ringkas Spektrofotometer Serapan Atom
Keterangan Gambar :
A = Lampu Katoda Berongga B = Nyala
C = Monokromator
E = Amplifier
F = Recorder ( Sony.2009) a. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini terdiri
atas tabung kaca tertutup yang mengandung suatu katoda dan anoda (Mulja, 1992)
b. Tempat sampel
Dalam analisis dengan spektofotometri serapan atom, sampel yang akan dianalisis
harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada
berbagai macam yang dapat digunakan untuk mengubah suatu sampel menjadi
uap atom-atom yaitu dengan nyala dan tanpa nyala.
1. Nyala (flameless)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
2. Tanpa nyala(flameless)
Pengatoman dapat dilakukan dalam tungku dari grafit. Sampel diletakkan dalam
tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan
cara melewatkan arus listrik grafit. Akibat pemanasan ini,maka gas yang akan
dianalisis berubah menjadi atom-atom netral (Rohman, 2007).
c. Monokromator
Monokromator memisahkan,mengisolasi dan mengontrol intensitas dari radiasi
energi yang mencapai detektor (Haswell, 1991).
d. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga tidak
memberikan respon terhadap nilai emisi yang berasal dari eksitasi
e. Read Out
Merupakan suatu alat petunjuk atau dapat juga diartikan sebagai sistem beberapa
pencatat hasil (Khopkar, 2007).
2.9.4 Gangguan Pada SSA dan Cara Mengatasinya
Gangguan nyata pada SSA adalah seringkali didapatkan suatu harga yang
tidak sesuai dengan konsentrasi sampel yang ditentukan. Penyebab dari gangguan
ini adalah faktor matriks sampel dan faktor kimia karena adanya gangguan
molekuler yang bersifat radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan
cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya
ionisasi atom akan menjadi kesalahan pada SSA oleh karena spektrum radiasi oleh
ion jauh berbeda denga spektrum absorpsi atom netral yang memang akan
ditentukan. Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA
yaitu dengan cara:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu
dipakai gas pembakar campuran C2H2 + N2O yang memberikan nyala
dengan temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat
kuat akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya
penentuan logam yang terikat sebagai garam, dengan penambahan logam
yang lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu.
3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi
(Mulja, 1995).
2.10. FTIR (Fourier Transform Infra Red)
Pancaran infra merah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak di antara daerah tampak dan daerah gelombang
mikro. Sebagian besar kegunaannya terbatas di daerah antara 4000 cm-1 dan 666
dekat, 14290-4000 cm-1 (0,7-2,5 µm) dan daerah infra merah jauh, 700-200 cm-1
(14,3-50 µm) (Silverstein, 1967).
Salah satu hasil kemajuan instrumentasi IR adalah pemrosesan data
seperti Fourier Transform Infra Red (FTIR). Teknik ini memberikan informasi
dalam hal kimia, seperti struktur dan konformasional pada polimer dan
polipaduan, perubahan induksi tekanan dan reaksi kimia. Dalam teknik ini
padatan diuji dengan cara merefleksikan sinar infra merah yang melalui tempat
kristal sehingga terjadi kontak dengan permukaan cuplikan. Sensitivitas FTIR
adalah 80-200 kali lebih tinggi dari instrumentasi dispersi standar karena
resolusinya lebih tinggi (Kroschwitz, 1990).
Teknik pengoperasian FTIR berbeda dengan spektrofotometer infra
merah. Pada FTIR digunakan suatu interferometer Michelson sebagai pengganti
monokromator yang terletak di depan monokromator. Interferometer ini akan
memberikan sinyal ke detektor sesuai dengan intensitas frekuensi vibrasi molekul
yang berupa interferogram (Bassler, 1986).
Interferogram juga memberikan informasi yang berdasarkan pada
intensitas spektrum dari setiap frekuensi. Informasi yang keluar dari detektor
diubah secara digital dalam komputer dan ditransformasikan sebagai domain,
tiap-tiap satuan frekuensi dipilih dari interferogram yang lengkap (fourier transform).
Kemudian sinyal itu diubah menjadi spektrum IR sederhana. Spektrofotometer
FTIR digunakan untuk :
1. Mendeteksi sinyal lemah.
2. Menganalisis sampel dengan konsentrasi rendah.