PENGARUH SUHU DAN LAMA PRA-PERLAKUAN MANITOL
TERHADAP PROLIFERASI KALUS PADA KULTUR ANTERA
Swainsona formosa
Zulkarnain1
ABSTRACT
The aim of this investigation was to study the effect of anther stress pre-treatment using mannitol at two different temperature regimes and four different periods of time on the growth of anthers cultured in vitro. Anthers with microspores at uninucleate stage were pre-treated with mannitol at 4oC or 25oC for 2, 4, 6 or 8 days in dark condition. Following this, the anthers were cultured on solid B5 medium supplemented with vitamins and 2% sucrose at light intensity of 50 µmol m-2 s-1 and 16 hours photoperiod at 25 ± 1oC. The results indicated that stress pre-treatment enhanced callus formation from cultured anthers. Pre-treatment of anthers with mannitol starvation at 4oC for 2 - 8 days produced more callus than mannitol starvation at 25oC for the same period. Although this pre-treatment might not sufficient to induce microspore embryogenesis in S. formosa, it was clear that anther pre-treatment with mannitol starvation at 4oC for 8 days showed the capacity of promoting the in vitro tissue growth.
Key words: anther culture, in vitro culture, mannitol, pre-treatment, Swainsona formosa.
PENDAHULUAN
Teknologi haploid sangat menarik bagi para peneliti biologi perkembangan dan genetika serta para pakar di bidang pemuliaan tanaman dan bioteknologi. Melalui embriogenesis mikrospora galur-galur homozigot dapat dihasilkan dalam waktu yang lebih cepat dari pada menggunakan teknik konvensional (Tomasi et al., 1999). Taji et al. (2002) menambahkan bahwa dengan teknologi haploid galur-galur homozigot dapat diperoleh dalam satu generasi, sedangkan bila menggunakan teknologi konvensional galur-galur tersebut baru dapat dihasilkan setidak-tidaknya setelah lima generasi. Pada tanaman haploid, sifat-sifat unggul seperti toleran terhadap kondisi lingkungan yang kurang menguntungkan,
1 Staf Pengajar pada Jurusan Budi Daya Pertanian, Fakultas Pertanian Universitas Jambi.
misalnya kekeringan, suhu rendah, logam berat atau kondisi hara rendah dapat dideteksi lebih dini.
mendukung pertumbuhan (Immonen and Anttila, 1999).
Kultur antera telah berhasil meregenerasikan tanaman pada sejumlah spesies seperti Brassica napus (Lichter, 1982), Triticum aestivum (Touraev et al., tanaman Swainsona formosa telah pernah dilakukan oleh Tade (1992). Penelitian yang dilaporkan ini mengkaji lebih lanjut mengenai potensi antera S. formosa dalam merespon kondisi kultur in vitro dengan memfokuskan kajian pada pra-perlakuan antera sebelum inisiasi kultur.
Penelitian ini bertujuan untuk mempelajari pengaruh starvasi manitol pada suhu rendah dan suhu kamar selama periode waktu yang berbeda sebelum antera diintroduksikan pada medium aseptik di dalam sistem perbanyakan in vitro.
METODE PENELITIAN
Penelitian ini dilaksanakan di Plant Biotechnology Laboratory, School of Rural Science and Agriculture, University of New England, Australia, pada bulan Maret hingga Juli 2002. Bahan tanaman induk yang digunakan diperoleh dari biji dan ditumbuhkan serta dipelihara di rumah kaca untuk menjaga keseragaman genotip.
Voucher specimen disimpan di NCW Beadle Herbarium, University of New England, Australia, dengan nomor aksesi NE79130.
Medium dasar yang digunakan untuk kultur in vitro adalah B5 (Gamborg et al., 1968) yang dilengkapi dengan vitamin dan 2% sukrosa serta dipadatkan dengan 8 g L
-1 Bacto Bitek. Ke dalam medium
ditambahkan zat pengatur tumbuh IBA konsentrasi 49.3 µM dan zeatin konsentrasi 4.61 µM. Kemasamam medium ditetapkan 5,8 ± 0,02 sebelum sterilisasi medium menggunakan otoklaf bertekanan 1.1 kg cm-1 (103 kPa) pada suhu 121oC selama 20 menit. Medium yang masih cair selanjutnya dibagi-bagi ke dalam cawan Petri berdiameter 10-cm masing-masing sebanyak 20 mL per cawan dan dibiarkan dingin dan membeku sebelum digunakan.
Tunas bunga muda berukuran panjang 15,0 – 15.5 mm diambil dari tanaman induk. Antera yang berada di dalam tunas tersebut mengandung mikrospora dengan tahap perkembangan uninukleat. Tangkai bunganya dipotong dan ditinggalkan sepanjang kira-kira 5 cm. Untuk aplikasi pra-perlakuan, tunas-tunas bunga tersebut disisipkan pada botol vial yang berisi larutan starvasi manitol. Larutan starvasi manitol disiapkan berdasarkan resep Kyo dan Harada (1986) yang terdiri atas KCl 1,49 g L-1, MgSO
4 0,12 g L-1, CaCl2 0,11 g
L-1, KH2PO4 0,14 g L-1 dan manitol 54,7 g
L-1 dengan pH 7,0. Selanjutnya tunas-tunas tersebut diinkubasikan pada suhu rendah (4oC) atau suhu kamar (25oC) dalam keadaan gelap total selama 2, 4, 6 dan 8 hari.
Setelah periode pra-perlakuan, antera diisolasi dari dalam tunas bunga dan dikulturkan pada medium yang telah disiapkan. Kultur selanjutnya dipelihara di dalam ruangan dengan intensitas cahaya 50 µmol m-2 s-1 dan fotoperiodesitas 16 jam serta suhu 25 ± 1oC. Perkembangan
perlakuan terdiri atas 5 ulangan (cawan Petri) yang masing-masing terdiri atas 10 antera yang berasal dari satu tunas bunga yang sama.
HASIL DAN PEMBAHASAN
Hasil pengamatan menunjukkan bahwa pra-perlakuan antera dengan larutan manitol pada suhu 4oC selama periode waktu 2 hingga 8 hari memberikan persentase eksplan membentuk kalus yang lebih tinggi dibandingkan dengan pra-perlakuan pada suhu 25oC untuk setiap periode waktu yang diuji (Tabel 1). Kecenderungan yang nampak adalah pada suhu 4oC persentase antera membentuk kalus meningkat seiring dengan bertambahnya masa inkubasi pra-perlakuan. Sebaliknya, pada suhu 25oC persentase antera membentuk kalus makin berkurang dengan bertambahnya masa inkubasi pra-perlakuan.
Proliferasi kalus terjadi dalam waktu dua minggu setelah inisiasi kultur.
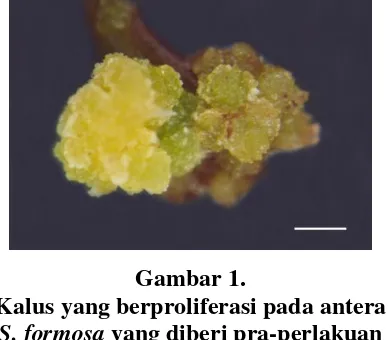
Selanjutnya kalus tersebut tumbuh dengan cepat dan dalam waktu 4 minggu kemudian hampir seluruh permukaan antera tertutup oleh massa kalus. Kalus yang terbentuk pada umumnya memiliki struktur yang remah dengan warna yang bervariasi dari kuning kehijauan pada pra-perlakuan suhu 4oC (Gambar 1) hingga
kuning kecoklatan pada pra-perlakuan suhu 25oC (Gambar 2).
Kalus pertama kali terbentuk pada bagian tengah antera di mana terjadi perlukaan filamen. Hal ini menjadi petunjuk bahwa jaringan kalus tersebut berkembang dari sel-sel somatik diploid. Identik dengan hal ini Henry (1998) mengemukakan bahwa pada kultur antera sejumlah tanaman seperti tembakau dan beberapa spesies dari famili Brassicaceae, Poaceae dan Solanaceae, seringkali jaringan-jaringan somatik seperti filamen, jaringan penghubung, dinding antera maupun tapetum meregenerasikan embrio-embrio diploid.
Tabel 1.
Pengaruh pra-perlakuan stress dalam periode waktu yang berbeda terhadap persentase pembentukan kalus pada kultur antera S. formosa.
Suhu Lama pra-perlakuan
inkubasi 2 hari 4 hari 6 hari 8 hari
4oC 98.2 ± 1,48 98.4 ± 1,48 98.4 ± 2,07 98.6 ± 1,35
25oC 92.6 ± 2,12 89.8 ± 1,48 86.2 ± 2,90 82.6 ± 2,84
Gambar 1.
Kalus yang berproliferasi pada antera
S. formosa yang diberi pra-perlakuan starvasi manitol pada suhu 4oC selama
8 hari. Bar = 1 mm.
Gambar 2.
Kalus yang berproliferasi pada antera
S. formosa yang diberi pra-perlakuan starvasi manitol pada suhu 25oC
selama 8 hari. Bar = 1 mm.
Dari penelitian ini terungkap bahwa pra-perlakuan stress dengan inkubasi manitol pada suhu 4oC penting bagi induksi kalus dari antera S. formosa. Namun demikian, pra-perlakuan stres ini belum memadai untuk kenginduksi respon androgenetik pada mikrospora yang terdapat di dalam antera yang dikulturkan. Hal ini dapat disebabkan oleh beberapa faktor, seperti genotipe tanaman, kondisi lingkungan kultur maupun komposisi medium kultur yang digunakan (Taji et
al., 2002). Pada kultur antera Nicotiana tabacum (Kyo and Harada, 1986) dan
Triticum aestivum (Touraev et al., 1996), pra-perlakuan stres diperlukan untuk menghambat perkembangan gametofitik dan memicu embriogenesis mikrospora. Namun pada S. formosa, pra-perlakuan stres saja nampaknya belum cukup untuk menginduksi embriogenesis mikrospora. Hal ini kemungkinan disebabkan oleh sifat rekalsitran dari jaringan tanaman ini. Menurut Van Doorne et al. (1995) tanaman legum (di mana S. formosa
termasuk di dalamnya) merupakan kelompok tanaman yang memiliki jaringan yang rekalsitran sehingga sulit untuk meregenerasikan tanaman melalui kultur
in vitro.
KESIMPULAN DAN SARAN
Dari penelitian ini dapat disimpulkan bahwa inkubasi antera di dalam larutan manitol pada suhu 4oC
sebelum inisiasi kultur dapat mendorong proliferasi kalus pada antera S. formosa.
Namun demikian, pra-perlakuan yang diberikan masih belum cukup memadai untuk menginduksi embriogenesis mikrospora. Diperkirakan ada beberapa faktor lain yang terlibat di dalamnya, sehingga penelitian lebih lanjut hendaknya difokuskan pada optimasi pra-perlakuan antera yang dikombinasikan dengan faktor-faktor lain yang mungkin berpengaruh.
DAFTAR PUSTAKA
and R Williams) pp. 201-208. (University of New England Press) Bayliss, K. L., Wroth, J. M. dan Cowling,
W. A. 2002. Production of multicellular microspores of Lupinus
species: first step toward haploid lupin embryos. In 'The Importance of Plant Tissue Culture and Biotechnology in Plant Sciences'. Armidale. (Eds A Taji and R Williams) pp. 145-157. (University of New England Press)
Custers, J., Visser, M., Snijder, R., Litovkin, K. dan Geest, L. v. d. 2001. 'Model plants pave the way to haploid
technology; microspore
embryogenesis in ornamentals.' Plant Research International B.V., Wageningen, The Netherlands. Gamborg, O. L., Millers, R. A. dan Ojima,
K. 1968. Nutrient requirements of suspension cultures of soybean root cells. Experimental Cell Research 50: 151-158.
Henry, Y. 1998. Origin of microspore-derived dihaploid and polyhaploid in vitro plants. Plant Tissue Culture and Biotechnology 4: 127-135.
Höfer, M., Touraev, A. dan Heberle-Bors, E. 1999. Induction of embryogenesis from isolated apple microspores. Plant Cell Reports 18: 1012-1017. Immonen, S. dan Anttila, H. 1999. Cold
pretreatment to enhance green plant regeneration from rye anther culture. Plant Cell, Tissue and Organ Culture 57: 121-127.
Kaur, P. dan Bhalla, J. K. 1998. Regeneration of haploid plants from microspore culture of pigeon pea (Cajanus cajun L.). Indian Journal of Experimental Biology 36: 736-738. Kyo, M. dan Harada, H. 1986. Control of
the developmental pathway of
tobacco pollen in vitro. Planta 168: 427-432.
Lentini, Z., Reyes, P., Martínez, C. P. dan Roca, W. M. 1995. Androgenesis of highly recalcitrant rice genotypes with maltose and silver nitrate. Plant Science 161: 677-683.
Lichter, R. 1982. Induction of haploid plants from isolated pollen of Brassica
napus. Zeitschrift für
Pflanzenphysiologie 105: 427-434. Tade, E. 1992. Anther and ovule culture
of Clianthus formosus. Master of Rural Science thesis, University of New England.
Taji, A., Kumar, P. dan Lakshmanan, P. 2002. 'In Vitro Plant Breeding.' (Haworth Press, Inc.: New York) Tomasi, P., Dierig, D. A., Backhaus, R. A.
dan Pigg, K. B. 1999. Floral bud and mean petal length as morphological predictors of microspore cytological stage in Lasquerella. HortScience 34: 1269-1270.
Touraev, A., Indrianto, A., Wratschko, I. dan Vicente, O. 1996. Efficient microspore embryogenesis in wheat (Triticum aestivum L.) induced by starvation at high temperature. Sexual Plant Reproduction 9: 209-215. Van Doorne, L. E., Marshal, L. E. dan
Kirkwood, R. C. 1995. Somatic embryogenesis in pea (Pisum sativum
L.): effect of explant, genotype and culture condition. Annals of Applied Biology 126: 169-174.
Zagorska, N., Dimitrov, B., Gadeva, P. dan Robeva, P. 1997. Regeneration and characterisation of plants obtained from anther culture of