point planetary ball mill selama 20 jam. Hasil penggerusan kemudian dikalsinasi pada suhu 400°C dan 800°C. Hasil kalsinasi kemudian dibentuk pellet dengan tekanan 140 MPa dan disinter pada suhu 1000°C dan 1100°C yang ditahan selama 12 jam. Proses penyinteran dilakukan dengan kondisi atmosfir udara bebas dan didiamkan dalam tungku sampai suhu kamar. Persentase rata-rata penyusutan massa sampel hasil penyinteran adalah 25,84% untuk kalsinasi 400°C dan 11,67% untuk kalsinasi 800°C. Hasil difraksi sinar-X sampel-sampel hasil penyinteran menunjukkan sudah terbentuknya fasa Ca3Co2O6, meskipun masih terdapat fasa-fasa yang lain. Sampel dengan kalsinasi 800°C yang disinter pada suhu 1000°C dan ditahan selama 12 jam menunjukkan mayoritas terbentuk fasa Ca3Co2O6.
Kata kunci: Sintesis, Reaksi padatan, Ca3Co2O6, Kalsinasi, Fasa
PENDAHULUAN
Material Ca3Co2O6 merupakan material yang dapat dimanfaatkan sebagai katoda
solid-oxide fuel cell (SOFC)[1], termoelektrik [2]–[4], dan pigmen untuk pelapisan[5]. Menurut Tao Wei, dkk, Senyawa Ca3Co2O6 (CCO) sangat menarik karena mempunyai perilaku
magnetik, listrik dan termoelektrik yang baik. Sedangkan menurut Kouta iwasaki, dkk, Ca3Co2O6 mempunyai nilai hambat jenis 1,63x102-1,33x10-1 Ωcm pada suhu 127 ke 897°C,
koefisien Seebeck dari 660 ke 140 μV/K seiring kenaikan suhu dari 77 ke 897°C dan faktor daya 1,6x10-5 W/(mK2) pada suhu 877°C, sehingga material ini mempunyai potensi sebagai termoelektrik meskipun nilai figure of merit pada suhu mutlak (ZT) 0,15 pada suhu 800°C (material termoelektrik, ZT > 1)[6].
Jika dibandingkan dengan material Ca3Co4O9 yang mempunyai nilai ZT ~0,87[7] nilai ZT Ca3Co2O6 sangat jauh, tetapi senyawa Ca3Co2O6 lebih stabil dibandingkan Ca3Co4O9[8]. Fasa Ca3Co4O9 stabil sampai suhu 926°C dan terurai menjadi Ca3Co2O6, dimana stabil pada
suhu1026°C [6], [9]. Sehingga beberapa penelitian dilakukan untuk meningkatkan performa material Ca3Co2O6 dengan cara pendopingan unsur-unsur tertentu[2], [4], [6], [9].
Gambar 1. Struktur kristal Ca3Co2O6[2,4]
Ca3Co2O6 mempunyai struktur kristal dengan sistem orthorombik dan grup ruang R-3c.
parameter kisi kristal Ca3Co2O6 adalah a = ~9,08Å, dan c = ~10,38 Å pada suhu kamar[2,4,10].
Berdasarkan sifat-sifat dan manfaat material Ca3Co2O6 tersebut maka dilakukan
percobaan sintesis material Ca3Co2O6. Sintesis menggunakan metode reaksi padatan dengan
bahan baku CaCO3 dan CoCO3[11,12].
METODE PERCOBAAN
Sintesis Ca3Co2O6 menggunakan metode reaksi padatan. Bahan baku yang digunakan
adalah serbuk CaCO3 dan CoCO3. Percobaan diawali dengan menimbang kedua bahan baku
sesuai dengan perhitungan stoikiometri. Setelah penimbangan, kedua bahan dicampur dan digerus menggunakan four point planetary ball mill selama 24 jam. Hasil penggerusan kemudian dikalsinasi pada suhu 400°C dan 800°C. Hasil kalsinasi digerus kembali dan kemudian dibentuk pellet dengan tekanan 140 MPa dan disinter pada suhu 1000°C dan 1100°C yang ditahan selama 20 jam. Proses penyinteran dilakukan dengan kondisi atmosfir udara bebas dan didiamkan dalam tungku sampai suhu kamar. Diagram alir percobaan ditunjukkan pada Gambar 2.
Dari Tabel 1 terlihat bahwa seiring dengan kenaikan suhu kalsinasi dan penyinteran, penyusutan massa semakin besar. Hal ini dapat dihubungkan dengan reaksi pembentukan material dari bahan baku. Reaksi pembentukan material Ca3Co2O6 dari bahan baku CaCO3
dan CoCO3 dituliskan pada persamaan 1.
3CaCO3(s) + 2CoCO3(s) + ½ O2(g) Ca3Co2O6(s) + 5CO2(g) (1)
Dari persamaan 1 terlihat bahwa reaksi pembentukan Ca3Co2O6 disertai dengan pelepasan gas
CO2. Pelepasan gas CO2 berasal dari reaksi dekomposisi CoCO3 menjadi Co3O4[11], [13]. Reaksi
dekomposisi CoCO3 dituliskan pada persamaan 2.
CoCO3(s) + ½O2(g) Co3O4(s) + CO2(g) (pada rentang suhu 250-370ºC)[13], [14] (2)
Selain reaksi dekomposisi CoCO3, pelepasan gas CO2 terjadi karena reaksi dekomposisi
CaCO3 menjadi CaO. Reaksi dekomposisi CaCO3 dituliskan pada persamaan 3.
CaCO3(s) CaO(s) + CO2(g) (pada suhu >800°C)[15] (3)
Menurut I. Halikia, dkk, reaksi dekomposisi CaCO3 terjadi pada suhu diatas 800°C,
sehingga terlihat bahwa penyusutan massa dengan suhu kalsinasi 800°C lebih besar dari suhu 400°C.
Dengan proses kalsinasi ini diharapkan bahwa pembentukan Ca3Co2O6 terjadi dari
senyawa logam oksidanya. Sehingga dapat mengurangi pengotor karbon dalam senyawa yang terbentuk.
Analisis difraksi sinar-x
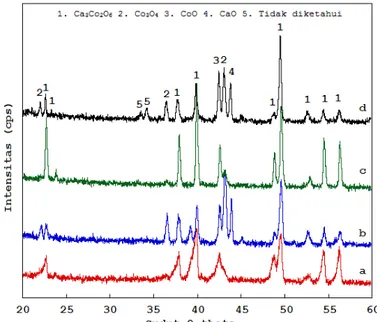
Sampel hasil penyinteran dikarakterisasi menggunakan difraktometer sinar-X untuk mengetahui fasa material yang terbentuk. Difraktometer sinar-x memakai cobalt dengan panjang gelombang, λ = 1,789 Å sebagai sumber radiasi. Pengukuran dilakukan pada rentang sudut 2 = 20 – 60. Pola difraksi sinar-x sampel-sampel hasil penyinteran ditunjukkan pada
Gambar 3. Pola difraksi sinar-x sampel, a). kalsinasi 400°C penyinteran 1000°C, b). kalsinasi 400°C penyinteran 1100°C, c). kalsinasi 800°C penyinteran 1000°C[11,12],
dan d). kalsinasi 800°C penyinteran 1100°C[11]
Berdasarkan pola difraksi sinar-x, terlihat bahwa pada sampel kalsinasi 400°C dan suhu penyinteran 1000°C sudah terlihat pembentukan fasa Ca3Co2O6. Puncak-puncak yang
merupakan puncak Ca3Co2O6 adalah puncak pada sudut 2= 22,74; 37,96; 39,94; 48,84; 49,6;
54,52; dan 56,3°. Puncak-puncak tersebut sesuai dengan JCPDS No. 089-0629[16]. Meskipun puncak-puncak pola difraksi sudah menunjukkan pembentukan fasa Ca3Co2O6, tetapi
intensitas puncak masih terlihat kasar. Jika dibandingkan dengan pola difraksi sampel kalsinasi 800°C dan suhu penyinteran 1000°C, terlihat intensitas puncak-puncak pola difraksi fasa Ca3Co2O6 terlihat sangat halus. Selain fasa Ca3Co2O6, ternyata masih terdapat fasa-fasa
lain yaitu, Co3O4[17] dan CoO[18]. Puncak-puncak yang memperlihatkan fasa Co3O4 adalah
puncak pada sudut 2=43,06°. Sedangkan puncak CoO pada sudut 2=42,62°. Masih terdapat fasa ikutan ini mungkin disebabkan oleh tidak ikut bereaksinya bahan baku CoCO3 dengan
CaCO3.
Sedangkan pola difraksi pada sampel kalsinasi 400°C dan 800°C dengan suhu penyinteran 1100°C terlihat bahwa fasa-fasa lain yang terbentuk selain Ca3Co2O6 adalah
Co3O4, CoO, CaO dan beberapa puncak tidak diketahui fasanya. Hal ini terlihat pada
intensitas pola difraksi yang semakin besar.
KESIMPULAN
Pembentukan material Ca3Co2O6 dapat dilakukan menggunakan metode reaksi
padatan. Meskipun fasa Ca3Co2O6 sudah terbentuk, ternyata masih ada fasa-fasa lain yang
terbentuk juga. Proses kalsinasi mempengaruhi pembentukan senyawa oksida. Untuk menghasilkan fasa Ca3Co2O6 yang paling baik dilakukan dengan suhu kalsinasi 800°C dan
penyinteran pada suhu 1000°C.
DAFTAR PUSTAKA
1. T. Wei, Y.-H. Huang, R. Zeng, L.-X. Yuan, X.-L. Hu, W.-X. Zhang, L. Jiang, J.-Y. Yang, and Z.-L. Zhang, “Evaluation of Ca3Co2O6 as cathode material for
high-of the Thermoelectric Application Using A Reaction- Sintering Process,” J. Aust. Ceram. Soc, vol. 44, no. 1, pp. 17–22, 2008.
8. N. Van Nong and M. Ohtaki, “Power factors of late rare earth-doped Ca3Co2O6 oxides,”
Solid State Commun., vol. 139, no. 5, pp. 232–234, 2006.
9. D. Lu, G. Chen, J. Pei, X. Yang, and H. Xian, “Effect of erbium substitution on thermoelectric properties of complex oxide Ca3Co2O6 at high temperatures,” J. Rare
Earths, vol. 26, no. 2, pp. 168–172, 2008.
10. B. Raveau and M. Seikh, Cobalt Oxides: From Crystal Chemistry to Physics, vol. 1. 2012.
11. S. D. Yudanto, “Sintesis Ca3Co2O6 dan CaMnO3 dari Bahan Baku CaCO3, CoCO3 dan
MnCO3 Melalui Proses Reaksi Padatan,” 2014.
12. S. D. Yudanto and A. Imaduddin, “Studi Arus Bolak-Balik Material Ca3Co2O6,” Maj.
Metal., vol. 29, no. 2, pp. 97–102, 2014.
13. C.-H. Wu, “Low Energy-Consumption Industrial Production of Ultra-Fine Spherical Cobalt Powders,” Energy Conserv., 2012.
14. S. D. Yudanto and S. A. Chandra, “Preparasi, Sintesis dan Karkaterisasi Material Oksida Ca3Co4O9,” Maj. Metal., vol. 30, no. 1, pp. 25–30, 2015.
15. I. Halikia, L. Zoumpoulakis, E. Christodoulou, and D. Prattis, “Kinetic study of the thermal decomposition of calcium carbonate by isothermal methods of analysis,” Eur. J. Miner. Process. Environ. Prot., vol. 1, no. 2, pp. 89–102, 2001.
16. S. Kahatta, N. Chaiyo, C. Ruttanapun, W. Techitdheera, B. Boonchom, and N. Vittayakorn, “Preparation and Thermoelectric Properties of Ca3Co2O6 Ceramics by
Microwave-Assisted Solution Combustion Method,” 38th Congr. Sci. Technol. Thail., 2008.
17. L. Xue, C. Zhang, H. He, and Y. Teraoka, “Promotion effect of residual K on the decomposition of N2O over cobalt–cerium mixed oxide catalyst,” Catal. Today, vol.
126, no. 3–4, pp. 449–455, 2007.
18. M. Th. Makhlouf, B. M. Abu-Zied, and T. H. Mansoure, “Direct Fabrication of Cobalt Oxide Nano-particles Employing Glycine as a Combustion Fuel,” Phys. Chem., vol. 2, no. 6, pp. 86–93, 2013.
![Gambar 1. Struktur kristal Ca 3 Co 2 O 6 [2,4]](https://thumb-ap.123doks.com/thumbv2/123dok/4077676.2791846/2.892.312.568.89.380/gambar-struktur-kristal-ca-co-o.webp)