4
Pembahasan
Pada penelitian ini tiga senyawa metabolit sekunder telah berhasil diisolasi dari dan
Desmodium triquetrum Linn. Senyawa tersebut antara lain asam p-hidroksi benzoat (58) dan
kaempferol (33), dan epikatekin (59).
4.1Senyawa Asam p-Hidroksi Benzoat (58)
Senyawa asam p-hidroksi benzoat (58) diperoleh berupa padatan berwarna putih sebanyak 12 mg. Senyawa ini larut dalam aseton. Pada spektrum 13C-NMR menunjukkan adanya 7 sinyal karbon 4 diantaranya menunjukkan sinyal karbon metin aromatik δC 132,7 ppm (2C)
dan δC 115,9 ppm (2C), 1 sinyal karbon kuarterner aromatik (δC 122,6 ppm), 1 sinyal oksiaril
(δC 162.5 ppm) dan satu sinyal karbonil terkonjugasi dari gugus asam karboksilat (δC 167.4
ppm).
Hasil data spektroskopi 1H NMR memberikan dua sinyal proton doblet dan simetri yaitu pada δH 7,90 ppm (2H) dan δH 6,91 ppm (2H) di daerah proton aromatik. Kedua sinyal ini
juga memberikan nilai tetapan kopling (J) yang sama yaitu 7,6 Hz. Hal ini menunjukkan adanya sinyal proton yang berorientasi orto.
Gambar 4.2 Spektrum 1H NMR dari asam p-hidroksi benzoat (58) (Aseton-d6, 300 MHz)
Untuk memperkuat asumsi bahwa senyawa yang diisolasi adalah asam p-hidroksi benzoat (58) maka dibandingkan data spektrum 1H NMR dan 13C NMR dengan data literatur yaitu asam p-hidroksi benzoat (58) dari Camellia oleifera (Bin, 2002).
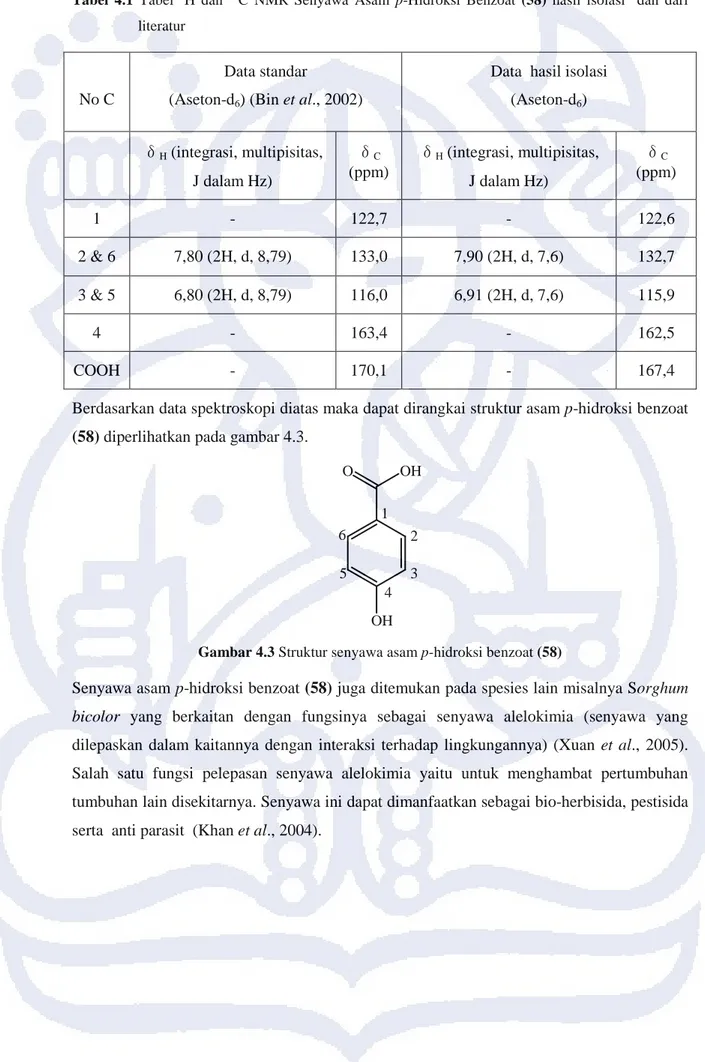
Tabel 4.1 Tabel 1H dan 13C NMR Senyawa Asam p-Hidroksi Benzoat (58) hasil isolasi dan dari literatur
No C
Data standar
(Aseton-d6) (Bin et al., 2002)
Data hasil isolasi (Aseton-d6) δH (integrasi, multipisitas, J dalam Hz) δC (ppm) δH (integrasi, multipisitas, J dalam Hz) δC (ppm) 1 - 122,7 - 122,6 2 & 6 7,80 (2H, d, 8,79) 133,0 7,90 (2H, d, 7,6) 132,7 3 & 5 6,80 (2H, d, 8,79) 116,0 6,91 (2H, d, 7,6) 115,9 4 - 163,4 - 162,5 COOH - 170,1 - 167,4
Berdasarkan data spektroskopi diatas maka dapat dirangkai struktur asam p-hidroksi benzoat (58) diperlihatkan pada gambar 4.3.
OH O OH 1 2 4 3 5 6
Gambar 4.3 Struktur senyawa asam p-hidroksi benzoat (58)
Senyawa asam p-hidroksi benzoat (58) juga ditemukan pada spesies lain misalnya Sorghum
bicolor yang berkaitan dengan fungsinya sebagai senyawa alelokimia (senyawa yang
4.2Senyawa Epikatekin (59)
Data spektroskopi yang diperoleh dalam menentukan struktur epikatekin (59) ini antara lain DEPT 135, DEPT 90, 13C NMR broad band decoupling, dan spektrum 1H NMR. DEPT 135 memberikan data yaitu sinyal positif untuk metil (-CH3) dan metin (-CH) serta sinyal negatif
untuk metilen (-CH2). DEPT 90 memberikan data sinyal metin saja (-CH) tanpa adanya
sinyal metilen (-CH2) dan metin (-CH). Bila dibandingkan dengan 13
C NMR broad band
decoupling maka akan diidentifikasi sinyal karbon kuarterner yang akan muncul di
spektroskopi 13C NMR total tetapi tidak muncul di DEPT 135 dan DEPT 90.
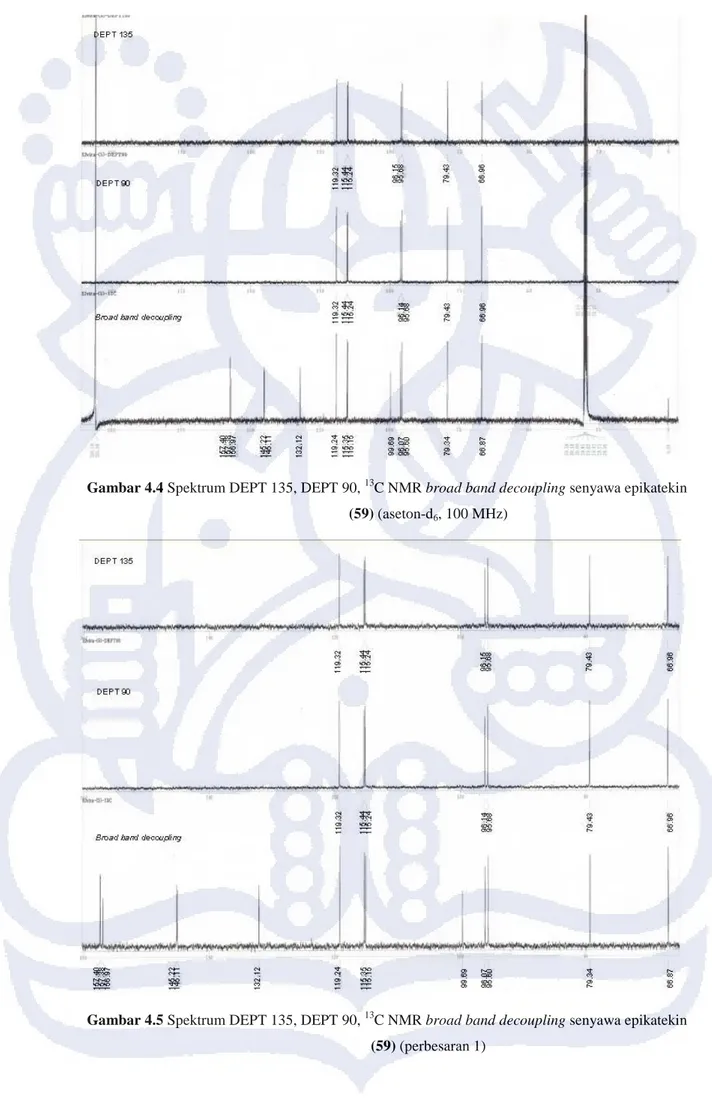
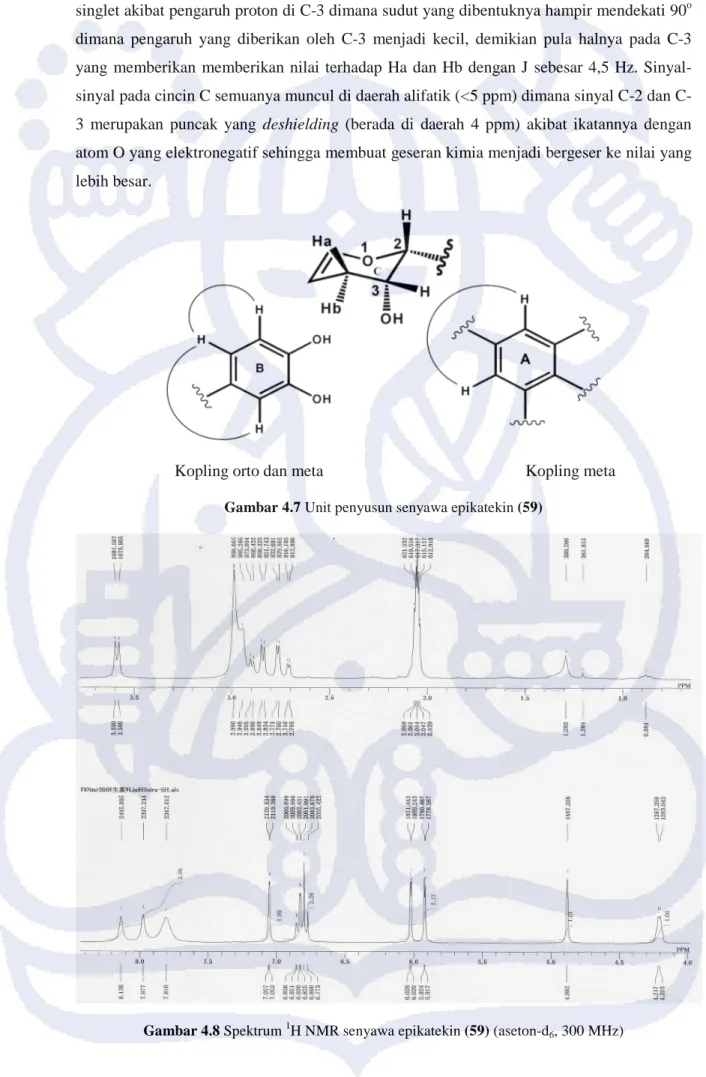
Hasil dari data DEPT 135, DEPT 90 dan NMR 13C broad band decoupling menghasilkan adanya puncak sebanyak 15 karbon seperti yang terlihat pada gambar 4.4. Kemungkinan dari jumlah total karbon sebanyak 15 adalah suatu senyawa alam seskuiterpen atau senyawa alam berupa flavonoid. Akan tetapi spektrum NMR memperlihatkan adanya sinyal di daerah aromatik sehingga dipastikan senyawa yang telah diisolasi berupa flavonoid. Pada gambar 4.5 terlihat pada DEPT 135 terdapat dua sinyal metin (-CH) SP3 yang berikatan dengan oksigen yaitu δC 66,96 ppm (C-3) dan δC 79,43 ppm (C-2). C-2 yang lebih deshieding akibat
pengaruh aromatik dan oksigen. Selain itu, terdapat 5 sinyal karbon aromatik berupa metin aromatik (=CH) 95,7 ppm (C-8), 96.1 ppm (C-6), 115,4 ppm (C-2’), 115,2 ppm (C-5’), 119,3 ppm (C-6’). Terdapat pula 5 sinyal untuk oksiaril yaitu 145,1 ppm (C-4’), 145,2 ppm (C-3’), 157,4 ppm (C-5), 157,4 ppm (C-7) dan 157,0 ppm (C-8a). Spektrum DEPT 90 dan sinyal positif pada DEPT 135 menunjukkan jumlah sinyal yang sama, oleh karena itu dapat dipastikan bahwa tidak terdapat gugus metil. Dari 13C NMR terdapat 2 sinyal karbon kuarterner di 99,7 ppm (C-4a) dan 132,1 ppm (C-1’). Sinyal negatif pada DEPT 135 menunjukkan adanya sinyal metilen (-CH2) di daerah alifatik 29.1 ppm dan dipastikan
Gambar 4.4 Spektrum DEPT 135, DEPT 90, 13C NMR broad band decoupling senyawa epikatekin
(59) (aseton-d6, 100 MHz)
Gambar 4.5 Spektrum DEPT 135, DEPT 90, 13C NMR broad band decoupling senyawa epikatekin
Gambar 4.6 Spektrum DEPT 135, DEPT 90, 13C NMR broad band decoupling senyawa epikatekin
(59) (perbesaran 2)
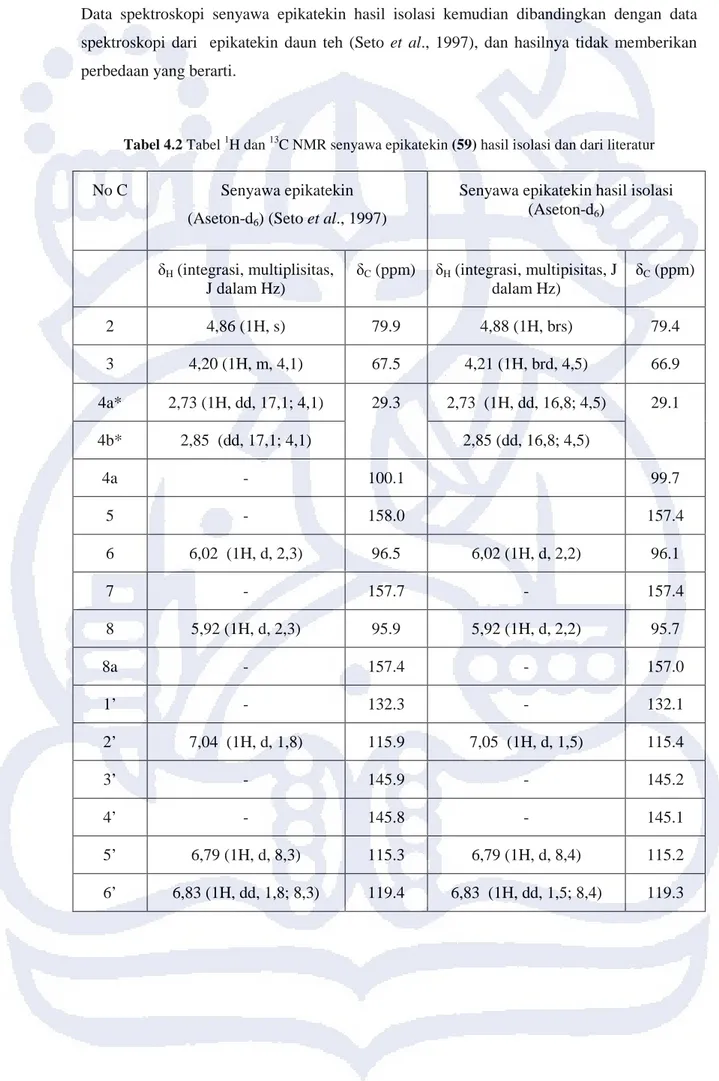
Data spektroskopi 1H NMR menunjukkan adanya sepasang sinyal proton aromatik di H-8 pada δH 5,92 (d, J= 2,2) dan H-6 pada δ 6,02 (d, J=2,2) di cincin A. Hal ini menunjukkan
adanya hubungan kopling meta dilihat dari nilai tetapan kopling sebesar 2,2 Hz. Sedangkan pada sinyal dengan δH 7,05 (1H, d, 1,5) di C-2’, di C-5’ pada δH 6,79 (1H, d, 8,4), dan di
C-6’ pada δH 6,83 (1H, dd, 1,5; 8,4) menunjukkan adanya spin ABX pada cincin B. Sinyal
yang memiliki multiplisitas doblet doblet yaitu pada δ 6,83 memiliki korelasi orto di J= 8,4 Hz dengan C-5’ dan korelasi meta dengan C-2’ dengan J= 1,5 Hz. C-2’ berkorelasi meta dengan C-6’ dengan nilai J=1,5 Hz demikian pula C-5’ yang berkorelasi orto dengan C-6’ dengan nilai J= 8,4 Hz.
singlet akibat pengaruh proton di C-3 dimana sudut yang dibentuknya hampir mendekati 90o dimana pengaruh yang diberikan oleh C-3 menjadi kecil, demikian pula halnya pada C-3 yang memberikan memberikan nilai terhadap Ha dan Hb dengan J sebesar 4,5 Hz. Sinyal-sinyal pada cincin C semuanya muncul di daerah alifatik (<5 ppm) dimana Sinyal-sinyal 2 dan C-3 merupakan puncak yang deshielding (berada di daerah 4 ppm) akibat ikatannya dengan atom O yang elektronegatif sehingga membuat geseran kimia menjadi bergeser ke nilai yang lebih besar.
Kopling orto dan meta Kopling meta
Gambar 4.7 Unit penyusun senyawa epikatekin (59)
Data spektroskopi senyawa epikatekin hasil isolasi kemudian dibandingkan dengan data spektroskopi dari epikatekin daun teh (Seto et al., 1997), dan hasilnya tidak memberikan perbedaan yang berarti.
Tabel 4.2 Tabel 1H dan 13C NMR senyawa epikatekin (59) hasil isolasi dan dari literatur
No C Senyawa epikatekin
(Aseton-d6) (Seto et al., 1997)
Berdasarkan data-data spektroskopi tersebut maka dapat dikemukakan bahwa struktur dari senyawa epikatekin (59) adalah sebagaimana ditunjukkan pada gambar dibawah ini
O OH OH OH OH HO 1 2 3 4 5 6 7 8 2' 3' 4' 5' 6'
Gambar 4.9 Struktur senyawa epikatekin (59)
Senyawa epikatekin (59) memiliki khasiat sebagai antioksidan dan banyak diperoleh pada tumbuhan teh yaitu Camellia sinensis dan juga terdapat pada D. uncinatum (Dixon et al., 2005).
4.3Senyawa Kaempferol (33)
Senyawa kaempferol (33) diisolasi dalam bentuk serbuk kuning sebanyak 2 mg dan 1,1 mg. Struktur senyawa ini dibuktikan dengan data spektroskopi yaitu 1H NMR. Hasil data spektroskopi menunjukkan terdapat enam siyal proton di daerah aromatik. Sinyal pada geseran kimia 6,26 ppm (d, J=1,7 Hz) dan 6, 53 ppm (d, J=1,7 Hz) menunjukkan adanya proton pada posisi C-6 dan C-8 dari cincin A.
Gambar 4.10 Spektrum 1H NMR dari senyawa kaempferol (33) (aseton-d6 300 MHz)
Sinyal δH 7,01 ppm dan δH 8,15 ppm terlihat adanya sinyal dengan multiplisitas doblet yang
nilai δH 7,01 ppm menunjukkan proton pada posisi 3’ dan 5’ dan sinyal pada δH 8,15 ppm
adalah proton di posisi 2’ dan 6’.
Tabel 4.3 Tabel 1H NMR senyawa kaempferol (33) hasil isolasi dan dari literatur
No 1H-NMR Kaempferol
δH (integrasi, multiplisitas, J dalam Hz)
(Aseton-d6, 300 MHz)
(Hadizadeh et al., 2003)
1
H-NMR Kaempferol hasil isolasi δH (integrasi, multiplisitas, J dalam
Hz) (Aseton-d6, , 300 MHz) H-6 6.28 (1H, d, 2) 6.26 (1H, d, 1,7) H-8 6.48 (1H, d, 2) 6.53 (1H, d, 1,7) H-2’ & 6’ 8.05 (2H, d, 9) 8.15 (2H, d , 8,8) H-3’ & 5’ 6.95 (2H, d, 9) 7.01 (2H, d, 8,8)
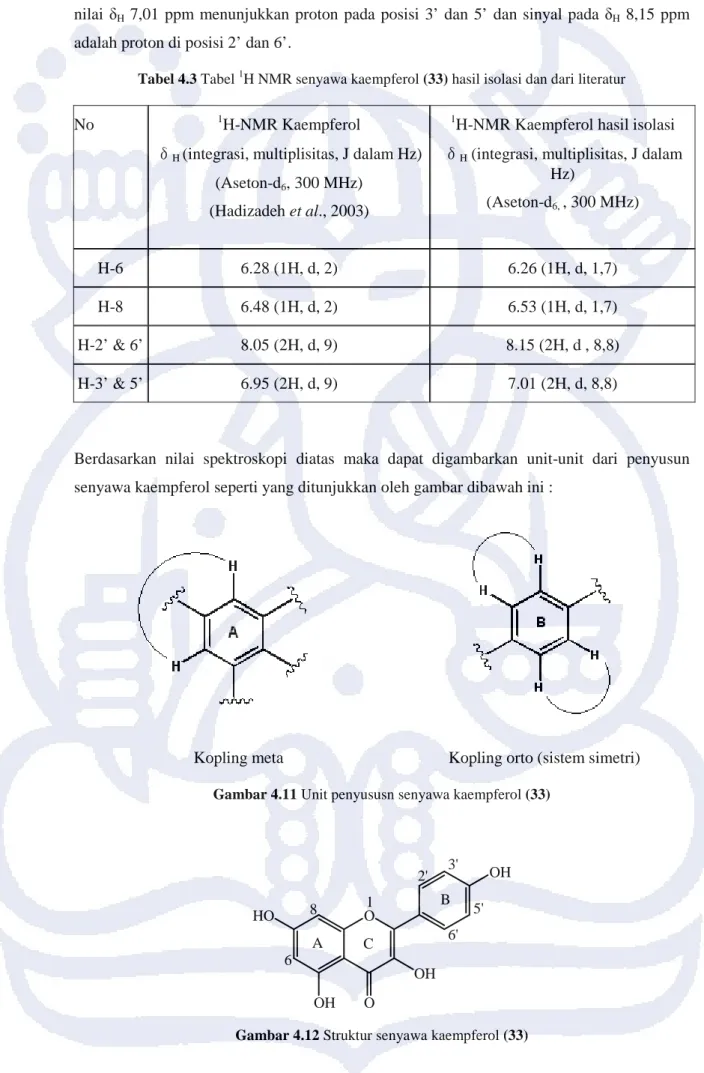
Berdasarkan nilai spektroskopi diatas maka dapat digambarkan unit-unit dari penyusun senyawa kaempferol seperti yang ditunjukkan oleh gambar dibawah ini :
Kopling meta Kopling orto (sistem simetri)
Gambar 4.11 Unit penyususn senyawa kaempferol (33)
A B O HO OH OH OH O 6 8 1 2' 3' 5' 6' C
Dilihat dari data hasil isolasi dan data literatur menunjukkan kesamaan seperti yang dapat dilihat pada tabel 4.3. Senyawa kempferol (33) diketahui memiliki bioaktifitas sebagai antiinflamasi dan ditemukan di tumbuhan D. styrachifolium (Park et al., 2007).
4.4Hubungan Biogenesis Senyawa yang Telah Berhasil Diisolasi
Senyawa kaempferol (33), asam p-hidroksi benzoat (58) dan epikatekin (59) jika dilihat dari jalur biosintesisnya dapat disimpulkan bahwa senyawa asam p-hidroksi benzoat (58) adalah senyawa yang paling sederhana sedangkan senyawa kaempferol (33) dan epikatekin (59) memiliki tingkat oksidasi yang lebih tinggi..
Jalur biogenesis asam p-hidroksi benzoat (58) bermula dari asam shikimat yang kemudian dengan banyak tahap menjadi asam p-kumarat, lalu asam p-kumarat dengan bantuan enzim
p-hidroksibenzaldehid sintase (HBS) dan p-hidroksibenzaldehid dehidrogenase (HBD)
membentuk senyawa asam p-hidroksi benzoat (58) (Schnitzler et al., 1992) (Sircar dan Mitra, 2007).
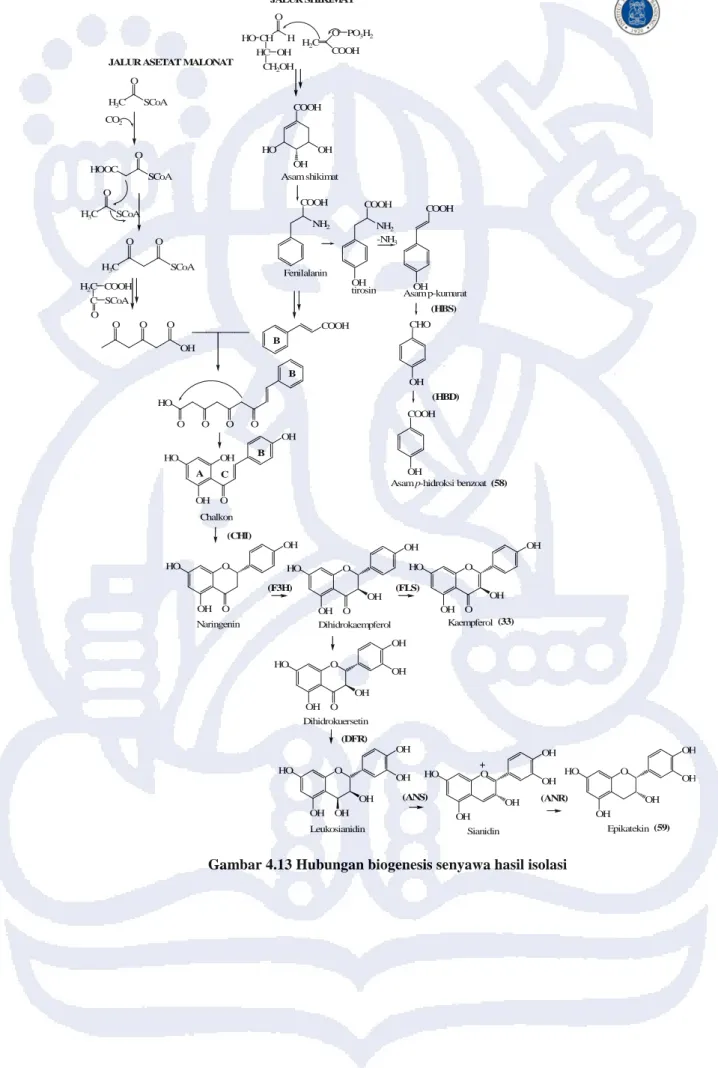
Berbeda dengan pembentukan senyawa asam p-hidroksi benzoat (58), pembentukan senyawa flavonoid bermula dari penggabungan dua jalur yaitu jalur shikimat dan jalur asetat malonat dan membentuk senyawa calkon, kemudian dengan bantuan enzim; chalkon isomerase (CHI); flavanon-3-β-hidroksilase (F3H); serta flavonol sintase (FLS) membentuk senyawa kaempferol (33), kemudian dari enzim dihidroflavonol reduktase (DFR); antosianin sintase (ANS) dan antosianidin reduktase (ANR) membentuk senyawa epikatekin (59). (Marles et
CH H O HC CH2OH OH HO O PO3H2 COOH H2C COOH OH HO OH COOH Asam shikimat JALUR SHIKIMAT
JALUR ASETAT MALONAT
H3C SCoA O CO2 SCoA HOOC O H3C SCoA O H3C SCoA O O H2C COOH C SCoA O OH O O O B B HO O O O O COOH NH2 Fenilalanin COOH NH2 OH -NH3 COOH OH Asam p-kumarat tirosin CHO OH COOH OH (HBD) O OH HO OH Chalkon B A C O OH HO O O OH HO O OH Naringenin Dihidrokaempferol O OH HO O OH Kaempferol OH OH OH OH OH OH HO O OH Leukosianidin OH HO O OH OH OH OH OH Epikatekin O OH HO O OH OH OH Dihidrokuersetin OH HO O OH OH OH Sianidin (CHI) (HBS) (F3H) (FLS) (DFR) (ANS) (ANR)
Asam p-hidroksi benzoat (58)
(33)
(59)
4.5Bioaktivitas Senyawa-Senyawa Hasil Isolasi
Bioaktivitas dari ekstrak D .triquetrum, pada ekstrak tumbuhan D.triquetrum terhadap hasil uji tirosin kinase inhibitor adalah sebesar 47% inhibisi (100 µg/ml) dengan kontrol positif sebesar 66,2 % (ekstrak metanol (I)) dan sebesar 59,4% dengan kontrol positif 60,1% (ekstrak metanol (II)) sedangkan uji terhadap sel murin P-388 adalah IC50 sebesar 6,5 µg/mL
(ekstrak metanol (II)). Hasil % inhibisi ekstrak terhadap uji inhibitor tirosin kinase mendekati positif kontrol, dengan demikian ekstrak metanol kemungkinan mengandung senyawa yang aktif terhadap inhibitor tirosin kinase atau menghambat perbanyakan sel pembuluh darah baru ke tumor (angiogenesis) (Manash dan Mukhopadhyay, 2004), Demikian halnya dengan uji terhadap sel murin leukimia P-388 dimana ekstrak metanol memiliki sitotoksik yang tinggi (ekstrak dikatakan memberikan keaktifan jika IC50 < 20