TRITERPENOID DARI EKSTRAK KULIT BATANG AGLAIA EXIMIA (MELIACEAE) Mayshah Purnamasari, Julinton Sianturi, Desi Harneti, Unang Supratman*
Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Padjadjaran Jalan Raya Bandung-Sumedang Km. 21 Jatinangor 45363, Sumedang, Indonesia
*email:[email protected] Abstrak
Dua triterpenoid, damar-24-en-3α ,20,25-triol (1) dan damar-23-en-3α ,20-diol (2) telah diisolasi dari ekstrak metanol kulit batang Aglaia eximia (Meliaceae). Struktur kimia senyawa 1-2 diidentifikasi berdasarkan data spektroskopi (IR, NMR (1D dan 2D) dan MS) dan perbandingan data spektrum yang diperoleh sebelumnya.
Kata kunci: Aglaia eximia, Meliaceae, damar-23-en-3α ,20,25-triol dan damar-24-en-3α ,20-diol.
Abstract:
Two triterpenoids, dammar-24-ene-3α ,20,25-triol (1) and dammar-23-ene-3α ,20-diol (2) structures of compounds 1-2 were identified based on spectroscopes data (UV, IR, NMR (1D and 2D) and MS) and comparison with those previously reported.
Keyword: Aglaia eximia, Meliaceae, dammar-23-ene-3α ,20,25-triol and dammar-24-ene-3α ,20-diol
PENDAHULUAN
Genus Aglaia merupakan genus terbesar dari famili Meliaceae, dengan jumlah lebih dari 130 spesies (Su et al., 2006). Kandungan metabolit sekunder terbanyak pada tumbuhan ini adalah senyawa triterpenoid (Joycharat et al., 2010; Zhang et al., 2010), flavaglin (Engelmeier et al., 2000; Kim et al., 2006a; Chaidir et al., 1999), bisamida (Saifah et al., 1999; Kim, et al., 2006b), steroids (Rivero-Crus et al., 2004; Mohamad et al., 1999), limonoid (Fuzzati et al., 1996),
sesquiterpen (Joycharat et al., 2010), lignan (Brader et al., 1998), dan flavonoid (Nugroho
et al., 1999).
Secara khusus, senyawa triterpenoid yang telah diisolasi dari genus Aglaia mempunyai aktivitas biologis yang menarik, salah satunya adalah sitotoksik (Awang et al., 2012; Harneti et al., 2014). Dari skrining awal pengujian sitotoksik terhadap sel murin leukemia P-388 pada ekstrak metanol kulit batang Aglaia eximia diperoleh nilai IC50 40 µg/mL (Harneti et al., 2014). Aglaia eximia secara etnobotani digunakan sebagai penurun demam, pelembab paru, dan dapat mengobati penyak kulit (Heyne, 1987). Pada penelitian berkelanjutan ini, kami mengisolasi senyawa triterpenoid, yaitu damar-24-en-3α ,20,25-triol (1) dan damar-23-en-3α ,20-diol (2) dari
ekstrak kulit batang Aglaia eximia yang mempunyai aktivtas sitotoksik terhadap sel murin leukemia P-388.
Gambar 1. Struktur kimia yaitu damar-24-en-3α ,20,25-triol (1) dan damar-23-en-3α ,20-diol (2)
BAHAN DAN METODE
Bahan Tumbuhan
Bahan Kimia
Bahan kimia yang digunakan terdiri dari berbagai jenis pelarut teknis (didestilasi ulang) seperti; n-heksana, eti asetat, metanol, aseton, dan pro-analis seperti; diklorometan dan kloroform. Silika GF254 untuk KLT (kromatografi lapis tipis), Silika G60 (10-40
µm) dan luas permukaan (500 m2
/g) untuk Kromatografi cair vakum dan silika G60 (70-230 dan (70-230-400 mesh) untuk kromatografi kolom terbuka, serta pereaksi penampak noda H2SO410% dalam etanol.
Peralatan
Peralatan yang digunakan meliputi alat gelas yang umum digunakan di laboratorium kimia organik, maserator, rotary evaporator R-200 Buchi dengan pompa vakum Vac V-500 Buchi dan penangas air B-490 Buchi, kolom kromatografi terbuka berbagai ukuran, lampu UV Vilbert Luomart (λ 254 nm dan λ 365 nm), spektrofotometer FTIR Spectrum One Perkin Elmer, Spektrometer Nuclear Magnetic Resonance (NMR) JEOL JNM ECA-500 dengan TMS sebagai standard, spektrum massa dicatat menggunakan HR-ESI-TOFMS.
Ekstraksi dan Isolasi
Sebanyak 30 g ekstrak metanol kulit batang A. eximia dipisahkan dengan kromatografi vakum cair (KVC) fase diam silika gel G60 sistem gradien 10% dengan diklorometan (MTC): metanol dihasilkan 11 fraksi (A-K). Semua fraksi dianalisi dengan KLT menggunakan eluen MTC: metanol (8:2). Fraksi D dipisahkan dengan kolom kromatografi (KK) fasa diam silika gel G60 (70-230 mesh) sistem isokratik dengan diklorometan: metanol (9:1) dihasilkan 71 fraksi, yang digabungkan berdasarkan hasil KLT (D1-D9). Fraksi D1 dipisahkan dengan KK fasa diam silika gel G60 (70-230 mesh) sistem isokratik menggunakan n-heksana: etil asetat (9:1) dihasilkan 54 fraksi, yang digabungkan berdasarkan hasil KLT (D1A-D1D). Fraksi D1A dipisahkan dengan KK fasa diam silika gel G60 (70-230 mesh) sistem gradien 2,5% menggunakan n-heksana: etil asetat (10:0-5:5) dihasilkan 21 fraksi, yang digabungkan berdasarkan hasil KLT (D1A1-D1A8). Fraksi D1A6 dipisahkan dengan KK fasa diam silika gel G60(70-230 mesh) sistem
gradien 1% menggunakan
n-heksana:aseton (10:0- 8:2) dihasilkan 21 fraksi, yang digabungkan berdasarkan hasil KLT (D1A6A-D1A6D). Fraksi D1A6C dipisahkan dengan KK fasa diam silika gel G60 (70-230 mesh) sistem gradien 2% menggunakan n-heksana: etil asetat (10:0-7:3) dihasilkan 21 fraksi, diperoleh senyawa murni dari fraksi D1A6C6 (senyawa 1 (5 mg)). Fraksi D1B dipisahkan dengan KK fasa diam silika gel G60 (70-230 mesh) sistem isokratik menggunakan n-heksana: etil asetat ((9:1) dihasilkan 140 fraksi yang digabungkan berdasarkan hasil KLT (D1B1-D1B6). Fraksi D1B3 dimurnikan menggunakan KLT preparatif dengan n-heksana: etil asetat (8:2) dan diperoleh senyawa 2 (15 mg).
HASIL DAN PEMBAHASAN
bahwa rantai samping dari triterpenoid terikat pada C-17. Berdasarkan perbandingan data spektra yang diperoleh dengan data literatur (Pakhathirathien et al., 2005), maka senyawa 1 diidentifikasi sebagai damar-23-en-3α ,20,25-triol.
Gambar 1. Korelasi HMBC senyawa 1
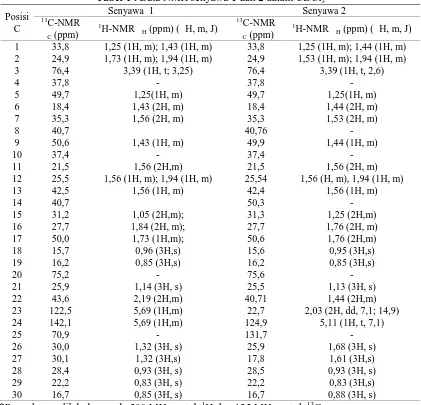
Tabel 1 . Data NMR senyawa 1 dan 2 dalam CDCl3 Posisi
C
Senyawa 1 Senyawa 2
13C-NMR
δ C(ppm)
1
H-NMRδ H(ppm) (Σ H, m, J)
13C-NMR
δ C(ppm)
1
H-NMRδ H(ppm) (Σ H, m, J)
1 33,8 1,25 (1H, m); 1,43 (1H, m) 33,8 1,25 (1H, m); 1,44 (1H, m)
2 24,9 1,73 (1H, m); 1,94 (1H, m) 24,9 1,53 (1H, m); 1,94 (1H, m)
3 76,4 3,39 (1H, t; 3,25) 76,4 3,39 (1H, t, 2,6)
4 37,8 - 37,8
-5 49,7 1,25(1H, m) 49,7 1,25(1H, m)
6 18,4 1,43 (2H, m) 18,4 1,44 (2H, m)
7 35,3 1,56 (2H, m) 35,3 1,53 (2H, m)
8 40,7 40,76
-9 50,6 1,43 (1H, m) 49,9 1,44 (1H, m)
10 37,4 - 37,4
-11 21,5 1,56 (2H,m) 21,5 1,56 (2H, m)
12 25,5 1,56 (1H, m); 1,94 (1H, m) 25,54 1,56 (H, m), 1,94 (1H, m)
13 42,5 1,56 (1H, m) 42,4 1,56 (1H, m)
14 40,7 50,3
-15 31,2 1,05 (2H,m); 31,3 1,25 (2H,m)
16 27,7 1,84 (2H, m); 27,7 1,76 (2H, m)
17 50,0 1,73 (1H,m); 50,6 1,76 (2H,m)
18 15,7 0,96 (3H,s) 15,6 0,95 (3H,s)
19 16,2 0,85 (3H,s) 16,2 0,85 (3H,s)
20 75,2 - 75,6
-21 25,9 1,14 (3H, s) 25,5 1,13 (3H, s)
22 43,6 2,19 (2H,m) 40,71 1,44 (2H,m)
23 122,5 5,69 (1H,m) 22,7 2,03 (2H, dd, 7,1; 14,9)
24 142,1 5,69 (1H,m) 124,9 5,11 (1H, t, 7,1)
25 70,9 - 131,7
-26 30,0 1,32 (3H, s) 25,9 1,68 (3H, s)
27 30,1 1,32 (3H,s) 17,8 1,61 (3H,s)
28 28,4 0,93 (3H, s) 28,5 0,93 (3H, s)
29 22,2 0,83 (3H, s) 22,2 0,83 (3H,s)
30 16,7 0,85 (3H, s) 16,7 0,88 (3H, s)
*Pengukuran dilakukan pada 500 MHz untuk1H dan 125 MHz untuk13C.
Senyawa 2: diperoleh sebagai kristal tidak berwarna. Spektrum HR-ESI-TOFMS (Ion positif) m/z 445,0527 [M-H]+ (sesuai dengan rumus molekul C30H52O2) dan NMR (Tabel 1) dengan derajat ketidakjenuhan (DBE) sebanyak 5. Spektrum IR senyawa 2 mempunyai pola yang sama seperti senyawa 1. Spektrum 13C-NMR dari senyawa 2 menunjukkan kehadiran 30 signal karbon, dengan 1 sampai 21 dan 28 sampai
1986), maka senyawa 2 diidentifikasi sebagai damar-24-en-3α ,20-diol.
KESIMPULAN
Berdasarkan hasil penelitian terhadap ekstrak metanol kulit batang A. eximia diperoleh dua senyawa golongan triterpenoid yaitu dammar-23-ene-3α ,20,25-triol and dammar-24-ene-3α ,20-diol
UCAPAN TERIMAKASIH
Kami mengucapkan terima kasih setinggi-tingginya kepada Direktorat Jendral Pendidikan Tinggi yang telah memberikan beasiswa melalui program Beasiswa Pendidikan Pascasarjana Dalam Negri (BPP-DN) 2013, Staf Herbarium Bogoriense, Bogor yang membantu dalam determinasi tumbuhan, Sofa Fajriah, M.Si dan Ahmad Dermawan, M.Si, staf Pusat Penelitian Kimia, LIPI serpong yang telah membantu dalam pengukuran spektra NMR. Staf Laboratorium Pusat Pelayanan Basic Sains Universitas Padjadjaran yang telah membantu dalam pengukuran MS.
DAFTAR PUSTAKA
Awang, K., Loong, X., Leong, K, H., Supratman, U., Litaudon, M., Mukhtar, M. R., Mohamad, K. 2012. Fitoterapia. 83. 1391-1395.
Bianchini, J.P., Gaydou, E. M., Rafaralahitsimba, G., Waegell, B. and Zahra, J.P. 1988. Phytochemistry. 27. 2301-2304.
Brader, G., Vajrodaya, S., Greger, H.; Bacher, M.,Halchhauser, H., Hofer, O. 1998. J. Nat. Prod. 61. 1482-1490.
Chaidir, J. Hiort, B. N., Bohnenstengel, F., Wray, V., Witte, L., Hung, P., Proksch, P. 1999. Phytochemistry. 52. 837-842. Engelmeier, D., Hadacek, F., Pacher, T.,
Vajrodaya, S., Greger, H.2000. J. Agric. Food Chem. 48. 1400-1404.
Fuzzati, N., Dyatmiko, W., Rahman, A., Achmad, F., Hostettmann, K. 1996. Phytochemistry. 42. 1395–1398.
Harneti, D., Supriadin, A., Ulfah, M., Safari, A., Supratman, U., Awang, K., Hayashi, H. 2014. Phytochemistry. 8. 28-31. Heyne, K. 1987. Tumbuhan Berguna
Indonesia. Penerjemah: Badan Litbang Kehutanan. Jakarta: Badan Litbang Kehutanan
Joycharat, N., Plodpai, P., Panthong, K.,
Yingyongnarongkul,
B.,
Voravuthikunchai, S. P.
2010.Can. J. Chem. 88. 937-944.Kim, S., Chin, Y., Su, B., Riswan, S., Kardono, L. B., Afriastini, J. J., Chai, H., Farnsworth, N. R., Cordell, G. A., Swanson, S. M., Kinghorn, A. D. 2006. J. Nat. Prod. 69. 1769-1775.
Kim, S.,
Salim, A. A., Swanson, S. M., Kinghorn, A. D.2006.
Anti-cancer Agents Med. Chem. 6.
319-345.Mohamad, K., Sevenet, T., Dumontet, V., Pais, M., Van Tri, M., Hadi, H., Awang, K., Martin, M. 1999. Phytochemistry. 51. 1031-1037
Nugroho, B., Edrada, R., Wray, V., Witte, L., Bringmann, G., Gehling, M., & Proksch, P. 1999. Phytochemistry. 51. 367-376.
Pakhathirathien, C., Karalai, C., Ponglimanony, C., Subhadhirasakul, S., Chantrapromma, K., 2005. J. Nat. Prod. 68. 1787-1789
Rivero-Cruz, J. F., Chai, H. B., Kardono, L. B. S., Setyowati, F. M., Afriastini, J. J., Riswan, S., Farnsworth, N. R., Cordell, G. A., Pezzuto, J. M., Swanson, S. M., Kinghorn, A. D. 2004. J. Nat. Prod. 67. 343–347
Saifah, E., Suttisri, R., Shamsub, S., Pengsuparp, T., & Lipipun, V. 1999 Phytochemistry. 52. 1085-1088.