22
IV. Hasil dan Pembahasan
A. Sampling dan Isolasi Bakteri
Bakteri dalam penelitian ini diisolasi dari Acropora
nasuta (Gambar 2) hasil sampling di Taka Cemara, Karimunjawa, Jepara yang secara geografis berada pada 0,5’ 49’ 33,6” lintang selatan dan 110’ 25’ 25,9” bujur timur. Pigmen berwarna kuning dihasilkan setelah 24
jam masa inkubasi pada suhu 35°C di media Zobell 2216E Agar (Gambar 3).
23
A B
Gambar 3. Koloni bakteri hasil kultur pada Media Zobell 2216E Agar (a)dan Zobell 2216E cair (b).
Sedangkan hasil pengamatan menggunakan
mikroskop binokuler dengan perbesaran 1000×
ditunjukkan pada Gambar 4. Pengamatan mikroskopis
menunjukkan bahwa bakteri tersebut berbentuk coccus.
Setelah dilakukan pengecatan gram dengan metode
gram staining, terjadi perubahan warna koloni menjadi merah, sehingga diketahui bahwa bakteri berjenis gram
negatif.
24 B. Polymerase Chain Reaction 16S rDNA
Hasil pengecekan terhadap PCR 16S rDNA
menunjukkan hasil positif dengan terdapatnya berkas
DNA isolat bakteri dengan panjang basa yang sesuai yaitu
sekitar 1.500 bp (Gambar 5).
Gambar 5. Elektroforesis PCR 16s rDNA. M: Marker ; (+): positif kontrol; KJ5: Berkas DNA bakteri yang diisolasi dari Acropora nasuta dengan panjang basa 1.500 bp.
C. Analisis Data BLAST Homologi
Dari analisis sekuensing didapatkan susunan basa
parsial 16S rDNA isolat bakteri dan kemudian
dibandingkan dengan sekuen DNA pada basis data (data
base) DNA (Altschul dkk., 1997). Hasil análisis BLAST menunjukkan bahwa bakteri yang berasosiasi dengan
2.000
1.000
500
M (+) (KJ5)
2.000
1.000
25 Acropora nasuta memiliki homologi sebesar 96% dengan Erythrobacter flavus
Tabel 1. Hasil penelusuran BLAST isolat bakteri KJ5
Kode
Bakteri Length Closest Relative Homology Accession
KJ5 1440 bp
Erythrobacter
flavus 100 %
NR_02524
5.1
Erythrobacter flavus strain LAMA 944 16S ribosomal RNA gene, partial sequence. Sequence ID: gb|KC583223.1|Length: 1338Number of Matches: 1
Score Expect Identities Gaps Strand
558 bits(302) 9e-156 314/326(96%) 0/326(0%) Plus/Plus
Query 2 GCCCTTAGGTTCGGAATAACTCAGAGAAATTTGAGCTAATACCGGATAATGTCTTCGGAC 61 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 46 GCCCTTAGGTTCGGAATAACTCAGAGAAATTTGAGCTAATACCGGATAATGTCTTCGGAC 105
Query 62 CAAAGATTTATCGCCTTTGGATGGGCCCGCGTAGGATTAGATAGTTGGTGGGGTAATGGC 121 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 106 CAAAGATTTATCGCCTTTGGATGGGCCCGCGTAGGATTAGATAGTTGGTGGGGTAATGGC 165
Query 122 CTACCAAGTCGACGATCCTTAGCTGGTCTGAGAGGATGATCAGCCACACTGGGACTGAGA 181 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 166 CTACCAAGTCGACGATCCTTAGCTGGTCTGAGAGGATGATCAGCCACACTGGGACTGAGA 225
Query 182 CACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGGACAATGGGCGAAAGCCT 241 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 226 CACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGGACAATGGGCGAAAGCCT 285
Query 242 GATCCAGCAATGCCGCGTGAGTGATGAAGGNCTNANGGTTGTAAANNNCTTTTACCNNGG 301 |||||||||||||||||||||||||||||| || | ||||||||| |||||||| || Sbjct 286 GATCCAGCAATGCCGCGTGAGTGATGAAGGCCTTAGGGTTGTAAAGCTCTTTTACCAGGG 345
26
Gambar 6. Pohon filogenetik antara isolat KJ5 dengan bakteri laut lainnya.
Genus Erythrobacter ditemukan pertama oleh Shiba
& Simidu (1982) yang pada awal penulisannya terdapat 8
spesies : Erythrobacter longus (Shiba dan Simidu, 1982), Erythrobacter litoralis (Yurkov dkk., 1994), Erythrobacter citreus (Denner dkk., 2002), Erythrobacter flavus (dkk., 2003), Erythrobacter aquimaris (Yoon dkk., 2004), Erythrobacter seohaensis (Yoon dkk., 2005), Erythrobacter gaetbuli (Yoon dkk., 2005) dan Erythrobacter vulgaris (Ivanova dkk., 2005).
Erythrobacter flavus merupakan bakteri gram negatif dengan koloni berwarna kuning, motil, halus,
mengkilap, bulat, tidak berspora dan berbentuk cembung
dengan diameter 10-15 mm setelah 3 hari kultivasi pada
KB5 Isolate
Erythrobacter flavus strain SW-46 16S ribosomal RNA, partial sequence Alpha proteobacterium B36 gene for 16S rRNA, partial sequence
Sphingomonas phyllosphaerae strain FA2 16S ribosomal RNA gene, partial sequence Erythrobacter sp. MBIC4118 gene for 16S rRNA, partial sequence
Erythrobacter flavus strain 2PR56-3 16S ribosomal RNA gene, partial sequence Erythrobacter citreus strain RKHC-1 16S ribosomal RNA gene, complete sequence
Erythrobacter gaetbuli partial 16S rRNA gene, isolate AMV17
27 suhu 30°C. Bakteri ini tumbuh optimal pada suhu 30– 37°C dengan pH optimal 6-7 (Yoon dkk., 2003)
Hampir semua spesies yang termasuk ke dalam
genus Erythrobacter mampu memproduksi pigmen dan beberapa diantaranya mampu memproduksi
bakterioklorofil (BChl) a. Erb. longus dan Erb. litoralis dilaporkan mengandung bakterioklorofil (BChl) a dan karotenoid (Shiba dan Simidu, 1982; Yurkov dkk., 1994),
namun pada spesies Erythrobacter lain tidak ditemukan
BChl a (Denner dkk., 2002; Yoon dkk., 2003, 2004, 2005;
Ivanova dkk., 2005). Spesies Erythrobacter mensintesis
pigmen fotosintetik dalam kondisi aerob, namun mereka
tidak mampu tumbuh anaerob meskipun dengan kondisi
pencahayaan yang sama dengan bakteri fotosintesik
lainnya (Shiba dan Simidu 1982).
D. Isolasi β-karoten bakteri dengan ekstraksi
Ekstraksi β-karoten bakteri dilakukan menggunakan pelarut aseton murni (Khalil dan
Varananis, 1996). Ekstraksi bakteri dilakukan dengan
menumbuhkan sampel bakteri ke dalam media padat
Zobell sebanyak 10 petri. Dari hasil ektraksi pigmen bakteri dengan aseton diperoleh pigmen berwarna kuning
dengan serapan ekstrak kasarnya pada gelombang
28
350 400 450 500 550
0.0
Selanjutnya dilakukan identifikasi pigmen bakteri dan
analisis kandungan pigmen dengan Kromatografi Cair
Kinerja Tinggi.
Gambar 7. Pigmen bakteri berwarna kuning hasil ekstraksi dengan aseton (A) ; Spektrum serapan ekstrak kasar pigmen dalam pelarut aseton (B).
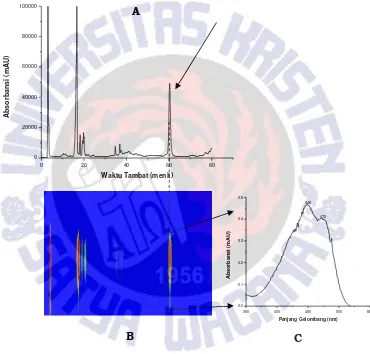
E. Analisis β Karoten dengan Kromatografi Cair Kinerja Tinggi (KCKT) dan Photo Diode Array (PDA)
Analisis ekstrak aseton Erb. flavus dengan KCKT berhasil mengidentifikasi beberapa pita yang diketahui
tergolong ke dalam pigmen fotosintetik dominan. Diantara
beberapa puncak yang muncul tersebut terdapat 1
puncak yang muncul pada menit-menit terakhir (60,24
29
350 400 450 500 550
0.0 menit) yang diidentifikasi sebagai β-karoten dengan puncak serapan (427),449,477 nm.
Gambar 8. Kromatogram KCKT ekstrak pigmen Erb. flavus
30
250 300 350 400 450 500
0.00
Untuk memperkuat hasil analisa, pigmen pada
waktu tambat 60,24 yang diduga sebagai pigmen β karoten ditampung dan dikeringkan kemudian diukur
spektrum serapannya menggunakan spektrofotometer
UV-Tampak pada panjang gelombang 300-500 nm dengan
beberapa pelarut yang berbeda (Gambar 9).
Gambar 9. Pola spektra β-karoten pada panjang gelombang 300-500 nm dengan pelarut aseton (..); etanol (--) dan heksana (-).
Dari hasil analisa UV-Tampak dengan 4 jenis pelarut
yang berbeda, terlihat bahwa pola serapan dan puncak
maksimum spektra yang muncul hampir sama. Pola
serapan dan puncak I, II, III, pigmen murni tersebut
31
Tabel 2. Perbandingan panjang gelombang maksimum β
-karoten pada beberapa pelarut
Hingga saat ini belum ditemukan penelitian yang
berhasil mengidentifikasi β-karoten pada Erb. flavus, namun Koblizek dkk. (2003) telah berhasil mengidentifikasi β-karoten dari genus Erythrobacter yaitu Erb.longus yang diisolasi dari Samudera Atlantik, Samudera Pasifik, Laut Mediterania dan Samudera
Hindia. Kurang lebih 18 jenis pigmen berhasil
diidentifikasi dari Erb. longus pada beberapa kondisi kultur yang berbeda. Karotenoid tersebut memiliki 3
struktur yang sangat berbeda, yaitu bisiklik, monosiklik
dan asiklik, dimana karotenoid golongan polar merupakan
karotenoid dominan pada spesies tersebut (70% dari total
karotenoidnya). Dibandingkan dengan bakteri fotosintetik
lainnya, Erb. longus memiliki jumlah karotenoid yang Pelarut Aseton Etanol n-Heksana Eluent Britton dkk.,
32 lebih variatif (Takaichi dkk., 1990). Erb. longus memiliki Reaction Centers (RCs) dan B865 complexes (dimana tidak ada komplek pemanen cahaya lain pada spesies ini)
(Shimada dkk., 1985). Oleh karenanya Erb. longus memiliki komposisi pigmen yang spesifik, yang tidak
ditemukan pada bakteri fotosintetik lainnya. Total
karotenoidnya jauh lebih banyak daripada
bakterioklorofilnya, berbeda dengan bakteri fotosintetik
lainnya yang perbandingan karotenoid dan
bakterioklorofilnya sebanding (Takaichi dkk, 1990). β -karoten dan turunannya merupakan komponen
karotenoid dominan pada mikroorganisme ini. Jenis
pigmen tersebut sangat jarang ditemukan pada bakteri
fotosintetik lainnya kecuali pada Rhodomicrobium vannielii
dalam jumlah yang relatif sedikit (Ryvarden dan
Liaaen-Jensen, 1964).
Selain Erb. longus, Baskar dkk. (2010) juga berhasil mengidentifikasi β-karoten dari Streptomyces sp. yang diisolasi dari sponge. Kruqel dkk, (1999) juga melaporkan
bahwa karotenoid golongan aromatik telah berhasil
ditemukan pada spesies Streptomyces sp. yang lain. Pada
Streptomyces sp. produksi karotenoid terjadi secara konstitutif dan tergantung pada cahaya (Koyama dkk.,
33 Informasi mengenai jalur sintesis maupun beberapa
gen yang terlibat dalam proses sintesis β-karoten pada genus Erythrobacter dapat kita temukan dalam genome database. Diantaranya adalah β carotene ketolase dan β
carotene hydroxylase yang telah berhasil disekuen Oh dkk. (2009) dari spesies Erythrobacter litoralis HTCC2594.
F. Kuantifikasi Kandungan β-Karoten
Untuk menghitung kandungan pigmen β-karoten pada bakteri Erb. flavus, fokus area yang diambil yaitu
pada tR 59,73 – 60,65 sesuai hasil analisa KCKT sebelumnya (Indrawati dkk., 2013).
Tabel 3. Luas puncak, yield dan berat kering kandungan β -karoten
Luas puncak rata-rata Y (µg/mL) C (µg/g berat kering)
1166,17 12.64 56.74
Dengan persamaan,
Y = 0.0108X + 12.677 Dimana :
X = Luas puncak serapan
Y = Konsentrasi (mikrogram/ml)
Maka, Y = (0,0108 x 1166,1688) + 12,677
Y = 12,59 + 12,64
Y = 25,27 µg/0,5 mL
Y = 12,64 µg/mL (2x pengenceran)
34 Jadi, Yield = 12,64 µg/0,42 gr atau 30,01 g/g
Jika kadar air sampel 47,10% maka :
Yield = 30,01 µg/0,53 g berat kering
= 56,74 µg/1 g berat kering
Jadi berat kering β-karoten Erb. flavus adalah 56,74 µg/ g berat kering
Jumlah kandungan β-karoten yang dihasilkan Erb. flavus ini masih dibawah kandungan β-karoten yang mampu diproduksi oleh Dunaliella salina yang berkisar 10% dari berat keringnya (Prieto dkk., 2011). Selain dari
golongan mikroalga, fungi dari jenis wild type Phycomyces
blakesleeanus juga dilaporkan mampu mensintesis β -karoten sekitar 0.05 mg/g berat kering dalam kondisi
normal, dan bahkan mencapai 10 mg untuk tipe mutant-nya (Murillo dkk., 1978). Sedangkan untuk fungi jenis
Blakeslea trispora, dengan stimulasi seksual pada jalur biosintesis karotenoidnya, mampu meningkatkan
produksi β-karoten hingga 35 mg/g (Mehta dkk., 1997). Namun demikian, kandungan karotenoid pada Erb. flavus
ini masih lebih tinggi jika dibandingkan dengan
Streptomyces sp. yang hanya mampu memproduksi β -karoten 4,88 µg per 100 gram (Baskar dkk., 2010).
Meskipun jumlah kandungan β-karoten yang
-35 karoten. Optimasi pada kondisi kultur dan lingkungannya
bisa dilakukan untuk mengoptimalisasi produksi β -karoten pada Erb. flavus. Choudhari dan Singhal (2008) berhasil mengoptimalisasi produksi β-karoten pada Blakeslea trispora hingga 1,209 μg/mL dengan menambahkan laktosa sebagai sumber karbon. Laktosa
dapat dengan mudah diasimilasi pada jalur metabolis β -karoten, begitupula dengan glukosa. Beberapa teknologi
juga telah digunakan untuk kultivasi Dunaliella sp. secara
komersial (Ben-Amotz, 1993). Ketika Dunaliella sp ditumbuhkan pada kondisi terbatas, β-karoten dalam jumlah besar berhasil disintesis dan diakumulasi
(Borowitzka dkk., 1984). Muthukannan dkk. (2010) juga
berhasil mengoptimalisasi produksi β-karoten Dunaliella sp dengan mengoptimasi parameter kondisi kulturnya
seperti pH dan intensitas cahaya. Parameter tersebut
sangat bermanfaat untuk megetahui kadar nutrisi yang
digunakan pada medium pertumbuhannya (De walne’s
medium) (Oreset dan Young, 1999).
Selain itu, dengan rekayasa genetika, Sacharomyces
36 ke dalam Zymomonas mobilis dan Agrobacterium tumefaciens. Dari penelitian tersebut diperoleh bahwa Z.mobilis dan A.tumefaciens memiliki koloni berwarna kuning dan mampu memproduksi β-karoten hingga 220 µg untuk Z. mobilis mutan dan 350 µg untuk mutan A. tumefaciens per gram berat kering pada fase stationer di medium cair.
Dengan menambahkan mineral atau sumber
karbon lain pada medium kultivasi, mengoptimasi
parameter pertumbuhan seperti pH, intensitas cahaya