1
METODE PENGAMBILAN DAN PEMBUATAN PREPARAT
OTOLITH UNTUK PENDUGAAN UMUR IKAN DI LOKA
RISET PERIKANAN TUNA DENPASAR BALI
PRAKTIK KERJA LAPANG
Oleh :
Eka Putri Rahayu
NPM : 170341100058
PROGRAM STUDI ILMU KELAUTAN
FAKULTAS PERTANIAN
UNIVERSITAS TRUNOJOYO MADURA
BANGKALAN
i
METODE PENGAMBILAN DAN PEMBUATAN PREPARAT
OTOLITH UNTUK PENDUGAAN UMUR IKAN DI LOKA
RISET PERIKANAN TUNA DENPASAR BALI
PRAKTIK KERJA LAPANG
Diajukan
Sebagai Salah Satu Syarat Untuk Memperoleh Derajat Sarjana Strata I
Pada Program Studi Ilmu Kelautan
Fakultas Pertanian Universitas Trunojoyo Madura
Oleh: Eka Putri Rahayu NPM 170341100058
PROGRAM STUDI ILMU KELAUTAN FAKULTAS PERTANIAN
UNIVERSITAS TRUNOJOYO MADURA BANGKALAN
iii
RIWAYAT HIDUP
Penulis bernama Eka Putri Rahayu, lahir di Kediri tanggal 26 September 1999. Alamat tempat tinggal di Jl. H. Syukur VII Gg. Garuda D 02 RT 5 RW 15, Kecamatan Sedati, Kabupaten Sidoarjo. Penulis merupakan anak pertama dari dua bersaudara putri dari suami istri bernama Slamet Joni dan Tasmiharti.
Riwayat pendidikan penulis dimulai dari TK Dharma Wanita tahun 2003-2005, kemudian SD Negeri 1 Tales tahun 2005-2011), SMP Negeri 1 Kras tahun 2011-2014, SMA Negeri 4 Kediri tahun 2014-2017. Mulai tahun 2017 penulis melanjutakan pendidikan sebagai mahasiswa Program Studi Ilmu Kelautan Jurusan Kelautan dan Perikanan Fakultas Pertanian Universitas Trunojoyo Madura Bangkalan.
Prestasi penulis yakni mahasiswa yang cukup aktif di Organisasi HIMALA (Himpunan Mahasiswa Ilmu Kelautan) tahun kepengurusan 2017/2018. Penulis juga mengikuti kegiatan kemaritiman dengan prestasi juara tiga tingkat nasional pada tahun 2018. Serta penulis berkesempatan mengikuti pelatihan drone dan webgis tahun 2020.
iv
PERNYATAAN KEASLIAN KARYA ILMIAH
” Saya Eka Putri Rahayu, menyatakan bahwa Laporan PKL berjudul Metode Pengambilan Dan Pembuatan Preparat Otolith Untuk Pendugaan Umur Ikan Di Loka Riset Perikanan Tuna Denpasar Bali merupakan karya pribadi saya kecuali yang disebutkan sumbernya, dan tidak pernah digunakan sebagian atau seluruh bagiannya untuk mendapatkan gelar akademik apapun”
13 Maret 2020
Eka Putri Rahayu NPM. 170341100058
v
KATA PENGANTAR
Puji Syukur saya ucaokan kepada Allah SWT atas Rahmat dan HidayahNya yang telah memberikan kesempatan untuk menyelesaikan laporan Praktik Kerja Lapang dengan judul Metode Pengambilan Dan Pembuatan Preparat Otolith Untuk Pendugaan Umur Ikan Di Loka Riset Perikanan Tuna Denpasar Bali. Kegiatan praktik kerja lapang bertujuan untuk menerapkan teori yang diperoleh di kampus sehingga mahasiswa dapat mengetahui tentang pelaksanaan di lapang serta memperoleh wawasan baru secara langsung. Kegiatan PKL yang saya lakukan merupakan langkah awal dari proses penentuan umur ikan melalui otolith yang nantinya dapat dikembangkan menjadi karya tulis lain dengan data yang diperoleh.
Penulis menyadari dalam penulisan laporan ini memiliki banyak kekurangan, namun penulis berharap dengan adanya karya ilmiah ini dapat memberikan manfaat dan wawasan baru bagi pembaca. Banyak pihak yang membantu untuk berlangsungnya kegiatan praktik kerja lapang dan penyusunan laporan hingga selesai. Oleh karena itu, penulis mengucapkan rasa terimakasih kepada:
1. Allah SWT yang telah memberikan kesempatan hingga kegiatan praktik kerja lapang berjalan dengan lancar
2. Kedua orang tua yang memberikan dukungan do’a dan semangat kepada penulis
3. Dekan Fakultas Pertanian Universitas Trunojoyo Madura
4. Ach. Fachruddin Syah selaku dosen pembimbing yang telah memberikan saran dan kritik dalam penyusunan laporan
5. Koordinator Program Studi Ilmu Kelautan
6. Fathur Rochman selaku dosen pembimbing lapang yang mengarahkan penulis dalam penyusunan laporan
vi
7. Segenap teman yang telah mendukung kelancaran penyusunan laporan ini
Semoga semua bantuan semua pihak dibalas oleh Allah SWT. Penulis menyadari bahwa laporan ini jauh dari sempurna, oleh karena itu kritik dan saran yang membangun sangan diharapkan penulis.
vii
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
RIWAYAT HIDUP ... iii
PERNYATAAN KEASLIAN KARYA ILMIAH ... iv
KATA PENGANTAR ... v
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xii
I. PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Tujuan Praktik Kerja Lapang ... 2
1.3Manfaat Praktik Kerja Lapang ... 2
II.TINJAUAN PUSTAKA ... 3
2.1Otolith Ikan ... 3
2.2Macam-macam Teknik Pengambilan Sampel Otolith...4
2.3Status Perikanan Tuna...7
2.4Distribusi dan Morfologi Ikan Tuna...8
2.5Metode Penangkapan...9
III.METODE PELAKSANAAN PKL ... 11
3.1Waktu dan Tempat ... 11
3.2 Metode Pengumpulan Data ... 11
a.Data primer ... 11
b.Data sekunder ... 12
3.3 Prosedur Kerja ... 12
viii
3.5 Tahapan Analisa Otolith...28
3.5.1 Proses Penerimaan Sampel...28
3.5.2 Proses Persiapan Sampel...29
3.5.3 Proses Morfometrik...30
3.5.4 Proses Pembuatan Preparat...33
IV. HASIL DAN PEMBAHASAN ... 39
4.1 Keadaan Umum Loka Riset Perikanan Tuna ... 39
Dasar Hukum ... 39
Visi dan Misi LRPT ... 39
Tujuan dan Sasaran LRPT ... 40
Struktur Organisasi LRPT ... 41
Sumberdaya Loka Riset Perikanan Tuna ... 42
Fasilitas Loka Riset Perikanan Tuna ... 43
4.2 Pengambilan Data Biologi Ikan ... 45
4.2.1Sampling di Pelabuhan Benoa-Bali ... 45
4.2.2 Identifikasi Jenis ikan ... 46
4.2.3 Pengukuran Panjang dan Berat Ikan ... 50
4.3 Bagian-Bagian Otolith ... 52
4.4 Pembacaan Preparat untuk Pendugaan Umur ... 54
4.5 Permasalahan yang dihadapi selama proses pengambilan sampel dan preparasi otolith ... 58
V. PENUTUP ... 59
5.1 Kesimpulan ... 59
5.2 Saran ... 59
ix
DAFTAR TABEL
Tabel 3.1 Prosedur Kerja... 12
Tabel 3.2 Alat yang digunakan dalam metode Up Trough the Gill ... 13
Tabel 3.3 bahan yang digunakan dalam metode Up Trough the Gill ... 14
Tabel 3.4 Alat yang digunakan dalam metode open the hatch ... 14
Tabel 3.5 Bahan yang digunakan dalam metode open the hatch ... 16
Tabel 3.6 Alat yang digunakan pada proses penanaman sampel otolith... 16
Tabel 3.7 Bahan yang digunakan pada proses penanaman sampel otolith ... 18
Tabel 3.8 Alat yang digunakan pada proses pemotongan sampel ... 19
Tabel 3.9 Bahan yang digunakan pada proses pemtongan sampel ... 20
Tabel 3.10 Alat yang digunakan pada proses pemolesan ... 21
Tabel 3.11 Bahan yang digunakan pada proses pemolesan ... 21
Tabel 3.12 Alat yang digunakan pada proses covering... 22
Tabel 3.13 Bahan yang digunakan pada proses covering ... 23
Tabel 4.1Hasil Kegiatan Sampling...45
Tabel 4.2 Pengukuran Panjang Kelompok Tuna... 50
Tabel 4.3 Hasil Pengambilan Data Biologi Ikan Kembung Lelaki (Rastrelliger kanagurta) ... 51
Tabel 4.4 Hasil Penimbangan Otolith Ikan Kembung Laki ... 54
x
DAFTAR GAMBAR
Gambar 2.1Gambar dari 3 bagian otolith dari Tuna Sirip Biru Pasifik (Thunnus
orientalis) (141 cmFL, Jantan) (Shimose dan Ishihara, 2015). ... 3
Gambar 2.2Macam-macam Teknik Pengambilan Sampel Otolith ... 4
Gambar 2.3 Ilustrasi Tuna Sirip Biru Selatan (Thunnus maccoyii) ... 8
Gambar 2.4.Spesifikasi alat tangkap rawai tuna yang digunakan oleh kapal tuna komersial di Indonesia ... 10
Gambar 3.2 Proses pengambilan otolith dengan metode Up Through The Gill ... 26
Gambar 3.6 Dokumentasi (Sumber: Dokumentasi Pribadi ... 32
Gambar 3.7 Penandaan Titik Primordium ... 33
Gambar 3.8 Proses Blocking ... 35
Gambar 3.9 Proses Pemotongan ... 36
Gambar 3.10 Proses Pemolesan ... 37
Gambar 3.11 Proses Covering... 38
Gambar 4.1 Struktur Organisasi Loka Riset Perikanan Tuna TA 2019 ... 41
Sumberdaya Loka Riset Perikanan Tuna ... 42
Gambar 4.2 Komposisi Pegawai LRPT Berdasarkan Tingkat Pendidikan 2018 .. 42
Gambar 4.3 Komposisi PNS LRPT Berdasarkan Golongan Tahun 2018 ... 43
Gambar 4.4 Komposisi Pegawai Berdasarkan Jabatan Fungsional Tahun 2018 .. 43
Gambar 4.5 Laboratorium Otolith (Sumber: Dokumentasi Pribadi) ... 44
Gambar 4.6 Tuna Sirip Biru Selatan ... 46
Gambar 4.7 Tuna Sirip Kuning ... 47
Gambar 4.8 Tuna Mata Besar (Sumber: Dokumentasi Pribadi) ... 48
Gambar 4.9 Kembung Lelaki ... 49
Gambar 4.10 Contoh Otolith Ikan Cakalang (Katsuwonus pelamis)...52
Gambar 4.11Bagian-bagian Otolith Kiri ikan kembung lelaki (Rastrelliger kanagurta ... 52
Gambar 4.12 Bagian-bagian Otolith Kanan ikan kembung lelaki (Rastrelliger kanagurta) ... 53
xi
Gambar 4.14 Kegiatan Dokumentasi Preparat ... 55 Gambar 4.15 Preparat Otolith Ikan Kembung Laki ... 56 Gambar 4.16 Preparat Otolith tuna sirip biru selatan ... 56
xii
DAFTAR LAMPIRAN
Lampiran 1. Logbook ...63
Lampiran 2. Resume...88
Lampiran 3. Hasil kegiatan Praktik Kerja Lapang...121
1
I.
PENDAHULUAN
1.1 Latar Belakang
Manajemen pengelolaan di sektor perikanan yang tepat adalah salah satu kunci untuk mengelola potensi sumberdaya alam dan pemanfaatan secara berkelanjutan. Salah satu langkah awal dalam manajemen pengelolaan perikanan adalah melakukan kajian stok dan struktur umur hasil tangkapan ikan (Rochman, 2019). Metode pengkajian stok ikan selama ini hanya menggunakan metode frekuensi panjang dan penandaan (tagging) (Neilson et al., 2006; Herrera dan Pierre, 2011). Kajian stok dan struktur umur spesies tidak dapat ditentukan secara langsung dengan metode ini dan hanya berupa estimasi struktur umur yang didasarkan pola gerak maju kohort populasi ikan. Sehingga diperlukan metode pengukuran yang lebih akurat dalam membaca umur suatu spesies ikan dengan metode pembacaan umur secara langsung (direct aging) menggunakan informasi jaringan keras seperti sisik, otolith, dan duri sirip (Kumbar and Swapnali, 2016).
Penanda umur menggunakan otolith lebih tepat digunakan untuk pembacaan umur secara langsung karena otolith menunjukkan pola lingkaran pertumbuhan yang lebih jelas sehingga metode ini merupakan teknik terbaik jika dibandingkan dengan penanda biologi lain seperti sisik dan tulang ikan (Kumbar and Swapnali, 2016). Otolith atau tulang telinga adalah salah satu bagian organ ikan yang dapat berfungsi sebagai pendengaran, keseimbangan, dan sejarah hidup ikan (Dehghani
et al., 2016). Umur ikan mampu diinterpretasikan dari analisis jaringan keras ikan
seperti otolith. Uji ini mampu diterapkan pada ikan bertulang sejati pada berbagai umur (Habibie et al., 2015). Berdasarkan ulasan tersebut otolith memiliki peranan penting dalam kajian stok dan struktur hasil tangkapan ikan sehingga pengelolaan dan manajemen sumberdaya perikanan dapat diatur dan dikelola secara berkelanjutan. Praktik kerja lapang ini bertujuan untuk meningkatkan kemampuan teknik pengambilan sampel, pembuatan preparat, pembacaan umur melalui
otolith. Disamping itu keterampilan yang diperoleh dapat digunakan dalam proses
2 1.2 Tujuan Praktik Kerja Lapang
Tujuan Praktik Kerja Lapang ini sebagai berikut :
1. Mengetahui teknik pengambilan data tangkapan (enumerasi) tuna di Pelabuhan Benoa-Bali.
2. Mengetahui metode pengambilan otolith.
3. Mengetahui metode pembuatan preparat otolith untuk pendugaan umur ikan.
1.3 Manfaat Praktik Kerja Lapang
Manfaat Praktik Kerja Lapang sebagai berikut : 1. Bagi Mahasiswa
Mampu menambahkan informasi mengenai metode pengambilan otolith yang tepat sekaligus menambah wawasan tentang metode pembuatan preparat otolith untuk analisis pendugaan umur ikan.
2. Bagi Perguruan Tinggi.
Menjalin kerjasama antara Universitas Trunojoyo Madura dengan Loka Riset Perikanan Tuna Denpasar Bali serta dapat mengevaluasi terhadap kurikulum yang diajarkan dengan kondisi dunia kerja.
3. Bagi Lembaga
3
II. TINJAUAN PUSTAKA
2.1 Otolith Ikan
Ikan memiliki otolith yang terletak di dalam telinga, sehingga otolith disebut juga dengan tulang telinga (Valinassab et al., 2012; Chulin dan Chen, 2013). Fungsi dari otolith adalah mengatur keseimbangan, pendengaran, koordinasi arah renang dan orientasi (Bani et ., 2013; Cabello et ., 2014) yang ditemukan pada semua jenis ikan kecuali ikan pari, hiu dan lamprey. Komponen utama dari otolith adalah kalsium karbonat (CaCO3) yang umumnya berbentuk aragonit (mineral karbonat) dan deposit garam yang tersusun sebagai materi protein anorganik (Cabello et al., 2014; Sadighzadeh et al., 2014).
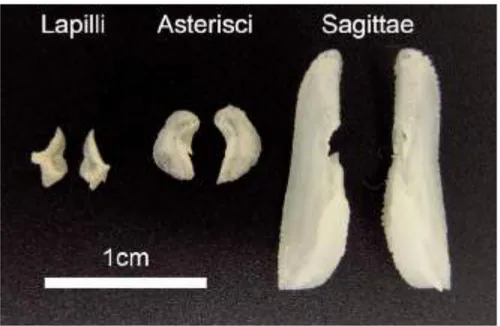
Otolith terdiri dari 3 bagian yakni sagittae, lapillus dan asteriscus (Campana,
2004; Wujdi et al., 2016). Bagian yang sering digunakan yakni sagittae karena memiliki ukuran relatif lebih besar (Yilmaz et al., 2015) dan relatif lebih memiliki struktur yang lebih stabil dibanding astericus dan lapillus (Bani et al., 2013). Oleh karena itu bagian otolith sagittae digunakan untuk memperoleh informasi dan pemahaman yang lebih baik dalam studi umur ikan (Campana dan Neilson, 1985).
Gambar 2.1 Gambar dari 3 bagian otolith dari Tuna Sirip Biru Pasifik (Thunnus orientalis) (141 cmFL, Jantan) (Shimose dan Ishihara, 2015).
Otolith secara permanen menyajikan sejarah hidup dan lingkungan sehingga
4 salinitas (kadar garam). Otolith merupakan organ yang dapat digunakan untuk mengetahui umur, pertumbuhan dan proses migrasi reproduksi (Darmanto, 2019). Menurut Bounket et al., (2019), umur dan pertumbuhan ikan diduga dengan adanya penambahan jumlah dan lebar dari zona kalsium karbonat. Pertambahan berupa pita konsentris yang dapat dianalisis sebagai garis pertumbuhan dapat berupa lingkaran harian maupun tahunan. Setiap penambahan lingkaran membentuk dua zona, yaitu zona kalsium karbonat dan zona protein. Zona kalsium karbonat merupakan lapisan yang berwarna putih yang disebut
translucent, sedangkan zona protein berwarna gelap disebut opaque. Menurut
Dehghani et al., (2016), pola lingkaran pertumbuhan pada otolith dapat dipengaruhi oleh adanya perubahan habitat, ketersediaan pangan dan kondisi perairan. Selanjutnya (Kumbar dan Swapnali, 2016) menyatakan perbedaan suhu air mempengaruhi struktur otolith, berkurangnya suhu mempengaruhi zona
opaque sedangkan meningkatnya suhu mempengaruhi zona translucent.
2.2 Macam-macam Teknik Pengambilan Sampel Otolith
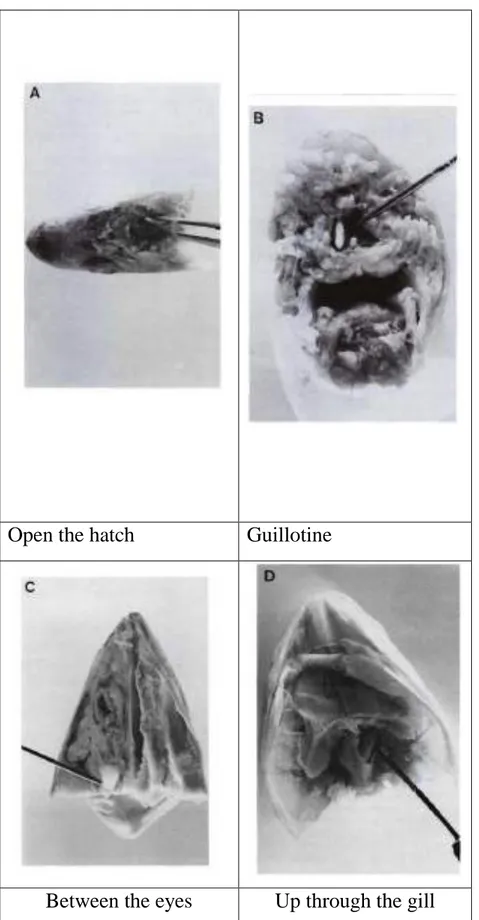
Menurut Secor et al., (1992), Metode pengambilan Otolith terdapat beberapa cara yakni up through the gill method, open the hatch method, between the eyes
method dan guillotine method (Gambar 2.2). Berdasarkan keempat cara tersebut
metode yang sering dilakukan di LRPT yakni up through the gill method dan open
the hatch method. Hal ini karena metode tersebut cenderung lebih aman
digunakan untuk pemula dan keberhasilan lebih tinggi dalam pengambilan otolith. Metode lain jarang digunakan karena resiko kegagalan lebih besar jika dilakukan oleh pemula.
a. Open the Hatch
Metode pengambilan sampel otolith dengan cara dipotong secara vertikal dan horizontal pada bagian kepala ikan. Pemotongan secara vertikal tepat diatas mata dengan jarak sekitar 2 cm. Pemotongan secara horizontal tepat diatas mata sehingga membentuk sudut siku-siku.
b. Guillotine
Pengambilan otolith memotong bagian kepala ikan hingga bagian kepala dan tubuh ikan terpisah. Otolith diambil dari bagian belakang kepala ikan.
5
c. Between the eyes
Metode ini dilakukan dengan bagian kepala ikan dibelah menjadi bagian kiri dan kanan tepat dipotong pada bagian kedua mata. Kemudian otolith diambil pada tiap sisi kepala tersebut
d. Up Through the Gill
Metode ini dilakukan untuk mengambil otolith dari sisi insangnya. Metode ini dapat dilakukan pada ikan berukuran kecil maupun besar.
-Ikan Besar : operkulum dan insang dibuka kemudian dibor pada daerah tulang tengkorak. Titik ini ditandai dengan adanya tulang yang menonjol. -Ikan Kecil : tulang belakang pada bagian leher dipatahkan kemudian otolith diambil menggunakan pinset.
6
Open the hatch
Guillotine
Between the eyes
Up through the gill
7 2.3 Status Perikanan Tuna
Luas wilayah laut Indonesia menjadikan negara ini sangat berpotensi di sektor sumber daya ikan laut. Hal ini diperkuat dengan peringkat ke-13 Indonesia sebagai negara produksi perikanan terbesar di dunia. Beberapa komoditas ikan unggul yang dihasilkan Indonesia mampu berdaya saing di pasar internasional salah satu nya komoditas ikan tuna. Perairan samudera Hindia, sebelah selatan jawa, bali dan nusa tenggara merupakan lokasi pemijahan beberapa jenis tuna salah satu nya ikan tuna sirip biru selatan (Thunnus maccoyii) ( Swatana et al. 2016).
Menurut Kementerian Kelautan dan Perikanan (KKP) sebanyak 70% produksi tuna di Indonesia merupakan hasil tangkapan nelayan skala kecil. Kontribusi perikanan tuna Indonesia sebesar 16% terhadap produksi perikanan tuna dunia tahun 2017. Hal ini didukung pada Samudera Hindia, khususnya selatan Jawa hingga selatan Nusa Tenggara, Laut Sawu, dan Laut Timor bagian barat masuk dalam wilayah pengelolaan perikanan Negara Republik Indonesia (WPPNRI) 573 dikenal memiliki potensi sumber daya ikan yang melimpah, terutama ikan tuna tongkol dan cakalang. Total hasil tangkapan kelompok sumber daya ikan tuna dan sejenis tuna Indonesia di Samudera Hindia (WPPNRI 571, 572, dan 573) pada tahun 2017 berjumlah sekitar 336.000 ton, dengan 151.000 ton adalah komoditas tuna. Tahun 2018 mengalami peningkatan menjadi 181.000 ton atau sekitar 18% dari total produksi tuna di IOTC yang sebesar 1 juta ton. Hasil tangkapan ini yang terbesar dibandingkan dengan negara-negara anggota IOTC lainnya. Tahun 2018 menunjukkan komoditas tuna total pada wilayah Indonesia sebesar 409.024,18 ton hal ini mengalami peningkatan sebesar 115.791,02 ton dengan total tahun 2017 sebesar 293.233, 16 ton (Satu Data KKP).
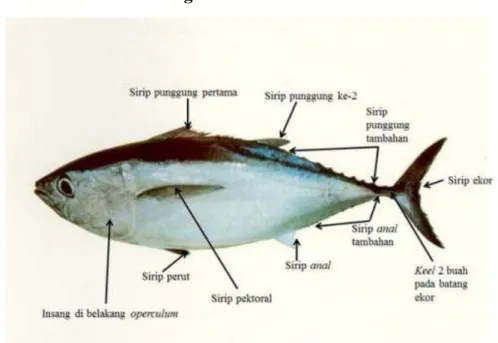
8 2.4 Distribusi dan Morfologi Ikan Tuna
Gambar 2.3 Ilustrasi Tuna Sirip Biru Selatan (Thunnus maccoyii) (May dan Maxwell, 1986).
Ikan tuna termasuk dalam keluarga Scrombidae, tuna digunakan sebagai nama grup dari beberapa jenis ikan yang terdiri dari, tuna besar (yellowfin tuna, bigeye, southern bluefin tuna, albacore) dan ikan mirip tuna (tuna-like species), yaitu marlin, sailfish, dan swordfish
Klasifikasi ikan tuna menurut Worms Kingdom : Animalia Phylum : Chordata SubPhylum : Vertebrata Class : Actinopterygii Subclass : Teleostei Ordo : Perciformes Subordo : Scombroidae Family : Scrombidae Genus : Thunnus
Tuna memiliki bentuk tubuh Streamline menyerupai torpedo dan tidak memiliki sisik. Tubuhnya licin, sirip dada melengkung dan sirip ekor bercagak dengan celah yang lebar. Bagian belakang sirip punggung dan sirip dubur juga
9 terdapat sirip-sirip tambahan yang kecil-kecil dan terpisah-pisah. Bagian sirip punggung, dubur, perut, dan dada pada pangkalnya mempunyai lekukan pada tubuh, sehingga dapat memperkecil daya gesekan pada air pada saat ikan sedang berenang dengan kecepatan penuh (Sarrimbul et al., 2017).
Tuna merupakan salah satu kelompok ikan pelagis besar. Kelompok jenis ikan ini adalah ikan-ikan dengan ukuran besar dan memiliki kemampuan untuk bermigrasi dalam jarak yang jauh bahkan mampu melintasi samudera. Distribusi ikan pelagis besar dipengaruhi oleh bentuk tubuh dan juga karakteristik fisika kimia lingkungan. Periairan hangat dengan massa air yang baik (well mixed) akibat pengaruh gelombang dan juga pertemuan dua massa air yang berbeda merupakan habitat untuk ikan tuna. Tuna ditemukan pada wilayah perairan lintang tinggi saat musim panas dan bergerak menuju daerah ekuator saat musim dingin untuk mencari wilayah periran panas. Kedalaman perairan memiliki hubungan dengan sinar matahari mengakibatkan ikan tuna melakukan migrasi secara vertikal di sepanjang kolom perairan. Beberapa jenis ikan pelagis berada pada permukaan perairan pada malam hari dan di kolom periaran di siang hari untuk mekanisme perlindungan diri dan ketersedian makanan (Sarrimbul et al., 2017).
2.5 Metode Penangkapan
Sumber daya ikan pelagis besar (tuna dan sejenisnya) ditangkap oleh berbagai jenis alat tangkap, diantaranya rawai tuna (tuna longline), pukat cincin (purse
seine), huhate (pole and line) dan pancing ulur (hand line) (Diniah et al., 2001).
Perikanan tuna di samudra Hindia terdapat 2 jenis yaitu tuna skala industri dan kecil. Tuna skala industri menggunakan alat tangkap rawai tuna, sedangkan tuna skala kecil menggunakan alat tangkap jaring insang hanyut (gillnet), pancing tonda (troll line) dan pukat cincin (Mertha et al., 2006). Pukat cincin, pancing tonda, pancing ulur dan huhate dalam pengoperasiannya menggunakan rumpon sebagai alat bantu penangkapan
.
Tuna longline atau rawai tuna merupakan alat tangkap yang efektif untuk
menangkap ikan oseanis pelagis, karena menurut Farid et al. (1989) konstruksinya mampu menjangkau swimming layer tuna. Hal ini dapat dilihat dari 40% produksi tuna di dunia dihasilkan oleh alat tangkap tuna longline dan selebihnya dihasilkan oleh purse seine, trolling, serta alat tangkap lainnya (Simorangkir, 1982). Selain
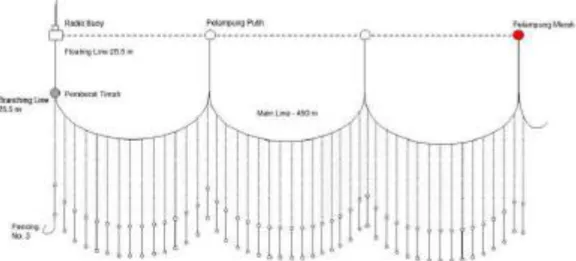
10 efektif alat tangkap tuna longline juga merupakan alat tangkap yang selektif terhadap hasil tangkapannya dan cara pengoperasiannya bersifat pasif sehingga tidak merusak sumber daya hayati perairan. (Nugraha et al 2010). Rawai tuna merupakan pengembangan teknik pada perikanan pancing. Alat ini bersifat pasif, terentang secara horisontal dan dihanyutkan (drifting) (Von Brandt, 1984). Menurut Soepriyono (2009), berdasarkan kedalaman mata pancing, rawai tuna dibedakan menjadi rawai tuna permukaan (surface/drifting longline) dan rawai tuna dalam (deep longline). Rawai tuna permukaan diatur dengan jangkauan mata pancing terdalam kurang dari 136 m. Terdiri dari 5 tali utama masing-masing berukuran 50 m, 4 tali 18 cabang/pancing masing-masing berukuran 20 m. Satu pelampung ditambah satu tali pelampung dengan panjang 20 m. Target utama adalah tuna dan ikan berparuh. Rawai tuna dalam diatur dengan jangkauan mata pancing terdalam lebih dari 200 m. Terdiri dari 11 atau lebih tali utama masing-masing berukuran 50 m, 10 atau lebih tali cabang/pancing, dengan 1 – 2 pelampung yang digabung jadi satu ditambah satu tali pelampung yang panjangnya 20 m atau lebih. Target utamanya adalah tuna mata besar, albakora dan Tuna Sirip Biru Selatan.
Gambar 2. 4. Spesifikasi alat tangkap rawai tuna yang digunakan oleh kapal tuna komersial di Indonesia (Soepriyono, 2009)
11
III. METODE PELAKSANAAN PKL
3.1 Waktu dan Tempat
Praktik Kerja Lapang (PKL) merupakan tahapan kegiatan bersifat wajib untuk mahasiswa program studi Ilmu Kelautan Universitas Trunojoyo Madura sebelum melakukan tugas akhir skripsi. Waktu pelaksanaan Praktik Kerja Lapang (PKL) selama 1 bulan yang dimulai tanggal 18 Desember 2019 hingga 24 Januari 2020. Kegiatan Praktek Kerja Lapang (PKL) di Loka Riset Perikanan Tuna Denpasar-Bali.
Gambar 3.1 Lokasi Praktik Kerja Lapang
3.2 Metode Pengumpulan Data
a. Data primer
Data primer yang diperoleh berupa sampel ikan yang digunakan sebagai praktik PKL di instansi. Sampel yang digunakan sebagai bahan praktik langsung
12 yakni Ikan Kembung Lelaki (Rastrelliger kanakurta) yang diperoleh dari pasar kedonganan denpasar bali dengan jumlah 14 ekor. Selain itu, mengikuti kegiatan sampling di Pelabuhan Benoa Bali sebagai bentuk kegiatan aktif mahasiswa di instansi LRPT untuk dasar wawasan cara pengambilan Otolith.
b. Data sekunder
Data sekunder yang diperoleh menjadi data pendukung untuk penulis. Data sekunder dapat diartikan sebagai informasi yang dikumpulkan untuk pendukung tujuan penelitian. Data sekunder yang diperoleh berupa hasil wawancara dan studi literatur yang sesuai dengan bidang penelitian.
3.3 Prosedur Kerja
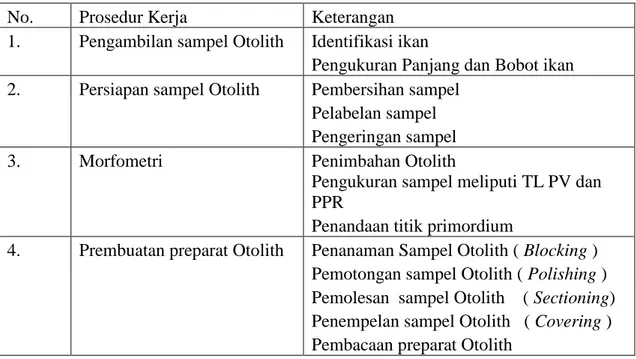
Tabel 3.1 Prosedur Kerja
No. Prosedur Kerja Keterangan
1. Pengambilan sampel Otolith Identifikasi ikan
Pengukuran Panjang dan Bobot ikan
2. Persiapan sampel Otolith Pembersihan sampel
Pelabelan sampel Pengeringan sampel
3. Morfometri Penimbahan Otolith
Pengukuran sampel meliputi TL PV dan PPR
Penandaan titik primordium
4. Prembuatan preparat Otolith Penanaman Sampel Otolith ( Blocking ) Pemotongan sampel Otolith ( Polishing ) Pemolesan sampel Otolith ( Sectioning) Penempelan sampel Otolith ( Covering ) Pembacaan preparat Otolith
3.4 Alat dan Bahan
Pengambilan Otolith dengan Metode Up Trough the Gill
Alat dan bahan yang digunakan untuk metode ini disajikan pada Tabel 3.2 dan Tabel 3.3
13 Tabel 3.2 Alat Yang Digunakan Dalam Metode Up Trough the Gill
No. Nama Alat Fungsi Gambar
1. Bor elektrik Mengebor bagian kepala ikan
2. Mata bor Membuat lubang pada
tulang tengkorak ikan
3. Pinset Mengambildan
memindahkan otolith
4. Tabung vial Wadah sampel otolith
5. Pisau Memotong operkulum
6. Kotak sampel Wadah sampel otolith sebelum dimasukkan ke tabung vial
14 Tabel 3.3 Bahan Yang Digunakan Dalam Metode Up Trough the Gill
No. Nama bahan Fungsi Gambar
1. kertas label Memberi identitas pada tabung vial
2. Plastik klip Wadah sampel otolith
Pengambilan Otolith dengan Metode Open the Hatch
Alat dan bahan yang digunakan untuk metode ini disajikan pada Tabel 3.4 dan Tabel 3.5
Tabel 3.4 Alat Yang Digunakan Dalam Metode Open The Hatch
No. Nama alat Fungsi Gambar
1. Timbangan Menimbang ikan
2. Pisau Membuat sayatan
15
3. Penggaris Mengukur panjang
4. Disetting set Membedah kepala
ikan dan
mengambil sampel otolith
5. Tabung vial Wadah otolith
16 Tabel 3.5 Bahan Yang Digunakan Dalam Metode Open The Hatch
No. Nama bahan Fungsi Gambar
1. Ikan kembung lelaki
Objek penelitian
2. Tisu Membersihkan
sampel otolith
3. Kertas label Memberi tanda pada tiap tabung vial
4. Sarung tangan Melindungi tangan dari pisau
Alat dan bahan yang digunakan dalam proses penanaman sampel otolith ini dapat dilihat pada Tabel 3.6 dan Tabel 3.7
Tabel 3.6 Alat Yang Digunakan Pada Proses Penanaman Sampel Otolith
No. Nama alat Fungsi Gambar
1. Pinset untuk membantu
penyusunan sampel ke
sillicon rubber mold
17 2. Sillicon
rubber mold
atau blok karet
Media untuk menanam sampel
otolith
3. Timbangan Menimbang resin dan
katalis
4. Oven Mengeringkan blok
sampel
18 Tabel 3.7 Bahan Yang Digunakan Pada Proses Penanaman Sampel Otolith
No. Nama bahan Fungsi Gambar
1. Resin Sebagai cairan
pembuat blok
2. Katalis Sebagai pengeras
(Hardener)
3. Paper cup Wadah pencampuran resin dan katalis
4. Stik kayu Pengaduk resin
dan katalis
5. Sarung tangan Menghindari kontak langsung dengan bahan kimia
19
6. Masker Menghindari
kontak langsung dari bahan kimia
7. Tusuk gigi Untuk
menyingkirkan gelembung
Adapun alat dan bahan yang digunakan dalam proses pemotongan sampel ini dapat dilihat pada Tabel 3.8 dan Tabel 3.9
Tabel 3.8 Alat Yang Digunakan Pada Proses Pemotongan Sampel
No. Nama alat Fungsi Gambar
1. Alat pemotong (Gemmasta Machine for sawing Gs10ts) Memotong blok sampel dengan ketebalan sesuai yang diinginkan 2. Pinset Membantu pengambilan sampel yang dipotong
20
3. Jas hujan Melindungi agar
tidak basah saat proses pemotongan
Tabel 3.9 Bahan Yang Digunakan Pada Proses Pemtongan Sampel
No. Nama bahan Fungsi Gambar
1. Paper cup Wadah blok sampel yang telah dipotong
2. Kertas label Memberi keterangan
id otolith
3. Masker Menghindari dari
serpihan blok sampel yang terpotong
21
Alat dan bahan yang digunakan pada proses pemolesan sampel ini dapat dilihat pada Tabel 3.10 dan Tabel 3.11.
Tabel 3.10 Alat Yang Digunakan Pada Proses Pemolesan
No. Nama alat Fungsi Gambar
1. Mesin pemoles (Gemmasta Faceting Machine gf4) Memoles sampel otolith
2. Pinset Mematahkan hasil
potongan blok sampel yang masih menyatu
Tabel 3.11 Bahan Yang Digunakan Pada Proses Pemolesan
No. Nama bahan Fungsi Gambar
1. Vaculab Menyimpan batangan
sampel yang akan dipoles
2. Paper cup Wadah sampel otolith yang tidak dipoles
3. Kertas label Memberikan kode
22
4. Tisu Mengeringkan
batangan hasil pemolesan
5. Sarung tangan Menghindari kontak langsung dengan pemoles
6. Masker Menghindari kontak
langsung dengan mesin pemoles
Alat dan bahan yang digunakan pada proses covering dapat dilihat pada Tabel 3.12 dan Tabel 3.13.
Tabel 3.12 Alat Yang Digunakan Pada Proses Covering
No. Nama alat Fungsi Gambar
1. Pinset Membantu
memindahkan,merapikan batangan sampel
2. Oven Mengeringkan hasil
23
3. Nampan Wadah hasil covering
Tabel 3.13 Bahan Yang Digunakan Pada Proses Covering
No. Nama alat Fungsi Gambar
1. Entellan Merekatkan sampel
otolith ke cover glass dan object glass
2. Kertas label Memberikan keterangan pada object glass
3. Masker Menghindari kontak
langsung dengan bahan kimia
24 4. Sarung
tangan
Menghindari kontak langsung dengan bahan kimia
5. Pipet tetes Mengambil larutan
entellan kemudian
menuangkan di object
glass dan di atas
batangan sampel
6. Paper Cup Wadah larutan entellan
7 Object glass Meletakkan objek
preparat yang sudah dipoles
25
Pengambilan Otolith dengan Metode Up Through the Gill
Prosedur metode Up Through the Gill sebagai berikut:
1. Letakkan ikan pada posisi miring ke kiri kemudian panjang dan berat ikan diukur, operkulum sebelah kanan dibuka agar mudah melakukan proses pengeboran, perhatikan bagian tulang yang menonjol titik tersebut letak untuk melakukan pengeboran.
2. Mata bor diletakkan tepat pada bawah tulang yang menonjol. Lakukan proses pengeboran dengan sudut kemiringan 75º - 80º hingga seluruh mata bor masuk ke tulang belakang kepala ikan. Kemudian gerakkan bor ke depan dan ke belakang agar tulang yang ada pada mata bor patah dan lepas dari pangkal tulang belakang, tarik mata bor dan keluarkan daging yang ada di mata bor. Jika hal ini dilakukan dengan tepat maka sepasang Otolith utuh dapat diambil. 3. Ambil bagian otolith kiri dari bekas lubang mata bor kemudian ambil otolith
dengan pinset dan jepit perlahan agar tidak patah.
4. Letakkan otolith pada kotak sampel kemudian tutup rapat agar darah, lendir dan lemak tidak kering. Jika dapat dicuci langsung dengan air yang mengalir serta dikeringkan pada suhu ruangan. Proses pengeringan pada bawah sinar matahari langsung dapat merusak jaringan otolith.
5. Otolith yang kering dapat dimasukkan ke tabung vial dengan keterangan
pada tiap tabung. Keterangan yang ditulis berupa jenis ikan, berat dan panjang ikan.
Berikut proses pengambilan otolith dengan metode Up Through The Gill
Membuka dan memotong operkulum
Mencari tulang yang menonjol untuk tempat pengeboran
26 Mengambil otolith dengan pinset di
daging yang ada di mata bor
Melubangi tulang tengkorak ikan dengan bor
Otolith yang telah diambil Meletakkan otolith di kotak sampel
Membersihkan otolith dengan air mengalir
Mengeringkan otolith dengan cara diangin-anginkan atau suhu ruangan
Hasil labelling sampel otolith dimasukkan ke plastik klip
Proses labelling sampel otolith
Gambar 3.2 Proses pengambilan otolith dengan metode Up Through The Gill
(Sumber: Dokumentasi Pribadi)
3 5 6 8 9 10 7 4
27
Proses pengambilan sampel otolith dengan metode open the hatch sebagai berikut: 1. Menyiapkan sampel ikan yang digunakan untuk pengambilan otolith
2. Membuat potongan di bagian atas kepala ikan secara vertikal sekitar 2 kali ukuran mata ikan dari bagian mata hingga diatas mata
3. Membuat potongan secara horizontal sehingga membentuk sudut siku-siku 4. Mengeluarkan isi otak menggunakan pinset secara perlahan dengan
memperhatikan letak otolith agar tidak patah atau ikut terbuang
5. Mencari sepasang otolith yang terletak pada rongga sebelah kanan dan kiri tepat berada dibawah otak.
6. Membersihkan otolith dengan tissue kemudian memasukkan ke tabung vial Proses pengambilan sampel otolith dengan metode open the hatch
Menimbang ikan Mengukur panjang
Memotong secara vertikal dan horizontal
Membuat sayatan secara vertikal dan horizontal
1 2
28 Mengeluarkan isi otak dan
mengambil otolith dengan pinset
Membersihkan otolith dengan tisu kemudian dimasukkan ke tabungvial Gambar 3.3 Proses pengambilan sampel otolith dengan metode Open The Hatch
(Sumber: Dokumentasi Pribadi)
3.5 Tahapan Analisa Otolith
3
.5.1 Proses Penerimaan Sampel
Sampel otolith yang dikumpulkan oleh enumerator perlu melalui proses
penerimaan sampel sesuai SOP yang berlaku di Loka Riset Perikanan Tuna sebagai berikut :
1. User ( mengisi formulir penerimaan sampel ) User memberikan sampel kepada penerima sampel
2. Petugas Penerima Sampel
Menyalin formulir penyerahan sampel, mengisi formulir pemeriksaan sampel dan memberikan kode ID untuk setiap sampel yang masuk
3. Kepala Laboratorium
Menerima formulir pemeriksaan sampel setelah melakukan kaji ulang tender dan kontrak. Tahap ini kepala laboratorium akan memeriksa sampel yang masuk jika sesuai akan diserahkan ke penyelia
4. Penyelia
Menerima formulir pemeriksaan sampel dan memeriksa kondisi sampel
29
5. Teknisi Laboratorium
Menerima formulir pemeriksaan sampel berikut sampel. Tahap ini teknisi akan memeriksa sampel kemudian memberikan kode ID baru serta melakukan preparasi sampel hingga dapat dianalisis
6. Analis Pengujian
Menerima preparat sampel dan melakukan pengujian kemudian hasil preparasi akan dicek ulang oleh kepala laboratorium dan penyelia laboratorium
3.5.2 Proses Persiapan Sampel Otolith
Proses persiapan sampel terdiri dari beberapa tahap sebagai berikut : 1. Pembersihan Sampel (cleaning)
Tahap ini sampel akan dibersihkan ulang oleh analis untuk memastikan tidak ada kotoran, darah yang menempel. Pembersihan ini dapat dilakukan secara langsung maupun tidak langsung. Ukuran otolith besar akan dilakukan pembersihan secara langsung sedangkan ukuran kecil akan dilakukan melalui mikroskop. Pembersihan dilakukan menggunakan aquades.
2.Pemberian label (labeling)
Pemberian label sesuai dengan peratuan yang ada yakni terdiri dari kode spesies, nomor sampel, tempat pengambilan sampel dan bulan pengambilan sampel. Contoh RK01212.
3.Pengeringan
Proses pengeringan dapat dilakukan menggunakan oven suhu 500C selama 4 jam. Namun dapat dilakukan dengan mengeringkan menggunakan tisu.
30 Gambar 3.4 Pembersihan Sampel Otolith
(Sumber: Dokumentasi Pribadi)
3.5.3 Proses Morfometri
Proses morfometri terdiri dalam 3 tahap sebagai berikut :
1. Penimbangan
Proses ini setiap sampel otolith kanan dan kiri ditimbang, cara menggunakan timbangan analitik digital sebagai berikut
Memastikan timbangan pada kondisi seimbang dengan memastikan
gelembung yang ada di pojok kanan bawah timbangan tepat ditengah garis lingkaran hitam
Menghidupkan timbangan analitik digital dengan ketelitian 0,01 gram
Mengkalibrasi timbangan
Cara mengkalibrasi dengan menekan tombol zero-tare-cal dan menunggu hingga loading selesai
Muncul “difference weight” kemudian muncul angka hasil kalibrasi jika
muncul tanda (-) maka hasil penimbangan ditambah dengan angka kalibrasi begitupun jika muncul tanda (+) maka berat dikurangi hasil angka kalibrasi.
31
Memasukkan cawan petri kemudian tutup rapat semua kaca timbangan dan tekan zero
Memasukkan sampel
Mematikan timbangan dengan cara menekan tombol zero kemudian tombol
on/off
Gambar 3.5 Penimbangan Otolith
(Sumber: Dokumentasi Pribadi)
2. Dokumentasi
Proses ini bertujuan untuk mengambil gambar yang akan dipreparasi dan untuk menentukan morfometrik otolith meliputi panjang otolith dari anterior ke
posterior (TL), panjang primordium ke ventral (PV) dan panjang primordium ke posrostrum (PPR). Beberapa hal yang perlu dipersiapkan meliputi mikroskop stereo dan komputer yang dilengkapi aplikasi Leica Application Suite Versi 4.8
(LAS. V.4.8). Langkah- langkah dokumentasi sebagai berikut:
Menghidupkan mikroskop dan komputer
Menyiapkan plastisin pada meja objek mikroskop agar memudahkan saat penandaan titik primordium sampel tidak bergeser
32 Melakukkan pengaturan dengan klik menu calibrasi setting untuk mengatur kalibrasi dan klik confirm on acquire, kemudian klik acquire dan muncul pertanyaan confirm microcope setting. Pastikan pembesaran sesuai dengan pembesaran pada mikroskop dan otomatis gambar akan muncul pada menu browser.
Meletakkan sampel otolith tepat ditengah meja mikroskop
Ketika sudah tepat maka klik menu acquire image
Gambar 3.6 Dokumentasi (Sumber: Dokumentasi Pribadi)
3. Penandaan Titik Primordium
Proses ini bertujuan untuk memberikan tanda pada titik inti otolith yang akan digunakan untuk pendugaan umur ikan. Cara penandaan titik primordium sebagai berikut :
Klik menu acquire kemudian mencari titik primordium, jika dirasa belum tepat maka mikroskop dapat diperbesar ukuran pembesarannya serta menggunakan
eyepiece mikroskop
Tandai titik primordium dengan pensil mekanik 0,35mm
Kemudian letakkan sampel sesuai kode
33 Gambar 3.7 Penandaan Titik Primordium
(Sumber: Dokumentasi Pribadi)
4. Pengukuran Otolith
Proses pengukuran sebagai berikut:
Klik menu process
Klik scale bar- klik show
Basic annotation- klik show
Ubah font 8 dan background hitam lalu klik show
Pilih only line untuk membuat garis bantu, distance line untuk membuat garis disertai angka pengkurannya dan arrow untuk membuat garis disertai tanda panah
Setiap selesai membuat garis klik merge all lalu duplicate untuk menduplikasi gambar dan yang kedua klik replace untuk mengganti gambar tiap penambahan pengukuran
3.5.4 Proses Pembuatan Preparat
1. Penanaman Sampel Otolith34 Blok karet dibersihkan dari sisa resin dengan pinset kemudian menyemprotkan WD-40. Namun pada praktik penulis tidak menggunakan WD-40 sebab bahan yang digunakan mudah dilepas
Resin dan katalis ditimbang kemudian mengaduk dengan cara searah dan perlahan agar tidak muncul gelembung yang akan menghalangi pembacaan preparat Rumus Blocking : Wtot : R+K : R + (R x 3/ 100) Keterangan : R : Resin K: Katalis
Campuran resin dan katalis dituangkan sampai sebagian blok dan tunggu hingga setengah kering
Sampel otolith ditata dengan ketetentuan titik primordium harus sejajar. Tiap satu blok terdiri dari 10 sampel
Tuang campuran resin dan katalis hingga menutupi seluruh bagian blok karet Bahan yang digunakan penulis cepat kering maka tidak perlu dimasukkan
oven namun pada umumnya memerlukan oven untuk proses pengeringan selama 3 jam dengan suhu 55oC.
35 Menimbang resin dan
katalis
Mengaduk resin dan katalis
Menuangkan resin ke blok karet
Menyisihkan gelembung Menyusun otolith Hasil blocking Gambar 3.8 Proses Blocking(Sumber: Dokumentasi Pribadi)
2. Pemotongan Blok Sampel (Sectioning)
Proses ini bertujuan untuk memperoleh sampel tepat pada titik primordium. Proses pemotongan sampel sebagai berikut
Menyiapkan alat dan bahan kemudian tempelkan kertas label pada paper cup yang terdiri dari dua nomor ID sampel. Letakkan blok sesuai Id sampel di
paper cup
Meletakkan blok sampel ke penjepit mesin pemotong sejajarkan blok dengan pisau pemotong, eratkan tuas untuk mengunci blok sampel
Mengatur tuas pada angka 0 untuk pemotongan sisi depan. Usahakan pertama lakukan pemotongan blok jauh dengan sampel otolith
1 2 3
5
36 Menyalakan mesin dan lakukan pemotongan secara horizontal dengan
mendorong secara perlahan blok sampel ke pisau pemotong.
Memutar tuas ke angka 5 karena ketebalan pemotongan yang digunakan 0,5 mm kemudian potong kembali, sisakan bagian yang tidak terpotong agar batangan sampel tidak memantul dari papan dan patah. Lakukan hal yang sama hingga 5-6 potongan dan letakkan kembali ke paper cup.
Gambar 3.9 Proses Pemotongan(Sumber: Dokumentasi Pribadi)
3. Pemolesan Sampel Otolith
Proses ini memiliki tujuan untuk menghaluskan bekas proses pemotongan. Proses pemolesan sebagai berikut
Memilih 4 batangan sampel yang diperkiraan letak titik primordium
Meletakkan potongan sampel otolith di piringan mesin pemoles lakukan pemolesan pada tiap sisi potongan sampel otolith dengan estimasi waktu 1-2 menit
37 Gambar 3.10 Proses Pemolesan(Sumber: Dokumentasi Pribadi)
4. Penempelan Sampel (covering)
Proses ini merupakan tahap terakhir dari proses preparat otolith tujuan dari
covering untuk meletakkan objek hasil preparat yang sudah dipoles agar bisa
diamati dengan jelas menggunakan mikroskop. Proses covering sebagai berikut:
Meletakkan entellan pada object glass (membentuk 2 garis memanjang) menggunakan pinset tetes.
Meletakkan batangan sampel di atas cairan perekat dengan memperhatikan bagian atas yang ditandai dengan potongan kertas
Meratakan kembali cairan perekat diatas batangan sampel kemudian tutup dengan cover glass
Meletakkan kertas label dengan keterangan Id otolith
Mengoven preparat untuk mengeringkan preparat dengan suhu 35oC selama 2,5 jam
38 Meletakkan entellan di
object glass
Menata batangan sampel kemudian ditutupi
entellan kembali
Menutup dengan cover
glass
Hasil setelah di tutup
cover glass
Batangan yang tidak digunakan covering dimasukkan ke vaculab
Mengoven dengan suhu 35oC selama 2,5 jam
Gambar 3.11 Proses Covering (Sumber: Dokumentasi Pribadi)
1 2 3
39
IV. HASIL DAN PEMBAHASAN
4.1 Keadaan Umum Loka Riset Perikanan Tuna
Loka Riset Perikanan Tuna (LRPT) didirikan atas kerja sama CSIRO Australia dan Balai penelitian Perikanan Laut (BPPL) pada tahun 1993 yakni fokus terhadap spesies ikan tuna sirip biru selatan kemudian tahun 2002 mengadakan kerjasana multilateral monitoring tuna The Commonwealth Scientific
and Industrial Research Organisation (CSIRO), Overseas Fishery Coorperation Foundation (OFCF-Jepang) dan Indian Ocean Tuna Commition (IOTC). Tahun
2005 terdapat program observer perikanan kemudian tahun 2009 dibentuk kantor yang berfungsi untuk monitoring perikanan tuna dibawah Balai Penelitian Perikanan Laut. Tahun 2011 resmi menjadi Loka Penelitan Perikanan Tuna (LP2T) yang berdiri dibawah Badan Penelitian dan Pengembangan Kelautan Perikanan (BALITBANG-KP). Pergantian nama berdasarkan instruksi menteri kelautan dan perikanan tahun 2017 menjadi Loka Riset Perikanan Tuna (LRPT).
Dasar Hukum
1. Persetujuan Menteri Negara Pendayagunaan Aparatur Negara dan Reformasi Birokrasi dalam Surat Nomor B-3677/M.PAN-RB/12/12 tanggal 2 desember 2010.
2. Peraturan Menteri Kelautan dan Perikanan Republik Indonesia Nomor: PER.27/MEN/2010 tentang Organisasi dan Tata Kerja Loka Penelitian Perikanan Tuna dimandatkan bahwa LRPT memiliki mandat.
“Melaksakan penelitian sumber daya perikanan tuna dan sejenisnya (tuna like
species) di wilayah negara Republik Indonesia pada perairan Samudera
Hindia”
3. Peraturan Menteri Kelautan dan Perikanan Republik Indonesia Nomor 16/PERMEN-KP/2017 tentang Organisasi dan Tata Kerja Loka Riset Perikanan Tuna
Visi dan Misi LRPT
40 Visi Loka Riset Perikanan Tuna yaitu :
“ Menjadi Institusi Utama Penyedia Data dan Informasi Perikanan Tuna di Samudera Hindia”
- Misi
Sebagai langkah konkret untuk mewujudkan visi tersebut, telah ditetapkan misi LRPT Benoa yang dirumuskan sebagai berikut :
1. Menyediakan data dan informasi terkini hasil penelitian perikanan tuna 2. Mengembangkan profesionalisme kelembagaan dan sumberdaya penelitian
perikanan tuna
Tujuan dan Sasaran LRPT
Tujuan Loka riset perikanan tuna sebagai berikut:
1. Menghasilkan data dan informasi karakteristik sumberdaya ikan tuna di Samudera Hindia
2. Menyiapkan bahan kebijakan bagi perencanaan pengelolaan perikanan tuna 3. Menggalang kerjasama penelitian perikanan tuna
4. Melaksanakan dan menyediakan bahan diseminasi hasil penelitian 5. Menyiapkan sarana dan prasarana bagi pelaksanaan kegiatan penelitian 6. Mengembangkan kapasitas kelembagaan dan kompetensi sumberdaya
penelitian perikanan tuna
7. Meningkatkan akuntabilitas dan kapabilitas kelembagaan
Sasaran Loka riset perikanan tuna sebagai berikut:
1. Teridentifikasi potensi produksi dan karakteristik sumberdaya ikan tuna di samudera hindia
2. Tersedianya bahan informasi bagi kebijakan perencanaan pengelolaan perikanan tuna
3. Terbentuknya kemitraan dan jejaring kerja 4. Tersedianya bahan diseminasi hasil penelitian
5. Terpenuhinya sarana dan prasarana pendukung kegiatan penelitian
6. Tersedianya sumberdaya manusia yang kompeten dan handal di bidangnya. 7. Terbentuknya institusi penelitian yang akuntabel
41 Struktur Organisasi LRPT
Struktur organisasi dan pejabat yang ada dalam organisasi LRPT terlihat pada gambar 4.1
Gambar 4.1 Struktur Organisasi Loka Riset Perikanan Tuna TA 2019 (Sumber : lp2t.kkp.go.id/)
Dalam pelaksanaan tugas dan fungsi LRPT dipimpin oleh seorang kepala, dengan struktur organisasi sebagai berikut:
1. Urusan tata usaha mempunyai tugas melaksanakan urusan tata usaha, keuangan, kepegawaian, perlengkapan dan rumah tangga serta penyusunan laporan.
2. Subseksi tata operasioanl mempunyai tugas melakukan penyusunan rencana , program dan anggaran, penyebarluasan hasil penelitian serta pemantauan dan evaluasi.
3. Subseksi pelayanan teknis mempunyai tugas melakukan pelayanan teknis, pengelolaan sarana dan prasarana serta kerja sama penelitian.
4. Kelompok jabatan fungsional mempunyai tugas melaksanakan kegiatan penelitian sumberdaya perikanan tuna dan sejenisnya (tuna like spesies) dan kegiatan lain sesuai dengan tugas masing-masing jabatan fungsional berdasarkan peraturan perundang- undangan.
42 Sumberdaya Loka Riset Perikanan Tuna
Tahun 2018, Loka Riset Perikanan Tuna memiliki 49 pegawai yang terdiri dari 21 orang Pegawai Negeri Sipil dan 28 orang Pegawai Pemerintah Non Pegawai Negeri Sipil. Berdasarkan pada tingkat pendidikan terakhir, pegawai LRPT bervariasi mulai dari SLTP (1), SLTA (11), Diploma III (3), Diploma IV (1), S-1 (27) dan S-2 (5). Komposisi pegawai LRPT berdasarkan tingkat pendidikan terakhir dapat dilihat pada gambar 4.2
Gambar 4.2 Komposisi Pegawai LRPT Berdasarkan Tingkat Pendidikan 2018 (Sumber : lp2t.kkp.go.id/)
Berdasarkan pada golongannya, Pegawai Negeri Sipil LRPT terdiri dari golongan II dan III dengan rincian golongan IIc (2), IId (1), IIIa (6), IIIb (6), IIIc (4), dan IIId (2). Komposisi pegawai LRPT berdasarkan perkembangan golongan tahun 2011-2018 dapat dilihat pada gambar 4.3
43 Gambar 4.3 Komposisi PNS LRPT Berdasarkan Golongan Tahun 2018
(Sumber : lp2t.kkp.go.id/)
Berdasarkan jabatan fungsional, LRPT memiliki tiga kelompok jabatan fungsional yang meliputi peneliti muda sebanyak 5 orang, peneliti pertama sebanyak 2 orang, calon peneliti sebanyak 6 orang. Komposisi jabatan fungsional pegawai LRPT dapat dilihat pada gambar 4.4
Gambar 4.4 Komposisi Pegawai Berdasarkan Jabatan Fungsional Tahun 2018 (Sumber : lp2t.kkp.go.id/)
Seluruh sumber daya manusia LRPT memiliki tugas dan fungsi masing-masing untuk mendukung pelaksanaan penelitian sumber daya perikanan tuna dan sejenisnya (tuna like species) di wilayah Negara Republik Indonesia pada Perairan Samudra Hindia.
44
Fasilitas Loka Riset Perikanan Tuna
Adapun fasilitas yang disediakan di Loka Riset Perikanan Tuna Denpasar Bali yaitu
1. Ruang Kepala Loka 2. Ruang Sub Sie Tata Usaha 3. Ruang Sub Sie Tata Operasional 4. Ruang Sub Sie Pelayanan Teknis 5. Ruang Peneliti 6. Ruang Rapat 7. Aula 8. Laboratorium Histologi 9. Laboratorium Genetik 10.Laboratorium Otolith
Laboratorium otolith Loka Riset Perikanan Tuna merupakan salah satu fasilitas laboratorium yang sudah beroperasi sejak 2016. Kegiatan analisis fokus pada umur dan pertumbuhan ikan dengan pengamatan lingkaran umur ikan menggunakan otolith. Metode ini disesuaikan dengan keahlian staf laboratorium dan ketersediaan alat yang ada.
45 11.Laboratorium Data 12.Mushola 13.Perpustakaan 14.Parkiran 15.Pura 16.Guest House
4.2 Pengambilan Data Biologi Ikan
4.2.1 Sampling di Pelabuhan Benoa-Bali
Kegiatan sampling ini dilakukan untuk menunjang pengetahuan sistem pengambilan sampel Otolith. Prosedur pengambilan data hasil tangkapan mengacu pada kegiatan yang dilakukan di LRPT terdiri dari beberapa tahap sebagai berikut
Tabel 4.1 Hasil Kegiatan Sampling
No. Nama Kegiatan Hasil
Sampling ke 1 Sampling ke 2 Sampling
ke 3 1. Mencatat data
kapal meliputi nama kapal dan GT kapal. KM Bali nusa 8 GT 77 KM Mulia GT 29, KM Hasil Jaya Sejati KM Primus Indah GT 29 KM Primus Jaya 99, KM Naga Mas Perkasa 18 2. Mencatat informasi ikan
jenis ikan BET YFT SBT BET, YFT,
SWO,
YFT, BET, SBT
jumlah ikan 128 ekspor 105 ekspor 85 ekspor
bobot ikan 6.971 kg 4.807 kg, 3.865 kg
panjang ikan 142,155,158 87-147cm 84-184 cm
3. Mengambil sampel otolith
Menggunakan metode Up through the gill 4. Mencatat data Data hasil sampling direkap sesuai kategori hasil
tangkapan Keterangan :
BET : big eye tuna YFT : Yellow fin tuna SBT : Southern bluefin tuna
46
4.2.2 Identifikasi Jenis ikan
Hasil kegiatan identifikasi ikan sebagai berikut:
a. Tuna Sirip Biru Selatan (Southern bluefin tuna)
Gambar 4.6 Tuna Sirip Biru Selatan (Sumber: Dokumentasi Pribadi)
Klasifikasi tuna sirip biru selatan menurut WoRMS (1997) sebagai berikut: Kingdom : Animalia Filum : Chordata Kelas : Actinopterygii Ordo : Perciformes Family : Scombridae Genus : Thunnus
Spesies : Thunnus maccoyii
Tuna sirip selatan merupakan spesies tuna yang memiliki kemampuan renang cepat. Ikan ini termasuk salah satu famili tuna sirip biru selain Pacific Bluefin Tuna (Thunnus orientalis) dan Atlantic Bluefin Tuna (Thunnus thynnus). Identifikasi eksternal ikan ini memiliki bentuk tubuh bulat melebar. Warna tubuh biru kehitam-hitaman pada bagian tubuh atas dan bagian bawah memiliki warna putih keperakan. Finlet berwarna kuning, bertepi hitam dan ujungnya putih. Keel berwarna kuning pucat.
47
b. Tuna Sirip Kuning (yellow fin tuna)
Gambar 4.7 Tuna Sirip Kuning (Sumber: Dokumentasi Pribadi)
Klasifikasi tuna sirip kuning menurut WoRMS (2004) sebagai berikut: Kingdom : Animalia
Filum : Chordata Class : Osteichthyes Family : Scombridae
Genus : Thunnus
Spesies : Thunnus albacares
Tuna sirip kuning atau dapat disebut Thunnus albacares memiliki ciri eksternal yakni memiliki tubuh cenderung memanjang ,bola mata lebih kecil. Bagian badan hingga ekor agak datar memanjang. Finlet berwarna kuning bertepi hitam tipis. Ujung keel berwarna putih. Warna tubuh cenderung biru metallic dan berubah keperakkan pada bagian perut serta memiliki corak garis pada tubuh bagian bawah.
48
c. Tuna Mata Besar (big eye tuna )
Gambar 4.8 Tuna Mata Besar (Sumber: Dokumentasi Pribadi)
Klasifikasi tuna mata besar menurut WoRMS (2009) sebagai berikut: Kingdom : Animalia Filum : Chordata Class : Pisces Ordo : Perciformes Family : Scombridae Genus : Thunnus
Spesies : Thunnus obesus
Tuna mata besar atau big eye tuna memiliki ciri eksternal seperti bentuk tubuh cenderung pendek dan membulat, Warna mata cenderung abu-abu bola mata cenderung lebih besar, jarak moncong ke operkulum lebih pendek. Finlet berwarna kuning bertepi hitam tebal. Jarak antara finlet cenderung pendek. Ujung
49
d. Kembung Lelaki
Gambar 4.9 Kembung Lelaki(Rastrelliger kanagurta) (Sumber: Dokumentasi Pribadi)
Klasifikasi ikan kembung lelaki menurut WoRMS (2004) sebagai berikut : Kingdom : Animalia Filum : Chordata Class ; Pisces Ordo : Percomorphi Family : Scombridae Genus : Rastrelliger
Spesies : Rastrelliger kanagurta
Ciri eksternal spesies ini memiliki bentuk tubuh torpedo dengan bagian dada lebih lebar dari bagian tubuh yang lain namun cenderung lebih gemuk jika dibandingkan dengan ikan kembung perempuan. Terdapat dua sirip punggung, sirip dada, sirip perut dan sirip dubur. Warna tubuh cenderung keperakan pada bagian atas dan terdapat bercak hitam hingga ekor.
50
4.2.3 Pengukuran Panjang dan Berat Ikan
Metode pengukuran berat dilakukan oleh petugas dari perusahaan prosesing sedangkan data panjang dilakukan oleh enumerator. Jenis Pengukuran panjang menurut IOTC (2002), disajikan pada Tabel 4.2
Tabel 4.2 Pengukuran Panjang Kelompok Tuna
Tipe Deskripsi Kode
Mengukur tepat rahang atas ke sirip ekor yang terpendek (fork)
FL
Mengukur badan dengan meteran melengkung dari ujung rahang atas ke sirip ekor terpendek
FLT
Mengukur tepat rahang atas ke duri sirip punggung pertama
LDI
Mengukur badan melengkung dari ujung rahang atas ke bagian duri sirip punggung pertama
LDIT
51
Data yang diperoleh dari pengukuran panjang dan berat sampel ikan yang diambil untuk metode analisa pengambilan otolith disajikan pada Tabel 4.3.
Tabel 4.3 Hasil Pengambilan Data Biologi Ikan Kembung Lelaki (Rastrelliger
kanagurta)
Keterangan :
Yang mempengaruhi kondisi yakni proses pengambilan Otolith FL: Fork Lenght
TL: Total Lenght W: Berat ikan
Berdasarkan praktik pengambilan otolith menggunakan 14 sampel ikan kembung lelaki hanya 13 otolith yang diperoleh sedangkan 1 otolith rusak.
SPESIES IKAN NAMA ILMIAH KODE IKAN FL(cm) TL(cm) W(gr) KONDISI OTOLITH Ikan kembung lelaki Rastrelliger
kanagurta RAG 27.5 31.5 418 UTUH
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 25 27.5 278 UTUH
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 26 28 292 TIDAK UTUH
Ikan kembung lelaki Rastrelliger kanagurta RAG 26 28.5 303 TIDAK UTUH Ikan kembung lelaki Rastrelliger kanagurta RAG 25.5 27.3 313 TIDAK UTUH Ikan kembung lelaki Rastrelliger
kanagurta RAG 27.5 30 369 UTUH
Ikan kembung lelaki Rastrelliger kanagurta RAG 26.6 28.5 302 TIDAK UTUH Ikan kembung lelaki Rastrelliger
kanagurta RAG 24.5 27 244 RUSAK
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 27.5 30.5 408 UTUH
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 29.2 31.7 452 UTUH
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 30.5 33.5 520 UTUH
Ikan kembung lelaki
Rastrelliger
kanagurta RAG 28 30.5 381 UTUH
Ikan kembung lelaki Rastrelliger kanagurta RAG 23 24.3 192 TIDAK UTUH Ikan kembung lelaki Rastrelliger
52 4.3 Bagian-Bagian Otolith
Setiap ikan memiliki Otolith ikan terdiri dari sepasang otolith kanan dan otolih
kiri. Contoh Otolith Ikan Cakalang (Katsuwonus pelamis) Wudji et al., 2017
Keterangan: Morfologi otolith pada Gambar 4.10 a: Rostrum (R), Antirostrum (Ar), Postrostrum (Pr), dan Excisura Major (Ej); sumbu pengukuran morfometri otolith pada Gambar 10b: Panjang otolith (OL), Lebar otolith (OW), Keliling otolith (OP), dan Luas otolith (OA)
Hasil sampel Otolith ikan kembung lelaki (Rastrelliger kanagurta)
Gambar 4.11 Bagian-bagian Otolith Kiri ikan kembung lelaki (Rastrelliger kanagurta) (Sumber: Dokumentasi Pribadi)
Primordium merupakan titik awal pertumbuhan atau awal terbentuknya Otolith yang digunakan sebagai acuan dalam pembacaan umur ikan.
anterior posterior
DORSAL
VENTRAL
53 Gambar 4.12 Bagian-bagian Otolith Kanan ikan kembung lelaki (Rastrelliger
kanagurta)(Sumber: Dokumentasi Pribadi).
Berdasarkan kedua jenis ikan ini memiliki bentuk Otolith yang tidak jauh berbeda Dikarenakan spesies ini termasuk satu kategori family yang sama yakni
scrombidae.
Gambar 4.13 Hasil Morfometri (Sumber: Dokumentasi Pribadi) Keterangan TL : anterior ke posterior PV : Primordium ke ventral PPR : Primordium ke posterior VENTRAL DORSAL posterior anterior TL PV PPR
54 Hasil penimbangan otolith ikan kembung lelaki disajikan pada Tabel 4.4.
Tabel 4.4 Hasil Penimbangan Otolith Ikan Kembung Laki ID
OTOLITH OW(gr) KETERANGAN
KA KI RK01212 0.0091 0.0089 UTUH RK02212 0.0074 0.0074 UTUH RK03212 0.0067 0.0069 TIDAK UTUH RK04212 0.0071 0.0053 TIDAK UTUH RK05212 0.0067 0.0063 TIDAH UTUH RK06212 0.0102 0.0104 UTUH RK07212 0.0073 - TIDAK UTUH RK08212 - - RUSAK RK09212 0.0094 0.0093 UTUH RK10212 0.0155 0.0144 UTUH RK11212 0.0203 0.0202 UTUH RK12212 0.0101 0.0105 UTUH RK13212 0.0085 0.0081 TIDAK UTUH RK14212 0.0073 0.0076 UTUH Keterangan :
RK : nama spesies (Rastrelliger kanagurta)
otolith pada tiap ikan memiliki berat dengan selisih yang kecil bahkan memiliki
berat yang sama. Hal ini berkaitan dengan awal pembentukan otolith terjadi pada waktu yang sama sehingga kedua otolith cenderung memiliki umur yang sama (Bahri et al.,2018). Namun jika dibandingkan antar sampel ikan terdapat perbedaan hasil penimbangan Otolith secara signifikan. Hal ini dikarenakan faktor lingkungan yang menyebabkan perbedaan pembentukan CaCo3 dan ketika proses pengambilan terdapat bagian yang pata (Wudji et al., 2017).
4.4 Pembacaan Preparat untuk Pendugaan Umur
Sampel otolith yang telah di preparat perlu didokumentasi untuk memperoleh gambar yang akan dilakukan pengamatan. Analisa preparat menggunakan mikroskop compound trinokuler yang terhubung dengan PC serta aplikasi LAZ EZ
V.3.4.10. Proses pembesaran yang tepat bertujuan untuk mempertajam garis-garis
umur pada otolith kemudian sampel siap dianalisis oleh kepala laboratorium dan penyelia. Hal yang perlu diperhatikan dalam proses ini yakni mampu
55
membedakan zona translucent (zona terang) dan zona opaque (zona gelap) dan mampu membedakan garis umur dan bukan garis umur. Contoh dokumentasi preparat dapat dilihat pada Gambar 4.14. Berikut contoh hasil dokumentasi preparat menunjukkan adanya increment otolith sebagai pola pertumbuhan pada ikan. Pendugaan berumur 5 tahun namun pembacaan umur ini divalidasi oleh penelitian sebelumnya.
Gambar 4.14 Kegiatan Dokumentasi Preparat
56 Gambar 4.15 Preparat Otolith Ikan Kembung Laki
(Sumber: Laboratorium Otolith LRPT)
Gambar 4.16 Preparat Otolith tuna sirip biru selatan
(Sumber: CCSBT 2002) 1 2 3 4 5
57
Cara Pembacaan Preparat Otolith SBT sebagai Berikut 1. Mulai dari primordium dan lanjutkan ke ujung terminal
2. Identifikasi wilayah bagian dalam, tengah dan luar
3. Hitung zona pertumbuhan dalam (beberapa pertama) Tidak ada zona pertumbuhan tahunan antara primordium dan infleksi pertama
4. Hitung zona pertumbuhan menengah (hingga sekitar infleksi kedua) 5. Hitung zona pertumbuhan luar (di luar infleksi kedua)
Konsistensi dan ketepatan pembacaan umur dapat diiketahu tingkat kesalahan baca dengan membandingkan hasil pembacaan umur antar pembaca. Salah satu metode yang dapat digunakan melalui metode Average Percentage Error (Beamish and Fournier 1981). Berikut penjelasan mengenai metode APE tersebut dan contoh simulasi pembacaan pada tabel 4.7
Keterangan:
APE : Average Percentage Error
Xij : Pendugaan umur pada pembaca ke-n Xj : Rata-rata umur otolith
R : Jumlah ikan yang dibaca umurnya
Tabel 4.5 Simulasi Average Percentage Error
No. ID OTOLITH TL umur Xij-Xj/Xj APE 1 RK06212 30 4 0,14286 10,60% 2 RK07212 28,5 3 0,1429 3 RK09212 30,5 3 0,06024 4 RK10212 31,7 4 0,14286 5 RK11212 33,5 4 0,14286 6 RK12212 30,5 4 0,14286 7 RK13212 24,3 3 0,1429 8 RK14212 28 3 0,1429 Jumlah 28 1,06038 rata-rata 3,5 APE
58
Hasil simulasi baca preparat yakni 10,60%, Menurut CCSBT (2002), nilai maksimal yang dianjurkan adalah 10%. Apabila melebihi nilai tersebut, pendugaan umur memiliki tingkat kesalahan baca . Simulasi ini untuk memastikan keakuratan pendugaan umur antar pembaca.
4.5 Permasalahan yang dihadapi selama proses pengambilan sampel dan preparasi otolith
Operkulum yang kurang terbuka menjadi faktor kesulitaan ketika proses pengeboran akibatnya bor sulit digerakkan ke depan dan belakang sehingga patahan tulang tidak sempurna. Selain itu pengeboran yang kurang tepat dapat menghancurkan otolith karena terkena mata bor.
Kondisi ikan yang berbeda menyulitkan saat proses identifikasi ikan Mengalami kesulitan menentukan titik primordium
Karena menyesuaikan bahan resin yang mudah kering sehingga terburu-buru ketika penyusunan otolith, sehingga dapat menyebabkan sampel tidak sejajar dengan rapi .
Proses pemotongan kurang teliti ketika memutar tuas sehingga hasil potongan blok sampel tidak sama, sering mengganti posisi penjepit blok sampel sehingga tidak sejajar dengan pisau pemotong mengakibatkan tidak terpotong maksimal
Melakukan pemotongan hingga habis sehingga batangan sampel patah dan memantul dari papan
Waktu yang tidak sama ketika pemolesan mengakibatkan garis umur tidak terbaca
Pada proses covering entellan pada kaca preparat tidak rata dan adanya gelembung sehingga preparat tidak bisa dibaca