Medula | Volume 7 | Nomor 4 | November 2017| 171
Aktivasi Jalur Protein Kinase C (PKC) oleh
Epigallocatechin-3-Gallate
(EGCG)
dalam Teh Hijau sebagai Pencegahan terhadap
Alzheimer’s
Disease
Debby Cinthya DV, Khairun Nisa
Fakultas Kedokteran, Universitas Lampung
Abstrak
Alzheimer’s disease (AD) adalah penyakit neurodegeneratif yang bergantung pada usia yang secara progresif menyerang bagian otak tertentu yang mengatur fungsi memori dan kognitif. Alzheimer’s disease juga merupakan tipe demensia terbanyak. Temuan khas pada AD adalah adanya plak amiloid beta (Aβ) dan neurofibrillary tangles mikroskopis. Perkembangan temuan tersebut melalui mekanisme sebagai berikut, yaitu inflamasi yang dipicu mikroglia, aktivasi berlebihan glutamat, dan disfungsi mitokondria. Sampai saat ini, belum ada terapi farmakalogi yang efektif untuk mengobati AD. Sementara, obat-obatan hanya bersifat simptomatis dengan sedikit keuntungan tanpa adanya aktivitas yang memodifikasi penyakit. Pencegahan atau penundaan onset AD dan progres penyakit akan meningkatkan kesehatan dan kualitas hidup lansia. Studi epidemiologi pada manusia dan hewan menunjukkan kegunaan konsumsi teh hijau dapat menurunkan insidensi demensia dan AD. Teh hijau mengandung epigallocatechin-3-gallate (EGCG), salah satu dari empat tipe cathecin yang terkandung dalam teh hijau, yang memiliki efek neuroprotektif terhadap AD melalui aktivasi protein kinase C (PKC) dengan meningkatkan sekresi sAPPα yang akan menurunkan kadar Aβ di otak dan aktivasi endothelial converting enzyme (ECE) yang dapat mendegradasi plak Aβ. Diharapkan manfaat ini dapat menjadi solusi yang lebih baik untuk mencegah AD di masa yang akan datang.
Kata kunci: Alzheimer’s disease, EGCG, pencegahan, PKC
The Activation of Protein Kinase C (PKC) Pathway by
Epigallocatechin-3-Gallate (EGCG) in Green Tea as Prevention of
Alzheimer’s Disease
Abstracts
Alzheimer’s disease (AD) is an age dependent neurodegenerative disease which progressively affects specific brain regions that control the functions of memory and cognitive. Alzheimer’s disease is also the most prevalent type of dementia. The hallmarks of AD are toxic beta amyloid (Aβ) plaque and neurofibrillary tangles found microscopically. The development of those findings is through the following mechanisms such as microglia-triggered inflamation, over activation of glutamate, and mitochondrial dysfunctions. Till now, there are no effective pharmacological treatments to treat AD. Meanwhile, the current medications are mainly symptomatic offering only partial benefits without any disease modifying activity. Preventing or postponing the onset of AD and delaying the progression would lead to improvement of health and quality of life of elderly. Epidemiological studies in human and animals suggest the benefits of drinking green tea may decrease the incidence of dementia and AD. Green tea contains epigallocatechin-3-gallate (EGCG), one of four types of cathecins found in green tea, which has the effect of neuroprotective against AD through the activation of protein kinase C (PKC) pathway. It leads to the increase of sAPPα secretion that can reduce the level of Aβ in the brain and the activation of endothelial converting enzyme (ECE) which degrades Aβ plaque. Hopefully, this can be a better solution to prevent AD in the future.
Keywords: Alzheimer’s disease, EGCG, prevention, PKC
Korespondensi: Debby Cinthya Damiri Valentina, alamat: Jl. Katu II Gg. Swadaya No. 11, No HP: 082379511443, e-mail: debbycinthya048@gmail.com
Pendahuluan
Penyakit neurodegeneratif menjadi beban tersendiri bagi suatu negara baik dari segi ekonomi maupun sosial. Salah satu penyakit neurodegeneratif yang paling banyak disoroti saat ini adalah Alzheimer’s disease (AD). Insidensi AD terbukti meningkat seiring bertambahnya usia. Perubahan neuropatologi pada AD pertama kali dideskripsikan oleh Alois Alzheimer pada 1906.1 Lesi mikroskopis utama
yaitu adanya plak amiloid beta (Aβ) ekstraseluler dan nerofibrillary tangles intraseluler yang secara signifikan banyak ditemukan pada pasien
AD dibandingkan pada populasi lanjut usia (lansia) normal.2
Alzheimer’s disease menjadi penyebab
umum terjadinya demensia dan gangguan kognitif pada lansia. Demensia pada AD memiliki onset yang gradual dan penurunan kognitif yang berkelanjutan termasuk gangguan memori dan satu atau lebih dari gejala seperti aphasia
(gangguan bahasa), apraxia (gangguan fungsi motorik), agnosia (gangguan fungsi sensoris), dan gangguan fungsi eksekutif seperti
ketidakmampuan perencanaan,
Medula | Volume 7 | Nomor 4 | November 2017| 172
normal.3,4,5,6 Diantara beberapa mekanisme
patogenesis AD, inflamasi, faktor genetik, dan stress oksidatif memegang peranan penting dalam terjadinya gejala-gejala tersebut.1
Terdapat sekitar 46 juta jiwa yang menderita AD di seluruh dunia dengan 22 juta diantaranya berada di Asia. Estimasi penderita AD di negara maju, seperti Amerika Serikat, yaitu sebanyak 4 juta orang. Angka ini diperkirakan akan meningkat kurang lebih 4 kali pada tahun 2050. Hal ini disebabkan meningkatnya angka harapan hidup negara maju sehingga populasi penduduk usia lanjut akan bertambah. Jumlah penderita AD di Indonesia pada tahun 2013 mencapai 1 juta orang. Jumlah tersebut diperkirakan akan meningkat dua kali lipat pada tahun 2030 dan akan menjadi 4 juta orang pada tahun 2050.7
Teh hijau banyak diteliti sebagai upaya pencegahan AD dalam dekade terakhir. Kandungan polifenol dalam teh hijau memiliki efek potensial untuk mencegah penyakit neurodegeneratif, penyakit inflamasi, dan kanker. Salah satu polifenol yang terkandung di dalam teh hijau, yaitu epigallocatechin-3-gallate
(EGCG), memiliki efek sebagai antioksidan, metal chelating, antikarsinogenik, dan antiapoptosis. Penelitian yang telah dilakukan menunjukkan potensi untuk meningkatkan proses penuaan yang sehat dengan memperbaiki morfologi dan fungsi yang terjadi pada proses penuaan alami di otak, menekan disfungsi kognitif, dan mengurangi kerusakan oksidatif di otak.2,8,9,10
Isi
Alzheimer’s disease (AD) merupakan kelainan neurodegeneratif yang ditandai dengan terbentuknya dua struktur protein abnormal,
neurofibrillary tangles yang terbentuk dari protein tau dan plak amiloid beta (Aβ), yang terdapat di neokorteks.11 Insiden AD dibagi
menjadi dua, yaitu onset dini dan onset lanjut. Pada onset dini, AD terjadi pada usia kurang dari 65 tahun dan terjadi <2% dari kejadian AD12,
digambarkan menjadi dua tipe lain berdasarkan pada pola bawaan, yaitu AD familial (FAD) yang mengikuti pola bawaan khusus dan AD sporadik yang tidak mengikuti pola bawaan. Diagnosis
pasti AD ditegakkan berdasarkan temuan pada autopsi pasca kematian dengan ditemukannya plak amiloid dan neurofibrillary tangles pada daerah spesifik otak. Pemeriksaan klinis, laboratorium, dan CT scan otak serta alat ukur memori, bahasa, dan kemampuan kognitif lainnya hanya sebatas untuk diagnosis probable
(kemungkinan) AD.13
Degenerasi neuron biasa ditemukan di lobus temporal bagian medial (korteks entorhinal/perirhinal dan hipokampus), korteks temporal bagian lateral, dan nukleus basalis Meynert. Temuan mikroskopis khas berupa plak Aβ dan neurofibrillary tangles yang ditemukan sangat sedikit pada proses normal namun sangat meningkat pada pasien AD. Amiloid beta (Aβ) merupakan protein yang terdiri atas 39-42 asam amino dan merupakan turunan dari protein transmembran yang lebih besar yaitu amyloid precursor protein(APP) yang terbagi oleh β- dan
ϒ- secretase. Polimerisasi amiloid dan pembentukan benang (fibril) selanjutnya akan membentuk plak neuritik yang ditengahnya dibentuk oleh amiloid, proteoglikan, Apo ε4, α
-antichymotrypsin, dan protein lain serta bercampur dengan bagian neuron, mikroglia, dan astrosit. Plak tersebut tidak dapat larut dan menjadi toksik bagi neuron. Selain itu, Aβ mengganggu hubungan intraseluler dan menurunkan respons pembuluh darah sehingga neuron rentan terhadap stresor. Adanya mikroglia menandakan adanya peradangan aktif yang merusak neuron.4,12,13
Neurofibrillary tangles terbentuk dari benang sitoplasma neuron yang terdiri dari protein tau yang mengalami fosforilasi abnormal. Normalnya, tau berikatan dengan mikrotubulus, mendukung transportasi organel pada akson, dan pertukaran zat lain pada sel. Ketika protein tau mengalami hiperfosforilasi dan tidak terikat dengan mikrotubulus secara sempurna, tau akan dibawa menuju sitoplasma neuron dan dendrit distal. Kemudian dengan kolapsnya sistem transpor internal, hubungan intraseluler tidak berfungsi, dan akhirnya sel akan mati. Pada model hewan AD, kehilangan protein tau menyebabkan defisit kognitif dan timbulnya kejang.12,13
Medula | Volume 7 | Nomor 4 | November 2017| 173
meningkatkan produksi dan agregasi dari Aβ di limbik dan korteks. Proses yang sama akan terjadi hingga menyebabkan disfungsi neuron dan hilangnya neuron selektif diikuti dengan penurunan neurotransmiter dan hilangnya sinaps hingga timbulnya demensia pada AD.4,13
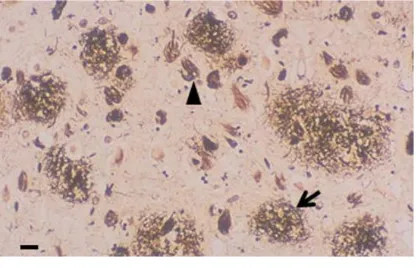
Gambar 1. Gambaran Mikroskopis pada Potongan
Otak Pasien AD. Terlihat adanya Plak Aβ (panah) dan Neurofibrillary Tangles (kepala panah)12
Disfungsi neuron dan sinaps pada
neokorteks dan hipokampus dapat
mengakibatkan defisit fungsional dan perilaku pada pasien AD.1 Perubahan kognitif pada AD
dimulai dari kerusakan memori dan secara progresif berkembang menjadi defisit pada bahasa dan visuospasial. Gejala yang timbul pada tahap awal disebabkan oleh rusaknya struktur saraf yang mengatur memori, khususnya hipokampus. Ketika saraf di bagian hipokampus tidak berfungsi, kemampuan memori jangka pendek akan hilang dan kemampuan untuk melakukan kegiatan mudah dan tugas biasa lambat laun akan berkurang. Pada pemeriksaan kemampuan memori standar, pasien pada tahap ini dikategorikan dalam penurunan kemampuan kognitif ringan atau mild cognitive impairment (MCI). Selanjutnya pasien
memasuki tahap pertengahan, terjadi
ketidakmampuan dalam berbahasa dimulai dari kesulitan penamaan, pemahaman, hingga kelancaran berbicara; menurunnya kemampuan untuk membuat keputusan; dan timbul perubahan kepribadian. Gejala-gejala tersebut muncul ketika neuron di korteks serebri mulai rusak khususnya di daerah yang mengatur bahasa dan pemikiran. Penurunan pada memori yang berhubungan dengan motorik (apraxia) muncul dan pasien akan mulai sulit untuk
melakukan aktivitas seperti berpakaian, makan, dan berjalan.12,13
Pada tahap lanjut, emosi yang meledak-ledak dan gangguan perilaku, seperti berjalan tanpa arah dan agitasi, serta perubahan waktu tidur akan muncul seiring perjalanan penyakit. Beberapa pasien mengalami kekakuan otot
secara keseluruhan sehingga terjadi
ketidakmampuan dalam melakukan gerakan. Selanjutnya pada tahap akhir, ketika banyak bagian otak yang terlibat dan mengalami atrofi, pasien AD hanya akan mampu berbaring di tempat tidur dan sangat bergantung pada orang lain untuk melakukan tugas pribadi yang paling mendasar, seperti makan, mandi, dan buang air. Refleks tendon hiperaktif dan kontraksi otot yang cepat secara tiba-tiba (myoclonic jerks) dapat terjadi secara spontan maupun setelah rangsangan fisik dan auditori.12,13
Penelitian tentang pengobatan AD sampai saat ini belum mendapatkan hasil optimal. Upaya pencegahan dapat dilakukan dengan memperlambat proses yang terjadi pada pasien AD dengan mengonsumsi zat yang bersifat neuroprotektif. Teh hijau mengandung salah satu polifenol, yaitu epigallocathecin-3-gallate
(EGCG), yang memiliki aktivitas neuroprotektif pada sel pada model hewan percobaan yang mengalami proses neurodegeneratif, yaitu AD.14,15
Teh hijau merupakan minuman tradisional dari tanaman Camellia sinesis yang banyak dikonsumsi oleh bangsa Asia. Terdapat empat senyawa derivat berdasarkan variasi struktural zat-zat tersebut, yaitu epicatechin (ECG),
epigallocatechin (EGC), epicatechin gallate
(ECG), dan epigallocathecin-3-gallate (EGCG) (Gambar 2). Kandungan EGCG dalam teh hijau merupakan kandungan terbanyak yaitu sebanyak 10% dari berat ekstrak kering dan 50%-80% dari 200-300 mg dalam teh hijau yang telah diseduh.2
Medula | Volume 7 | Nomor 4 | November 2017| 174
Gambar 2. Cathecin dalam Teh Hijau dan Derivatnya2
Aktivitas EGCG sebagai neuroprotektif salah satunya adalah dengan menghambat proses amiloidogenesis dengan mengaktivasi jalur protein kinase C (PKC) yang berefek pada penurunan kematian sel secara signifikan.15,17
PKC juga memiliki peran dalam pengaturan cell survival, program kematian sel, dan konsolidasi memori serta proteksi neuron dari berbagai jenis rangsangan eksogen, salah satunya Aβ toksik pada neuron di korteks dan hipokampus.15
Peningkatan kerja PKC mampu meningkatkan kemampuan memori, kognitif, dan efek anti-demensia.2
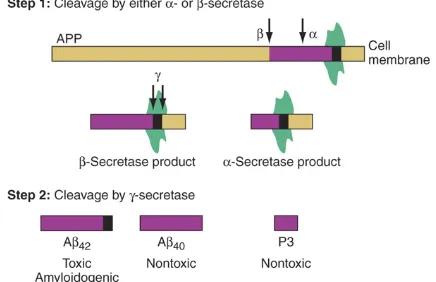
Amiloid β dihasilkan dari APP yang
dipecah oleh α dan β secretase pada tahap satu
menghasilkan produk α-secretase (sAPPα)
melalui proses non-amiloidogenikdan produk β
-secretase(sAPPβ) melalui proses amiloidogenik. Selanjutnya, kedua produk tersebut akan melalui
proses pemecahan tahap dua oleh ϒ-secretase.
Produk α-secretase (sAPPα) akan menghasilkan peptida P3 nontoksik, sedangkan sAPPβ akan menghasilkan Aβ40 nontoksik dan Aβ42 toksik.
Penumpukan Aβ42 merupakan inisiator
kerusakan sel saraf pada AD. Proses ini dijelaskan dalam Gambar 3.12
Penelitian pada mencit AD, EGCG terbukti
meningkatkan sAPPα melalui aktivasi jalur
non-amiloidogenik, yaitu pembelahan APP oleh α
-secretase, via jalur PKC teraktivasi15, Peningkatan
sAPPα tersebut diikuti oleh inhibisi pembentukan Aβ amiloidogenik sehingga terjadi reduksi kadar Aβ di serebral dan penurunan
pembentukan plak Aβ. Berkebalikan dengan efek Aβyang toksik terhadap neuron, sAPPα memiliki
efek berupa neuroprotektif terhadap
eksitotoksik dan oksidatif pada sel serta
meningkatkan pertumbuhan neuron dan
sinaptogenesis pada neuron serebral.15 Hasil
yang terjadi yaitu berupa berkurangnya
akumulasi Aβ, penurunan hiperfosforilasi protein
tau, dan penurunan proses apoptosis di otak.17
Selain itu, studi pada mencit transgenik menunjukan aktivasi jalur PKC juga akan meningkatkan aktivasi dan kerja endothelin converting enzyme (ECE) yang mampu
mendegradasi Aβ dan mencegah fibrilasi Aβ.
Epigallocatechin-3-gallate (EGCG) dapat
menurunkan kadar Aβ melalui rangsangan sekresi sAPPα dan meningkatkan klirens Aβ serta degradasi plak Aβ melalui peningkatan aktivitas ECE.2,15,18
Gambar 3. Katabolisme Amyloid Precursor Protein (APP) oleh α-, β-, ϒ- secretase12
Dosis per oral yang pernah diberikan pada hewan coba sebesar 50 mg/kgBB/ hari selama enam bulan menunjukkan hasil berupa
penurunan kadar oligomer Aβ solubel dan
Medula | Volume 7 | Nomor 4 | November 2017| 175
dengan konsumsi EGCG belum dapat secara pasti ditentukan karena minimnya percobaan klinis yang dilakukan.19
Ringkasan
Alzheimer’s disease (AD) adalah penyakit yang bersifat degeneratif dan progresif yang terjadi pada otak dan menyebabkan cacat spesifik pada neuron serta mengakibatkan gangguan memori, berpikir, dan tingkah laku. Pasien AD mengalami gangguan pada hubungan antar sel saraf, metabolisme, dan proses perbaikan yang meluas. Gangguan ini akhirnya menyebabkan banyak sel saraf tidak berfungsi, kehilangan kontak dengan sel saraf lain, dan mati. Berdasarkan usia, AD dibagi menjadi onset dini dan lanjut, sedangkan berdasarkan pola bawaan, AD dibedakan menjadi tipe familial dan sporadik.
Penyebab AD diantaranya adalah faktor genetik, inflamasi, stress oksidatif, dan disfungsi mitokondria. Semua faktor tersebut akan menghasilkan gejala yang sama dari gejala awal berupa kehilangan kemampuan kognitif dan memori hingga gejala akhir yang menyebabkan pasien hanya dapat berbaring dan tidak dapat melakukan hal-hal dasar sehari-hari. Secara pasti diagnosis AD ditegakkan dengan ditemukannya
gambaran mikroskopis berupa plak Aβ dan
neurofibrillary tangles yang didapatkan dari potongan otak hasil autopsi.
Pencegahan dilakukan dengan
memperlambat terbentuknya plak neuritik di otak. Salah satu zat yang memiliki manfaat tersebut adalah EGCG, salah satu jenis cathecins
dalam teh hijau.
Kandungan EGCG dalam teh hijau memiliki manfaat dalam mengaktivasi jalur PKC. Aktivasi jalur PKC ini selanjutnya akan meningkatkan produksi peptida solubel non toksik lewat jalur
non-amiloidogenik dan mengurangi
pembentukan Aβ dengan meningkatkan sekresi
dari α-secretase.
Selain itu, plak neuritik Aβ akan
mengalami degradasi oleh ECE yang juga teraktivasi oleh ekspresi jalur PKC. Sehingga plak yang terbentuk akan berkurang.
Tidak terbentuknya plak amiloid akan mencegah hiperfosforilasi protein tau yang dapat menyebabkan neurofibrillary tangles, sehingga gejala yang timbul seperti demensia dan gangguan kognitif dapat dicegah pada penderita AD.
Simpulan
Kandungan EGCG yang terdapat di dalam teh hijau memiliki efek neuroprotektif melalui peningkatan aktivitas PKC yang akan
menurunkan kadar Aβ dan mendegradasi plak Aβ yang telah terbentuk sehingga pencegahan
manifestasi klinis dan penurunan perburukan penyakit AD dapat tercapai.
Daftar Pustaka
1. Rasoolijazi H, Joghataie MT, Roghani M, Nobakht M. The beneficial effect of
(-)-epigallocatechin-3-gallate in an
experimental model of alzheimer’s disease
in rat: a behavioral analysis. IBJ. 2007; 11(4):237-43.
2. Singh NA, Mandal AKA, Khan ZA. Potential
neuroprotective properties of
epigallocatechin-3-gallate (egcg). Nutrition Journal. 2016; 15(60):1-17.
4. Pattni KAM. Beta-amyloid sebagai
patogenesis pada penyakit alzheimer. Denpasar: Bagian Psikiatri Rumah Sakit Umum Pusat Sanglah Fakultas Kedokteran Universitas Udayana; 2013.
5. Richardsz SS, Sweet RA. Dementia. Dalam: Sadock BJ, Sadock VA, Ruiz P, editors. Comprehensive text book of psychiatry. Volume 1. Edisi ke-9. Philadelphia: Lippincott Williams and Wilkins; 2009. hlm. 1176-85.
6. Salloway S, Correia S. Alzheimer disease: time to improve its diagnosis and treatment. Cleveland Clinic Journal of Medicine. 2009; 1:49-58.
7. Kemenkes RI. Lansia yang sehat, lansia yang jauh dari demensia [diperbarui tanggal 10 inflammation and arthritis. Life Sci. Elsevier Inc. 2010; 86(25-26):907–18.
Medula | Volume 7 | Nomor 4 | November 2017| 176
consumption of green tea catechin delays memory regression in aged mice. Biogerontology. 2007; 8(2):89–95.
10. Schaffer S, Asseburg H, Kuntz S, Muller WE, Eckert GP. Effects of polyphenols on brain ageing and alzheimer’s disease: focus on mitochondria. Mol Neurobiol. 2012; 46(1):161–78.
11. Hasegawa M. Molecular Mechanisms in the
pathogenesis of alzheimer’s disease and
tauopathies-prion-like seeded aggregation and phosphorylation. Biomolecules. 2012; 24(6):1-12.
12. Seeley WW, Miller BL. Alzheimer’s disease and other dementias. Dalam: Kasper DL, Hauser SL, Jameson JL, Fauci AS, Longo DL,
Loscalzo J, editors. Harrison’s principles of
internal medicine. Volume 2. Edisi ke-19. USA: Mc-Graw Hill. hlm. 2598-02.
13. Hartwig MS. Gangguan neurologis dalam simtomatologi generalisata. Dalam: Hartanto H, editor. Patofisiologi: konsep klinis dan proses-proses penyakit. Volume 2. Edisi ke-6. Jakarta: EGC; 2006. hlm. 1134-7.
14. Lim HJ, Shim SB, Jee SW, Lee SH, Lim CJ, Hong JT, et al. Green tea catechin leads to global improvement among alzheimer’s disease-related phenotypes in
nse/happ-c105 tg mice. J Nutr Biochem. 2013; 24(7):1302–13.
15. Mandel SA, Amit T, Weinreb O, Reznichenko L, Youdim H. Simultaneous manipulation of multiple brain targets by green tea catechins: a potential neuroprotective strategy for alzheimer and parkinson diseases. CNS Neuroscience & Therapeutics. 2008; 14:352-65.
16. Sharma VK, Bhattacharya A, Kumar A, Sharma HK. Health benefits of tea consumption. Trop J Pharm Res. 2007; 6(3):785–92.
17. Kalfon L, Youdim MB, Mandel SA. Green tea polyphenol(-)-epigallocatechin-3-gallate promotes the rapid protein kinase C- and proteasome-mediated degradation of bad: implications for neuroprotection. J Neurochem. 2007; 100:992–1002.
18. Smid SD, Maag JL, Musgrave IF. Dietary polyphenol-derived protection against neurotoxic b-amyloid protein: from molecular to clinical. Food Funct. 2012; 3:1242-50.
19. Walker JM, Klakotskaia D, Ajit D, Weisman GA, Wood WG, Sun GY, et al. Beneficial effects of dietary egcg and voluntary
exercise on behavior in an alzheimer’s
disease mouse model. Journal of