73
PENENTUAN KAPASITAS ADSORPSI KITOSAN TERIMOBILISASI DITIZON TERHADAP Cd(II)
Nofa Agustrya1*, Lia Destiarti1, Titin Anita Zaharah1 1
Jurusan Kimia, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi,
*
email: nofaagustrya@gmail.com
ABSTRAK
Telah dilakukan penelitian mengenai penentuan kapasitas adsorpsi kitosan terimobilisasi ditizon terhadap Cd(II). Penelitian ini menggunakan adsorben kitosan terimobilisasi ditizon sebagai pengisi kolom adsorpsi. Kitosan bead diimobilisasi dengan ditizon untuk meningkatkan selektivitas adsorben dalam menyerap Cd(II). Adsorben yang diperoleh dikarakterisasi menggunakan spektrofotometer inframerah (IR). Spektrum IR menunjukkan adanya ikatan pada kitosan terimobilisasi ditizon yang terlihat pada bilangan gelombang 1419,61 cm-1 (N-H) dan bilangan gelombang 1080,14 cm-1 (S=C). Parameter adsorpsi yang diteliti meliputi penentuan pH adsorpsi dengan variasi pH 4, 5, 6, dan 7 dan konsentrasi ion logam yaitu 4,796; 8,824; 12,704 dan 16,707 ppm. Adsorpsi dilakukan dengan mengalirkan 20 mL Cd(II) 3 ppm pada kolom adsorpsi yang telah terisi adsorben kitosan terimobilisasi ditizon, eluat hasil kolom adsorpsi dianalisis menggunakan spektrofotomer serapan atom. Berdasarkan hasil penelitian diperoleh bahwa adsorpsi Cd(II) optimum pada pH 6 dengan penurunan konsentrasi sebesar 98,55% sedangkan kapasitas adsorpsi maksimum kitosan terimobilisasi ditizon menurut isoterm Langmuir untuk Cd(II) sebesar 0,315 mg/g.
Kata kunci:kapasitas adsorpsi, kitosan terimobilisasi ditizon, Cd(II)
PENDAHULUAN
Pencemaran logam berat terhadap lingkungan perairan berhubungan erat dengan penggunaan logam oleh manusia baik dalam bidang industri, pertanian maupun rumah tangga. Logam berat yang sering terdapat dalam pencemaran air salah satunya adalah kadmium (Cd) dalam bentuk senyawa toksik yang sangat berbahaya bagi kesehatan manusia (Tarigan dkk, 2003). Ion logam Cd(II) sering dijumpai pada limbah pertambangan, pertanian, dan limbah industri. Logam Cd(II) termasuk dalam logam non essensial sehingga tidak bermanfaat bagi tubuh dan dapat merusak organ tubuh (Rahardjo, 2001). Beberapa metode untuk menghilangkan logam berat dari perairan maupun air limbah telah banyak dilakukan salah satunya adalah adsorpsi (Safrianti dkk, 2012; Priadi dkk, 2014).
Saat ini telah dikembangkan beberapa jenis adsorben untuk mengadsorpsi logam berat, salah satunya adalah dengan memanfaatkan kitosan komersial dari limbah cangkang udang. Kitosan memiliki selektivitas dan kapasitas
adsorpsi yang tinggi sehingga berpotensi untuk penyerapan logam, mudah mengalami biodegradasi dan tidak beracun (Agusnar, 2003 ; Hastuti, 2011). Penggunaan kitosan sebagai adsorben ion logam telah banyak dilakukan. Ketkangplu (2005) menggunakan kitosan sebagai adsorben logam Cd menghasilkan penyerapan sebesar 62% pada pH 6. Oleh karena itu perlu dilakukan modifikasi adsorben kitosan untuk meningkatkan kapasitas adsorpsi dan selektivitas pemisahan, salah satunya dengan menggunakan ligan organik yaitu ditizon (Rohyami, 2013). Ditizon (1,5-difeniltiokarbazon) merupakan ligan yang sangat spesifik dan sensitif terhadap logam Pb, Cd, Hg dan Cu karena mengandung atom N, -NH, dan kelompok –SH sebagai pendonor elektron untuk membentuk khelat dengan adsorben (Mudasir et al., 2008).
Penelitian kitosan terimobilisasi ditizon telah dilakukan oleh Allen dkk (2014) untuk mendapatkan recovery timbal (Pb) dengan menggunakan EDTA sebagai agen pendesorpsi. Muslimah dkk (2015) menggunakan kitosan terimobilisasi ditizon
74 untuk prekonsentrasi Pb(II) pada air sungai Kapuas. Oleh karena itu penelitian ini menggunakan kitosan terimobilisasi ditizon sebagai pengisi kolom untuk mengadsorpsi Cd(II). Adapun variabel dalam penelitian ini yaitu variasi pH dan konsentrasi ion logam untuk menentukan kapasitas adsorpsi maksimum kitosan terimobilisasi ditizon. Penentuan kadar Cd(II) dianalisis dengan Atomic Absorption Spectrophotometry (AAS).
METODOLOGI PENELITIAN Alat dan Bahan
Alat
Alat yang digunakan pada penelitian ini adalah peralatan gelas standar yang digunakan di laboratorium kimia, neraca analitik dengan ketelitian 0,001 g, kolom gelas, pengaduk magnetik, Atomic
Absorption Spectrophotometry (AAS)
Shimadzu AA-7000, spektrofotometer FT-IR 8201PC Shimadzu.
Bahan
Bahan-bahan yang digunakan pada penelitian ini yaitu akua demineralisasi, asam asetat glasial (CH3COOH), ditizon
(C13H12N4S), kitosan (C6H11NO4)n, kloroform
(CH3Cl), larutan buffer fosfat pH 4, 7, dan
10, larutan NaOH dan HNO3 0,1 M, sampel
berupa larutan stok Cd(NO3)2
Prosedur Penelitian
Pembuatan Larutan Kitosan
Serbuk kitosan ditimbang sebanyak 20 gram dan dilarutkan dalam asam asetat 2,5% sebanyak 500 mL sambil diaduk sampai kitosan larut. Campuran tersebut didiamkan sampai semua larut sempurna (Allen dkk, 2014).
Pembuatan Kitosan Terimobilisasi Ditizon
Larutan kitosan dimasukkan kedalam syringe yang berukuran volume 3 mL dan diteteskan kedalam 1000 mL larutan NaOH sampai larutan kitosan habis. Kitosan yang berbentuk bead diaduk dengan pengaduk magnetik selama 15 menit. Selanjutnya, kitosan bead dicuci sampai mencapai pH netral dan diimobilisasi dengan ditizon sebanyak 100 mL. Kemudian kitosan bead direndam selama 6 hari. Kitosan yang telah terimobilisasi ditizon dicuci sampai pH
netral. Adsorben tersebut selanjutnya dikarakterisasi menggunakan
Spektrofotometer Infra Merah (IR) (Allen dkk, 2014).
Penentuan pH Optimum
Sebanyak 20 mL larutan sampel Cd(II)konsentrasi 3 ppm dengan variasi pH 4, 5, 6 dan 7 dialirkan pada kolom adsorpsi dan digunakan massa adsorben kitosan terimobilisasi ditizon sebanyak 5 gram sebagai fase diam dengan laju alir 1 mL/menit. Larutan yang telah melalui kolom ditampung dengan wadah dan dilakukan analisis konsentrasi logam menggunakan AAS. Prosedur dilakukan sebanyak 3 kali pengulangan (Allen dkk, 2014). Kondisi optimum dapat dilihat dari hasil penyerapan mengunakan rumus (Priadi, 2014):
R =
%
dimana,
R : Hasil penyerapan (%)
Co : Konsentrasi logam awal (mg/L) Ce : Konsentrasi logam pada eluat (mg/L)
Penentuan Kapasitas Adsorpsi Maksimum dan Model Isoterm Adsorpsi
Larutan sampel Cd(II)dengan variasi konsentrasi 5, 10, 15 dan 20 ppm sebanyak 20 mL pada pH optimum dialirkan kedalam kolom adsorpsi dan digunakan massa adsorben kitosan terimobilisasi ditizon sebanyak 5 gram sebagai fase diam dengan laju alir sebesar 1 mL/menit. Larutan yang telah melalui kolom ditampung dengan wadah dan dianalisis konsentrasi logam menggunakan AAS (Nurhasni, 2014). Prosedur dilakukan sebanyak 3 kali pengulangan. Kapasitas adsorpsi dihitung berdasarkan persamaan berikut (Zhao et al., 2013):
( )
dimana q adalah kapasitas adsorpsi (mg/g), m adalah massa adsorben yang digunakan (gram) dan v adalah volume larutan (liter).
Penentuan kapasitas adsorpsi maksimum menggunakan persamaan isoterm Langmuir, yaitu (Ozacar, 2011):
dimana qe adalah konsentrasi adsorbat yang terserap (mg/g), Q adalah kapasitas adsorpsi maksimum (mg/g), b adalah
75 konstanta adsorpsi, dan Ce adalah konsentrasi adsorbat di larutan.
Persamaan isoterm Freundlich yang digunakan pada penelitian ini yaitu (Ozacar, 2011):
dimana Kf dan n merupakan konstanta
adsorpsi dan intensitas adsorpsi. HASIL DAN PEMBAHASAN
Karakterisasi Kitosan Terimobilisasi Ditizon
Kitosan yang berbentuk bead diimobilisasi menggunakan ditizon. Modifikasi ini bertujuan meningkatkan kinerja adsorpsi dan selektivitas kitosan. Ditizon merupakan ligan organik yang dapat bereaksi dengan ion-ion logam tertentu seperti Pb2+, Hg2+, Cu2+ dan Cd2+ (Mudasir et al, 2008).
Tabel 1 merupakan interpretasi spektrum kitosan dan kitosan terimobilisasi ditizon. Dua serapan baru yang muncul pada bilangan gelombang 1419,61 cm-1 dan 1080,14 cm-1 pada kitosan terimobilisasi ditizon masing-masing diidentifikasi sebagai gugus N-H dan gugus S=C. Hal ini menandakan terbentuknya ikatan kitosan ke ditizon. Hasil ini diperkuat oleh penelitian yang telah dilakukan Putra dkk (2015) tentang keberadaan gugus S=C (1200-1050 cm-1) dari zeolit terimobilisasi ditizon.
Tabel 1. Interpretasi Spektrum IR Kitosan dan Kitosan Terimobilisasi Ditizon Bilangan Gelombang (cm-1) Gugus Fungsional Kitosan* Kitosan Terimobilisasi Ditizon** 3417,86 3471,87 O-H 2931,80 2931,80 -CH2 1635,64 1635,64 -C=O - 1419,61 N-H 1381,03 1381,03 -CH3 1327,03 1317,03 -CH2bending 1257,59 1265,30 -CH3 bending 1149,57 1149,57 C-O streching - 1080,14 S=C 1033,85 1033,85 C-N
Keterangan : *hasil isolasi Allen dkk (2014) ; **hasil isolasi peneliti
Penentuan pH Optimum
Penentuan pH optimum dilakukan pada variasi pH 4, 5, 6 dan 7 yang sesuai dengan bentuk spesies Cd2+ pada pH
tertentu. Hubungan antara variasi pH terhadap persentase logam yang teradsorpsi dapat dilihat pada Gambar 2. Pada rentang 4-7, spesies Cd yang dominan terbentuk adalah Cd2+ yang dapat terikat baik pada permukaan kitosan terimobilisasi ditizon. Kesetimbangan adsorpsi antara konsentrasi adsorbat yang diserap dengan konsentrasi adsorbat yang tersisa didalam larutan terjadi pada pH 5, 6, dan 7. O OH H H NH2 H H CH2OH H O .. .. +H C H H C O O OH O OH H H NH2 H H CH2 H O+ H H O +H C H H C O O --H2O O OH H H NH2 H H H2C + H O +H C H H C O O -O OH H H NH2 H H CH2 H C O C H H H O Kitosan Asam Asetat
Larutan Kitosan dalam Asam Asetat Tahap 1 : O OH H H NH2 H H CH2 H O C O C H H H O + C N N N S Ph H N Ph H .. -C2H3O -C N N N S Ph H N+ H Ph C H H O O H OH NH2 OH .. .. -H+ C N N N S Ph H N Ph C H H O O H OH NH2 OH Kitosan Ditizon
Kitosan Terimobilisasi Ditizon Tahap 2 :
Gambar 1. Reaksi imobilisasi kitosan terhadap ditizon (Allen dkk, 2014)
Gambar 2. Pengaruh pH larutan terhadap penurunan konsentrasi ion logam Cd2+ 96,37 98,55 98,55 98,55 0 25 50 75 100 3 4 5 6 7 % P e nurunan K onse nt ra s i Ion Logam C d 2+ pH Larutan
76 Presentase Cd yang teradsorpsi menunjukkan kestabilan presentase adsorbat. Hal ini disebabkan karena gugus aktif pada permukaan adsorben telah terpenuhi dengan adsorbat sehingga peluang untuk terjadinya ikatan antara Cd dengan situs aktif adsorben semakin kecil (Darjito, 2006). Menurut Nuryono dan Suyanta (2004), berdasarkan korelasi antara distribusi spesies Cd(II) dengan pH larutan menunjukkan bahwa semua Cd(II) berada sebagai ion Cd2+ pada pH 7.
Hasil uji statistik menunjukkan bahwa terdapat perbedaan yang signifikan pada pH 4 dengan pH 5, 6 dan 7. Dengan demikian pemilihan pH 6 berdasarkan pH air sungai Kapuas yang berada di kisaran pH 6-7, sehingga jika diaplikasikan pada sampel air sungai tidak diperlukan pengkondisian pH. Hasil ini sesuai dengan penelitian sebelumnya bahwa adsorpsi ion logam Cd oleh kitin terimobilisasi ditizon secara optimum terjadi pada pH 6 (Mudasir et al., 2008 ; Rohyami, 2013). C N N N S Ph H N Ph C H H O O H OH NH2 OH C N N N S Ph H N Ph C H H O O H OH N H2 O H Cd2+
Gambar 3. Interaksi Cd(II) dengan adsorben kitosan terimobilisasi ditizon (Rohyami, 2013)
Interaksi ion logam dengan adsorben ditunjukkan pada Gambar 3. Adanya atom N akan membentuk ikatan kovalen dengan ion logam Cd. Ion logam Cd dengan pasangan elektron pada atom S digunakan untuk membentuk ikatan kovalen koordinasi sehingga terbentuk khelat antara ditizon dengan ion logam (Rohyami, 2013). Kapasitas Adsorpsi Kitosan Terimobilisasi Ditizon Terhadap Cd(II)
Peningkatan jumlah konsentrasi Cd(II) teradsorpsi dari konsentrasi 4,796 ppm hingga 16,707 ppm terlihat pada Gambar 4. Semakin tinggi konsentrasi ion logam maka semakin besar adsorpsi ion logam. Hal ini disebabkan karena gugus aktif pada permukaan adsorben masih
belum terisi sepenuhnya oleh molekul-molekul adsorbat sehingga penambahan konsentrasi ion logam meningkatkan kapasitas adsorpsi. Gultom dan Lubis (2014) menyatakan bahwa selama situs aktif belum jenuh oleh adsorbat, maka kenaikan konsentrasi adsorbat akan diikuti pula dengan kenaikan jumlah adsorbat yang teradsorpsi
Gambar 4. Hubungan konsentrasi logam terhadap kapasitas adsorpsi oleh kitosan terimobilisasi ditizon
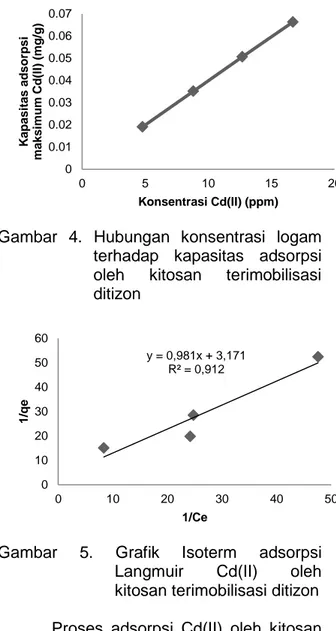
Gambar 5. Grafik Isoterm adsorpsi Langmuir Cd(II) oleh kitosan terimobilisasi ditizon Proses adsorpsi Cd(II) oleh kitosan terimobilisasi ditizon dapat dijelaskan dengan menggunakan dua persamaan isoterm yaitu persamaan isoterm Langmuir dan persamaan isoterm Freundlich. Gambar 5 merupakan grafik isoterm Langmuir dan gambar 6 merupakan grafik isoterm Freundlich. Kapasitas adsorpsi maksimum kitosan terimobilisasi ditizon menurut isoterm Langmuir adalah sebesar 0,315 mg/g dan menurut isoterm Freundlich adalah sebesar 0,314 mg/g. 0 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0 5 10 15 20 K a pas it a s a dsorps i m a k s im um C d( II ) (m g/ g) Konsentrasi Cd(II) (ppm) y = 0,981x + 3,171 R² = 0,912 0 10 20 30 40 50 60 0 10 20 30 40 50 1 /qe 1/Ce
77 Gambar 6. Grafik Isoterm adsorpsi
Freundlich Cd(II) oleh kitosan terimobilisasi ditizon Berdasarkan nilai R2 yang diperoleh pada hasil analisis, adsorpsi Cd(II) oleh kitosan terimobilisasi ditizon secara matematis sesuai dengan model isoterm Langmuir dan Freundlich. Namun nilai R2 pada isoterm Langmuir sebesar 0,912 lebih tinggi daripada isoterm Freundilch yaitu 0,818. Hal ini menunjukan bahwa proses adsorpsi Cd(II) ke permukaan kitosan terimobilisasi ditizon lebih dominan terjadi secara kimia karena adanya ikatan kimia antara adsorbat dengan permukaan adsorben.
SIMPULAN
Adsorpsi Cd(II) optimum pada pH 6. Secara matematis kedua isoterm Langmuir dan Freundlich dapat menggambarkan proses adsorpsi Cd(II) oleh kitosan terimobilisasi ditizon namun yang paling dominan adalah model isoterm Langmuir dengan kapasitas adsorpsi maksimum sebesar 0,315 mg/g.
DAFTAR PUSTAKA
Agusnar, H, 2003, Analisa Keefektifan Penggunaan Kitosan untuk Menurunkan Kadar Logam Berat, J. Sains Kimia, Vol. 7(1) : 7-10
Allen, C.V, Destiarti, L, Zaharah, T.A, 2014, Recovery Timbal dengan Ekstraksi Fase Padat Menggunakan Kitosan Terimobilisasi Ditizon, J. Kimia Khatulistiwa, Vol. 3(1) : 57-63
Darjito, Purwonugroho, D, Nisa, S, N, 2006, Kajian Adsorpsi Cd(II) Pada Kitosan-Alumina, Indonesia Jurnal Chemistry, Vol. 6(3) : 238-244
Gultom, E, M dan Lubis, M, T, 2014, Aplikasi Karbon Aktif dari Cangkang
Kelapa Sawit dengan aktivator H3PO4
untuk Penyerapan Logam Berat Cd Dan Pb, J. Teknik Kimia, Vol. 3(1) : 5-10 Hastuti, B, Masykur, A, dan Ifada, F, 2011,
Modifikasi Kitosan Melalui Proses
Swelling dan Crosslinking
Menggunakan Glutaraldehit sebagai Pengadsorpsi Logam Cr (VI) pada Limbah Industri Batik, J. EKOSAINS, Vol. 3(3) : 14-21
Ketkangplu, P, Chanyut, Unob, F, 2005, Preconcentration of Heavy Metals from Aqueous Solution Using Chitosan Flake, J.Sains Res Chula University, Vol 30 (1): 87-95
Muslimah, Destiarti, L, Zaharah, T, A, 2015, Prekonsentrasi Timbal(II) pada Air Sungai Kapuas Menggunakan Kitosan Terimobilisasi Ditizon, Jurnal Kimia Khatulistiwa, Vol. 4(3): 22-27
Mudasir, Ginanjar, R, Iqmal, T dan Endang, T.W, 2008, Immobilization of Dithizone onto Chitin Isolated from Prawn Seawater Shells (P. merguensis) and Its Preliminary Study for the Adsorption of Cd(II) Ion, Journal Physical Science, Vol. 19(1): 63-78
Nurhasni, Hendrawati, Saniyyah, N, 2014, Sekam Padi untuk Menyerap Ion Logam Tembaga dan Timbal dalam Air Limbah, Valensi, Vol. 4(1): 36-44
Nuryono dan Suyanta, 2004, Kajian Interaksi Cd(II) dengan Adsorben Tanah Diatomit pada Proses Adsorpsi, Indonesian Journal of Chemistry, Vol. 4(2) : 125-131
Ozacar, M., 2003, Phosphate Adsorption Characteristics of Alunite To Be Used as A Cement Additive, Cement and Concerete Research., 33: 1583-1587 Priadi, C.R, Anita, Sari, P.N, Moersidik, S.S,
2014, Adsorpsi Logam Seng dan Timbal pada Limbah Cair Industri Keramik oleh Limbah Tanah Liat, Vol. 15(1), 10-19 Putra, R, Khamidinal, Kridiyanto, D, 2015,
Adsorpsi Ion Mn(II) pada Zeolit yang Disintesis dari Abu Dasar Batubara Terimodifikasi Ditizon, Prosiding Seminar, hal 1-11
Rahardjo, M, Rosita, S.M.D, Darwati, I, 2001, Status Logam Berat Kadmium (Cd) dan Hasil Rimpang Temu Ireng (Curcuma aeruginosa Roxb.) pada Pemupukan Fosfat, Warta Tumbuhan Obat Indonesia, Vol. 7(1) : 16-20.
y = 0,676x - 0,502 R² = 0,818 -2 -1.8 -1.6 -1.4 -1.2 -1 -0.8 -0.6 -0.4 -0.2 0 -2 -1.5 -1 -0.5 0 Log qe Log Ce
78
Rohyami, Y, 2013, Penentuan Cu, Cd dan Pb dengan AAS Menggunakan Solid Phase Extraction, J. Inovasi dan
Kewirausahaan, Vol. 2(1): 19-25
Safrianti, I, Wahyuni, N, Zaharah, T, A, 2012, Adsorpsi Timbal (II) oleh Selulosa Limbah Jerami Padi Teraktivasi Asam Nitrat: Pengaruh pH dan Waktu Kontak, J. Kimia Khatulistiwa, Vol. 1(1) : 1-7 Tarigan, Z, Edward dan Rozak, A, 2003,
Kandungan Logam Berat Pb, Cd, Cu, Zn dan Ni dalam Air Laut dan Sedimen di Muara Sungai Membramo, Papua dalam Kaitannya dengan Kepentingan
Budidaya Perikanan, Makara Sains, Vol. 7(3) : 119-127
Zhao, F, Repo, E, Yin, D, Silapaa, M, 2013, Adsorption of Cd(II) and Pb(II) by a novel EGTA-modified chitosan material: Kinetics and isotherms, Journal of Colloid and Interface Science, 409 : 174-182.