PENGARUH VARIASI
UKURAN PARTIKEL GRANUL TERHADAP EVALUASI SEDIAAN KAPSUL
LIDAH BUAYA
Diajukan sebagai
Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
FILDZA DIAH ASFARINA
PROGRAM STUDI SARJANA FARMASI UNIVERSITAS SUMATERA UTARA
PENGARUH VARIASI JENIS BAHAN PENGISI DAN UKURAN PARTIKEL GRANUL TERHADAP HASIL
SEDIAAN KAPSUL SERBUK SIMPLISIA LIDAH BUAYA (Aloe vera (L.) Burm.f.)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperolehgelar Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
OLEH:
FILDZA DIAH ASFARINA NIM 141501045
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2019
BAHAN PENGISI DAN HASIL SIMPLISIA DAUN
salah satu syarat untuk memperolehgelar Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
Universitas Sumatera Utara
PENGARUH VARIASI
UKURAN PARTIKEL GRANUL TERHADAP EVALUASI SEDIAAN KAPSUL
LIDAH BUAYA
Diajukan sebagai salah satu syarat untuk
Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
PROGRAM STUDI SARJANA FARMASI UNIVERSITAS SUMATERA UTARA
PENGARUH VARIASI JENIS BAHAN PENGISI DAN UKURAN PARTIKEL GRANUL TERHADAP
SEDIAAN KAPSUL SERBUK SIMPLISIA LIDAH BUAYA (Aloe vera (L.) Burm.f.)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperolehgelar Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
OLEH:
FILDZA DIAH ASFARINA NIM 141501045
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2019
BAHAN PENGISI DAN UKURAN PARTIKEL GRANUL TERHADAP HASIL
SIMPLISIA DAUN Burm.f.)
memperolehgelar Sarjana Farmasi pada Fakultas FarmasiUniversitas Sumatera Utara
PROGRAM STUDI SARJANA FARMASI
Universitas Sumatera Utara
Universitas Sumatera Utara
iv
KATA PENGANTAR
Bismillaahirrohmaanirrohiim,
Puji syukur kehadirat Allah SWT yang telahmelimpahankan rahmat, hidayah dan karunia-Nya kepada penulis sehingga dapat menyelesaikan penyusunan skripsi yang berjudul "Pengaruh Variasi Jenis Bahan Pengisi Dan Ukuran Partikel Granul Terhadap Hasil Evaluasi Sediaan Kapsul Serbuk Simplisia Daun Lidah Buaya (Aloe vera(L.) Burm.f.)". Skripsi ini diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut. Tanaman lidah buaya memiliki manfaat untuk mengobati panas dalam, mengurangi gula dalam darah dan obat pencahar. Tujuan penelitian ini adalah untuk mengetahui apakah dapat dibuat sediaan kapsul dari serbuk simplisia daun lidah buaya. Ternyata bahwa serbuk simplisia daun lidah buayadapat dibuat menjadi sediaan kapsul dengan menggunakan berbagai jenis granul sebagai bahan pengisi, yaitu granul amilum manihot dan granul laktosa dengan berbagai perbandingan. Penulis berharap penelitian ini dapat bermanfaat dan bisa dijadikan referensi untuk peneliti selanjutnya terutama yang berkaitan dengan serbuk simplisia.
Penulis menyampaikan terimakasih yang sebesar-besarnya kepada Ibu Prof. Dr. Masfria, M.S., Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara, BapakDrs. Agusmal Dalimunthe, M.S., Apt., selaku dosen pembimbing yang telah memberikan waktu, bantuan, tenaga, bimbingan dan nasihat selama penelitian hingga selesainya penyusunan skripsi ini, dan juga
Universitas Sumatera Utara
v
kepadaIbu Prof. Dr. Anayanti Arianto, M.Si., Apt., dan Ibu Dra. Nazliniwaty, M.Si., Apt., selaku dosen penguji yang telah memberikan saran, arahan, kritik dan masukan kepada penulis untuk penyempurnaanskripsi ini. Ucapan terima kasih juga disampaikan kepada Bapak Prof. Dr. Urip Harahap., Apt., selaku penasehat akademik yang telah memberikan arahan dan bimbingankepada penulis selama ini, serta Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik penulis selama masa perkuliahan.
Penulis juga mengucapkan terima kasih yang tak terhingga dan penghargaan yang tulus kepada kedua orang tua, Ayahanda Erwin dan Ibunda Purwanti dan juga kepada Adik tercintaIbnu Hibban Ghozi dan M.Athif Al-Ghani yang tak pernah berhenti mendoakan demi kelancaran dan kesuksesan dalam penelitian hingga selesainya penyusunan skripsi ini. Penulis juga mengucapkan terima kasih kepada sahabat-sahabat yaitu Widad, Dilva,Mafda, Dwi, Nurul, Ayu, Yuni, Rossy,Mukhlis, Aspan dan teman-teman mahasiswa/i Farmasi stambuk 2014 yang selalu memberikan doa, dorongan dan semangat dalam penyelesaian skripsi ini.
Penulis menyadari bahwa penulisan skripsi ini masih memiliki banyak kekurangan, oleh karena itu dengan segala kerendahan hati penulis bersedia menerima kritik dan saran yang membangun pada skripsi ini.Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, 27 Februari 2019 Penulis,
Fildza Diah Asfarina NIM 141501045
Universitas Sumatera Utara
vi
SURAT PERNYATAAN ORISINALITAS
Saya yang bertanda tangan di bawah ini:
Nama : Fildza Diah Asfarina
Nomor Induk Mahasiswa : 141501045 Program Studi : Sarjana Farmasi
Judul Skripsi : Pengaruh Variasi Jenis Bahan Pengisi Dan Ukuran Partikel Granul Terhadap Hasil Evaluasi Sediaan Kapsul Serbuk Simplisia Daun Lidah Buaya (Aloe vera (L.) Burm.f.)
Dengan ini menyatakan bahwa skripsi yang saya buat adalah asli karya sendiri dan bukan plagiat. Apabila dikemudian hari diketahui skripsi saya tersebut terbukti plagiat karena kesalahan sendiri, maka saya bersedia diberi sanksi apapun oleh Program Studi Sarjana Farmasi Fakultas Farmasi Universitas Sumatera Utara. Saya tidak akan menuntut pihak manapun atas perbuatan saya tersebut.
Demikian surat pernyataan ini saya perbuat dengan sebenarnya dan dalam keadaan sehat.
Medan, 27 Februari 2019
Fildza Diah Asfarina NIM 141501045
Universitas Sumatera Utara
vii
PENGARUH VARIASI JENIS BAHAN PENGISI DAN UKURAN PARTIKEL GRANUL TERHADAP HASIL EVALUASI SEDIAAN KAPSUL SERBUK SIMPLISIA DAUN LIDAH BUAYA (Aloe vera (L.)
Burm.f.)
ABSTRAK
Latar Belakang: Penggunaan obat tradisional dinilai memiliki efek samping yang lebih kecil dibandingkan dengan obat yang berasal dari bahan kimia, di samping itu harganya lebih terjangkau. Peneliti ingin memformulasi sediaan kapsul yang mengandung serbuk simplisia daun lidah buaya dengan variasi jenis bahan pengisi dan ukuran partikel granul. Selain itu untuk meningkatkan daya alir bahan pengisi, dilakukan ko-proses bahan pengisi amilum-laktosa.
Tujuan: Untuk mengetahui serbuk simplisia daun lidah buaya (Aloe vera L.) dapat dibuat menjadisediaan kapsul, dan evaluasipengaruh ukuran partikel granul terhadap sifat fisik dan persyaratan kapsul dari serbuk simplisia daun lidah buaya (Aloe vera L.).
Metode: Serbuk simplisia daun lidah buaya diperoleh dengan menggunakan ayakan mesh 80, dan dibuat dalam bentuk granul dengan bahan pengikat PVP dan dicampur dengan variasi jenis bahan pengisi ko proses amilum-laktosa dan ukuran partikel granul sebanyak 4 formula yaitu dengan jumlah perbandingan bahan pengisi F1(laktosa 100%, mesh 20), F2 (amilum 100%, mesh 40), F3 (laktosa-amilum 50%:50%, mesh 20), F4 (amilum-laktosa 50%:50%, mesh 40), kemudian dimasukkan kedalam cangkang kapsul sesuai dengan perhitungan bobot massa kapsul untuk setiap formula.Kemudian dilakukan uji evaluasi kapsul.
Hasil: Keempatformula memenuhi persyaratan kapsul yang meliputi keseragaman bobot dan waktu hancur, namun F1 yang mengandung laktosa 100%
lebih mendekati bobot standar massa kapsul dibandingkan ketiga formula lainnya untuk kapasitas cangkang kapsul ukuran 00.
Kesimpulan: Serbuk simplisia lidah buaya (Aloe vera L.) dapat dibuat menjadi sediaan kapsul.Perbedaan jenis bahan pengisi amilum-laktosa dan ukuran partikel granul memberikan pengaruh terhadap hasil uji evaluasi. F1 (laktosa 100%, mesh 20) lebih mendekati bobot standar massa kapsul dibandingkan ketiga formula lainnya untuk kapasitas cangkang kapsul ukuran 00.
Kata Kunci: kapsul, simplisia daun lidah buaya, serbuk simplisia daun lidah buaya, daun lidah buaya, bahan pengisi, ukuran partikel granul.
Universitas Sumatera Utara
viii
THE EFFECT OF VARIATION OF FILLER TYPES AND PARTICLE SIZE OF GRANULES ON THE EVALUATION RESULTS SIMPLICIA POWDER CAPSULE OF ALOE VERA LEAF (Aloe Vera(L.) Burm.f.)
ABSTRACT
Background: The use of traditional medicines is considered to have smaller side effect compared to drugs derived from chemicals, in addition the price is also more affordable. The reseachers wanted toformulatecapsule supply which containing simplicia powder of aloe vera leaf with variation types of filler and particle size of granuls. In addition, to increasing the flow rate of the filler material, a co-process of the amylum-lactose filler is carried out.
Purpose: To find out the simplicia powder of aloe vera leaf can be made into a capsulepreparation, and evaluation of the effect of granule particle size on the physical characteristic and requirements of capsule of simplicia powed of aloe vera leaf (Aloe vera L.).
Methods: Simplicia powder of aloe vera leafs were obtained by using 80 mesh sieves, and made in granule form with PVP binder and mixed with variation type of filler amylum laktose co-process and granule particle size of 4 formulas that was by the number offiller comparisons of F1 (lactose 100%, mesh 20), F2 (lactose-amylum 50%:50%, mesh 40), F3 (amylum 100%, mesh 20), F4 (amylum- lactose 50%:50%, mesh 40), then put into the capsule shell according to the calculation of capsule mass weight for each formula. Then the capsule evaluation test was carried out.
Results: The four formulas fulfilled the capsule requirements which included uniformity of weight and time of disintegration, but F1 is closer to the standard weight of the capsule than the other three formulas for the capacity of a capsule shell of size 00.
Conclusion: Simplicia powder of aloe vera leaf can be made into a capsule preparation. The difference types of filler and granule particle size have an effect on the results of the evaluation test. F1 (lactose 100%, mesh 20) is closer to the standard weight of the capsule than the other five formulas for the capacity of a capsule shell of size 00.
Keywords: capsule, simplicia of aloe vera, simplicia powder of aloe vera leaf, aloe vera leaf, filler material, granule particle size.
Universitas Sumatera Utara
ix DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN ORISINALITAS ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis Penelitian ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tanaman Lidah Buaya ... 6
2.1.1 Klasifikasi Tanaman Lidah Buaya ... 6
2.1.2 Sinonim Tanaman Lidah Buaya ... 6
2.1.3 Nama Asing Tanaman Lidah Buaya ... 6
2.1.4Nama Daerah Tanaman Lidah Buaya ... 6
2.1.5Morfologi Tanaman Lidah Buaya ... 6
2.1.6Kandungan Tanaman Lidah Buaya ... 7
2.1.7Manfaat Tanaman Lidah Buaya ... 7
2.2Simplisia ... 8
2.2.1Pengertian Simplisia ... 8
2.2.2Penggolongan Simplisia ... 8
2.3Granul ... 9
2.4Uraian Sediaan Kapsul ... 9
2.4.1Pengertian Kapsul ... 9
2.4.2Jenis dan Ukuran Sediaan Kapsul ... 10
2.4.3Metode Pengisian Kapsul ... 12
2.4.4Penyimpanan Kapsul ... 13
2.5 Ko-Proses Bahn Pengisi ... 13
2.6 Uraian Bahan ... 14
2.6.1 Amilum Manihot ... 14
2.6.2 Laktosa ... 14
2.6.3 Mg Stearat ... 14
Universitas Sumatera Utara
x
2.6.4 Talkum ... 15
2.6.5 Amilum Jagung ... 15
2.6.6 Polivinil Pirolidon ... 15
BAB III METODE PENELITIAN ... 16
3.1 Alat dan Bahan ... 16
3.1.1 Alat ... 16
3.1.2 Bahan ... 16
3.2 Pembuatan Larutan Pereaksi ... 17
3.2.1 Pereaksi Mayer ... 17
3.2.2 Pereaksi Natrium Hidroksida ... 17
3.2.3 Pereaksi Bouchardat ... 17
3.2.4 Pereaksi Dragendroff ... 17
3.2.5 Larutan Besi (III) Klorida 1%... 17
3.2.6 Larutan Asam Klorida 2 N ... 17
3.2.7 Larutan Timbal (II) Asetat ... 17
3.2.8 Pereaksi Liebermann Burchard ... 18
3.2.9 Pereaksi Molish ... 18
3.2.10 Pereaksi Kloralhidrat ... 18
3.3 Penyiapan Sampel ... 18
3.3.1 Pengambilan Bahan Tanaman ... 18
3.3.2 Identifikasi Sampel ... 18
3.3.3 Pembuatan Simplisia ... 18
3.3.4 Pembuatan Serbuk Simplisia ... 19
3.4 Pemeriksaan Karakteristik Simplisia ... 19
3.4.1 Pemeriksaan Makroskopik dan Organoleptik... 19
3.4.2 Pemeriksaan Mikroskopik ... 19
3.4.3 Penetapan Kadar Air ... 19
3.4.4 Penetapan Kadar Sari Larut Air ... 20
3.4.5 Penetapan Kadar Sari Larut Etanol ... 20
3.4.6 Penetapan Kadar Abu Total ... 21
3.4.7 Penetapan Kadar Abu Tidak Larut Asam... 21
3.5 Skrining ... 21
3.5.1 Pemeriksaan Alkaloid ... 22
3.5.2 Pemeriksaan Flavonoida... 22
3.5.3 Pemeriksaan Saponin ... 23
3.5.4 Pemeriksaan Tanin ... 23
3.5.5 Pemeriksaan Glikosida ... 23
3.5.6 Pemeriksaan Steroid/Triterpenoid ... 24
3.6 Pembuatan Sediaan Kapsul ... 24
3.6.1 Penyalutan Serbuk Simplisia Daun Lidah Buaya ... 24
3.6.2 Pembuatan Ko-Proses Laktosa-Amilum ... 24
3.6.3 Distribusi Ukuran Partiel ... 25
3.7 Perencanaan ... 26
Universitas Sumatera Utara
xi
3.7.1 Perencanaan Formula ... 26
3.7.2 Penetapan Dosis Kapsul ... 26
3.7.3 Mencari Bobot Jenis Kapsul ... 27
3.8 Formula Kapsul Serbuk Simplisia Daun Lidah Buaya ... 27
3.8.1 Dasar Penetapan Formula ... 27
3.9 Formula Bahan Pengisi ... 28
3.9.1 Pembuatan Bahan Pengikat ... 29
3.9.2 Pembuatan Granul Pengisi ... 29
3.10 Uji Preformulasi Granul ... 30
3.10.1 Indeks Tap ... 30
3.10.2 Waktu Alir ... 30
3.10.3 Sudut Diam ... 30
3.11 Pembuatan Sediaan Kapsul ... 31
3.12 Pengisian Massa Granul ke Cangkang Kapsul ... 31
3.13 Evaluasi Kapsul ... 32
3.13.1 Uji Keseragaman Bobot ... 32
3.13.2 Uji Waktu Hancur ... 32
BAB IV HASIL DAN PEMBAHASAN ... 34
4.1 Hasil Identifikasi Sampel ... 34
4.1.1 Hasil identifikasi Daun Lidah Buaya ... 34
4.2 Hasil Karakteristik simplisia ... 34
4.2.1 Hasil Pemeriksaan Maksroskopik Daun Lidah Buaya ... 34
4.2.2 Hasil Pemeriksaan Mikroskopik Simplisia Daun Lidah Buaya ... 34
4.2.3 Hasil Karakterisasi Simplisia Daun Lidah Buaya ... 34
4.3 Hasil Pembuatan Serbuk Simplisia Daun Lidah Buaya ... 35
4.4 Hasil Skrining Fitokimia ... 35
4.5 Uji Preformulasi Granul ... 36
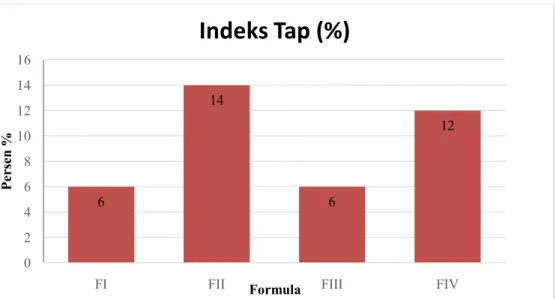
4.5.1 Sudut Diam ... 36
4.5.2 Waktu alir ... 38
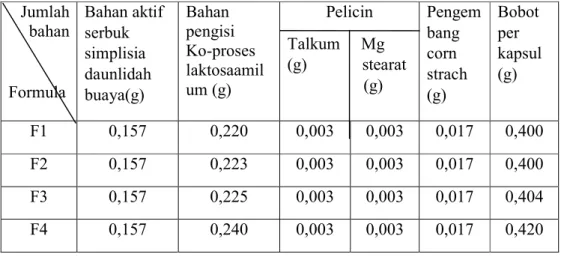
4.5.3 Indeks Tap ... 38
4.6 Hasil Massa Bobot Kapsul ... 39
4.7 Hasil Evaluasi Kapsul ... 40
4.7.1 Uji Keseragaman Bobot ... 40
4.7.2 Uji Waktu Hancur ... 42
BAB V KESIMPULAN DAN SARAN ... 44
5.1 Kesimpulan ... 44
5.2 Saran ... 44
DAFTAR PUSTAKA ... 45
LAMPIRAN ... 47
Universitas Sumatera Utara
xii
DAFTAR TABEL
3.1 Orientasi Bobot Kapsul ... 28
3.2Formula Bahan Pengisi Kapsul ... 29
3.3Persyaratan Keseragaman Bobot ... 32
4.1Hasil Uji Karakterisasi Simplisia Daun Lidah Buaya... 35
4.2 Hasil Skrining Fitokimia Simplisia Daun Lidah Buaya ... 36
4.3 Hasil Uji Sudut Diam Granul ... 37
4.4 Hasil Uji Waktu Alir Granul ... 38
4.5 Hasil Uji Indeks Tap Granul... 39
4.6 Hasil Bobot Massa Kapsul ... 40
4.7 Hasil Uji Keseragaman Bobot Kapsul ... 40
4.8 Hasil Uji Waktu Hancur ... 42
Universitas Sumatera Utara
xiii
DAFTAR GAMBAR
4.1 Histogram Uji Sudut Diam Granul ... 37
4.2 Histogram Uji Waktu Alir Granul ... 38
4.3 Histogram Uji Indeks Tap Granul ... 39
4.4 Histogram Evaluasi Keseragaman Bobot ... 41
4.5 Histogram Evaluasi Waktu Hancur ... 42
Universitas Sumatera Utara
xiv
DAFTAR LAMPIRAN
1. Hasil Identifikasi Tumbuhan Lidah Buaya ... 47
2. Gambar Tumbuhan, Simplisia dan Serbuk Simplisia Daun Lidah Buaya ... 48
3. Hasil Mikroskopik Serbuk Simplisia Lidah Buaya ... 49
4. Skema Pembuatan Simplisia Daun Lidah Buaya ... 50
5. Skema Pembuatan Serbuk Simplisia Daun Lidah Buaya Mesh 80 ... 51
6. Skema Pembuatan Sediaan Kapsul ... 52
7. Perhitungan Hasil Karakterisasi Simplisia Daun Lidah Buaya ... 53
8. Perhitungan Dosis Kapsul ... 56
9. Perhitungan Massa Kapsul ... 57
10. Perencaan Formula Kapsul ... 59
11. Contoh Perhitungan Pembuatan Sediaan Kapsul ... 60
12. Gambar Granul Kapsul ... 64
13. Gambar Sediaan Kapsul ... 66
14. Hasil Evaluasi Kapsul ... 67
15. Gambar Alat-alat yang Digunakan ... 73
Universitas Sumatera Utara
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Pemanfaatan bahan alam sebagai obat tradisional di Indonesia akhir-akhir ini meningkat, bahkan beberapa bahan alam telah diproduksi secara fabrikasi dalam skala besar. Penggunaan obat tradisional dinilai memiliki efek samping yang lebih kecil dibandingkan dengan obat yang berasal dari bahan kimia, di samping itu harganya lebih terjangkau (Tampubolon, 1981).
Lidah buaya (Aloe vera L.) juga merupakan tanaman yang telah lama digunakan untuk pengobatan. Secara tradisional lidah buaya telah digunakan sebagai obat secara tersendiri atau dicampur dengan bahan lain. Berdasarkan penelitian sebelumnya, ekstrak daun lidah buaya mampu menghambat pertumbuhan bakteri Staphylococcus aureus secara invitro (Rahmawati, 2007).
Daun lidah buaya mengandung Anthroquinone yang merupakan senyawa fenolik dan ditemukan dalam getah. Senyawa ini berperan sebagai pencahar, agen antimikroba dan memiliki efek analgesik yang kuat. Lidah buaya juga memiliki anti infla-masi dan anti bakteri dan membantu penyembuhan luka jaringan nekrotik (Thirupphati dkk., 2010).
Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut (Ditjen POM, 1995).Keuntungan sediaan kapsul diantaranya : Dapat menutupi rasa dan bau yang tidak enak dari bahan obat, lebih mudah ditelan, cukup stabil dalam penyimpanan, dapat diisi dengan bahan obat tunggal atau campuran dan bahan obat berupa granul, proses pembuatan lebih cepat dan praktis karena tidak memerlukan banyak bahan tambahan/pembantu seperti tablet.
Universitas Sumatera Utara
2
Berdasarkan survei pendahuluan yang dilakukan di Apotek Kota Medan diketahui bahwa obat tradisional yang mengandung serbuk simplisia daun lidah buaya dalam bentuk sediaan kapsul belum ada beredar dipasaran. Oleh sebab itu, peneliti tertarik untuk membuat kapsul yang mengandung serbuk simplisia daun lidah buaya.
Tanaman lidah buaya sudah dikenal oleh masyarakat sebagi tanaman obat dan tanaman hias yang biasa ditanam di pekarangan rumah. Manfaat tanaman lidah buaya adalah untuk mengobati panas dalam, luka bakar, menghentikan pendarahan, untuk obat cacing, obat bisul, amandel, sakit mata, kosmetik, jerawat, mengurangi gula dalam darah, obat pencahar, serta regenarasi kulit. Selain itu, tanaman lidah buaya juga bermanfaat melebatkan dan menghitamkan rambut.
Dosis kapsul yang digunakan disesuaikan dengan sifat lidah buaya untuk mengatasi gangguan pencernaan yaitu pada dosis 150 mg (Lutfi, 2015). Dalam penelitian ini menggunakan zat aktif serbuk simplisia daun lidah buaya.
Pada penelitian ini, peneliti membuat 4 formula sediaan kapsul dari serbuk simplisia daun lidah buaya dengan memvariasikan jenis bahan pengisi dan ukuran partikel granul. Formula 1 dengan bahan pengsi Laktosa 100%
menggunakan mesh 20, formula 2 dengan bahan pengisi amilum 100%
menggunakan mesh 40, formula 3 dengan bahan pengisi laktosa dan amilum 50%:50% meggunakan mesh 20 dan formula 4 dengan bahan pengisi amilum dan laktosa 50%:50% menggunakan mesh 40.
Agar bentuk granul semakin baik, maka zat aktif diikat menggunakan PVP sehingga bentuk granul semakin baik, dan bahan pengisi diikat menggunakan musilago amili. Selain itu, untuk meningkatkan fungsi bahan pengisi, dilakukan metode ko-proses amilum-laktosa.
Universitas Sumatera Utara
3 1.2 Rumusan masalah
a. Apakah serbuk simplisia daun lidah buaya dapat diformulasikan menjadi sediaan kapsul?
b. Formula manakah yang mendekati bobot massa orientasi kapsul?
c. Apakah ukuran partikel granul akan mempengaruhi hasil evaluasi sediaan kapsul serbuk simplisia daun lidah buaya?
d. Untuk mengetahui pengaruh perbedaan jumlah bahan pengisi terhadap hasil evaluasi sediaan kapsul serbuk simplisia daun lidah buaya?
1.3 Hipotesis
a. Diduga serbuk simplisia daun lidah buaya (Aloe vera) dapat dibuat menjadi sediaan kapsul.
b. Salah satu dari keempat formula mendekati bobot massa orientasi kapsul.
c. Perbedaan ukuran partikel granul mempengaruhi hasil evaluasi sediaan kapsul lidah buaya (Aloe vera L.).
d. Perbedaan jumlah bahan pengisi memberikan pengaruh terhadap hasil evaluasi sediaan kapsul simplisia lidah buaya.
1.4 Tujuan
a. Untuk mengetahui serbuk simplisia daun lidah buayadapat dibuat menjadisediaan kapsul.
b. Untuk mengetahui formula yangmendekati bobot massa orientasi kapsul.
c. Untuk mengetahui pengaruh ukuran partikel granul terhadap sifat fisik kapsul serbuk simplisia daun lidah buaya.
Universitas Sumatera Utara
4
d. Untuk mengetahui pengaruh perbedaan jumlah bahan pengisi terhadap hasil evaluasi sediaan kapsul dari simplisia lidah buaya.
1.5 Manfaat
Manfaat dari penelitian ini yaitu sebagai bahan informasi serbuk simplisia daunlidah buaya (Aloe vera L.) dapat dibuat menjadi sediaan kapsul, adanya ukuran partikel granul terhadap hasil evaluasi kapsul, serta formula kapsul serbuk simplisa daun lidah buaya yang memberikan hasil terbaik.
Universitas Sumatera Utara
5 1.6 Kerangka Pikir Penelitian
Kerangka pikir penelitian ini dapat dilihat pada Gambar 1.1 di bawah ini:
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Diagram Kerangka Pikir Penelitian Simplisia daun
lidah buaya
Karakteristik simplisia
Makroskopik
Mikroskopik
Kadar air
Kadar abu total
Kadar abu tidak larut dalam asam
Kadar sari larut air
Kadar sari larut dalam etanol
Skrining fitokimia
1. Alkaloid 2. Flavonoid 3. Saponin 4. Tanin 5. Glikosida 6. Steroida/Triterpe
Formulasi sediaan kapsul serbuk simplisia daun lidah buaya
1. Uji preformulasi 2. Uji evaluasi
Universitas Sumatera Utara
6 BAB II
TINJAUAN PUSTAKA 2.1 Uraian Tanaman Lidah Buaya
2.1.1 Klasifikasi Tanaman Lidah Buaya
Klasifikasi tanaman daun lidah buaya adalah sebagai berikut : Kingdom : Plantae
Division : Spermatophyta Class : Monocotyledoneae Ordo : Asparagales
Family : Asphodelaceae Genus : Aloe
Species : Aloe vera(L.) Burm.f.
2.1.2 Sinonim Tanaman Lidah Buaya
Aloe barbadensis Mill, Aloe indica Royle, Aloe vulgaris Lam, Aloe officinalisForsk, Aloe elongata Murray (Ditjen POM, 2008).
2.1.3 Nama Asing Tanaman Lidah Buaya
Aloe (Inggris, Amerika Serikat, Venezuela), Bunga raja-raja, sabila (Malaysia), Salvila (Spanyol), Lu hui (Cina), chirukattali, dickwar, gawar, ghai kunwar (India) (Ditjen POM, 2008).
2.1.4 Nama Daerah Tanaman Lidah Buaya
Ilat baya, lidah buaya (Jawa), Letah buaya (Sunda) (Ditjen POM, 2008).
2.1.5 Morfologi Tanaman Lidah Buaya
Lidah buaya sama seperti tanaman lainnya yang mempunyai struktur akar, batang, daun dan bunga, namun yang sering digunakan di dalam pengobatan adalah bagian daun. Daun lidah buaya merupakan daun tunggal berbentuk tombak
Universitas Sumatera Utara
7
dengan helaian memanjang berupa pelepah dengan panjang mencapai kisaran 40 60 cm dan lebar pelepah bagian bawah 8–13 cm dan tebal antara 2–3 cm.
Daunnya berdaging tebal, tidak bertulang, berwarna hijau keabu- abuan dan mempunyai lapisan lilin di permukaan serta bersifat sukulen, yakni mengandung air, getah dan lendir yang mendominasi daun. Bagian atas daun rata dan bagian bawahnya membulat (cembung). Daun lidah buaya muda memiliki bercak berwarna hijau pucat sampai putih. Bercak ini akan hilang saat daun lidah buaya dewasa. Namun tidak demikian halnya dengan tanaman lidah buaya jenis kecil atau lokal. Hal ini kemungkinan disebabkan faktor genetiknya. Sepanjang tepi daun berjajar gerigi atau duri yang tumpul dan tidak berwarna (Furnawanthi, 2007).
2.1.6 Kandungan Kimia Tanaman Lidah Buaya
Kandungan utama adalah air dan polisakarida (pektin, hemiselulosa, glukomanan, asemanan, dan derivat manosa). Selain itu mengandung asam amino, lipida, sterol, tanin dan enzim (Ditjen POM, 2008).
2.1.7 Manfaat Tanaman Lidah Buaya
Lidah buaya mampu menyembuhkan penyakit sariawan. Lidah buaya ini dapat menyembuhkan penyakit sariawan setelah dilakukan pengolesan selama lebih kurang 3 hari. Penyembuhan ini terjadi dikarenakan lidah buaya memiliki enzim bradykinase dan karboxypeptidase yang berperan sebagai antiinflamasi (Purbaya, 2003).
Selain itu juga berfungsi sebagai pencahar dan membantu meningkatkan usus besar. Getahnya bila dicampur dengan gula dapat mengobati asma dalam dosis rendah untuk dyspepsia dan obat batuk (Perry, 1985).
Universitas Sumatera Utara
8 2.2 Simplisia
2.2.1 Pengertian Simplisa
Simplisia atau herbal adalah bahan alam yang telah dikeringkan yang digunakan untuk pengobatan dan belum mengalami pengolahan, kecuali dinyatakan lain suhu pengeringan simplisia tidak lebih dari 60oC (Ditjen POM, 2008).
Simplisia merupakan bahan awal pembuatan sediaan herbal. Mutu sediaan herbal sangat dipengaruhi oleh mutu simplisia yang digunakan. Oleh karena itu, sumber simplisia, cara pengolahan, dan penyimpanan harus dapat dilakukan dengan cara yang baik. Simplisia adalah bahan alam yang digunakan sebagai bahan sediaan herbal yang belum mengalami pengolahan apapun dan kecuali dinyatakan lain simplisia merupakan bahan yang telah dikeringkan (Ditjen POM, 2008).
Simplisia yang aman dan berkhasiat adalah simplisa yang tidak mengandung bahan kimia, mikrobiologis, dan bahan fisik, serta mengandung zat aktif yang berkhasiat. Ciri simplisia yang baik adalah kondisi kering (kadar air
<10%), untuk simplisia daun, bila diremas bergemerisik dan berubah menjadi serpihan, simplisia bunga bila diremas bergemerisik dan berubah menjadi serpihan atau mudah dipatahkan. Ciri lain simplisia yang baik adalah tidak berjamur, dan berbau khas menyerupai bahan segarnya (Herawati, 2012).
2.2.2 Penggolongan Simplisa
Simplisia dibagi menjadi tiga golongan, yaitu : a. Simplisia nabati
Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan. Eksudat tumbuhan adalah isi sel yang secara spontan
Universitas Sumatera Utara
9
keluar dari tumbuhan atau dengan cara tertentu dikeluarkan dari selnya atau zat nabati lain yang dengan cara tertentu dipisahkan dari tumbuhannya (Ditjen POM, 1995).
b. Simplisia hewani
Simplisia hewani adalah simplisia berupa hewan utuh atau zat-zat berguna yang dihasilkan oleh hewan. Contohnya adalah minyak ikan dan madu (Gunawan dan mulyani, 2010).
c. Simplisia pelikan atau mineral
Simplisia pelikan atau mineral adalah simplisia berupa bahan pelikan atau mineral yang belum diolah atau telah diolah dengan cara sederhana. Contohnya serbuk seng dan serbuk tembaga (Gunawan dan mulyani, 2010).
2.3 Granul
Granul adalah gumpalan-gumpalan dari partikel yang lebih kecil.umumnya granul dibuat dengan cara melembabkan serbuk yang diinginkan atau campuran serbuk yang digilig dan melewatkan adonan yang sudah lembab pada celah ayakan dengan ukuran lubang ayakan yang sesuai dengan ukuran granul yamg ingin dihasilkan (Ansel, 1989).
2.4 Uraian Sediaan Kapsul 2.4.1 Pengertian Kapsul
Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut. Cangkang umumnya terbuat dari gelatin, bisa juga dari pati atau bahan lain yang sesuai (Ditjen POM, 1995). Umumnya kapsul
Universitas Sumatera Utara
10
gelatin keras dipakai untuk menampung isi antara 65 mg - 1 g bahan serbuk, termasuk bahan obat dan bahan pengencer lainnya.
Beberapa keuntungan sediaan kapsul gelatin keras diantaranya adalah (Augsburger, 2000; Lachman, 1994).
a. Dapat menutupi rasa dan bau yang tidak enak dari bahan obat.
b. Mudah untuk ditelan.
c. Mudah dalam penyiapan karena hanya sedikit bahan tambahan dan tekanan yang dibutuhkan.
d. Dapat digunakan untuk menggabungkan beberapa jenis obat pada kebutuhan yang mendadak.
e. Bahan obat terlindung dari pengaruh luar (cahaya, kelembaban).
Kerugian sediaan kapsul adalah (Ansel, 1989; Augsburger, 2000):
1. Garam kelarutan tinggi umumnya tidak dapat digunakan pada kapsul gelatin keras.
2. Kapsul tidak cocok untuk bahan obat mengembang.
3. Peralatan pengisi kapsul mempunyai kecepatan yang lebih lambat dibanding mesin pencetak tablet.
2.4.2 Jenis dan Ukuran Kapsul
Kapsul terdiri dari dua macam kapsul, yaitu:
1. Kapsul gelatin keras (Capsulae gelatinosae operculatae)
Kapsul gelatin keras merupakan kapsul yang mengandung gelatin, gula, dan air. Kapsul dengan tutup diberi warna-warna. Diberi tambahan warna adalah untuk dapat menarik dan dibedakan warnanya. Menurut besarnya, kapsul diberi nomor urut dari besar ke kecil sebagai berikut: No. 000; 00; 0; 1; 2; 3. Kapsul
Universitas Sumatera Utara
11
harus disimpan dalam wadah gelas yang tertutup kedap, terlindung dari debu, kelembaban dan temperatur yang ekstrim (panas) (Anief, 1986).
2. Kapsul lunak (Soft capsules)
Kapsul lunak merupakan kapsul yang tertutup dan diberi warna macam- macam. Perbedaan komposisi kapsul gelatin lunak dengan kapsul gelatin keras yaitu gula diganti dengan plasticizer yang membuat lunak, 5% gula dapat ditambahkan agar kapsul dapat dikunyah. Sebagai plasticizer digunakan gliserin dan sorbitol atau campuran kedua tersebut, atau polihidris alkohol lain (Anief, 1986).
3. Kapsul cangkang keras
Kapsul cangkang keras biasanya diisi dengan serbuk, butiran, atau granul.
Bahan semi padat atau cairan dapat juga diisikan ke dalam kapsul cangkang keras, tetapi jika cairan dimasukkan dalam kapsul, salah satu teknik penutupan harus digunakan untuk mencegah terjadinya kebocoran. Kapsul cangkang keras dapat diisi dengan tangan. Cara ini memberikan kebebasan bagi penulis resep untuk memilih obat tunggal atau campuran dengan dosis yang tepat yang paling baik bagi pasien. Fleksibelitas ini merupakan kelebihan kapsul cangkang keras dibandingkan bentuk sediaan tablet atau kapsul cangkang lunak (Anief, 2006).
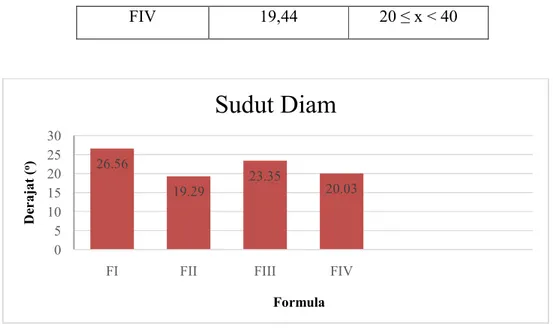
Ukuran cangkang kapsul keras bervariasi dari nomor paling kecil (5) sampai nomor paling besar (000). Umumnya ukuran (00) adalah ukuran terbesar yang dapat diberikan kepada pasien (Ditjen POM, 1995).
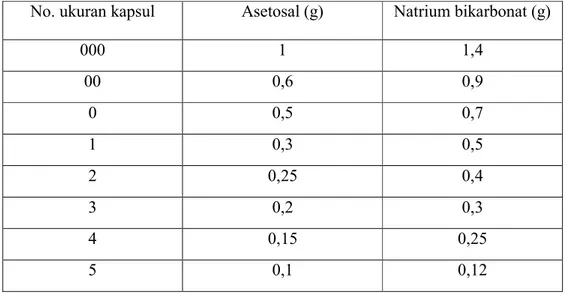
Variasi kapasitas ukuran cangkang kapsul dapat dilihat pada Tabel 2.1 (Syamsuni, 2013).
Universitas Sumatera Utara
12
Tabel 2.1 Variasi kapasitas ukuran cangkang kapsul
No. ukuran kapsul Asetosal (g) Natrium bikarbonat (g)
000 1 1,4
00 0,6 0,9
0 0,5 0,7
1 0,3 0,5
2 0,25 0,4
3 0,2 0,3
4 0,15 0,25
5 0,1 0,12
2.4.3 Metode Pengisian Kapsul
Ada tiga cara pengisian kapsul, yaitu:
1. Dengan tangan
Cara ini erupakan cara yang paling sederhana, yaitu dengan tangan tanpa bantuan alat lain. Cara ini sering digunakan di apotek untuk melayani resep dokter. Pada pengisian dengan cara ini sebaiknya digunakan sarung tangan untuk mencegah alergi yang mungkin timbul akibat petugas tidak tahan terhadap obat tersebut.
Untuk memasukan obat dapat dilakukan dengan cara sebagai berikut:
a. Serbuk dibagi dahulu sesuai dengan jumlah kapsul yang diminta.
b. Tiap bagian serbuk tadi dimasukkan ke dalam badan kapsul dan ditutup.
2. Dengan Alat Bukan Mesin
Alat yang dimaksud di sini adalah alat yang menggunakan tangan manusia. Dengan menggunakan alat ini akan didapatkan kapsul yang lebih seragam dan pengerjaannya dapat lebih cepat, sebab sekali buat dapat dihasilkan
Universitas Sumatera Utara
13
berpuluh-puluh kapsul. Alat ini terdiri atas 2 bagian, yaitu bagian yang tetap dan bagian yang bergerak.
Cara pengisian kapsul:
a. Buka bagian-bagian kapsul.
b. Badan kapsul dimasukkan ke dalam lubang pada bagian alat yang tidak bergerak.
c. Taburkan serbuk yang akan dimasukkan ke dalam kapsul.
d. Ratakan dengan bantuan alat kertas film.
e. Tutup kapsul dengan cara merapatkan atau menggerakkan bagian alat yang bergerak.
3. Dengan Mesin
Untuk memproduksi kapsul secara besar-besaran dan menjaga keseragaman kapsul, perlu dipergunakan alat yang otomatis mulai dari membuka, mengisi sampai dengan menutup kapsul (Syamsuni, 2006).
2.4.4 Penyimpanan Kapsul
Penyimpanan kapsul ditempat yang lembab akan menyebabkan kapsul menjadi lunak dan lengket serta sukar dibuka, karena kapsul tersebut menyerap air dari udara yang lembab. Sebaliknya, bila kapsul disimpan ditempat yang terlalu kering, maka kapsul akan kehilangan air dan cangkangnya menjadi rapuh dan mudah pecah. Oleh sebab itu kapsul disimpan pada suhu ruangan yang kelembabannya sedang dan tidak terlalu kering, dan disimpan dalam botol kaca atau botol plastik yang tertutup rapat dan diberi pengering (silika) (Ditjen POM, 1995).
Universitas Sumatera Utara
14 2.5 Ko-Proses Bahan Pengisi
Ko-proses merupakan teknik yang dilakukan untuk memperoleh eksipien baru dengan mengkombinasikan dua atau lebih eksipien yang telah ada, dimana kombinasi bahan tersebut akan saling melengkapi, sehingga diperoleh eksipien baru dengan sifat alir yang lebih baru (Gohel, 2005).
2.6 Uraian Bahan 2.6.1 Amilum Manihot
Amilum manihot berbentuk serbuk, tidak berbau dan tidak berasa berwarna putih atau sedikit putih dengan pH 4,5-7,0 dan mengandung 17-20%
amilosa. Tidak larut dalam etanol 96% dan air dingin, amilum mengembang secara langsung dalam air pada suhu 37°C. Larut dalam pelarut dimetilsulfoksida dan dimetilformamida. Amilum mengandung amilosa linear dan amilopektin bercabang, yaitu dua polisakarida dengan dasar a-(D)-glukosa. Amilum manihot juga disebut tapioka (Rowe, 2009).
Amilum merupakan suatu bahan tambahan farmasi yang biasa digunakan sebagai bahan pengembang, pengering (diluen), serta bahan pengikat pada tablet maupun kapsul. (Rowe, 2009).
2.6.2 Laktosa
Laktosa hidrat merupakan pengisi yang paling luas digunakan dalam formulasi sediaan tablet dan kapsul. Zat ini menunjukkan stabilitas yang baik dalam gabungan dengan kebanyakan zat aktif hidrat ataupun anhidrat. Laktosa hidrat mengandung kira-kira 5% air kristal. Laktosa merupakan eksipien yang baik sekali digunakan dalam tablet dan kapsul yang mengandung zat aktif
Universitas Sumatera Utara
15
berkonsentrasi kecil karena mudah melakukan pencampuran yang homogen (Siregar dan Wikarsa, 2010).
2.6.3 Mg Stearat
Mg stearat digunakan sebagai glidan dan antiadheren untuk mengurangi gesekan antar partikulat sehingga serbuk dapat mengalir ke lubang pada alat pengisi kapsul (Siregar dan Wikarsa, 2010).
2.6.4 Talkum
Talkum berfungsi sebagai lubrikan dan glidan. Talk juga digunakan secara luas dan mempunyai sifat menguntungkan, yaitu meminimalkan setiap kecenderungan zat yang melekat pada permukaan alat (Banker dan Anderson, 1994).
2.6.5 Amilum Jagung
Salah satu amilum yang dapat digunakan sebagai bahan penghancur yaitu amilum jagung. Amilum jagung mudah diperoleh dan harganya terjangkau.
Amilum jagung mengandung 28% amilosa dan 72% amilopektin (Wicaksono, 2008).
2.6.6 Polivinil Pirolidon
PVP merupakan polimerasi dari 1-vinilpirolidon-2-on. Bentuknya berupa serbuk putih atau putih kekuningan, berbau lemah atau tidak berbau dan higroskopis. Salah satu bahan pengikat yang sering digunakan adalah polivinil pirolidon (PVP). Granul dengan polivinil pirolidon memiliki sifat alir yang baik, sudut diam minimum dan daya kompaktibilitasnya lebih baik. PVP sebagai bahan pengikat dapat digunakan dalam bentuk larutan berair maupun alkohol. PVP juga berkemampuan sebagai pengikat kering (Banker dan Anderson, 1994).
Universitas Sumatera Utara
16 BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental yang meliputi tahap penyiapan sampel, identifikasi sampel, pembuatan simplisia, skrining fitokimia, penyalutan simplisia, uji preformulasi granul, pengisian granul ke dalam kapsul dan evaluasi kapsul. Penelitian ini dilaksanakan di laboratoriumLaboratorium Fitokimia dan Teknologi Sediaan Farmasi II Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah alat pengisi kapsul, ayakanmesh80,ayakanmesh 20,ayakan mesh 40, blender (Philips), batangpengaduk, corong, corong pisah, cawan porselen, cawan porselen berdasar rata,disintegration test, kertas perkamen, kertas saring, lemari pengering, lumpang dan alu, neraca kasar,neraca analitis (Ohaus),penjepit tabung, oven (Memmert), pipet tetes, penangas air,spatel, spatula, stopwatch dan sejumlah alat gelas lainnya.
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalahamilum manihot, cangkang kapsul, corn strach, lidah buaya,etanol 80%, air suling, polivinil pirolidon, laktosa, talkum, magnesium stearat dan bahan-bahan berkualitas proanalisa : α-naftol, amil alkohol, asam nitrat pekat, asam asetat anhidrat, asam klorida pekat, asam sulfat pekat, benzena, besi (III) klorida, bismuth nitrat,etilasetat, iodium, isopropanol, kalium iodida, kloroform, metanol, natrium
Universitas Sumatera Utara
17
hidroksida, natrium klorida, n-heksana, raksa (II) klorida, serbuk magnesium, timbal (II) asetat dan toluene.
3.2 Pembuatan Larutan Pereaksi 3.2.1 Pereaksi Meyer
Sebanyak 2,266 g raksa (II) klorida dilarutkan dalam air suling hingga 100 ml dan pada wadah lain dilarutkan 50 g kalium iodida dalam 100 ml air suling. 60 ml larutan I dicampurkan dengan 10 ml larutan II dan ditambahkan air suling hingga 100 ml (Ditjen POM, 1995).
3.2.2 Pereaksi Natrium Hidroksida 2 N
Sebanyak 8,002 g natrium hidroksida ditimbang, kemudian dilarutkan dalam air suling hingga 100 ml (Ditjen POM, 1979).
3.2.3 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dan 2 g iodium dilarutkan dalam air suling secukupnya hingga 100 ml (Ditjen POM, 1995).
3.2.4 Pereaksi Dragendorff
Pereaksi dibuat dua larutan persediaan : (1) 0,6 g bismut nitrat dalam 2 ml HCl pekat dan 10 ml air; (2) 6 g kalium iodida dalam 10 ml air. Larutan persediaan ini dicampur dengan 7 ml HCl pekat dan 15 ml air (Ditjen POM, 1979).
3.2.5 Larutan Besi (III) Klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air suling hingga 100 ml, lalu disaring (Ditjen POM, 1979).
3.2.6 Larutan Asam Klorida 2 N
Asam klorida pekat sebanyak 16,6 ml ditambahkan air suling sampai 100 ml (Ditjen POM, 1979).
Universitas Sumatera Utara
18 3.2.7 Larutan Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g timbal asetat ditimbang, kemudian dilarutkan dalam air suling bebas karbon dioksida hingga 100 ml (Ditjen POM, 1995).
3.2.8 Pereaksi Liebermann-Burchard
Sebanyak 10 tetes asam asetat anhidrat dicampur dengan 1 tetes asam sulfat pekat. Ditambahkan dengan hati-hati asetat anhidrida ke dalam campuran tersebut, didinginkan (Ditjen POM, 1995).
3.2.9 Pereaksi Molisch
Sebanyak 3 g alfa naftol dilarutkan dalam 15 ml etanol 95 % ditambahkan dengan asam nitrat 0,5 N secukupnya hingga diperoleh larutan 100 ml (Ditjen POM, 1995).
3.2.10 Pereaksi Kloralhidrat
Pereaksi kloralhidrat dibuat dengan cara melarutkan kloralhidrat sebanyak 50 g dalam 20 ml air (Ditjen POM, 1995).
3.3 Penyiapan Sampel
3.3.1 Pengambilan Bahan Tanaman
Pengambilan bahan tanaman dilakukan secara purposif yaitu tanpa membandingkan tanaman yang sama dengan daerah lain. Bahan tanaman yang digunakan adalah lidah buaya yang diperoleh dari Desa Dalu Sepuluh B Tanjung Morawa Kabupaten Deli Serdang Sumatera Utara.
3.3.2 Identifikasi Tanaman
Identifikasi bahan tanaman dilakukan di “Herbarium Medanense”, Universitas Sumatera Utara.
Universitas Sumatera Utara
19 3.3.3 Pembuatan simplisia
Daun lidah utuh yang masih segar dicuci dengan air mengalir dan ditiriskan, ditimbang berat basahnya, kemudian diiris tipis dan dikeringkan di lemari pengering dengan suhu 40-50oC selama ± 5 hari, ditimbang berat kering simplisia.
3.3.4 Pembuatan Serbuk Simplisia
Simplisia daun lidah buayayang sudah kering dihaluskan dengan blender sehingga diperoleh serbuk simplisia daun lidah buaya, kemudian diayak dengan menggunakan ayakan mesh 80 untuk mendapatkan serbuk simplisia yang lebih halus, setelah didapat serbuk simplisia daun lidah buaya disimpan dalam wadah yang tertutup rapat.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut asam (Ditjen POM, 1995; WHO, 1998).
3.4.1 Pemeriksaan Makroskopik dan Organoleptik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan mengamati bentuk, bau, rasa dan warna dari daunlidah buaya.
3.4.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun lidah buaya. Serbuk simplisia daun lidah buaya diletakkan di atas kaca objek yang telah ditetesi dengan kloralhidrat dan ditutup dengan kaca penutup, selanjutnya diamati di bawah mikroskop.
Universitas Sumatera Utara
20 3.4.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluena). Alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung penyambung, dan tabung penerima.
Cara kerja:
Dimasukkan 200 ml toluena dan 2 ml air suling ke dalam labu alas bulat, lalu destilasi selama 2 jam. Setelah itu, toluena dibiarkan mendingin selama 30 menit, dan dibaca volume air pada tabung penerima dengan ketelitian 0,05 ml.
Kemudian ke dalam labu tersebut dimasukkan 5 gram serbuk simplisia yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluena mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluena. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluena memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa.
3.4.4 Penetapan Kadar Sari Larut dalam Air
Sebanyak 5 gram serbuk simplisia dikeringkan dimaserasi selama 24 jam dalam 100 ml campuran air dan kloroform (2,5 kloroform dalam air sampai 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Disaring, sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata dan telah ditara, sisanya
Universitas Sumatera Utara
21
dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Ditjen POM, 1995).
3.4.5 Penetapan Kadar Sari Larut dalam Etanol
Sebanyak 5 gram serbuk simplisia yang telah dikeringkan dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring, 20 ml filtrat diuapkan sampai kering dalam cawan berdasar rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot tetap.
Kadarsari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
3.4.6 Penetapan Kadar Abu Total
Sebanyak 2 gram serbuk simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam kurs porselin yang telah dipijar dan ditara, kemudian diratakan. Kurs dipijar perlahan-lahan, kemudian naikkan suhu secara bertahap hingga 600oC sampai arang habis, jika arang masih tidak dapat dihilangkan, ditambahkan air panas, saring melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring dalam kurs yang sama. Masukkan filtrat ke dalam kurs, uapkan, pijarkan hingga bobot tetap, timbang. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
3.4.7 Penetapan Kadar Abu Tidak Larut Asam
Abu yang diperoleh dalam penetapan kadar abu total dididihkan dalam 25 ml asam klorida 2N selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu dan dicuci dengan air panas, dipijarkan kemudian didinginkan dan ditimbang sampai bobot tetap. Kadar
Universitas Sumatera Utara
22
abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
3.5 Skrining Fitokimia
Skrining fitokimia dilakukan untuk mengetahui golongan senyawa kimia yang terkandung di dalam serbuk simplisia daunlidah buaya (Aloe vera L.).Golongan senyawa kimia yang diperiksa meliputi senyawa alkaloid, flavonoid, saponin, glikosida, tanin dan steroid/triterpenoid.
3.5.1 Pemeriksaan alkaloida
Simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanasakan di atas penangas air selama 2 menit.
Didinginkan dan disaring. Filtrat dipakai untuk percobaan sebagai berikut : a. Filtrat sebayak 3 tetes ditambah dengan 2 tetes larutan pereaksi Meyer, akan
terbentuk endapan menggumpal bewarna putih atau kuning.
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat, akan terbentuk endapan berwarna coklat sampai hitam.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Dragendorff, akan terbentuk endapan merah atau jingga.
Simplisia mengandung alkaloida jika sekurang-kurangnya terbentuk endapan dengan menggunakan dua golongan larutan percobaan yang digunakan.
Tetapi jika reaksi 1 dan 2 hanya terjadi kekeruhan dilanjutkan pemeriksaan berikut:
Sebanyak 8 ml filtrat ditambahkan 2 ml ammonia pekat dan dikocok dengan 5 ml campuran eter-kloroform (3:1) dan dibiarkan memisah, diambil
Universitas Sumatera Utara
23
lapisan eter-kloroform, ditambahkan sedikit natrium sulfat anhidrat, disaring dan diuapkan filtrat di dalam gelas arloji di atas penangas air, dm ilarutkan residunya dengan sedikit HCl 2N. Alkaloid positif jika terjadi endapan atau kekeruhan paling banyak dua dari tiga percobaan di atas (Ditjen POM, 1979).
3.5.2 Pemeriksaan flavonoida
Sebanyak 0,5 g ekstrak ditambahkan 20 ml air panas, dididihkan selama 10 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.5.3 Pemeriksaan saponin
Sebanyak 0,5 g simplisia dimasukkan ke dalam tabung reaksi, ditambahkan 10 ml air panas, didinginkan kemudian dikocok selama 10 detik, jika terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Ditjen POM, 1995).
3.5.4 Pemeriksaan tanin
Sebanyak 0,5 g simplisia disari dengan 10 ml air suling lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil sebanyak 2 ml dan ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida 1 %. Jika terjadi warna hijau, biru, atau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.5.5 Pemeriksaan glikosida
Sebanyak 3 gram simplisia disari dengn 30 ml campuran etanol 95%
dengan air suling (7:3), fitambahkan asam sulfat pekat hingga diperoleh pH 2, kemudian direfluks selama 10 menit, didinginkan dan disaring. Sebanyak 20 ml
Universitas Sumatera Utara
24
filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran isopropanol dan kloroform (2:3), dilakukan berulang sebanyak 3 kali. Kumpulan sari air diuapkan dengan temperatur tidak lebih dari 50 oC. Sisanya dilarutkan dalam 2 ml metanol.
Larutan sisa dipakai untuk percobaan berikut:
a. Larutan sisa dimasukkan ke dalam tabung reaksi selanjutnya diuapkan di atas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish.
Tambahkan hati-hati 2 ml asam sulfat pekat melalui dinding tabung, terbentuk cincin ungu pada batas kedua cairan, menunjukkan adanya ikatan gula.
b. Larutan percobaan diuapkan di atas penangas air. Larutkan sisa dalam 5 ml asam asetat anhidrat. Tambahkan 10 tetes asam sulfat pekat, akan terjadi warna biru atau hijau, menunjukkan adanya glikosida (Ditjen POM, 1995).
3.5.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g simplisia dimaserasi dengan n-heksana selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan 2 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat. Timbul warna biru atau hijau menunjukkan adanya steroid dan timbul warna merah, pink atau ungu menunjukkan adanya triterpenoid (Farnsworth, 1966).
3.6 Pembuatan Sediaan Kapsul
3.6.1Penyalutan Serbuk Simplisia Daun Lidah Buaya
Pada ko-proses serbuk simplisia daun lidah buaya yang dikeringkan ditambahkan dengan larutan polivinil pirolidon 2% dalam etanol 96 % sampai terbentuk massa yang kompak. Lalu diayak F1 dan F3 menggunakan mesh 20
Universitas Sumatera Utara
25
sementara untuk F2dan F4 menggunakan mesh 40 karena telah terjadi perbesaran ukuran partikel setelah dilakukan pengcoatan dan disimpan dalam lemari pengering. Kemudian simplisiayang sudah kering diayak kembali dengan ukuran mesh 20 dan 40.
3.6.2 Pembuatan Ko-proses laktosa-amilum
Menurut Hadisoewignyo (2015), ada beberapa metode pembuatan bahan ko-proses yaitu dengan metode semprot kering (spray drying), fluid bed spray granulation, granulasi basah (wet granulation), granulasi kering (dry granulation/roller compaction), granulasi pelelehan (melt granulation), penggilingan (milling/dry grinding).
Pada pembuatan ko-proses laktosa-amilum manihot digunakan dengan metode granulasi basah. Dimana bahan pengisi laktosa dan amilum diikat dengan mengguanakan mucilago amyli. Dengan menimbang laktosa dan amilum sesuai jumlah yang dibutuhkan, kemudian dimasukkan kedalam lumpang dan digerus, lalu dimasukkan mucilago amyli sedikit demi sedikit sampai terbentuk massa yang kompak, kemudian dimesh dengan mesh 20 dan 40. Dimana F1dan F3 menggunakan Mesh 20 sedangkan F2, dan F4 menggunakan Mesh 40 dengan formula:
F1 R/ Laktosa 100%
Pasta amilum manihot 8% b/b qs
F2 R/ Amilum Manihot 100%
Pasta amilum manihot 8% b/b qs
F3 R/ Amilum Manihot 50%
Laktosa 50%
Pasta amilum manihot 8% b/b qs
Universitas Sumatera Utara
26
F4 R/ Amilum Manihot 50%
Laktosa 50%
Pasta amilum manihot 8% b/b qs 3.6.3 Distribusi Ukuran Partikel
Distribusi ukuran partikel ditetapkan dengan prosedur pengayakan (Siregar dan Wikarsa 2010). Ayakan disusun dengan berbagai ukuran. Mesh terbesar diletakkan paling atas dan dibawahnya disusun pengayak dengan mesh yang semakin kecil.
3.7 Perencanaan
3.7.1 Perencanaan Formula
Perencanaan awal untuk pembuatan formula dilihat daridosis yang akan digunakan yaitu serbuk simplisia daun lidah buaya 53,5 mg.
3.7.2 Penetapan Dosis Serbuk Simplisia Daun Lidah Buaya Sediaan Kapsul Penelitian terdahulu oleh Chabib L, dkk (2015) dalam pembuatan tablet effervescent ekstrak lidah buaya dengan menggunakan formulasi dalam bentuk serbuk kering. Dosis dalam satu kapsul terdiri dari 150 mg lidah buayadari total bobot isi kapsul.
Karena jumlah dosis yang terlalu tinggi sehigga sulit dicetak menjadi satu kapsul. Peneliti memetapka dosis terbagi menjadi tiga kapsul sekali minum dengan dosis 50 mg lidah buaya. Setelah simplisia disalut dosis menjadi 53,5 mg lidah buaya. Jadi dosis lidah buaya dalam satu kapsul adalah 53,5 mg.
Serbuk simplisia daun lidah buaya= × 300 = 53,5
Dosis didasarkan pada sediaan yang beredar dipasaran yaitu Kaplet Lidah Buaya Aloe Vera (PT. Citra Deli Kreasitama). Kaplet dihancurkan, dilakukan
Universitas Sumatera Utara
27
analisis terhadap massa kaplet. Diayak dengan mesh 80, kemudian ditambahkan aquadest. Hasilnya yang didapat dari analisis sediaan kaplet, bahwa sediaan kaplet tersebut tidak mengandung ekstrak tetapi mengandung serbuk simplisia daun lidah buaya dengan ukuran yang tidak sama. Dengan komposisi tiap kaplet mengandung ekstrak Aloe vera 630 mg. Aturan pakai 3 x sehari, 1 sampai 2 kaplet. Rendemen simplisia kering dari sampel lidah buaya segar adalah :
. x 100% = 2,22%
Jika dimisalkan rendemen ekstrak dari simplisia kering sebesar 20%, maka ekstrak lidah buaya yang dibutuhkan = 0,2 x 2,22% = 0,44%
~ , x 0,630 g = 0,0027 g
Simplisia kering yang dibutuhkan = x 0,0027 g = 0,0135 g 3.7.3 Mencari Bobot Jenis Kapsul
Untuk menegetahui bobot kapsul dengan cara terlebih dahulu dilakukan orientasi dengan memasukkan bahan aktifkemudian ditambahkandengan bahan tambahan.
3.8 Formula Kapsul Serbuk Simplisia DaunLidah Buaya
Pengisi yang digunakan dalam bentuk granul yaitu ko-proses laktosa- amilum manihot. Selain itu zat aktif simplisia lidah buayamasing masing juga dibuat dalam bentuk granul dengan menggunakan metode ko-proses. Bobot massa kapsul dalam 1 kapsul adalah 498 mg.
R/ Serbuk simplisia daun lidah buaya 53,5 mg
Corn stacrh 5%
Talkum 1%
Universitas Sumatera Utara
28
Magnesium stearat 1%
Granul Ko proses bahan pengisi 410 mg m.f.pulv. dtd No.L
da in caps
3.8.1 Dasar Penetapan Formula
Bobot ideal untuk cangkang kapsul ukuran 00 adalah 400 mg – 600 mg.
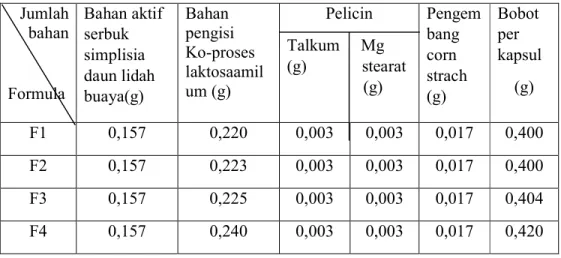
Dilakukan orientasi bobot dengan perbandingan bahan aktif dan bahan pengisi.
Pada formula orientasi bobot perbandingan simplisia kering lidah buaya dan ko- proses adalah 32,7% : 67,3%. Hasil orientasi bobot dapat dilihat pada tabel 3.1.
Tabel 3.1 Orientasi Bobot Kapsul Jumlah
bahan
Formula
Bahan aktif serbuk simplisia daun lidah buaya(g)
Bahan pengisi Ko-proses laktosaamil um (g)
Pelicin Talkum Mg (g) stearat (g)
Pengem bang corn strach (g)
Bobot per kapsul
(g)
F1 0,157 0,220 0,003 0,003 0,017 0,400
F2 0,157 0,223 0,003 0,003 0,017 0,400
F3 0,157 0,225 0,003 0,003 0,017 0,404
F4 0,157 0,240 0,003 0,003 0,017 0,420
Keterangan:
F1 : Formula kapsul serbuk simplisia daunlidah buaya dengan bahan pengisi granullaktosa 100% dengan ukuran mesh 20
F2 : Formula kapsul serbuk simplisia daunlidah buaya dengan bahan pengisi granul amilum 100%dengan ukuran mesh 40
F3 : Formula kapsul serbuk simplisia daunlidah buaya dengan bahan pengisi granul ko proses amilum-laktosa dengan perbandingan 50%:50% dengan ukuran mesh 20
Universitas Sumatera Utara
29
F4 : Formula kapsul serbuk simplisia daunlidah buayadengan bahan pengisi granul ko proses amilum-laktosa dengan perbandingan 50%:50% dengan ukuran mesh 40
3.9 Formula Bahan Pengisi
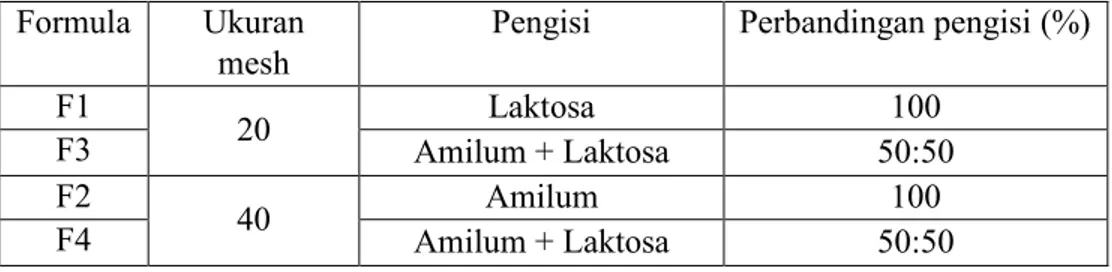
Formula bahan pengisi kapsul simplisia lidah buaya dapat dilihat pada Tabel 3.2 berikut :
Tabel 3.2 Formula bahan pengisi Formula Ukuran
mesh
Pengisi Perbandingan pengisi (%)
F1 20 Laktosa 100
F3 Amilum + Laktosa 50:50
F2 40 Amilum 100
F4 Amilum + Laktosa 50:50
3.9.1 Pembuatan bahan pengikat musilago amilum manihot 8% b/b
Amilum manihot ditimbang sesuai jumlah yang dibutuhkan dimasukkankedalam beaker glass ditambahkan sama banyak air suling sehingga terbentuk seperti suspensi. Dicukupkan dengan air suling hingga konsentrasi yang dibutuhkan, kemudian dipanaskan langsung dengan api sambil diaduk-aduk sampai mendidih hingga terbentuk pasta. Ditimbang dan dicek bobotnya, dicukupkan dengan air suling sehingga diperoleh massa amilum manihot yang dibutuhkan (Cartensen dan Chan ,1977).
3.9.2 Formula Pembuatan granul laktosa dan amilum dengan perbedaan ukuran mesh
Ditimbang laktosa dan amilum dengan perbandingan yang ditentukan sesuai jumlah yang dibutuhkan dimasukkan kedalam lumpang sambil digerus dan ditambahkan mucilago amili 8% hingga diperoleh massa yang kompak, lalu F1
Universitas Sumatera Utara
30
dan F3 digranulasi dengan ayakan mesh 20 dan F2 dan F4 digranulasi dengan ayakan mesh 40. Granulat dikeringkan pada suhu 40-60 oC pada lemari pengering.
Granul kering diayak kembali F1 dan F3 dengan ayakan mesh 20 dan F2 dan F4 dengan ayakan mesh 40 dan di cek lagi beratnya.
3.10 Uji Preformulasi Granul 3.10.1 Indeks Tap
Penentuan indeks tap dilakukan dengan cara granul dimasukkan ke dalam gelas ukur sampai garis tanda dan dinyatakan sebagai volume awalnya (V1), kemudian gelas ukur dihentakkan sebanyak 20 kali dengan alat yang dimodifikasi sehingga diperoleh volume akhir (V2). Indeks tap dapat dihitung dengan rumus :
= 1 − 2
2 × 100%
Syarat indeks tap lebih kecil dari 20 % (Voigt, 1995).
3.10.2 Waktu Alir
Penentuan waktu granul dilakukan dengan cara granul sebanyak 100 g, ditimbang, kemudian dimasukkan ke dalam corong yang telah dirangkai kemudian permukaanya diratakan. Penutup bawah dibuka bersamaan dengan dihidupkan stopwatch. Stopwatch dihentikan tepat pada saat garnul habis melewati corong dan dicatat waktu alirnya. Syarat waktu alir granul lebih kecil dari 10 detik (Voigt, 1995).
3.10.3 Sudut Diam
Penentuan sudut diam granul dilakukan dengan cara: Granul sebanyak 100 gram ditimbang, kemudian dimasukkan ke dalam corong alir yang telah dirangkai,
Universitas Sumatera Utara
31
permukaan granul di dalam corong diratakan, lalu penutup corong dibuka, sehingga granul mengalir sampai habis. Tinggi tumpukan granul yang terbentuk diukur. Sudut diam dapat dihitung dengan menggunakan rumus:
=2 Keterangan: = sudut diam
H = tinggi tumpukan granul (cm) D = diameter tumpukan granul (cm)
Granul yang memiliki daya alir bebas akan memiliki sudut diam antara 20° sampai 40° (Voigt, 1995).
3.11 Pembuatan Massa Granul Kapsul
Pembuatan sediaan kapsul dilakukan dengan cara mencampurkan hingga homogen granul simplisia lidah buaya, bahan pengisi berupa granul, dan bahan pelicin, lalu dimasukkan ke dalam cangkang kapsul keras ukuran 00.
Pembuatan massa granul kapsul :
a. Ditimbang serbuk simplisia daunlidah buaya yang telah disalut.
b. Campurkan granulat pengisi dengan granul serbuk simplisia daunlidah buaya c. Ditimbang magnesium stearat, talkum, dan corn strach sesuai jumlah yang
dibutuhkan
d. Homogenkan diatas lumpang menggunakan sudip
3.12Pengisian Massa Granul ke Cangkang Kapsul a. Dudukkan alat pengisi kapsul
Universitas Sumatera Utara
32
b. Masukkan badan cangkang kapsul ke dalam alat sebanyak 50 dan tutup lubang cangkang yang tidak digunakan disusun dengan posisi terbalik menghadap bawah
c. Naikkan alat sampai bagian atas badan kapsul rata dengan permukaan alat pengisi kapsul.
d. Curahkan massa granul ke permukaan alat
e. Ratakan permukaan alat, sampai cangkang terisi penuh f. Turunkan alat, dan tutup kapsul
3.13 Evaluasi Kapsul
Evaluasi kapsul yang dilakukan adalah uji keseragaman bobot dan uji waktu hancur kapsul.
3.13.1 Uji Keseragaman bobot
Keseragaman bobot: Cara untuk kapsul yang berisi obat kering. Timbang 20 kapsul. Timbang lagi kapsul satu persatu. Keluarkan isi semua kapsul, timbang seluruh bagian cangkang kapsul, hitung bobot isi kapsul dan bobot rata-rata tiap isi kapsul (Ditjen POM, 1979).
Deviasi = Bobot tablet – bobot rata-rata
bobot rata-rata
x 100%
Persyaratan keseragaman bobot dapat dilihat pada Tabel 3.3 Tabel 3.3Persyaratan keseragaman bobot
Bobot rata-rata isi kapsul
Perbedaan bobot isi kapsul dalam %
A B
Universitas Sumatera Utara
33 120 mg atau lebih
Lebih dari 120 mg
±10%
± 7,5 %
±20%
±15%
Persyaratan: Perbedaan dalam persen bobot isi tiap kapsul terhadap bobot rata-rata isi kapsul tidak boleh lebih dari yang ditetapkan kolom A dan untuk setiap 2 kapsul tidak lebih dari yang ditetapkan kolom B (Ditjen POM, 1979).
3.13.2 Uji Waktu Hancur Alat : Disintegration tester
Cara : Dimasukkan satu kapsul kedalam masing-masing tabung keranjang, lalu dimasukkan satu cakram pada tiap tabung, alat dijalankan. Sebagai media digunakan air dengan suhu 37 + 1 oC. Pada akhir batas waktu dinyatakan sebagai waktu hancur kapsul, kapsul dinyatakan hancur jika tidak ada lagi kapsul yang tertinggal pada kawat kasa. Pengujian dilakukan dengan 5 kapsul, dimana selama 15 menit seluruh kapsul telah hancur dan melewati kasa pada tabung (Ditjen POM, 1979).
Universitas Sumatera Utara
34 BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Identifikasi Sampel
Hasil identifikasi tanaman yang dikirim ke Laboratorium HerbariumMedanese, Universitas Sumatera Utara, dinyatakan tumbuhan yang digunakan adalah daun lidah buaya (Aloe vera(L.) Burm.f.).Hasil identifikasi daun lidah buaya dapat dilihat di Lampiran 1 halaman 47.
4.2 Hasil Karakterisasi Simplisia
4.2.1. Hasil dari Pemeriksaan Makroskopik
Hasil pemeriksaan makroskopik daun lidah buaya yaitu daun tunggal berbentuk tombak dengan helaian memanjang berupa pelepah dengan panjang mencapai 40-60cm dan lebar pelepah bagian bawah 8-13cm dan tebal 2-3cm.
Daunnya berdaging tebal, tidak bertulang, berwarna bening kehijauan,permukaan bawah kasar, kusam, berwarna lebih muda dari permukaan atas. Bau khas dan rasa agak pahit.
Gambar makroskopik dapat di lihat pada lampiran 2 halaman 48.
4.2.2. Hasil dari Pemerikasaan Mikroskopik
Hasil pemeriksaan mikroskopik serbuk simplisia daun lidah buaya menunjukkan adanya kristal Ca oksalat berbentuk jarum. Gambar mikroskopik dapat di lihat pada Lampiran 3halaman 49.
4.2.3. Hasil dari Pengujian Karakterisasi Simplisia
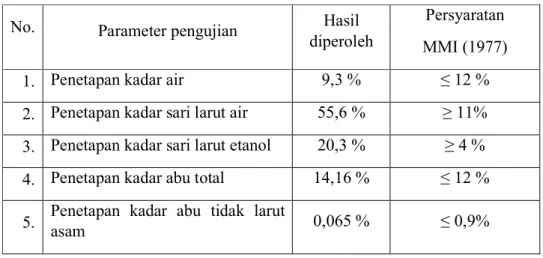
Hasil dari pengujian karakterisasi simplisia lidah buaya dapat dilihat pada Tabel 4.1.
Universitas Sumatera Utara
35
Tabel 4.1 Hasil Uji Karakterisasi Simplisia DaunLidah Buaya
No. Parameter pengujian Hasil
diperoleh
Persyaratan MMI (1977)
1. Penetapan kadar air 9,3 % ≤ 12 %
2. Penetapan kadar sari larut air 55,6 % ≥ 11%
3. Penetapan kadar sari larut etanol 20,3 % ≥ 4 % 4. Penetapan kadar abu total 14,16 % ≤ 12 % 5. Penetapan kadar abu tidak larut
asam 0,065 % ≤ 0,9%
4.3 Hasil Pembuatan Serbuk Simplisia Daun Lidah Buaya
Berat daun lidah buaya utuh 10 kg, kemudian dilakukan pemotongan untuk memperkecil ukuran daun lidah buaya dan berat basah yang dipakai 9000 gr. Setelah itu simplisia yang diperoleh sebanyak 500 gr. Simplisia dihaluskan untuk mendapatkan serbuk simplisa daun lidah buaya. Serbuk simplisia daun lidah buaya diperoleh sebanyak 300 gram.
4.4 Skrining Fitokimia
Uji skrining fitokimia dilakukan untuk mengetahui golongan senyawa kimia yang terkandung di dalam simplisia lidah buaya. Hasil skrining fitokimia terhadap simplisia lidah buaya dapat dilihat pada Tabel 4.2 di bawah ini :
Tabel 4.2 Hasil Skrining Fitokimia Simplisia lidah buaya No. Golongan Senyawa
Kimia
Simplisia lidah buaya 1.
2.
3.
Alkaloid
Flavonoid Glikosida
+ + +
Universitas Sumatera Utara