INDUKSI KALUS HAPLOID DAN DIHAPLOID CABAI MELALUI
KULTUR ANTER
(Induction of haploid and diploid calli of anther-cultured chili)
Yusniwati1)
1 Program Studi Agroekoteknologi, Fakultas Pertanian, Unand, Padang
ABSTRACT
An experiment on induction of haploid and diploid calli of anther-cultured chili was conducted on local chilli (cabai keriting), PBC 375 and PBC 378. The objectives of the experiment were to study the response of chili anther cultured on callus-initiation medium and to determine appropriate period of time of colchicine application to double the chromosomes of chili plants. Data show that 0.5 ppm 2,4-D and kinetin induced callus formation of anther culture of all types of chili studied. Callus texture and color were not affected by chili types or growth regulator as indicated by similar color and texture of all calli formed. None of the calli from the anther culture produced plantlet on the medium enriched with BA, kinetin, and NAA. Consequently, the application of colchicines was not preformed. Determination of an appropriate composition of plant growth regulators to promote shootlet and rootlet formation for chili anther culture is necessary to be pursued.
PENDAHULUAN
anaman cabai (Capsicum annuum L.) mempunyai nilai ekonomis yang tinggi dan seiring dengan peningkatan jumlah penduduk maka permintaan akan cabai juga terus meningkat. Menurut Departemen Pertanian (2006), pada tahun 2004 luas panen cabai merah Indonesia mencapai 110 170 ha dengan produksi 714 705 ton/tahun dan daya hasil 6,49 ton/ha. Daya hasil cabai merah Indonesia masih jauh dari potensi produksinya yang mencapai 12 ton/ha (Duriat 1996). Jika dibandingkan dengan negara-negara asia lainnya, daya hasil cabai merah Indonesia tertinggal jauh. Sebagai contoh, daya hasil cabai merah Cina mencapai 14,5 ton/ha (Rubatzky dan Yamaguchi, 1997). Daya hasil cabai merah Indonesia yang rendah disebabkan oleh penggunaan varietas yang berdaya hasil rendah.
T
Produksi cabai dapat ditingkatkan melalui program perluasan pertanaman dan intensifikasi budidaya. Benih yang berkualitas tinggi dapat diperoleh melalui persilangan konvensional yang diikuti dengan proses seleksi. Keberhasilan perbaikan genetik melalui persilangan konvensional sangat ditentukan oleh tetua yang homozigot, untuk itu perlu cara guna mendapatkan tanaman yang homozigot dengan cara yang murah dan cepat.
Penelitian ini direncanakan terdiri dari 2 tahapan. Tahap awal adalah mendapatkan tanaman haploid yang berasal dari kultur anter (haploid) yang kemudian dijadikan dihaploid melalui doubling (penggandaan) kromosom secara in vitro pada tahap akhir.
Keberhasilan kultur anter dipengaruhi oleh beberapa faktor komposisi media dan kondisi kultur. Berdasarkan metode yang dikem-bangkan oleh Sibi, Vaullx dan Chambonnet (1979) dengan memberikan perlakuan suhu 4oC selama 48 jam
terhadap kuncup bunga sebelum ditanam. Penelitian ini bertujuan: 1) melihat tanggapan anter beberapa varietas cabe yang dikulturkan dalam media inisiasi kalus haploid dan 2) mengetahui konsentrasi pemberian cholchichine yang tepat untuk doubling (penggandaan) kromosom.
BAHAN DAN METODE
Percobaan dilaksanakan di
laboratorium Kultur Jaringan Jurusan Budidaya Pertanian, Fakultas Pertanian, Universitas Andalas Padang.
Kultivar cabai yang akan digunakan adalah cabai keriting (CK), PBC 535, dan PBC 398, polibag, media tanam, pupuk, Media MS, Colchichine, BAP, 2,4 D, IAA, Kinetin, botol kultur, aluminium foil, skapel, pinset, alkohol, aquades, label, sprayer, plastik, dan lain-lain.
Percobaan ini menggunakan Rancangan Acak Lengkap dengan 3 ulangan. Faktor yang diuji adalah beberapa varietas cabai dengan 3 taraf (C):
Percobaan ini terdiri dari dua tahap : a) Kultur anter pada medium inisiasi, dan b) Inisiasi dihaploid.
Anter yang digunakan berasal dari kuncup bunga yang mengandung sel-sel bakal serbuk sari pada fase berinti tunggal (uninukleat) atau binukleat awal, ciri morfologi dari bunga fase ini adalah pada saat petal dan sepal sama tinggi atau sepal sedikit lebih tinggi dari petal pada cabai besar dan petal sedikit lebih tinggi pada cabai keriting. Kuncup bunga dengan ciri tersebut disimpan pada suhu 4o C selama 48
jam. Media yang digunakan adalah media MS (Lampiran 2) yang ditambahkan ZPT 0.5 ppm kinetin, 0.5 ppm 2,4 D selama 2 bulan. Parameter pengamatan: tekstur dan warna kalus.
Rancangan yang digunakan disusun secara Faktorial dalam Rancangan Acak Lengkap dengan 3 ulangan. Faktor
jam. Data hasil pengamatan dianalisis secara statistik dan bila berbeda nyata, dilanjutkan dengan DNMRT pada taraf 5 %.
Parameter pengamatan dilakukan terhadap persentase kalus yang terbentuk , warna kalus yang dihasilkan dan tektur kalusnya.
HASIL DAN PEMBAHASAN
Hasil pengamatan terhadap
tanggapan anter beberapa varietas cabai dalam media induksi kalus yang terdiri dari media MS yang ditambahkan ZPT 0.5 ppm kinetin, 0.5 2,4_D menunjukkan respon yang hampirama, dimana semua varietas yang dipakai tanggapannya hampir mendekati 100% (Tabel 1)
Tabel 1. Tanggapan anter beberapa varietas cabai dalam pembembentukan kalus pada media MS yang ditambah ZPT 0.5 ppm kinetin dan 0.5 ppm 2,4_D 16 minggu setelah tananam
Varietas Cabai Kalus yang terbentuk (%) Cabai Keriting
PBC 375 PBC 378
92 95 97
Nilai Indeks Perkecambahan
Kalus yang terbentuk tidak dalam waktu yang bersamaan, yang dimulai minggu ke dua hingga mingu ke 12 dari saat anter dikulturkan. Lamanya waktu
yang dibutuhkan untuk pembentukan kalus ini diduga karena media yang digunakan dalam bentuk padat, sehingga penetrasi media ke dalam anter untuk merangsang pembelahan sel-sel mikrospora berlangsung cukup lama.
Hasil sidik ragam pada pengamatan 16 minggu setelah tanaman menunjukkan hasil yang mendekati nilai 100% untuk ketiga varieats yang diperlakukan. Kalus yang dihasilkan pada perlakuan ini berwarna putih kekuningan dan bertekstur remah.
Tidak satupun kalus yang diperoleh dari kultur anter ini, baik yang bertektur kompak maupun remah, menghasilkan tanaman pada berbagai media regenerasi yang mengandung BA, Kinetin dan NAA sampai dengan umur 16 minggu setelah inisiasi kalus, beberapa kalus berwarna putih kehijauan menjadi besar, dapat dilihat pada Gambar 4.
Beberapa kalus lainnya tidak berkembang, berwarna coklat, merah dan akhirnya mati. Media regenerasi yang digunakan belum mampu merangsang terbentuknya tunas. Kondisi kultur yang mampu merangsang perkembangan kalus menjadi tanaman masih harus dicari. Untuk mendapatkan tanaman melalui kultur anter harus melalui embriogenesis, seperti yang telah berhasil dilakukan oleh Dumas de Vaulx et al. (1981); Maheswary dan Mak (1993); Dolcet-Sanjuan et al. (1997)..
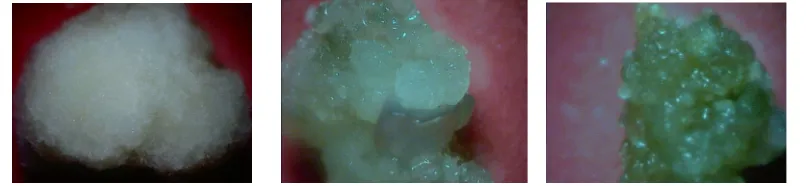
Gambar 1 Morfologi kalus anter cabai varietas lokal (Cabai Keriting)
Gambar 3 Morfologi kalus dari anter cabai 378
Gambar 4 Kalus yang berasal dari anter cabai yang berkembang berubah warna jadi hijau
Gambar 5 Morfologi kalus yang berasal dari anter cabai yang tidak menghasilkan tanaman dan akhirnya mati
KESIMPULAN
Pemberian 2,4_D dan Kinetin dapat menginduksi terbentuknya kalus pada kultur anter cabai varietas lokal, PBC 375 dan PBC 378. Tekstur dan warna kalus tidak dipengaruhi oleh kultivar maupun zat pengatur tumbuh. Kalus yang berasal dari kultur anter ini tidak satu pun yang menghasilkan tanaman pada media regenerasi yang mengandung BA, Kinetin dan NAA. Karena tanaman tidak didapatkan maka aplikasi kolkisin tidak dapat dilakukan..
DAFTAR PUSTAKA
Bajaj, YPS. 1983. In Vitro of Haploid.
Ammiroto PV, Yamada Y, editor. Handbook of plant cell culture. Volume 1. Macmillan Publishing Company. New York. Pp 229-271. Bosland PW, Votata, EJ. 2000. Peppers:
vegetables and spice Capsicums. Cabi Publishing. New York.
Coughan, TP. 1995. Anther culture for doubled haploid production. Dalam: Gamborg OL, Philips GC, editor. Plant cell, Tissue and organ culture. Fundamental methods. Springer-Verlag. Berlin. Pp 143-154
Cambridge university Press. New York. Pp 1-24.
Departemen Pertanian. 2006. Pusat Data dan Informasi Pertanian Sub Sektor Tanaman Pangan dan Hortikultura Komoditi Cabe Besar. Luas Panen, Produksi dan Produktifitas Nasional tahun 2004. Jakarta: Departemen Pertanian. http://database.deptan.go.id/bdsp web/f4-free-frame.asp 920 Jan 2006). 1997. androgenesis in Capsicum annuum L. Effects of carbohydrate and carbon dioxide enrichment. J Amer Soc Hort Sci 122:468-475
Dumas de Vaulx R, Chambonnet D, pochard E. 1981. Culture in vitro d’anteres de pigment (Capsicum annuum L.): amelioration de taux d’obtention de plantes chez differents genotypes des traitements a+ 35ºC. Agronomie 1:859-1864.
Duriat AS. 1996. Cabai Merah: Komoditas Prospek dan Andalan. Di dalam Duriat AS, Hadisoeganda AWW, Soetiassa TA, Prabaningrum
parthenogenesis. Dalam: Bosemark NO. Hayward MD, Romagosa I (Ed). Plant Breeding: Principles and Prospects. London: Chapman and Hall. Hal. 261-276
Gandawidjaya, D. 1992. Pertumbuhan dan perkembangan anter Solanum khasianum Clarke dalam kultur in vitro
Gunawan, L.W. 1987. Teknik kultur Jaringan. Lab Kultur jaringan tanaman. PAU Bioteknologi IPB. Bogor. 244 hal.
Hu H, and Zeng, JZ. 1984. Development of new varietas via anther culture. Dalam: Ammirato PV, Evans DA,
Rubatzky, VE, Yamaguchi M. 1997. Word Vegertable, Principle, Production and Nutritive Value. Ed. ke-2. London: Chapman and Hall. Rukmana R, 1996. Usaha Tani Cabe
Hibrida Sistem Mulsa Plastik. Yogyakarta. Kanisius. 91 hal. Setiadi. 1993. Bertanam cabai. Penebar
Swadaya. Jakarta
.Sibi, M, Dumas de Vaullx and R Chambonnet. 1979. Obtention de plantes haploids par androgenese
Universitas. Institut Pertanian Bogor.