BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
Kitosan ditemukan pertama kali oleh C. Rouget pada tahun 1859 dengan cara merefluks kitin dengan kalium hidroksida pekat. Dalam tahun 1934, dua paten didapatkan oleh Rigby yaitu penemuan mengenai pengubahan kitin menjadi kitosan dan pembuatan film dari serat kitosan. Perkembangan penggunaan kitin dan kitosan meningkat pada tahun 1940-an, dan semakin berkembang pada tahun 1970-an seiring dengan diperlukan nya bahan alami dalam berbagai bidang industri.(Kaban, 2009)
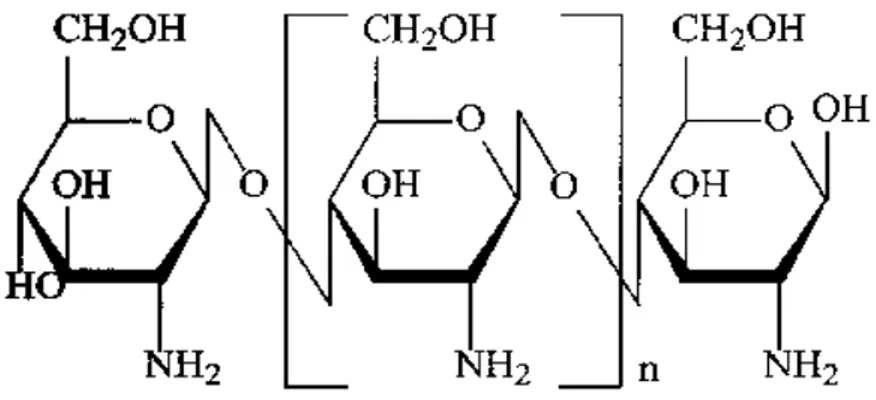
Kitosan adalah poli-(2-amino-2-deoksi-β(1-4)-D-glukopiranosa) dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin (Gambar 2.1). Kitosan juga dijumpai secara alamiah di beberapa organisme (Sugita,2009).
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun ezimatik. Proses kimiawi menggunakan basa misalnya NaOH, dan dapat menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai 85-93%. Namun proses kimiawi menghasilkan kitosan dengan bobot molekul yang beragam dan deasetilasinya juga sangat acak , sehingga sifat fisik dan kimia kitosan tidak seragam. Selain itu proses kimiawi juga dapat menimbulkan pencemaran lingkungan, sulit dikendalikan, dan melibatkan banyak reaksi samping yang dapat menurunkan rendemen. Proses enzimatik dapat menutupi kekurangan proses kimiawi. Pada dasarnya deasetilasi secara enzimatik bersifat selektif dan tidak merusak struktur rantai kitosan, sehingga menghasilkan kitosan dengan karakteristik yang lebih seragam agar dapat memperluas bidang aplikasinya (Sugita.2009).
2.1.1 Sifat Fisika-Kimia Kitosan
Kitosan merupakan padatan amorf yang berwarna putih dengan rotasi spesifik [α]D11 -3 hingga -10o (padatan konsentrasi asam asetat 2%). Kitosan larut pada kebanyakan larutan asam organik, pada pH sekitar 4,0 tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alcohol dan aseton. Dalam asam mineral HCl dan HNO3, kitosan larut pada konsentrasi 0,15-1,1%, tetapi tidak larut pada konsentrasi 10%. Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan dalam H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu kita ketahui, bahwa kelarutan kitosan dipengaruhi oleh bobot molekul, derajat deasetilasi dan rotasi spesifiknya yang beragam tergantung pada sumber dan metode isolasi serta transformasinya (Sugita, 2009).
Kitosan tidak larut dalam air, pelarut-pelarut organik, juga tidak larut dalam alkali dan asam-asam mineral pada pH di atas 6,5. Dengan adanya sejumlah asam, maka dapat larut dalam air - metanol, air - etanol, dan campuran lainnya. Kitosan larut dalam asam formiat dan asam asetat dan menurut Peniston dalam 20% asam sitrat juga dapat larut. Asam organik lainnya juga tidak dapat melarutkan kitosan, asam-asam anorganik lainnya
pada pH tertentu setelah distirer dan dipanaskan dan asam sitrat juga dapat melarutkan kitosan.
Kitosan bersifat polikationik yang dapat mengikat lemak dan logam berat pencemar. Kitosan yang mempunyai gugus amina yaitu adanya unsur N bersifat sangat reaktif dan bersifat basa. (Inoue. 1994 ).
Kitosan mempunyai sifat spesifik yaitu adanya sifat bioaktif, biokompatibel, pengkelat, anti bakteri dan dapat terbiodegradasi. Kualitas kitosan dapat dilihat dari sifat intrinsiknya, yaitu kemurniannya, massa molekul, dan derajat deasetilasi. Umumnya kitosan mempunyai derajat deasetilasi 75-100%. Massa molekul kitosan dan distribusinya berpengaruh terhadap sifat-sifat fisiko-kimia polisakarida, seperti sifat reologi kitosan, fleksibilitas rantai. Derajat deasetilasi dan massa molekul kitosan hasil deasetilasi kitin pada dasarnya dipengaruhi oleh konsentrasi alkali/basa, rasio larutan terhadap padatan, suhu dan waktu reaksi, lingkungan/kondisi reaksi selama deasetilasi. Konsentrasi alkali, rasio padatan dan larutan yang tinggi dapat memfasiltasi proses deasetilsi menghasilkan kitosan yang memiliki sifat fisiko-kimia yang memenuhi syarat untuk berbagai aplikasi.(Ramadhan,L.O.A.N, 2010)
Sedangkan sifat biologi kitosan antara lain:
a. Bersifat biokompatibel (sebagai polimer alami sifatnya tidak mempunyai akibat samping, tidak beracun, tidak dapat dicerna serta mudah diuraikan oleh mikroba).
b. Dapat berikatan dengan sel mamalia dan mikroba secara agresif.
c. Mampu meningkatkan pembentukan yang berperan dalam pembentukan tulang.
d. Bersifat hemostatik, fungistatik, spermisidal, antitumor, antikolesterol. e. Bersifat sebagai depresan pada system saraf pusat.
2.1.2 Aplikasi dan Kegunaan Kitosan
Kitosan dapat dimaanfaatkan di berbagai bidang biokimia, obat-obatan dan farmakologi, pangan dan gizi, pertanian, mikrobiologi, penanganan air limbah, industri-industri kertas, tekstil membran atau film, kosmetik dan lain sebagainya.(Wirdaniati, 2006)
Dalam penggunaannya kitosan tidak beracun dan mampu menurunkan kadar kolesterol dalam darah. Kitosan juga dapat digunakan dalam penjernihan atau pengolahan air minum. Pemakaian kitosan pada pengolahan air minum lebih baik dari pada memakai alum atau tawas dan Poli Aluminium Klorida (PAC), karena tawas dan PAC dapat mengakibatkan efek racun bagi kesehatan manusia (Roberts,J.B.1991).
Karena adanya gugus amino, kitosan merupakan polielektrolit kationik (pKa ≈ 6,5) hal yang sangat jarang terjadi secara alami. Sifat yang basa ini menjadikan kitosan :
a. Dapat larut dalam media asam encer membentuk larutan yang kental sehingga dapat digunakan dalam pembuatan gel. Dalam beberapa variasi konfigurasi seperti butiran, membran, pelapis kapsul, serat dan spons.
b. Membentuk kompleks yang tidak larut dengan air dengan polianion yang dapat juga digunakan untuk pembuatan butiran gel, kapsul dan membran.
c. Dapat digunakan sebagai pengkelat ion logam berat dimana gelnya menyediakan system produksi terhadap efek dekstruksi dari ion.
(Meriaty,2002).
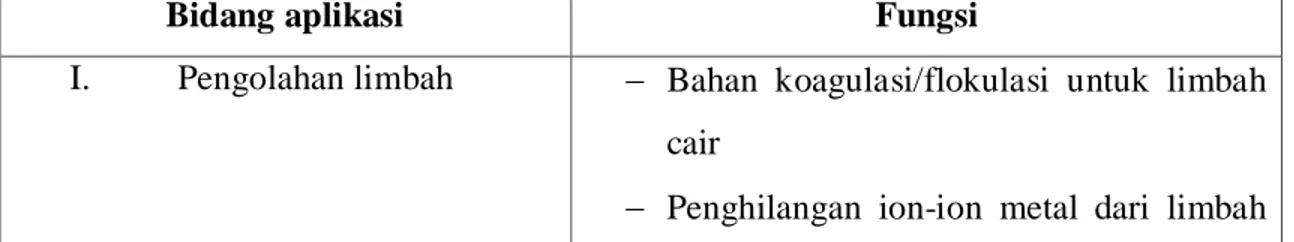
Tabel 2.1 Aplikasi dan fungsi kitosan diberbagai bidang
Bidang aplikasi Fungsi
I. Pengolahan limbah − Bahan koagulasi/flokulasi untuk limbah cair
cair
II. Pertanian − Dapat menurunkan kadar asam sayur,
buah dan ekstrak kopi
− Sebagai pupuk
− Bahan antimicrobakterial III. Industri tekstil − Serat tekstil
− Meningkatkan ketahanan warna IV. Bioteknologi − Bahan-bahan immobilisasi enzim V. Klarifikasi / Penjernihan
• Limbah industri pangan
• Industry sari buah
• Pengolahan minuman
beralkohol
• Penjernihan air minum
• Penjernihan kolam renang
• Penjernihan zat warna
• Penjernihan tannin − Koagulasi/flokulasi − Flokulan pectin/protein − Flokulan protein/mikroba − Koagulasi − Flokulan mikroba − Pembentuk kompleks − Pembentuk kompleks
VI. Kosmetik − Bahan untuk rambut dan kulit
VII. Biomedis − Mempercepat penyembuhan luka
− Menurunkan kadar kolesterol VIII. Fotografi − Melindungi film dari kerusakan (Robert, 1992)
2.2 Kitosan Oligomer
Kitosan dari kulit udang mempunyai berat molekul yang cukup tinggi dan tergantung dari sumber bahan baku. Oleh karena itu, untuk memperluas aplikasi dari kitosan perlu dilakukan usaha untuk memperkecil berat molekul dari kitosan dengan melakukan proses hidrolisis untuk memecahkan ikatan β-glikosidik dari kitosan. Selain itu hasil dari
penelitiannya Li et al (2005) menemukan bahwa nilai berat molekul kitosan yang semakin rendah karena proses hidrolisis enzimatis akan menurunkan nilai dari derajat deasetilasi juga karena enzim selektif dalam memutus ikatan glikosidiknya.
Kitosan oligomer merupakan gula amino dengan bobot molekul rendah dengan derajat depolimerisasi 20.3 dan memiliki berat molekul rataan sekitar 2.000 g/mol serta tidak bersifat toksik. Kitosan oligomer merupakan campuran oligomer dari D-glukosamin yang terbentuk melalui proses depolimerisasi kitosan dengan memutus ikatan β -glikosidik.
Kitosan oligomer merupakan kitosan yang telah mengalami depolimerisasi sehingga memiliki ukuran molekul yang lebih kecil. Proses depolimerisasi terjadi melalui pemutusan ikatan β-glikosidik, sehingga akan mempunyai bobot molekul yang lebih kecil daripada kitosan sebelum terdepolimerisasi. Berkurang nya bobot molekul dari kitosan tersebut akan menyebabkan sifat kelarutan yang semakin besar.(Srijanto, 2006)
2.2.1 Sifat Kitosan Oligomer
Berkurang nya bobot molekul dari kitosan tersebut akan menyebabkan sifat kelarutan yang semakin besar. Oligokitosan sangat menarik perhatian para peneliti karena dapat larut dalam air dan mempunyai aktivitas biologis.(Srijanto, 2006)
Adanya gugus karboksil merupakan suatu indikasi kuat kitosan larut air. Hasil penelitian menunjukkan bahwa rendemen kitosan larut air antara 118,0 – 129,4 % yang dihitung terhadap bobot kitosan. Dalam pembuatan kitosan larut air suhu sangat berpengaruh. Nilai rendemen meningkat seiring dengan peningkatan suhu.(Basmal, et al, 2007)
2.2.2 Manfaat Kitosan Oligomer
Saat ini kitosan oligomer diterapkan secara luas dalam bidang kesehatan sebagai anti bakteri, anti jamur dan anti virus, suplement makanan yang berguna untuk meningkatkan system kekebalan terhadap penyakit, pemulihan kesehatan setelah sakit, mencegah penuaan dan control emosi serta berbagai klaim khasiat antara lain anti kanker, antidiabetes dan lain-lain.(Srijanto, 2006)
Kitosan dengan bobot molekul rendah memiliki banyak perubahan dalam kelarutannya dan beberapa manfaat biologis khusus seperti aktivitas anti tumor, efek peningkatan imunitas dan aktivitas anti jamur. Belakangan ini, efek bobot molekul kitosan oligomer terhadap bioaktivitasnya telah dipelajari. Yang menyatakan aktivitas penangkapan radikal dari dua kitosan oligomer Ch 1100 dan Ch 500 dan menemukan bahwa Ch 1100 memiliki aktivitas penangkapan radikal yang tinggi. Kim mempelajati aktifitas antioksidan dari kitosan dengan bobot molekul yang bervariasi (kitosan 30, 90 dan 120 kDa) dalam salmon (Salmosalar) dengan uji penangkapan menggunakan asam 2-tiobarbiturat reaktif (TBARS) dan 2,2-diphenyl-picrylhydrzyl (DPPH). Je menyatakan aktivitas antioksidan dari Sembilan heteo-kitooligosakarida (hetero-COSs) didasarkan terhadap potensi penangkapan pada radikal 1,1-dyphenyl-2-picrylhydrazyl (DPPH) dan menemukan bahwa hetero COSs mempunyai aktivitas antioksidan yang tergantung kepada derajat deasetilasi dengan bobot molekulnya. Xie menyatakan peranan dari gugus NH2 pada kitosan dalam proses penangkapan radikal bebas.(Sun, 2007)
2.3 Metode viskositas
Pengukuran-pengukuran viskositas larutan encer memberikan teknik yang paling sederhana dan paling banyak dipakai untuk penetapan berat molekul secara rutin. Viskometri bukan metode yang mutlak; masing-masing sistem polimer mula-mula harus dikalibrasi dengan penetapan berat molekul mutlak yang dijalankan terhadap sampel-sampel polimer yang terfraksionasi. Viskositas diukur pada konsentrasi sekitar 0,5 g/100
mL pelarut dengan cara menetapkan lamanya aliran sejumlah volume larutan melalui kapiler yang panjangnya tetap. Lamanya aliran dalam detik dicatat sebagai waktu untuk meniscus lewat antara dua tanda batas pada viskometer. Viskositas-viskositas ditetapkan pada suhu konstan, biasanya 30,0 ± 0,010C.(Stevens, 2001)
Sebagai batasan, larutan polimer encer adalah yang mengandung tidak lebih dari 1 gram polimer tiap 100 ml larutan, yang pada kondisi ini larutan senyawa berbobot molekul rendah tidak mengalami interaksi antara molekul zat terlarut. Di dalam larutan, molekul polimer selalu berinteraksi satu sama lain membentuk suatu agregat, walau pada konsentrasi rendah di bawah 0,5 gram per 100 ml larutan. Agar molekul polimer terpisah total tanpa interaksi satu sama lain, larutan perlu diencerkan sampai konsentrasi yang cukup rendah, bilamana faktor interaksi ini berpengaruh, untuk pembahasan selanjutnya perlu dilakukan pendekatan dan ekstrapolasi data ke keadaan pengenceran tak terhingga. Sebagai gambaran bahwa viskositas larutan polimer berbobot molekul tinggi yang sangat encer mencapai 10-20 kali lebih besar dari viskositas pelarutnya (Wirjosentono,B,1995).
Eksperimen menunjukkan hubungan antara berat molekul dengan viskositas intrinsik adalah (Govaerts,1947 dan Quackenbos, 1980).
[𝜼]= k Ma (1)
Dimana :
𝜂 = viskositas intrinsik K, a = tetapan
Persamaan diatas disebut persamaan Mark-Kuhn-Houwink.
Dalam larutan polimer encer dipakai istilah viskositas relatif, yaitu perbandingan viskositas larutan dengan viskositas pelarut.(Tager,A, 1972)
𝜼𝒓= 𝜼𝜼𝐥𝐚𝐫𝐮𝐭𝐚𝐧𝐩𝐞𝐥𝐚𝐫𝐮𝐭 (2) [𝜼]= k Ma
Untuk menentukan viskositas relatif, waktu alir larutan dan pelarut diukur pada alat yang sama dan mengambil harga densiti pelarut sama dengan larutan.
𝜼 r = t/to (3)
Viskositas spesifik, ηsp, adalah pertambahan viskositas larutan dibagi dengan viskositas pelarut murni.
𝜼 sp = µr – 1 (4)
Viskositas tereduksi, ηred, adalah perbandingan viskositas spesifik dengan konsentrasi
𝜼red= 𝜼sp/C (5)
Variasi viskositas tereduksi dengan konsentrasi adalah merupakan garis lurus yang dituliskan dengan persamaan,
𝜼 sp/C = a1 + a2C (6) dimana : a1 = intersept
a2 = kemiringan dengan jelas
a1 = ( lim 𝜼 sp/C ) C 0 Besaran ini disebut dengan viskositas intrinsik,
[𝜼]= ( lim 𝜼sp/C )C (7) 𝜼r = t/to 𝜼sp = µr – 1 𝜼red= 𝜼sp/C 𝜼sp/C = a1 + a2C [𝜼]= ( lim 𝜼sp/C )C 0
2.4 Spektroskopi FTIR
Spektroskopi adalah ilmu yang mempelajari segala sesuatu tentang interaksi antara materi dengan radiasi elektromagnetik (REM). Interaksi yang terjadi dalam spektroskopi inframerah ini merupakan inteaksi dengan REM melalui absorbsi radiasi. Pancaran inframerah pada umumnya mengacu pada bagian spectrum elektromagnetik yang terletak di antara daerah tampak dan glombang mikro. Molekul menyerap radiasi elektromagnetik dengan panjang gelombang yang khusus. Absorbansi cahaya ultraviolet mengakibatkan pindahnya sebuah electron ke orbital dengan energy yang lebih tinggi. Radiasi inframerah tidak cukup mengandung energy untuk melakukan eksitasi tersebut, absorbsinya hanya mengakibatkan membesarnya amplitude getaran atom-atom yang terikat satu sama lain (Sudarmadji, 1989).
Konsep radiasi infra merah diajukan pertama kali oleh Sir William Herschel (1800) melalui percobaannya mendispersikan radiasi matahari dengan prisma. Ternyata pada daerah sesudah sinar merah menunjukkan adanya kenaikan temperatur tertinggi yang berarti pada daerah panjang gelombang radiasi tersebut banyak kalori (energi tinggi). Daerah spektrum tersebut selanjutnya disebut infrared. Spektroskopi inframerah ditujukan untuk maksud penentuan gugus-gugus fungsi molekul pada analisa kualitatif, disamping untuk tujuan analisis kuantitatif (Mulja, M., 1995 ).
Pengukuran pada spectrum inframerah dilakukan pada cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2,5 – 50 µm atau bilangan gelombang 4000-200 cm-1. Energy yang dihasilkan oleh radiasi ini akan enebakan vibrasi atau getaran pada molekul. Pita absorsi inframerah sangatkhas dan spesifik ntuk setiap tipe ikatan kimia atau gugus fungsi. Spektrum yang dihasilan berupa grafik yang menunjukkan persentase transmitan yang bervariasi pada setiap frekuensi radiasi inframerah (Dachriyanus, 2004).
Jumlah energy yang diserap juga bervariasi untuk setiap ikatan. Hal ini disebabkan karena terjadinya perubahan momen ikatan suatu absorbsi. Ikatan non polar (C-H atau C-C) pada umumnya akan memberikan absorbansi lemah, sedangkan ikatan
polar (C-O) akan terlihat sebagai absorbansi yang kuat. Spektroskopi FTIR dapat digunakan untuk analisa kualitatif maupun kuantitatif. Analisa kualitatif spektroskopi FTIR secara uum dipergunakan untuk identifikasi gugus-gugus fungsional yag terdapat dalam suatu senyawa yang dianalisa (Silverstein, 1986).
Analisa kuantitatif dari spektroskopi FTIR dapat dilakukan berdasarkan spectra inframerah yang dihasilkan, salah satu contohnya adalah penentuan derajat deasetilasi dari kitin dan kitosan menggunakan persamaan Domszy dan Roberts (Sugita,2009).
%D = 1 - �𝐴1665
𝐴3450 𝑥
1
1,33� x 100%
dimana: A1665 = absorbansi pada bilangan gelombang 1665 cm-1 A3450 = absorbansi pada bilangan gelombang 3450 cm-1
1,33 = tetapan yang diperoleh dari perbandingan A1665 / A3450 untuk kitosan dengan asetilasi penuh
2.5 Bahan Pendegradasi Hidrogen Peroksida
Hidrogen peroksida (H2O2) merupakan peroksida yang paling sederhana (senyawa dengan ikatan oksigen-oksigen tunggal). Zat ini juga merupakan oksidator kuat. Hidrogen peroksida merupakan cairan bening dan sedikit lebih kental dibandingkan dengan air. Dalam larutan encer tampak tidak berwarna. Karena memiliki sifat sebagai oksidator, hidrogen peroksida sering digunakan sebagai pemutih atau bahan pembersih. Kapasitas oksidasi hidrogen peroksida begitu kuat sehingga dianggap sebagai jenis oksigen yang sangat reaktif. (Hill, C. N. 2001)
Hidrogen peroksida mempunyai kemampuan melepaskan oksigen yang cukup kuat dan mudah larut dalam air. Keuntungan penggunaan hidrogen peroksida antara lain tidak menghasilkan residu atau endapan, larutan hidrogen peroksida menghasilkan produk
yang putih bersih dan bahan organik yang diputihkannya sedikit sekali mengalami kerusakan, bahkan tidak rusak sama sekali. Selain itu OOH- yang berperan dalam oksidasi bersifat ramah terhadap lingkungan.
Hidrogen peroksida dalam air akan terurai menjadi H+ dan OOH-. Ion OOH- ini merupakan oksidator kuat. Hidrogen peroksida dapat memutus ikatan C𝛼 dan C𝛽 dan mampu membuka cincin. Peroksida merupakan oksidan yang kuat juga mempunyai kemampuan mengoksidasi senyawa fenolik, amina, eter aromatik dan senyawa aromatik polisiklik. (Jayanudin,2009)
2.6 Ultrasonic Bath
Ultrasonic menggunakan gelombang suara dengan frekuensi tinggi untuk proses agitasi dalam larutan. Kavitasi gelembung disebabkan oleh proses agitasi pada kontaminan yang terdapat dalam substrat. Proses ini juga berguna dalam blind-hole, peretakan dan peredaman.(Todd,R.H. 1970)
Degradasi yang berarti sebuah proses penurunan ireversibel dari panjang rantai yang disebabkan oleh pembelahan, dan tidak tentu dalam setiap perubahan kimia yang mengacu pada rantai polimer. Sejumlah besar penelitian telah menunjukkan bahwa laju degradasi dan Mlim tidak sensitif terhadap sifat polimer ketika disonikasi dalam kondisi yang sama. Encina dkk, menemukan bahwa tingkat degradasi poli (vinil pirolidon) meningkat sepuluh kali lipat ketika polimer disiapkan dengan sejumlah kecil peroksida pada rantai tersebut dan pembelahan rantai dapat terjadi secara istimewa di titik-titik lemah dalam rantai.(Suslick, K.1999)
Proses degradasi bergantung kepada berat molekul, yaitu molekul dengan rantai lebih panjang lebih utama dihilangkan dan polidispersitas polimer berubah. Dengan demikian, degradasi dapat digunakan sebagai proses tambahan sebagai parameter dalam mengontrol distribusi berat molekul. Dalam keseluruhan polimer dengan rantai karbon
dipelajari pada saat ini, produk utama degradasi diperoleh ketika bahan radikal yang timbul dari kerusakan ikatan homolytic sepanjang rantai. Bukti radikal makromolekul muncul dari proses percobaan penangkapan radikal serta dari penggunaan resonansi spin elektron spektroskopi (Tabata, M.1980).
Proses degradasi lebih cepat dengan berat molekul lebih rendah pada temperatur yang lebih rendah dalam larutan dengan pelarut yang memiliki volatilitas yang lebih rendah juga. Pola ini mengikuti pengaruh dari parameter pada pengurangan gelembung pengkavitasi. Sonikasi pada suhu yang lebih tinggi atau dalam pelarut yang mudah menguap menghasilkan uap lebih banyak masuk ke gelembung dan terjadi penurunan pelunakan, sehingga tingkat kekerasan nya berkurang. Dalam larutan encer, rantai polimer tidak terjerat dan bebas untuk bergerak dalam daerah aliran sekitar gelembung. Seperti yang diharapkan, degradasi lebih efisien pada intensitas ultrasonik yang lebih tinggi, karena semakin banyak jumlah gelembung dengan jari-jari yang lebih besar. (Suslick, K.1999)
Kebanyakan dari senyawa polimer organik dipersiapkan dari monomer dengan ikatan rangkap reaktif yang mengalami proses pertumbuhan rantai atau raeksi addisi. Proses kavitasi dapat menghasilkan radikal dengan konsentrasi tinggi. Oleh karena itu, penerapan ultrasonic sangat terkendali dengan adanya metode inisiasi. Air itu sendiri sangat rentan terhadap kavitasi, dalam proses awal secara sonokimia menghasilkan radikal H• dan OH• yang digunakan oleh Henglein,A (1954) untuk menyiapkan larutan poliakrilonitril