BAB II
TINJAUAN PUSTAKA
2.1. Menopause
Sutanto (2005), mendefinisikan menopause proses alami dari penuaan, yaitu ketika wanita tidak lagi haid selama 1 tahun. Penyebab terhentinya haid karena ovarium tidak lagi memproduksi hormon estrogen dan progesteron. Webster’s Ninth New Collegiate Dictionary mendefinisikan menopause sebagai periode berhentinya haid secara alamiah yang biasanya terjadi antara usia 45 dan 50 tahun. Menopause adalah perdarahan terakhir dari uterus yang masih dipengaruhi oleh hormon dari otak dan sel telur.16
Menopause terjadi karena produksi sel telur habis sama sekali dan biasanya terjadi pada usia 45-50 tahun. Diagnosis dibuat setelah terdapat amenorrea (tidak haid) sekurang-kurangnya 1 tahun. Shimp & Smith (2000) mendefinisikan menopause sebagai akhir periode menstruasi, tetapi seorang wanita tidak diperhitungkan postmenopause sampai wanita tersebut telah 1 tahun mengalami amenorea. Berhentinya haid dapat didahului oleh siklus yang lebih panjang dengan perdarahan yang berkurang. Operasi atau radiasi dapat menyebabkan menopause yang umumnya menimbulkan keluhan lebih banyak dibanding menopause secara alami.17
Menopause merupakan salah satu fase dari kehidupan normal seorang wanita. Pada masa menopause kapasitas reproduksi seorang
wanita berhenti. Ovarium tidak lagi berfungsi, produksi hormon steroid dan peptida berangsur-angsur hilang dan terjadi sejumlah perubahan fisiologik. Sebagian disebabkan oleh berhentinya fungsi ovarium dan sebagian lagi disebabkan oleh proses penuaan. Banyak wanita yang mengalami gejala dan keluhan akibat perubahan tersebut di atas. Gejala dan keluhan tersebut biasanya berangsur-angsur menghilang. Walaupun tidak menyebabkan kematian, namun menimbulkan rasa tidak nyaman dan kadang-kadang menyebabkan gangguan dalam pekerjaan sehari-hari.18,19,20
Keluhan-keluhan yang biasa dialami pada masa ini antara lain mudah tersinggung, depresi, kelelahan, kurang bersemangat, sulit tidur,
hot flush, berkeringat, rasa dingin, dan sakit kepala. Ketika seseorang
memasuki masa menopause, terjadi ketidaknyamanan fisik seperti rasa kaku dan linu yang dapat terjadi secara tiba-tiba di sekujur tubuh. Rasa kaku ini terkadang disertai rasa panas atau dingin, pening, kelelahan, resah, kesal, cepat marah, dan berdebar-debar. Setelah menopause, wanita akan mengalami masa senile. Pada masa ini tercapai keseimbangan hormonal yang baru sehingga tidak ada lagi gangguan vegetatif maupun psikis.16
2.1.1. Gejala Menopause
Bentuk dari gejala-gejala merupakan dasar diagnosis. Gejala-gejala yang ada sangat bervariasi diantara wanita-wanita. Oleh karena itu
diperlukan pendekatan secara individual dalam penilaian dan pengobatan.14,17,21 A. Ketidakstabilan vasomotor Hot flushes Keringat malam Gangguan tidur
Hot flushes diduga terjadi karena adanya mekanisme yang
berhubungan dengan penurunan kadar katekolamin hipotalamus dan labilnya pusat termoregulator tubuh di hipotalamus yang diinduksi oleh penurunan kadar estrogen dan progesteron.
B. Gangguan psikologis/kognitif Depresi
Irritabilitas
Perubahan mood
Kurang konsentrasi, pelupa. C. Gangguan seksual
Kejadian gangguan seksual pada wanita perimenopause bervariasi dan meningkat dengan bertambahnya umur.
Gejala-gejala berupa; berkurangnya lubrikasi vagina, menurunnya libido, dispareuni dan vaginismus.
D. Gejala-gejala somatik Sakit kepala
Pusing E. Sindroma urogenital
Secara embrional uretra dan vagina sama-sama berasal dari sinus urogenital dan duktus Muller. Selain itu pula, di uretra dan vagina banyak dijumpai reseptor estrogen, sehingga kedua organ tersebut mudah mengalami gangguan begitu kadar estrogen serum mulai berkurang. Gangguan–gangguan tersebut dapat berupa berkurangnya aliran darah, turgor, dan jaringan kolagen. Kekurangan estrogen juga dapat menyebabkan mitosis sel dan pemasukan asam amino ke dalam sel berkurang. Pada vulva terjadi atrofi sel dan epitel vulva menipis. Dijumpai fluor dan perdarahan subepitelial (kolpitis senilis), vagina menjadi kering, mudah terjadi iritasi, dan infeksi.
2.2. Penuaan (Aging) dan Menopause.
Sejak lahir bayi wanita memiliki sekitar 770.000 sel telur yang belum berkembang. Pada fase pubertas, yaitu usia 8-12 tahun, mulai timbul aktivitas ringan dari fungsi endokrin reproduksi. Pada usia 12-13 tahun umumnya seorang wanita akan mendapatkan menarche (haid pertama kalinya) yang dikenal sebagai masa pubertas. Pada saat itu organ reproduksi wanita mulai berfungsi optimal secara bertahap. Ovarium mulai mengeluarkan sel-sel telur yang siap untuk dibuahi yang disebut dengan fase reproduksi atau periode fertil yang berlangsung hingga usia sekitar 45 tahun. Periode fertil ketika telur dibuahi, akan terjadi
Menopause biasanya terjadi pada umur akhir 40-an atau awal 50-an. Menurut WHO, menopause adalah berhentinya menstruasi secara permanen disebabkan oleh hilangnya aktifitas folikel ovarium dimana estrogen disekresikan oleh folikel primordial ovarium. Meskipun ovarium dari wanita eumenorrheic mengandung rata-rata 1.000 folikel, pada saat masa transisi (perimenopause) jumlah folikel ini akan berkurang sekitar 10 kali lipat, dan hampir tidak ada folikel yang ditemukan dalam ovarium pasca menopause. Mekanisme penurunan folikel dan menopause belum diketahui.2 Hal ini menimbulkan pertanyaan apakah menopause merupakan konsekuensi dari proses penuaan atau defisiensi endokrin atau kombinasi dari kedua faktor tesebut.2
2.3. Reactive Oxygen Spesies (ROS)
Radikal bebas diartikan sebagai molekul yang mempunyai satu atau lebih elektron yang tidak berpasangan di orbit luarnya sehingga relatif tidak stabil. Untuk mendapatkan kestabilannya, molekul yang bersifat reaktif tersebut mencari pasangan elektronnya, sehingga disebut juga sebagai reactive oxygen species (ROS). Mekanismenya dapat dengan donasi, meski umumnya dengan “mencuri” dari sel tubuh lain.
Terdapat 2 jenis ROS, yakni:
(1) molekul oksigen dengan elektron yang tidak mempunyai pasangan, (2) molekul oksigen tunggal.
Molekul yang termasuk ke dalam radikal bebas tipe 1 diantaranya ialah anion superoksida (+O2-), radikal hidroksil (OH-), dan radikal
peroksil lipid (LOO). +O2- merupakan molekul reaktif yang pertama
terbentuk saat metabolisme lipid dan protein, untuk selanjutnya dapat dikonversi menjadi hidrogen peroksida (H2O2) atau dimetabolisme oleh sistem enzim. H2O2 merupakan oksidan yang relatif lemah, namun mampu menginisiasi reaksi oksidatif dan membentuk spesies radikal bebas. Perubahan bentuk H2O2 menjadi OH terjadi melalui reaksi yang dikatalisasi oleh metal transisi (Fe2+ atau Cu+). ROS dapat mengakibatkan disfusi sel akibat pengambilan elektron dari komponen lipid, protein, dan DNA. Saat sel tubuh kehilangan elektronnya, maka sel tersebut juga akan menjadi radikal bebas yang akan memulai rangkaian proses serupa berikutnya. 23
Stres oksidatif adalah ketidakseimbangan antara radikal bebas dan anti oksidan yang dipicu oleh dua kondisi umum yakni kurangnya anti oksidan dan kelebihan produksi radikal bebas. Berbagai enzim pada sel dan proses metabolik yang terkontrol, akan menjaga agar kerusakan oksidatif ditingkat sel tetap minimal. Pada saat produksi ROS meningkat, maka kontrol protektif tidak akan mencukupi sehinggu memicu kerusakan oksidatif. Kondisi ini akan memberi dampak berupa kerusakan oksidatif mulai dari tingkat sel, jaringan, hingga ke organ tubuh menyebabkan terjadinya percepatan proses penuaan dan munculnya beragam penyakit. Penuaan dapat diartikan sebagai penumpukan kerusakan, maupun penurunan fungsi biologis dan kemampuan organisme untuk beradaptasi terhadap stres metabolik. 24
ROS sebagai elektron yang tidak berpasangan, dan merupakan metabolisme dari mitokondria. Mitokondria memproduksi superoxide yang merupakan radikal bebas, superoxide sebagai radikal bebas diproduksi pada dua titik rantai transport elektron, yang pertama pada komplek I (NADPH Dehydrogenase) dan komplek III (Ubiquinone-cytochrome c
reductase). Dalam metabolisme yang tidak normal, kompleks III
merupakan sumber dari produksi ROS, metabolisme yang tidak normal dapat berupa proses penuaan. Pada komplek III ini terbentuk suatu radikal bebas yaitu semiquinone anion spesies (Q-) yang merupakan suatu hasil sampingan dari regenerasi coenzyme q. Pembentukan ROS kemudian akhirnya akan mempengaruhi proses metabolik. Pada keadaan dengan terpapar oksidan, maka akan terbentuk glyoxal dan methylglioxal, keduanya akan menghasilkan glycation end product yang berkontribusi pada proses penuaan secara fenotipe.24
Secara evidence base, pada penelitian in vitro, mitokondria mengubah 1-2% dari molekul oksigen yang digunakan sebagai pembentukan ATP menjadi superoxide anion. Berapapun jumlah dari
superoxide anion yang menjadi ROS, tetap akan berefek buruk, sehingga
menyebabkan tubuh memproduksi anti oksidan untuk membatasi pengeluaran oksidan ini. Suatu postulat diungkapkan dalam mengurangi produksi oksidan oleh mitokondria adalah dengan meningkatkan metabolisme uncoupling. Ketika pemakaian oksigen dari metabolisme
uncoupling untuk membentuk ATP maka akan terbentuk panas.
Bagaimanapun juga, konsumsi oksigen tanpa terbentuknya ATP akan menurunkan kadar molekular oksigen bebas dalam pembentukan
superoxide anion.25
Efek buruk dari ROS sebagian besar akan dinetralisir oleh sistem anti oksidan yang meliputi suatu enzim yang memakan superoxide
dismutase (SOD), Katalase dan Gluthatione peroxidase. SOD akan
mempercepat perubahan superoxide menjadi hydrogen peroxidase, dan katalase serta glutathione peroxidase mengubah hydrogen peroxidase menjadi air. Selain enzim, terdapat beberapa molekul kecil yang berperan dalam memakan ROS, seperti ascorbate, piruvat, flavonoid, karotenoid, dan gluthation yang muncul dalam kosentrasi milimolar dalam sel. 24,25
Keseimbangan antara produksi ROS dan mekanisme pertahanan dari anti oksidan mencerminkan derajat stres oksidatif. Efek samping dari stres ini akan memodifikasi selular protein, lemak dan DNA. Kebanyakan
studi, stres oksidatif akan memodifikasi protein sehingga terbentuk derivat
carbonyl, yang nantinya menjadi penanda dalam derajat stres oksidatif.13
Beberapa penelitian mengungkapkan bahwa sel-sel yang tua dan organisme berakumulasi meningkatkan kadar oksidan yang merusak nukleus DNA. Mungkin karena kedekatannya dengan sumber utama pembentukan oksidan, atau karena sistem perbaikan DNA yang terbatas, mitokondria DNA umumnya dianggap lebih sensitif dibandingkan nukleus DNA dalam kerusakan oksidatif. Terdapat dua penelitian yang mengungkapkan bahwa stres oksidatif menimbulkan kerusakan pada mitokondria DNA. Peningkatan kerusakan mitokondria akan menyebabkan kerusakan fungsi dan integritas mitokondria, sehingga menyebabkan produksi ROS yang berlebih dan ini merupakan suatu siklus atau lingkaran dalam terjadinya kerusakan DNA.25
2.3.1. Stres Oksidatif Pada Menopause dan Penuaan (Aging)
Stres oksidatif, yang didefinisikan sebagai ketidakseimbangan antara oksidan dan anti oksidan, yang memainkan peran penting dalam proses penuaan normal. Stres oksidatif juga terlibat dalam patogenesis sejumlah proses penyakit, termasuk yang berkaitan dengan usia degeneratif proses seperti penyakit jantung, aterosklerotik, sirosis hati non-alkohol, dan berbagai patologi yang mengenai sistem reproduksi wanita. Berbagai penelitian telah menunjukkan bahwa gangguan vasomotor, osteoporosis, dan penyakit kardiovaskular secara signifikan berkorelasi dengan hilangnya estrogen secara progresif dan efek
pelindungnya, dikombinasikan dengan kekurangan pertahanan anti oksidan yang mengarah ke ketidakseimbangan redoks yang nyata. 26
Vural et al. membandingkan serum TNF-a, IL-4, IL-10, dan IL-12 pada saat fase folikular pada pada wanita premenopause, usia 19-38 tahun, dengan postmenopause, usia 37-54 tahun. Konsentrasi serum yang lebih tinggi dari TNF-a, IL-4, IL-10, dan IL-12 terlihat pada postmenopause dibandingkan dengan premenopause. Kadar TNF-a dan sitokin inflamasi telah diketahui tinggi pada keadaan stres oksidatif. Oleh karena itu, dapat dispekulasikan bahwa stres oksidatif meningkat pada pascamenopause. Penelitian ini juga menunjukkan hubungan antara kompensasi TNF-a dan IL-4. Peningkatan kadar IL-4, dengan efek anti-inflamasinya, dapat digunakan untuk melawan efek keadaan pro-inflamasi yang disebabkan oleh peningkatan kadar TNF-a.27
Signorelli juga melaporkan temuan yang menunjukkan kadar stres oksidatif yang tinggi pada menopause. Kadar serum darah digunakan untuk menilai malondialdehyde (MDA), 4-hydroxynenal (4-HNE), LDL teroksidasi, dan glutation peroksidase (GSH-Px) yang dibandingkan pada dua kelompok: wanita usia subur, antara usia 30-35 dan pascamenopause, antara usia 45-55. Kelompok postmenopause menunjukkan peningkatan yang signifikan pada biomarker pro-oksidan: MDA, 4-HNE, dan LDL teroksidasi, sedangkan kadar anti oksidan GSH-Px secara signifikan menurun bila dibandingkan dengan subjek kontrol premenopause. 28
Estrogen terlibat dalam sejumlah proses fisiologis dalam jaringan pada sistem kardiovaskular. Hal ini dikenal sebagai perlindungan terhadap penyakit kardiovaskular dengan cara efek yang dimediasi oleh endotel dan non-endotel dan efek menguntungkan pada homeostasis lipoprotein, glukosa, dan insulin, perubahan komposisi matriks ekstraseluler, destabilisasi plak aterosklerosis dan fasilitasi pembentukan pembuluh darah kolateral. Defisiensi estrogen pada postmenopause dihubungkan dengan kadar asam lemak bebas yang tinggi, yang berkontribusi pada patogenesis dari sindrom metabolik dan resistensi insulin. Menopause dengan komplikasi diabetes yang tidak terkontrol dikaitkan dengan peningkatan risiko aterosklerosis dan penyakit kardiovaskular. Risiko penyakit kardiovaskular muncul pada wanita postmenopause nondiabetes dengan adanya faktor risiko yang seperti kadar lipid dan glukosa dalam plasma yang tinggi. Aterogenesis dianggap sebagai inflamasi, proses fibroproliferatif. Insiden aterosklerosis meningkat pada menopause, sebagai pengaruh estrogen sebagai anti oksidan yang hilang, yang menyebabkan peningkatan oksidasi kolesterol LDL. Moreau et al. menunjukkan peningkatan kadar plasma LDL teroksidasi pada wanita menopause dibandingkan dengan perempuan premenopause. Pemberian anti oksidan vitamin C ditujukan untuk membalikkan efek ini, dengan penurunan konsentrasi LDL teroksidasi yang mengarah kepada perbaikan dalam parameter kesehatan vaskular seperti aliran darah dan konduktansi vaskular. 27
Teori radikal bebas dewasa ini lebih banyak dianut dan dipercaya sebagai mekanisme proses penuaan. Radikal bebas adalah sekelompok elemen dalam tubuh yang mempunyai elektron yang tidak berpasangan sehingga tidak stabil dan reaktif hebat. Sebelum memiliki pasangan, radikal bebas akan terus menerus menghantam sel-sel tubuh guna mendapatkan pasangannya termasuk menyerang sel-sel tubuh yang normal. Teori ini mengemukakan bahwa terbentuknya gugus radikal bebas (hydroxyl, superoxide, hydrogen peroxide, dan sebagainya) adalah akibat terjadinya otooksidasi dari molekul intraselular karena pengaruh sinar UV. Radikal bebas ini akan merusak enzim anti oksidant seperti
superoksida-dismutase (SOD) yang berfungsi mempertahankan fungsi sel
sehingga fungsi sel menurun dan menjadi rusak.2
2.3.2. Pemeriksaan Laboratorium Pada Stres Oksidatif.
Untuk menilai keseimbangan antara kerusakan oksidatif dan dalam penilaian ini. Regulasi jumlah radikal bebas secara normal dalam sistem biologis tubuh dilakukan oleh enzim-enzim anti oksidan endogenous seperti enzim SOD, GPx, dan Catalase. Pengukuran radikal bebas di dalam tubuh sangat sulit dilakukan karena radikal bebas bereaksi sangat cepat sehingga seringkali dilakukan pengukuran tidak langsung melalui produk turunannya seperti MDA dan 4-hidroksinonenal.Kedua senyawa tersebut sering digunakan untuk pengukuran reaksi radikal bebas lipid.27
Kita dapat menilai kapasitas dari anti oksidan tubuh, enzim yang merusak radikal bebas, marker yang mengevaluasi kerusakan oleh karena produksi radikal bebas. Berikut pemeriksaan yang dapat dilakukan: 11 1. Sampel darah, dalam hal ini dapat diperiksa kapasitas dari anti
oksidan dan enzim yang berfungsi memproteksi yang meliputi:
Glutathione darah, total kapasitas anti oksidan, enzim Superoxidase Dismutase,Gluthatione peroxidase dan enzim katalase. Sementara,
sampel darah yang menggambarkan kerusakan dari tubuh, pemeriksaan Lipid peroxidase dan Malondialdehida.
2. Sampel urin, dalam hal ini dapat diperiksa kerusakan oleh karena radikal bebas, meliputi: lipid peroxidase (kerusakan oxidatif pada membran sel) dan 8-hydroxy-deoxy Guanosine (kerusakan oxidatif pada DNA).
2.4. Enzim Katalase
Enzim katalase pertama kali diduga tahun 1811 saat Louis Jacques Thenard menemukan H2O2 (Hidrogen Peroksida) diduga terurai oleh suatu
substansi yang tidak diketahui namanya. Tahun 1900, Oscar Loew pertama kali memberikan nama enzim katalase dan banyak ditemukan pada tanaman dan hewan.
Katalase merupakan enzim yang sering ditemukan hampir di semua makhluk hidup yang terpapar oksigen. Mengkatalisis perubahan dari hydrogen peroxide menjadi air dan oksigen. 29
Enzim ini sangat penting dalam reaksi biokimia reproduktif. Demikian juga, katalase memiliki satu proses reaksi dengan angka aktifitas tertinggi pada seluruh enzim. Satu molekul katalase dapat merubah jutaan molekul hydrogen peroxide menjadi air dan oksigen tiap detik. 30
Katalase sebagai salah satu anti oksidan endogen merupakan senyawa hemo- tetramer dari empat rantai polipeptida, dengan masing-masing rantai polipeptida mengandung lebih dari 500 rantai asam amino yang panjang. 31 Katalase mengandung empat kelompok porphyrin heme
(iron) dengan Fe sebagai kofaktor di sandi oleh gen kromosom 11. Bila
terjadi mutasi pada gen ini akan menyebabkan akatalasemia. Katalase termasuk golongan enzim hidroperoksidase karena dapat mengkatalisis substrat hidrogen peroksida atau peroksida organik. PH optimum untuk aktifitas enzim katalase pada manusia kira-kira 7, dan memiliki rentang maksimal (nilai reaksi tidak dapat berubah cukup besar pada pH antara 6,8 dan 7,5). pH optimum untuk variasi katalisis lainnya antara 4 dan 11 tergantung jenisnya.Suhu optimum juga bervariasi tergantung jenisnya.2,22
Di dalam sel, katalase banyak ditemukan di dalam peroksisom. Enzim ini dapat ditemukan juga di dalam darah, sumsum tulang, membrane mukosa, ginjal, dan hati.22
Kapasitas reduksi katalase tinggi pada suasana H2O2 konsentrasi tinggi, sedangkan pada konsentrasi rendah kapasitasnya menurun. Hal ini disebabkan karena katalase memerlukan reaksi dua molekul H2O2 dalam
konsentrasi substrat rendah . Pada konsentrasi H2O2 yang rendah seperti yang dihasilkan dari proses metabolism normal, peroxiredoksin (PRX) yang berfungsi mengikat H2O2 dan mengubahnya menjadi oksigen dan
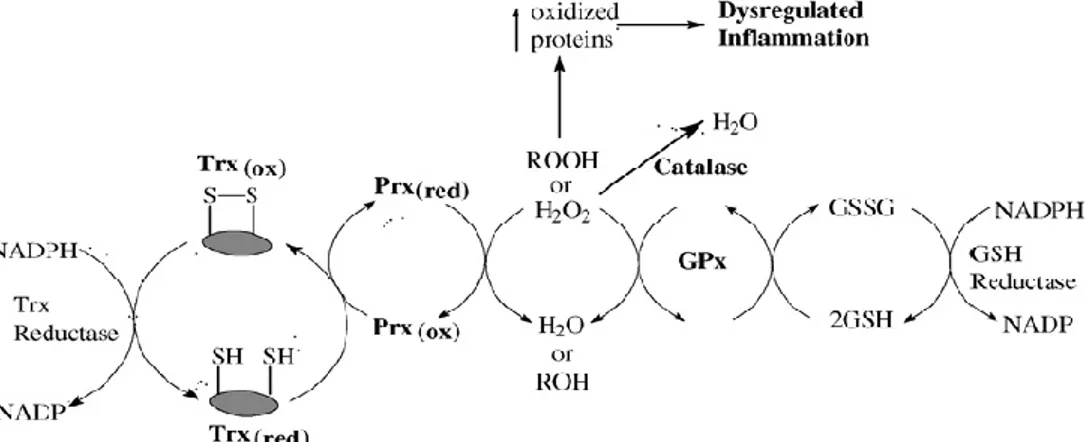
air. Reaksi pemecahan hydrogen peroksida hidroperoksida organik secara enzimatik digambarkan dalam gambar 2.
Gambar 2. Penangkapan Endogen Peroksida Seluler32
Senyawa H2O2 merupakan salah satu senyawa oksigen reaktif
yang dihasilkan pada metabolisme di dalam sel. H2O2 merupakan sumber
toksik berbagai macam penyakit karena dapat bereaksi menimbulkan kerusakan jaringan. Selain itu H2O2 dianggap sebagai metabolit kunci
karena stabilitasnya relatif tinggi, cepat menyebar dan terlibat dalam sirkulasi sel.
Enzim katalase disamping mendukung aktivitas enzim SOD juga dapat mengkatalisis perubahan berbagai macam peroksida dan radikal bebas menjadi oksigen dan air serta mampu menghambat pembentukan radikal bebas dengan cara memutus reaksi berantai dan mengubahnya menjadi produk yang lebih stabil. Reaksi ini disebut sebagai
Katalase dan glutation peroksidase (GPX) mempunyai sifat yang sama dalam mengkatalisis H2O2. Namun GPX mempunyai aktivitas yang
tinggi terhadap H2O2 daripada katalase. Hal ini disebabkan adanya
perbedaan kinetik dari kedua enzim tersebut. Katalase mengkatalisis H2O2
secara linier sesuai dengan konsentrasi H2O2, sedangkan GPX
mempunyai peranan yang lebih dominan untuk mengkatalisis H2O2
daripada katalase.32
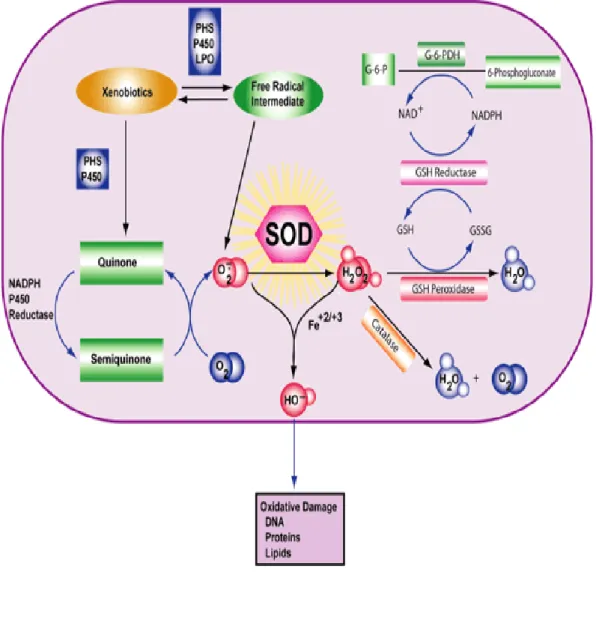
Tingginya kadar glukosa darah di duga menghalangi aktivitas anti oksidan endogen. Sebuah penelitian tentang pengaruh berbagai tingkat kadar glukosa terhadap enzim katalase, ditemukan penurunan aktivitas enzim pada kadar glukosa yang tinggi. Pada penelitian yang lain dikatakan bahwa aktivitas enzim katalase yang ditingkatkan melalui manipulasi transgenic-spesifik dapat melindungi jantung dari progresi penyakit diabetes kardiomiopati.12
Gambar 3. Mekanisme kerja Enzim Katalase Melindungi Kerusakan Sel.32
2.5. Mekanisme Molekuler
Saat mekanisme komplit dari katalase tidak diketahui secara pasti, reaksi ini diyakini terjadi dalam 2 tingkat:25,33,34
H2O2 + Fe(III)-E H2O + O = Fe(IV)-E(.+)
Disini Fe(III)-E mewakili zat besi dari kelompok heme yang berikatan dengan enzim. Fe(IV)-E(.+) adalah bentuk mesomerik dari Fe(V)-E, yang berarti iron tidak sepenuhnya teroksidasi menjadi +V, tetapi menerima beberapa “elektron pendukung” dari ikatan heme.
Ketika hidrogen peroksida memasuki situs aktif, ia berikatan dengan asam amino Asn147 ( aspargin pada posisi 47 ) dan His74, menyebabkan sebuah proton (ion hydrogen) tertransfer diantara atom oksigen. Atom oksigen bebas berkoordinasi, membebaskan molekul air yang baru terbentuk dan Fe(IV)=O. Fe(IV)=O bereaksi dengan molekul hydrogen peroksida untuk membentuk Fe(III)-E dan menghasilkan air dan oksigen.33 Reaktivitas daripada inti besi dapat ditingkatkan dengan adanya ligan phenolat Tyr357 pada ligan besi kelima, yang dapat membantu dalam oksidasi Fe(III) ke Fe(IV). Efisiensi reaksi kemungkinan dapat ditingkatkan melalui interaksi His74 dan Asn147 dengan reaksi intermediate.33
2.6. Hubungan Stres Oksidatif dan Anti Oksidan Terhadap Menopause
Berdasarkan penelitian yang dilakukan oleh Sánchez. MA, didapatkan data bahwa kadar lipoperoksidase lebih tinggi pada wanita postmenopause dibandingkan dengan premenopause. (0,357+ 0,05 vs 0,331 + 0,05 mmol/L, p<0,001. Dijumpai bahwa menopause memiliki risiko terhadap keberadaan stres oksidatif (OR 2,62, CI95% 1,35-5,11 p<0,01).35
Penelitian oleh Shrivastava, 2004 dijumpai bahwa nilai anti oksidan (Glutathion peroksidase) lebih rendah pada wanita post menopause dibandingkan dengan non menopause dan terdapat hubungan yang bermakna secara signifikan (3,59 + 1,37 vs 8,9 + 0,47, p < 0,01). Sedangkan enzim katalase lebih tinggi pada wanita menopause dibandingkan dengan non menopause dan terdapat hubungan yang bermakna secara signifikan (7,51 + 0,74 vs 6,04 + 0,22, p < 0,01).7
2.7. Menopause Specific Quality Of Life (MENQOL) Questionnnaire Salah satu cara yang dapat digunakan untuk menilai kualitas hidup wanita menopause yaitu dengan The Menopause-Specific Quality of Life
Questionnaire (MENQOL) yang diperkenalkan pada tahun 1996 oleh
Hildrich dari Kanada sebagai instrumen untuk menilai kesehatan yang berhubungan dengan kualitas hidup pada periode pasca menopause. MENQOL terdiri dari 29 bagian / pertanyaan dalam format skala Likert. Setiap pertanyaan menilai dampak dari salah satu dari empat domain gejala menopause, yaitu:
1. Gejala Vasomotor (item 1 – 3 ) 2. Gejala Psikososial (item 4 – 10) 3. Gejala Fisik (item 11 – 26) 4. Gejala Seksual (item 27 – 29)
Gejala menopause yang dinilai yang dialami wanita menopause pada 1 bulan sebelumnya. Bila jawaban „tidak‟ maka dilanjutkan ke pertanyaan berikutnya. Bila jawabannya „ya‟ maka responden diharapkan
ranging dimulai dari angka 0 dengan keluhan tidak mengganggu hingga
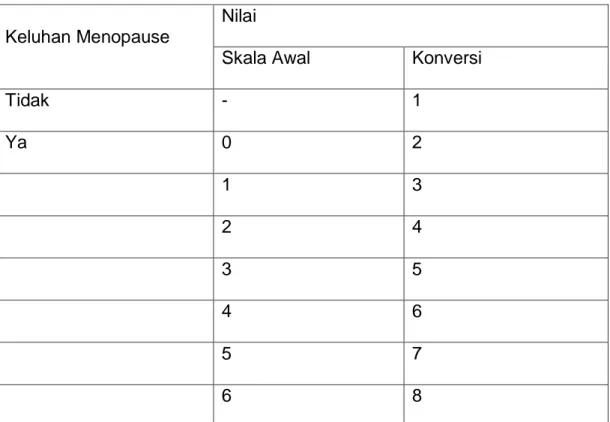
angka 6 keluhan mengganggu dengan sangat ekstrim. Untuk analisis, skor nilai dikonversikan menjadi 1 untuk „tidak‟ dan untuk „ya‟ mulai dari nilai 2 hingga skor 8 (keluhan mengganggu dengan sangat ekstrim). Namun kuesioner ini tidak jelas menyatakan tingkat atau derajat keluhan berdasarkan ringan, sedang, dan berat seperti kuesioner keluhan menopause lain seperti Menopause Rating Scale (MRS). Konversi nilai keluhan dapat diringkas sebagai berikut:15,21,37,38
Keluhan Menopause
Nilai
Skala Awal Konversi
Tidak - 1 Ya 0 2 1 3 2 4 3 5 4 6 5 7 6 8
Tabel 2.1.Tabel Konversi Nilai MENQOL
Banyak negara telah melakukan penelitian tentang kualitas hidup wanita menopause dihubungkan dengan tingkat keluhan menopause dengan menggunakan perangkat kuesioner MENQOL. Kuesioner ini telah divalidasi dan diterima oleh WHO dan telah divalidasi di Indonesia dan
menjadi salah satu acuan pada organisasi PERMI (Perkumpulan Menopause Indonesia) untuk menilai kualitas hidup wanita menopause.
Kuesioner ini juga sering digunakan untuk menilai dan membandingkan tingkat perubahan kualitas hidup dasar sebelum mendapat perlakuan atau tidakan terapi terhadap suatu penyakit degenerative atau kronis yang disebabkan oleh efek stres metabolik pada wanita menopause seperti penyakit kardiovaskular ,osteoporosis,diabetes mellitus,dan gangguan depresi maupun penyakit yang bersifat malignansi atau keganasan.39-44
2.8. Kerangka Teori
MENOPAUSE Penurunan fungsi oleh
hipotalamus Pituitari Gonad Axis ketidak teraturan
siklus haid
Jumlah folikel ovarium sangat berkurang bahkan
tidak ada
Ovarium tidak merespon hormone hipofisis
FSH meningkat, LH meningkat, Estrogen, dan
Progesteron menurun
Ketidakseimbangan Oksidan dan anti
Oksidan Peningkatan akumulasi ROS ROS Terjadi proses penuaan / aging EFEK JANGKA
PENDEK EFEK JANGKA PANJANG
Stres Oksidatif Peningkatan kadar enzim katalase Keluhan Vasomotor Keluhan Psikososial Keluhan Fisik Keluhan Seksual Penyakit Kardiovaskular Osteoporosis Keganasan
2.9. Kerangka Konsep
Variabel tergantung
Variabel bebas
Confounding
Menopause-Spesific Quality of Life Questionnaire (MENQOL)
Umur BMI
Status perkawinan Pekerjaan
Lama menopause
Tingkat Keluhan Menopause menurut domain Pengangkatan rahim dan
kedua indung telur Terapi sulih hormon Gangguan kejiwaan Penyakit keganasan
Riwayat penyakit jantung, DM, tekanan darah tinggi, osteoporosis
Merokok Minum alkohol
Enzyme Katalase