BioLink
Jurnal Biologi Lingkungan, Industri, Kesehatan
Available online http://ojs.uma.ac.id/index.php/biolink
PENGARUH KONSENTRASI BASA TERHADAP PRODUK HIDROLISIS
ESTER
Effect of Base Concentration on Ester Hydrolysis Product
Sri Wahyuna Saragih
Pendidikan Kimia Pasca Sarjana Universitas Negeri Medan, Jl. Willem Iskandar Psr. V Medan
*Corresponding author: E-mail:yunasaragih@gmail.com
Abstrak
Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi basa terhadap produk hidrolisis ester. Ester dapat dihidroisis dengan katalis basa pada konsentrasi yang berbeda. Dalam penelitian ini konsentrasi metal asetat yang digunakan adalah 1 M sedangkan konsentrasi bsa NaOH adalah 0,5 M, 0,75 M, 1 M, 1,25 M. Reaksi hidrolisis ini menggunakan pelarut etanol dan direfluks selama 2 jam pada suhu kamar. Hidrolisis ester metil asetat menghasilkan senyawa metanol dengan kemurnian yang berbeda-beda berdasarkan perbedaan konsentrasi metil asetat dan NaOH. Pada Konsentrasi NaOH 0,5 M diperoleh kemurnian metanol 79,5068 %, konsentrasi NaOH 0,75 M kemurnian metanol 85,6665 %, konsentrasi NaOH 1 M kemurnian metanol 99,6311 % dan konsentrasi NaOH 1,25 M kemurnian metanol 100,0000 %. Berdasarkan kemurnian produk hasil hidrolisis menunjukkan adanya pengaruh konsentrasi basa NaOH terhadap produk hidrolisis ester. Struktur senyawa metanol dianalisis dengan spectrometer infra merah dan spectrometer massa.
Kata Kunci: Ester, Hidrolisis, Konsentrasi basa dan Metanol
Abstract
This study aims to determine the effect of concentration of base to ester hydrolysis products. Ester can dihidroisis with an alkaline catalyst at different concentrations. In this study, the concentration of metal acetate used was 1 M NaOH while coud concentration was 0.5 M, 0.75 M, 1 M, 1.25 M. The hydrolysis reaction using ethanol and refluxed for 2 hours at room temperature. Hydrolysis of methyl acetate ester compounds produced methanol with purity varies by different concentrations of methyl acetate and NaOH. At concentrations of 0.5 M NaOH acquired 79.5068% purity methanol, 0.75 M NaOH concentration 85.6665% purity methanol, 1 M NaOH concentration 99.6311% purity methanol and NaOH concentration of 1.25 M purity methanol 100,0000 %. Based on the results of the hydrolysis product purity shows the influence of the concentration of NaOH to the product ester hydrolysis. Methanol compound structure was analyzed by an infrared spectrometer and a mass spectrometer.
Keywords :Ester Hydrolysis, bases and Methanol Concentration
82
PENDAHULUAN
Ester merupakan salah satu dari kelompok senyawa organik yang sangat
berguna dan dapat diubah menjadi
senyawa-senyawa lain.Ester sering dijumpai dialam. Tatanama suatu ester terdiri dari dua suku kata, kata pertama ialah nama gugus alkil yang terikat pada oksigen ester. Kata kedua berasal dari nama asam karboksilatnya, dengan membuang kata asam(Hadyana,1992).
Ester adalah turunan asam
karboksilat yang gugus OH dari
karboksilatnya diganti dengan gugus OR dari alkohol. Anhidrida dengan alkohol fenol atau dari karboksilat dengan alkil halida reaktif(Hadyana, 1992) Produksi ester secara industri dilakukan dengan mereaksikan anhidrida asam dengan alkohol. (Wilbrahim,1992).
Jika ester dipanaskan dalam air beberapa jam,tidak akan terjadi sesuatu yang berarti(Wilbrahim,1992). Oleh karena itu ester dapat dihidrolisis
dengan menggunakan asam dan
basayang merupakan kebalikan dari
reaksi esterifikasidengan
basamenghasilkan asam karboksilat dengan alkohol.
Ester dapat dihidrolisis menjadi komponennyaasam dan alkohol. Ester dihidrolisis dengan katalis asam bertangsung cepat karena adanya katalis ion hidrogen. Reaksi ini akan mengalami reaksi bolak-balik(reversibel), sehingga air yang berlebihan akan menekan reaksi kekanan(Wilbrahim,1992).
Hidrolisis ester dengan alkali berair merupakan metode yang efektif terhadap ester(Fieser,1956).Tetapi ion karboksilat yang terbentuk sangat stabil dan tidak
sanggup bereaksi dengan
alkohol.Senyawa yang lazim untuk hidrolisis ester ialah larutan NaOH dan KOH. Adapun reaksi yang terjadi dalam
suasana basa ini adalah reaksi
imeversibel(searah/tidak bolak-balik).
METODE PENELITIAN
Alat yang digunakan terdiri dari suatu set alat refluks, magnetic stirrer, evaporator, alat-alat gelas laboratorium, corong pisah 100 ml, spektrofotometer IR, kromatografi gas – spektra massa (GC-MS).
Bahan-bahan terdiri dri metil asetat, NaOH, dietil eter, aquades, etanol, Na2SO4 anhidrous pa, HCl pekat, Kertas
lakmus universal, kertas saring.
Prosedur Kerja
Penelitian yang dilakukan
merupakan metode eksperimen dengan langkah sebagai berikut :
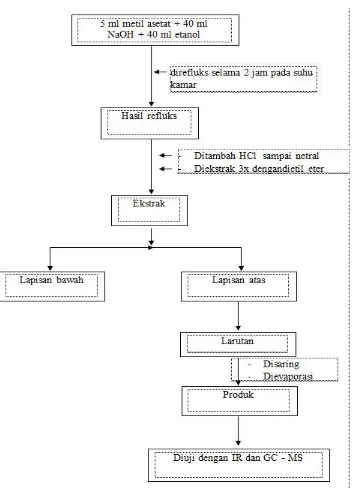
Keadaan labu leher tiga kapasitas 500 ml yang dilengkapi dengan magnetic stirrer dimasukkan 5 ml metil asetat 1M, kemudian ditambahkan 40 ml NaOH 1 M dan 40 ml etanol absolut. Setelah penambahan NaOH dan etanol, kemudian larutan direfluks selama 2 jam pada suhu kamar. Kelebihan NaOH dinetralkan dengan penambahan HCl pekat tetes demi tetes yang diuji dengan lakmus universal, kemudian diekstrak dengan 20 ml dietil eter dalam corong pisah dan diulang sebanyak 3 kali. Hasil ekstraksi ditambahkan Na2SO4anhidrous, disaring
lalu dievaporasi. Hasilnya dianalisi dengan IR dan GC-MS.
asetat dengan NaOH dapat dilihat pada tabel 1.
Tabel 1 : Perbandingan Konsentrasi Metil Asetat dengan NaOH
Metil asetat NaOH Perbandingan Konsentrasi (M)
7,96 ml (100 ml) 5,03 gr (100 ml) 1 : 1,25
7,96 ml (100 ml) 4,04 gr (100 ml) 1 : 1
7,96 ml (100 ml) 3,02 gr (100 ml) 1 : 0,75
7,96 ml (100 ml) 2,06 gr (100 ml) 1 : 0,5
84 HASIL DAN PEMBAHASAN
Hidrolisis ester asetat dengan basa NaOH dan menggunakan pelarut etanol. Pada suhu kamar direfluks selama 2 jam kemudian kelebihan NaOH dinetralkan dengan penambahan HCI pekat tetes
demi tetes. Adapun data analisa yang
diperoleh berupa data spektrum
kromatografi gas (GC), FT-IR, dan MS. Spektrum data tersebut adalah sebagai berikut :
1. Spektrum kromatografi gas (GC)
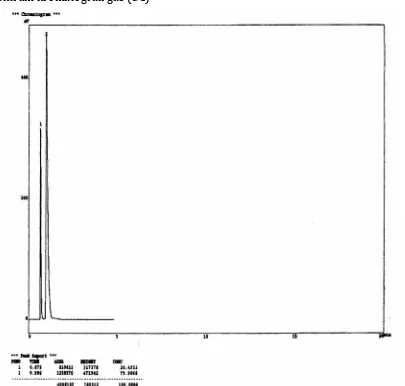
Gambar 6. Kromatogram senyawa metanol hasil hidrolisis metil asetat dengan basa NaOH dengan Perbandingan konsentrasi 1 M : 0, 75 M.
86
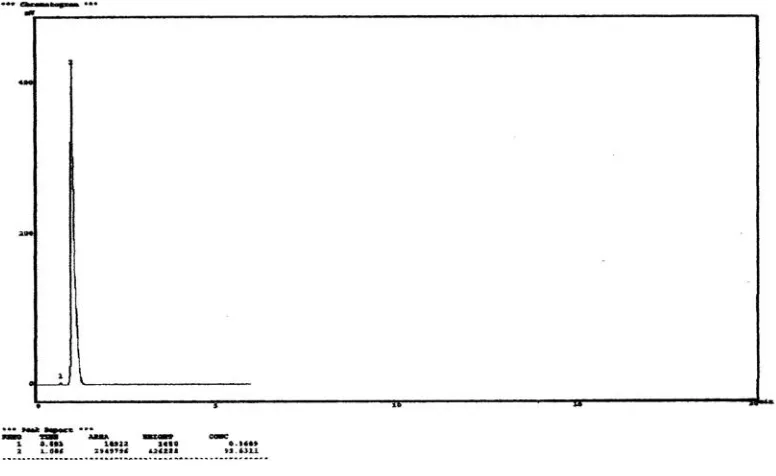
Gambar 8. Kromotgram senyawa metanol hasil hidrolisis metil asetat dengan basa NaOH dengan dengan perbandingan konsentrasi 1 M : 1,25 M.
2. Spektrum FT-IR
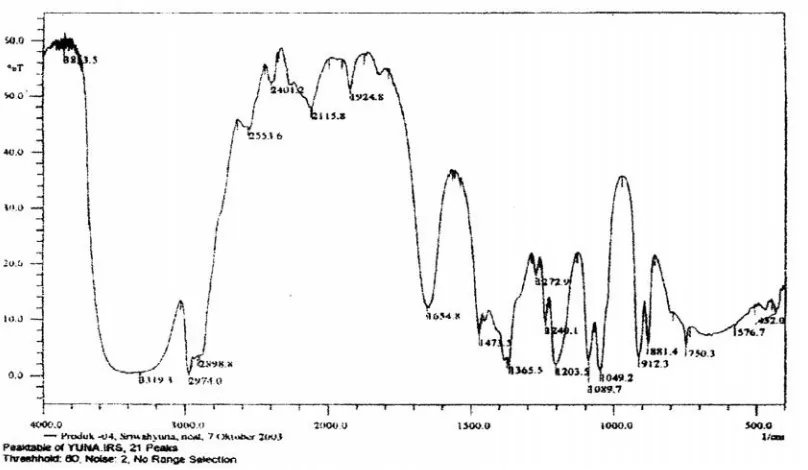
Spektrum FT-IR terhadap hasil hidrolisis ester metil asetat dengan basa NaOH disajikan pada gambar 9 dibawah ini.
3. Spektrum MS (mass-spektra)
Spektrum MS hasil analisa senyawa metanol hasil hidrolisis ester dengan basa NaOH disajikan pada gambar 10 dibawah ini.
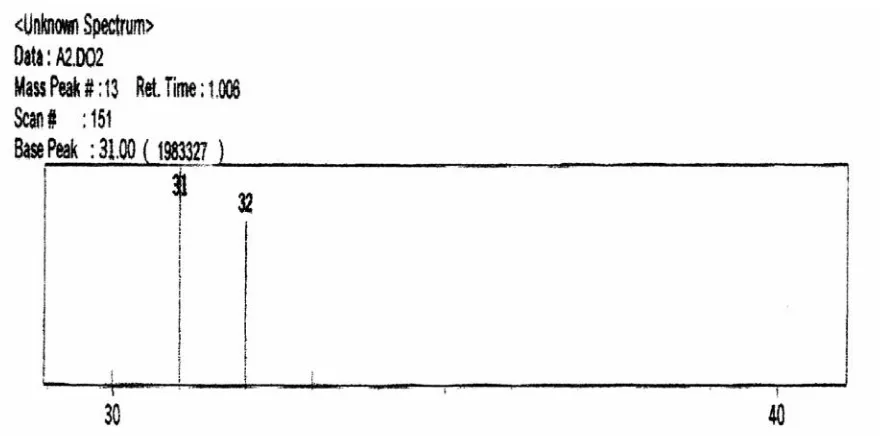
Gambar 10. Spektrum massa senyawa metanol hasil hidrolisis ester metil asetat dengan basa NaOH
Pembahasan
1. Spektrum Kromatografi Gas (GC)
Berdasarkan Spektrum
kromtagrafi gas (GC) yang di dihasilakan diperolah data sebagai berikut :
Tabel 2. Data GC senyawa metanol NO Perbandingan Konsentrasi Metil
Asetat dan Basa NaOH
Hasil data GC senyawa Metanol (%)
1.
Konsentrasi yang paling tepat digunakan untuk menghodrolisis ester dengan basa NaOH adalah 1 M :1 M. Karena pada perbandingan 1 M : 0, 75 M menjadi 99,6311% pada 1 M : 1M dengan selisish () adalah 13,9646, sedangkan perbandingan 1 M: 1,25 M produknya meningkat menjadi 100, 000 %. Hal ini sesuai karena perbandingan konsentrasi NaOH yang berlebih. Maka konsentrasi 1 M pada metil asetat dan konsentrasi 1 M
pada basa NaOH dalam reaksi hidrolisis 1 M pada metil asetat dan konsentrasi tersebut telah memberikan produk yang tinggi sampai dengan 100%.
2. Spektrum Spektrometer FT-IR
Hasil spketrum infra merah ( gambar 5 ) terlihat bahwa daerah rentangan antara 1750 cm-1– 1730 cm-1
88 menunjukkan bahwa gugus karbonil dari ester telah putus dan muncul serapan pada 3319,3 yang merupakan serapan khas - OH dari alkohol. Jadi telah terjadi proses hidrolisis ester metil asetar menghasilkan alkohol dalam hal ini metanol.
3. Spektrum Spektrometer Massa
Analisis spektrum massa
menunjukkan puncak ion molekuler m/e = 32 yang berarti berat molekul senyawa yang dianalisiis adalah 32, berat molekul 32 sesuai massa rumus metanol (CH3OH)
yang disajikan pada gambar 6. Puncak dasar senyawa metanol dengan m/e = 31 sebagai puncak dasar senyawa metanol yaitu senyawa metoksi (CH3OH) yang
dapat diteruskan menjadi metanol. Maka dalam proses hidrolisis telah terbentuk metanol.Dari hasil analisis IR dan spektra
massa dapat dinyatakan bahwa
hidrolisiis metil asetat dengan basa (OH) menghasilkan alkohol (metanol).
SIMPULAN
Produk hasil hidrolisi metil asetat menunjukkan bahwa ada pengaruh konsentrasi basa NaOH. Kemurnian produk hasil hidrolisis yang diperoleh yaitu pada konsentrasi perbandingan metil asetat : NaOH adalah konsentarsi 1 M : 0,5 M kemurnian metanol 79,5068 %, konsentrasi 1 M : 0,75 M kemurnian metanol 85,6665 %, konsentrasi 1 M : 1 M kemurnian metanol 99,6311 % dan konsentrasi 1 M : 1,25 M kemurnian metanol 100,0000 %.
Berdasarkan analisis spectrometer IR dan spectrometer massa produk hasil hidrolisis adalah senyawa methanol.
DAFTAR PUSTAKA
Allinger, N. L., M. P. Cava, D. C. De Jough, C. R.
Johnson, N. A.Lebel,and C. L.
Stevens,1976, Organic Chemestry, second
edition, Wort Publisher, Inc, New York.
Atkins, R. C., 2002, Organic Chemistry, thurd
edition, MC Graw Hill Inc, New York.
Considen, D. M., 1984,Encyclopedia of Chemstry,
fourth edition, Van Nostrand Reinhold Company, New York.
Deshayes, K. D., 1995,Encylopedia of Reagent for
Organic Synthesis, Jhon Willey and Sons, Chichester.
Elviana, S., 2003, Pengaruh Konsentrasi Asam
Format Terhadap Produk Reaksi Adisi Asam Format dengan Metil Eugenol, fourth edition, Longman, Group, Ltd, England
Handyana, A. P., 1982, Kimia Organik Jilid 2, edisi ketiga diterjemahkan dari Organic Chemistry, third edition by Fessenden and Fessenden, Penerbit Erlagga, Jakarta. Hartomo, A. J., 1989, Penuntun Mekanisme
Reaksi Kimia Oragnik, edisi keenam diterjemahkan dari A Guidebook to Mechanism in Organic Chemistry by Peter Sykes, PT Gramedia, Jakarta.
Issaac, N. S., 1973, Reactive Intermediate in Organic Chemistry, Jhon Willey, New York.
Loudon, G. M., 1995, Organic Chemistry, third
edition, The Benjamin/Cummings
Publishing Company, Inc, California. Maun, S., 1997, Dasar-Dasar Kimia Organik,
diterjemahkan dari Fundamentals of Organic Chemistry, by Fessenden and Fessenden, Binarupa Aksara, Jakarta. March, J., 1992, Advanced Organic Chemistry,
fourth edition, Jhon Wiley and Sons, New York.
Salomons, T. W. Graham, 1983, Organic Chemistry, third edition, Jhon Wiley and Sons, New York.
Shirley, A. D, 1966, Organic Chemistry, Holt Rinehart and Winston, Inc, New York. Wilbrahim, A. C, and Smatta, M., 1992, Kimia