PEMBUATAN ELEKTRODA SELEKTIF ION La
3+TIPE
KAWAT TERLAPIS DENGAN IONOFOR SENYAWA
KARBOKSIMETOKSI TERTIERBUTIL KALIKS[n]ARENA
MAKING THE COATED WIRE La3+ ION SELECTIVE ELECTRODE
WITH CARBOXYMETHOXY TERTIERBUTHYL CALIX[n] ARENE COMPOUND
Muji Harsini(1) dan Hamami(1) ABSTRACT
Preparation and characterization of coated wire La3+ selective electrode has studied in this research. The aim of this research is to look for analysis method of lanthanum using coated wire La3+ ion selective electrode with carboxymethoxy tertierbuthyl calix[n] arene compound as ionophore with 4, 6, and 8 condensation degree. Construction of coated wire ISE-La3+ started with preparation of the membrane from mixture polyvinyl chloride (PVC), ni-trophenyl octhyl ether (NPOE), potassium tetrakis chlorophenyl borate (KTCPB) and calyx[n] arene and solven tetrahydrufunan (THF). Electrode body made for platinum wire. End point platinum wire immersed in mem-brane. Result of research show that condensation degree influential to po-tential response. Carboxymethoxy tertierbuthyl calix[6] arene compound give potential response is best to La3+ ion with membrane composition 45 mg of PVC, 90 mg of NPOE, 10 mg of KTCPB and 5 mg of carboxymethoxy tertier-buthyl calix[6] arene. Characteristic of this electrode was 19.588 mV/decade, 10-7- 10-1 M, 5.807. 10-8 M respectively to Nernst factor, range concentration and detection limit. Accuracy, and precision in this method was 102,8% and 0,35 – 5, 5% coefficients of variance respectively.
Key words: calix[n]arene, La3+ ion selective electrode, coated wire
PENDAHULUAN
Lantanum merupakan golongan lantanida yang keberadaannya di alam sangat kecil, sehingga disebut unsur tanah jarang (Cotton, Wilkin-son, Gaus, 1987). Untuk menganalisis lantanum dibutuhkan metode analisis yang mempunyai batas deteksi kecil, sensitivitas dan selektivitas tinggi. Teknik pengukuran yang sudah per-nah dilakukan untuk analisis lanta-num diantaranya spektrometri sera-pan atom (AAS), inductively coupled plasm-mass spectrophotometer (ICP-MS) dan inductively coupled plasma-atomic emission spectrophotometer (ICP-AES) (Skoog, and Leary, 1998). Teknik AAS mempunyai kekurangan yaitu kemampuan deteksinya sangat besar sehingga tidak dapat digunakan pada sampel yang konsentrasinya sangat kecil. Sedangkan ICP-MS dan ICP-AES diperlukan investasi yang sangat besar dan biaya operasional mahal.
Pengukuran secara potensiometri dengan elektroda selektif ion (ESI) memiliki keunggulan lebih antara lain: analisis cepat, akurat, selektivi-tas yang tinggi, sehingga tidak perlu pemisahan, jangkau pengukuran yang luas serta biaya analisis yang rendah (Baily, 1976). Keunggulan lainnya adalah peralatannya praktis dan mu-dah dibawa sehingga dapat digunakan untuk pengukuran secara langsung di lapangan. Elektroda selektif ion tipe kawat terlapis (coated wire electrode) merupakan elektroda yang mudah pembuatannya, yaitu dengan cara me-lapiskan polimer, seperti polivinil kloroda (PVC) berisi ionofor, pada ka-wat konduktor (Pt, Ag, Cu), (Cattral, 1997 dan Wang, 2000). Pada pembua-tan ESI dibutuhkan membran yang berisi ionofor (ligan pengkompleks). Membran ESI yang baik harus memiliki komposisi bahan-bahan aktif yang dapat berikatan dengan analit pada permukaan membran - larutan sampel dengan reaksi yang cepat,
re-versibel dan selektif (Buhlmaa, Pretsch, Bakker, 1998).
Senyawa 37, 38, 39, 40, 41, 42-heksakis(karboksimetoksi)-5, 11, 17, 23, 29, 35-heksakis (tertierbutil) kaliks[n]arena (Selanjutnya dalam penelitian ini disebut sebagai senyawa
karboksimetoksi tertierbutil kaliks[n]arena) merupakan ligan baru
yang dapat digunakan untuk ek-straksi tanah jarang (Hamami, 2001). Berdasar kemampuannya tersebut, maka dalam penelitian ini senyawa kaliks[n]arena akan digunakan seba-gai ionofor dalam pada ESI-La3+.
Suy-anta (2006) telah pula meneliti peng-gunaan senyawa lariat 1,10-diaza-18-crown-6 sebagai ionofor pada
ESI-La3+, yang memberikan jangkau kerja
10-5-10-1 M (Suyanta, 2006).
Selektivitas pengompleksan ion logam dan kaliks[n]arena tergantung pada struktur molekulnya, seperti derajat kondensasi[n] yang berdam-pak pada ukuran rongga (cavity), kon-formasi molekul, sifat gugus fungsi yang terikat pada oksigen fenol serta substituen atas dari cincin (Ikeda, dan Shinkai, 1997). Oleh karena itu, dalam penelitian ini akan dipelajari karakteristik potensiometri senyawa kaliks[n]arena dengan derajat kon-densasi [n] 4, 6 dan 8 terhadap ion
La3+ dengan pembuatan elektroda
se-lektif ion (ESI).
METODE PENELITIAN
Bahan kimia yang digunakan dalam penelitian ini antara lain seny-awa karboksimetoksi tertierbutil kaliks[4]arena, karboksimetoksi ter-tierbutil kaliks[6]arena, karboksime-toksi tertierbutil kaliks[8]arena yang diperoleh dari Universitas Louise Pas-teur, Prancis, kalium tetrakis (4-klorofenil)borat (KTCPB) (fluka), poli-vinil klorida (PVC) (fluka), 2-nitrofenil oktil eter (1-nitro-2-oktilobenzena) (NPOE) (fluka), tetrahidrofuran (THF), kawat platina diameter 0,5 mm den-gan panjang 10 cm, larutan HCl 0,1
M, larutan NaOH 0,1 M dan akuademineralisata. Sedangkan sampel berupa lantanum(III) klorida
heptahidrat (LaCl3.7H2O) merk
UNIVAR.
Alat yang digunakan dalam penelitian ini adalah seperangkat peralatan potensiometer merk Cyberscan yang terdiri dari elektroda pembanding Ag/AgCl, pengaduk magnetik, pH meter merk Mettler, kabel RG-58 koaksial dan alat-alat gelas yang biasa digunakan di laboratorium kimia analitik.
Pada penelitian ini membran dibuat dengan mencampur bahan aktif ionofor kaliks[n]arena, plasticizer
NPOE, anionic site KTCPB dan matrik
dasar PVC dalam pelarut THF dengan komposisi yang berbeda-beda. Hal ini bertujuan untuk mendapatkan kom-posisi optimal membran yang dapat memberikan potensial optimum. Kaliks[n]arena yang digunakan yaitu kaliks[4]arena, kaliks[6]arena dan kaliks[8]arena. Perbedaan rongga di antara ketiga jenis ionofor tersebut diharapkan dapat memberikan respon potensial yang berbeda terhadap ion La3+. Sehingga dapat ditentukan jenis
ionofor mana yang paling tepat dalam pengukuran ion La3+.
Badan elektroda dibuat dari ka-wat platina dengan diameter 0,5 mm sepanjang 10 cm. Pada kedua ujung atas dan bawah sepanjang 1,5 cm di-biarkan terbuka, sedang bagian lain-nya ditutup dengan plastik polietilen atau kaca. Konstruksi badan elek-troda dapat dilihat pada Gambar 1.
Gambar 1.
Konstruksi badan elektroda kawat terlapis
Bagian ujung bawah kawat platina kemudian dicelupkan pada membran polimer yang telah dibuat. Membran yang telah menempel pada elektroda tersebut selanjutnya diker-ingkan dalam oven pada suhu 50ºC selama 12 jam dan kemudian diren-dam dalam larutan La3+ 0,1 M selama
12 jam agar ion La3+ dapat menempel
secara tetap dalam komponen mem-bran. Elektroda selektif ion yang telah diprekondisikan disimpan ditempat kering dan setiap akan digunakan ha-rus dilakukan prekondisi lagi dengan
merendamnya dalam larutan La3+
minimal 1 jam (Atikah, 1994).
HASIL DAN PEMBAHASAN
Penentuan ionofor dan komposisi mem-bran
Membran yang digunakan dalam
pembuatan ESI-La3+ tipe kawat
terlapis disini terdiri dari ionofor, anionic site, matriks dasar, plasticizer dan pelarut. Ionofor yang digunakan merupakan hasil optimasi dari kaliks[4]arena, kaliks[6]arena dan kaliks[8]arena yang memiliki ukuran rongga hampir sama dengan ukuran logam-logam tanah jarang. Sedangkan untuk anionic site dipilih KTCPB. Hal ini dikarenakan KTCPB memiliki ru-mus molekul yang besar, sehingga dapat mencegah masuknya anion-anion lain yang tidak diharapkan ke dalam membran selama pengukuran dan tidak mempengaruhi respon po-tensial yang diberikan analit.
Kedua zat aktif tersebut ke-mudian diamobilkan dalam matrik PVC dan pelarut THF dengan
penam-bahan plasticizer (zat pemlastis)
NPOE. Pada umumnya penggunaan plasticizer dalam ESI bertujuan untuk
menurunkan Tg dari PVC, sehingga
dapat meningkatkan kekuatan dan fleksibilitas dan memperpanjang usia pemakaian (Laksimanarayanaiah, 1974).
Membran merupakan bagian ter-penting dari suatu elektroda selektif
ion (ESI) yang dapat memberikan re-spon potensial (emf) dan selektivitas terhadap suatu analit tertentu [13]. Untuk itu perlu diketahui ionofor yang paling baik dan berapa kom-posisi optimal untuk pembuatan membran ESI La3+. Penentuan ionofor
dan komposisi optimal membran dila-kukan dengan membuat 5 (lima) vari-asi komposisi PVC, NPOE, KTCPB dan kaliks[n]arena pada membran, dengan nilai n adalah 4, 6 dan 8. Kelima variasi tersebut selanjutnya digunakan dalam pembuatan elektroda dan disebut A1, A2, E-A3, E-A4 dan E-A5 untuk ionofor kaliks[4]arena. B1, B2, B3, E-B4 dan E-B5 untuk ionofor kaliks[6]arena. C1, C2, C3,
E-C4 dan E-C5 untuk ionofor kaliks[8]arena.
Berdasarkan beberapa penelitian yang telah dilakukan, komposisi PVC dan NPOE optimal yaitu pada perbandingan 30%:60%. Sehingga di sini komposisi PVC dan NPOE dibuat tetap yaitu 45 mg dan 90 mg. Dengan tetapnya komposisi PVC dan NPOE, maka respon potensial hanya ditentu-kan oleh ionofor dan anionic site.
Kelima elektroda kemudian digunakan dalam pengukuran poten-sial La3+ dengan konsentrasi 10-8, 10 -7, 10-6, 10-5, 10-4, 10-3, 10-2 dan 10-1
M. Dari pengukuran diketahui bahwa faktor Nernst dan linieritas yang dihasilkan tiap elektroda menunjuk-kan perbedaan yang signifimenunjuk-kan (Tabel 1 s.d 3).
Tabel 1. Pengaruh ionofor kaliks[4]arena dan komposisi membran terhadap potensial La3+
Elektroda (MG) PVC NPOE (MG) KTCPB (MG) Kaliks[4] Arena
(MG) Faktor nernst R E-A1 45 90 5 - 16,48 0,9876 E-A2 45 90 5 5 23,61 0,9997 E-A3 45 90 - 5 19,14 0,9953 E-A4 45 90 5 10 22,505 0,9961 E-A5 45 90 10 5 21,02 0,9993
Tabel 2. Pengaruh ionofor kaliks[6]arena dan komposisi membran terhadap potensial La3+
Elektroda (MG) PVC NPOE (MG) KTCPB (MG) Kaliks[6] Arena
(MG) Faktor nernst R E-B1 45 90 5 - 16,268 0,9480 E-B2 45 90 5 5 14,840 0,8912 E-B3 45 90 - 5 17,704 0,9590 E-B4 45 90 5 10 20,079 0,9980 E-B5 45 90 10 5 19,589 0,9958
Tabel 3. Pengaruh ionofor kaliks[8]arena dan komposisi membran terhadap potensial La3+
Elektroda (MG) PVC NPOE (MG) KTCPB (MG) Kaliks[8] Arena
(MG) Faktor nernst R E-C1 45 90 5 - 23,36 0,9972 E-C2 45 90 5 5 22,78 0,9945 E-C3 45 90 - 5 25 0,9766 E-C4 45 90 5 10 21,13 0,9947 E-C5 45 90 10 5 22,33 0,9999
Selektivitas suatu alat/metode dapat dilihat dari nilai faktor Nernst. Untuk kation trivalent, nilai faktor Nernst yang mendekati 19,7 mem-berikan selektivitas yang tinggi terha-dap suatu analit. Kurva Nernstian ±1-2mV dari nilai teori, super-Nernstian > Nernstian: 0,059/n (±1-2mV)> sub-Nernstian. Nilai faktor Nernst di luar nilai tersebut menunjukkan bahwa elektroda tidak cukup baik dalam merespon La3+. Hal tersebut tidak
se-lalu menunjukkan kejelekan elek-troda, tetapi lebih bermakna sebagai kepekaan kinerja dan selektivitas suatu elektroda.
Sedangkan untuk alat/metode baru, hal yang harus diperhatikan adalah linieritasnya. Linieritas suatu fungsi dapat menunjukkan sensitivitas alat/metode terhadap analit. Semakin linier suatu fungsi menunjukkan bahwa dengan penam-bahan sedikit konsentrasi memberi-kan respon potensial yang signifimemberi-kan. Linieritas ditunjukkan dengan harga koefisien korelasi (r). Dari kelima elektroda, E2-E5 memiliki linieritas yang mendekati 1. Sehingga keempat elektroda memiliki sensitifitas yang tinggi.
Dengan memperhatikan selek-tivitas dan sensiselek-tivitas alat/metode, maka komposisi membran kelima, yaitu PVC (45 mg), NPOE (90 mg), KTCPB (10 mg) dan kaliks[4]arena (5 mg) merupakan komposisi yang paling
tepat untuk ESI La3+ tipe kawat
terlapis. Tetapi E-3 dan E-4 juga dapat digunakan karena nilai faktor Nernst dan linieritas keduanya masih bagus.
Hal yang menarik pada penelitian ini ditunjukkan pada E-3. Tanpa menggunakan KTCPB (anionic site), faktor Nernst yang dihasilkan lebih bagus dari pada E-4 yaitu dengan perbandingan KTCPB dan kaliks[4]arena sebesar 1: 2. Hal ini
dikarenakan kaliks[4]arena merupakan suatu anion, sehingga
selain berfungsi sebagai ionofor juga dapat berperan sebagai anionic site. Optimasi pH
Optimasi pH dilakukan dengan tujuan untuk mengetahui apakah kondisi pH mempengaruhi kinerja membran sebagai sensor kimia.
Un-tuk mengkondisikan larutan La3+
pada suasana pH tersebut, digunakan larutan HCl dan NaOH. Kemudian di-lakukan pengukuran beda potensial pada larutan LaCl3 konsentrasi 10-1 M
dan konsentrasi 10-3 M dengan
ren-tang pH 1-9 sedangkan pH 10 tidak dilakukan pengukuran, hal ini di-karenakan pada larutan sampel pH 10 dihasilkan endapan putih. Kurva hubungan antara pH larutan dan potensial (EMF) seperti pada Gambar 2 s.d. 5. Dari gambar tersebut terlihat bahwa senyawa kaliks [4] dan [8] arena dapat digunakan sebagai sensor kimia pada rentang pH 3-7, namun pada senyawa kaliks[6]arena dapat digunakan sebagai sensor kimia pada rentang pH 4-8. Kaliks[4] arena 0 20 40 60 80 100 120 0 2 4 6 8 10 pH EM F ( m V) Gambar 2.
Kurva hubungan antara beda potensial
(EMF) dengan pH larutan La3+
menggunakan ESI-La3+ dengan ionofor
Kaliks[6] arena -100 -80 -60 -40 -20 0 20 40 60 80 0 1 2 3 4 5 6 7 8 9 10 pH EM F ( m V) 10-1 M 10-3 M Gambar 3.
Kurva hubungan antara beda potensial
(EMF) dengan pH larutan La3+
mengguna-kan ESI-La3+ dengan ionofor kaliks[6]arena
Kaliks[8] arena -100 -80 -60 -40 -20 0 20 0 2 4 6 8 10 pH EM F ( m V) Gambar 4.
Kurva hubungan antara beda potensial
(EMF) dengan pH larutan La3+
menggunakan ESI-La3+ dengan ionofor
kaliks[8]arena
Dari Gambar 2 s.d 4 dapat diketahui bahwa suasana pH sangat
berpengaruh terhadap potensial La3+
yang dihasilkan. Hal ini terjadi karena
adanya pengaruh ion H+ dalam
kesetimbangan kaliks[n]arena. Pada
pH rendah (1-3), konsentrasi ion H+
yang besar sangat berpengaruh terhadap respon potensial. Sedangkan pada pH 4-7 atau bahkan sampai
pada pH 8 adanya ion H+ cenderung
tidak berpengaruh, sehingga potensial yang dihasilkan relatif konstan. Tetapi pada pH di atas 8, potensial kembali tidak stabil. Hal ini terjadi karena
pada pH tersebut La3+ sudah mulai
membentuk endapan hidroksidanya,
sehingga jumlah La3+ dalam larutan
berkurang. Selain itu dimungkinkan karena adanya pengaruh potensial
Na+, sehingga mengganggu
pengukuran.
Uji Kinerja Elektroda Selektif Ion La3+ Tipe Kawat Terlapis
Jangkauan pengukuran
Penentuan jangkauan
pengu-kuran ESI-La3+ dilakukan pada
elek-troda ke 4 dan 5 untuk masing-masing ionofor. Semakin lebar jang-kauan pengukuran, maka elektroda dikatakan baik karena dapat
mem-berikan respon potensial La3+ pada
jangkauan konsentrasi yang luas.
Berdasarkan Tabel 4, ESI La3+
dengan membran kaliks[n]arena memberikan linieritas dan faktor Nernst yang baik (Nerntian). Untuk ESI bermembran kaliks[4] konsentrasi yang memberikan hubungan yang linier dan memenuhi Hukum Nerst adalah 10-5- 10-1 M, kaliks [6] arena
10-7 – 10-1 M dan [8]arena 10-5- 10-1
M. Dengan demikian kalik[6] arena
memberikan respon terhadap ion La3+
dengan jangkau kerja paling luas. Batas deteksi
Penentuan batas deteksi bertujuan untuk mengetahui batas terendah konsentrasi suatu zat yang masih dapat ditentukan dengan metode yang digunakan secara tepat dan teliti. Pada penelitian ini, penentuan batas deteksi diperoleh dari data pengukuran potensial
larutan standar La3+ dengan rentang
konsentrasi (10-8–10-1) M. Nilai batas
deteksi diperoleh dengan membuat titik potong antara garis linier dengan garis non linier dari kurva hubungan potensial dengan log konsentrasi La3+
122
Tabel 4. Perolehan faktor Nernst elektroda 4 dan 5 untuk kaliks[n]arena pada berbagai
rentang konsentrasi La3+
Elektroda Konsentrasi (M) Faktor Nernst r
10-7 - 10-1 14,721 0,9205 10-6 - 10-1 18,567 0,9679 E-A4 10-5 - 10-1 22,505 0,9961 10-7 - 10-1 15,48 0,9613 10-6 - 10-1 18,3 0,9851 Kaliks[4] arena E-A5 10-5 - 10-1 21,02 0,9993 10-7 - 10-1 20,079 0,9980 10-6 - 10-1 20,723 0,9996 E-B4 10-5 - 10-1 20,690 0,9994 10-7 - 10-1 19,589 0,9958 10-6 - 10-1 20,145 0,9996 Kaliks[6] arena E-B5 10-5 - 10-1 21,066 0,9974 10-7 - 10-1 16,843 0,9576 10-6 - 10-1 18,783 0,9723 E-C4 10-5 - 10-1 21,13 0,9895 10-7 - 10-1 18,282 0,9721 10-6 - 10-1 20,063 0,9832 Kaliks[8] arena E-C5 10-5 - 10-1 22,33 0,9999
Berdasarkan analisis perhitungan diperoleh batas deteksi ESI La3+ tipe
kawat terlapis membran kaliks[4], [6] dan [8]arena masing-masing sebesar
8,9125 x 10-6 M, 5,807.10-8 M dan
9,39 x 10-6 M dan data selengkapnya
dapat dilihat pada Lampiran 3. Dengan batas deteksi yang sangat kecil menunjukkan bahwa penggunaan ESI-La tipe kawat terlapis sangat baik.
Gambar 5.
Gambar kurva standar kaliks[n]arena
Akurasi
Persen akurasi ditentukan untuk
mengetahui keakuratan ESI-La3+,
yaitu dengan menentukan
perbandingan antara konsentrasi La3+
yang diperoleh dari pengukuran
menggunakan ESI-La3+ dengan
konsentrasi La3+ sebenarnya. Pada
penelitian ini, data akurasi diperoleh melalui pengulangan pengukuran
potensial untuk larutan La3+ pada
konsentrasi (10-1, 10-3, dan 10-5) M.
Berdasarkan analisis perhitungan didapatkan nilai persen akurasi sesuai dengan Tabel 5.
Melalui tabel tersebut terlihat bahwa ESI tipe kawat terlapis dengan ionofor kaliks[n]arena menghasilkan nilai persen akurasi yang baik apabila digunakan untuk mengukur kadar pada konsentrasi kecil, yaitu 10-5 M,
sedangkan untuk konsentrasi besar relatif kurang sesuai. Dengan melihat perbandingan perolehan potensial pada awal dan pengulangannya kembali, dapat diketahui bahwa dengan perbedaan respon potensial yang tidak terlalu jauh akan menghasilkan persen perolehan kembali yang kurang sesuai.
Tabel 5. Persen akurasi pada konsentrasi La3+ (10-1, 10-3, dan 10-5) M untuk kaliks[n]arena
Seharusnya Terukur
Ionofor Konsentrasi
(M) Potensial (mV) Potensial (mV) Konsentrasi (M) % akurasi
10-5 -205 -204 1,0023 x 10-5 100,23% 10-3 -159,9 -163 8,9433 x 10-4 89,433% Kaliks[4] arena 10-1 -121 -122 7,9799 x 10-2 79,799% 10-5 -160,0 -155,1 1,028.10-5 102,8% 10-3 -114,3 -120,3 6,683.10-4 66,8% Kaliks[6] arena 10-1 -79,2 –79,8 8,6.10-2 86% 10-5 -89,8 -88,0 1,68 x 10-5 168% 10-3 -58,8 -60,3 7,97 x 10-4 79,7% Kaliks[8] arena 10-1 -23,8 -22,6 1,5 x 10-1 150%
Pada kenyataannya, banyak elek-troda komesial menghasilkan nilai akurasi yang tidak memenuhi kriteria dari akurasi. Hal ini disebabkan selisih 0.1 mV dari beda potensial yang terukur pertama dan kedua den-gan kondisi dan perlakuan sama menghasilkan perbedaan konsentrasi yang sangat besar. Sehingga dapat disimpulkan bahwa ESI ini dapat digunakan untuk mengukur konsen-trasi La3+ secara akurat karena
perbe-daan beda potensial yang terukur ti-dak melebihi 7 mV.
Presisi
Presisi atau keterulangan merupakan keseksamaan metode jika dilakukan oleh analis yang sama dan dalam interval waktu yang pendek. Presisi dilakukan untuk menilai ketepatan metode analisis dengan ketelitiannya. Kriteria presisi
dinyatakan dengan koefisien variasi atau simpangan baku relatif yaitu sebesar 2% atau kurang (Harahap, dkk, 2006).
Pada penelitian ini, presisi diperoleh dari replikasi pengukuran
potensial La3+menggunakan elektroda
pada konsentrasi 10-8-10-1 M
sebanyak 3 (tiga) kali dalam satu waktu. Presisi dinyatakan dengan nilai koefisien variasi (KV). Nilai presisi menyatakan derajat kedapatulangan (repeatability) dimana repeatability baik jika%KV kecil (≤
2%). Tidak hanya dipengaruhi oleh elektroda, pengukuran potensial juga dipengaruhi oleh instrumen yang digunakan. Dalam penelitian ini, po-tensiometer yang digunakan mem-berikan sinyal yang kurang stabil. Perolehan presisi untuk kaliks[n]arena dapat dilihat pada Tabel 6.
Tabel 6. Perolehan Presisi Untuk Kaliks[n]arena
Jenis ionofor Range konsentrasi (M) % KV
Kaliks[4]arena 10-5 – 10-1 1,11 – 10,55
Kaliks[6]arena 10-7 – 10-1 0,39 – 5,5
Kaliks[8]arena 10-5 – 10-1 1,44 – 4,77
Melalui Tabel 6 dapat di simpulkan bahwa ketiga senyawa Kaliks[n]arena memiliki presisi lebih dari 2%.
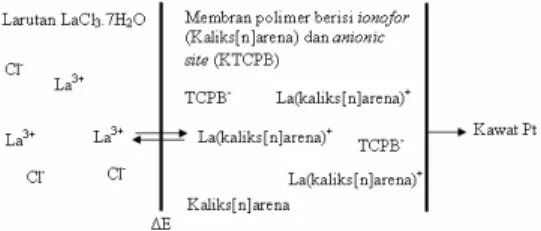
Mekanisme Timbulnya Beda Potensial Pada metode ESI La tipe kawat terlapis, di dalam membran terjadi
kesetimbangan antara La3+ dengan
kaliks[n]arena. Sehingga potensial sel yang terukur merupakan beda potensial yang diakibatkan oleh
adanya perpindahan La3+ melalui
antarfasa. Gambar 6 menunjukkan bahwa dengan membran yang telah
membran dianggap tetap dan besarnya potensial hanya ditentukan
oleh potensial La3+ dari larutan
sampel.
Gambar 6. Skema timbulnya beda potensial
Peranan anionic site pada
membran juga ditunjukkan pada Gambar 6. Anionic site digunakan pada membran untuk menghalangi masuknya anion (counter ion) yang
mungkin ada bersama La3+, yaitu
pada sampel. Sehingga potensial yang
terbaca hanya potensial La3+. Oleh
karena itu, anionic site harus berupa anion yang memiliki rumus molekul besar.
SIMPULAN DAN SARAN Simpulan
Berdasarkan hasil penelitian dan pembahasan dapat disimpulkan seba-gai berikut. Derajat kondensasi ber-pengaruh terhadap respon potencial. Senyawa karboksimetoksi tertierbutil kaliks[6]arena memberikan respon yang terbaik terhadap ion La3+ dengan
komposisi membran 45 mg PVC, 90 mg NPOE, 10 mg KTCPB dan 5 mg kaliks[6] arena, faktor Nernst 19,588 mV/dekade, jangkau pengukuran 10-7–
10-1 M, batas deteksi sebesar 5,807.10-8
M, akurasi 102,8% untuk pengukuran
La3+ 10-5 M serta presisi dengan
koefiasien variasi 0,39 – 5,5%.
Saran
Perlu dilakukan penelitian
penen-tuan koefisien selektivitas ESI-La3+
dengan mengujinya terhadap penga-ruh adanya ion logam lain, utamanya ion logam tanah jarang.
DAFTAR PUSTAKA
Atikah, 1994. Pembuatan dan Karak-terisasi Elektroda Selektif Ion Nitrat tipe Kawat Terlapis, Tesis, Institut Teknologi Bandung, 196p.
Baily, P.L., 1976. Analysis with Ion-Selective Electrodes, Heyden Interna-tional, London.
Buck, Richard. P., and Linder, Ernö., 1994, Recommendations for Nomen-clature of Ion-Selective Electrodes, Pure and Appl. Chem., Vol. 68, no. 12, pp. 2527-2536
Buhlmaa, P., Pretsch, E., Bakker, E., 1998. Carier-based Ion Selective Elec-trodes and Bulk Optodes (2). Iono-phores for Potentiometric and Optical Sensor, Chem. Review, 98, 1593-1687 Cattral, R.W, 1997. Chemical Sensors,
Zeneca, Oxford Science Publication, Oxford,
Cotton F. Albert, Wilkinson, G., Gaus, P.L,
1987. Basic Inorganic Chemistry,
Sec-ond Edition, John Wiley and Sons Inc, USA
Hamami, 2001. Ekstraksi Kompleks Sm, Er dan Yb-37, 38, 39, 40, 41, 42-Heksakis (karboksimetoksi)-5, 11, 17, 23, 29, 35-heksakis(tert-butil)kaliks [6]arena dalam Dikloroetana dan Kloroform, Tesis, Universitas Indone-sis.
Harahap, Yahdiana, dkk, 2006, Analisa Glimepirida dalam Plasma Tikus, Majalah Ilmu Kefarmasin, Vol. III, No.1, April 2006, 22 – 37, UI, Jakarta Ikeda, A., dan Shinkai, S., 1997. Chem.
Rev., 97, 1713-1734
Laksimanarayanaiah, 1974, Membrane electrode, Academic Press, New York Skoog, D.A., and Leary, J.J., 1998.
Princi-ples of Instrumental Analysis, 4th Ed., A Harcourt Brace Jovanovich College Publisher, United States of America
Suyanta, 2006. Elektroda Selektif Ion-La(III) dengan Ionofor Lariat 1,10-diaza-18-crown-6, Disertasi, Institut Teknologi Bandung, 139p
Wang, J., 2000. Analytical
Electroche-mistry, 2nd ed., John Wiley and Sons,
![Tabel 1. Pengaruh ionofor kaliks[4]arena dan komposisi membran terhadap potensial La 3+](https://thumb-ap.123doks.com/thumbv2/123dok/2397728.2749450/4.918.177.762.571.690/tabel-pengaruh-ionofor-kaliks-arena-komposisi-membran-potensial.webp)
![Tabel 4. Perolehan faktor Nernst elektroda 4 dan 5 untuk kaliks[n]arena pada berbagai rentang konsentrasi La 3+](https://thumb-ap.123doks.com/thumbv2/123dok/2397728.2749450/7.918.161.740.176.499/tabel-perolehan-faktor-nernst-elektroda-berbagai-rentang-konsentrasi.webp)
![Tabel 5. Persen akurasi pada konsentrasi La 3+ (10 -1 , 10 -3 , dan 10 -5 ) M untuk kaliks[n]arena Seharusnya Terukur Ionofor Konsentrasi (M) Potensial (mV) Potensial (mV) Konsentrasi (M) % akurasi 10 -5 -205 -204 1,0023 x 10-5 100,23% 10](https://thumb-ap.123doks.com/thumbv2/123dok/2397728.2749450/8.918.181.760.166.344/persen-konsentrasi-terukur-ionofor-konsentrasi-potensial-potensial-konsentrasi.webp)