7
KALSIUM ALGINAT SEBAGAI PENDUKUNG AMOBILISASI
L-ASPARAGINASE DARI BAWANG PUTIH
(Allium sativum)
Nindy Kusumaningtias
*, Nies Suci Mulyani dan Purbowatiningrum Ria
Sarjono
Laboratorium Biokimia Jurusan Kimia Fakultas Sains dan Matematika Universitas Diponegoro, Semarang, Indonesia
*Keperluan korespondensi, telp: 081226283898, email: nindykusuma94@gmail.com
Received: July 22 , 2016 Accepted: August 15, 2016 Online Published: August 31, 2016
ABSTRAK
Enzim Asparaginase adalah enzim yang mampu menghidrolisis asam amino L-Asparagin menjadi L-Aspartat dan amonia. Dalam Industri makanan, L-asparagin merupakan salah satu asam amino yang mampu bereaksi dengan suatu gugus karbonil dalam bahan makanan yang dipanaskan. Reaksi tersebut berjalan melalui jalur reaksi Maillard membentuk senyawa akrilamida yang bersifat karsinogenik. Tujuan dari penelitian ini adalah untuk mendapatkan enzim Asparaginase serta memperoleh karakter suhu dan pH optimum L-Asparaginase dari bawang putih (Allium sativum) dalam bentuk enzim bebas maupun enzim amobil dengan pendukung kalsium alginat. Tahap pertama penelitian dimulai dari isolasi L-Asparaginase dari bawang putih dan pemurnian melalui pengendapan dengan amonium sulfat dan dialisis. Tahap kedua melakukan uji aktivitas spesifik dan karakterisasi L-Asparaginase dengan cara menghitung jumlah produk amonia yang terbentuk menggunakan pereaksi Nessler dan mengukur kadar protein total dengan metode Lowry. Tahap selanjutnya yaitu amobilisasi L-Asparaginase dalam matriks alginat dengan metode penjebakan. Tahap terakhir dari penelitian ini yaitu karakterisasi L-Asparaginase amobil. Hasil penelitian ini menunjukkan aktivitas spesifik tertinggi L-Asparaginase dari bawang putih ada pada fraksi 5 (80-100%) yaitu 1423,0248 U/mg protein. Kondisi optimum L-Asparaginase bebas yaitu pada suhu 37°C, pH 8,6. Enzim LAsparaginase dapat diamobil dalam matriks kalsium alginat dengan aktivitas spesifiik sebesar 1367,6741 U/mg protein yang diukur pada kondisi optimumnya yaitu pada suhu 42°C, pH 8,6.
Kata Kunci: Allium sativum, L-Asparaginase, Amobilisasi, Kalsium Alginat
ABSTRACT
Enzyme L-asparaginase hydrolizes L-asparagine into L-aspartate and ammonia. In the food industry L-asparagine in one of amino acid that is reactable with a carbonyl group in heated foodstuffs. The reaction comes through Maillard reactions to form carcinogenic compound, acrylamide. This study aims to obtain the enzyme L-Asparaginase from garlic (Allium sativum) as free enzymes and immobilized enzymes using calcium alginate supporters, and as well as its characterizations of temperature and pH optimum. This research was conducted into four steps. First step: isolation of L-Asparaginase from garlic and purification by precipitation with ammonium sulfate and dialysis. Second step: determination of specific activity of the purified L-Asparaginase based on ammonia product detected by Nessler reagent, protein concentration were measured using Lowry methods. The third step: immobilization of L-Asparaginase into the alginate matrix with trapping methods. The last step of this research is characterization of L-Asparaginase immobilized. The results showed that the highest specific activity of L-Asparaginase of garlic were found in fraction 5 (80-100%), 1423.0248 U/mg protein. Optimum condition of L-Asparaginase as free form is at a temperature of 37 °C and pH 8.6. That enzymes can be ammobilized into calcium alginate matrix and hahe spesifiik activities of 1367.6741 U/mg protein at a temperature of 42 ° C and pH 8.6.
PENDAHULUAN
Enzim L-Asparaginase (L-Asparagin
amidohidrolase, E.C.3.5.1.1) merupakan
enzim yang mampu mengkatalisis reaksi
hidrolisis Asparagin menjadi asam
L-Aspartat dan amonia [5]. Enzim
L-Asparaginase juga terbukti dapat
menurunkan kadar akrilamida di dalam
makanan. Enzim L-Asparaginase dapat
mencegah pembentukan akrilamida dengan
mengkonversi asam amino L-Asparagin
sebagai prekusornya menjadi bentuk asam
amino lain yaitu asam L-Aspartat yang
umum terdapat dalam makanan [1].
Akrilamida bersifat karsinogenik pada
manusia. Akrilamida dapat muncul pada
makanan apabila dipanaskan sebagai
konsekuensi terjadinya reaksi antara
L-Asparagin dan sumber karbonil melalui
reaksi Maillard [1]. Beberapa penelitian
membuktikan bahwa pre-treatment
menggunakan enzim L-Asparaginase
terhadap kentang dan dough efektif
mereduksi akrilamida tanpa merusak
penampilan dan rasa dari hasil akhir produk
makanan [3]. Efektivitas enzim
L-Asparaginase dalam mereduksi akrilamida
juga telah teruji dan dijadikan beberapa
paten yang berbeda dalam pengolahan
makanan seperti camilan, keripik, dough, dll
[4].
Selama ini, bawang putih (Allium
sativum) dimanfaatkan sebagai bumbu
penyedap makanan dan diekstrak kemudian
dikapsulkan sebagai suplemen untuk
memelihara kesehatan tubuh. Di sisi lain,
bawang putih juga mengandung enzim
L-Asparaginase [7]. Untuk itu, padapenelitian
ini digunakan bawang putih sebagai sumber
enzim L-Asparaginase. Penelitian yang
dilakukan Rizki dkk (2009) menunjukkan
bahwa bawang putih mengandung enzim
L-Asparaginase dengan aktivitas spesifik
sebesar 506,158 U/mg protein pada suhu
optimum 37°C, dan pH optimum 8,6.
Aktivitas spesifik ini dinilai cukup tinggi untuk
kemudian diteliti dan dilakukan amobilisasi
agar dapat dilakukan pemakaian secara
berulang.
Amobilisasi dilakukan dengan matriks
alginat karena sifatnya yang tidak beracun,
mekanisme kestabilan dan porositasnya
tinggi, memerlukan prosedur yang
sederhana untuk ammobilisasi, dan
harganya murah untuk diaplikasikan dalam
industri makanan atau farmasi [2].
Dari uraian diatas, penelitian ini
bertujuan untuk memperoleh enzim
L-Asparaginase baik bebas maupun amobil
dan memberikan informasi karakter enzim
L-Asparaginase bebas dan amobil dari
bawang putih pada matriks kalsium alginat.
METODE PENELITIAN
Bahan dan Alat
Bahan: Bawang putih, bufer
tris-hidroksimetil aminometan p.a., amonium
sulfat p.a., L-asparagin p.a., Trichloro
acetate (TCA) p.a., Bovine serum albumine
(BSA) p.a., Follin ciocalteau p.a., natrium
alginat, kalsium klorida p.a., barium klorida
p.a., akuades, natrium karbonat p.a., kalium
natrium tartrat p.a., tembaga sulfat p.a.,
reagen Nessler (kalium iodida dan raksa (II)
iodida).
Alat: Sentrifugasi (Centrific-228),
spektrofotometer UV-Vis (Shimadzu),
neraca analitik (kern 870), magnetic stirer
(Quart), kulkas, membran selofan, kertas
saring, gunting, tali, botol semprot,
aluminium foil, plastic wrap, dan alat-alat
gelas untuk analisa.
Cara Kerja
1. Isolasi Enzim
Sampel penelitian berupa 250 g umbi
bawang putih Allium sativum yang ditumbuk
kemudian ditambahkan dengan 125 mL 0,2
M bufer tris-hidroksimetil aminometan pH
8,6 dan dihomogenkan. Homogenat yang
diperoleh selanjutnya di didiamkan 1-2 jam
pada suhu 5oC kemudian disaring dan
filtratnya disentrifugasi. Supernatan yang
diperoleh merupakan ekstrak kasar enzim
(EK).
2. Pemurnian Enzim
2.1 Fraksinasi Amonium Sulfat
Pengendapan dengan garam
amonium sulfat dilakukan untuk memurnikan
enzim (enzim kasar) dengan prinsip
pengendapan. Amonium sulfat ditimbang
sesuai fraksi yang dikehendaki 0-20% (dari
tabel fraksinasi) dimasukkan dalam gelas
beaker berisi ekstrak kasar sambil diaduk
dengan magnetic stirer dalam keadaan
dingin. Campuran didiamkan semalam
dalam keadaan dingin kemudian
disentrifugasi dengan kecepatan 5000 rpm
selama 15 menit sehingga diperoleh
endapan dan filtrat untuk fraksi 0-20% (F1).
Endapan dipisahkan dan disuspensi dengan
0,2 M bufer Tris-hidroksimetil aminometan
pH 8,6. Endapan tersebut merupakan fraksi
0-20%. Filtrat diperlakukan sama dengan
diatas sehingga diperoleh fraksi-fraksi
protein dengan tingkat kejenuhan 20-40%,
40-60%, 60-80%, 80-100%.
2.2 Dialisis Enzim
Dialisis dilakukan dengan membran
selofan.Selofan yang telah berisi enzim
direndam dalam bufer tris-hidroksimetil
aminometan 0,002 M pH 8,6 dalam keadaan
dingin. Bufer diaduk dengan magnetic stirrer
dan dilakukan pengujian kandungan
amonium sulfatnya setiap 2 jam dengan
penambahan BaCl2. Dialisis dihentikan jika
hasil pengujian tidak lagi menghasilkan
endapan putih.
2.3 Penentuan Aktivitas Enzim
Larutan substrat 1 mL L-asparagin
ditambahkan dengan 0,05 mL enzim bebas
dan 2,5 bufer tris-hidroksimetil aminometan
0,2 M pH 8,6 diinkubasi pada suhu 37oC
selama 30 menit kemudian ditambahkan
larutan TCA 1,5 M sebanyak 1 mL dan
disentrifugasi pada kecepatan 5000 rpm
selama 15 menit untuk memisahkan
endapan. Filtrat diambil sebanyak 0,5 mL
lalu ditambah 4 mL akuades dan 1 mL
pereaksi Nessler. Campuran ini kemudian
diukur absorbansinya pada panjang
gelombang optimum (402 nm) dengan
spektrofotometer UV-Vis. Aktivitas enzim
ditentukan secara regresi linier terhadap
kurva standar amonium sulfat.
2.4 Penentuan Kadar Protein dengan
Metode Lowry
Sebanyak 9,8 mL larutan Na2CO3
ditambah 0,1 mL larutan kalium natrium
tartrat dan 0,1 mL larutan CuSO4 kemudian
dikocok perlahan. Campuran ini kemudian
ditambahkan 0,1 mL larutan ekstrak kasar
atau enzim (F1, F2, F3, F4 dan F5) dan
diinkubasi selama 10 menit pada suhu
kamar. Campuran ini ditambahkan 1 mL
folin-ciocalteau kemudian diinkubasi kembali
tersebut selanjutnya diukur absorbansinya
menggunakan spektrofotometer UV-Vis
pada panjang gelombang optimum BSA
(726 nm). Kadar protein ditentukan secara
regresi linier terhadap kurva standar BSA.
3. Karakterisasi Enzim
3.2 Penentuan Suhu Optimum
Larutan substrat L-Asparagin 1 mL,
ditambah 0,05 mL enzim dan 2,5 mL bufer
tris-hidroksimetil aminometan 0,2 M pH 8,6
dan diinkubasi selama 30 menit dengan
variasi suhu (27, 32, 37, 42, 47)°C. Tahap
selanjutnya ditambahkan larutan TCA 1,5 M
sebanyak 1 mL. Campuran ini diambil
sebanyak 0,5 mL lalu ditambahkan 4 mL
akuades dan 1 mL pereaksi Nessler.
Larutan ini kemudian diukur absorbansinya
pada panjang gelombang optimum (402 nm)
dengan spektrometer UV-Vis.
3.3 Penentuan pH Optimum
Larutan substrat L-Asparagin 1 mL,
ditambah 0,05 mL enzim dan 2,5 mL bufer
tris-hidroksimetil aminometan 0,2 M dengan
variasi pH (8,2; 8,4; 8,6; 8,8; 9,0) dan
diinkubasi pada suhu 37°C selama 30 menit.
Campuran ini ditambahkan larutan TCA 1,5
M sebanyak 1 mL. Larutan tersebut diambil
sebanyak 0,5 mL lalu ditambahkan 4 mL
akuades dan 1 mL pereaksi Nessler.
Campuran ini kemudian diukur
absorbansinya pada panjang gelombang
optimum (402 nm) dengan spektrometer
UV-Vis.
3.4 Amobilisasi Enzim
Pembuatan larutan Natrium Alginat
3%. Natrium alginat dilarutkan dalam bufer
tris-hidroksimetil aminometan 0,2 M pH 8,6
dalam keadaan panas dan diaduk hingga
homogen. Suhu diturunkan menjadi 37°C,
natrium alginat ditambahkan 0,1 mL enzim
sambil diaduk hingga homogen. Penetesan
dilakukan menggunakan pipet tetes ke
dalam larutan CaCl2 0,2 M dingin kemudian
diinkubasi selama 2 jam. Manik-manik enzim
yang telah terbentuk disaring menggunakan
kertas saring untuk dipisahkan dari larutan
kalsium klorida lalu dicuci menggunakan
akuades sebanyak 3 kali. Larutan kalsium
klorida ini selanjutnya digunakan untuk
mengukur kadar protein teramobil.
4. Karakterisasi Enzim Amobil
4.1 Penentuan Suhu Optimum
Enzim amobil ditambah larutan
substrat L-Asparagin sebanyak 1 mL dan
2,5 mL bufer tris-hidroksimetil aminometan
0,2 M pH 8,6 dan diinkubasi selama 30
menit dengan variasi suhu (27, 32, 37, 42,
47)°C. Campuran ini ditambahkan larutan
TCA 1,5 M sebanyak 1 mL. Larutan tersebut
diambil sebanyak 0,5 mL lalu ditambahkan 4
mL akuades dan 1 mL pereaksi Nessler.
Campuran ini kemudian diukur
absorbansinya pada panjang gelombang
optimum (402 nm) dengan spektrometer
UV-Vis.
4.2 Penentuan pH optimum
Enzim amobil ditambah larutan
substrat L-Asparagin sebanyak 1 mL,
ditambah 0,05 mL enzim dan 2,5 mL bufer
tris-hidroksimetil aminometan 0,2 M dengan
variasi pH (8,2; 8,4; 8,6; 8,8; 9,0) dan
diinkubasi selama 30 menit pada suuhu
37°C. Campuran ini ditambahkan larutan
TCA 1,5 M sebanyak 1 mL. Selanjutnya
filtrat diambil sebanyak 0,5 mL lalu
ditambahkan 4 mL akuades dan 1 mL
pereaksi Nessler. Campuran ini kemudian
gelombang optimum (402 nm) dengan
spektrometer UV-Vis.
4.3 Penentuan Kadar Protein Enzim
Amobil
Filtrat hasil rendaman (CaCl2) dan
larutan hasil pencucian (akuades) enzim
amobil diukur kadar proteinnya dengan
metode Lowry. Sebanyak 9,8 mL larutan
Na2CO3 ditambah 0,1 mL larutan kalium
natrium tartrat dan 0,1 mL larutan CuSO4
dikocok perlahan. Campuran ini kemudian
ditambahkan 1 mL filtrat dan diinkubasi
selama 10 menit pada suhu kamar.
Sebanyak 1 mL folin-ciocalteau
ditambahkan pada campuran tersebut
secara cepat dan diinkubasi pada suhu
kamar selama 30 menit. Larutan tersebut
diukur absorbansinya pada panjang
gelombang optimum BSA (726 nm)
kemudian ditentukan kadar protein yang
terserap dilakukan dengan menghitung
selisih antara kadar protein enzim bebas
dengan kadar protein filtrat.
HASIL DAN PEMBAHASAN
1. Isolasi dan Purifikasi L-Asparaginase
dari Bawang Putih.
Isolasi L-Asparaginase dilakukan
secara mekanik yaitu dengan mengekstrak
bawang putih melalui pemecahan jaringan
bawang putih.
Ekstrak kasar enzim merupakan
campuran protein enzim dan protein non
enzim yang diperoleh dari proses ekstraksi
bawang putih. Untuk memperoleh enzim
L-Asparaginase dengan tingkat kemurnian
yang tinggi maka perlu dilakukan pemurnian
terhadap ekstrak kasar. Pemurnian yang
dilakukan adalah dengan pengendapan
protein menggunakan garam amonium
sulfat, sentrifugasi dan dialisis.
Ammonium sulfat lebih sering
digunakan karena memiliki beberapa
kelebihan dibandingkan garam-garam yang
lain, yaitu mempunyai kelarutan yang tinggi,
tidak mempengaruhi aktivitas enzim,
mempunyai daya pengendapan yang efektif,
mempunyai efek penstabil terhadap
kebanyakan enzim, dapat digunakan pada
berbagai pH dan harganya murah [8].
Hasil pemurnian yang diperoleh
berupa fraksi endapan protein dengan
berbagai tingkat kemurnian. Penambahan
garam pada konsentrasi tinggi akan
menurunkan kelarutan protein. Hal ini
dikarenakan adanya peningkatan muatan
listrik di sekitar protein yang akan menarik
molekul-molekul air dari protein. Interaksi
hidrofobik sesama molekul protein pada
suasana ionik tinggi akan menyebabkan
pengendapan protein, yang disebut salting
out. Protein yang hidrofobisitasnya tinggi
akan mengendap lebih dahulu, sedangkan
protein yang memiliki sedikit residu non
polar (lebih hidrofilik) akan tetap larut
meskipun pada konsentrasi garam yang
paling tinggi [8].
Pada tahap pemurnian selanjutnya,
dialisis dilakukan sebagai metode untuk
memisahkan partikel-partikel kecil dari
partikel-partikel yang lebih besar
menggunakan membran semipermeabel
berdasarkan prinsip difusi, yaitu
perpindahan molekul dari larutan
berkonsentrasi tinggi ke larutan
berkonsentrasi rendah.Enzim yang
merupakan molekul berukuran besar akan
tetap tertahan di dalam membran karena
selofan. Garam amonium sufat sebagai
molekul kecil akan bermigrasi keluar
membran sehingga enzim menjadi lebih
murni.
2. Uji Aktivitas Spesifik Enzim
L-Asparaginase.
Penentuan aktivitas spesifik ini
bertujuan untuk mengetahui kemurnian tiap
fraksi enzim. Enzim L-Asparaginase dalam
menghidrolisis substrat L-Asparagin
menghasilkan produk asam L-Aspartat dan
amonia. Aktivitas enzim L-Asparaginase
dapat diketahui dari total amonia yang
dihasilkan dari reaksi enzimatis melalui
metode Nessler.
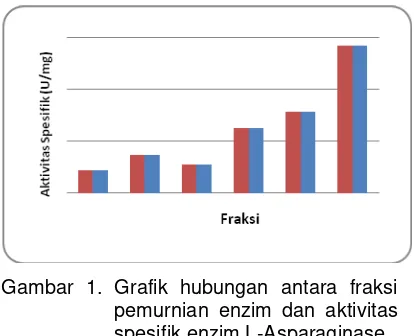
Aktivitas spesifik enzim
L-Asparaginase dari bawang putih dapat
dilihat pada Gambar 1. Satu unit aktivitas
enzim L-Asparaginase didefinisikan sebagai
aktivitas enzim yang menghasilkan 1μmol
produk L-Aspartat maupun amonia per
satuan menit pada kondisi optimum.
Aktivitas spesifik enzim L-Asparaginase
ditentukan berdasarkan perhitungan unit
aktivitas enzim L-Asparaginase (Unit/mL)
per kadar protein enzim L-Asparaginase
(mg/mL protein).
Gambar 1 menunjukkan pada setiap fraksi
enzim memiliki aktivitas spesifik yang
berbeda. Pada fraksi 5 memiliki nilai
aktivitas spesifik tertinggi yaitu sebesar
1423,0248 U/mg protein. Hasil tersebut
menunjukkan bahwa dalam fraksi 5 terdapat
enzim L-Asparaginase lebih banyak
dibandingkan dengan fraksi lainnya.
Pada fraksi 5 menunjukkan aktivitas spesifik
yang lebih besar dibandingkan dengan fraksi
protein sebelumnya. Hal ini menunjukkan
bahwa pada fraksi 5 banyak asam amino
penyusun protein enzim L-asparaginase
yang bersifat hidrofil, sehingga
membutuhkan garam amonium sulfat lebih
banyak untuk mengendapkannya.
Gambar 1. Grafik hubungan antara fraksi pemurnian enzim dan aktivitas spesifik enzim L-Asparaginase
3. Penentuan Karakter Optimum Enzim
Bebas
Karakterisasi L-Asparaginase ini
bertujuan untuk mengetahui kondisi
optimum dari L-Asparginase hasil isolasi.
Fraksi enzim yang dikarakterisasi
merupakan fraksi enzim yang memiliki
aktivitas spesifik tertinggi yaitu fraksi 5.
4. Suhu Optimum L-Asparaginase Bebas
Ditinjau dari struktur protein, suhu
berpengaruh terhadap kerenggangan dan
kerapatan ikatan pada struktur protein
enzim. Hasil penentuan suhu optimum
L-Asparaginase bebas dapat dilihat pada
Gambar 2.
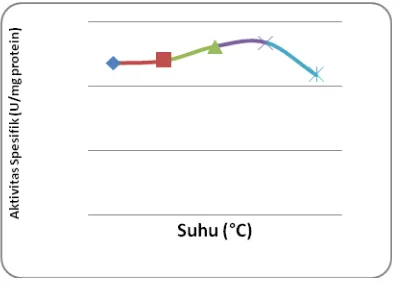
Berdasarkan Gambar 2 dapat dilihat
bahwa suhu optimum dari L-Asparaginase
hasil isolasi adalah 37°C yang ditunjukkan
dengan meningkatnya aktivitas enzim. Pada
suhu optimum, konformasi dari struktur
protein enzim berada tepat untuk mengikat
substrat dalam membentuk produk sehingga
Gambar 2. Grafik hubungan antara suhu dan aktivitas spesifik enzim L-asparaginase.
Enzim merupakan protein yang tersusun
dari ribuan asam-asam amino dimana
protein dapat mengalami denaturasi pada
suhu tinggi. Kenaikan aktivitas enzim di
bawah suhu optimum disebabkan karena
kenaikan energi kinetika molekul-molekul
enzim yang bereaksi. Akan tetapi apabila
suhu tetap dinaikkan terus, energi kinetika
molekul-molekul enzim menjadi besar
sehingga memecahkan ikatan-ikatan
sekunder yang mempertahankan enzim
dalam bentuk aslinya, akibatnya struktur
sekunder dan tersier berubah sehingga
aktivitas enzim menurun.
5. pH Optimum L-Asparaginase Bebas
Struktur protein enzim salah satunya
dipengaruhi oleh pH [6]. Hasil penentuan pH
optimum ditunjukkan pada Gambar 3.
Berdasarkan Gambar 3 dapat diketahui
bahwa pH optimum enzim L-Asparaginase
dari bawang putih adalah 8,6. Pada pH
tersebut, enzim berada pada konformasi
struktur enzim 3 dimensi yang tepat untuk
mengikat substrat. Pada kondisi di luar pH
optimum, konformasi enzim mulai berubah
menyebabkan posisi substrat berada tidak
tepat pada sisi aktif enzim. Hal ini
menyebabkan proses katalisis tidak berjalan
optimal sehingga aktivitas enzim menurun
atau kurang optimal.
Gambar 3. Grafik hubungan antara pH
lingkungan enzim dan aktivitas
spesifik enzim L-Asparaginase
Dengan demikian perubahan pH
berpengaruh terhadap efektivitas sisi aktif
enzim dalam membentuk kompleks enzim
substrat.
6. Amobilisasi Enzim L-Asparaginase
dengan Pendukung Kalsium Alginat
Amobilisasi enzim merupakan suatu
proses dimana pergerakan molekul enzim
ditahan sedemikian rupa sehingga terbentuk
sistem enzim yang aktif dan tidak larut
dalam air. Hasil amobilisasi L-Asparaginase
pada matriks alginat yaitu berupa
manik-manik enzim amobil.
Aktivitas spesifik L-Asparaginase amobil
mengalami penurunan aktivitas spesifik
sebesar 4% jika dibandingkan dengan
aktivitas spesifik enzim bebas (aktivitas
spesifik enzim amobil 1367,6741 U/mg,
aktivitas spesifik enzim bebas 1423,0248
U/mg). Penurunan aktivitas enzim amobil
disebabkan adanya matriks yang
dengan enzim. Amobilisasi enzim dengan
metode penjebakan akan menyebabkan
penghambatan kerja enzim [9].
7. Penentuan Karakter Optimum
L-Asparaginase Amobil.
a. Penentuan Suhu Optimum
L-Asparaginase Amobil
Penentuan suhu optimum bertujuan
untuk mengetahui kondisi optimum enzim
setelah dilakukan amobil. Hasil penentuan
suhu optimum L-Asparaginase amobil dapat
dilihat pada Gambar 4.
Gambar 4. Grafik hubungan antara suhu dan aktivitas spesifik enzim L-Asparaginase amobil.
Berdasarkan grafik di atas, dapat dilihat
bahwa suhu optimum dari L-Asparaginase
amobil adalah 42°C. Suhu optimum pada
enzim amobil lebih tinggi dari enzim bebas
dikarenakan matriks kalsium alginat mampu
melindungi enzim L-Asparaginase amobil
terhadap panas sehingga enzim
L-Asparaginase mampu bertahan pada suhu
yang lebih tinggi dibandingkan dengan
enzim L-Asparaginase bebas. Hal tersebut
menunjukkan bahwa matriks kalsium alginat
mampu melindungi enzim L-Asparaginase
amobil terhadap peningkatan suhu sehingga
enzim L-Asparaginase amobil mampu
bertahan pada suhu yang lebih tinggi
dibandingkan dengan enzim L-Asparaginase
bebas.
b.
PenentuanpH Optimum L-Asparaginase
Amobil.
Penentuan pH optimum perlu
dilakukan untuk mengetahui kondisi
optimum enzim dalam bereaksi dengan
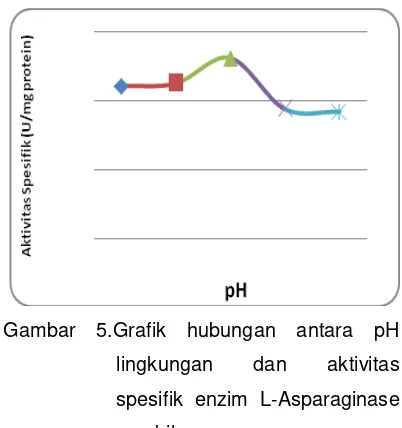
substrat. Hasil karakterisasi pH optimum
dapat dilihat pada Gambar 5.
Gambar 5.Grafik hubungan antara pH
lingkungan dan aktivitas
spesifik enzim L-Asparaginase
amobil.
Berdasarkan grafik di atas dapat diketahui
bahwa pH optimum L-Asparaginase amobil
dari bawang putih adalah pada pH 8,6.
Kondisi optimum dari enzim bebas dan
amobil adalah sama. Hal ini menunjukkan
bahwa penggunaan matriks alginat dalam
amobilisasi L-Asparaginase dari bawang
putih tidak menyebabkan perubahan muatan
sisi aktif enzim maupun struktur enzim
KESIMPULAN
Berdasarkan penelitian yang telah
dilakukan dapat disimpulkan beberapa hal
sebagai berikut:
1. L-Asparaginase dapat diisolasi dari
bawang putih dengan aktivitas spesifik
tertinggi pada fraksi 5 (80-100%) yaitu
1423,0248 U/mg protein.
2. Kondisi optimum L-Asparaginase bebas
diperoleh pada suhu 37°C dan pH 8,6.
3. L-Asparaginase dapat diamobil pada
matriks kalsium alginat 3% dengan
penurunan aktivitas sebesar 4% dari
aktivitas L-Asparaginase bebas.
4. Kondisi optimum L-Asparaginase amobil
diperoleh pada suhu 42°C dan pH 8,6.
UCAPAN TERIMA KASIH
Penelitian ini sukses dan berjalan
dengan lancar berkat dukungan dari dosen
pembimbing, dosen lab. biokimia, dosen
jurusan kimia, laboran jurusan kimia, serta
teman-teman jurusan kimia angkatan 2011.
DAFTAR RUJUKAN
[1] Article of Journal: Anese, M., Quarta,
B., dan Frias, J.M., 2011, Modelling
Effect of Asparginase in Reducing
Acrylamide Formation in Biscuits Food
Chemistry, Ireland.
[2] Article of Journal: Bucke, C., 1987,
Industrial Use of Immobilized Enzyme
and Cells, In: Immobilized Microbial
Enzyme and Cells, Bangkok.
[3] Article of Journal: Ciesarová, Z., Kukurová, K., dan Benešová, C., 2010,
Enzymatic Elimination of Acrylamide in
Potato-Based Thermally Treated
Foods, Slovak Republic.
[4] Article of Journal: Corrigan, P.J., 2008,
Methods for Reducing Asparagine in a
Dough Food Component Using Water
Activity, Patent No
US20080166450-A1.
[5] Article of Journal: Lincoln, L., dan More,
S.S., 2014, Isolation and Production of
Clinical and Food Grade
L-Asparaginase Enzyme from
Fungi,India.
[6] Chapter of Book: Lehninger, A.L., 1982,
Principles of Biochemistry: 1st Edition,
Worth Pub, New York.
[7] Thesis: Rizki, R.A., 2009, Isolasi dan
Karakterisasi Enzim L-Asparaginase
dari Bawang Putih (Allium sativum),
Jurusan Kimia, Fakultas Sains dan
Matematika, Universitas Diponegoro,
Semarang.
[8] Whole Book: Scopes, R.K., 1987,
Protein Purification, Priciple and
Practice, 2nd ed, Springer Verlag, New
York.
[9] Whole Book: Smith, J.E., 1990,
Biotechnology, Diterjemahkan oleh
Hartono, A., Penerbit Buku Kedokteran