LAPORAN KEMAJUAN
PENELITIAN LABORATORIUM
DANA ITS 2020
Biomonitoring Kualitas Air Danau Ranupani
Tim Peneliti :
Bieby Voijant Tangahu, ST., MT., PhD. (Teknik Lingkungan/FTSPK)
Dr. Dewi Hidayati, SSi., MSi. (Biologi/FSAD)
Anak Agung Gde Kartika, ST., MSc. (Teknik Sipil/FTSPK)
DIREKTORAT RISET DAN PENGABDIAN KEPADA MASYARAKAT
INSTITUT TEKNOLOGI SEPULUH NOPEMBER
SURABAYA
Daftar Isi
Daftar Isi ... i
Daftar Tabel ... ii
Daftar Gambar ... iii
Daftar Lampiran ... v
BAB I RINGKASAN ... 1
BAB II HASIL PENELITIAN ... 2
2.1 Kualitas Air ... 2
2.2 Komponen Biologi ... 24
2.3 Status Pencemaran Danau Ranupani ... 32
2.4 Pengelolaan Lingkungan ... 43
BAB III STATUS LUARAN ... 48
BAB IV PERAN MITRA ... 49
BAB V KENDALA PELAKSANAAN PENELITIAN ... 50
BAB VI RENCANA TAHAPAN SELANJUTNYA ... 51
BAB VII DAFTAR PUSTAKA ... 52
Daftar Tabel
Tabel 2. 1 Jenis-jenis vegetasi yang teramati di riparian Danau Ranupani (Titik sampling Vg1) 26
Tabel 2. 2 Jenis-jenis Burung yang Teramati di Sekitar Danau Ranupani ... 29
Tabel 2. 3 Hasil Analisis Plankton di Perairan Danau Ranupani ... 30
Tabel 2. 4 Jenis-jenis Ikan yang Ditemukan di Danau Ranupani dan Status Konservasi Spesies
Ikan menurut IUCN ... 32
Tabel 2. 5 Status Mutu Air Danau Ranupani dengan Baku Mutu Kelas I ... 36
Tabel 2. 6 Status Mutu Air Danau Ranupani dengan Baku Mutu Kelas II ... 37
Tabel 2. 7 Status Mutu Air Danau Ranupani dengan Baku Mutu Kelas III ... 39
Tabel 2. 8 Status Mutu Air Danau Ranupani dengan Baku Mutu Kelas IV ... 40
Tabel 2. 9 Indeks Pencemaran Danau Ranupani ... 42
Daftar Gambar
Gambar 2. 1 Peta Lokasi Sampling Air ... 2
Gambar 2. 2 Parameter Suhu ... 3
Gambar 2. 3 Konsentrasi Parameter Total Dissolved Solid (TDS) ... 4
Gambar 2. 4 Trend konsentrasi TDS Tahun 2011-2020 ... 4
Gambar 2. 5 Konsentrasi Total Suspended Solid ... 5
Gambar 2. 6 Trend Konsentrasi TDS Tahun 2011-2020 ... 5
Gambar 2. 7 Parameter pH ... 6
Gambar 2. 8 Trend pH Tahun 2011-2020 ... 6
Gambar 2. 9 Konsentrasi Biological Oxygen Demand (BOD)... 7
Gambar 2. 10 Trend Konsentrasi BOD Tahun 2011-2020 ... 7
Gambar 2. 11 Konsentrasi Chemical Oxygen Demand (COD) ... 8
Gambar 2. 12 Trend Konsentrasi COD Tahun 2011-2020 ... 9
Gambar 2. 13 Konsentrasi Dissolved Oxygen (DO) ... 9
Gambar 2. 14 Trend Konsentrasi DO Tahun 2011-2020 ... 10
Gambar 2. 15 Konsentrasi Amonia (NH
3-N) ... 10
Gambar 2. 16 Konsentrasi Nitrat (NO
3-N) ... 11
Gambar 2. 17 Trend Konsentrasi NO
3-N Tahun 2011-2020 ... 12
Gambar 2. 18 Konsentrasi Nitrit (NO
2-N) ... 13
Gambar 2. 19 Konsentrasi Cobalt (Co)... 14
Gambar 2. 20 Konsentrasi Barium (Ba) ... 14
Gambar 2. 21 Konsentrasi Boron (B) ... 15
Gambar 2. 22 Konsentrasi Cadmium (Cd) ... 15
Gambar 2. 23 Konsentrasi Chrom Hexavalent (Cr
6+) ... 16
Gambar 2. 24 Konsentrasi Besi (Fe) ... 17
Gambar 2. 25 Konsentrasi Mangan (Mn) ... 17
Gambar 2. 26 Konsentrasi Tembaga (Cu) ... 18
Gambar 2. 27 Analisis Parameter Seng (Zn) ... 18
Gambar 2. 28 Analisis Parameter Timbal (Pb) ... 19
Gambar 2. 29 Konsentrasi Chlorida (Cl
-) ... 20
Gambar 2. 30 Konsentrasi Sianida (CN) ... 20
Gambar 2. 31 Konsentrasi Fluorida ... 21
Gambar 2. 33 Konsentrasi Free Chlorine (Cl
2) ... 22
Gambar 2. 34 Konsentrasi Total Coli ... 23
Gambar 2. 35 Konsentrasi Fecal Coli ... 23
Gambar 2. 36 A. Kegiatan pembersihan S. molesta di Danau Ranupani tahun 2018; B. Hasil
pengamatan Vegetasi di sekitar Danau Ranupani (Titik sampling Vg1); C.
Tumbuhan air yang teramati di permukaan danau Ranupani; D. Tumbuhan air yang
teramati pada saat survei: Alternanthera philoxeroides (Kremah air); E. Kondisi area
pertanian di perbukitan yang curam di sekitar Danau Ranupani yang menjadi
ancaman terjadinya longsoran (di dalam kotak merah). ... 25
Gambar 2. 37 Kiri dan tengah: kondisi vegetasi yang teramati di sekitar Danau Ranupani (Titik
sampling Vg1) dan kanan: vegetasi yang teramati di area pertanian (Titik sampling
Vg2) antara lain tanaman kentang (Solanum tuberosum). ... 26
Gambar 38 Jenis vegetasi yang teramati di riparian Danau Ranupani (titik sampling Vg1) ... 28
Gambar 2. 39 Burung yang Teramati di Sekitar Danau Ranupani ... 29
Gambar 2. 40 Lokasi Plankton diambil dari 4 titik sampling perairan Danau Ranupani (Kode
RP1; RP2; RP3 dan RP4) ... 30
Gambar 2. 41 Ikan Tombro atau ikan mas, Pemancing dan Hasil Pancingan yang Teramati di
Danau Ranupani ... 31
Gambar 2. 42 Lokasi Sampling Komponen Biologi ... 32
Gambar 2. 43 Peta Drainase... 44
Gambar 2. 44 Layout Pembangunan Drainase di Desa Ranupani ... 46
Daftar Lampiran
BAB I RINGKASAN
Desa Ranupani, Kecamatan Senduro, Kabupaten Lumajang sebagian wilayahnya masuk
dalam kawasan Taman Nasional Bromo Tengger Semeru (TNBTS), merupakan desa terakhir
pada rute pendakian Gunung Semeru yang memiliki ketinggian 3.676 meter di atas permukaan
laut. Di Desa Ranupani terdapat Danau Ranupani yang merupakan kawasan Taman Nasional
yang saat ini mengalami pendangkalan dan terjadi pencemaran air danau dari limbah pupuk
lahan pertanian akibat pola pertanian di daerah tangkapan air yang ada di Desa Ranupani.
Indikasi pencemaran air danau dapat dilihat secara visual dari warna kehijauan yang tampak di
permukaan danau. pencemaran air danau oleh limbah pupuk dari lahan pertanian dan sampah
rumah tangga dari aktivitas penduduk Desa Ranupani, serta penutupan badan air Ranupani oleh
gulma Salvinia molesta. Biomonitoring dilakukan untuk mengetahui tingkat pencemaran air di
Danau Ranupani serta menentukan alternatif pengelolaan untuk mengatasi pencemaran
tersebut.
Beberapa warga Ranupani menggantungkan pekerjaannya sebagai petani dan sebagian
lainnya juga berprofesi menjadi pemandu pendakian Gunung Semeru yang sering dikenal
sebagai porter. Namun, kegiatan warga di bidang pertanian merupakan salah satu faktor
terjadinya penyempitan yang luas di Danau Ranupani, pembukaan dan pemanfaatan perbukitan
sebagai lahan pertanian merupakan sebab terjadinya erosi. Fungsi pepohonan besar adalah
sebagai instrumen ekologis untuk menahan pengikisan tanah. Hal tersebut tidak dapat
digantikan oleh tanaman pertanian. Implikasi dari hal tersebut kemudian mengakibatkan
kedalaman danau semakin berkurang. Sebelumnya pada tahun 1998, kedalaman Danau
Ranupani mencapai 12 meter, namun pada tahun 2013 Danau Ranupani kedalamanya
berkurang hingga mencapai 7 meter.
Penelitian ini bertujuan untuk menentukan tingkat pencemaran air yang terjadi pada
Danau Ranupani, sehingga nantinya dapat digunakan untuk menentukan alternatif pengelolaan
yang tepat untuk mengatasi pencemaran air pada Danau Ranupani. Penelitian dilakukan dalam
skala kajian lapangan, dengan pengambilan data primer dan pengumpulan data sekunder yang
terkait. Data primer berupa kualitas air dan analisis organisme (plankton dan bentos) Danau
Ranupani. Pengambilan data primer untuk kualitas air dilakukan secara random, grab dan
composite sampling, sedangkan analisis organisme dilakukan dengan sampling menggunakan
metode transek dan observasi lapangan.
Ringkasan penelitian berisi latar belakang penelitian,tujuan dan tahapan metode penelitian, luaran yang ditargetkan, kata kunci
BAB II HASIL PENELITIAN
2.1 Kualitas Air
Titik pengambilan sampel kualitas air ditunjukkan pada peta yang dapat dilihat pada Error!
Reference source not found., sedangkan kualitas air sumber air serta perbandingannya dengan baku
mutu berdasarkan PP No 82 Tahun 2001 tentang Pengelolaan Kualitas Air dan Pengendalian Pencemaran Air dengan Kriteria Mutu
Air Kelas II ditampilkan dalam bentuk grafik seperti pada
Error! Reference source not found. sampai dengan Error! Reference source not found.35.
Kualitas air permukaan dianalisis pada Laboratorium PDAM Surya Sembada Surabaya.
Gambar 2. 1 Peta Lokasi Sampling Air
Keterangan:
- Sampel 1: Danau Ranupani Saluran Drainase - Sampel 2: Danau Ranupani
- Sampel 3: Saluran Drainase Jembatan
- Sampel 4: Danau Dekat Drainase Kebun Kentang
A. Suhu
Berdasarkan Error! Reference source not found.1, suhu di 4 titik pengambilan sampel menunjukkan nilai yang sama yaitu 27oC. Fluktuasi suhu di perairan tropis umumnya sepanjang tahun mempunyai
Titik 3 Titik 4
Titik 2 Titik 1
fluktuasi suhu udara yang tidak terlalu tinggi sehingga mengakibatkan fluktuasi suhu air juga tidak terlalu besar (Barus, 2004) dalam (Gazali et al., 2015). Suhu suatu badan air dipengaruhi oleh musim, lintang (latitude), waktu dalam hari, sirkulasi udara, penutupan awan, dan aliran serta kedalaman badan air. Perubahan suhu berpengaruh terhadap proses fisika, kimia, dan biologi badan air. Kisaran suhu optimum bagi pertumbuhan fitoplankton di perairan adalah 20oC – 30oC (Effendi, 2003).
Gambar 2. 2 Parameter Suhu
Suhu yang diperoleh pada penelitian ini lebih tinggi dibandingkan penelitian sebelumnya yang dilakukan oleh Gazali et al. (2015) yang menyatakan bahwa rata-rata suhu air di perairan Ranupani sebesar 18,36oC. Selain itu, penelitian oleh Suheriyanto et al. (2012) juga memperoleh hasil 18,36oC
pada pengukuran parameter suhu.
B. Total Dissolved Solid (TDS)
Total Dissolved Solid (TDS) merupakan semua komponen yang terlarut terlarut baik itu unsur-unsur
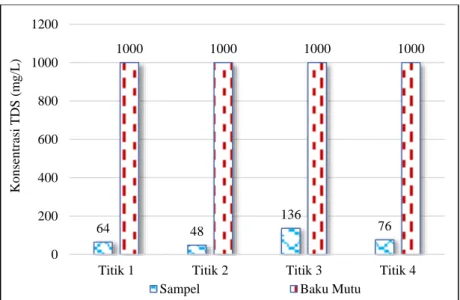
organik maupun anorganik. TDS berasal dari bahan-bahan anorganik berupa ion-ion yang biasa ditemukan di perairan antara lain seperti Sodium (Na), Kalsium (Ca) dan Magnesium (Mg) (Gazali et al., 2015). Error! Reference source not found. menunjukkan bahwa semua titik pengambilan sampel berada di bawah baku mutu 1.000 mg/L. Konsentrasi TDS tertinggi pada titik ketiga di drainase jembatan dapat disebabkan oleh limbah domestik dari rumah tangga. Pada penelitian yang dilakukan oleh Arlindia dan Afdal (2015) juga menunjukkan hal yang sama, semakin dekat menuju daerah wisata maka semakin banyak kontaminasi perairan tersebut oleh sampah-sampah yang dibuang oleh pedagang maupun wisatawan di sekitar lokasi wisata, sedangkan semakin dekat ke area sekitar hutan menyebabkan perairan di lokasi tersebut lebih sedikit terkontaminasi dari zat-zat pencemar yang berasal dari aktivitas warga.
27 27 27 27 0 5 10 15 20 25 30
Titik 1 Titik 2 Titik 3 Titik 4
(
oC)
Gambar 2. 3 Konsentrasi Parameter Total Dissolved Solid (TDS)
Berdasarkan Error! Reference source not found., konsentrasi TDS yang diperoleh pada penelitian ini yaitu paling tinggi sebesar 136 mg/L dan paling rendah sebesar 48 mg/L. Konsentrasi rata-rata yang didapatkan adalah 64 mg/L yang menunjukkan penurunan dibandingkan dengan penelitian sebelumnya yang memberikan nilai sebesar 7,5 mg/L (Sawitri dan Takandjanji, 2019) dan 57,5 mg/L (Pramono, 2011). Grafik trend konsentrasi berdasarkan penelitian yang telah dilakukan sebelumnya dapat dilihat pada Error! Reference source not found..
Gambar 2. 4 Trend konsentrasi TDS Tahun 2011-2020
C. Total Suspended Solid (TSS)
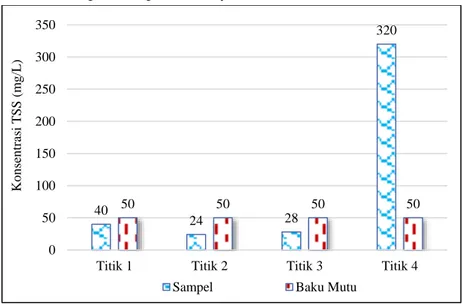
Total Suspended Solid (TSS) pada Error! Reference source not found. menunjukkan bahwa tiga lokasi
sampel memiliki nilai yang di bawah baku mutu. Namun, di titik ke 4, yaitu di dekat drainase kebun kentang, memberikan nilai yang sangat tinggi hingga melebihi baku mutu. Padatan yang terbawa dari area perkebunan kentang menyebabkan nilai TSS meningkat dan menunjukkan nilai yang paling tinggi dibandingkan ketiga titik lainnya. Menurut BLH Sumsel (2011) dalam Firdaus et al. (2014), pada
64 48 136 76 1000 1000 1000 1000 0 200 400 600 800 1000 1200
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i T DS (m g /L )
Sampel Baku Mutu
0 20 40 60 80 100 120 140 160 180 200 2010 2012 2014 2016 2018 2020 2022 Ko n sen tr asi T DS (m g /L ) Tahun Penelitian
penelitian yang telah dilakukan di bagian hulu sungai terdapat aktivitas perkebunan dan pertanian serta limbah rumah tangga dan industri sebagai sumber utama meningkatnya total suspended solid (TSS) dan total dissolved solid (TDS) diperairan pesisir Banyuasin.
Gambar 2. 5 Konsentrasi Total Suspended Solid
Konsentrasi TSS yang diperoleh pada penelitian ini menunjukkan peningkatan dibandingkan dengan penelitian yang pernah dilakukan sebelumnya. Seperti yang ditunjukkan pada Error! Reference source
not found., peningkatan konsentrasi TSS dapat disebabkan oleh meningkatnya aktivitas domestik warga
dan wisatawan di Desa Ranupani. Selain itu, juga dapat disebabkan oleh penggunaan pupuk pada lahan-lahan perkebunan yang semakin banyak sehingga semakin banyak tanah dan pupuk dari lahan-lahan tersebut terbawa erosi.
Gambar 2. 6 Trend Konsentrasi TDS Tahun 2011-2020
D. pH
Baku mutu berdasarkan PP No 82 Tahun 2001 untuk pH adalah 6-9. Hasil analisis parameter pH di 4 titik pengambilan sampel menunjukkan nilai yang sesuai dengan baku mutu yang ditetapkan yaitu antara
40 24 28 320 50 50 50 50 0 50 100 150 200 250 300 350
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i T S S (m g /L )
Sampel Baku Mutu
0 20 40 60 80 100 120 2010 2012 2014 2016 2018 2020 2022 Ko n sen tr asi T SS ( m g /L ) Tahun Penelitian
7,06 – 7,77 yang dapat dilihat pada Error! Reference source not found.. Nilai pH rata-rata yang diperoleh dari analisis ini, yaitu sebesar 7,36 menunjukkan nilai yang cenderung naik dibandingkan dengan nilai pH pada penelitian sebelumnya yang dilakukan oleh Farida (2008), Gazali et al. (2015), Pramono (2016), dan Sawitri dan Takandjanji (2019). Peningkatan nilai pH pada perairan Ranupani dapat disebabkan oleh peningkatan aktivitas warga dan yang menggunakan detergen, sabun mandi, sampo dan sejenisnya. Trend hasil analisis parameter pH dapat dilihat pada Error! Reference source
not found..
Gambar 2. 7 Parameter pH
Gambar 2. 8 Trend pH Tahun 2011-2020
Perairan yang memiliki kadar pH ideal bagi kehidupan organisme akuatik pada umumnya berkisar antara 7 sampai 8,5. Kondisi perairan yang asam akan membahayakan kelangsungan hidup organisme karena menyebabkan terjadinya berbagai gangguan seperti gangguan metabolisme dan respirasi, termasuk pada benthos (Barus, 2004) dalam Putri et al., 2017. Berdasarkan hal tersebut serta baku mutu
7,11 7,06 7,48 7,77 6,6 6,8 7 7,2 7,4 7,6 7,8 8
Titik 1 Titik 2 Titik 3 Titik 4
pH Sampel 0 1 2 3 4 5 6 7 8 9 10 2000 2005 2010 2015 2020 2025 pH Tahun Penelitian
PP No 82 Tahun 2001, maka pH danau Ranupani ini masih dalam kisaran optimal untuk keberlangsungan hidup biota perairan.
E. Biological Oxygen Demand (BOD)
Kandungan BOD yang melebihi baku mutu pada keseluruhan titik pengambilan sampel di Danau Ranupani seperti pada Error! Reference source not found. menunjukkan bahwa danau ini telah tercemar oleh bahan organik yang mudah terurai. BOD yang tinggi pada Titik 3 yaitu di saluran drainase jembatan dapat disebabkan oleh penumpukan limbah organik yang bersumber dari aktivitas warga di dasar perairan. Anggoro (1996) dalam Marganof (2007) menyatakan bahwa menumpuknya bahan pencemar organik di perairan akan menyebabkan proses dekomposisi oleh organisme pengurai juga semakin meningkat, sehingga konsentrasi BOD5 juga meningkat.
Gambar 2. 9 Konsentrasi Biological Oxygen Demand (BOD)
Gambar 2. 10 Trend Konsentrasi BOD Tahun 2011-2020 16 38 48 23 3 3 3 3 0 10 20 30 40 50 60
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i BOD (m g /L )
Sampel Baku Mutu
0 5 10 15 20 25 30 35 2000 2005 2010 2015 2020 2025 Ko n sen tr asi B OD (m g /L ) Tahun Penelitian
Konsentrasi BOD5 apabila dibandingkan dengan penelitian yang sebelumnya pernah dilakukan di Danau
Ranupani menunjukkan peningkatan. Dapat dilihat pada Error! Reference source not found. bahwa konsentrasi BOD5 cenderung naik sejak tahun 2011. Konsentrasi BOD rata-rata dari hasil penelitian
yaitu sebesar 31,25 mg/L, meningkat dibandingkan penelitian sebelumnya pada tahun 2019 yang menunjukkan nilai 23,7 mg/L dan 2015 dengan konsentrasi BOD sebesar 2,62 mg/L. Peningkatan BOD5
merupakan indikasi menurunnya kandungan oksigen terlarut di perairan karena adanya aktivitas organisme pengurai (Canter dan Hill, 1979 dalam Marganof, 2007).
F. Chemical Oxygen Demand (COD)
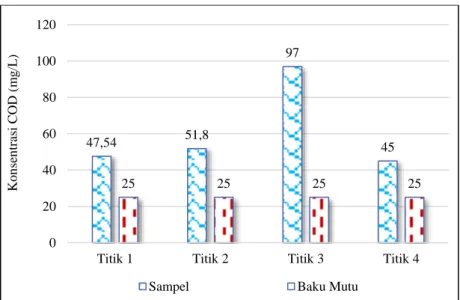
Nilai COD menggambarkan total oksigen yang dibutuhkan untuk mengoksidasi bahan organik secara kimiawi, baik yang dapat didegradasi secara biologi (biodegradable) maupun yang sukar didegradasi (non biodegradable) menjadi CO2 dan H2O (Marganof, 2007). Nilai COD yang melebihi baku mutu
menunjukkan bahwa perairan Danau Ranupani telah tercemar oleh zat pencemar yang mudah diuraikan dan yang sulit diuraikan. Pada Error! Reference source not found., konsentrasi COD di semua titik melebihi baku mutu yang telah ditetapkan sehingga tidak sesuai untuk persyaratan sumber air kelas II.
Gambar 2. 11 Konsentrasi Chemical Oxygen Demand (COD)
Tingginya nilai BOD dan COD
dapat disebabkan oleh kinerja IPAL yang belum optimal (baru
beroperasi 3 bulan), sehingga menyebabkan parameter BOD dan COD yang keluar dari efluen
belum memenuhi baku mutu.
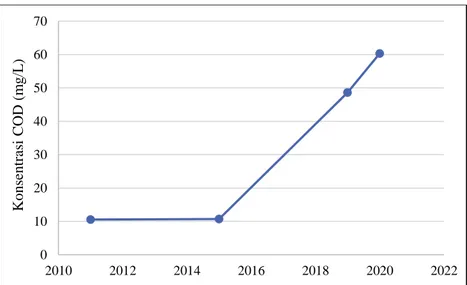
Berdasarkan trend penelitian yang pernah dilakukan sebelumnya yangdapat dilihat pada Error! Reference source not found., menunjukkan bahwa konsentrasi COD juga mengalami peningkatan seperti konsentrasi BOD. Dengan konsentrasi COD rata-rata sebesar 60,355 mg/L, meningkat dari 48,6 mg/L (Sawitri dan Takandjanji, 2019) dan 10,69 (Gazali et al., 2015).
47,54 51,8 97 45 25 25 25 25 0 20 40 60 80 100 120
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i COD (m g /L )
Gambar 2. 12 Trend Konsentrasi COD Tahun 2011-2020
G. Dissolved Oxygen (DO)
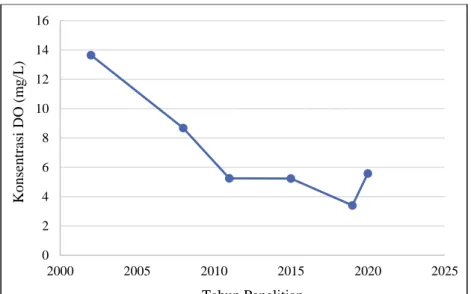
DO memiliki perbandingan terbalik dengan COD. Terlihat bahwa titik dengan konsentrasi COD tinggi maka nilai DO perairan rendah. Pada nilai COD tertinggi, yaitu pada Titik 3, nilai DO yang terkandung hanya 5,3 mg/L. Sedangkan pada nilai COD terendah pada Titik 4, menunjukkan nilai DO yang relatif tinggi, yaitu 6,2 mg/L. Semakin tinggi kandungan bahan organik dalam perairan maka kebutuhan oksigen terlarut dalam proses dekomposisi oleh bakteri juga semakin meningkat sehingga akan menurunkan kandungan oksigen terlarut dalam perairan (Suwari dan Rozari, 2011).
Gambar 2. 13 Konsentrasi Dissolved Oxygen (DO)
Berdasarkan hasil penelitian yang telah dilakukan oleh Kartono (2002); Farida (2008); Pramono (2011); Gazali et al. (2015); Sawitri dan Takandjanji (2019) menunjukkan penurunan konsentrasi DO sejak tahun 2002. Kemudian mengalami peningkatan nilai DO pada penelitian ini, yaitu 5,58 mg/L, setelah pada penelitian Sawitri dan Takandjanji (2019) memperoleh nilai DO sebesar 3,4 mg/L. Grafik penurunan konsentrasi DO berdasarkan penelitian yang telah dilakukan dapat dilihat pada Error!
Reference source not found..
0 10 20 30 40 50 60 70 2010 2012 2014 2016 2018 2020 2022 Ko n sen tr asi C OD (m g /L ) Tahun Penelitian 6 5 5,3 6,02 4 4 4 4 0 1 2 3 4 5 6 7
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i DO (m g /L )
Gambar 2. 14 Trend Konsentrasi DO Tahun 2011-2020
Konsentrasi BOD dan COD yang tinggi pada perairan ini berdampak pada nilai DO yang selanjutnya ditunjukkan pada Error! Reference source not found., Nilai BOD dan COD tertinggi yaitu pada titik ketiga menyebabkan DO yang rendah yaitu hanya 5,3 mg/L. Sedangkan BOD dan COD yang rendah yaitu pada titik pertama menghasilkan nilai DO yang cukup tinggi yaitu 6 mg/L.
H. Amonia (NH
3-N)
Amonia di perairan bersumber dari hasil metabolisme organisme akuatik dan dekomposisi bahan organik oleh bakteri (Boyd 1989). Selain itu, amonia dapat berasal dari nitrogen organik yang masuk ke perairan (urea), respirasi bakteri, organisme mati, dan sel yang pecah (Painter 1970 dalam Novotny dan Olem, 1994). Meskipun amonia bersumber dari hasil ekskresi hewan akuatik, namun proporsinya terhitung kecil jika dibandingkan dengan pembentukan amonia dari dekomposisi oleh bakteri (Wetzel, 2001) dalam (Ervinia, 2011).
Gambar 2. 15 Konsentrasi Amonia (NH3-N)
0 2 4 6 8 10 12 14 16 2000 2005 2010 2015 2020 2025 Ko n sen tr asi DO (m g /L ) Tahun Penelitian 0,0666 0,102 0,0149 0,088 0 0,02 0,04 0,06 0,08 0,1 0,12
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i NH 3 -N (m g /L ) Sampel
Amonium merupakan bentuk unsur nitrogen yang terdapat di dalam air berasal dari pupuk yang larut, kotoran hewan dan lain lain. Amonium berfungsi sebagai hara atau pupuk untuk tanaman air. Kandungan yang tinggi di dalam air sehingga kandungan oksigen di dalam air semakin berkurang dan menyebabkan hewan air sulit berkembang bahkan mati (Rahayu et al. (2009) dalam Ariella (2017)). Tingginya konsentrasi amonia pada titik di titik ke 2 dapat disebabkan oleh penguraian daun-daun yang gugur di sekitar Danau Ranupani di titik ke 2. Seperti pada penelitian yang dilakukan oleh menyatakan bahwa serasah yang bertambah dari mangrove yang berupa batang, daun dan ranting akan jatuh ke bawah, serasah ini merupakan penyumbang utama bahan organik di perairan. Kemudian pada titik tertinggi kedua yaitu di titik ke 4 dapat disebabkan oleh pupuk yang larut bersama air menuju perairan.
I. Nitrat (NO
3-N)
Nitrat yang tinggi pada titik keempat yang berlokasi dekat dengan kebun kentang dapat bersumber dari pupuk yang terbawa bersama erosi tanah yang terbawa dengan aliran air. Pupuk nitrogen diserap tanaman dalam bentuk nitrat dan amonium. Nitrat (NO3-) yang berlebihan akan hilang ke badan air
mengalami residu di lingkungan yaitu di saluran irigasi dan badan air yang pada akhirnya dapat menyebabkan penurunan kualitas air (Elmi et al., 2004) dalam (Wantasen, 2015. Seperti penelitian yang dilakukan oleh Wantasen (2015), sumber nitrat terbesar adalah dari outlet saluran irigasi persawahan yang memiliki pertumbuhan vegetatif aktif. Pada penelitian ini juga menunjukkan hal yang sama, yaitu konsentrasi Nitrat terbesar di titik ke 4 yang merupakan titik pengambilan sampel terdekat dengan perkebunan yang ditunjukkan pada Error! Reference source not found..
Gambar 2. 16 Konsentrasi Nitrat (NO3-N)
Konsentrasi yang diperoleh masih berada di bawah baku mutu lingkungan sesuai Peraturan Pemerintah Nomor 82 Tahun 2001 Kelas II Tentang Pengelolaan Kualitas Air dan Pengendalian Pencemaran Air (konsentrasi nitrat: 10 mg/L). Selain itu, nitrat juga dihasilkan dari proses nitrfikasi amonium menjadi nitrat dalam keadaan oksigen yang cukup (aerob). Nitrat (NO3-) adalah nutrien yang pada kadar
berlebihan, dapat menyebabkan penurunan kualitas air suatu badan air yang akhirnya menimbulkan
3,12 3,08 2,41 5,17 10 10 10 10 0 2 4 6 8 10 12
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i NO 3 -N (m g /L )
pencemaran air serta berakibat pada eutrofikasi (eutrophication) (Arthana, 2006) dalam (Wantasen, 2015).
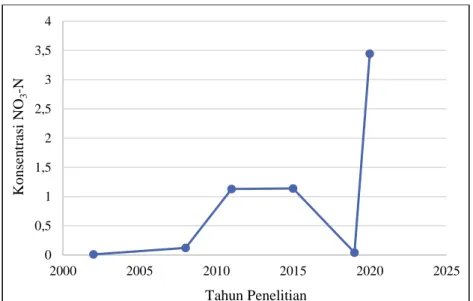
Gambar 2. 17 Trend Konsentrasi NO3-N Tahun 2011-2020
Meskipun mengalami penurunan pada tahun 2019, konsentrasi NO3-N mengalami peningkatan kembali.
Sejak penelitian yang dilakukan pada tahun 2002, konsentrasi NO3-N perairan Danau Ranupani
cenderung meningkat. Peningkatan nilai NO3-N menunjukkan bahwa konsentrasi NH3-N juga
meningkat. Hal ini dikarenakan NO3-N merupakan hasil oksidasi dari NH3-N sehingga kedua parameter
ini saling berhubungan. Error! Reference source not found. merupakan trend perubahan konsentrasi NO3-N sejak tahun 2002. Terlihat bahwa terjadi penurunan konsentrasi pada penelitian yang dilakukan
tahun 2019, yaitu dari 1,14 mg/L menjadi 0,04 mg/L. Namun kemudian kembali meningkat pada tahun 2020 sehingga diperoleh konsentrasi rata-rata sebesar 3,445 mg/L.
J. Nitrit (NO
2-N)
Parameter nitrit memiliki korelasi dengan pH. Semakin tinggi nilai pH maka semakin tinggi pembentukan nitrit (NO2-N). Seperti yang disampaikan pada penelitian Wantasen (2015) yang
menunjukkan bahwa terdapat korelasi negatif antara nitrat dan pH, peningkatan pH mendorong terbentuknya gas NH3 dan NO2 serta penurunan konsentrasi nitrat (NO3). Proses Nitrifikasi berlangsung
pada pH basa ((Wantasen, 2012) dalam (Wantasen, 2015)), yang pada penelitian ini pH basa ditunjukkan dengan pH > 7. Konsentrasi nitrit di perairan alami biasanya ditemukan dalam jumlah yang sedikit yaitu lebih sedikit dari pada nitrat (Wantasen, 2015).
0 0,5 1 1,5 2 2,5 3 3,5 4 2000 2005 2010 2015 2020 2025 Ko n sen tr asi NO 3 -N Tahun Penelitian
Gambar 2. 18 Konsentrasi Nitrit (NO2-N)
Aktivitas pemupukan, dalam hal ini pupuk Urea: NH2CONH2 di lingkungan, dapat mengalami
proses mineralisasi, yaitu proses berubah spesies menjadi Ammonia (NH3) dan Amonium (NH4) (Bush,
2000) dalam (Wantasen, 2015). Faktor-faktor lingkungan yang mempengaruhi transformasi nitrogen di perairan antara lain adalah temperatur, pH, dan konsentrasi oksigen terlarut. Lingkungan perairan yang memiliki pH tinggi/suasana alkalis lebih banyak ditemukan ammonia yang tidak terionisasi dan bersifat toksik (Manahan, 2005) dalam (Wantasen, 2015).
Penguraian NH3 oleh bakteri dan aktivitas lain yang menambah konsentrasi nitrit di perairan
menyebabkan konsentrasi nitrit melebihi baku mutu yang telah ditetapkan pada Titik 3 dan Titik 4. Keberadaan nitrit menggambarkan berlangsungnya proses biologis perombakan bahan organik yang memiliki kadar oksigen terlarut rendah (Wantasen, 2015). Pada proses nitrifikasi, erat kaitannya kandungan DO dengan penguraian amonia dalam air. Berdasarkan hasil analisis parameter amonium, nitrat dan nitrit. Dapat dilihat bahwa dengan kadar DO yang paling tinggi dibandingkan dengan ketiga titik lainnya, terjadi penguraian amonium menjadi nitrat dan nitrit pada titik 4. Sedangkan, pembentukan nitrat mengalami perlambatan sebanding dengan nilai DO yang rendah pada titik kedua.
K. Cobalt (Co)
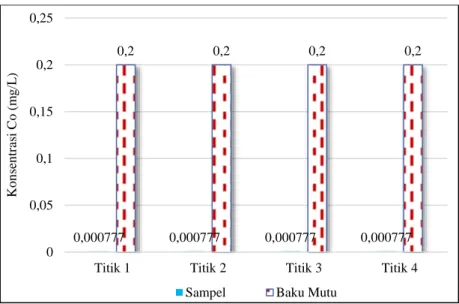
Parameter Cobalt dari hasil analisis sampel di Danau Ranupani menunjukkan nilai yang berada jauh di bawah konsentrasi maksimal baku mutu yang ditetapkan. Perairan tawar alami biasanya memiliki kadar kobalt < 0,001 mg/L (Moore, 1991) dalam (Effendi, 2003). Kobalt termasuk kedalam unsur renik yang dibutuhkan dalam pertumbuhan dan reproduksi pada tumbuhan dan hewan. Bersama dengan ion logam lainnya, (misalnya tembaga, seng, besi dan magnesium), kobalt dibutuhkan oleh enzim sebagai koenzim yang berfungsi untuk mengikat molekul substrat (Effendi, 2003).
0,02 0,02 0,069 0,11 0,06 0,06 0,06 0,06 0 0,02 0,04 0,06 0,08 0,1 0,12
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i NO 2 -N (m g /L )
Gambar 2. 19 Konsentrasi Cobalt (Co)
L. Barium (Ba)
Konsentrasi Barium di keempat titik sampel berada di bawah 0,1 mg/L berdasarkan Error! Reference
source not found.20. Meskipun parameter Barium tidak dipersyaratkan untuk baku mutu air kelas II,
namun konsentrasi Barium ini lebih rendah jika dibandingkan dengan syarat untuk baku mutu air kelas I. Sehingga konsentrasi Barium di Danau Ranupani ini sesuai untuk memenuhi kriteria Mutu Air Kelas II.
Gambar 2. 20 Konsentrasi Barium (Ba)
M. Boron (B)
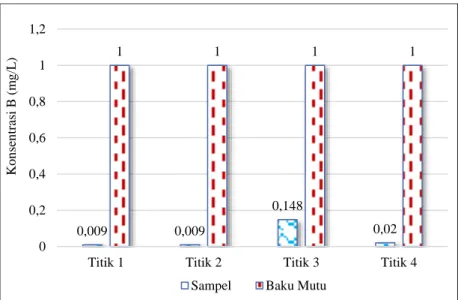
Konsentrasi Boron yang diperoleh pada parameter ini berada di bawah baku mutu yang ditetaokan untuk syarat air minum kelas II. Seperti yang ditunjukkan pada Error! Reference source not found., konsentrasi tertinggi diperoleh pada Titik 3.
0,000777 0,000777 0,000777 0,000777 0,2 0,2 0,2 0,2 0 0,05 0,1 0,15 0,2 0,25
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Co (m g /L )
Sampel Baku Mutu
0,018 0,0136 0,0107 0,038 0 0,005 0,01 0,015 0,02 0,025 0,03 0,035 0,04
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Ba (m g /L ) Sampel
Gambar 2. 21 Konsentrasi Boron (B)
N. Cadmium (Cd)
Cadmium dapat bersumber dari aktivitas alam yaitu berasal dari letusan gunung berapi, debu yang terbawa angin, kebakaran hutan yang menyebabkan kandungan logam kadmium di dalam pohon terlepas, pupuk yang mengandung kandungan kadmium yang digunakan pada lahan pertanian dan aliran sungai yang berasal dari lahan pertanian tersebut. Pencemaran logam kadmium pada lahan pertanian juga berasal dari penggunaan pestisida dan pupuk fosfat anorganik (Fang dan Zhu 2014). Berbagai jenis pestisida mengandung unsur kadmium baik sebagai komponen utama maupun bahan komplementer yang berfungsi sebagai bahan perekat dan peningkat efektivitas senyawa racun yang dikandungnya (Agency 1998). Peningkatan penggunaan pestisida dan pupuk anorganik secara berlebihan secara terus menerus dalam kurun waktu lama menyebabkan kontaminasi kadmium pada lahan pertanian semakin meningkat (Schipper et al. 2011 dalam Sutrisno dan Kuntyastuti, 2015).
Gambar 2. 22 Konsentrasi Cadmium (Cd)
0,009 0,009 0,148 0,02 1 1 1 1 0 0,2 0,4 0,6 0,8 1 1,2
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i B (m g /L )
Sampel Baku Mutu
0,07 0,096 0,000199 0,000199 0,01 0,01 0,01 0,01 0 0,02 0,04 0,06 0,08 0,1 0,12
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Cd (m g /L )
Konsentrasi Kadmium yang melampaui baku mutu terjadi pada Titik 1 dan Titik 2. Dengan demikian, dapat disimpulkan bahwa perairan Danau Ranupani telah terkontaminasi logam berat Kadmium dan tidak dapat memenuhi persyaratan untuk baku mutu syarat air Kelas II. Sedangkan untuk kedua titik lainnya, terpantau masih berada jauh di bawa baku mutu. Konsentrasi Kadmium yang tinggi.
O. Chrom Hexavalent (Cr
6+)
Konsentrasi Chrom Hexavalent pada penelitian ini diperoleh sebesar 0,01 mg/L pada titik ke 4, sedangkan 0 mg/L pada ketiga titik lainnya seperti yang dapat dilihat pada Error! Reference source
not found.. Baku mutu yang ditetapkan adalah sebesar 0,05 mg/L sehingga konsentrasi parameter
Chrom Hexavalent sesuai dengan baku mutu yang ditetapkan.
Gambar 2. 23 Konsentrasi Chrom Hexavalent (Cr6+)
P. Besi (Fe)
PP No 82 Tahun 2001 tidak menetapkan parameter logam Besi sebagai baku mutu untuk persyaratan sumber air kelas II. Konsentrasi tertinggi diperoleh di titik 3 sebesar 0,0275 mg/L dan terendah sebesar 0,0058 mg/L. Meskipun tidak dipersyaratkan untuk baku mutu sumber air kelas II. Namun jika dibandingkan dengan Kelas I, maka konsentrasi logam Besi pada penelitian ini di bawah baku mutu sehingga masih aman untuk dipergunakan sebagai persyaratan untuk kelas II. Hasil analisis parameter Besi ditunjukkan pada Error! Reference source not found..
0 0 0 0,01 0,05 0,05 0,05 0,05 0 0,01 0,02 0,03 0,04 0,05 0,06
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Cr 6+ (m g /L )
Gambar 2. 24 Konsentrasi Besi (Fe)
Q. Mangan (Mn)
Diketahui bahwa konsentrasi logam berat Mangan (Mn) pada penelitian ini diperoleh dari titik 3 dengan konsentrasi 0,02 mg/L dan titik 4 dengan konsentrasi 0,009 mg/L. seperti yang ditunjukkan pada gambar
Error! Reference source not found.. Sedangkan di titik 1 dan titik 2 tidak menunjukkan adanya
kontaminasi oleh logam berat Mangan. Mangan tidak bersifat toksik tetapi keberadaannya dapat mengendalikan kadar unsur toksik lainnya di perairan seperti logam berat (Effendi, 2003) dalam (Kamarati et al., 2018).
Gambar 2. 25 Konsentrasi Mangan (Mn)
R. Tembaga (Cu)
Tembaga yang termasuk dalam golongan logam berat menunjukkan konsentrasi tertinggi sebesar 0,0045 mg/L di titik 4 dengan baku mutu yang ditetapkan 0,02 mg/L. Meskipun konsentrasi berada di bawah
0,02 0,0058 0,0275 0,013 0 0,005 0,01 0,015 0,02 0,025 0,03
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i F e (m g /L ) Sampel 0 0 0,02 0,009 0 0,005 0,01 0,015 0,02 0,025
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i M n (m g /L ) Sampel
baku mutu, namun keempat titik menunjukkan bahwa perairan Danau Ranupani mengandung sejumlah konsentrasi logam berat Tembaga.
Gambar 2. 26 Konsentrasi Tembaga (Cu)
S. Seng (Zn)
Berdasarkan hasil analisis, Danau Ranupani mengandung beberapa jenis logam berat yang mungkin bersumber dari aktivitas warga Desa Ranupani. Logam berat yang memiliki konsentrasi tertinggi adalah seng (Zn). Pupuk anorganik seperti pupuk NPK dan TSP mengandung logam berat seng (Zn) dan tembaga (Cu). Kedua logam berat ini termasuk dalam logam berat esensial, dimana keberadaannya dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup yang dalam hal ini yaitu tanaman, tetapi jika dalam jumlah yang berlebihan dapat menimbulkan efek racun (Widowati et al., 2008) dalam (Parmiko et al., 2014). Pemupukan yang terus menerus tidak saja menyebabkan tingginya residu pupuk di dalam tanah, tetapi juga meningkatkan kandungan logam berat seperti Cu dan Zn (Widaningrum et al., 2007) dalam (Parmiko et al., 2014). Berdasarkan keterangan tersebut, maka dapat disimpulkan bahwa kandungan seng yang terkandung di perairan ini diperoleh dari pupuk kimia yang digunakan warga karena lingkungan Danau Ranupani yang mayoritas dikelilingi wilayah perkebunan milik warga.
0,0026 0,0028 0,0044 0,0045 0,02 0,02 0,02 0,02 0 0,005 0,01 0,015 0,02 0,025
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Cu (m g /L )
Gambar 2. 27 Analisis Parameter Seng (Zn)
T. Timbal (Pb)
Parameter seng yang ada di perairan ini dapat bersumber dari penggunaan pupuk pestisida. Terjadinya peningkatan Zn dan Pb disebabkan adanya aktivitas pembuangan limbah rumah tangga, limbah pertanian yang banyak menggunakan pupuk pestisida yang banyak mengandung Zn sehingga terjadi pertambahan jumlah yang signifikan pada sore hari (Sunti, 2012) dalam (Maddusa et al., 2017).
Gambar 2. 28 Analisis Parameter Timbal (Pb)
U. Chlorida (Cl
-)
Konsentrasi parameter klorida di di Danau Ranupani terpantau paling tinggi di Titik 3 yang berada di drainase jembatan sebesar 12,11 mg/L. Meskipun tidak terdapat persyaratan baku mutu untuk air Kelas II, namun apabila dibandingkan dengan Kelas I sebesar 600 mg/L, maka parameter chlorida ini masih berada di bawah baku mutu. Sehingga dapat disimpulkan bahwa konsentrasi parameter ini sudah sesuai untuk persyaratan air Kelas II.
0,000188 0,000188 0,000193 0,000193 0,05 0,05 0,05 0,05 0 0,01 0,02 0,03 0,04 0,05 0,06
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Zn (m g /L )
Sampel Baku Mutu
0,003344 0,003344 0,003832 0,005 0 0,001 0,002 0,003 0,004 0,005 0,006
Sampel 1 Sampel 2 Sampel 3 Sampel 4
Ko n se n tras i (m g /L ) Timbal (Pb)
Gambar 2. 29 Konsentrasi Chlorida (Cl-)
V. Cianida (CN)
Pada Error! Reference source not found., konsentrasi Sianida di danau pada penelitian ini menunjukkan bahwa air di danau ini telah terkontaminasi logam berat Sianida dengan konsentrasi yang telah mencapai baku mutu yang telah ditetapkan yaitu 0,02 mg/L. Sianida yang terkonsumsi oleh biota perairan juga akan mempengaruhi manusia yang memakan biota tersebut, sehingga dapat berefek pada tekanan darah, penglihatan, paru, sistem syaraf (saraf pusat dan otonom), jantung dan sistem endokrin hingga berakhir dengan kematian (Maksum, 2017).
Gambar 2. 30 Konsentrasi Sianida (CN)
Bentuk sianida alami ditemukan dalam tanaman yang mengandung sianogen glikosida berikut enzimnya yang berfungsi membantu pelepasan (hidrolisis) sianida (Yuningsih, 2012). Sianida di alam dapat ditemukan dalam beberapa jenis tanaman yang secara alami memproduksi zat-zat yang apabila dikonsumsi dapat menghasilkan sianida dalam jumlah yang sangat sedikit.
8,72 8,23 12,11 7,27 0 2 4 6 8 10 12 14
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Cl -(m g /L ) Sampel 0,002 0,02 0,02 0,02 0,02 0,02 0,02 0,02 0 0,005 0,01 0,015 0,02 0,025
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i CN (m g /L )
Secara alami, ada beberapa bahan makanan yang menghasilkan sianida dosis rendah seperti singkong, kacang lima, kacang merah, bayam, kedelai, rebung, tapioka, kecambah millet dan almond. Biji buah-buahan seperti aprikot, apel, dan buah persik juga diduga memiliki sejumlah besar bahan kimia yang dapat dimetabolisme menjadi sianida (https://nationalgeographic.grid.id/read/13303334/sianida-di-dalam-makanan-kita-sehari-hari). Bahan makanan tersebut dapat dikonsumsi oleh warga secara langsung atau dikonsumsi oleh hewan yang kemudian menjadi bahan makanan. Setelah dikonsumsi oleh warga dan keluar melalui proses pencernaan atau metabolisme, zat tersebut mengalir menuju perairan.
W. Fluorida (F)
Fluorida yang terkandung di perairan Ranupani menunjukkan nilai yang rendah dan masih memenuhi baku mutu air Kelas II dengan konsentrasi tertinggi yaitu sebesar 0,293 mg/L. Konsentrasi fluorida di empat titik pengambilan sampel dapat dilihat pada Error! Reference source not found.. Pada perairan alami biasanya memiliki kadar fluoride kurang dari 0,2 mg/L (McNeely, 1979) dalam (Effendi, 2003). Sedangkan perairan yang diperuntukkan bagi air minum sebaiknya memiliki kadar fluorida 0,7 – 1,2 mg/L (Davis dan Cornwell, 1991) dalam (Effendi, 2003). Meskipun tidak melebihi standar baku mutu yang ditetapkan, namun konsentrasi fluoride melebihi baku
Gambar 2. 31 Konsentrasi Fluorida
X. Sulfat (SO
4)
Pada Error! Reference source not found., dapat dilihat bahwa konsentrasi tertinggi di Danau Ranupani diperoleh di titik 4 dengan konsentrasi sebesar 106,7 mg/L dan terendah di titik kedua yaitu sebesar 36,9 mg/L. Menurut Effendi (2003), ion sulfat (SO42-) merupakan salah satu bentuk sulfur anorganik di
perairan. Ion sulfat merupakan salah satu ion utama dalam perairan dan penting bagi makhluk hidup karena merupakan elemen penting dalam protoplasma. Sumber sulfat di perairan dapat berasal dari limbah industri, serta limbah rumah tangga termasuk penggunaan deterjen. Surfaktan sulfat adalah linear alkil benzene sulfonat, etoksisulfat, alkil sulfat, etoksilat, senyawa amonium kuarterner, imidazoline dan betain yang biasa digunakan dalam deterjen.
0,061 0,098 0,293 0,119 1,5 1,5 1,5 1,5 0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i F (m g /L )
Gambar 2. 32 Konsentrasi Sulfat (SO4)
Y. Free Chlorine (Cl
2)
Klorin bebas di Danau Ranupani terpantau memiliki konsentrasi 0 mg/L. Dengan demikian, parameter Cl2 memenuhi syarat baku mutu air Kelas II sebesar 0,03 mg/L seperti yang ditunjukkan pada Error!
Reference source not found..
Gambar 2. 33 Konsentrasi Free Chlorine (Cl2)
Z. Total Coli dan Fecal Coli
Titik kedua pengambilan sampel Total Coli dan Fecal Coli menujukkan nilai yang tidak melebihi baku mutu seperti yang dapat dilihat pada Error! Reference source not found. dan Error! Reference
source not found.. Sedangkan ketiga titik lainnya melebihi baku mutu. Karena ketiga titik tersebut
dekat dengan pemukiman sehingga sangat dimungkinkan bahwa tingginya nilai Total Coli dan Fecal Coli disebabkan oleh rembesan tangki septik milik warga yang tidak kedap air. Tingginya Total Coli dan Fecal Coli di danau ini menjadikan air di danau ini tidak memenuhi baku mutu sebagai klasifikasi
37,4 36,9 59,7 106,7 0 20 40 60 80 100 120
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i S O4 (m g /L ) Sampel 0 0 0 0 0,03 0,03 0,03 0,03 0 0,005 0,01 0,015 0,02 0,025 0,03 0,035
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i Cl 2 (m g /L )
air Kelas II, yaitu
air yang peruntukannya dapat digunakan untuk prasarana/ sarana rekreasi air,
pembudidayaan ikan air tawar, peternakan, air untuk mengairi pertanaman, dan atau peruntukan
lain yang mempersyaratkan mutu air yang sama dengan kegunaan tersebut.
Gambar 2. 34 Konsentrasi Total Coli
Gambar 2. 35 Konsentrasi Fecal Coli
Pada penelitian terdahulu yang dilakukan oleh Sawitri dan Takandjanji (2019), konsentrasi
bakteri pencemar Fecal Coli yang diperoleh adalah sebesar 1100 MPN/100 mL. Hal tersebut
menunjukkan bahwa parameter Fecal Coli yang diperoleh pada penelitian ini telah mengalami
peningkatan, yang saat ini memiliki konsentrasi rata-rata 2.817,5 MPN/100 mL. Dapat
disimpulkan bahwa Danau Ranupani semakin tercemar dengan adanya bakteri ini, meskipun
pada titik kedua pengambilan sampel menunjukkan nilai yang rendah.
11000 280 22000 13000 5000 5000 5000 5000 0 5000 10000 15000 20000 25000
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i T o tal Co li (M P N/1 0 0 m L )
Sampel Baku Mutu
2000 170 4600 4500 1000 1000 1000 1000 0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000
Titik 1 Titik 2 Titik 3 Titik 4
Ko n se n tras i F ec al Co li (M P N/1 0 0 m L )
2.2 Komponen Biologi
Menurut Fitri (2015) dan Kenedie (2016) dalam Sawitri dan Takandjandji (2019), Danau
Ranupani merupakan salah satu danau di dalam kawasan TNBTS yang merupakan kaldera atau
kawah raksasa yang terbentuk akibat letusan Gunung Semeru ribuan tahun lalu, dan kemudian
terisi air larian dari curah hujan dan rembesan tanah. Fungsi kaldera adalah sebagai
penyeimbang ekosistem. Danau merupakan habitat air tawar yang tergenang (lentik). Istilah
lentik digunakan untuk perairan danau yang tenang, yang menawarkan kondisi lingkungan,
yang sangat berbeda dengan sungai yang merupakan habitat lotik (mengalir). Pada habitat
lentik, cahaya hanya menembus ke kedalaman tertentu tergantung pada kekeruhan. Karena
hanya sebagian kecil yang bersentuhan langsung dengan atmosfer dan karena penguraian
berlangsung secara aktif di bagian bawah, kandungan oksigen ekosistem lentik relatif rendah
jika dibandingkan dengan habitat lotik
(http://wgbis.ces.iisc.ernet.in/energy/water/paper/Tr-115/chapter1.htm).
Berdasarkan Budiyanti (2015) menjelaskan bahwa eutrofikasi telah menjadi masalah yang
signifikan dalam ekosistem Danau Ranupani. Sedimentasi dan Eutrofikasi disebabkan karena
pola pertanian intensif tanpa metode ‘teraserring’. Topografi area pertanian yang terletak di
perbukitan yang curam di sekitar Danau Ranupani menjadi ancaman terjadinya longsoran tanah
pertanian yang mengandung pupuk. Hal ini menunjukkan bahwa resiko sedimentasi dan
eutrofikasi di perairan danau Ranupani masih mungkin terjadi. Kondisi air yang tenang dan
adanya eutrofikasi dapat memicu melimpahnya makrofita atau tumbuhan air di perairan danau.
Oleh karena itu melimpahnya makrofita di perairan danau dapat menjadi indikator bahwa danau
telah
mengalami
eutrofikasi
(Szoszkiewicz
et
al.,
2014)
(http://wgbis.ces.iisc.ernet.in/energy/water/paper/Tr-115/chapter1.htm). Menurut Indira et al.
(2013) dalam Sawitri dan Takandjandji (2019) dalam e-Journal Penelitian Hutan dan
Konservasi
Alam
(http://ejournal.forda-mof.org/ejournal-litbang/index.php/JPHKA/article/view/4675/4723) dilaporkan bahwa Danau Ranupani
menerima sedimen melalui aliran permukaan yang terangkut sebesar 46.999,18 ton/ha/tahun.
Hal tersebut mengakibatkan munculnya ruang tumbuh bagi tumbuhan air, seperti ki ambang
(Salvinia molesta) yang memiliki sistem perakaran yang lebat dengan persen penutupan
mencapai 80%. Berdasar laporan situs website TNBTS disampaikan bahwa pada tahun 2018,
permukaan perairan Danau Ranupani tertutupi oleh melimpahnya pertumbuhan tumbuhan air
kiambang (S. molesta). Hal ini mengindikasikan bahwa danau Ranupani telah mengalamai
eutrofikasi. Sebagai upaya melestarikan Danau Ranupani, pada tahun 2018, BBTNBTS telah
melakukan kegiatan pembersihan danau dari S. molesta sebagaimana ditunjukkan. Saat
dilakukan survei pada studi ini (tahun 2020) terlihat bahwa kondisi air Danau Ranupani telah
terbebas dari tumbuhan air S. molesta. Hal ini menunjukkan keberhasilan program pembersihan
Danau Ranupani dari S. molesta. Namun demikian, ditemukan tumbuhan air lainnya yang
tumbuh di perairan danau, seperti Alternanthera philoxeroides (Kremah air). Gambaran kondisi
lahan pertanian di perbukitan sekitar danau Ranupani tersebut berdasar data Google Image
tahun 2019 serta kondisi danau dan lingkungan sekitarnya ditunjukkan dalam Error!
Reference source not found..
Gambar 2. 36
A. Kegiatan pembersihan S. molesta di Danau Ranupani tahun 2018; B. Hasil
pengamatan Vegetasi di sekitar Danau Ranupani (Titik sampling Vg1); C. Tumbuhan air yang
teramati di permukaan danau Ranupani; D. Tumbuhan air yang teramati pada saat survei:
Alternanthera philoxeroides (Kremah air); E. Kondisi area pertanian di perbukitan yang
curam di sekitar Danau Ranupani yang menjadi ancaman terjadinya longsoran (di dalam kotak
merah).
Berdasar Gambar 2. 37, ditunjukkan bahwa tutupan vegetasi yang teramati di riparian
Danau Ranupani (Titik sampling Vg1) umumnya terdiri dari semak, herba dan rumput-
rumputan. Tegakan pohon yang teramati umumnya adalah Family cemara (Casuarinaceae).
Sementara berdasar pengamatan dan wawancara, vegetasi di area pertanian yang terletak di
perbukitan (Titik sampling Vg2) umumnya didominasi tanaman kentang (Solanum tuberosum),
kubis (Brassica oleracea) dan daun bawang (Allium fistulosum). Di sela-sela lahan pertanian
juga teramati beberapa tegakan pohon cemara.
Hasil pengamatan vegetasi disajikan dalam Tabel 2. 1 ditunjukkan bahwa jenis-jenis
tanaman herba yang sering ditemui di lokasi titik sampling Vg1 (riparian danau) antara lain
Rumex aquaticus dan gulma air Alternanthera philoxeroides (Kremah air). Jenis tumbuhan
tersebut umumnya mampu hidup di daratan (terrestrial) maupun area tergenang. Berdasarkan
pengamatan pada saat survey, teramati spesies tersebut ditemukan di area terrestrial dekat danau
maupun area danau yang dangkal (Error! Reference source not found. D dan Gambar 2. 37).
Tegakan pohon yang dijumpai antara lain cemara, akasia dan bambu.
Status konservasi spesies tumbuhan yang ada di riparian Danau Ranupani menurut IUCN
Red List Sebagian besar masuk kategori Least Concern (LC; Berisiko Rendah) dan Data
Deficient (DD; Informasi Kurang). LC diberikan untuk spesies yang telah dievaluasi namun
tidak masuk ke dalam kategori manapun. Sedangkan DD diinyatakan “informasi kurang”
artinya informasi yang ada kurang memadai untuk membuat perkiraan akan risiko
kepunahannya berdasarkan distribusi dan status populasi. Namun ada spesies yang masuk
kategori NT atau Near Threatened (hampir terancam) yaitu Acacia aulacocarpa (akasia)
(https://www.iucnredlist.org/species/38360/10113765) dan satu spesies tergolong EW (Extinct
in the Wild=Punah di alam liar) yaitu Brugmansia suaveolens (Kecubung gunung) (
https://www.iucnredlist.org/es/species/51247699/58913403)
Status
NT
adalah
status
konservasi yang diberikan kepada spesies yang mungkin berada dalam keadaan terancam atau
mendekati terancam kepunahan, meski tidak masuk ke dalam status terancam. Sedangkan EW
adalah status konservasi yang diberikan kepada spesies yang hanya diketahui berada di tempat
penangkaran atau di luar habitat alami mereka. Jenis-jenis vegetasi yang teramati di riparian
Danau Ranupani (Titik sampling Vg1), status dominansi dan status konservasinya menurut
IUCN disajikan dalam Tabel 2. 1.
Tabel 2. 1 Jenis-jenis vegetasi yang teramati di riparian Danau Ranupani
(Titik sampling Vg1)
No. Spesies
Nama
Famili
Dominansi
Status
Gambar 2. 1
Gambar 2. 37 Kiri dan tengah: kondisi vegetasi yang teramati di sekitar Danau Ranupani (Titik sampling
Vg1) dan kanan: vegetasi yang teramati di area pertanian (Titik sampling Vg2) antara lain tanaman kentang (Solanum tuberosum).
Indonesia
IUCN
KATEGORI POHON dan PALEM
1
Casuarina equisetifolia
Cemara
Casuarinaceae
O
LC
2
Acacia aulacocarpa
Akasia
Fabaceae
O
NT
3
Cibotium barometz
Pakis monyet
Cibotiaceae
O
DD
4
Casuarina
junghuhniana
Cemara gunung
Casuarinaceae
F
DD
5
Vasconcellea
pubescens
Pepaya gunung
Caricaceae
R
DD
6
Bambusa sp
Bambu
Poaceae
O
DD
KATEGORI SEMAK, HERBA dan RUMPUT
1
Alternanthera
philoxeroides
Kremah air
Amaranthaceae
F
LC
2
Panicum hemitomon
Ijon ijon
Poaceae
F
LC
3
Rumex aquaticus
-
Polygonaceae
F
LC
4
Brugmansia suaveolens
Kecubung
gunung
Solanaceae
R
EW
5
Ruellia angustifolia
Kencana ungu
Acanthaceae ·
O
LC
6
Panicum repens
Rumput
Poaceae
F
LC
7
Canna lily
Bunga tasbih
Cannaceae
R
LC
8
Zantedeschia aethiopica
Kala lili
Araceae
R
Keterangan: Dominansi vegetasi: D (dominant) (sangat berlimpah) = 80%-100%; A
(abundant) (berlimpah) = 60%-80%; F (frequent) (sering) = 40%-59%; O (occasional)
(jarang)= 20%-39%; R (rare) (sangat jarang) = 0-19%. Status Konservasi menurut IUCN: LC
(Least concern =resiko rendah) ; NT (Near Threatened =hampir terancam); EW (Extinct in
the Wild= Punah di alam liar )
Alternanthera philoxeroides
(Kremah air) yang ditemukan
area terrestrial (riparian )
Alternanthera philoxeroides
(Kremah air) yang ditemukan
area perairan danau
Rumex aquaticus dan
Panicum
hemitomon
(rumput)
Brugmansia
suaveolens
(Merkubung hutan)
Zantedeschia
aethiopica
(Kala lili)
Acacia
aulacocarpa
(Akasia)
Selain tanaman, Fauna Darat yang diamati adalah burung. Teramati beberapa jenis burung
antara lain Elang Hitam (Ictinaetus malayensis); Burung-gereja Erasia (Passer montanus);
Layang- layang batu (Hirundo tahitica; Tekukur biasa (Spilopelia chinensis); Cucak kutilang
(Pycnonotus aurigaster); Kerak kerbau (Acridotheres javanicus); Walet linci (Collocalia
linchi). Sebagian burung yang teramati ditunjukkan dalam Tabel 2. 2 dan Error! Reference
source not found.. Hasil pengamatan adanya elang hitam dan tekukur dalam survei ini sama
dengan data survei sebelumnya yang dilakukan oleh Nugroho et al. (2013)
(https://repository.ipb.ac.id/handle/123456789/71019). Berdasarkan Tabel 2. 2 ditunjukkan
bahwa burung yang teramati di sakitar Danau Ranupani memiliki status konservasi LC: Least
concern (resiko rendah) dan DD: Data deficient (kekurangan data). Tidak ada spesies yang
terancam punah.
Tabel 2. 2 Jenis-jenis Burung yang Teramati di Sekitar Danau Ranupani
No. Spesies (Burung)
Nama
Indonesia
Famili
Jumlah
(ind.)
Status
IUCN
1
Ictinaetus malayensis
Elang hitam
Accipitridae
1
LC
2
Passer montanus
Burung-gereja
Erasia
Passeridae
52
LC
3
Hirundo tahitica
Layang-layang
batu
Hirundinidae
27
LC
4
Spilopelia chinensis
Tekukur biasa
Columbidae
29
LC
5
Pycnonotus aurigaster
Cucak kutilang
Pycnonotidae 21
LC
6
Acridotheres javanicus
Kerak kerbau
Sturnidae
1
LC
7
Collocalia linchi
Walet linchi
Apodidae
30
DD
8
Lonchura punctulata
Bondol peking
Estrildidae
6
LC
Total
167
Keterangan: LC: Least concern (resiko rendah); DD: Data deficient (Informasi Kurang)
Lonchura punctulata (Bondol peking)
Pycnonotus aurigaster (Cucak kutilang)
Ictinaetus malayensis (Elang hitam)
Spilopelia chinensi (Tekukur biasa)
Biota perairan yang diamati di perairan Ranupani adalah plankton dan ikan. Plankton
diambil dari 4 titik sampling perairan Danau Ranupani (Kode RP1; RP2; RP3 dan RP4),
dengan lokasi dan koordinat sampling ditunjukkan pada Error! Reference source not found..
Hasil Analisa plankton (Tabel 2.
3) menunjukkan bahwa secara umum, struktur komunitas perairan Danau Ranupani tergolong
cukup stabil hingga stabil, dengan kualitas air kategori sedang hingga buruk. Area Perairan
yang dekat dengan area pemukiman dan pertanian (Titik RP1; RP2 dan RP3) menunjukkan
nilai Indeks Diversitas (H’) Plankton yang lebih kecil (H’=1.206-1,303) daripada dari perairan
yang jauh dari pemukiman dan pertanian (Titik RP4) dengan H’=1.678. Hal ini menunjukkan
bahwa kegiatan di pemukiman dan pertanian memberi pengaruh negatif terhadap kualitas air
Danau Ranupani. Analisis dominansi plankton akan dijelaskan pada dokumen ANDAL.
Tabel 2. 3 Hasil Analisis Plankton di Perairan Danau Ranupani
Plankton
Kondisi Struktur Komunitas dan Kualitas Pencemaran
Perairan di Danau Ranupani berdasar Indeks Diversitas (H’)
Plankton
Nilai/Status
RP1
RP2
RP3
RP4
Phytoplankton
H’
1.281
1.303
1.206
1.678
Kondisi
struktur
komunitas
Stabil
Stabil
Stabil
Stabil
Kualitas perairan
Sedang
Sedang
Sedang
Sedang
Gambar 2. 40 Lokasi Plankton diambil dari 4 titik sampling perairan Danau Ranupani (Kode
Plankton
Kondisi Struktur Komunitas dan Kualitas Pencemaran
Perairan di Danau Ranupani berdasar Indeks Diversitas (H’)
Plankton
Nilai/Status
RP1
RP2
RP3
RP4
Zooplankton
H’
1.061
1.040
1.040
1.213
Kondisi
struktur
komunitas
Cukup
stabil
Cukup
stabil
Cukup
stabil
Stabil
Kualitas perairan
Buruk
Buruk
Buruk
Sedang
Berdasar laporan analisis kualitas air, diketahui bahwa Efluen IPAL dari limbah domestik
dialirkan melalui pipa dan kemudian dibuang ke Ranupani. Kualitas air efluen yang dihasilkan
oleh IPAL mengandung BOD sebesar 190 mg/L O
2yang jauh lebih tinggi dari baku mutu (30
mg/L O
2). Tingginya BOD dari IPAL tersebut mengindikasikan tingginya polutan organik.
Selain menerima beban pencemar organik dari pemukiman, Danau Ranupani juga beresiko
menerima run off sedimen dari lahan pertanian yang mengandung unsur hara dari lahan
pertanian. Kondisi tersebut dapat meningkatkan pencemaran organik dan menimbulkan
eutrofikasi di perairan Ranupani. Hal ini sesuai dengan hasil kualitas perairan berdasarkan
plankton yang menunjukkan kualitas buruk hingga sedang.
Biota perairan lain yang diamati adalah ikan. Berdasarkan pengamatan hasil tangkapan
pemancing setempat, diketahui beberapa jenis ikan di Danau Ranupani, antara lain Tawes
(Barbonymus gonionotus), Ikan mas atau tombro (Cyprinus carpio), Lele (Clarias sp) dan ikan
gatul (Poecilia reticulata) seperti pada Error! Reference source not found. dan Tabel 2. 4.
Jenis-jenis ikan di Ranupani tersebut sama dengan hasil studi sebelumnya oleh Nugorho dkk
(2013) (https://repository.ipb.ac.id/handle/123456789/71019).
Berdasarkan pemeriksaan status konservasi menurut IUCN, diketahui bahwa sebagian besar
spesies ikan di Danau Ranupani termasuk kategori LC (Least concern=resiko rendah), namun
terdapat 1 spesies tergolong VU (Vulnerable=rentan) yaitu Cyprinus carpio (ikan tombro/ ikan
Gambar 2. 41 Ikan Tombro atau ikan mas, Pemancing dan Hasil Pancingan yang Teramati di Danau Ranupani
mas/ ikan karper). Vulnerable (VU: Rentan) merupakan status konservasi untuk kategori
spesies yang menghadapi risiko kepunahan di alam liar di waktu yang akan datang.
Tabel 2. 4 Jenis-jenis Ikan yang Ditemukan di Danau Ranupani dan Status Konservasi Spesies
Ikan menurut IUCN
No.
Spesies
Nama Indonesia
Famili
Status
1
Clarias sp.
Lele
Clariidae
LC
2
Cyprinus carpio
Tombro/ ikan mas
Cyprinidae
VU
3
Barbonymus gonionotus
Tawes
Cyprinidae
LC
4
Poecilia reticulata
Gatul
Poeciliidae
LC
Keterangan: LC (Least concern=resiko rendah); VU (Vulnerable=rentan)
Peta lokasi sampling biologi dapat dilihat pada Error! Reference source not found. berikut.
Gambar 2. 42
Lokasi Sampling Komponen Biologi
2.3 Status Pencemaran Danau Ranupani
Berdasarkan hasil analisis parameter lengkap yang telah diuraikan, maka dapat dilakukan
penentuan status pencemaran Danau Ranupani dengan metode Indeks Pencemaran (IP).
Metode IP dibangun berdasarkan dua indeks kualitas. Yang pertama adalah Indeks Rata-rata
(IR). Indeks ini menunjukkan tingkat pencemaran rata-rata dari seluruh parameter dalam satu
kali pengamatan. Yang kedua adalah indeks maksimum (IM). Indeks ini menunjukkan satu
jenis parameter yang dominan menyebabkan penurunan kualitas air pada satu kali pengamatan
(Marganingrum, 2013) dalam (Romdania et al., 2018).
Status mutu air berdasarkan hasil perhitungan Indeks Pencemaran sebagai berikut:
No Skor IP Deskripsi 1 0 – 1,0 Kondisi Baik 2 1,1 – 5,0 Cemar Ringan 3 5,1 – 10 Cemar Sedang 4 >10 Cemar Berat
Sumber: KepMen LH No 115 Tahun 2003
Berdasar Keputusan Menteri Lingkungan Hidup Nomor 115 Tahun 2003, status mutu air
dapat ditentukan dengan menggunakan Indeks Pencemaran. memiliki konsep yang berlainan
dengan Indeks Kualitas Air (Water Quality Index). Indeks Pencemaran (IP) ditentukan untuk
suatu peruntukan, kemudian dapat dikembangkan untuk beberapa peruntukan bagi seluruh
bagian badan air atau sebagian dari suatu sungai.
Jika Lij menyatakan konsentrasi parameter kualitas air yang dicantumkan dalam Baku Mutu
Air (j), dan Ci menyatakan konsentrasi parameter kualitas air (i) yang diperoleh dari hasil
analisis cuplikan air pada suatu lokasi pengambilan cuplikan dari suatu alur sungai, maka PIj
adalah Indeks Pencemaran bagi peruntukan (j) yang merupakan fungsi dari Ci/Lij.
PIj = (C1/L1j, C2/L2j,…,Ci/Lij)
Tiap nilai Ci/Lij menunjukkan pencemaran relatif yang diakibatkan oleh parameter kualitas
air. Nisbah ini tidak mempunyai satuan. Nilai Ci/Lij = 1,0 adalah nilai yang kritik, karena nilai
ini diharapkan untuk dipenuhi bagi suatu Baku Mutu Peruntukan Air. Jika Ci/Lij >1,0 untuk
suatu parameter, maka konsentrasi parameter ini harus dikurangi atau disisihkan, kalau badan
air digunakan untuk peruntukan (j). Jika parameter ini adalah parameter yang bermakna bagi
peruntukan, maka pengolahan mutlak harus dilakukan bagi air itu. Pada model IP digunakan
berbagai parameter kualitas air, maka pada penggunaannya dibutuhkan nilai ratarata dari
keseluruhan nilai Ci/Lij sebagai tolok-ukur pencemaran, tetapi nilai ini tidak akan bermakna
jika salah satu nilai Ci/Lij bernilai lebih besar dari 1. Jadi indeks ini harus mencakup nilai Ci/Lij
yang maksimum
PIj = {(Ci/Lij)R,(Ci/Lij)M}
Nilai (Ci/Lij)R : nilai Ci/Lij rata-rata
(Ci/Lij)M : nilai Ci/Lij maksimum
Perairan akan semakin tercemar untuk suatu peruntukan (j) jika nilai (Ci/Lij)Rm dan
atau (Ci/Lij)M adalah lebih besar dari 1,0. Jika nilai maksimum Ci/Lij dan atau nilai rata-rata
Ci/Lij makin besar, maka tingkat pencemaran suatu badan air akan makin besar pula.
PIj = m √(
𝐶𝑖 𝐿𝑖𝑗)
𝑀 2+ (
𝐶𝑖 𝐿𝑖𝑗)
𝑅 2Dimana m = faktor penyeimbang
Keadaan kritik digunakan untuk menghitung nilai m
PIj = 1,0 jika nilai maksimum Ci/Lij = 1,0 dan nilai rata-rata Ci/Lij = 1,0 maka
1,0 = m√(1)
2+ (1)
2m = 1/√2, maka persamaan tersebut menjadi:
Pij =
√
(𝐿𝑖𝑗𝐶𝑖) 𝑀 2 +(𝐿𝑖𝑗𝐶𝑖) 𝑅 2 2Harga Pij ini dapat ditentukan dengan cara:
1. Memilih parameter-parameter yang jika harga parameter rendah maka kualitas air akan
membaik
2. Memilih kosentrasi parameter baku mutu yang tidak memiliki rentang
3. Menghitung harga Ci/Lij untuk tiap parameter ada setiap stasiun pengambilan sampel
4. Untuk nilai kosentrasi parameter DO, yang menurun akan menyatakan tingkat pencemaran
meningkat misal DO. Perlu ditentukan nilai teoritik atau nilai maksimum Cim (yang merupakan
DO jenuh = 7). Kemudian nilai Ci/Lij hasil pengukuran digantikan oleh nilai Ci/Lij hasil
perhitungan, yaitu:
(Ci/Lij) baru =
𝐶𝑖𝑚−𝐶𝑖𝐶𝑖𝑚−𝐿𝑖𝑗
5. Jika nilai baku Lij memiliki rentang
- Untuk Ci < Lij rata-rata
(Ci/Lij) baru =
𝐶𝑖𝑚−(𝐿𝑖𝑗)𝑟𝑎𝑡𝑎−𝑟𝑎𝑡𝑎(𝐿𝑖𝑗) min − (𝐿𝑖𝑗)𝑟𝑎𝑡𝑎−𝑟𝑎𝑡𝑎
- Untuk Ci < L ij rata-rata
(Ci/Lij) baru =
𝐶𝑖𝑚−(𝐿𝑖𝑗)𝑟𝑎𝑡𝑎−𝑟𝑎𝑡𝑎(𝐿𝑖𝑗) maks − (𝐿𝑖𝑗)𝑟𝑎𝑡𝑎−𝑟𝑎𝑡𝑎