BAB II
TINJAUAN PUSTAKA
2.1. Antibiotik
2.1.1 Definisi Antibiotik
Menurut asalnya antibakteri dapat dibagi menjadi dua, yaitu antibiotik dan agen kemoterapetik.Antibiotik merupakan zat kimia yang dihasilkan oleh mikroorganisme yang mempunyai kemampuan dalam larutan encer untuk menhambat pertumbuhan atau membunuh mikroorganisme, contohnya penisilin, sefalosporin, kloramfenikol, tetrasiklin, dan lain-lain.Antibiotik yang relatif non toksis bagi pejamunya digunakan sebagai agen kemoterapetik dalam pengobatan penyakit infeksi pada manusia, hewan dan tanaman.Istilah ini sebelumnya digunakan terbatas pada zat yang dihasilkan oleh mikroorganisme, tetapi penggunaan istilah ini meluas meliputi senyawa sintetik dan semisintetik dengan aktivitas kimia yang mirip, contohnya sulfonamida, kuinolon dan fluorikuinolon (Setiabudy, 2011; Dorland, 2010).
2.1.2 Penggolongan Antibiotik
Infeksi bakteri terjadi bila bakteri mampu melewati barrier mukosa atau kulit dan menembus jaringan tubuh. Pada umumnya, tubuh berhasil mengeliminasi bakteri tersebut dengan respon imun yang dimiliki, tetapi bila bakteri berkembang biak lebih cepat daripada aktivitas respon imun tersebut maka akan terjadi penyakit infeksi yang disertai dengan tanda-tanda inflamasi. Terapi yang tepat harus mampu mencegah berkembang biaknya bakteri lebih lanjut tanpa membahayakan host(Kemenkes, 2011).
Penggolongan antibiotik berdasarkan struktur kimia dapat dibedakan sebagai berikut (Kasper et. al 2005, Setiabudi, 2007, Katzung, et. al. 2011) :
1. Beta laktam, penisilin (contohnya: penisilin, isoksazolil penisilin, ampisilin), sefalosporin (contohnya sefadroksil, sefaklor), monobaktam (contohnya: azteonam) dan karbapenem (contohnya: imipenem).
2. Tetrasiklin, contohnya tetrasiklin dan doksisiklin. 3. Makrolida, contohnya eritromisin dan klaritromisin 4. Linkomisin, contohnya linkomisin dan klindamisin 5. Kloramfenikol, contohnya kloramfenikol dan tiamfenikol
6. Aminoglikosida, contohnyastreptomisn, neomisin dan gentamisin. 7. Sulfonamida (contohnya: sulfadizin, sulfisoksazol) dan kotrimoksazol
(kombinasi trimetroprim dan sulfametoksazol).
8. Kuinolon (contohnya: asam nalidiksat) dan fluorokuinolon (contohnya: siprofloksasin dan levofloksasin)
9. Glikopeptida, contohnyavankomisin dan telkoplanin. 10. Antimikrobakterium, isoniazid, rifampisin, pirazinamid.
11. Golongan lain, contohnya polimiksin B, basitrasin, oksazolidindion.
Berdasarkan sifat toksisitas selektif, ada antibiotik yang bersifat menghambat pertumbuhan bakteri, dikenal sebagai aktivitas bakteriostatik (contohnya sulfonamid, trimetroprim, kloramfenikol, tetrasiklin, linkomisin dan klindamisin) dan ada yang bersifat membunuh bakteri, dikenal sebagai aktivitas bakterisid (contohnya penisilin, sefalosporin, streptomisn, neomisin, kanamisin, gentamisin dan basitrasin). Pada kondisi immunocompromised (misalnya pada pasien neutropenia) atau infeksi dilokasi yang terlindung (misalnya pada cairan cerebrospinal), maka antibiotik bakterisid harus digunakan (Kemenkes, 2011; Setiabudy, 2011).
Antibiotik bisa diklasifikasikan berdasarkan mekanisme kerjanya, yaitu (Kasper et. al., 2005, Setiabudy, 2011) :
1. Menghambat sintesis atau merusak dinding sel bakteri. Dinding sel bakteri terdiri dari polipeptidoglikan yaitu suatu komples polimer mukopeptida (glikopeptida).Obat ini dapat melibatkan otolisin bakteri (enzim yang mendaur ulang dinding sel) yang ikut berperan terhadap lisis sel. Antibiotik
yang termasuk dalam kelompok ini seperti beta-laktam (penisilin, sefalosporin, monobaktam, karbapenem, inhibitor beta-laktamase), basitrasin, dan vankomisin.Pada umumnya bersifat bakterisidal.
2. Memodifikasi atau menghambat sintesis protein. Sel bakteri mensintesis berbagai protein yang berlangsung di ribosom dengan bantuan mRNA dan tRNA.Penghambatan terjadi melalui interaksi dengan ribosom bakteri.Yang termasuk dalam kelompok ini misalnya aminoglikosid, kloramfenikol, tetrasiklin, makrolida (eritromisin, azitromisin, klaritromisin), klindamisin, mupirosin, dan spektinomisin.Selain aminoglikosida, pada umumnya antibiotik ini bersifat bakteriostatik.
3. Menghambat enzim-enzim esensial dalam metabolisme folat, misalnya trimetoprim dan sulfonamid.Pada umumnya antibiotik ini bersifat bakteriostatik.
4. Mempengaruhi sintesis atau metabolisme asam nukleat, misalnya kuinolon, nitrofurantoin.
5. Mempengaruhi permeabilitas membran sel bakteri. Antibiotika yang termasuk adalah polimiksin.
Berdasarkan spektrum kerjanya, antibiotik terbagi atas dua kelompok besar, yaitu antibiotik dengan aktivitas spektrum luas (broad-spectrum) dan aktivitas spektrum sempit (narrow (broad-spectrum).
1. Antibiotik spektrum luas (broad-spectrum)
Spektrum luas, bekerja terhadap lebih banyak bakteri, baik gram negatif maupun gram positif serta jamur. Contohnya: tetrasiklin dan kloramfenikol.
2. Antibiotik spektrum sempit (narrow spectrum)
Antbiotik spektrum sempit bekerja terhadap beberapa jenis bakteri saja. Contohnya: penisilin hanya bekerja terhadap bakteri gram positif dan gentamisin hanya bekerja terhadap bakteri gram negatif.
2.1.3 Golongan antibiotik yang digunakan pada Terapi Profilaksis
Antibiotik beta-laktam merupakan obat yang menghambat sintesis atau merusak dinding sel bakteri.Terdiri dari berbagai golongan obat yang
mempunyai struktur cincin beta-laktam, yaitu penisilin, sefalosporin, monobaktam, karbapenem, dan inhibitor beta-laktamase.Obat-obat antibiotik beta-laktam umumnya bersifat bakterisid, dan sebagian besar efektif terhadap organisme Gram-positif dan negatif.Antibiotik beta-laktam mengganggu sintesis dinding sel bakteri, dengan menghambat langkah terakhir dalam sintesis peptidoglikan, yaitu heteropolimer yang memberikan stabilitas mekanik pada dinding sel bakteri (Kemenkes, 2011).
Golongan penisilin diklasifikasikan berdasarkan spektrum aktivitas antibiotiknya.Salah satu golongan penisilin yang digunakan sebagai terapi sefalosporin adalah golongan aminopenisilin, sebagai contoh Ampisilin dan Amoksisilin.Selain mempunyai aktivitas terhadap bakteri Gram-positif, juga mencakup mikroorganisme Gram-negatif, seperti Haemophilus influenzae, Escherichia coli, dan Proteus mirabilis.Obat-obat ini sering diberikan bersama inhibitor beta-laktamase (asam klavulanat, sulbaktam, tazobaktam) untuk mencegah hidrolisis oleh beta-laktamase yang semakin banyak ditemukan pada bakteri Gram-negatif. Obat Ampisilin diberikan secara intramuskular, intravena dan oral sedangkan obat Amoksisilin hanya dapat diberikan secara oral dengan waktu paruh obat yaitu, 1,1-1,5 jam untuk ampisilin dan 1,2-2,0 jam untuk amoksisilin (Kemenkes, 2011).
Sefalosporin menghambat sintesis dinding sel bakteri dengan mekanisme serupa dengan penisilin. Sefalosporin diklasifikasikan berdasarkan generasinya, yaitu generasi I hingga IV (Setiabudy, 2011) :
- Generasi I, yaitu Sefaleksin, sefalotin, sefazolin, sefradin dan sefadroksil merupakan antibiotik yang efektif terhadap Gram-positif dan memiliki aktivitas sedang terhadap Gram-negatif.
- Generasi II, yaitu Sefaklor, sefamandol, sefuroksim, sefoksitin, sefotetan, sefmetazol dan sefprozil memiliki aktivitas antibiotik Gram-negatif yang lebih tinggi daripada generasi I.
- Generasi III, yaitu Sefotaksim, seftriakson, seftazidim, sefiksim, sefoperazon, seftizoksim, sefpodoksim dan moksalaktam. Memiliki aktivitas kurang aktif terhadap kokus Gram-postif dibanding generasi I, tapi lebih aktif terhadap Enterobacteriaceae, termasuk strain yang memproduksi beta-laktamase. Seftazidim dan sefoperazon juga aktif terhadap P.aeruginosa, tapi kurang aktif dibanding generasi III lainnya terhadap kokus Gram-positif.
- Generasi IV, yaitu sefepim dan sefpirom memiliki aktivitas lebih luas dibanding generasi III dan tahan terhadap beta-laktamase.
Banyak rumah sakit di negara berkembang menggunakan antibiotik sefalosporin dalam jumlah berlebihan, terutama di bagian bedah sebagai pilihan antibiotik profilaksis. Mikroorganisme yang digunakan sebagai terapi sefalosporin adalah organisme komensal, seperti stafilokokkus gram negatif, Pseudomonas aeruginosa, enterococci dan Candida albicans, dan organisme yang lebih patogen seperti Clostridium difficile, penicillin-resistant pneumococci, multiply-resistant coliforms dan methicillin-resistant Staphylococcus aureus (MRSA). Beberapa organisme ini secara konstitutif resisten terhadap sefalosporin sementara yang lain telah resisten, biasanya akibat resistensi ganda.(Dancer, 2001).
2.1.4. Farmakokinetik dan Farmakodinamik Antibiotik
Pemahaman mengenai sifat farmakokinetik dan farmakodinamik antibiotik sangat diperlukan untuk menetapkan jenis dan dosis antibiotik secara tepat. Agar dapat menunjukkan aktivitasnya sebagai bakterisida ataupun bakteriostatik, antibiotik harus memiliki beberapa sifat berikut ini (Kemenkes, 2011, Setiabudy, 2011) :
a. Aktivitas mikrobiologi. Antibiotik harus terikat pada tempat ikatan spesifiknya (misalnya ribosom atau ikatan penisilin pada protein).
b. Kadar antibiotik pada tempat infeksi harus cukup tinggi. Semakin tinggi kadar antibiotik semakin banyak tempat ikatannya pada sel bakteri.
c. Antibiotik harus tetap berada pada tempat ikatannya untuk waktu yang cukup memadai agar diperoleh efek yang adekuat.
d. Kadar hambat minimal. Kadar ini menggambarkan jumlah minimal obat yang diperlukan untuk menghambat pertumbuhan bakteri.
Secara umum terdapat dua kelompok antibiotik berdasarkan sifat farmakokinetikanya, yaitu;
a. Time dependent killing. Lamanya antibiotik berada dalam darah dalam kadar diatas Kadar Hambat Minimum (KHM) sangat penting untuk memperkirakan outcome klinik ataupun kesembuhan. Pada kelompok ini kadar antibiotik dalam darah diatas KHM paling tidak selama 50% interval dosis. Contoh antibiotik yang tergolong time dependent killing antara lain penisilin, sefalosporin, dan makrolida.
b. Concentration dependent. Semakin tinggi kadar antibiotika dalam darah melampaui KHM maka semakin tinggi pula daya bunuhnya terhadap bakteri. Untuk kelompok ini diperlukan rasio kadar/ KHM sekitar 10. Ini mengandung arti bahwa rejimen dosis yang dipilih haruslah memiliki kadar dalam serum atau jaringan 10 kali lebih tinggi dari KHM. Jika gagal mencapai kadar ini di tempat infeksi atau jaringan akan mengakibatkan kegagalan terapi. Situasi inilah yang selanjutnya menjadi salah satu penyebab timbulnya resistensi.
Farmakokinetik (PK) membahas tentang perjalanan kadar antibiotik di dalam tubuh, sedangkan farmakodinamik (PD) membahas tentang hubungan antara kadar-kadar itu dan efek antibiotiknya. Dosis antibiotik dulunya hanya ditentukan oleh parameter PK saja. Namun, ternyata PD juga memainkan peran yang sama, atau bahkan lebih penting. Pada abad resistensi antibiotika yang terus meningkat ini, PD bahkan menjadi lebih penting lagi, karena parameter-parameter ini bisa digunakan untuk mendesain rejimen dosis yang melawan atau mencegah resistensi.Jadi walaupun efikasi klinis dan keamanan masih menjadi standar emas untuk membandingkan antibiotik, ukuran farmakokinetik dan
farmakodinamik telah semakin sering digunakan.Beberapa ukuran PK dan PD lebih prediktif terhadap efikasi klinis. (Kemenkes RI, 2011)
2.1.5Prinsip Penggunaan Antibiotik
Penggunaan antibitik yang rasional didasarkan pada pemahaman dari banyak aspek penyakit infeksi.Faktor yang berhubungan dengan pertahanan tubuh pasien, identitas, virulensi dan kepekaan mikroorganisme, farmakokinetika dan farmakodinamika dari antibiotik perlu diperhatikan (Gould IM, et. al., 2005).
Pada fasilitas pelayanan kesehatan, antibiotik digunakan pada keadaan berikut (Gyssens, 2005; Kemenkes RI.,2011) :
1. Terapi empiris.
Pemberian antibiotika untuk mengobati infeksi aktif pada pendekatan buta (blind) sebelum mikroorganisme penyebab diidentifikasi dan antibiotik yang sensitif ditentukan.Tujuan pemberian antibiotik untuk terapi empiris adalah eradikasi atau penghambatan pertumbuhan bakteri yang diduga menjadi penyebab infeksi, sebelum diperoleh hasil pemeriksaan mikrobiologi.
Indikasi pemberian antibiotik pada terapi empiris adalah ditemukan sindrom klinis yang mengarah pada keterlibatan bakteri tertentu yang paling sering menjadi penyebab infeksi.Rute pemberian pada antibiotik oral seharusnya menjadi pilihan pertama untuk terapi infeksi.Pada infeksi sedang sampai berat dapat dipertimbangkan menggunakan antibiotik parenteral.durasi pemberian pada antibiotik empiris diberikan untuk jangka waktu 48-72jam.
2. Terapi definitif.
Pemberian antibiotik untuk mikroorganisme spesifik yang menyebabkan infeksi aktif atau laten. Penggunaan antibiotik untuk terapi definitif adalah penggunaan antibiotik pada kasus infeksi yang sudah diketahui jenis bakteri penyebab dan pola resistensinya.Tujuan pemberian antibiotik untuk terapi definitif adalah eradikasi atau penghambatan pertumbuhan bakteri yang menjadi penyebab infeksi,
berdasarkan hasil pemeriksaan mikrobiologi.Indikasi pemberian antibiotik pada terapi definitif adalah sesuai dengan hasil mikrobiologi yang menjadi penyebab infeksi.
Rute pemberian adalah antibiotik oral seharusnya menjadi pilihan pertama untuk terapi infeksi.Pada infeksi sedang sampai berat dapat dipertimbangkan menggunakan antibiotik parenteral.Jika kondisi pasien memungkinkan, pemberian antibiotik parenteral harus segera diganti dengan antibiotik peroral.Durasi pemberian antibiotik definitif berdasarkan pada efikasi klinis untuk eradikasi bakteri sesuai diagnosis awal yang telah dikonfirmasi.
3. Terapi profilaksis
Pemberian antibiotik profilaksis untuk mencegah timbulnya infeksi.Pemberian antibiotik sebelum, saat dan hingga 24 jam pasca operasi pada kasus yang secara klinis tidak didapatkan tanda-tanda infeksi dengan tujuan untuk mencegah terjadi infeksi luka operasi. Diharapkan pada saat operasi antibiotik di jaringan target operasi sudah mencapai kadar optimal yang efektif untuk menghambat pertumbuhan bakteri.
2.2.Antibiotika Profilaksis
2.2.1Definisi Antibiotik Profilaksis
Antibiotik profilaksis adalah antibiotik yang digunakan pada pasien yang belum terkena infeksi, tetapi diduga mempunyai peluang besar untuk mendapatkannya, atau bila terkena infeksi dapat menimbulkan dampak buruk bagi pasien. Obat-obatan profilaksis harus diarahkan terhadap organisme yang mempunyai kemungkinan terbesar dapat menyebabkan infeksi, tetapi tidak harus membunuh atau melemahkan seluruh pathogen (Kemenkes RI, 2011)
Profilaksis merujuk pada pencegahan infeksi dan dapat dikategorikan menjadi profilaksis primer, sekunder, atau eradikasi.Profilaksis primer merupakan pencegahan pada infeksi awal.Sedangkan profilaksis sekunder merupakan pencegahan dari munculnya kembali atau re-aktivasi dari infeksi
yang sudah ada.Dan eradikasi merupakan eliminasi dari organisme kolonisasi untuk mencegah perkembangan infeksi (Thirion, 2013; Ongom 2013).
2.2.2 Tujuan Pemberian Antibiotik Profilaksis
Tujuan dari pemberian antibiotik profilaksis adalah untuk mengurangi insidensi infeksi luka pasca bedah.Profilaksis merupakan prosedur yang berhubungan dengan angka infeksi yang tinggi. Antibiotik sebaiknya dapat menutupi organisme yang paling mungkin akan mengkontaminasi dan akan berada di jaringan pada saat dilakukan insisi awal. Antibiotik profilaksis dibutuhkan dalam keadaan – keadaan berikut (Kemenkes RI, 2011):
1. Untuk melindungi seseorang yang terkena kuman tertentu.
2. Mencegah endokarditis pada pasien yang mengalami kelainan katup jantung atau defek septum yang akan menjalani prosedur dengan resiko bakteremia, misalnya ekstrasi gigi, pembedahan dan lain – lain.
3. Untuk kasus bedah, profilaksis diberikan untuk tindakan bedah tertentu yang sering disertai infeksi pasca bedah atau yang berakibat berat bila terjadi infeksi pasca bedah.
Idealnya sediaan antibiotik yang digunakan untuk profilaksis pada operasi harus :
1. Mencegah infeksi luka pasca operasi pada luka operasi 2. Mencegah morbiditas dan mortalitas infeksi pascaoperasi 3. Mengurangi durasi dan biaya perawatan
4. Tidak menimbulkan efek yang merugikan baik bagi flora normal pasien dan bagi rumah sakit.
Diharapkan dari pemberian antibiotik profilaksis dapat memberikan manfaat yaitu :
a. Penurunan angka kejadian infeksi pasca bedah b. Penurunan jumlah flora pathogen penyebab infeksi
d. Pengurangan biaya dan lamanya rawat inap di rumah sakit
e. Terhindarinya pembentukan resistensi antibiotik serta peningkatan kondisi pasien
f. Kualitas hidup pasien pasca operasi.
Penggunaan antibiotik merupakan sejarah dalam upaya mencegah luka infeksi.Konsep antibiotik profilaksis diperkenalkan tahun 1960an ketika data eksperimen menetapkan bahwa antibiotik harus berada dalam sistem peredaran darah pada dosis yang cukup tinggi pada saat insisi supaya efektif.Umumnya disepakati bahwa antibiotik profilaksis
diindikasikan untuk luka yang terkontaminasi dan
terkontaminasi.Antibiotik untuk luka kotor merupakan bagian dari terapi karena infeksi sudah terbentuk.Sedangkan pada prosedur operasi bersih masih menjadi perdebatan.Pada penggunaan antibiotik profilaksis dalam prosedur bersih dimana alat buatan palsu dimasukkan. Infeksi dalam kasus ini akan menjadi bencana bagi pasien. Namun, prosedur bersih lainnya (misalnya operasi payudara) masih menjadi perdebatan (Singhal, 2017),
Kriteria penggunaan antibiotik profilaksis sistemik dalam prosedur pembedahan adalah sebagai berikut:
• Antibiotik profilaksis sistemik harus digunakan dalam kasus berikut: Risiko infeksi yang tinggi dikaitkan dengan prosedur (misalnya reseksi usus besar); Konsekuensi infeksi sangat parah (misalnya penggantian total sendi); pasien memiliki indeks risiko NNIS yang tinggi.
• Antibiotik harus diberikan sebelum operasi tetapi mendekati waktu insisi seperti pada kebanyakan kasus antibiotik harus diberikan sebelum induksi anestesi.
• Antibiotik yang dipilih harus memiliki aktivitas melawan patogen yang mungkin dalam prosedur tersebut.
• Pemberian antibiotik sistemik pasca operasi lebih dari 24 jam belum ditunjukkan untuk mengurangi risiko infeksi luka operasi.
Berdasarkan CDC, Indeks risiko NNIS (National Nosocomial Infections Surveillance) adalah metode penyesuaian risiko yang paling
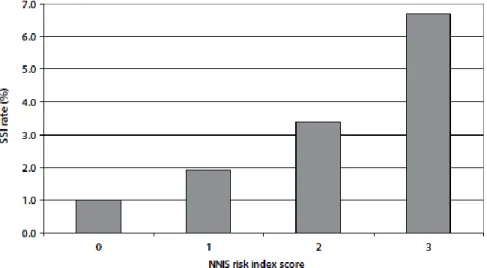
banyak digunakan secara internasional. Penyesuaian risiko didasarkan pada tiga faktor risiko utama: Skor American Society of Anesthesiologists (ASA) , yang mencerminkan kondisi kesehatan pasien sebelum operasi, kelas luka yang mencerminkan keadaan kontaminasi, dan durasi operasi, yang mencerminkan aspek teknis pembedahan. Indeks risiko NNIS dinilai nol, satu, dua atau tiga sesuai dengan jumlah risiko yang ada (skor ASA,kelas luka, durasi operasi).Tingkat infeksi meningkat dengan meningkatnya skor risiko (lihat Gambar 1) (SIGN, 2014).
Gambar 1.Kejadian Infeksi Luka Operasi seiring meningkatnya skor risiko indeks NNIS (SIGN, 2014).
Patogen normal pada permukaan kulit dan mukosa adalah kokkus-gram positif (terutama stafilokokus); Namun, kuman aerob kokkus-gram negatif dan bakteri anaerob dapat mengkontaminasi kulit di daerah pangkal paha/perineum.Patogen yang terkontaminasi dalam operasi gastrointestinal adalah banyak flora usus intrinsik, yang meliputi bakteri gram negatif basili (misalnya Escherichia coli) dan mikroba gram positif, termasuk organisme enterococci dan anaerob (Lihat Tabel 1 di bawah).Organisme gram positif, terutama stafilokokus dan streptokokus, menjelaskan kebanyakan flora luar yang terlibat dalam infeksi luka operasi.Asal patogen semacam itu termasuk dari personil bedah / rumah sakit dan
keadaan intraoperatif, termasuk instrumen bedah, barang yang dibawa ke lapangan operasi, dan udara ruang operasi. (Singhal, 2017)
Kelompok bakteri yang paling sering bertanggung jawab untuk infeksi luka operasi adalah strain Staphylococcus aureus. Munculnya strain resisten telah meningkatkan angka morbiditas dan mortalitas yang terkait dengan infeksi luka.Methicillin-resistant Staphylococcus aureus (MRSA) terbukti menjadi masalah utama pada operasi. Seperti strain S Aureus lainnya, MRSA dapat berkoloni di kulit dan tubuh seseorang tanpa menyebabkan penyakit, dan dengan cara ini, dapat disebarkan ke orang lain tanpa sadar. Timbulnya masalah dalam pengobatan infeksi MRSA karena pilihan antibiotik sangat terbatas. Infeksi MRSA tampak meningkat dan menunjukkan resistensi terhadap antibiotik yang lebih luas. Yang menjadi perhatian khusus adalah vancomycin intermediate S aureus (VISA) bagian dari MRSA. Strain ini mulai resisten terhadap vankomisin, yang saat ini merupakan antibiotik yang paling efektif melawan MRSA. Resistensi ini baru muncul karena jenis bakteri lain, yang disebut enterococci, umumnya menunjukkan resisten terhadap vankomisin (Hsiao, 2012).
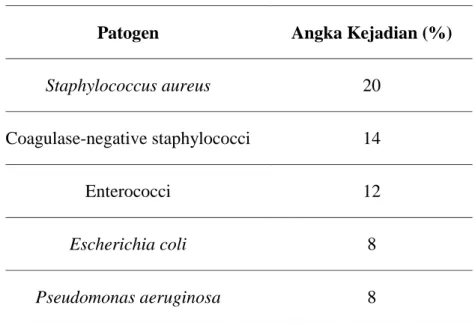
Tabel 1. Patogen yang Berkaitan dengan Infeksi Luka dan Angka Kejadiannya (Singhal, 2017)
Patogen Angka Kejadian (%)
Staphylococcus aureus 20
Coagulase-negative staphylococci 14
Enterococci 12
Escherichia coli 8
Enterobacter species 7
Proteus mirabilis 3
Klebsiella pneumoniae 3
Infeksi Terkait Pelayanan Kesehatan (Health Care Associated Infections/HAI) merupakan infeksi yang terjadi pada pasien selama perawatan di rumah sakit dan fasilitas pelayanan kesehatan lainnya dimana ketika masuk tidak ada infeksi dan tidak dalam masa inkubasi, termasuk infeksi dalam rumah sakit tapi muncul setelah pasien pulang, juga infeksi karena pekerjaan pada petugas rumah sakit dan tenaga kesehatan terkait proses pelayanan kesehatan di fasilitas pelayanan kesehatan(Permenkes, 2017).
Infeksi daerah operasi paling banyak bersumber dari patogen flora endogenous kulit pasien, membran mukosa.Bila membran mukosa atau kulit di insisi, jaringan tereksposur risiko dengan flora endogenous.Selain itu terdapat sumber exogenous dari infeksi daerah operasi. Sumber exogenous tersebut adalah tim bedah, lingkungan ruang operasi, peralatan, instrumen dan alat kesehatan, kolonisasi mikroorganisme, daya tahan tubuh lemah, lama rawat inap pra bedah (Permenkes, 2017).
RSUP Sanglah Denpasar sendiri rutin dilakukan pemeriksaan sterilitas di ruang operasi. Berdasarkan hasil pemeriksaan pada September 2017 ditemukan bakteri Staphylococcus coagulase negatif dan Pseudomonas alcaligenes positif dengan Jumlah Koloni : 625 cfu/m3 di kamar operasi 1 (OK IBS 1). Seperti kita ketahui, bakteri Staphylococcus coagulase negatif merupakan flora normal kulit dan bakteri Pseudomonas alcaligenes merupakan bakteri lingkungan yang dapat menyebabkan infeksi oportunisik rumah sakit pada penderita dengan sistem imunitas yang menurun. Dari segi indeks angka kuman menurut fungsi ruang yang
mengacu pada Permenkes RI No 1204/Menkes/SK/X/2004 semua ruangan tersebut tidak layak digunakan.
RSUP Sanglah Denpasar juga melakukan pemeriksaan lanjutan pada 10 November 2017, dari hasil pemeriksaan tersebut ditemukan bakteri Pseudomonas stutzeri dengan jumlah koloni : 6 cfu/m3 pada kamar operasi I IBS (OK I IBS) dan juga bakteri Bacillus sp dengan jumlah koloni : 23 cfu/m3 pada kamar operasi 3 IBS (OK 3 IBS). Diidentifikasi bakteri Bacillus sp, Pseudomonas stutzeri merupakan bakteri lingkungan yang dapat menyebabkan infeksi oportunistik rumah sakit pada penderita dengan sistem imunitas yang menurun. Dari segi indeks angka kuman menurut fungsi ruang yang mengacu pada Permenkes RI No 1204/Menkes/SK/X/2004 ruangan OK III tidak layak digunakan, OK I layak digunakan.
2.2.3. Indikasi Penggunaan Antibiotik Profilaksis
Indikasi penggunaan antibiotik profilaksis didasarkan pada kelas operasi, yaitu operasi bersih, operasi bersih – kontaminasi, operasi kontaminasi serta operasi kotor (lihat tabel 2) (SIGN, 2014).Tujuan pemberian antibiotik profilaksis pada kasus pembedahan adalah terjadi penurunan dan pencegahan kejadian Infeksi Luka Operasi (ILO), penurunan morbiditas dan mortalitas pascaoperasi, penghambatan muncul flora normal yang resisten dan meminimalkan biaya pelayanan kesehatan (Kemenkes RI, 2011).
Tabel 2. Klasifikasi Operasi (Mayhall Classification) (SIGN, 2014) Kelas
Operasi
Definisi Penggunaan Antibiotik
Operasi Bersih Operasi yang dilakukan pada daerah dengan kondisi pra bedah tanpa infeksi, tanpa membuka traktus (respiratorius, gastro intestinal, urinarius, bilier), operasi terencana, atau penutupan kulit primer dengan atau tanpa
Kelas operasi bersih terencana umumnya tidak memerlukan antibiotik profilaksis kecuali pada beberapa jenis operasi, misalnya mata, jantung, dan sendi.
digunakan drain tertutup.
Operasi Bersih
– Kontaminasi Operasi yang dilakukan pada traktus (digestivus, bilier, urinarius, respiratorius,
reproduksi kecuali ovarium) atau operasi tanpa disertai kontaminasi yang nyata.
Pemberian antibiotika profilaksis pada kelas operasi bersih kontaminasi perlu dipertimbangkan manfaat dan risikonya karena bukti ilmiah mengenai efektivitas antibiotik profilaksis belum ditemukan. Operasi
Kontaminasi
Operasi yang membuka saluran cerna, saluran empedu, saluran kemih, saluran napas sampai orofaring, saluran reproduksi kecuali ovarium atau operasi yang tanpa pencemaran nyata (Gross Spillage).
Kelas operasi kontaminasi memerlukan antibiotik terapi (bukan profilaksis).
Operasi Kotor Adalah operasi pada perforasi saluran cerna, saluran urogenital atau saluran napas yang terinfeksi ataupun operasi yang melibatkan daerah yang purulen
(inflamasi bakterial). Dapat pula operasi pada luka terbuka lebih dari 4 jam setelah kejadian atau terdapat jaringan non vital yang luas atau nyata kotor.
Kelas operasi kotor memerlukan antibiotik terapi.
Lanjutan tabel 2. Antibiotik profilaksis diberikan pada pembedahan dengan klasifikasi operasi bersih-terkontaminasi (lihat tabel 3).Profilaksis pada operasi bersih pada umumnya tidak diperlukan, namun dapat diberikan pada operasi bersih dengan memasang alat implan atau bahan protesis. Namun tidak menutup kemungkinan juga diberikan antibiotik profilaksis jika diindikasikan akan terjadi infeksi yang dapat menimbulkan dampak yang serius seperti operasi bedah syaraf, bedah jantung dan mata. Operasi kontaminasi dan operasi kotor telah terjadi kolonisasi kuman dalam jumlah besar atau sudah ada infeksi yang secara klinis belum bermanifestasi. Untuk kasus ini terapi empirik akan lebih tepat (David, 2010).
2.2.4. Dasar Pemberian Antibiotik profilaksis pada Operasi
Dasar pemilihan jenis antibiotik untuk tujuan profilaksis yaitu sesuai dengan sensitivitas dan pola bakteri patogen terbanyak pada kasus bersangkutan dan spektrum sempit untuk mengurangi risiko resistensi bakteri, toksisitas rendah, tidak menimbulkan reaksi merugikan terhadap pemberian obat anestesi, bersifat bakterisidal dan harga terjangkau (Ongom, 2013).
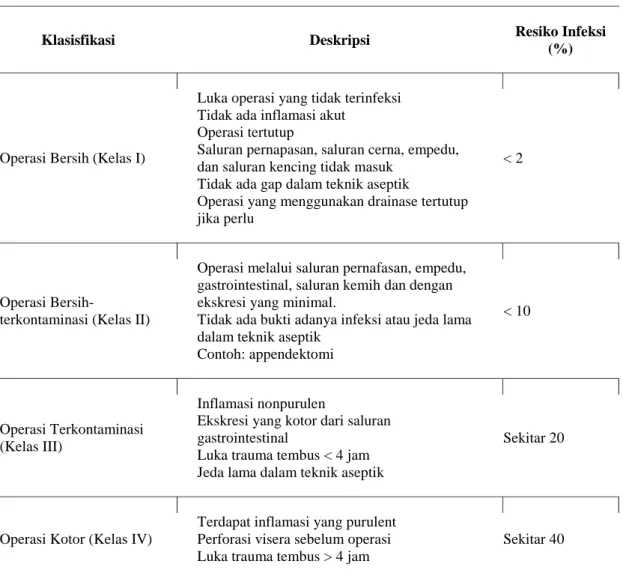
Tabel 3. Klasifikasi luka operasi dan risiko infeksi selanjutnya (jika tidak menggunakanantibiotik) (Singhal, 2017)
Klasisfikasi Deskripsi Resiko Infeksi
(%)
Operasi Bersih (Kelas I)
Luka operasi yang tidak terinfeksi Tidak ada inflamasi akut
Operasi tertutup
Saluran pernapasan, saluran cerna, empedu, dan saluran kencing tidak masuk
Tidak ada gap dalam teknik aseptik
Operasi yang menggunakan drainase tertutup jika perlu
< 2
Operasi
Bersih-terkontaminasi (Kelas II)
Operasi melalui saluran pernafasan, empedu, gastrointestinal, saluran kemih dan dengan ekskresi yang minimal.
Tidak ada bukti adanya infeksi atau jeda lama dalam teknik aseptik
Contoh: appendektomi
< 10
Operasi Terkontaminasi (Kelas III)
Inflamasi nonpurulen
Ekskresi yang kotor dari saluran gastrointestinal
Luka trauma tembus < 4 jam Jeda lama dalam teknik aseptik
Sekitar 20
Operasi Kotor (Kelas IV)
Terdapat inflamasi yang purulent Perforasi visera sebelum operasi Luka trauma tembus > 4 jam
Sekitar 40
Antibiotik profilaksis hanya bisa digunakan jika terbukti dapat memberikan keuntungan dan harus dihentikan bila terbukti tidak
memberikan manfaat. SIGN dalam guideline-nya membagi 4 rekomendasi terhadap pemberian antibiotik profilaksis pada operasi (SIGN, 2014).
a. Highly Recomendation, Profilaksis yang dengan terbukti tegas menurunkan morbiditas, menurunkan biaya perawatan dan menurunkan konsumsi antibiotik secara keseluruhan.
b. Recomended; Profilaksis yang menurunkan morbilitas jangka pendek, mengurangi biaya perawatan dan bila dimungkinkan menurunkan konsumsi antibiotik secara keseluruhan.
c. Should be considered; Profilaksis yang belum memiliki bukti yang kuat dapat memberikan keuntungan, dan kemungkinan dapat meningkatkan biaya perawatan dan peningkatan konsumsi antibiotk utamanya untuk pasien dengan low risk ILO.
d. Not recomended; profilaksis yang tidak memiliki bukti kuat efektif secara klinis serta tidak menurunkan morbiditas jangka pendek. Dan dapat meningkatkan biaya perawatan serta meningkatkan konsumsi antibiotik sedangkan keuntungan secara klinis sangat rendah.
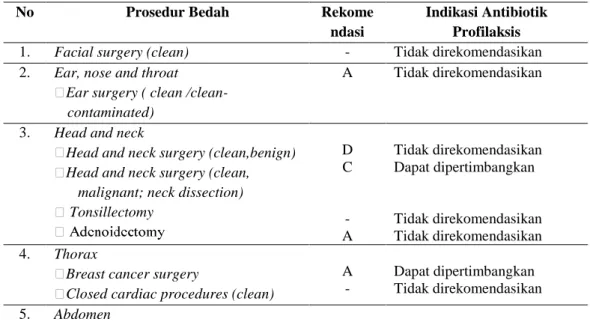
Rekomendasi antibiotik yang digunakan pada profilaksis bedah pada operasi bersih secara rinci diuraikan pada tabel 4.
Tabel 4.Rekomendasi Antibiotik Profilaksis Bedah Operasi Bersih (Kemenkes RI, 2011).
No Prosedur Bedah Rekome
ndasi
Indikasi Antibiotik Profilaksis 1. Facial surgery (clean) - Tidak direkomendasikan 2. Ear, nose and throat
Ear surgery ( clean /clean-contaminated)
A Tidak direkomendasikan
3. Head and neck
Head and neck surgery (clean,benign) Head and neck surgery (clean,
malignant; neck dissection) Tonsillectomy D C - A Tidak direkomendasikan Dapat dipertimbangkan Tidak direkomendasikan Tidak direkomendasikan 4. Thorax
Breast cancer surgery
Closed cardiac procedures (clean)
A -
Dapat dipertimbangkan Tidak direkomendasikan 5. Abdomen
Hernia repair-groin (inguinal/femoral with or without mesh)
Hernia repair-groin (laparoscopic with or without mesh)
Hernia repair ( incisional with or without mesh)
Open/laparoscopic surgery with mesh Diagnostic endoscopic procedures Therapeutic endoscopic procedures (endoscopic retrograde cholangiopancreatography and percutaneous endoscopic gastrostomy) A B C B D D Tidak direkomendasikan Tidak direkomendasikan Tidak direkomendasikan Tidak direkomendasikan Tidak direkomendasikan Dapat dipertimbangkan pada pasien resiko tinggi
6. Urogenital
Transrectal prostate biopsy A Direkomedasikan 7. Orthopaedic surgery (without implant) D Tidak direkomendasikan
Keterangan: Lanjutan tabel 4.
A : Bukti ilmiah berasal dari paling tidak satu meta analisis, sistematik review atau Randomized Controlled Trial (RCT) yang mempunyai level 1++ dan dapat secara langsung diaplikasikan ke populasi target, atau Bukti ilmiah berasal dari beberapa penelitian dengan level 1+ dan menunjukkan adanya konsistensi hasil, serta dapat secara langsung diaplikasikan ke populasi target.
B : Bukti ilmiah berasal dari beberapa penelitian dengan level 2++ dan menunjukkan adanya konsistensi hasil, serta dapat secara langsung diaplikasikan ke populasi target, atau Ekstrapolasi bukti ilmiah dari penelitian level 1++ atau 1+.
C : Bukti ilmiah berasal dari beberapa penelitian dengan level 2+ dan menunjukkan adanya konsistensi hasil, serta dapat secara langsung diaplikasikan ke populasi target, atau Ekstrapolasi bukti ilmiah dari penelitian level 2++.
D : Bukti ilmiah berasal dari level 3 atau 4, atau Ekstrapolasi bukti ilmiah dari penelitian level 2+
2.2.5. Pemilihan Antibiotik Profilaksis pada Operasi
Pemilihan antibiotik profilaksis dipengaruhi oleh beberapa faktor.Oleh karena itu penting untuk menanyakan ke pasien tentang riwayat penggunaan antibiotik dan alergi.Betalaktam merupakan antibiotik yang banyak digunakan sebagai profilaksis.Bila terdapat riwayat alergi penisilin yang berat (anafilaksis atau angiodema) menunjukkan bahwa pasien tidak dapat menerima penisilin dan juga berarti sefalosporin juga dikontraindikasikan terhadap pasien tersebut.Meski cukup sederhana, tapi dapat memberikan dampak reaksi yang signifikan. Paling penting yang harus diperhatikan yaitu antibiotik harus aktif terhadap bakteri yang dapat menyebabkan Infeksi Luka Operasi (ILO) (Kemenkes,2011).
Umumnya infeksi pascaoperasi disebabkan oleh bakteri flora pasien itu sendiri.Profilaksis tidak harus dapat menghambat semua jenis bakteri flora pasien tersebut.Ada beberapa bakteri yang tidak bersifat patogen atau jumlahnya hanya sedikit atau keduanya.Sangat penting untuk memilih antibiotik dengan spektrum sempit sesuai dengan yang dibutuhkan untuk meminimalisir multi resisten terhadap antibiotik.
Pemilihan antibiotik harus didasarkan pada biaya, profil efek yang dapat merugikan, kemudahan pemberian, profil farmakokinetik, dan aktifitas antibakterinya.Antibiotik yang dipilih harus memiliki aktivitas terhadap bakteri yang sering mengakibatkan infeksi pada operasi. Pada operasi bersih terkontaminasi, antibiotik yang digunakan harus efektif terhadap bakteri patogen yang terdapat dalam saluran gastrointestinal dan genitourinari. Pada operasi bersih, bakteri gram positif cocci (S. aureus dan S. epidermidis) paling banyak ditemukan(Munckhof,2005).Kualitas antibiotik profilaksis meliputi efikasi terhadap mikroorganisme bakteri yang diduga paling mungkin menyebabkan infeksi, penetrasi jaringan yang baik untuk mencapai luka, efektivitas biaya, dan gangguan yang minim pada flora intrinsik tubuh (misalnya usus) (Woodfield, 2009).
Antibiotik pilihan yang digunakan pada profilaksis bedah adalah golongan sefalosporin generasi I-II.Pada kasus tertentu yang dicurigai melibatkan bakteri anaerob dapat ditambahkan metronidazol.Selain itu, tidak dianjurkan menggunakan sefalosporin generasi III dan IV, golongan karbapenem, dan golongan kuinolon untuk profilaksis bedah.Antibiotik spektrum luas mungkin akan dibutuhkan kemudian jika pasien mengalami sepsis yang serius. Oleh karena itu penggunaan sefalosporin generasi ketiga seperti ceftriakson dan cefatoksim harus dihindari sebagai profilaksis pada operasi (Munckhof,2005).
Kebanyakan prosedur cefazolin merupakan antibiotik pilihan karena durasinya panjang, dan efektif melawan bakteri yang banyak menyebabkan infeksi saat operasi disamping itu harganya juga relatif
murah.Pemberian secara parenteral sefalosporin generasi kedua misalnya cefotetan memiliki aktifitas antibakteri yang lebih baik terhadap bakteri anaerobik dan aerobik Garam negatif bila dibandingkan dengan sefalosporin generasi pertama dan kadang-kadang juga menjadi pilihan yang lebih disukai, namun lebih mahal. Alternatif lain yang dapat digunakan yaitu dengan kombinasi metronidazol dengansefalosporin generasi pertama atau dengan gentamisin untuk profilaksis pada operasi abdominal (Munckhof,2005).
Meskipun berbagai organisme dapat menyebabkan infeksi pada pasien bedah, Infeksi luka operasi biasanya diakibatkan oleh sejumlah kecil patogen umum (kecuali dengan adanya implantasi biomaterial).Hal tersebut dapat dilihat pada tabel 5.Hanya patogen tersebut yang perlu dicakup oleh antibiotik yang diresepkan. (SIGN, 2014)
Berikut ini adalah antibiotik yang sering digunakan sebagai profilaksis pada operasi (Munckhof,2005) :
a. Sefalosporin generasi pertama (cefazolin atau cefalotin) b. Gentamisin
c. Metronidazol (jika disebabkan oleh bakteri anaerobik) d. Oral tinidazol (jika disebabkan oleh bakteri anaerobik)
e. Flucloxacillin (jika infeksi methicillin-susceptible staphylococcal) f. Vankomicin (jika infeksi methicillin-resistant Staphylococcal)
Tabel 5.Patogen Umum yang ditemukan pada infeksi luka operasi dan antibiotik yang sesuai
(SIGN,2014).
2.2.6. Jalur dan Waktu Pemberian Antibiotik Profilaksis
Antibiotik profilaksis biasanya diberikan sebagai bolus intravena yang disertai dengan induksi anastesi untuk memastikan konsentrasi efektif pada jaringan tercapai sebelum pembedahan dimulai.Idealnya diberikan pada saat induksi anestesi.Untuk menghindari risiko yang tidak diharapkan dianjurkan pemberian antibiotik intravena drip.Waktu pemberian antibiotik ini sangat penting utamanya untuk beta-laktam yang memiliki waktu paruh relatif singkat. Vankomisin membutuhkan waktu infus selama satu jam oleh karena itu pemberiannya harus dimulai lebih cepat agar infus selesai tepat ketika pembedahan akan dimulai. Pemberian
antibiotik profilaksis secara intramuskular jarang dilakukan dibandingkan intravena. Pemberiannya biasanya dilakukan beberapa saat sebelum operasi karena waktu yang dibutuhkan untuk mencapai level konsentrasi antibiotik yang efektif pada jaringan cukup lama (ASF, 2003; SIGN, 2014).
Cara pemberian antibiotik bedah profilaksis agar efektif adalah dosis pertama antibiotik profilaksis harus sedekat mungkin dengan waktu operasi.Pada luka yang bersih, apabila operasinya kurang dari dua jam, cukup satu dosis.Namun, jika luka bersih terkontaminasi, satu atau dua dosis sebelum dan setelah operasi.Dan pada luka yang terkontaminasi, antibiotik diberi selama dua atau tiga hari dan diberikan melalui intravena dosis tinggi (Tjay, 2007).
Oral dan rektal juga harus diberikan lebih awal untuk memastikan kadar efektif pada jaringan telah tercapi pada saat pembedahan. Metronidazol suppositoria banyak digunakan pada pembedahan usus besar dan harus diberikan 2-4 jam sebelum tindakan operasi dilakukan.Antibiotik topikal tidak direkomendasikan kecuali untuk bedah mata atau akibat luka bakar.(ASF, 2003; SIGN, 2014).Rekomendasi pemberian antibiotik profilaksis dengan jenis operasi dan infeksi mikroorganisme yang terlibat dapat dilihat pada tabel 6 di bawah ini (Bratzler et. al, 2013)
Tab el 6. Rek ome ndas i Anti bioti k Prof ilaks is den gan Jeni s Ope rasi dan Infe ksi Mik roor gani sme yan g terli bat (Bra tzler et. al, 2013 ) (lanj utan ) Tab el 6. Rek ome nda si Anti bioti k Prof ilak sis den gan Jeni s Ope rasi dan Infe ksi Mik roor gani sme yan g terli bat (Bra tzler et. al, 201 3)
Tabe l 6. Reko men dasi Anti bioti k Profi laksi s deng an Jenis Oper asi dan Infek si Mikr oorg anis me yang terlib at (Brat zler et. al, 2013) (lanj utan)
Waktu pemberian antibiotik untuk mencapai konsentrasi aktif dalam jaringan sangat bergantung pada profil farmakokinetik dan rute administrasinya.Antibiotik profilaksis yang diberikan terlalu cepat atau terlalu lambat dapat menurunkan efek dari dari antibiotik tersebut dan mungkin dapat meningkatkan resiko terjadinya ILO.Waktu pemberian antibiotik profilaksis diberikan ≤30 menit sebelum insisi kulit. Dosis pemberian untuk menjamin kadar puncak yang tinggi serta dapat berdifusi dalam jaringan dengan baik, maka diperlukan antibiotik dengan dosis yang cukup tinggi. Pada jaringan target operasi kadar antibiotik harus mencapai kadar hambat minimal hingga 2 kali lipat kadar terapi. (SIGN, 2014).
Beberapa literatur menyebutkan sebaiknya pemberian profilaksis secara intravena dilakukan < 30 menit sebelum tindakan operasi dilakukan untuk semua kategori operasi kecuali operasi sesar.National Surgical Infection Prevention Project melaporkan tingkat kepatuhan antibiotik profilaksis dalam kurun waktu 1 jam sebelum insisi adalah 55,7% (Bratzler, 2013).
2.2.7. Durasi Pemberian Antibiotik Profilaksis
Durasi pemberian antibiotik yang efektif dengan waktu yang paling singkat untuk profilaksis infeksi paska bedah belum diketahui.Untuk beberapa prosedur, durasi antimikroba profilaksis seharusnya 24 jam atau kurang, kecuali untuk operasi bedah jantung toraksyang membutuhkan durasi 72 jam.Durasi pemberian adalah dosis tunggal.Dosis ulangan dapat diberikan atas indikasi perdarahan lebih dari 1500 ml atau operasi berlangsung lebih dari 3 jam.Pemberian profilaksis lebih dari 3 jam setelah tindakan operasi akan berdampak pada penurunan efektifitasnya secara signifikan.Mempertahankan konsentrasi antibiotik setelah operasi dan pemulihan fisiologi normal setelah anastesi tidak meningkatkan efikasi dari antibiotik profilaksi, melainkan dapat meningkatkan toksisitas dan meningkatkan biaya (SIGN, 2014).
Jika operasi dilakukan selama empat jam atau kurang, pemberian antibiotik dengan dosis tunggal sudah cukup. Pada operasi dengan waktu
yang panjang lebih dari empat jam penambahan dosis antibiotik mungkin dibutuhkan untuk menjaga konsentrasi efektif antibiotik dalam jaringan, khususnya untuk antibiotik yang memiliki waktu paruh yang singkat. Pemberian antibiotik profilaksis hingga luka bedah mengering sudah dihapuskan (tidak digunakan lagi) dan tidak logis juga tidak terbukti dapat memberikan keuntungan (SIGN, 2014).
2.2.8. Prinsip Penggunaan Antibiotik Bijak (Prudent) (Kemenkes RI,2011) 1. Penggunaan antibiotik bijak yaitu penggunaan antibiotik dengan
spektrum sempit, pada indikasi yang ketat dengan dosis yang adekuat, interval dan durasi pemberian yang tepat.
2. Kebijakan penggunaan antibiotik (antibiotic policy) ditandai dengan pembatasan penggunaan antibiotik dan mengutamakan penggunaan antibiotik lini pertama.
3. Pembatasan penggunaan antibiotik dapat dilakukan dengan menerapkan pedoman penggunaan antibiotik, penerapan penggunaan antibiotik secara terbatas (restricted), dan penerapan kewenangan dalam penggunaan antibiotik tertentu (reserved antibiotics).
4.Indikasi ketat penggunaan antibiotik dimulai dengan menegakkan diagnosis penyakit infeksi, menggunakan informasi klinis dan hasil pemeriksaan laboratorium seperti mikrobiologi, serologi, dan penunjang lainnya. Antibiotik tidak diberikan pada penyakit infeksi yang disebabkan oleh virus atau penyakit yang dapat sembuh sendiri (self - limited).
5. Pemilihan jenis antibiotik harus berdasar pada :
a. Informasi tentang spektrum kuman penyebab infeksi dan pola kepekaan kuman terhadap antibiotik.
b. Hasil pemeriksaan mikrobiologi atau perkiraan kuman penyebab infeksi.
d. Melakukan deeskalasi setelah mempertimbangkan hasil mikrobiologi dan keadaan klinis pasien serta ketersediaan obat.
e. Cost effective: obat dipilih atas dasar yang paling cost effective dan aman.
6. Penerapan penggunaan antibiotik secara bijak dilakukan dengan beberapa langkah sebagai berikut:
a. Meningkatkan pemahaman tenaga kesehatan terhadap penggunaan antibiotik secara bijak.
b. Meningkatkan ketersediaan dan mutu fasilitas penunjang, dengan penguatan pada laboratorium hematologi, imunologi, dan mikrobiologi atau laboratorium lain yang berkaitan dengan penyakit infeksi.
c. Menjamin ketersediaan tenaga kesehatan yang kompeten di bidang infeksi.
d. Mengembangkan sistem penanganan penyakit infeksi secara tim (teamwork).
e. Membentuk tim pengendali dan pemantau penggunaan antibiotik secara bijak yang bersifat multidisiplin.
f. Memantau penggunaan antibiotik secara intensif dan berkesinambungan.
g. Menetapkan kebijakan dan pedoman penggunaan antibiotik secara lebih rinci ditingkat nasional, rumah sakit, fasilitas pelayanan kesehatan lainnya dan masyarakat.
2.2.9.Resistensi Antibiotik
Resistensi adalah kemampuan bakteri untuk menetralisir dan melemahkan daya kerja antibiotik.WHO mendefinisikan resistensi antimikroba sebagai resistensi mikroorganisme terhadap obat antimikroba yang pernah mampu mengobati infeksi oleh mikroorganisme tersebut.Seseorang tidak dapat menjadi resisten terhadap antibiotik. Resistensi terjadi pada mikroba, bukan pada orang atau organisme lain yang terinfeksi oleh mikroba (WHO, 2009).
Resistensi patogen mikroba terhadap antibiotik meningkat di seluruh dunia sangat pesat, sejalan dengan peningkatan morbiditas dan mortalitas yang terkait dengan infeksi yang disebabkan oleh patogen yang resisten terhadap antibiotik.Setidaknya 2 juta orang terinfeksi bakteri resisten antibiotik setiap tahun di AS saja, dan setidaknya 23.000 orang meninggal sebagai akibat langsung dari infeksi ini. Di Uni Eropa, diperkirakan 400.000 pasien dengan resisten strain bakteri setiap tahun, dimana 25.000 pasien meninggal. Akibatnya, WHO telah memperingatkan bahwa jangkauan terapeutik tidak mencukupi dalam waktu 10 tahun, menempatkan dunia berisiko memasuki era "pasca antibiotik", di mana antibiotik tidak akan lagi efektif melawan penyakit infeksi (WHO, 2009; CDC, 2014).
Bakteri dapat bersifat resisten pada obat secara intrinsik (misalnya bakteri anaerob resisten terhadap aminoglikosida) atau mendapatkan resistensi melalui mutasi terhadap gen tertentu atau membentuk gen baru. Mekanisme utama resitensi yang dilakukan bakteri yaitu inaktivasi obat, mempengaruhi atau overproduksi target antibiotik, akuisisi target baru yang tidak sensitif obat, menurunkan permeabilitas obat dan efluks aktif terhadap obat (Kasper, et.al., 2005).
Hal ini dapat terjadi dengan beberapa cara, yaitu : 1) Merusak antibiotik dengan enzim yang diproduksi. 2) Mengubah reseptor titik tangkap antibiotik.
3) Mengubah fisiko-kimiawi target sasaran antibiotik pada sel bakteri. 4) Antibiotik tidak dapat menembus dinding sel, akibat perubahan sifat
dinding sel bakteri.
5) Antibiotik masuk ke dalam sel bakteri, namun segera di keluarkan dari dalam sel melalui mekanisme transport aktif keluar sel.
Satuan resistensi dinyatakan dalam satuan KHM (Kadar Hambat Minimal) yaitu kadar terendah antibiotik (μg/mL) yang mampu menghambat tumbuh dan berkembangnya bakteri. Peningkatan nilai KHM menggambarkan tahap awal menuju resisten. Enzim perusak antibiotik
khusus terhadap golongan beta-laktam, pertama dikenal pada Tahun 1945 dengan nama penisilinase yang ditemukan pada Staphylococcus aureus dari pasien yang mendapat pengobatan penisilin. Masalah serupa juga ditemukan pada pasien terinfeksi Escherichia coli yang mendapat terapi ampisilin. Resistensi terhadap golongan beta-laktam antara lain terjadi karena perubahan atau mutasi gen penyandi protein (Penicillin Binding Protein, PBP). Ikatan obat golongan beta-laktam pada PBP akan menghambat sintesis dinding sel bakteri sehingga sel mengalami lisis (Kemenkes, 2011).
Infeksi yang disebabkan oleh mikroorganisme yang resisten terhadap antimikroba di rumah sakit dikaitkan dengan peningkatan morbiditas, mortalitas dan biaya kesehatan.Resistensi muncul bahkan pada agen antimikroba yang lebih baru dan lebih poten seperti karbapenem.Seleksi dan penyebaran mikroorganisme yang resisten terhadap antimikroba difasilitasi oleh penggunaan obat yang tidak rasional, dan pengobatan sendiri yaitu penyalahgunaan obat antibiotik.Resistensi antimikroba sangat terkait dengan penggunaan antimikroba yang tidak tepat.Diperkirakan 50% atau lebih penggunaan antimikroba di rumah sakit tidak tepat.Diperlukan kebutuhan untuk meningkatkan pengetahuan dan kesadaran tentang resistensi antimikroba di kalangan petugas kesehatan profesional (Desai, 2016).
Multiple drug resistance (MDR), resistensi beberapa obat atau multiresistensi adalah resistensi antimikroba yang ditunjukkan oleh spesies mikroorganisme terhadap beberapa antimikroba.Jenis yang paling mengancam bagi kesehatan masyarakat adalah bakteri MDR yang melawan banyak antibiotik; termasuk virus MDR, jamur, dan parasit (resisten terhadap banyak antijamur, antiviral, dan antiparasit dari berbagai jenis bahan kimia).Mengetahui tingkat MDR yang berbeda, istilah yang resistan terhadap obat secara ekstensif drug resistant (XDR) dan pandrug-resistant (PDR), istilah tersebut telah diperkenalkan pada tahun 2011. (Singhal, 2017)
Organisme MDR didapatkan resisten terhadap pengobatan dengan beberapa agen antimikroba yang sering tidak berkaitan.
Beberapa jenis organisme MDR penting yang telah ditemui meliputi: 1. MRSA - methicillin / oxacillin-resistant Staphylococcus aureus 2. VRE - vancomycin-resistant enterococci
3. ESBLs - beta-laktamase spektrum luas yang menghasilkan bakteri Gram-negatif (yang resisten terhadap sefalosporin dan monobaktam) 4. PRSP - penicillin-resistant Streptococcus pneumoniae
5. Carbapenemase yang memproduksi Klebsiella pneumonia (KPC)
6. gram negatif MultiDrug-Resistant (MDR GNR) Bakteri MDRGN seperti spesies Enterobacter, E.coli, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa.
7. Grup bakteri gram positif dan gram negatif yang baru-baru ini dianggap sebagai kelompok ESKAPE (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa dan spesies Enterobacter).
8. MDR Tuberkulosis
MRSA dan VRE adalah organisme MDR yang paling banyak ditemui pada pasien yang berada di fasilitas kesehatan non-rumah sakit, seperti panti jompo danfasilitas perawatan jangka panjang lainnya.PRSP lebih sering terjadi pada pasien yang mencari perawatan di tempat rawat jalan seperti klinik dokter, terutama di lingkungan anak-anak.ESBL paling sering dijumpai di rumah sakit (perawatan intensif), namun MRSA dan VRE juga memiliki ekologi nosokomial yang signifikan.
Peningkatan kejadian resistensi bakteri terhadap antibiotik bisa terjadi dengan 2 cara, yaitu (Kemenkes, 2011) :
1) Mekanisme Selection Pressure. Jika bakteri resisten tersebut berbiak secara duplikasi setiap 20-30 menit (untuk bakteric yang berbiak cepat ), maka dalam 1-2 hari, seseorang tersebut dipenuhi oleh bakteri resisten. Jika seseorang terinfeksi oleh bakteri yang resisten maka upaya penanganan infeksi dengan antibiotik semakin sulit.
2) Penyebaran resistensi ke bakteri yang non-resisten melalui plasmid. Hal ini dapat disebarkan antar kuman sekelompok mau pun dari satu orang ke orang lain.
Bila seseorang terinfeksi bakteri yang resisten terhadap antibiotik, tidak hanya perawatan pasien itu lebih sulit, tapi bakteri tersebut dapat menyebar ke orang lain. Jumlah bakteri yang resisten terhadap antibiotik semakin meningkat.Resistensi antibiotik dapat meningkatkan penyakit pada manusia, penderitaan dan kematian, kenaikan biaya dan lamanya perawatan; dan meningkatkan efek samping penggunaan kombinasi obat yang lebih kuat.
Pasien yang terinfeksi mikroba yang resisten terhadap antibiotik secara signifikan lebih mungkin mengalami komplikasi dan efek jangka panjang. Begitu mikroorganisme infektif memasuki tubuh, ia bisa berpindah dari infeksi primer ke tempat yang lain. mikroba yang resisten terhadap antibiotik biasanya membutuhkan waktu untuk berkembang, menyebar ke organ lain dan menjadi komplikasi. Misalnya pasien yang terinfeksi oleh strain methicillin resistant S.aureus(MRSA) memiliki risiko menjadi komplikasi, 69% lebih tinggi dibandingkan pasien sejenis yang terinfeksi oleh strainmethicillin-susceptible S. aureus (MSSA) (Desai, 2016).
Komplikasi paling sering terjadi adalah perkembangan infeksi lokal [risiko relatif (RR) sama dengan 3,25] . Sebagai contoh: orang yang terinfeksi MRSA 3,25 kali lebih mungkin mengalami infeksi lokal dibandingkan dengan orang yang terinfeksi oleh MSSA. Jika mikroorganisme yang infektif memasuki sistem peredaran darah dan menyebar luas, dapat menyebabkan sepsis (yaitu inflamasi seluruh tubuh yang berespon terhadap infeksi) dan syok.Pasien yang terinfeksi ARM lebih cenderung mengalami sepsis dan 12% lebih mungkin mengalami syok.Beberapa komplikasi serius jangka panjang lainnya yang mungkin berkembang termasuk efek di sistem saraf pusat (RR 1.7) atau kehilangan anggota badan (RR 1.13) (Desai, 2016).
Terdapat dua strategi pencegahan peningkatan resistensi bakteri, yaitu :
1) Untuk selection pressure dapat diatasi melalui penggunaan antibiotik secara bijak (prudentuse of antibiotics).
2) Untuk penyebaran bakteri resisten melalui plasmid dapat diatasi dengan meningkatkan ketaatan terhadap prinsip-prinsip kewaspadaan standar (universal precaution).
2.3Evaluasi Penggunaan Antibiotik Profilaksis Di Rumah Sakit
2.3.1 Penggunaan Antibiotik Profilaksis di Rumah Sakit (Kemenkes RI,2011) 1. Tepat indikasi
Untuk bedah bersih kontaminasi, bersih yang memasang bahan prostesis, operasi bersih yang jika sampai terjadi infeksi akan menimbulkan dampak yang serius seperti operasi bedah syaraf, bedah jantung, dan mata.
2. Tepat obat
Dengan mempertimbangkan spektrum antibiotik dan potensi bakteri. 3. Tepat dosis
Untuk tujuan profilaksis diperlukan antibiotika dosis tinggi, agar didalam sirkulasi dan didalam jaringan tubuh dicapai kadar diatas MIC. Dosis yang kurang adekuat, tidak hanya tidak mampu menghambat pertumbuhan bakteri, tetapi justru merangsang terjadinya resistensi bakteri.
4. Tepat rute pemberian.
Agar antibiotik dapat segera didistribusikan ke jaringan maka pemberiannya dilakukan secara intravena
5. Tepat waktu pemberian
Pemberian antibiotik umumnya 30-60 menit sebelum pembedahan 6. Tepat lama pemberian
Mempertimbangkan proses pembedahan, jika lama dapat diberikan dosis tambahan dapat diberikan setiap 2 jam untuk sefoksitin atau setiap 4 jam untuk sefazolin.
2.3.2 Kualitas Penggunaan Antibiotik
Penilaian Kualitas Penggunaan Antibiotik di Rumah Sakit (Gyssens, 2005) : 1. Kualitas penggunaan antibiotik dapat dinilai dengan melihat rekam
pemberian antibiotik dan rekam medik pasien.
2.Penilaian dilakukan dengan mempertimbangkan kesesuaian diagnosis (gejala klinis dan hasil laboratorium), indikasi, regimen dosis, keamanan dan harga.
3.Alur penilaian menggunakan kategori /klasifikasi Gyssens.
4. Kategori hasil penilaian kualitatif penggunaan antibiotik sebagai berikut (Gyssens IC,2005):
Kategori 0 = Penggunaan antibiotik tepat/bijak Kategori I = Penggunaan antibiotik tidak tepat waktu Kategori II A = Penggunaan antibiotik tidak tepat dosis
Kategori II B = Penggunaan antibiotik tidak tepat interval pemberian Kategori II C = Penggunaan antibiotik tidak tepat cara / rute pemberian Kategori III A = Penggunaan antibiotik terlalu lama
Kategori III B = Penggunaan antibiotik terlalu singkat Kategori IV A = Ada antibiotik lain yang lebih efektif
Kategori IV B = Ada antibiotik lain yang kurang toksik / lebih aman Kategori IV C = Ada antibiotik lain yang lebih murah
Kategori IV D = Ada antibiotik lain yang spektrumnya lebih sempit Kategori V = Tidak ada indikasi penggunaan antibiotik
Kategori VI = Data rekam medik tidak lengkap dan tidak dapat dievaluasi
Kualitas penggunaan antibiotika untuk terapi empiris dan
resistensi mikroba serta dari informasi yang didapatkan pada epidemiologi infeksi dan organisme penyebab secara lokal.Laboratorium mikrobiologi berperan penting pada pengumpulan data, analisis dan pelaporan data surveilan dan menyediakan informasi yang digunakan untuk terapi empiris (perkiraan berdasarkan data) atau profilaksis.Pedoman terapi empiris dan profilaksis berdasarkan surveilans ini seharusnya ada pada fasilitas pelayanan kesehatan.
Akses terhadap fasilitas laboratorium mikrobiologi sangat penting untukmengidentifikasi patogen dan obat yang sensitif agar dapat dilakukan terapi definitif dengan spektrum aktivitas yang lebih sempit dibandingkan terapi empiris.Audit penggunaan antibiotika didefinisikan sebagai analisis kesesuaian peresepan individual.Audit merupakan metode lengkap untuk menilai seluruh aspek terapi. Proses evaluasi dapat dilakukan dengan alat evaluasi yang didesain oleh peneliti sendiri atau dengan alat evaluasi yang sudah baku seperti Metode Kunin dan Metode Gyssens (Utomo H, 2008). Metode Gyssens berbentuk diagram alir yang diadaptasi dari kriteria Kunin et. al. Metode ini mengevaluasi seluruh aspek peresepan antibiotika, seperti: penilaian peresepan, alternatif yang lebih efektif, lebih tidak toksik, lebih murah, spektrum lebih sempit. Selain itu juga dievaluasi durasi pengobatan dandosis, interval dan rute pemberian serta waktu pemberian.
Diagram alir ini merupakan alat yang penting untuk menilai kualitaspenggunaan antibiotika. Pengobatan dapat tidak sesuai dengan alasan yang berbeda pada saat yang sama dan dapat ditempatkan dalam lebih dari satu kategori. Dengan alat ini, terapi empiris dapat dinilai, demikian juga terapi
Bagan 1. Alur Penilaian Kualitatif Penggunaan Antibiotik (Gyssens Classification) (Gyssens, 2005)
Evaluasi antibiotika dimulai dari kotak yang paling atas, yaitu dengan melihat apakah data lengkap atau tidak untuk mengkategorikan penggunaan antibiotika
(Gyssens, 2005).
1. Bila data tidak lengkap, berhenti di kategori VI
Data tidak lengkap adalah data rekam medis tanpa diagnosis kerja, atau ada halaman rekam medis yang hilang sehingga tidak dapat dievaluasi.Pemeriksaan penunjang/laboratorium tidak harus dilakukan karena mungkin tidak ada biaya, dengan catatan sudah direncanakan pemeriksaannya untuk mendukung diagnosis.Diagnosis kerja dapat ditegakkan secara klinis dari anamnesis dan pemeriksaan fisis.Bila data lengkap, dilanjutkan dengan pertanyaan di bawahnya, apakah ada infeksi yang membutuhkan antibiotika?
2. Bila tidak ada indikasi pemberian antibiotika, berhenti di kategori V
Bila antibiotika memang terindikasi, lanjutkan dengan pertanyaan di bawahnya. Apakah pemilihan antibiotika sudah tepat?
3. Bila ada pilihan antibiotika lain yang lebih efektif, berhenti di kategori IVa.
Bila tidak, lanjutkan dengan pertanyaan di bawahnya, apakah ada alternatif lain yang kurang toksik?
4. Bila ada pilihan antibiotika lain yang kurang toksik, berhenti di kategori IVb.
Bila tidak, lanjutkan dengan pertanyaan di bawahnya, apakah ada alternatif lebih murah?
5. Bila ada pilihan antibiotika lain yang lebih murah, berhenti di kategori IVc.Pada alternatif lain yang lebih murah, peneliti berpatokan pada daftar
harga obat yang dikeluarkan dari RSCM dan semua antibiotika dianggap sebagai obat generik dalam penghitungan harganya. Bila tidak, lanjutkan
dengan pertanyaan di bawahnya, apakah ada alternatif lain yang spektrumnya lebih sempit?
6. Bila ada pilihan antibiotika lain dengan spektrum yang lebih sempit, berhenti di kategori IVd.
Jika tidak ada alternatif lain yang lebih sempit, lanjutkan dengan pertanyaan di bawahnya, apakah durasi antibiotika yang diberikan terlalu panjang?
7. Bila durasi pemberian antibiotika terlalu panjang, berhenti di kategori IIIa.
Bila tidak, diteruskan dengan pertanyaan apakah durasi antibiotika terlalu singkat?
8. Bila durasi pemberian antibiotika terlalu singkat, berhenti di kategori IIIb.
Bila tidak, diteruskan dengan pertanyaan di bawahnya. Apakah dosis antibiotika yang diberikan sudah tepat?
9. Bila dosis pemberian antibiotika tidak tepat, berhenti di kategori IIa.
Bila dosisnya tepat, lanjutkan dengan pertanyaan berikutnya, apakah interval antibiotika yang diberikan sudah tepat?
10. Bila interval pemberian antibiotika tidak tepat, berhenti di kategori IIb.
Bila intervalnya tepat, lanjutkan dengan pertanyaan di bawahnya. Apakah rute pemberian antibiotika sudah tepat?
11. Bila rute pemberian antibiotika tidak tepat, berhenti di kategori IIc.
Bila rute tepat, lanjutkan ke kotak berikutnya.
12. Bila antibiotika tidak termasuk kategori I sampai dengan VI, antibiotika tersebut merupakan kategori 1
2.2 Pengetahuan dan Sikap dan Parameter Outcome
2.2.3 Pengetahuan dan Sikap
Pengetahuan atau kognitif merupakan hasil dari tahu dan ini terjadi setelah orang melakukan penginderaan terhadap suatu obyek tertentu, pengetahuan tentang segi positif dan negatif dari suatu hal yang mempengaruhi sikap dan perilaku.Pengetahuan dan kognitif merupakan doain yang sangat penting untuk terbentuknya tindakan seseorang (overt
behaviour). Terbentuknya suatu perilaku baru, terutama pada orang dewasa
dimulai pada domain kognitif, dalam artian subyek tahu terlebih dahulu terhadap stimulus yang berupa materi atau obyek diluarnya sehingga menimbulkan pengetahuan baru pada subyek tersebut, dan selanjutnya menimbulkan respon batin dalam bentuk sikap subyek erhadap obyek yang diketahuinya itu. Akhirnya rangsang yang telah diketahui dan disadari sepenuhnya akan menimbulkan respon lebih jauh berupa tindakan (action) terhadap stimulus. Namun demikian dalam kenyatannya, stimulus yang diterima subyek dapat langsung menimbulkan tindakan.Artinyam seseorang dapa bertindak atau berperilaku baru tanpa terlebih dahulu mengetahui makna stimulus yang diterimanya. Dengan kata lain, tindakan (practice) seseorang tidak harus disadari oleh pengetahuan atau sikap (Notoatmodjo, 2003)
Menurut Soekidjo Notoatmodjo (2003) pengetahuan yang mencakup domain kognitif memiliki enam tingkatan, yaitu:
1. Tahu (Know)
Tahu diartikan sebagai mengingat suatu materi yang telah dipelajari sebelumnya.Termasuk di dalam pengetahuan tingkat ini adalah mengingat kembali (recall) terhadap suatu yang spesifik dari seluruh bahan yang dipelajari atau rangsangan yang telah diterima. Kata kerja untuk mengukur bahwa orang tahu tentang apa yang dipelajari antara lain
menyebutkan, menguraikan, mendefinisikan, menyatakan dan
sebagainya.
Memahami diartikan sebagai suatu kemampuan untuk menjelaskan secara benar obyek yang diketahui dan dapat menginterpretasikan materi tersebut dengan benar.Orang yang telah paham terhadap obyek atau materi harus dapat menjelaskan, menyebutkan contoh, menyimpulkan, meramalkan terhadap obyek yang dipelajari.
3. Aplikasi (Aplication)
Aplikasi diartikan sebagai kemampuan untuk menggunakan materi yang telah dipelajari pada situasi atau kondisi sebenarnya. Aplikasi disini dapat diartikan sebagai aplikasi atau penggunaan hukum-hukum, rumus, metode, prinsip dan sebgainya dalam konteks atau situasi yang lain. 4. Analisis
Analisis adalah suatu kemampuan untuk menjabarkan materi atau suatu obyek ke dalam komponen-komponen, tetapi masih di dalam satu struktur organisasi dan masih ada kaitannya satu sama lain. Kemampuan analisis ini dapat dilihat dari penggunaan kata kerja, seperti dapat
menggambarkan (membuat bagan), membedakan, memisahkan,
mengelompokkan dan sebagainya. 5. Sintesis
Sintesis menunjukkan kepada suatu kemampuan untuk meletakkan atau menghubungkan bagian-bagian di dalam suatu bentuk keseluruhan yang baru. Dengan kata lain sintesis adalah suatu kemampuan untuj menyusun formulasi baru dari formulasi yang ada.
6. Evaluasi
Evaluasi ini berkaitan dengan kemampuan untuk melakukan justifikasi atau penilaian terhadap suatu materi atau obyek.Penilaian-penilaian itu didasarkan pada suatu kriteria yang ditentukan sendiri atau menggunakan kriteria yang ada.
2.2.4 Parameter outcome
Parameter outcome evaluasi dapat dikategorikan sebagai outcome proses, outcome pasien dan outcome mikrobiologi (Gyssens, 2005):
- Outcome proses (pola peresepan) :Umpan balik dari hasil evaluasi bisa merupakan suatu intervensi untukmeningkatkan kualitas peresepan. - Outcome Operator bedah : Beberapa variabel outcome Operator bedah
yang dapat diperoleh dari studi intervensi diantaranya perubahan pengetahuan dan sikap dalam penggunan antibiotik profilaksis rasional pada tindakan bedah elektif operasi bersih.
- Outcome mikrobiologi : Beberapa parameter outcome mikrobiologi pada studi intervensi diantaranya perubahan jumlah kejadian resistensi mikroba dan jumlah strain bakteri yang resisten terhadap antibiotika.