IV. HASIL DAN PEMBAHASAN
A. ANALISIS ASAP CAIR TEMPURUNG KELAPA
1. Komponen spesifik pada asap cair
Analisis komponen spesifik pada asap cair dilakukan dengan GC-MS. Campuran senyawa yang dilewatkan pada kromatografi gas akan terpisah menjadi komponen-komponen individual. Tujuh senyawa dominan dari masing-masing sampel dapat dilihat pada Tabel 4.
Tabel 4. Senyawa Dominan Asap Cair Tempurung Kelapa Hasil Deteksi GC-MS
Komponen Senyawa Spesifik Waktu Retensi (menit)
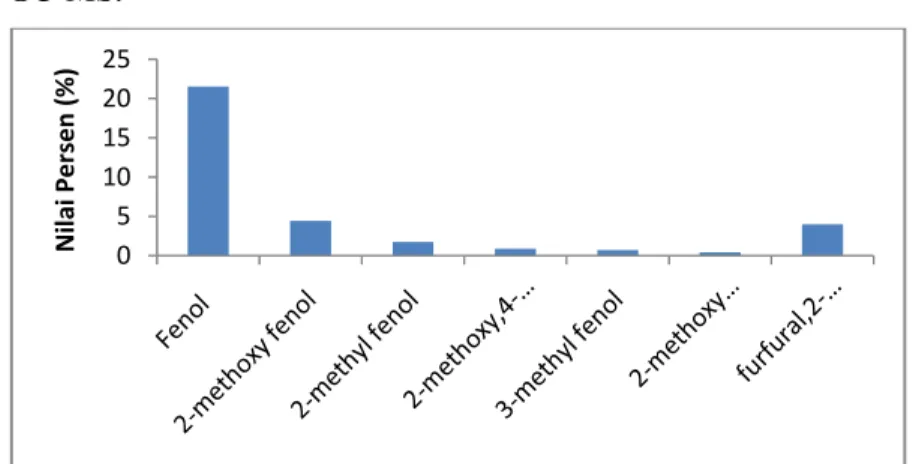
Nilai Persen Area (%) Fenol 10.53 21.55 2-methoxy fenol 12.48 4.44 furfural,2- furancarboxaldehid 8.04 3.98 2-methyl fenol 11.78 1.73 2-methoxy,4-methyl fenol 14.11 0.89 3-methyl fenol 12.10 0.72 2-methoxy benzeneethanol 15.41 0.43
Hasil analisis GC-MS menunjukkan bahwa senyawa dominan pada asap cair tempurung kelapa adalah fenol (C6H6O, BM = 94) dengan luas area bervariasi dengan rata-rata 21,55 %. Hasil ini sesuai dengan penelitian Luditama (2006), dimana senyawa asap cair tempurung kelapa paling dominan yang dihasilkan adalah fenol, dengan luas area 31,93 % untuk suhu pembakaran 500 ºC dan luas area 34,45 % untuk suhu pembakaran 300 ºC. Demikian pula Tranggono, et al., (1996) dimana senyawa dominan dari asap cair hasil penelitiannya adalah fenol dengan luas area sebesar 44,13 %.
Fenol dan turunannya menjadi senyawa paling dominan pada asap cair tempurung kelapa. Hal ini, dikarenakan komponen paling dominan pada komposisi kimia tempurung kelapa adalah lignin. Menurut Djatmiko et al., (1985) komposisi kimia paling dominan pada tempurung kelapa adalah lignin dengan konsentrasi sebesar 33,30 %. Fenol dihasilkan dari dekomposisi lignin
yang terjadi pada suhu 300 ºC dan berakhir pada suhu 450 ºC (Girrard, 1992). Kadar maksimum senyawa fenol tercapai pada suhu pirolisis 600 ºC (Hamm dan Potthast, 1976 dalam Girrard, 1992). Pada lampiran 3 dapat dilihat hasil lengkap senyawa penyusun dominan asap cair tempurung kelapa hasil deteksi GC-MS.
Gambar 2. Histogram Senyawa Dominan Asap Cair Tempurung Kelapa Darmadji (1995), menyebutkan bahwa senyawa fenol berperan sebagai antimikrobial. Sifat bakteriosidal dari pengasapan adalah faktor nyata dalam perlindungan nilai gizi produk yang diasap terhadap perusakan biologis (Harris dan Karmas, 1989). Efek fungisidal dalam asap disebabkan oleh fenol dan formaldehid (Daun, 1979; Toth dan Potthast, 1984). Fenol selain bersifat bakteriosidal juga sebagai antioksidan. Sifat ini terutama pada senyawa fenol dengan titik didih tinggi, seperti 2,6-dimethoksi fenol, 2,6-dimethoksi-4-metil-fenol dan 2,6-dimethoksi-4-ethyl 2,6-dimethoksi-4-metil-fenol (Pearson dan Tauber, 1973).
2. Nilai pH
Salah satu yang menjadi parameter bagus tidaknya kualitas asap cair yang dihasilkan adalah nilai pH. Nilai pH juga menunjukkan tingkat proses penguraian komponen kayu yang terjadi untuk menghasilkan asam organik pada asap cair. Jika nilai pH asap cair rendah hal ini menunjukkan bahwa kualitas asap cair yang digunakan tinggi, karena secara keseluruhan berpengaruh terhadap nilai awet dan daya simpan produk asap maupun sifat organoleptiknya. Nilai pH diukur dengan pH meter.
0 5 10 15 20 25 Ni la i Persen (%)
Hasil pengukuran nilai pH pada asap cair tempurung kelapa adalah 3,29. Nilai pengukuran pH ini menunjukkan bahwa kualitas asap cair yang digunakan sebagai pengawet memiliki kualitas yang tinggi. Hal ini karena nilai pH yang dihasilkan memiliki nilai yang rendah. Selain itu nilai pH asap cair yang digunakan sesuai dengan kualitas Wood Vinegar asal Jepang. Menurut Japan Wood Vinegar Association (2001) nilai pH standar asap cair berkisar antara 1,5 – 3,7.
Menurut Luditama (2006), nilai pH asap cair tempurung kelapa memiliki nilai pH yang lebih rendah dibandingkan asap cair yang berbahan baku sabut kelapa. Hal ini dikarenakan tempurung kelapa memiliki komponen hemiselulosa dan selulosa lebih besar daripada sabut kelapa sehingga jumlah asam yang dihasilkan lebih besar. Hemiselulosa dan selulosa adalah komponen kayu yang apabila terdekomposisi akan menghasilkan senyawa-senyawa asam organik seperti asam asetat yang merupakan turunan dari asam karboksilat. Menurut Grimwood (1975), tempurung kelapa mengandung hemiselulosa 8,8 % dan selulosa sebesar 19,24 %, sedangkan sabut kelapa memiliki kandungan hemiselulosa, yang merupakan penghasil asam organik ketika dibakar, sebesar 7,69 % dan selulosa sebesar 18,24 %. Selain itu, menurut Luditama (2006), tinggi rendahnya nilai pH pada asap cair dipengaruhi oleh kadar fenol, suhu pirolisis dan sitem destilasi. Semakin tinggi kadar fenol, suhu pirolisis dan suhu destilasi dari asap cair, semakin rendah pula nilai pH dari asap cair tersebut.
3. Kadar asam
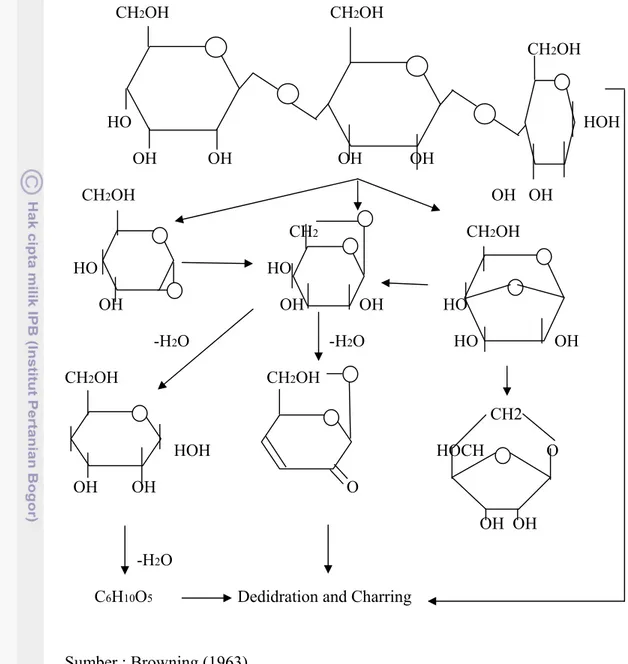
Kadar asam merupakan salah satu sifat kimia yang menentukan kualitas dari asap cair yang diproduksi. Asam asetat merupakan senyawa asam organik yang memiliki peranan tinggi dalam asap cair. Asam asetat kemungkinan terbentuk sebagian dari lignin dan sebagian dari komponen karbohidrat dari selulosa. Browning (1963) menggambarkan pembentukan asam asetat sebagai berikut :
CH2OH CH2OH CH2OH HO O HOH OH OH OH OH CH2OH OH OH CH2 CH2OH HO HO OH OH OH HO -H2O -H2O HO OH CH2OH CH2OH CH2 HOH HOCH O OH OH O OH OH -H2O
C6H10O5 Dedidration and Charring
Sumber : Browning (1963)
Gambar 3. Formulasi Produksi Asam Asetat
Lalu jika (C6H10O5)n dihidrolisis akan membentuk glukosa : (C6H10O5) + nH2O (C6H12O6)
C6H12O6 CH3COOH
Sifat senyawa-senyawa asam pada asap cair bersifat antimikroba. Jika asam organik berada bersama fenol maka sifat antimikroba senyawa-senyawa asam semakin meningkat. Senyawa asam organik terbentuk dari pirolisis komponen-komponen kayu seperri hemiselulosa dan selulosa. Penentuan kadar asam ini dilakukan dengan GC-MS. Hasil lengkap penentuan kadar asam disajikan di Lampiran 4.
Hasil pengukuran menunjukkan bahwa asap cair tempurung kelapa memiliki kadar asam sebesar 37 %. Kadar asam yang diperoleh pada penelitian ini sesuai dengan penelitian Luditama (2006) yaitu berkisar antara berkisar antara 9,58 sampai 59,93 %. Menurut Luditama (2006), keasaman dari asap cair dipengaruhi oleh kadar fenol pada asap cair tersebut. Semakin tinggi kadar fenol, maka asap cair akan menjadi semakin asam. Selain itu menurut Luditama (2006), kadar asam dari asap cair dipengaruhi oleh suhu fraksi destilasi dan suhu pirolisis sebelum destilasi. Semakin tinggi suhu fraksi destilasi, maka kadar asamnya semakin besar. Semakin rendah suhu pirolisis maka kadar asamnya semakin besar. Perbedaan jumlah kadar asam ini dikarenakan asam organik yang dihasilkan dari dekomposisi komponen hemiselulosa dan selulosa mengalami proses pirolisis pada suhu pembakaran dibawah 300 ºC. Asap cair pada suhu pembakaran 500 ºC memiliki kadar asam yang lebih rendah karena menurut Maga (1988) pada suhu pembakaran diatas 300 ºC senyawa-senyawa fenol, guaikol, dan siringol telah terdekomposisi dari lignin sehingga mempengaruhi kadar asam asap cair. 4. Kadar fenol
Kadar fenol merupakan zat aktif yang memiliki sifat antimikroba dan efek antibakteri pada asap cair. Selain itu, fenol juga dapat memberikan efek antioksidan kepada bahan makanan yang diawetkan. Identifikasi fenol terhadap kualitas asap cair yang dihasilkan, diharapkan dapat mewakili kriteria dari mutu asap cair tersebut, sehingga dapat dinyatakan bahwa asap cair yang digunakan sangat sesuai dengan aplikasi produk yang diawetkan.
Pengukuran kadar fenol pada asap cair dilakukan dengan GC-MS. Hasil lengkap penentuan kadar fenol disajikan di Lampiran 4. Kadar fenol yang dihasilkan sebesar 38 %. Hasil ini sangat berbeda dengan hasil penelitian
Luditama (2006) yang berkisar antara 0,44 – 0,78 % dan hasil penelitian Maga (1988) yaitu antara 0,2 – 2,9 %. Menurut Luditama (2006), suhu pirolisis atau pembakaran 300 ºC dan 500 ºC dari suatu bahan tidak mempengaruhi kadar fenol dari asap cair. Akan tetapi, perbedaan kadar fenol pada asap cair dipengaruhi oleh perbedaan kandungan lignin pada bahan pengasap. Lignin merupakan komponen kayu yang apabila terdekomposis akan menghasilkan senyawa fenol. Menurut Djatmiko, et al. (1985), tempurung kelapa memiliki lignin sebesar 33,30 %, sedangkan menurut Joseph dan Kindagen (1993), sabut kelapa mengandung lignin sebesar 29,23 %.
Faktor utama yang menentukan kadar fenol dalam asap cair adalah banyaknya asap yang dihasilkan selama pembakaran. Hal ini terkait pada faktor suhu dan bahan pengasap yang digunakan. Intensitas pirolisis berhubungan langsung dengan suhu yang dicapai yang terdiri dari transfer panas dan keberadan oksigen (reaksi oksidasi). Sedangkan bahan pengasap berhubungan langsung dengan jenis bahan yang terdiri atas kayu keras ataupun bahan yang dapat dibakar yaitu selulosa, hemiselulosa, lignin, persenyawaan protein dan mineral yang mempengaruhi keberadaan senyawa-senyawa kimia asap (Djatmiko et al., 1985).
B. ANALISIS IKAN TERI NASI (Stolephorus commersonii, Lac.) SEGAR Analisis pada ikan teri nasi (Stolephorus commersonii, Lac.) segar berupa analisa komponen gizi atau analisa proksimat. Hasil analisis komponen gizi ikan teri nasi (Stolephorus commersonii, Lac.) dapat dilihat pada Tabel 5. Analisa yang dilakukan yaitu analisa kadar abu, kadar air, kadar protein, dan kadar lemak. Tabel 5. Hasil Analisis Proksimat Ikan Teri Nasi
Komposisi Gizi Ikan Teri Nasi
Segar Nilai Persen (%)
Kadar Air 80.39
Kadar Abu 3.25
Kadar Protein 13.74
Kadar Lemak 2.45
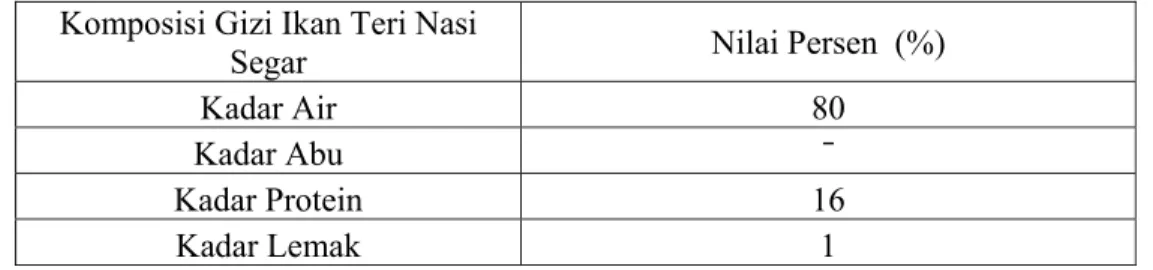
Tabel 6. Hasil Analisis Proksimat Menurut Hardinsyah dan Briawan (1990) Komposisi Gizi Ikan Teri Nasi
Segar Nilai Persen (%)
Kadar Air 80
Kadar Abu ¯
Kadar Protein 16
Kadar Lemak 1
Bahan makanan tersusun dari empat komponen utama, yaitu air, protein, karbohidrat, dan lemak. Selain empat hal tersebut, makanan memiliki komponen lain berupa senyawa organik seperti mineral, vitamin atau pigmen-pigmen.
Abu merupakan residu organik dari pembakaran senyawa organik bila bahan dibakar sempurna dalam tungku pengabuan. Kandungan abu total termasuk kadar logam merupakan parameter nilai nutrisi dari makanan. Kadar air adalah kandungan suatu bahan yang dapat dinyatakan berdasarkan berat basah dan berat kering. Kadar air sangat berpengaruh terhadap mutu bahan pangan, dan hal ini merupakan salah satu sebab mengapa di dalam pengolahan pangan, air tersebut sering dikurangi ataupun dikeluarkan dengan cara penguapan atau pengeringan. Menurut Winarno et al. (1984), keawetan bahan pangan memiliki hubungan yang erat dengan kadar air yang dikandungnya. Protein merupakan zat makanan yang penting bagi tubuh karena zat ini disamping berfungsi sebagai bahan bakar dalam tubuh juga berfungsi sebagai zat pembangun dan pengatur (Winarno, 1997). Lemak dan minyak merupakan zat makanan yang penting untuk menjaga tubuh manusia. Selain itu, lemak dan minyak merupakan sumber energi yang lebih efektif dibandingkan karbohidrat dan protein (Winarno, 1997).
Hasil uji proksimat atau kandungan gizi ikan teri nasi (Stolephorus
commersonii, Lac.) menunjukkan hasil yang tidak jauh berbeda dengan hasil
penelitian Hardinsyah dan Briawan (1990) pada ikan teri. Hasil uji kadar air diperoleh sebesar 80,39 %, sedangkan hasil penelitian kadar air Hardinsyah dan Briawan (1990) yaitu sebesar 80 %. Hasil uji kadar protein sebesar 13,74, sedangkan hasil penelitian kadar protein Hardinsyah dan Briawan (1990) yaitu sebesar 16 %. Pada hasil uji lemak diperoleh sebesar 2,45 %, sedangkan hasil penelitian kadar lemak Hardinsyah dan Briawan (1990) yaitu sebesar 1 %.
Selain dilakukan uji proksimat, pada ikan teri nasi juga diuji jumlah total mikroba melalui uji TPC dan uji kapang dan khamir. Data hasil uji total mikroba awal dapat dilihat pada Tabel 7.
Tabel 7. Hasil Uji Jumlah Total Mikroba Awal Ikan Teri Nasi (Stolephorus
commersonii, Lac.)
Analisa Jumlah (koloni/gram) TPC (Total Plate Count) 5.85 x 10³ Kapang dan Khamir 3.45 x 10³
Berdasarkan uji proksimat, ikan teri nasi (Stolephorus commersonii, Lac.) segar memiliki kandungan gizi yang sangat baik, yaitu kadar protein sebesar 13,74 % dan kadar lemak sebesar 2,45 %. Hal ini karena kandungan gizi yang dihasilkan tidak jauh berbeda dengan kriteria kandungan gizi ikan teri (Stolephorus. Sp) segar pada Direktorat Gizi Depkes (1981), yaitu kadar protein 16 % dan kadar lemak 1 %. Hasil uji jumlah total mikroba pada Tabel 7, diperoleh uji TPC sebesar 5.85 x 10³ koloni/gram dan uji kapang dan khamir sebesar 3.45 x 10³ koloni/gram. Hasil ini menunjukkan bahwa produk ikan teri nasi masih bisa dinyatakan sebagai produk yang layak dikonsumsi dan bisa dipertahankan keawetan atau kesegarannya. Hal ini karena hasil uji masih berada dibawah zona aman konsumsi yakni 5 x 10 berdasarkan SNI 02-2725-1992 (BSN, 1992).
C. PROSES PERENDAMAN (ANALISIS KADAR FENOL)
Pada proses perlakuan ini ikan teri nasi (Stolephorus commersonii, Lac.) direndam di dalam asap cair dengan konsentrasi yang berbeda dan lama waktu perendaman yang berbeda. Setelah proses perendaman dilakukan proses pengukuran kadar fenol. Hasil analisis terhadap kadar fenol dapat dilihat pada Tabel 8.
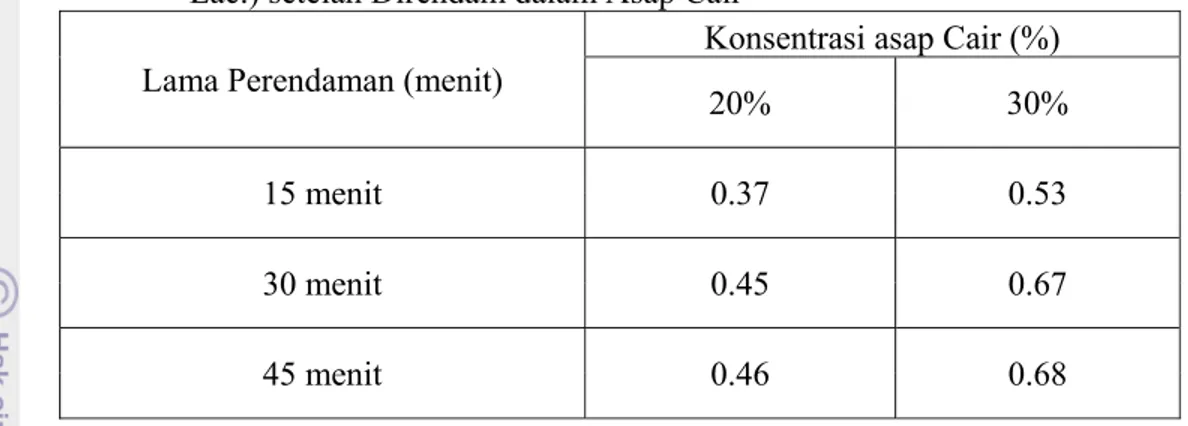
Tabel 8. Nilai Rata-Rata Kadar Fenol Ikan Teri Nasi (Stolephorus commersonii, Lac.) setelah Direndam dalam Asap Cair
Lama Perendaman (menit)
Konsentrasi asap Cair (%)
20% 30%
15 menit 0.37 0.53
30 menit 0.45 0.67
45 menit 0.46 0.68
Pada Tabel 8 dapat dilihat bahwa perlakuan konsentrasi asap cair dan lama perendaman dapat mempengaruhi kadar fenol dari ikan teri nasi (Stolephorus
commersonii, Lac.) asap cair. Semakin besar konsentrasi asap cair semakin
meningkat kadar fenol ikan teri nasi, semakin lama perendaman dalam asap cair semakin meningkat kadar fenol dari ikan teri nasi. Hal ini diduga disebabkan karena pada konsentrasi asap cair lebih tinggi terdapat kandungan fenol yang lebih tinggi pula dan semakin lama perendaman mempengaruhi pencapaian titik keseimbangan antara permukaan luar ikan dengan titik pusat dalam ikan terhadap konsentrasi fenol. Hasil ini sesuai dengan penelitian Haras (2004) yang menyatakan bahwa semakin besar konsentrasi asap cair dan semakin lama perendaman dalam asap cair, maka semakin meningkat kadar fenol dari ikan teri nasi.
Menurut Reinhold (1993), sebagai antiseptik banyaknya fenol dalam makanan mempengaruhi pertumbuhan bakteri. Selain itu, sebagai antioksidan banyaknya fenol dalam makanan mempengaruhi proses oksidasi sehingga dapat mempengaruhi mutu bahan makanan tersebut (Girrard, 1992 ; Pszczola, 1995).
Pada Tabel 8 dapat dilihat bahwa penggunaan asap cair dengan konsentrasi 30 % dan lama perendaman 45 menit memiliki kadar fenol tertinggi yaitu 0,68 % dan masih dalam batas aman fenol untuk dikonsumsi yaitu 0,02 – 1,00 % (Davidson and Branen, 1981).
Berdasarkan uji Anova didapatkan perbedaan nyata pada perlakuan konsentrasi asap cair, perlakuan lama perendaman dalam asap cair, dan interaksi
kedua perlakuan tersebut dengan nilai F hitung masing-masing sebesar 7200, 1158, dan 72 dan sangat layak untuk dilakukan uji lanjut. (Lampiran 5).
Berdasarkan uji lanjut Beda Nyata Jujur didapatkan perbedaan nyata terhadap kadar fenol pada perlakuan lama perendaman yang digunakan, perbedaan tertinggi terdapat pada perlakuan lama perendaman 45 menit dan 15 menit yaitu sebesar 0,125. Pada perlakuan konsentrasi tidak perlu dilakukan uji lanjut karena perlakuan konsentrasi hanya terdapat dua taraf yaitu 20 % dan 30 %, sedangkan uji Anova menunjukkan bahwa kedua konsentrasi sudah memberikan perbedaan nyata. Berdasarkan Tabel 8 jika dihitung nilai rata-rata kadar fenol pada tiap perlakuan konsentrasi diperoleh bahwa pada perlakuan konsentrasi 30 % memiliki nilai rata-rata tertinggi yaitu 0,62 % daripada perlakuan konsentrasi 20 % yaitu 0,43 %. Hal ini dikarenakan kandungan fenol lebih banyak pada konsentrasi asap cair yang tinggi berdasarkan data spesifikasi liquid smoke dari
International Flavor and Fragrances.
Pada uji lanjut interaksi perlakuan antara konsentrasi asap cair dan lama perendaman asap cair perbedaan tertinggi terdapat pada perlakuan konsentrasi asap cair 20 % lama perendaman 15 menit (kode perlakuan 101) dengan perlakuan konsentrasi asap cair 30 % lama perendaman 45 menit (kode perlakuan 106) sebesar 0,315. Hal ini menunjukkan kuatnya interaksi antara perlakuan konsentrasi asap cair dan lama perendaman asap cair terhadap kadar fenol pada ikan teri nasi (Stolephorus commersonii, Lac.). Hasil ini sesuai dengan penelitian Haras (2004), yang menunjukkan bahwa perbedaan nyata tertingi terdapat pada kombinasi antara konsentrasi asap cair paling tinggi dengan waktu perendaman paling lama (konsentrasi asap cair 2,0 % dan lama perendaman 15 menit) dan konsentrasi asap cair terendah dengan waktu lama perendaman terendah (konsentrasi asap cair 0,5 % dan lama perendaman 5 menit). Adapun kombinasi yang tidak menunjukkan perbedaan nyata antara lain : pada kode perlakuan 103 (konsentrasi 20% 30 menit) dengan 105 (konsentrasi 20% 45 menit) dan 104 (konsentrasi 30% 30 menit) dengan 106 (konsentrasi 30% 45 menit).
D. ANALISIS SELAMA PENYIMPANAN SUHU RUANG
Berdasarkan uji kadar fenol pada proses perendaman didapatkan perlakuan terbaik yaitu konsentrasi asap cair 30 % lama perendaman 45 menit. Analisa yang dilakukan selama penyimpanan adalah kadar air, kadar TPC dan kapang khamir, dan uji protein.
1. Analisis kadar air
Kadar air bahan pangan merupakan jumlah air yang dikandung tersebut dan sangat berpengaruh pada mutu dan keawetan pangan (Martinez et
al, 2007). Analisis kadar air bertujuan untuk mengetahui pengaruh
perendaman asap cair terhadap perubahan kadar air ikan teri nasi (Stolephorus
commersonii, Lac.) segar. Hasil pengukuran kadar air selama penyimpanan
disajikan pada Tabel 9 dan Gambar 6.
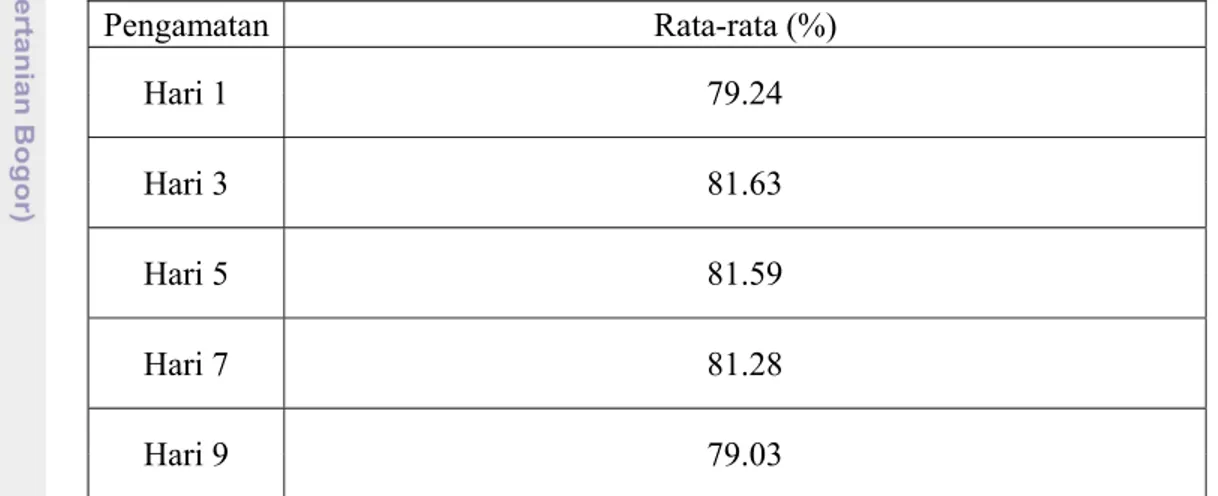
Tabel 9. Nilai Rata-Rata Kadar Air Selama Penyimpanan
Pengamatan Rata-rata (%) Hari 1 79.24 Hari 3 81.63 Hari 5 81.59 Hari 7 81.28 Hari 9 79.03
Air merupakan komponen penting dalam bahan makanan karena air dapat mempengaruhi penampakan, tekstur, serta cita rasa makanan. Selain itu, air merupakan sumber utama yang menjadi pemicu kecepatan mikrobiologi untuk merusak sumber pangan.
Istilah umum yang sering dipakai untuk air yang terdapat dalam bahan pangan adalah “air terikat” (bound water). Menurut derajat keterikatan air, Winarno (1992) menyatakan bahwa air terikat dibagi atas empat tipe. Tipe I, adalah molekul air yang terikat pada molekul-molekul lain melalui suatu ikan hidrogen yang berenergi besar. Molekul air membentuk hidrat dengan
molekul-molekul lain yang mengandung atom-atom O dan N seperti karbohidrat, protein, atau garam. Air tipe ini tidak dapat membeku pada proses pembekuan, tetapi sebagian air ini dapat dihilangkan dengan cara pengeringan biasa. Air tipe ini terikat kuat dan sering kali disebut air terikat dalam arti sebenarnya. Derajat pengikatan air sedemikian rupa sehingga reaksi-reaksi yang terjadi sangat lambat dan tidak terukur.
Tipe II, yaitu molekul-molekul air membentuk ikatan hidrogen dengan molekul air lain, terdapat dalam mikrokapiler dan sifatnya agak berbeda dari air murni. Air jenis ini lebih sukar dihilangkan dan penghilangan air tipe II akan mengakibatkan penurunan aw (water activity). Bila sebagian air tipe II dihilangkan, pertumbuhan mikroba dan reaksi-reaksi kimia yang bersifat merusak bahan makanan seperti browning, hidrolisis, atau oksidasi lemak akan dikurangi. Tipe III, adalah air yang secara spesifik terikat dalam jaringan matriks bahan seperti membran, kapiler, serat, dan lain-lain. Air tipe III inilah yang sering kali disebut air bebas. Air tipe ini mudah diuapkan dan dapat dimanfaatkan untuk pertumbuhan mikroba dan media bagi reaksi-reaksi kimiawi. Tipe IV, adalah air yang tidak terikat dalam jaringan suatu bahan atau air murni, dengan sifat-sifat air biasa dan keaktifan penuh.
Selain itu, Winarno (1992) membagi tipe-tipe air dibagi menjadi dua, yaitu air imbibisi dan air kristal. Air imbibisi merupakan air yang masuk ke dalam bahan pangan dan akan menyebabkan pengembangan volume, tetapi air ini tidak merupakan komponen penyusun bahan tersebut. Misalnya air dengan beras bila dipanaskan akan membentuk nasi, atau pembentukan gel dari bahan pati. Air kristal adalah air terikat dalam semua bahan, baik pangan maupun nonpangan yang berbentuk kristal, seperti gula, garam, CuSO4 dan lain-lain.
Adanya kandungan air yang lebih tinggi akan menunjang meningkatnya pertumbuhan bakteri serta aktivitas bakteri tersebut dalam merombak senyawa-senyawa kompleks menjadi senyawa-senyawa sederhana yang disebut pembusukan. Pada Tabel 9 dapat dilihat bahwa pada hari ke-1 proses perendaman dalam asap cair memberikan perubahan terhadap nilai kadar air pada ikan teri nasi segar yaitu dari 80,39 % (analisa proksimat Tabel 5) menjadi 79,24 %. Hal ini menunjukkan berdifusinya asap cair ke dalam
ikan teri nasi memberikan pengaruh yang cukup signifikan terhadap perubahan konsentrasi nilai kadar air pada ikan teri nasi (Stolephorus
commersonii, Lac.). Pada pengamatan hari ke-3 nilai kadar air menjadi
bertambah tinggi yaitu 81,63 %, hal ini diduga pada ikan teri nasi sudah mulai terjadi perombakan senyawa-senyawa kimia dalam bahan pangan, sehingga air yang terikat pada jaringan bahan pangan memisahkan diri dan meningkatkan nilai kadar air. Penurunan nilai kadar air secara terus menerus terjadi hari ke-3 sampai hari ke-9, yaitu dari 81,63 % menurun menjadi 81,59 % (hari ke-5), menjadi 81,28 % (hari ke-7), dan menjadi 79,03 % (hari ke-9). Dilihat dari nilai dari Tabel 9, nilai penurunan kadar air ini sebenarnya tidak sangat signifikan. Akan tetapi nilai penurunan kadar air ini bisa disebabkan dua hal, yaitu pengaruh pemanasan suhu dari sinar matahari pada ruang penyimpanan dan keasaman dari asap cair. Hal ini karena posisi lemari penyimpanan berada pada posisi masuknya sinar matahari pada ruangan. Suhu panas dari sinar matahari akan menyebabkan air yang ada dipermukaan daging (tubuh) ikan akan menguap terlebih dahulu. Hal ini akan menyebabkan pengkerutan jaringan daging sehingga mempersempit rongga-rongga antar sel dan pipa-pipa kapiler. Akibatnya air dibagian dalam daging ikan akan lambat menguap (Van Arsdel and Coplay, 1963). Penguapan air selama penyimpanan erat kaitannya dengan keadaan keseimbangan antara kelembaban relatif, suhu, dan kadar air. Aliran udara dapat menyebabkan tekanan parsial uap air di atas permukaan daging ikan menurun. Hal ini menyebabkan penguapan air dari daging ikan (Van Arsdel and Copley, 1963). Sedangkan pengaruh tingkat keasaman asap cair menurut Gomez-Guillen at al. (2003) dapat menyebabkan ketidaklarutan protein daging, sehingga berakibat pada keluarnya air dari daging ikan.
2. Analisis mikrobiologi (TPC, Kapang dan Khamir)
Kandungan bakteri dalam suatu produk merupakan salah satu parameter mikrobiologis dalam menentukan layak tidaknya produk tersebut dikonsumsi (Kristinsson et al., 2007). Kontaminasi mikroba pada produk perikanan dapat terjadi saat panen, penanganan, distribusi maupun penyimpanan, dan proses pengolahan. Analisis terhadap jumlah bakteri
bertujuan untuk mengetahui jumlah total bakteri dalam suatu produk dan mengetahui tingkat pertumbuhannya selama penyimpanan. Hasil analisis TPC terhadap ikan teri nasi (Stolephorus commersonii, Lac.) selama penyimpanan dapat dilihat pada Tabel 10.
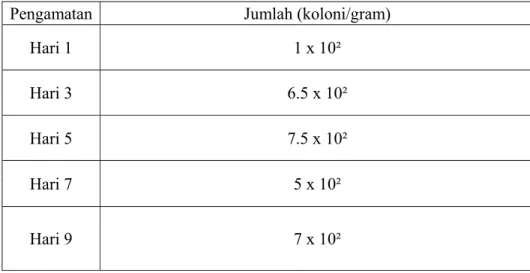
Tabel 10. Nilai Rata-Rata TPC Ikan Teri Nasi Selama Penyimpanan
Pengamatan Jumlah (koloni/gram)
Hari 1 1 x 10²
Hari 3 6.5 x 10²
Hari 5 7.5 x 10²
Hari 7 5 x 10²
Hari 9 7 x 10²
Berdasarkan Tabel 10 dapat dilihat bahwa hasil analisis pada hari ke-1 jumlah mikroba mengalami penurunan dari keadaan awal 5,85 x 10³ koloni/gram (Tabel 7) menjadi 1 x 10² koloni/gram (Tabel 10). Hasil ini menggambarkan bahwa fenol dalam asap cair dapat bekerja sebagai antiseptik, dimana mikroba tidak dapat tumbuh secara maksimal. Menurut Daun (1979), cara kerja fenol dalam menghambat pertumbuhan mikroba adalah dengan cara mengganggu metabolisme dari mikroba dengan menghambat pembentukan spora dari mikroba tersebut dan memperpanjang fase lag.
Pada hari ke3 terjadi kenaikan jumlah mikroba pada sampel ikan teri nasi (Stolephorus commersonii, Lac.) dari 1 x 10² koloni/gram (hari ke-1) menjadi 6.5 x 10² koloni/gram (hari ke-3). Demikian pula pada hari ke-5 terjadi kenaikan jumlah mikroba dari 6.5 x 10² koloni/gram (hari ke-3) menjadi 7.5 x 10² koloni/gram (hari ke-5). Peningkatan jumlah mikroba pada hari ke-3 dan hari ke-5 dikarenakan oleh sudah mulai menurunnya aktivitas dari fenol dari asap cair yang terdifusi ke dalam ikan teri nasi (Stolephorus
commersonii, Lac.). Selain itu, terjadinya kenaikan ini menunjukkan bahwa
diri dengan kondisi lingkungan yang ada. Salah satu faktor yang menjadi alat atau media yang mendukung proses adaptasi pada mikroba adalah adanya penggunaan suhu penyimpanan yang sesuai untuk pertumbuhan mikroba yaitu pada suhu kamar (37 ºC), sehingga akan semakin mempercepat pertumbuhan mikroba. Hal lain yang menjadi nilai positif bagi mikroba untuk mengalami kenaikan jumlah mikroba adalah terjadinya kenaikan kadar air dari hari ke-1 sampai hari ke-5 (Tabel 9). Semakin tinggi kadar air dalam suatu bahan pangan maka nilai aw makin meningkat, sehingga kemampuan aktivitas mikroba untuk tumbuh semakin meningkat. Menurut Winarno (1992) bakteri dapat tumbuh dengan baik pada aw minimum 0,9. Akan tetapi, kenaikan jumlah mikroba yang terjadi pada hari ke-3 dan hari ke-5 jumlah kenaikannya tidak terlalu signifikan karena masih berada pada jumlah pangkat 10².
Mulai dari hari ke-5 sampai hari ke-9 terjadi perubahan jumlah mikroba yang bersifat fluktuatif atau tidak terjadi kecenderungan naik atau turun. Jumlah mikroba dari 7.5 x 10² koloni/gram (hari ke-5) berubah atau menurun menjadi 5 x 10² koloni/gram (hari ke-7), sedangkan dari hari ke-7 terjadi kenaikan dari jumlah 5 x 10² koloni/gram menjadi 7 x 10² koloni/gram (hari 9). Terjadinya penurunan jumlah mikroba pada hari 7 dari hari ke-5 disebabkan oleh penurunan jumlah kadar air pada ikan teri nasi (Stolephorus
commersonii, Lac.) dari 81,59 % (hari ke-5) menjadi 81,28 %. (hari ke-7)
(Tabel 9). Penurunan jumlah kadar air ini menyebabkan nilai aw mengalami penurunan, sehingga hal ini menyebabkan terhambatnya proses pertumbuhan mikroba. Sedangkan penyebab terjadinya kenaikan jumlah mikroba pada hari ke-9 disebabkan oleh mulai menurunnya pengaruh keasaman dari asap cair, sehingga nilai pH-nya menjadi naik dan berada pada nilai pH optimum pertumbuhan bakteri. Bakteri tumbuh pada pH antara 4,0 – 8,0. Pada hari pengamatan terakhir (hari ke-9) jumlah mikroba sebesar 7 x 10² koloni/gram. Jumlah ini menunjukkan bahwa jumlah mikroba pada hari ke-9 masih berada pada di bawah zona aman konsumsi yaitu 5 x 10 koloni/gram berdasarkan SNI 02-2725-1992 (BSN, 1992).
Mengenai hasil analisis jumlah kapang dan khamir ikan teri nasi (Stolephorus commersonii, Lac.) bisa dilihat pada Tabel 11.
Tabel 11. Nilai Rata-Rata Jumlah Kapang dan Khamir Ikan Teri Nasi (Stolephorus commersonii, Lac.) Selama Penyimpanan.
Pengamatan Jumlah (koloni/gram)
Hari 1 1 x 10² Hari 3 6 x 10² Hari 5 6.5 x 10² Hari 7 2 x 10² Hari 9 2 x 10²
Dari Tabel 11 dapat dilihat bahwa pada hari ke-1 jumlah total kapang dan khamir mengalami penurunan dari kondisi analisis awal sebesar 3.45 x 10³ koloni/gram (Tabel 7) menjadi 1 x 10² koloni/gram. Nilai penurunan ini sama dengan penurunan pada hari ke-1 pada analisis jumlah total bakteri. Hal ini menunjukkan bahwa sifat antimikroba pada asap cair oleh fenol pada kapang dan khamir juga bekerja secara maksimal. Hal ini sesuai dengan pendapat Reinhold (1993) yang menyatakan bahwa fenol merupakan senyawa antiseptik dan desinfektan terhadap berbagai mikroba.
Kemudian pada hari ke-1 sampai hari ke-5 terjadi kenaikan jumlah total kapang dan khamir menjadi 6,5 x 10² koloni/gram. Faktor yang paling berkaitan dengan naiknya jumlah total kapang dan khamir adalah terjadinya kenaikan jumlah kadar air dari hari ke1 sampai hari ke-5 (Tabel 9). Hal ini menyebabkan naiknya nilai aw, sehingga meningkatkan aktivitas pertumbuhan mikroorganisme kapang dan khamir. Menurut Winarno (1992) kapang dapat tumbuh pada aw minimum 0,6 – 0,7 dan khamir dapat tumbuh pada aw minimum 0,8 – 0,9. Selanjutnya hasil analisis dari hari ke-5 sampai hari ke-7 jumlah total kapang dan khamir menurun menjadi 2 x 10² koloni/gram, dan dari hari ke-7 sampai hari ke-9 jumlah total kapang dan khamir bersifat konstan sebesar 2 x 10² koloni/gram. Nilai penurunan ini disebabkan oleh
menurunnya nilai kadar air pada pengamatan hari ke-7, sehingga hal ini akan menyebabkan menurunnya nilai aw dan secara simultan akan menghambat pertumbuhan kapang dan khamir. Sedangkan dari hari ke-7 sampai hari ke-9 nilai penurunan air tidak mempengaruhi jumlah penurunan total kapang dan khamir. Hal ini dikarenakan kapang dan khamir sudah mengalami titik jenuh dan berada pada fase lag optimum pertumbuhan atau berada dalam fase pertumbuhan tetap (statis). Hal ini bisa dilihat dari jumlah total kapang dan khamir dari hari ke-7 sampai hari ke-9 jumlahnya konstan yaitu 2 x 10² koloni/gram. Jumlah total kapang dan khamir pada hari pengamatan terakhir (hari ke-9) sebesar 2 x 10² koloni/gram, dan masih berada di bawah batas aman konsumsi yaitu 1 x 10 koloni/gram.
3. Analisis kadar protein
Kadar protein merupakan salah satu komponen komposisi gizi terpenting dalam sebuah produk pangan, terutama pada ikan teri nasi (Stolephorus commersonii, Lac.). Analisis kadar protein bertujuan untuk mengetahui pengaruh pengaruh perendaman asap cair terhadap perbahan kadar protein ikan teri nasi (Stolephorus commersonii, Lac.) segar selama penyimpanan. Hasil analisis kadar protein terhadap ikan teri nasi (Stolephorus
commersonii, Lac.) selama penyimpanan 9 hari dapat dilihat pada Tabel 12
dan Gambar 8 di bawah ini :
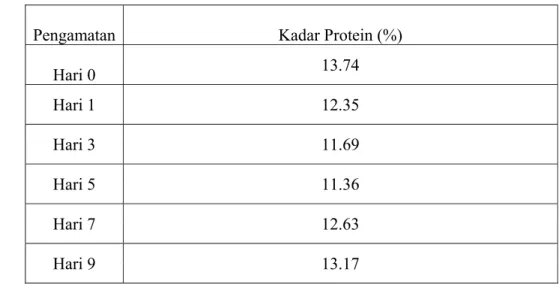
Tabel 12. Nilai Rata-Rata Kadar Protein Selama Penyimpanan Pengamatan Kadar Protein (%)
Hari 0 13.74 Hari 1 12.35 Hari 3 11.69 Hari 5 11.36 Hari 7 12.63 Hari 9 13.17
Protein adalah sumber asam-asam amino yang mengandung unsur-unsur C, H, O, dan N yang tidak dimiliki oleh lemak atau karbohidrat. Protein mempunyai bermacam-macam fungsi bagi tubuh, yaitu sebagai enzim, zat pengatur pergerakan, pertahanan tubuh, alat pengangkut dan lain-lain (Winarno, 1992). Molekul protein mengandung pula fosfor, belerang, dan ada jenis protein yang mengandung unsur-unsur logam, seperti besi dan tembaga. Protein dalam bahan makanan yang dikonsumsi manusia diserap oleh usus dalam bentuk asam amino. Bila suatu protein dihidrolisis dengan asam, alkali, atau enzim, akan dihasilkan campuran asam-asam amino.
Protein yang terdapat di dalam ikan dengan bantuan bakteri pembusuk akan terurai menjadi amoniak, amines yang lazim disebut basa-basa volatil (Buckle et al., 1985). Senyawa-senyawa yang tidak diinginkan dalam proses pembusukan yaitu senyawa-senyawa yang berbau busuk, seperti indol, skatol, merkaptan, putresin, dan asam sulfida atau H2S.
Pada Tabel 12 dan Gambar 8 dapat dilihat, bahwa pada hari ke1 jumlah kadar protein pada ikan teri nasi (Stolephorus commersonii, Lac.) mengalami penurunan dari keadaan awal 13,74 % (Tabel 5) mnjadi 12,35%. Penurunan ini disebabkan mikroorganisme pembusuk pengurai protein mulai memecah protein atau mendegradasi protein menjadi asam amino. Nilai penurunan kadar protein yang terjadi tidak terlalu signifikan, hal ini dikarenakan jumlah mikroorganisme yang ada pada hari ke-1 masih terlalu sedikit, sehingga tingkat penguraian protein menjadi asam amino jumlahnya tidak terlalu maksimal.
Pada hari ke-3 sampai hari ke-5 jumlah kadar protein menurun dari 12,35 % (hari ke-1) menjadi 11,69 % (hari ke-3) dan 11,36 % (hari ke-5). Penurunan ini terjadi karena mikroorganisme yang ada pada hari ke-3 dan hari ke-5 mulai tumbuh dan bertambah meningkat (Tabel 10 dan Tabel 11). Hal itu ditandai dengan meningkatnya jumlah kadar air yang menunjang atau mempercepat pertumbuhan mikroorganisme serta aktivitas pembusuk pada pangan. Pengamatan dari hari ke-5 sampai hari ke-9 menunjukkan terjadinya kenaikan nilai kadar protein menjadi 12,63 % (hari ke-7) dan 13,17 % (hari
ke-9). Terjadinya kecenderungan kenaikan nilai dari kadar protein ini disebabkan oleh menurunnya jumlah mikroorganisme dari hari ke-5 sampai hari ke-9 (Tabel 10 dan Tabel 11) yang ditandai dengan menurunnya kadar air pada periode waktu yang sama. Hal ini menyebabkan asam amino yang terbentuk berubah lagi menjadi protein. Menurut Winarno (1992) kumpulan asam amino (> 100 buah) dapat membentuk ikatan peptida dan membentuk rantai polipeptida yang tidak bercabang. Nilai kadar protein pada hari ke-9 yaitu 13,17 % tidak jauh berbeda dengan nilai kadar protein awal yaitu 13,74 % (Tabel 5), sehingga produk ikan teri nasi segar yang diawetkan melalui proses perendaman dalam asap cair masih layak untuk dikonsumsi. Hal ini sesuai dengan penelitian Febriani (2006) dimana ikan belut yang direndam asap cair tempurung kelapa dapat awet pada suhu kamar sampai hari ke-9.