PENETAPAN KADAR KURKUMIN DALAM SEDIAAN CAIR OBAT HERBAL TERSTANDAR MERK KIRANTI® SECARA
KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Martinus Supriyadi Krisantoro
NIM : 078114065
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENETAPAN KADAR KURKUMIN DALAM SEDIAAN CAIR OBAT HERBAL TERSTANDAR MERK KIRANTI® SECARA
KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Martinus Supriyadi Krisantoro
NIM : 078114065
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
iv
HALAMAN PERSEMBAHAN
Lebih baik hidup
daripada tidak hidup
Lebih baik berjuang dan gagal
daripada tidak berjuang samasekali
(Henri J.M. Nouwen)
Semua usaha dan jerih lelahku ini
Kupersembahkan untuk
Seluruh keluarga,
Sahabat,
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang telah saya tulis ini tidak memuat karya atau bagian orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 1 Juni 2011 Penulis
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Martinus Supriyadi Krisantoro
Nomor Mahasiswa : 07 8114 065
Demi perkembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan
Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PENETAPAN KADAR KURKUMIN DALAM SEDIAAN CAIR OBAT
HERBAL TERSTANDAR MERK KIRANTI® SECARA KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK.
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan
kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan,
mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan
data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau
media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya
ataupun memberi royalti kepada saya selama tetap mencantumkan nama saya
sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal: 11 Juli 2011
Yang menyatakan
vii
PRAKATA
Puji dan syukur penulis haturkan kepada Tuhan yang Maha Pengasih
karena atas berkat, kasih karunia, dan penyertaan-Nya penulis dapat
menyelesaikan skripsi yang berjudul “Penetapan Kadar Kurkumin dalam Sediaan
Cair Obat Herbal Terstandar Merk Kiranti® secara Kromatografi Cair Kinerja
Tinggi Fase Terbalik dengan baik. Skripsi ini disusun untuk memenuhi salah satu
syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi
Universitas Sanata Dharma, Yogyakarta.
Dalam proses penyusunan skripsi ini banyak bantuan dan dukungan yang
penulis terima dari berbagai pihak, oleh karena itu pada kesempatan ini penulis
ingin mengucapkan terima kasih sebesar-besarnya kepada:
1. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Christine Patramurti, M.Si., Apt. selaku Dosen Pembimbing yang dengan
sabar membimbing dan mendampingi serta memberikan masukan, kritik,
solusi dan semangat kepada penulis selama penelitian dan penyusunan
skripsi.
3. Jefrry Julianus, M.Si. dan Prof. Dr. C. J. Soegihardjo, Apt selaku Dosen
Penguji atas saran dan kritik yang diberikan.
4. Yohanes Dwiatmaka, M.Si. selaku Dosen Pembimbing Akademik yang telah
viii
5. Rini Dwi Astuti, M.Sc., Apt. selaku Kepala Laboratorium Fakultas Farmasi
Universitas Sanata Dharma yang telah memberikan ijin kepada penulis untuk
melakukan penelitian di laboratorium.
6. Prof. Dr. Sudibyo Martono, M.S., Apt. yang telah memberikan senyawa
kurkumin baku untuk keperluan penelitian yang dilakukan oleh penulis.
7. Petugas Laboratorium Kimia Fakultas Farmasi Universitas Sanata Dharma
yang selalu membantu penulis selama melakukan penelitian di laboratorium
Kimia Analisis Instrumental.
8. Petugas sekretariat Fakultas Farmasi Farmasi Universitas Sanata Dharma atas
bantuanya untuk mengurus segala keperluan administrasi skripsi.
9. Segenap dosen, karyawan dan laboran Fakultas Farmasi Universitas Sanata
Dharma yang telah banyak memberikan bantuan selama proses penyusunan
skripsi.
10. Katiti Dwi Krisnayanti dan Marsella Widjaja, sebagai teman satu tim penulis
dalam melakukan penelitian, atas kebersamaan, kerja sama, dan bantuan yang
diberikan. Terima kasih atas smua dukungan dan semangat yang selalu
diberikan.
11. Tim penelitian kurkumin dalam sediaan OHT, atas dukungan, semangat dan
kebersamaan selama penelitian di laboratorium serta sharing ilmu yang
berguna dalam penelitian ini.
12. Teman-teman FST 2007 atas segala candaan dan kekonyolannya selama ini
ix
13. Patrisia Dian Anggraini yang selalu memberikan dukungan, dorongan dan
motivasi kepada penulis.
14. Yohanes Suryanto, Petrus Sonny Santoso Putro dan semua teman-teman
Mudika St. Ignatius de Loyola yang telah memberikan warna dalam hidup
penulis.
15. Semua orang yang telah banyak memberikan bantuan kepada penulis dan
tidak dapat disebutkan satu per satu, terima kasih atas semua bantuan yang
telah diberikan.
Penulis menyadari tentunya masih banyak kekurangan yang terdapat
dalam skripsi ini. Oleh karena itu, penulis mengharapkan kritik dan saran yang
berguna penulis dalam perkembangan selanjutnya. Akhir kata, semoga Tuhan
selalu memberikan berkat bagi kita semua yang menyembahnya dan semoga
skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan. Amrih Mulya
Dalem Gusti.
Yogyakarta, 1 Juni 2011
x
DAFTAR ISI
HALAMAN JUDUL ...……….. i
HALAMAN PERSETUJUAN PEMBIMBING ………... ii
HALAMAN PENGESAHAN ………... iii
HALAMAN PERSEMBAHAN ……….... iv
PERNYATAAN KEASLIAN KARYA ……… v
PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH ……….. vi
PRAKATA ………... vii
DAFTAR ISI ……….. x
DAFTAR TABEL ……….. xiv
DAFTAR GAMBAR ………. xv
DAFTAR LAMPIRAN ……….. xvii
xi
B. Sediaan Cair Obat Dalam ………... 10
C. Obat Herbal Terstandar ………... 10
D. Cara Pembuatan Obat Taradisional yang Baik (CPOTB)…... 11
1. Personalia ……….. 12
2. Bangunan ………... 12
3. Peralatan ……… 13
4. Sanitasi dan higiene ……….. 13
5. Penyiapan bahan baku ………... 13
6. Pengolahan dan pengemasan ………. 13
7. Pengawasan mutu ……….. 14
8. Inspeksi diri ………... 14
9. Dokumentasi ……….. 15
10.Keluhan, laporan dan penarikan kembali produk …….. 15
E. Kiranti® ………... 16
F. Spektrofotometri ………. 17
G. Kromatografi Cair Kinerja Tinggi ………... 19
1. Definisi dan instrumentasi ………. 19
2. Kromatografi partisi ……….. 22
3. Waktu retensi dan pemisahan puncak dalam kromatografi 23 4. Analisis kualitatif dan kuantitatif ……….. 25
H. Landasan Teori ……….. 26
I. Hipotesis ……… 37
xii
A. Jenis dan Rancangan Penelitian ……… 28
B. Variabel Penelitian ……… 28
1. Variabel bebas ……….. 28
2. Variabel tergantung ………. 28
3. Variabel pengacau terkendali ……… 28
C. Definisi Operasional ………. 28
D. Bahan-bahan Penelitian ……… 29
E. Alat-alat Penelitian ……… 29
F. Tata Cara Penelitian ……….. 30
1. Pembuatan fase gerak KCKT ……… 30
2. Pembuatan pelarut metanol pH 4 ……….. 30
3. Pembuatan larutan baku kurkumin ……… 30
4. Penentuan panjang gelombang maksimum (λ) kurkumin.. 31
5. Pembuatan kurva baku kurkumin ………. 31
6. Pemilihan sampel ………... 32
7. Optimasi waktu ekstraksi kurkumin dari sediaan ………. 32
8. Preparasi sampel ……… 32
9. Penetapan kadar kurkumin dalam sampel ………. 33
G. Analisis Hasil ………. 33
1. Uji parametrik Shapiro-Wilk ………. 33
xiii
A. Pemilihan sampel ………... 35
B. Pembuatan Fase Gerak ………... 37
C. Pembuatan Pelarut ……….. 38
D. Penentuan Panjang Gelombang Maksimum ……….. 38
E. Analisis Kulitatif Berdasarkan Waktu Retensi (tR) Kurkumin 40 F. Pembuatan Kurva Baku ……….. 44
G. Optimasi Waktu Ekstraksi Kurkumin dalam Sedian Kiranti® 46 H. Penetapan Kadar Kurkumin dalam Sediaan Kiranti® ……… 49
BAB V. KESIMPULAN DAN SARAN ………... 55
A. Kesimpulan ………. 55
B. Saran ………... 55
DAFTAR PUSTAKA ……… 56
LAMPIRAN ………... 61
xiv
DAFTAR TABEL
Tabel I. Keseragaman Volume Kiranti® ……… 36
Tabel II. Penentuan Kurva Baku Kurkumin ……… 44
Tabel III. Penentuan Kurva Baku Kurkumin Modifikasi ………. 45
Tabel IV. Respon AUC pada masing-masing waktu ekstraksi ………. 48
Tabel V. Kadar Kurkumin dalam sampel Kiranti® pada setiap nomor batch ………. 50
Tabel VI. Nilai normalitas data dari batch 1, 2 dan 3 ……….. 52
Tabel VII. Uji Homogenitas Data ……….. 52
Tabel VIII. Uji Anova ………. 53
xv
DAFTAR GAMBAR
Gambar 1. Struktur kurkuminoid ……….. 7
Gambar 2. Keto-enol tautomeri ………. 8
Gambar 3. Reaksi degradasi kurkumin dalam suasana basa …………. 8
Gambar 4. Logo Obat Herbal Terstandar (OHT) ………... 10
Gambar 5. Kiranti Sehat Datang Bulan ……….. 16
Gambar 6. Diagram tingkat energy elektronik ………... 18
Gambar 7. Skema instrumentasi KCKT ………. 20
Gambar 8. Reaksi silanisasi ……… 23
Gambar 9. Kromatogram hasil pemisahan dua senyawa secara KCKT.. 24
Gambar 10. Reaksi degradasi kolom C18 oleh HCL (pH ≤ 2) ………….. 38
Gambar 11. Gugus kromofor dan auksokrom pada struktur kurkumin ... 39
Gambar 12. Spektra panjang gelombang maksimum kurkumin ……….. 40
Gambar 13. Kromatogram kurkumin baku (A) dan Kromatogram kuekumin dalam sampel Kiranti® ……… 41
Gambar 14. Gugus polar dan gugus nonpolar pada struktur kurkumin… 42 Gambar 15. Interaksi kurkumin dengan fase gerak metanol : asam asetat glasial 2% (90 : 10) ………... 43 Gambar 16. Interaksi kurkumin dengan fase diam C18 ……… 43
Gambar 17. Kurva baku kurkumin ………... 46
xvi
Gambar 19. Kurva optimasi waktu ekstraksi kurkumin dalam sampel
Kiranti® ……… 49
xvii
DAFTAR LAMPIRAN
Lampiran 1. Pernyataan jaminan keaslian bahan kurkumin standar hasil
sintesis ………... 62
Lampiran 2. Spektra panjang gelombang maksimum kurkumin ……… 63
Lampiran 3. Hasil uji stabilitas kurkumin pada pH 3-5 ……… 64
Lampiran 3. Kromatogram pelarut metanol pH 4 (blanko) ... 65
Lampiran 4. Kromatogram baku kurkumin ……… 67
Lampiran 5. Perolehan AUC seri baku kurkumin ……….. 78
Lampiran 6. Persamaan dan gambar kurva baku kurkumin …………... 79
Lampiran 7. Kromatogram optimasi waktu ekstraksi ………. 80
Lampiran 8. Nilai AUC hasil Optimasi waktu ekstraksi dan kurva baku hubungan antara waktu ekstraksi dengan nilai AUC. 82 Lampiran 9. Contoh perhitungan resolusi pemisahan kurkumin dalam sampel ……… 83
Lampiran 10. Perhitungan kadar kurkumin teoritis dalam setiap botol OHT merk Kiranti® ………... 84
Lampiran 11. Kromatogram hasil penetapan kadar ………. 86
Lampiran 12. Data kadar kurkumin dalam sediaan cair OHT Kiranti® … 94 Lampiran 13. Contoh perhitungan kadar kurkumin dalam sediaan cair OHT Kiranti® ………. 95
xviii
PENETAPAN KADAR KURKUMIN DALAM SEDIAAN CAIR OBAT HERBAL TERSTANDAR MERK KIRANTI® SECARA
KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK
INTISARI
Kiranti® merupakan salah satu jenis sediaan cair obat herbal terstandar (OHT) yang diproduksi oleh PT Ultra Prima Abadi (Orang Tua Group). Kunyit merupakan komponen utama yang terdapat dalam Kiranti®. Senyawa aktif yang menyusun sebagian besar kunyit adalah kurkumin. Kurkumin dapat ditetapkan kadarnya menggunakan metode Kromatografi Kinerja Tinggi (KCKT) fase terbalik.
Penelitian ini bersifat noneksperimental deskriptif karena tidak terdapat manipulasi dan perlakuan terhadap subjek uji. Kurkumin dianalisis secara kuantitatif dengan sistem KCKT fase terbalik dengan kolom oktadesilsilan (C18) dan detektor Ultraviolet-Visible (UV-VIS) pada panjang gelombang 432 nm serta menggunakan fase gerak campuran metanol dan asam asetat glasial 2% (90:10 v/v). Metode yang digunakan dalam penelitian ini telah dioptimasi dan divalidasi.
Penetapan kadar kurkumin yang ada di dalam sediaan cair OHT merk Kiranti® dilakukan untuk melihat kesesuaian kadar kurkumin terukur dengan kadar kurkumin yang tertulis pada label dan kesamaan kadar kurkumin dalam tiga
batch sediaan Kiranti®. Kadar rata-rata kurkumin dalam tiga batch Kiranti®
berturut-turut sebagai berikut batch 1 sebesar 14,0364±0.2033 mg/ml; batch 2 sebesar 36,1886±0,6878 mg/ml; dan batch 3 sebesar 17,0578±0,2546 mg/ml. Kadar tersebut lebih tinggi daripada kadar teoritis kurkumin dalam sampel Kiranti®. Kadar kurkumin dalam ketiga batch Kiranti® tersebut tidak sama.
xix
QUANTIFICATION OF CURCUMIN IN LIQUID DOSAGE FORM OF SCIENTIFIC BASED HERBAL MEDICINE KIRANTI® USING HIGH PERFORMANCE LIQUID CHROMATOGRPHY REVERSE PHASE
ABSTRACT
Kiranti® is the one of scientific based herbal medicine liquid dosage form which produced by PT Ultra Prima Abadi (Orang Tua Group). Turmeric is the main component in Kiranti®. The main active compound in turmeric is curcumin. Curcumin can be quantified by reverse phase of High Pressure Liquid Chromatography (HPLC) method.
This experiment was descriptive non-experimental because there were no manipulation and treatment to the test subject. Curcumin was determined quantitatively by reverse phase of High Pressure Liquid Chromatography (HPLC) method. The experiment was using octadecylsilane (C18) column and ultraviolet-visible (UV-Vis) Detector. The maximum wavelength was 432 nm. Methanol and Glacial acetic acid (2%) mixture (90:10 v/v) were used as mobile phase in HPLC. The method that used in this experiment, was optimized and validated.
The determination of curcumin in Kiranti was done for inspecting the compatibility of determined curcumin concentration with curcumin concentration which written in the label. Besides that, the similarity of curcumin concentration in three batches Kiranti was inspected too. The average of curcumin concentration in first batch was 14,0364±0.2033 mg/ml; in second batch was 36,1886±0,6878 mg/ml; and the third batch was 17,0578±0,2546 mg/ml. The concentration was higher than curcumin concentration theoretically in Kiranti. The curcumin concentration in three batches Kiranti was not similar.
1
BAB I PENDAHULUAN
A.Latar Belakang
Tren pengobatan yang berkembang di masyarakat saat ini adalah
pengobatan dengan obat-obat tradisional memanfaatkan sumber daya alam yang
ada (back to nature). Masyarakat umum beranggapan bahwa pengobatan menggunakan Obat Tradisional (OT) lebih aman daripada pengobatan dengan
menggunakan obat-obat modern karena OT efek sampingnya relatif lebih kecil.
Dari segi efek samping dapat dikatakan bahwa OT memiliki efek samping relatif
kecil dibandingkan obat modern, tetapi perlu dipertimbangkan bahwa belum ada
penjaminan mutu yang dilakukan bila ditinjau dari kepastian bahan aktif dan
konsistensinya (Katno dan Pramono, 2004).
Obat Tradisional terdiri atas tiga macam jenis, yaitu Jamu, Obat Herbal
Terstandar (OHT) dan Fitofarmaka. OHT adalah sediaan obat bahan alam yang
telah dibuktikan keamanan dan khasiatnya secara ilmiah melalui uji praklinik dan
bahan bakunya telah di standarisasi (Badan Pengawas Obat dan Makanan, 2005b).
Dari pengertian tersebut, dapat dilihat bahwa yang menjadi syarat utama OHT
hanya terbatas pada keamanan, klaim khasiat yang dibuktikan secara ilmiah
melalui uji praklinik dan standarisasi bahan baku. Dari beberapa penelitian untuk
bentuk sediaan dengan obat herbal sebagai bahan baku yang berkembang saat ini
juga hanya difokuskan pada isolasi, identifikasi, dan studi farmakologi zat aktif,
stabil setelah distribusi sangat jarang ditemukan (Musfiroh, Indriyanti, Susilawati,
dan Percekawati, 2009). Penjaminan reprodusibilitas kadar ini perlu dilakukan
terutama jika penggunaan obat tradisional ini akan diarahkan pada pelayanan
kesehatan formal.
Simplisia yang banyak digunakan dalam OT yang beredar di Indonesia
adalah kunyit (Curcumae domesticae). Kunyit memiliki senyawa yang bertanggung jawab terhadap respons biologis berupa zat warna, yaitu
kurkuminoid. Kurkuminoid di antaranya merupakan campuran kurkumin,
demetoksikurkumin, dan bis-demetoksikurkumin (Batubara, Rafi, dan Darusman, 2005). Dari ketiga senyawa kurkuminoid tersebut, kurkumin merupakan
komponen terbesar sehingga sering kadar total kurkuminoid dihitung sebagai %
kurkumin (Sumiati, 2003). Kurkumin memiliki sifat fotosensitif, terutama jika
berada dalam bentuk larutan, sehingga stabilitasnya sangat dipengaruhi oleh
adanya cahaya. Selain itu, stabilitas kurkumin juga sangat dipengaruhi oleh pH
lingkungan. Kurkumin stabil pada pH asam dan mudah terurai pada pH di atas
netral.
Salah satu produk OT yang menggunakan kunyit sebagai komponen
utama untuk menimbulkan efek yang diinginkan adalah Kiranti®. Kiranti®
merupakan salah satu jenis sediaan cair obat herbal terstandar (OHT) yang
diproduksi oleh PT Ultra Prima Abadi (Orang Tua Group). Dalam satu botol
Kiranti® kemasan 150 ml mengandung Curcumae domesticae Rhizoma (30g),
Tamarindi Pulpa (6g), Kaempferiae Rhizoma (3g), Arengae pinnata Fructose
(0,1g), Air (sampai dengan 150ml). Kiranti® memiliki klaim khasiat untuk
memperlancar haid serta mengatasi keluhan haid seperti nyeri, letih, lesu,
keputihan serta bau badan, membuat tubuh terasa bersih, sehat dan segar
(Anonim, 2011).
Kiranti® merupakan produk yang sangat diminati masyarakat terutama
kaum wanita untuk mengatasi keluhan-keluhan yang timbul ketika haid. Sebagai
produk yang sangat diminati masyarakat maka menuntut produksi dalam skala
yang besar dari Kiranti®. Hal ini menuntut pula dilakukannya pengendalian mutu
sediaan yang mana akan memberikan jaminan bahwa sediaan akan memberikan
efek yang sama pada setiap kemasan.
Penjaminan mutu terhadap produk Kiranti® juga perlu dilakukan terkait
dengan stabilitas bahan aktif kurkumin yang menjadi komponen utama dalam
sediaan Kiranti®. Penjaminan mutu ini dapat dilakukan dengan menetapkan kadar
kurkumin yang terkandung dalam sediaan Kiranti®. Penetapan kadar kurkumin
dapat digunakan untuk mengetahui stabilitas kurkumin selama proses produksi,
dan penyimpanan Kiranti®. Kadar yang sama dalam setiap kemasan
menggambarkan bahwa stabilitas kurkumin tetap terjaga sehingga setiap kemasan
sediaan tersebut akan memberikan efek yang sama pula.
Analisis kuantitatif kurkumin membutuhkan suatu metode analisis yang
cepat dan tepat. Metode analisis kuantitatif yang saat ini banyak digunakan adalah
analisis dengan metode spektroskopi, metode Kromatografi Lapis
Tipis-Desitometri (KLT-Densitometri) dan metode Kromatografi Cair Kinerja Tinggi
memungkinkan untuk melakukan analisis kuantitatif menggunakan sistem fase
terbalik dengan kolom oktadesilsilan (C18), fase gerak asetonitril:asam asetat 2%
(45:55) dan detektor Ultraviolet-Visible (UV-VIS) (Musfiroh dkk., 2009). Pada
penelitian ini, sistem KCKT yang digunakan adalah sistem KCKT fase terbalik,
dengan kolom oktadesilsilan (C18) dan fase gerak campuran metanol p.a dan asam asetat glasial p.a 2%.
Penelitian ini merupakan tahap akhir dari rangkaian penelitian
“Penetapan Kadar Kurkumin dalam Sediaan Cair Obat Herbal Terstandar (OHT)
Merk Kiranti® secara Kromatografi Cair Kinerja Tinggi (KCKT) Fase Terbalik”
yang meliputi tahap optimasi, validasi dan aplikasi. Dari hasil optimasi didapatkan
sistem KCKT yang optimum menggunakan fase gerak campuran metanol p.a. dan asam asetat glasial p.a. 2% (90:10 v/v, pH 4), fase diam oktadesilsilan (C18) dengan kecepatan alir 0,5 ml/menit (Krisnayanti, 2011). Sistem ini juga
memenuhi syarat parameter validitas yang baik, meliputi selektivitas (Rs =
1,4383, linearitas (r = 0,9992), akurasi dan presisi (pada konsentrasi 3,030 ppm)
(Widjaja, 2011).
1. Permasalahan
Permasalahan yang dapat dirumuskan berdasarkan latar belakang tersebut
antara lain:
a. apakah kadar kurkumin dalam sediaan cair OHT merk Kiranti® yang
ditetapkan dengan metode KCKT fase terbalik sesuai dengan kadar yang
b. apakah ada perbedaan kadar kurkumin dalam tiga nomor batch sediaan cair OHT merk Kiranti® yang diteliti?
2. Keaslian penelitian
Sejauh pengetahuan penulis dari penulusuran pustaka dan jurnal, belum
pernah dilakukan penetapan kadar kurkumin dalam sediaan cair sirup OHT Merk
Kiranti® menggunakan metode KCKT fase terbalik dengan fase diam kolom C18
dan fase gerak campuran asam asetat glasial p.a 2% dan metanol p.a untuk
melihat reprodusibilitas kadar sediaan. Beberapa penelitian analisis kurkumin
yang telah dilakukan menggunakan metode kromatografi antara lain: KLT dengan
detektor visibel (Dwivedi, Raman, Seth, dan Sarin, 1992; Tonnesen dan Karlsen,
1986; Martono, 1996), kromatografi elektrokinetik mikroemulsi (Nhujak,
Saisuwan, Srisaart, dan Petsom, 2006), KCKT dengan kolom Nucleosil NH2
detektor UV-Vis dan fluorometri (Tonnesen dan Karlsen, 1983), KCKT dengan
kolom RP18 dan Nucleosil NH2 detektor UV-Vis (Tonnesen dan Karlsen, 1985a),
KCKT dengan kolom RP18 dan Nucleosil NH2 detektor UV-Vis dan fluoresensi
(Tonnesen, 1986), KCKT dengan kolom C18 detektor fluoresensi (Tonnesen dan
Karlsen, 1986), KCKT dengan kolom Nucleosil NH2 detektor UV (Khurana dan
Ho, 1988), KCKT dengan kolom C18 detektor visibel (Jayaprakasha, Rao, dan
Sakariah, 2002), KCKT dengan kolom ODS menggunakan detektor UV (Smith
dan Witowska, 1984), KCKT menggunakan kolom HiQ-Sil C18
(Rungphanichkul, 2004), KCKT menggunakan kolom C18 detektor UV (Heath,
detektor visibel (Jadhav dkk., 2007), KCKT dengan kolom amino-bonded
detektor visibel (Sumule, 2007), kromatografi high-speed countercurrent (Inoue, Nomura, Ito, Nagatsu, Hino, dan Oka, 2008), Kromatografi Lapis Tipis Kinerja
Tinggi (KLTKT) dengan detektor visibel (Paramasivam, Aktar, Poi, Banerjee, dan
Bandyopadhyay, 2008).
3. Manfaat penelitian
a. Manfaat metodologis
b.
. Memberikan informasi tentang penetapan kadar
kurkumin dalam sediaan cair OHT menggunakan metode Kromatografi Cair
Kinerja Tinggi (KCKT) fase terbalik
Manfaat praktis. Memberikan informasi kepada masyarakat tentang
keberadaan dan kadar kurkumin dalam sediaan cair OHT Merk Kiranti®.
B. Tujuan Penelitian
Tujuan dari dilakukannya penelitian ini adalah:
1. mengetahui kesesuaian kadar kurkumin dalam sediaan cair OHT merk
Kiranti® yang ditetapkan dengan metode KCKT fase terbalik dengan kadar
yang tertera pada label kemasan.
7
BAB II
PENELAAHAN PUSTAKA
A. Kurkumin
Kurkumin adalah serbuk kristal oranye-kuning yang praktis tidak larut
dalam air dan eter namun larut dalam etanol, dimetilsulfoksida, dan aseton.
Rumus molekul kurkumin adalah C21H20O6 dengan titik didih 1830C, dan bobot
molekul 368,37 g/mol. Kurkumin komersial mengandung sekitar 77% kurkumin,
17% demetoksikurkumin, dan 3% bis-demetoksikurkumin sebagai komponen utama (Shishodia, Chaturvedi, dan Aggarwal, 2007).
Gambar 2. Struktur kurkuminoid (Aggarwal, Kumar, Aggarwal dan Shishodia, 2005)
Keterangan: A = kurkumin (77%), B = demetoksikurkumin (17%), C = bis-demetoksikurkumin (3%)
Menurut Prasad (cit. Aggarwal, Bhatt, Ichikawa, Ahn, Sethi, Sandur, Natarajan, Seeram, dan Shishodia, 2006) kurkumin dalam metanol memiliki
A
B
serapan maksimum (λmax) 430 nm. Dalam bentuk cairan komponen utama
kurkumin akan mengalami keto-enol tautomeri dan lebih dari 95% berada dalam
bentuk enol, tergantung dari solven yang digunakan (Stankovic, 2004).
keto enol
Gambar 2. Keto-enol tautomeri (Stankovic, 2004)
Komponen warna utama kurkumin relatif stabil pada pH asam, tetapi
akan cepat terurai di atas pH netral. Menurut penelitian yang dilakukan oleh
Tonnesen dan Karlsen, dalam suasana basa (pH 7 – 10) kurkumin akan
terdegradasi menghasilkan produk asam ferulat dan feruloil metan. Feruloil metan
ini secara cepat akan membentuk produk kondensasi yang berwarna kuning muda
sampai kuning kecoklatan. Selanjutnya feruloil metan akan mengalami hidrolisis
menghasilkan produk degradasi berupa vanilin dan aseton (Stankovic, 2004).
Menurut Sasaki dkk. (cit Stankovic, 2004), kurkumin juga tidak stabil terhadap cahaya, terutama jika kurkumin berada dalam bentuk cairan. Setelah
terjadi paparan cahaya, maka akan terbentuk produk siklisasi serta produk
dekomposisi seperti asam vanilat, vanilin, dan asam ferulat.
Kurkumin dalam kunyit banyak digunakan sebagai pewarna makanan.
Selain itu, dalam bidang kesehatan secara tradisional sering digunakan sebagai
anti inflamasi, untuk mengobati perut kembung, penyakit kuning, melancarkan
haid, hematuria, perdarahan, dan kolik. Saat ini penelitian tentang kurkumin
banyak difokuskan untuk mengetahui daya antioksidan, hepatoprotektif, anti
inflamasi, anti kanker, dan antimikroba dari kurkumin serta daya untuk mengobati
penyakit kardiovaskular dan gangguan gastrointestinal (Thorne Research, 2002)
Kurkumin dapat diisolasi dari tanaman famili Zingiberaceae terutama pada tanaman Curcuma longa, Curcuma mangga, Curcuma zedoaria, Costus speciosus, Curcuma xanthorrhiza, Curcuma aromatica, Cucruma phaeocaulis,
Etlingera elatior dan Zingiber cassumunar. Kurkumin merupakan senyawa
fitokimia yang memberikan warna kuning untuk kunyit dan saat ini dipercaya
sebagai senyawa yang bertanggung jawab untuk sebagian besar efek terapi dari
kunyit. Diperkirakan bahwa 2-5% dari kunyit merupakan kurkumin. Kurkumin
diisolasi pertama kali dari kunyit pada tahun 1815, dan struktur kurkumin
digambarkan pertama kali pada tahun 1910 sebagai diferuloilmetan (Aggarwal
B. Sediaan Cair Obat Dalam
Cairan obat dalam obat tradisional adalah sediaan obat tradisional berupa
larutan emulsi atau suspensi dalam air, bahan bakunya berasal dari serbuk
simplisia atau sediaan galenik dan digunakan sebagai obat dalam. Persyaratan
yang harus dipenuhi untuk cairan obat dalam obat tradisional antara lain dalam hal
keseragaman volum, angka lempeng total tidak lebih dari 10, angka kapang
khamir tidak lebih dari 10, mikroba patogen negatif, aflatoksin tidak lebih dari 30
bpj, bahan tambahan, wadah dan penyimpanan, penandaan (Kementerian
Kesehatan Republik Indonesia, 1994)
C. Obat Herbal Terstandar
Menurut keputusan Keputusan Kepala Badan Pengawas Obat dan
Makanan Tentang Ketentuan Pokok Pengelompokan dan Penandaan Obat Bahan
Alam Indonesia, berdasarkan cara pembuatan serta jenis klaim penggunaan dan
tingkat pembuktian khasiat, Obat Bahan Alam Indonesia dikelompokkan menjadi
Jamu, Obat Herbal Terstandar, Fitofarmaka (Badan Pengawas Obat dan Makanan,
2004).
Gambar 4. Logo obat herbal terstandar (OHT) (Badan Pengawas Obat dan Makanan, 2004).
Obat herbal terstandar (OHT) adalah sediaan obat bahan alam yang telah
bahan bakunya telah distandarisasi (Badan Pengawas Obat dan Makanan, 2005b).
Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan Republik
Indonesia, No: HK. 00.05.4.2411, OHT harus memenuhi beberapa criteria, yakni
aman sesuai dengan persyaratan yang ditetapkan, klaim kasiat dibuktikan secara
ilmiah/uji pra klinik, telah dilakukan standarisasi terhadap bahan baku yang
digunakan dalam produk jadi dan memenuhi persyaratan mutu yang berlaku. Jenis
klaim penggunaan sesuai dengan tingkat pembuktian yaitu tingkat pembuktian
umum dan medium (Badan Pengawas Obat dan Makanan, 2004).
Untuk dapat memiliki izin edar obat tradisional, obat herbal terstandar
dan fitofarmaka harus memenuhi kriteria sebagai berikut: menggunakan bahan
berkhasiat dan bahan tambahan yang memenuhi persyaratan mutu, keamanan dan
kemanfaatan/khasiat; dibuat sesuai dengan ketentuan tentang Pedoman Cara
Pembuatan Obat Tradisional yang Baik atau Cara Pembuatan Obat yang Baik
yang berlaku; penandaan berisi informasi yang lengkap dan obyektif yang dapat
menjamin penggunaan obat tradisional, obat herbal terstandar dan fitofarmaka
secara tepat, rasional dan aman sesuai dengan hasil evaluasi dalam rangka
pendaftaran (Badan Pengawas Obat dan Makanan, 2005b).
D. Cara Pembuatan Obat Tradisional yang Baik (CPOTB)
Cara Pembuatan Obat Tradisional yang Baik (CPOTB) meliputi seluruh
aspek yang menyangkut proses pembuatan obat tradisional. CPOTB bertujuan
untuk menjamin agar produk yang dihasilkan senantiasa memenuhi persyaratan
tergantung dari bahan awal, proses produksi dan pengawasan mutu, bangunan,
peralatan dan personalia yang menangani (Badan Pengawas Obat dan Makanan,
2005a).
1. Personalia
Personalia hendaklah mempunyai pengetahuan, pengalaman, ketrampilan
dan kemampuan yang sesuai dengan tugas dan fungsinya, dan tersedia dalam
jumlah yang cukup. Mereka hendaklah dalam keadaan sehat dan mampu
menangani tugas yang dibebankan kepadanya. Dalam struktur organisasi
perusahaan, bagian produksi dan pengawasan mutu hendaklah dipimpin oleh
orang yang berbeda dan tidak ada keterkaitan tanggungjawab satu sama lain.
Hendaklah dijabarkan kewenangan dan tanggungjawab personil-personil lain
yang ditunjuk untuk menjalankan Pedoman CPOTB dengan baik. Semua personil
yang langsung terlibat dalam kegiatan pembuatan hendaklah dilatih dalam
pelaksanaan pembuatan sesuai dengan prinsip-prinsip Cara Pembuatan yang Baik.
Pelatihan CPOTB hendaklah dilakukan secara berkelanjutan dan dievaluasi secara
periodik (Badan Pengawas Obat dan Makanan, 2005a).
2. Bangunan
Bangunan industri obat tradisional hendaklah menjamin aktifitas industri
dapat berlangsung dengan aman, berada di lokasi yang bebas dari pencemaran dan
tidak mencemari lingkungan serta memenuhi persyaratan higienis dan sanitasi
3. Peralatan
Peralatan yang digunakan dalam pembuatan produk hendaknya memiliki
rancang bangun konstruksi yang tepat, ukuran yang memadai serta ditempatkan
dengan tepat, sehingga mutu yang dirancang bagi tiap produk terjamin secara
seragam dari batch ke batch, serta untuk memudahkan pembersihan dan
perawatannya (Badan Pengawas Obat dan Makanan, 2005a).
4. Sanitasi dan higiene
Dalam pembuatan produk hendaknya diterapkan tindakan sanitasi dan
higiene pada setiap bangunan, peralatan dan perlengkapan, personalia, bahan dan
wadah serta faktor lain sebagai sumber pencemaran produk (Badan Pengawas
Obat dan Makanan, 2005a).
5. Penyiapan bahan baku
Setiap bahan baku yang digunakan untuk pembuatan hendaklah
memenuhi persyaratan yang berlaku mulai dari data penerimaan bahan baku
simplisia, pelabelan, sortasi, pencucian, pengeringan, penyimpanan sampai pada
bahan baku siap untuk diolah (Badan Pengawas Obat dan Makanan, 2005a).
6. Pengolahan dan pengemasan
Pengolahan dan pengemasan hendaknya dilaksanakan dengan mengikuti
cara yang telah ditetapkan oleh industri sehingga dapat menjamin mutu produk
yang dihasilkan senantiasa memenuhi persyaratan yang berlaku (Badan Pengawas
7. Pengawasan mutu
Pengawasan mutu merupakan bagian yang essensial dari cara pembuatan
obat tradisional yang baik. Keterikatan dan tanggung jawab semua unsur dalam
semua rangkaian pembuatan adalah mutlak untuk menghasilkan produk yang
bermutu mulai dari bahan awal sampai pada produk jadi. Untuk keperluan
tersebut bagian pengawasan mutu hendaknya merupakan bagian yang tersendiri.
Sistem pengawasan mutu hendaknya dirancang dengan tepat untuk menjamin
bahwa tiap produk mengandung bahan dengan mutu yang benar dan dibuat pada
kondisi yang tepat serta mengikuti prosedur standar sehingga produk tersebut
senantiasa memenuhi persyaratan produk jadi yang berlaku (Badan Pengawas
Obat dan Makanan, 2005a).
8. Inspeksi diri
Tujuan inspeksi diri adalah untuk melakukan penilaian apakah seluruh
aspek pengolahan, pengemasan dan pengendalian mutu selalu memenuhi CPOTB.
Program inspeksi diri hendaknya dirancang secara teratur untuk mengevaluasi
pelaksanaan CPOTB dan untuk menetapkan tindak lanjut. Tindakan perbaikan
yang disarankan hendaknya dilaksanakan (Badan Pengawas Obat dan Makanan,
2005a).
Untuk pelaksanaan inspeksi diri hendaknya ditunjuk tim inspeksi yang
mampu menilai secara obyektif pelaksanaan CPOTB. Tim inspeksi diri ini
ditunjuk oleh pimpinan perusahaan terdiri dari sekurang-kurangnya 3 (tiga) orang
dibuat prosedur dan catatan mengenai inspeksi diri (Badan Pengawas Obat dan
Makanan, 2005a).
9. Dokumentasi
Dokumentasi pembuatan produk merupakan bagian dari sistem informasi
manajemen yang meliputi spesifikasi, label/etiket, prosedur, metoda dan instruksi,
catatan dan laporan serta jenis dokumentasi lain yang diperlukan dalam
perencanaan, pelaksanaan, pengendalian serta evaluasi seluruh rangkaian kegiatan
pembuatan produk. Dokumentasi sangat penting untuk memastikan bahwa setiap
petugas mendapat instruksi secara rinci dan jelas mengenai bidang tugas yang
harus dilaksanakannya, sehingga memperkecil risiko terjadinya salah tafsir dan
kekeliruan yang biasanya timbul karena hanya mengandalkan komunikasi lisan
(Badan Pengawas Obat dan Makanan, 2005a).
10.Keluhan, laporan dan penarikan kembali produk
Keluhan dan laporan menyangkut kualitas, efek yang merugikan atau
masalah medis lainnya hendaknya diselidiki dan dievaluasi serta diambil tindak
lanjut yang sesuai. Penarikan kembali produk adalah penarikan kembali satu atau
beberapa batch atau seluruh produk tertentu dari semua mata rantai distribusi. Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak
memenuhi persyaratan atau atas dasar pertimbangan adanya efek yang tidak
diperhitungkan yang merugikan kesehatan. Penarikan kembali seluruh produk
tertentu dapat merupakan tindak lanjut penghentian pembuatan satu jenis produk
E. Kiranti®
Kiranti Sehat Datang Bulan adalah minuman tradisional Indonesia
dengan ramuan warisan nenek moyang, yang memiliki khasiat untuk melancarkan
haid, mengatasi keluhan-keluhan nyeri haid, mencegah mual dan muntah,
mencegah keputihan dan bau badan, serta meningkatkan ketahanan tubuh agar
tetap sehat dan aktif di masa haid (Research and Innovation Center, 2005).
Gambar 5. Kiranti Sehat Datang Bulan
Standarisasi produksi Kiranti dilakukan mulai dari bahan baku sampai
produk akhir dan diformulasikan secara rasional; bahan-bahan yang digunakan
sudah teruji khasiatnya secara ilmiah; menggunakan bahan-bahan tumbuhan obat
yang sudah diketahui tingkat keamanannya dan tidak menimbulkan efek samping
negatif; khasiat dan keamanannya sudah terbukti berdasarkan pengalaman nenek
moyang (Research and Innovation Center, 2005).
Kiranti merupakan salah satu Obat Herbal Terstandar yang berdedar di
Indonesia dan diproduksi oleh PT Ultra Prima Abadi (Orang Tua Group). Setiap
kemasan Kiranti® mengandung Curcumae domesticae Rhizoma (30g), Tamarindi
Rhizoma (0,8g), Paulliniacupana (0,23g), Cinnamomi Cortex (0,1g), Air (sampai dengan 150ml) (Anonim, 2011).
Berdasarkan hasil uji praklinik yang telah dilakukan menunjukkan bahwa
Kiranti Sehat Datang Bulan adalah minuman tradisional dengan ramuan warisan
nenek moyang Indonesia yang menggunakan bahan tumbuhan obat yang benar,
sesuai khasiatnya, terstandarisasi, aman untuk dikonsumsi jangka panjang dan
terbukti bermanfaat untuk mengatasi gangguan nyeri haid dan gangguan
keputihan (Research and Innovation Center, 2005).
F. Spektrofotometri
Spektrofotometri visibel merupakan suatu teknik analisis spektroskopik
menggunakan sumber radiasi elektromagnetik sinar tampak (380-780 nm) dengan
menggunakan spektrofotometer (Khopkar, 1990).
Prinsip kerja spektrofotometri berdasarkan atas interaksi antara radiasi
elektromagnetik dengan atom atau molekul yang menyebabkan terjadinya
absorpsi, yaitu perpindahan energi dari sinar radiasi ke molekul (Mulja dan
Suharman, 1995).
Absorbsi ini menyebabkan peralihan elektronik atau transisi elektronik,
yaitu peningkatan energi elektron dari tingkat dasar (ground state) ke tingkat energi yang lebih tinggi (excited state). Transisi ini terjadi bila energi yang dihasilkan oleh radiasi sama dengan energi yang diperlukan untuk melakukan
transisi. Hasil interaksi antara radiasi elektromagnetik dengan atom atau molekul
elektromagnetik yang diserap dengan panjang gelombang, yang disebut dengan
spektrum absorpsi (Rohman dan Gandjar, 2007).
Ada empat tipe transisi elektronik yang mungkin terjadi yaitu σ→σ*,
n→σ*, n→π*, dan π→π*. Eksitasi elektron (σ→σ*) memberikan energi yang
terbesar dan terjadi pada daerah ultraviolet jauh yang diberikan oleh ikatan
tunggal, misalnya alkana. Untuk mengeksitasikan elektron yang berada pada suatu
ikatan kovalen tunggal terikat kuat (orbital σ) diperlukan radiasi berenergi tinggi
atau panjang gelombang pendek. Oleh karena itu, serapan maksimum yang
disebabkan oleh transisi ini tidak pernah teramati pada daerah ultraviolet (Mulja
dan Suharman, 1995).
Eksitasi elektron (n→σ*) terjadi juga pada gugus karbonil (dimetil keton
dan asetaldehid) yang terjadi pada daerah ultraviolet jauh (Mulja dan Suharman,
1995). Energi yang diperlukan untuk transisi jenis ini lebih kecil dibanding
transisi σ→σ* sehingga sinar yang diabsorbsi pun memiliki panjang gelombang
yang lebih panjang, yaitu sekitar 150-250 nm (Rohman dan Gandjar, 2007).
Transisi elektron n→π* dan π→π* merupakan transisi yang paling cocok
untuk analisis karena memberikan spektra pada panjang gelombang antara
200-700 nm (Rohman dan Gandjar, 2007). Kedua transisi ini membutuhkan adanya
kromofor dan auksokrom dalam struktur molekulnya. Kromofor adalah suatu
gugus fungsional tidak jenuh yang menyediakan orbital π yang dapat menyerap
pada daerah ultraviolet. Molekul yang mengandung kromofor disebut kromogen.
Sedangkan auksokrom merupakan gugus jenuh yang bila terikat pada kromofor
mengubah panjang gelombang dan intensitas serapan maksimum, cirinya adalah
heteroatom yang langsung terikat pada kromofor (Sastrohamidjojo, 2002).
G. Kromatografi Cair Kinerja Tinggi 1. Definisi dan Instrumentasi
Kromatografi Cair Kinerja Tinggi (KCKT) adalah teknik pemisahan
campuran senyawa berdasarkan interaksi dengan fase diam di bawah aliran fase
gerak, dimana fase gerak dialirkan dengan bantuan tekanan menuju kolom secara
cepat dan dideteksi dengan detektor yang sesuai (Hendayana, 2006).
Kromatografi Cair Kinerja Tinggi (KCKT) memanfaatkan kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sensitif
sehingga kromatografi kolom cair dapat menjadi sistem pemisahan dengan
kecepatan dan efisiensi yang tinggi (Direktorat Jenderal Pengawasan Obat dan
Makanan RI, 1995).
Metode KCKT merupakan metode yang banyak digunakan dalam
analisis karena metode ini memiliki beberapa keuntungan, antara lain: mampu
kecepatan analisis dan kepekaan tinggi, dapat menghindari terjadinya
dekomposisi atau kerusakan bahan yang dianalisis, resolusi yang baik, dapat
digunakan untuk bermacam-macam detektor, kolom dapat digunakan kembali,
mudah melakukan “sample recovery” (Snyder dan Kirkland, 1979). Selain itu, pemisahan pada sistem KCKT dapat terjadi dalam waktu cepat sehingga dapat
memisahkan zat-zat yang tidak menguap atau tidak tahan panas tanpa perlu
membuat derivat yang mudah menguap (Direktorat Jenderal Pengawasan Obat
dan Makanan RI, 1995).
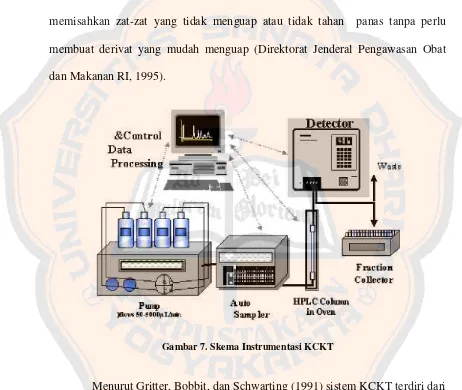
Gambar 7. Skema Instrumentasi KCKT
Menurut Gritter, Bobbit, dan Schwarting (1991) sistem KCKT terdiri dari
tiga variabel utama, yaitu fase diam, fase gerak dan detektor.
1. Fase diam. Fase diam berupa kolom yang merupakan bagian yang
sangat penting dalam pemisahan komponen-komponen sampel. Keberhasilan
Suharman, 1995). Kolom pada KCKT dapat berupa gelas atau baja tidak berkarat.
Kolom gelas dapat menahan tekanan sampai 50 atm. Panjang kolom bervariasi
antara 15-150 cm dan diameter antara 3-5mm. Pengisi kolom biasanya adalah
silika gel, alumina dan elit (Khopkar, 1990). Fase diam yang biasa digunakan
pada kromatografi partisi fase balik adalah oktadesilsilan (ODS). Selain ODS,
dikenal pula silika dengan substitusi oktil (C8) (Munson, 1991).
2. Fase gerak.
Fase gerak yang digunakan untuk analisis secara KCKT harus murni,
tanpa cemaran, tidak bereaksi dengan kemasan, dapat melarutkan analit (solute), viskositas rendah, memungkinkan memperoleh kembali analit dengan mudah,
serta harganya wajar (Johnson dan Stevenson, 1978). Fase gerak KCKT juga
harus bebas dari gas terlarut karena dapat mempengaruhi respon detektor sehingga
memunculkan sinyal palsu dan akan mempengaruhi kolom (Gritter dkk., 1985).
Selain itu, kolom juga haruslah tidak mudah terbakar dan memiliki toksisitas
rendah (Skoog, Holler, dan Nieman, 1985).
Banyaknya senyawa yang dapat dipisahkan oleh KCKT
terutama tergantung pada keanekaragaman fase gerak. Fase gerak pada KCKT
sangat berpengaruh pada tambatan dan pemisahan senyawa (Munson, 1984). Fase
gerak dapat berupa pelarut tunggal atau pelarut campuran (Gritter dkk., 1991).
Pemisahan dengan pelarut tunggal disebut elusi isokratik, sedangkan elusi gradien
dua pelarut dengan berbagai perubahan komposisi dialirkan. Pelarut dialirkan ke
botol penyampur pada berbagai laju aliran. Sebagian besar pompa KCKT
mempunyai keluaran tekanan 1000-6000 psi dan mampu menghasilkan aliran
Pemilihan fase gerak yang digunakan adalah terutama berdasarkan
kepolaran campuran pelarut yang semakin linier dengan pelarut murni. Tingkat
kepolaran pelarut menggambarkan kekuatan pelarut dalam mengelusi suatu
senyawa (Gritter dkk., 1991).
3. Detektor.
Secara umum detektor dibagi menjadi dua kategori, yakni Bulk property
detectors dan Solut property detectors. Bulk property detectors adalah detektor
sebagai pengukur perubahan sifat fisik fase gerak dan solut. Detektor tipe ini
cenderung relatif tidak sensitif dan menghendaki temperatur yang terkendali,
contohnya adalah detektor bias, sedangkan Solut property detectors adalah detektor yang hanya mengukur sifat fisik solut. Solut property detectors 1000 kali lebih sensitif dan mampu mengukur analit sampai satuan nanogram atau lebih
kecil lagi. Contoh detektor jenis ini, yaitu detektor fluorensensi, detektor
penyerapan (UV-Vis) dan detektor elektrokimia (Munson, 1991).
Menurut Johnson dan Stevenson (1978), detektor diperlukan
untuk mendeteksi adanya komponen analit yang terdapat dalam kolom serta untuk
mengukur jumlah komponen yang ada dalam analit (Mulja dan Suharman, 1995).
2. Kromatografi partisi
Pada kromatografi partisi, fase diam dapat polar atau nonpolar. Bila fase
diam polar dan fase gerak nonpolar disebut kromatografi partisi fase normal,
sedangkan bila fase diam nonpolar dan fase gerak polar dinamakan kromatografi
fase terbalik (Munson, 1984).
Prinsip kromatografi partisi didasarkan pada partisi solut di antara dua
masing-masing senyawa. Jika solut ditambahkan ke dalam sistem yang terdiri dari
dua pelarut tidak saling campur dan keseluruhan sistem dibiarkan setimbang,
maka solut akan tersebar di antara kedua faseberdasarkan persamaan:
Dimana K adalah koefisien distribusi, Cs adalah konsentrasi solut dalam fase
diam, dan Cm adalah konsentrasi solut dalam fase gerak (Jhonson dan Stevenson,
1978).
KCKT partisi fase terbalik biasanya mengandung bagian organik yang
terikat secara kimia dengan gugus silanol pada permukaan silika. Bagian organik
tersebut umumnya merupakan hidrokarbon rantai panjang sehingga fase gerak
yang digunakan umumnya bersifat polar. Gugus silanol permukaan dapat
direakasikan dengan berbagai cara untuk menempelkan berbagai jenis gugus
organik. Kemasan fase terikat dengan tipe ikatan siloksan dibuat dengan
mereaksikan organoklorosiloksan dengan gugus silanol pada permukaan silika gel
yang terhidrolisis seperti tampak pada reaksi berikut:
Si OH + Cl Si(CH3)2R Si O Si(CH3)2R + HCl
Gambar 8. Reaksi silanisasi (Harris, 1999)
3. Waktu retensi dan pemisahan puncak dalam kromatografi
Waktu retensi (t
R) atau waktu tambat (retention time) adalah selang
waktu yang diperlukan oleh analit mulai saat injeksi sampai keluar dari kolom dan
berdasarkan waktu di mana sampel diinjeksikan sampai sampel menunjukkan
ketinggian puncak yang maksimum dari senyawa itu. Senyawa-senyawa yang
berbeda memiliki waktu retensi yang berbeda. Untuk beberapa senyawa, waktu
retensi akan sangat bervariasi dan bergantung pada tekanan yang digunakan
(karena itu akan berpengaruh pada laju alir dari pelarut), kondisi dari fase diam
(tidak hanya terbuat dari material apa, tetapi juga pada ukuran partikel),
komposisi yang tepat dari pelarut, dan temperatur pada kolom. Hal ini berarti
bahwa kondisi harus dikontrol secara hati-hati jika menggunakan waktu retensi
sebagai saran untuk mengidentifikasi senyawa-senyawa (Ahuja dan Dong, 2005).
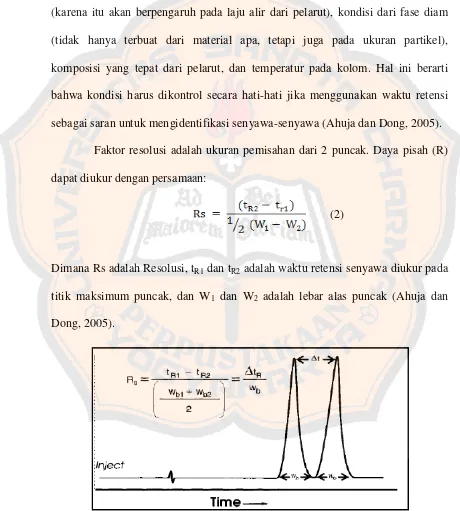
Faktor resolusi adalah ukuran pemisahan dari 2 puncak. Daya pisah (R)
dapat diukur dengan persamaan:
Dimana Rs adalah Resolusi, tR1 dan tR2 adalah waktu retensi senyawa diukur pada
titik maksimum puncak, dan W1 dan W2 adalah lebar alas puncak (Ahuja dan
Dong, 2005).
Gambar 9. Kromatogram hasil pemisahan dua senyawa secara KCKT (Ahuja dan Dong, 2005)
Nilai Rs sebesar 1,5 menunjukkan bahwa baseline resolution tercapai dengan pemisahan dari dua puncak dengan ukuran yang sama sehingga diperoleh
perhitungan yang dapat dipercaya. Dalam penelitian, nilai Rs sebesar 1
menunjukkan pemisahan yang sudah memadai (Ahuja dan Dong, 2005).
4. Analisis kualitatif dan kuantitatif
Analisis kualitatif dilakukan dengan cara membandingkan waktu retensi
senyawa murni dengan waktu retensi senyawa yang dimaksud dalam sampel
(Gritter dkk., 1985). Setiap senyawa memiliki waktu retensi yang spesifik pada
kondisi tertentu seperti kolom, suhu, laju dan sebagainya sehingga dapat
digunakan sebagai salah satu dasar uji kualitatif (Noegrohati, 1994).
Analisis kuantitatif dapat dilakukan dengan dua cara yakni dengan
perbandingan tinggi senyawa sampel terhadap senyawa standar dan perbandingan
luas puncak kromatogram senyawa sampel terhadap senyawa standar. Tinggi
puncak diperoleh dengan membuat garis antara kedua dasar sisi puncak dan
mengukur jarak tegak lurus dari garis ini sampai puncak kromatogram. Bila
variasi keadaan kolom tidak menyebabkan pelebaran puncak, maka analisis
berdasarkan tinggi puncak dapat memberikan ketelitian tinggi. Sedangkan analisis
berdasarkan luas puncak tidak dipengaruhi oleh pelebaran puncak. Oleh karena itu
cara ini lebih disukai dalam perhitungan kuantitatif daripada dengan menghitung
H. Landasan Teori
Simplisia yang banyak digunakan dalam OT yang beredar di Indonesia
adalah Kunyit (Curcumae domesticae). Kunyit memiliki senyawa yang bertanggung jawab terhadap respons biologis berupa zat warna yaitu
kurkuminoid. Kurkuminoid di antaranya merupakan campuran kurkumin,
demetoksikurkumin, dan bis-demetoksikurkumin. Dari ketiga senyawa kurkuminoid tersebut, kurkumin merupakan komponen terbesar sehingga sering
kadar total kurkuminoid dihitung sebagai % kurkumin. Kurkumin memiliki sifat
fotosensitif sehingga stabilitasnya sangat dipengaruhi oleh adanya cahaya. Selain
itu, stabilitas kurkumin juga sangat dipengaruhi oleh pH lingkungan. Kurkumin
stabil pada pH asam sehingga pH diatur pada pH 4.
Kiranti® merupakan salah satu produk OHT yang diproduksi oleh PT Ultra
Prima Abadi (Orang Tua Group). Klaim khasiat dari Kiranti adalah untuk
mengatasi gangguan nyeri haid dan gangguan keputihan. Dalam satu botol Kiranti
kemasan 150 ml mengandung Curcumae domesticae Rhizoma (30g), Tamarindi
Pulpa (6g), Kaempferiae Rhizoma (3g), Arengae pinnata Fructose (3g), Zingiberis
Rhizoma (0,8g), Paulliniacupana (0,23g), Cinnamomi Cortex (0,1g), Air (sampai dengan 150ml).
Sebagai salah satu produk OHT, Kiranti® harus memenuhi syarat
keamanan dan khasiat yang dibuktikan secara ilmiah serta bahan bakunya telah
distandarisasi. Untuk menjamin keseragaman khasiat yang dihasilkan oleh setiap
produk Kiranti®, maka kesamaan kadar dan kesesuaian kadar kurkumin harus
Adanya gugus kromofor dan auksokrom serta gugus polar dan non-polar
pada kurkumin memungkinkan untuk melakukan analisis kuantitatif dengan
menggunakan metode KCKT sistem fase terbalik dengan kolom oktadesilsilan
(C18) menggunakan detektor Ultraviolet-Visible (UV-VIS). Pada penelitian ini,
sistem KCKT yang digunakan adalah sistem KCKT fase terbalik, dengan kolom
oktadesilsilan dan fase gerak campuran metanol p.a dan asam asetat glasial p.a
2%. Metode yang digunakan sebelumnya telah dilakukan optimasi metode dan
validasi metode.
I. Hipotesis
1. Kadar kurkumin dalam sampel sediaan cair OHT Merk Kiranti® yang
ditetapkan dengan metode KCKT fase terbalik sesuai dengan kadar yang
tertera pada label kemasan.
28
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan bersifat non eksperimental deskriptif karena
tidak terdapat manipulasi dan perlakuan terhadap subjek uji.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas pada penelitian ini adalah nomor batch sampel sediaan cair OHT merk Kiranti®.
2. Variabel tergantung
Variabel tergantung pada penelitian ini adalah kadar kurkumin dalam
sampel sediaan cair OHT merk Kiranti® dan reprodusibilitas kadar kurkumin
dalam tiga nomor batch sampel sediaan cair OHT merk Kiranti®.
3. Variabel pengacau terkendali
Variabel pengacau terkendali pada penelitian ini adalah tempat
pengambilan sampel sediaan cair OHT merk Kiranti®.
C. Definisi Operasional
1. Sistem KCKT fase terbalik yang digunakan terdiri atas fase diam berupa
asam asetat glasial p.a 2 % dengan perbandingan komposisi optimum hasil optimasi.
2. Sediaan cair OHT yang digunakan adalah sediaan cair OHT merk Kiranti®
yang mengandung ekstrak Curcumae domesticae Rhizoma sebesar 30 mg. 3. Kadar kurkumin dinyatakan dalam satuan miligram per mililiter (mg/ml)
D. Bahan-bahan Penelitian
Bahan yang digunakan dalam penelitian adalah kurkumin baku hasil
sintesis pemberian Prof. Sudibyo Martono yang telah dikonfirmasi strukturnya
dengan metode spektroskopi 1H-NMR dan Mass Spectra dengan titik lebur 181,2-182,40C, metanol p.a (E. Merck), asam asetat glasial p.a (E. Merck), aquabidestilata for HPLC dan sediaan cair obat herbal terstandar (OHT) merk Kiranti® yang mengandung kurkumin.
E. Alat-alat Penelitian
Alat yang digunakan adalah organic solvent membrane filter (Whatman)
ukuran pori 0,45μm; diameter 47mm, indikator pH, penyaring millipore,
mikropipet, neraca kasar, neraca analitik (Ohaus PAJ 1003), ultrasonicator
(Retsch tipe T460 no V935922013 Ey), Mixer (merk Philips HR 1568),
seperangkat alat KCKT fase terbalik merk Shimadzu dengan sistem gradien
(Shimadzu LC-2010C HT Serial No. C21254706757LP, CAT No. 228-46703-38),
kolom C-18 merek KNAVER C-18 (No. 25EE181KSJ (B115Y620), dimensi 250
RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet D2566 HP-024-000 625 730), seperangkat alat spektrofotometri UV-VIS merk Milton Ray Spectronic
3000 Array yang dihubungkan dengan printer merk Epson LQ-1170, dan alat-alat
gelas yang umum digunakan dalam analisis.
F. Tata Cara Penelitian 1. Pembuatan fase gerak KCKT
Campuran fase gerak yang digunakan dalam penelitian ini adalah
metanol p.a dan asam asetat glasial p.a. 2%. Keduanya masing-masing disaring menggunakan kertas saring Whatman dengan bantuan alat vacuum dan diawaudarakan dengan menggunakan ultrasonikator selama 15 menit.
2. Pembuatan pelarut metanol pH 4
Pelarut yang digunakan berupa metanol yang diatur pada pH 4.
Pengaturan pH dilakukan dengan menambahkan asam asetat glasial 2% sebanyak
1 bagian ke dalam 9 bagian metanol.
3. Pembuatan larutan baku kurkumin
a.Pembuatan Larutan stok.
b.
Timbang seksama lebih kurang 10 mg serbuk
kurkumin kemudian dilarutkan dengan metanol p.a pH 4 dalam labu takar 10,0 ml hingga tanda.
Larutan intermediet. Ambil 1 ml larutan induk baku kurkumin,
c.Larutan seri baku. Buat konsentrasi seri larutan baku kurkumin 1,5;
2,0; 2,5; 3,0; 3,5; 4,0; dan 4,5 ppm dengan mengambil 150; 200; 250; 300; 350;
400; dan 450 µl larutan intermediet, masukkan dalam labu takar 10,0 ml
tambahkan metanol p.a pH 4 hingga tanda. Larutan disaring dengan millipore dan diawaudarakan dengan menggunakan ultrasonikator selama 15 menit.
4. Penentuan panjang gelombang (λ) maksimum kurkumin
Sebanyak 40; 100 dan 160 µl larutan intermediet kurkumin diencerkan
dengan metanol p.a pH 4 dalam labu takar 10,0 ml sampai tanda sehingga
diperoleh konsentrasi 0,4; 1,0 dan 1,6 ppm. Dari kadar baku kurkumin tersebut
dilakukan pengukuran absorbansi pada rentang panjang gelombang 300-500 nm
menggunakan spektrofotometer UV-Vis. Kemudian dari spektrum yang
dihasilkan tersebut ditentukan panjang gelombang maksimumnya. Nilai panjang
gelombang maksimum yang diperoleh selanjutnya digunakan sebagai panjang
gelombang deteksi pada sistem KCKT.
5. Pembuatan kurva baku kurkumin
Sebanyak 20 µl larutan kurkumin konsentrasi 1,5; 2,0; 2,5; 3,0; 3,5; 4,0;
dan 4,5 ppm (larutan baku) yang telah disaring dengan millipore dan diawaudarakan dengan menggunakan ultrasonikator selama 15 menit diinjeksikan
pada sistem KCKT fase terbalik dengan kolom oktadesilsilan (C18) dan fase gerak
metanol : asam asetat glasial 2% (90:10 v/v), kecepatan alir 0,5 ml/menit.
6. Pemilihan sampel
Sampel yang dipilih adalah sediaan cair obat herbal terstandar (OHT)
merk Kiranti® yang berasal dari suatu distributor di Yogyakarta dan
mencantumkan komposisi kurkumin di dalamnya. Sampel yang diambil terdiri
dari 3 batch yang berbeda dan tiap batch diambil sampel sebanyak 10 botol serta dilakukan replikasi pengukuran 5 kali.
7. Optimasi waktu ekstraksi kurkumin dari sediaan
Ambil 1,0 ml sampel Kiranti® dan dimasukkan ke dalam 4 buah labu
takar 10,0 ml ditambahkan metanol p.a pH 4 hingga tanda dan diekstraksi dengan menggunakan ultrasonikator selama 5, 10, 15 dan 20 menit. Sampel kemudian
disaring dengan kertas saring, filtrat dimasukkan dalam labu takar 10,0 ml dan
ditambahkan metanol p.a hingga tanda. Ambil 1,0 ml filtrat, encerkan dengan metanol p.a hingga tanda dalam labu takar 10,0 ml. Injeksikan masing-masing 20,0 μl pada sistem KCKT fase terbalik dengan kolom oktadesilsilan (C18) dan
fase gerak metanol : asam asetat glasial 2% (90:10 v/v), kecepatan alir 0,5
ml/menit.
8. Preparasi sampel
Campur homogen 10 botol Kiranti® menggunakan mixer dengan skala
kecepatan 1. Ambil 1,0 ml sampel homogen dan dimasukkan ke dalam labu takar
kertas saring, filtrat dimasukkan dalam labu takar 10,0 ml dan ditambahkan
metanol p.a hingga tanda. Ambil 3,0 ml (batch 1), 1,5 ml (batch 2), 3,0 ml (batch 3) filtrat, encerkan dengan metanol p.a hingga tanda dalam labu takar 10,0 ml (Larutan A).
9. Penetapan kadar kurkumin dalam sampel
Sebanyak masing-masing 20,0 μl larutan A hasil preparasi sampel
diinjeksikan pada sistem KCKT fase terbalik dengan kolom oktadesilsilan (C18)
dan fase gerak metanol : asam asetat glasial 2% (90:10 v/v), kecepatan alir 0,5
ml/menit. Penetapan kadar dilakukan dengan 5 kali replikasi dari tiga batch
berbeda.
G. Analisis Hasil
Kadar kurkumin dalam sampel dihitung dengan menggunakan persamaan
kurva kaliberasi yang telah dibuat dan dikalikan dengan faktor pengenceran. Hasil
penetapan kadar kurkumin dalam sediaan cair OHT dikatakan memenuhi
persyaratan ketelitian yang baik jika KV < 4% untuk kadar analit dalam sampel
1% (AOAC, 2002). Selanjutnya dilakukan analisis statistik untuk hasil kadar antar
batch yang meliputi:
1. Uji parametrik Shapiro – Wilk
Uji ini digunakan untuk melihat apakah distribusi data yang didapat
2. Independent sample One Way Anova dengan taraf kepercayaan 95%
Dilakukan analisis statistik Independent sample One Way Anova dengan taraf kepercayaan 95% untuk melihat apakah ada perbedaan kadar kurumin yang
35
BAB IV
HASIL DAN PEMBAHASAN
A. Pemilihan Sampel
Penelitian ini menggunakan sampel sediaan cair obat herbal terstandar
merk Kiranti® yang berasal dari salah satu distributor yang berada di Daerah
Istimewa Yogyakarta. Sampel yang dipilih berasal dari tiga nomor batch yang berbeda dan mengandung Curcuma domestica Rhizoma (Rimpang Kunyit) sebagai komposisi utamanya (30g). Rimpang kunyit mengandung senyawa aktif
kurkumin yang memiliki khasiat sebagai anti inflamasi, untuk mengobati perut
kembung, penyakit kuning, melancarkan haid, hematuria, perdarahan, dan kolik
(Thorne Research, 2002).
Sampel diambil dari satu distributor yang sama dengan tujuan untuk
mengkontrol kondisi penyimpanan sampel mulai dari setelah sampel selesai
diproduksi sampai pada sampel siap untuk dianalisis. Hal ini dilakukan karena
stabilitas kurkumin sangat dipengaruhi oleh suhu, kondisi pH dan paparan cahaya.
Ketiga batch sampel diasumsikan akan mengalami perlakuan yang sama dengan diambilnya sampel dari satu distributor yang sama sehingga akan meminimalisir
bias yang terjadi.
Pengambilan sampel dilakukan pada tiga nomor batch yang berbeda untuk melihat reprodusibilitas kadar antar batch sediaan Kiranti®. Jika kadar antar
batch yang diperoleh reprodusibel maka dapat dipastikan bahwa dari keseluruhan
sediaan. Keseragaman kadar ini perlu dijamin terkait dengan efek yang didapatkan
dari sediaan yang dibuat. Jika keseragaman kadar terjamin maka keseragaman
efek juga akan terjamin atau dengan kata lain dari keseluruhan sediaan yang ada
akan memberikan efek yang sama sehingga keamanan dan mutu sediaan pun akan
lebih terjamin.
Pengambilan sampel dilakukan dengan teknik probability/random
sampling dan secara khusus dengan teknik simple random sampling. Teknik ini
akan memberikan kesempatan yang sama setiap pada unit populasi untuk
dijadikan sampel kerena sampel diambil secara random sehingga kemungkinan
terjadinya bias dapat diminimalisir (Nasution, 2003).
Menurut Sugiono (2008) ukuran sampel yang layak untuk penelitian
adalah antara 30 sampai dengan 500. Dari ketiga batch yang digunakan diambil masing-masing 10 botol sampel, sehingga total sampel yang digunakan berjumlah
30 botol sampel. Pada kesepuluh botol sampel dari masing-masing batch dihitung
volume rata-ratanya dan dihomogenkan. Replikasi pengukuran sebanyak lima kali
dilakukan pada kesepuluh sampel homogen.
Tabel I. Keseragaman Volume Kiranti®
Batch Volume masing-masing botol (ml) Keterangan
1 145
Penyimpangan 5% = 145,5 ± 7,275
2 148
Volume rata-rata = 146,9 ml SD = 1,1972
CV = 0,8150%
Penyimpangan 5% = 146,9 ± 7,345
3 146
Berdasarkan hasil uji keseragaman volume didapatkan volume rata-rata
Kiranti® pada masing-masing batch berturut-turut adalah 145,5 ml, 146,9 ml dan 146,8 ml (Tabel I). Ketiga batch memenuhi syarat keseragaman volume sediaan cair. Hal ini ditunjukkan dengan tidak ada satupun volume masing-masing botol
yang menyimpang 5% dari volume rata-rata. Sediaan cair obat dalam dikatakan
memenuhi syarat keseragaman volume apabila perbedaan volume cairan setiap
wadah takaran tunggal terhadap volume rata-rata tidak lebih dari 5%
(Kementerian Kesehatan Republik Indonesia, 1994). Selain itu, jika dilihat dari
nilai CV pada ketiga batch seluruhnya memiliki nilai CV kurang dari 2%. Hal ini menunjukkan bahwa sediaan cair Kiranti® memiliki keseragaman volume yang
baik.
B. Pembuatan Fase Gerak
Sistem KCKT yang digunakan dalam penelitian ini adalah sistem KCKT
fase terbalik dimana fase gerak yang digunakan lebih polar daripada fase
diamnya. Fase gerak yang digunakan dalam penelitian ini adalah campuran
metanol p.a. dan asam asetat glasial p.a. 2% dengan perbandingan 90:10 (v/v) (Krisnayanti, 2011). Kedua komposisi fase gerak ini dipilih karena keduanya
dapat melarutkan kurkumin dengan baik sehingga diharapkan kurkumin dapat
terelusi dengan baik.
Campuran metanol p.a. dan asam asetat glasial p.a. 2% (90:10 v/v) ini memiliki nilai pH 4 sehingga tidak akan merusak kolom oktadesilsilan (C18) pada
menjadi bentuk silanol pada pH ≤ 2 karena adanya reaksi antara C18 dengan asam.
Berikut ini adalah contoh reaksi degradasi kolom oktadesilsilan (C18) karena
adanya asam kuat HCl:
Si O Si (CH2)17CH3 Si OH + Cl Si (CH2)17CH3 H2O/HCl
Gambar 10. Reaksi degradasi kolom C18 oleh HCl (pH ≤ 2) (Skoog dkk., 1985).
C. Pembuatan Pelarut
Pelarut yang digunakan dalam penelitian ini adalah metanol p.a. yang telah diatur pHnya menjadi pH 4. Pengaturan dilakukan dengan penambahan
asam asetat glasial p.a. 2% pada metanol p.a. dengan perbandingan metanol : asam asetat glasial 2% (9:1 v/v). Pengaturan ini dilakukan untuk menjaga
stabilitas kurkumin. Berdasarkan hasil orientasi pengujian stabilitas kurkumin,
kurkumin stabil pada pH 4 (lampiran 3). Stabilitas kurkumin sangat dipengaruhi
oleh pH dan cahaya. Kurkumin akan terdegradasi pada pH di atas 7 menjadi asam
ferulat dan feruloil metan (Stankovic, 2004).
D. Penentuan Panjang Gelombang Maksimum
Penentuan panjang gelombang maksimum dilakukan untuk mengetahui
pada panjang gelombang berapa kurkumin akan memberikan serapan maksimum.
Penentuan panjang gelombang dilakukan dengan menggunakan spektrofotometer
visibel karena kurkumin akan memberikan serapan warna pada daerah panjang
Syarat suatu senyawa dapat diukur serapannya pada panjang gelombang
visibel adalah senyawa tersebut harus memiliki gugus kromofor dan auksokrom
yang bertanggung jawab atas terjadinya serapan radiasi sinar. Kurkumin memiliki
gugus kromofor dan auksokrom pada struktur senyawanya sehingga kurkumin
dapat memberikan serapan warna pada daerah panjang gelombang visibel. Gugus
kromofor dan auksokrom pada kurkumin dapat dilihat pada gambar berikut:
O O
H3CO
HO
OCH3
OH
Gambar 11. Gugus kromofor dan auksokrom pada struktur kurkumin
Keterangan : kromofor auksokrom
Penentuan panjang gelombang maksimum dilakukan pada tiga
konsentrasi larutan kurkumin yang berbeda, yakni yakni 0,4; 1,0; dan 1,6 ppm.
Pembacaan dilakukan pada rentang panjang gelombang 300-500 nm. Rentang
panjang gelombang ini ditentukan berdasarkan panjang gelombang teoritis
Spektra hasil penentuan panjang gelombang maksimum dengan
menggunakan tiga konsentrasi yang berbeda adalah sebagai berikut:
Gambar 12. Spektra panjang gelombang maksimum kurkumin pada pelarut metanol
Keterangan: A : konsentrasi rendah (0,4 ppm) B : konsentrasi sedang (1,0 ppm) C : konsentrasi tinggi (1,6 ppm)
Dari hasil penentuan panjang gelombang maksimum kurkumin dalam
pelarut metanol didapatkan hasil bahwa panjang gelombang maksimum kurkumin
pada konsentrasi 0,4; 1,0; dan 1,6 ppm berturut-turut adalah 432; 433; dan 432
nm. Oleh karena itu, dapat ditetapkan panjang gelombang maksimum kurkumin
yang digunakan dalam penelitian ini adalah 432 nm. Menurut Direktorat Jenderal
Pengawasan Obat dan Makanan (1979), panjang gelombang maksimum hasil
pengukuran dapat digunakan apabila penyimpangannya ± 2 nm dari panjang
gelombang teoritis.
E. Analisis Kualitatif Berdasarkan Waktu Retensi (tR) Kurkumin
Analisis kualitatif dalam penelitian ini dilakukan dengan
membandingkan waktu retensi sampel Kiranti® dengan waktu retensi baku
kurkumin. Analisis kualitatif ini dilakukan untuk membuktikan bahwa di dalam
sampel Kiranti® yang diuji terdapat kurkumin. Hal ini ditujukkan oleh adanya
kemiripan waktu retensi (tR) peak yang didapatkan pada pemisahan sampel
dengan peak hasil elusi baku kurkumin.
Gambar 13. Kromatogram kurkumin baku (A) dan Kromatogram Kurkumin dalam sampel Kiranti® (B)
Jika dilihat dari kromatogram yang dihasilkan, antara kurkumin sampel
dengan kurkumin baku memiliki waktu retensi yang tidak jauh berbeda. Waktu
retensi baku kurkumin adalah 6,055 menit sedangkan waktu retensi sampel