MAKALAH UTILITAS MAKALAH UTILITAS BAHAN BAKAR PADAT BAHAN BAKAR PADAT
Kelas B Kelas B Dikerjakan Oleh Dikerjakan Oleh Kelompok 2 Kelompok 2 Hendri
Hendri Yudisai Yudisai 121140004121140004 Ganang
Ganang Pamungkas Pamungkas 121140033121140033 Siti
Siti Nuzul Nuzul Isrizkyah Isrizkyah 121140040121140040
UTILITAS UTILITAS
PROGRAM STUDI TEKNIK KIMIA PROGRAM STUDI TEKNIK KIMIA
FAKULTAS TEKNIK INDUSTRI FAKULTAS TEKNIK INDUSTRI UNIVERSITAS PEMBANGUNAN
UNIVERSITAS PEMBANGUNAN NASIOAN “VETERAN” NASIOAN “VETERAN” YOGYAKARTA
YOGYAKARTA 2017
Bahan Bakar Padat
Bahan bakar adalah suatu materi apapun yang bisa diubah menjadi energi. Biasanya bahan bakar mengandung energi panas yang dapat dilepaskan dan dimanipulasi. Kebanyakan bahan bakar digunakan manusia melalui proses pembakaran (reaksi redoks) di mana bahan bakar tersebut akan melepaskan panas setelah direaksikan dengan oksigen di udara. Proses lain untuk melepaskan energi dari bahan bakar adalah melalui reaksi eksotermal dan reaksi nuklir (seperti Fisi nuklir atau Fusi nuklir).
Berdasarkan bentuknya, bahan bakar terbagi menjadi tiga : 1. Bahan bakar cair
2. Bahan Bakar Padat 3. Bahan bakar gas.
Bahan bakar padat merupakan bahan bakar berbentuk padat, dan kebanyakan menjadi sumber energi panas. Misalnya kayu dan batubara. Energi panas yang dihasilkan bisa digunakan untuk memanaskan air menjadi uap untuk menggerakkan peralatan dan menyediakan energi. Bahan balar berbentuk padat sudah digunakan sejak lama untuk kebutuhan sehari-hari dan industri karena harganya yang relatif lebih murah dibandingkan dengan bahan bakar jenis lain.
Bahan bakar padat yang digunakan umumnya batubara, meskipun ada beberapa industri menggunakan kayu seperti genting. Industri kelapa sawit menggunakan tempurung kelapa. Bahan bakar padat umumnya terjadi karena proses alami selama berjuta-juta tahun yang lalu dan umumnya mengandung C, H, O, N, S, P dan yang pokok C, H, O, S.
Dibawah ini merupakan contoh dari bahan bakar padat. Diantaranya adalah :
1. Kayu dan sisa tumbuhan: kadar abu rendah, kadar air relatif tinggi (tergantung pada spesies dan umur pohon, iklim, kondisi penyimpanan).
Kandungan air = W
Nilai kalor (rumus pendekatan): QL = (4400 - 50W)
Termasuk sisa tanaman: batang tebu, kulit buah, sekam, jerami, dll.
2. “Peat”, bahan yang terbentuk dari dekomposisi dan disintegrasi tanaman graminae (seperti tebu, bambu, alang-alang) oleh tekanan air di dalam rawa. Kandungan abunya
tergantung pada lumpur rawa. Bahan bersifat higroskopis. Kandungan airnya tergantung pada kondisi pengeringan, transportasi dan penyimpanan. Nilai kalor bawahnya 1700-3000 kkal/kg.
3. Batubara (= Bahan Bakar Fosil)
Berdasarkan asal dan umur geologisnya, digolongkan sebagai berikut:
-
lignite,-
bituminous coal,-
anthracite.3.1. Lignite: terbentuk dari tumbuh-tumbuhan yang mengalami karbonisasi atau perkayaan akan kandungan C di bawah lapisan tanah dalam jangka waktu yang
lama.
Berdasarkan umur geologisnya digolongkan atas:
-
pitch lignite: lebih muda daripada lignite,-
lignite.Kadar N, O, VCM, S dan air tinggi. Lignite bersifat higroskopis, nilai kalor bawah
sekitar 1500-4500 kkal/kg.
3.2. Bituminous coal: terbentuk pada periode geologi “carboniferous” dari tumbuh-tumbuhan yang mengalami karbonisasi. Nilai kalor 7000-8000 kkal/kg. Kandungan abu dan airnya rendah (5-10%). Kalau kandungan abunya tinggi, biasanya dipakai pada “steam power plant”. Batubara yang berwarna hitam tidak bersifat higroskopis.
3.3. Anthracite: batubara yang terjadi pada umur geologi yang paling tua. Struktur kompak, berat jenis tinggi, berwarna hitam metalik, kandungan VCM rendah, kandungan abu dan air rendah, mudah ditepung. Kalau dibakar, hampir seluruhnya habis terbakar tanpa timbul nyala. Nilai kalor atas ³ 8300 kkal/kg. Semi-anthracite mempunyai sifat antara bituminous coal dan anthracite.
3.4. Shale, adalah hasil penguraian tumbuh-tumbuhan dan binatang mikroorganisme di dasar rawa atau danau membentuk bahan seperti lumpur yang disebut “sapropel”. Sapropel yang bercampur dengan sedimen mineral membentuk massa yang kompak yang disebut “combustible shale”.
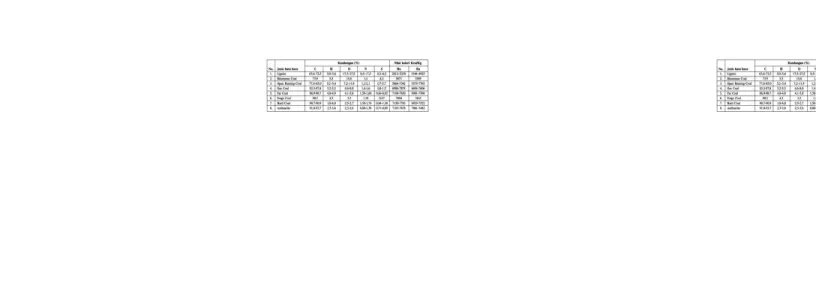
Tabel Klasifikasi dan kandungan dalam batu bara
4. Uranium
Uranium merupakan bahan bakar nuklir utama. Sama seperti batu bara, uranium didapatkan melalui penambangan karena keberadaannya yang terdapat di dalam tanah. Untuk mendapatkan energi dari uranium, tidak terlepas dari pembakaran. Namun, harus melalui pemisahan atom. Pemisahan tersebut harus disertai dengan
energi yang tinggi berupa energi panas.
Energi panas yang dihasilkan antara lain dapat digunakan untuk memanaskan air sehingga akan terbentuk uap. Di PLTN uap tersebut dimanfaatkan sebagai penggerak turbin yang akan menggerakan generator listrik. Pada pemisahan atom dalam uranium ini, neutron-neutron dilepaskan dan disertai dengan energi tinggi. Neutron ini akan membentuk sinar radioaktif.
Kelebihan dan kekurangan dari bahan bakar pada adalah
Kelebihan :
1. Murah
2. Energi atau panas yang dihasilkan besar 3. Distribusi lebih mudah
4. Tidak menimbulkan green house effect pada uranium
Kekurangan :
1. Menimbulkan polusi lebih besar
2. Memerlukan kontrol lebih besar untuk tidak terjadi kecelakaan produksi
Cara Produksi bahan bakar padat 1. Destilasi Kerin / Pirolisis
Distilasi kering yaitu satu metoda pembelahan beberapa zat kimia. Dalam sistem distilasi kering, bahan padat dipanaskan hingga membuahkan beberapa produk berbentuk cairan atau gas (yang bisa berkondensasi jadi padatan). Beberapa produk
itu disaring, dan ketika yang berbarengan mereka berkondensasi dan dihimpun. Distilasi kering umumnya memerlukan suhu yang lebih tinggi di banding distilasi umum. Cara ini bisa dipakai untuk peroleh bahan bakar cair dari batubara dan kayu. 2. Pembakaran langsung dengan udara
roses pembakaran batubara yang umumnya terjadi di dalam boiler pada pembangkit listrik tenaga uap, dan merupakan reaksi kimia yang dilakukan dengan menambah oksigen O2 dari udara pembakaran dengan reaksi kimia sebagai berikut.
Proses pembakaran batubara yang umumnya terjadi di dalam boiler pada pembangkit listrik tenaga uap, dan merupakan reaksi kimia yang dilakukan dengan menambah oksigen O2 dari udara pembakaran dengan reaksi kimia sebagai berikut.
C + O2 – > CO2+ energi panas
Karena di dalam batubara terdapat ikatan-ikatan kimia antara karbon, hidrogen, oksigen, nitrogen, dan sulfur maka pada proses pembakaran batubara juga akan timbul reaksi kimia antara ikatan-ikatan kimia tersebut dengan oksigen yang terdapat di udara yang ditunjukkan pada reaksi kimia beikut.
2H2 + O2 – >2H2O N2 + O2 – > NOX
Kegunaan bahan bakar padat di industri
Secara umum, bahan bakar berbentuk padat digunakan untuk memanaskan air untuk mendapatkan uap air yang kemudian akan digunakan pada proses selanjutnya. Maka, bahan bakar padat dapat diaplikasikan pada alat boiler dan sebagai salah satu sumber pembangkit
listrik dalam suatu industri. 1. Solid Fuel Boiler
Type boiler ini menggunakan bahan bakar padat seperti kayu, batu bara, dengan karakteristik seperti harga bahan bakar relatif lebih murah dan lebih efesiensi bila dibandingkan dengan boiler listrik.
Prinsip Kerja: Pemanasan bersumber dari pembakaran bahan bakar padat atau bisa juga campuran dari beberapa bahan bakar padat (batu bara dan kayu) yang dibantu
dengan oksigen.
Kelebihan: Bahan bakar mudah untuk didapatkan dan lebih murah. Kekurangan: Sisa pembakaran sulit untuk dibersihkan,.
Untuk menghasilkan energi listrik pada PLTU Batubara, awalnya batu bara yang ditampung dalam bak penampungan dibawa ke dalam mesin pencacah batubara melalui conveyor belt untuk dipecah menjadi ukuran yang lebih kecil/ halus, agar batubara lebih mudah terbakar pada saat di dalam boiler. Batubara yang telah halus
tadi dibawa ke dalam boiler untuk digunakan sebagai bahan bakar pada proses pembakaran.
Kembali lagi pada proses pembakaran, pada boiler ini terjadi proses pemanasan air yang sebelumnya telah dimurnikan agar tidak mudah menimbulkan korosi (untuk air laut), air tersebut melalui pipa-pipa boiler dan dipanaskan sehingga akan berubah menjadi uap panas yang bertekanan tinggi. Tetapi karena kadar air pada uap masih terlalu tinggi, maka kadar air harus dihilangkan terlebih dahulu melalui superheater sehingga akan berubah menjadi uap kering. Kemudian uap kering ini dialirkan menuju ke turbin untuk mendorong sudu-sudu turbin sehingga poros turbin akan berputar. Poros turbin terhubung langsung dengan generator sehingga ketika turbin berputar maka generator juga akan ikut berputar dan menghasilkan energi listrik yang akan dikirimkan ke trafo untuk dirubah tegangannya dan kemudian disalurkan melalui saluran transmisi PLN