BAB I
BAB I
PENDAHULUAN
PENDAHULUAN
1.1
1.1Latar BelakangLatar Belakang
Peridustrian skala kecil atau biasa disebut industri rumah tangga masih mendominasi kegiatan perekonomian yang ada di Indonesia.Industri tersebut berkembang sejalan dengan pemikiran masyarakat untuk berwirausaha.Upaya tersebut cukup bagus untuk meningkatkan perekonomian masyarakat.Namun,banyak industri skala kecil yang belum memperhatikan upaya pelestarian lingkungan.Salah satunya adalah pembuangan limbah ke lingkungan yang di dalamnya terdapat aktivitas kegiatan masyarakat. Tentunya ini akan berdampak pada lingkungan dan juga manusia.
Salah satunya adalah industri tahu yang banyak bermunculan di lingkungan masyarakat, khususnya di Kota Bandung.Limbah dari industri tersebut banyak yang tidak diolah terlebih dahulu sebelum masuk ke lingkungan.Salah satunya adalah limbah dari salah satu industri tahu di Desa Cihanjuang.
Limbah cair yang dihasilkan oleh rata-rata industri tahu mengandung tingkat keasaman yang cukup tinggi dengan kadar BOD, COD, maupun TSS yang tinggi pula (Fatha, 2007). Akibat dari limbah cair tersebut, dapat menimbulkan pengendapan bahan organik dan menimbulkan proses pembusukan oleh mikroba sehingga dapat
mencemari lingkungan.
Oleh karena itu, diperlukan suatu solusi untuk mengolah limbah cair tersebut.Salah satunya adalah dengan metode koagulasi dan flokulasi untuk
1.2
1.2 TujuanTujuan
Adapun tujuan daripada praktikum ini adalah sebagai berikut:
1. Menentukan dosis optimum koagulan pada limbah cair yang berasal dari industri tahu yang ada di salah satu industri tahu di Desa Cihanjuang.
2. Mengetahui pengaruh penambahan koagulan berupa tawas terhadap limbah cair tahu.
3. Mengetahui pengaruh penambahan flokulan berupa aquaclear terhadap limbah cair tahu.
1.3
1.3ManfaatManfaat
Manfaat dari praktikum ini adalah mengetahui dengan benar cara pengolahan limbah cair tahu dengan metode koagulasi-flokulasi, sehingga dapat menambah pengetahuan mengenai hal tersebut.
1.4
1.4 PelaksanaanPelaksanaan
Praktikum ini dilaksanakan di Laboratorium Pengelolaan Air dan Limbah Industri, Jurusan Teknik Kimia, Politeknik Negeri Bandung (Polban).Adapun waktu pelaksanaannya yaitu pada pukul 07.00-10.40 WIB.
BAB II
BAB II
TINJAUAN PUSTAKA
TINJAUAN PUSTAKA
2.12.1Industri TahuIndustri Tahu
2.1.1
2.1.1 Limbah Industri TahuLimbah Industri Tahu
Proses produksi tahu di industri tahu menghasilkan dua macam limbah yaitu limbah padat dan limbah cair. Limbah padat pada umumnya dimanfaatkan sebagai pakan ternak. Industri tahu membutuhkan air untuk melakukan proses sortasi, perendaman, pengupasan kulit, pencucian, penggilingan, perebusan, dan penyaringan. Kemudian, air buangan dari proses
tersebut yang dinamakan limbah cair (Fatha,2007).
Limbah cair industri tahu memiliki kandungan senyawa organik yang cukup tinggi. Tanpa proses penanganan yang baik, limbah tahu dapat menyebabkan berbagai dampak negatif seperti polusi air, sumber penyakit, bau tak sedap, meningkatkan pertumbuhan nyamuk, dan menurunkan estetika lingkungan. Limbah cair yang dibuang ke perairan tanpa pengelohan terlebih dahulu dapat mengakibatkan kematian makhluk hidup dalam air termasuk mikroorganisme yang berperan penting dalam mengatur keseimbangan biologi maupun kimia dalam air .
2.1.2
2.1.2 Karakteristik Limbah Cair TahuKarakteristik Limbah Cair Tahu
Karakteristik buangan industri tahu meliputi dua hal, yaitu karakteristik fisika dan kimia.Karakteristik fisika meliputi padatan total, padatan tersuspensi, suhu, warna, dan bau.Karakteristik kimia meliputi bahan
organik, bahan anorganik, dan gas.
Suhu air limbah tahu berkisar 37-45°C; kekeruhan 535-585 FTU; warna 2.225-2.250 Pt.Co; amonia 23,3-23,5 mg/l; BOD5 6.000-8.000 mg/l;
Suhu buangan industri tahu berasal dari proses pemasakan kedelai. Suhu limbahcair tahu pada umumnya lebih tinggi dari air bakunya, yaitu 400oC-460oC. Suhu yang meningkat di lingkungan perairan akan mempengaruhi kehidupan biologis, kelarutan oksigen dan gas lain, kerapatan air, viskositas, dan tegangan permukaan. Bahan-bahan organik yang terkandung di dalam buangan industri tahu pada umumnya sangat tinggi.Senyawa-senyawa organik di dalam air buangan tersebut dapat berupa protein, karbohidrat, lemak, dan minyak.Diantara senyawa-senyawa tersebut, protein dan lemak adalah memiliki jumlah paling besar.Protein mencapai 40-60%, karbohidrat 25-50%,dan lemak 10%. Air buangan industri tahu kualitasnya bergantung dari proses yang digunakan. Apabila air prosesnya baik, kandungan bahan organik pada air buangannya biasanya rendah. Komponen terbesar dari limbah cair tahu yaitu protein (Ntotal) sebesar 226,06-434,78 mg/l, sehingga masuknya limbah cair tahu ke lingkungan perairan akan meningkatkan total nitrogen di perairan tersebut (Herlambang,
2002).
2.2
2.2 Metode Koagulasi-FlokulasiMetode Koagulasi-Flokulasi 2.2.1
2.2.1 KoagulasiKoagulasi
Koagulasi merupakan penggumpalan partikel koloid dan dapat membentuk endapan.Dengan terjadinya koagulasi, berarti zat terdispersi tidak lagi membentuk koloid.Koagulasi dapat terjadi secara fisika seperti pemanasan, pendinginan, dan pengadukan. Dapat juga secara kimiawi seperti penambahan senyawa penggumpal dan penambahan elektrolit lain.
Secara umum, proses koagulasi bermanfaat untuk:
1. Mengurangi padatan tersuspensi dalam air limbah yang menyebabkan kekeruhan pada air limbah.
3. Mengurangi zat warna yang terdapat dalam air limbah.
4. Mengurangi bau yang diakibatkan padatan tersuspensi dalam air limbah.
Pada koagulasi dapat dilakukan pengadukan cepat. Tujuannya yaitu untuk menghasilkan turbulensi pada air baku sehingga membentuk sejumlah flok.
Untuk koagulasi dengan secara kimiawi, bahan yang biasa digunakan yaitu:
1. Ferro Sulfat (FeSO4.7H2O)
Ferro sulfat (FeSO4.7H2O) dapat bereaksi dengan cepat jika air limbah
mengandung alkalitas dalam bentuk ion hidroksida. Oleh karena itu, senyawa Ca(OH)2 dan NaOH biasanya ditambahkan untuk meningkatkan
pH sampai titik dimana ion Fe2+ dapat terendapkan sebagai Fe(OH)3. pH
optimum pada koagulan ferro sulfat (FeSO4.7H2O) adalah 7,0 sampai 9,5.
2. Aluminium Sulfat (Al2(SO)3.18H2O)
Kelebihan dari alumunium sulfat (Al2(SO)3.18H2O) adalah harganya
yang murah dan mudah diperoleh. Disamping itu, untuk menyempurnakan proses koagulasi dengan menggunakan alum perlu ditambahkan ion hidroksida (Ca(OH)2) atau ion karbonat (NaCO3) karena akan menambah
alkalitas dimana alkalitas ini akan bereaksi dengan alum, dan nilai pH limbah harus berada pada pH optimum yaitu 4,5 sampai 8,0.
2.2.2
2.2.2 FlokulasiFlokulasi
Flokulasi adalah proses pengadukan lambat agar campuran koagulan dan air baku yang telah merata membentuk gumpalan atau flok dan dapat mengendap.
Tujuan utama flokulasi adalah menyatukan partikel flok sehingga partikel-partikel tersebut saling bertabrakan, kemudian melekat, dan tumbuh
menjadi ukuran yang siap turun untuk mengendap.Adapun jenis flokulan adalah sebagai berikut:
1. Kopolimer dari akrilamida dan N,N−dimetil amino propilen akrilat Kopolimer yang linier dan kationik.Kepadatan muatanelektrostatik tergantung dari status kopolomerisasi (n/m + n) dan pH.
2. Poli (Natriumakrilat)
Kopolimer dengan akril amida dan anionik. 3. Poli akrilamida
2.3
2.3 Jar TestJar Test
Metode jar test mensimulasikan proses koagulasi dan flokulasi untuk menghilangkan padatan tersuspensi ( suspended solid ) dan zat-zat organik yang dapat menyebabkan masalah kekeruhan, bau, dan rasa. Jar test mensimulasikan beberapa tipe pengadukan dan pengendapan yang terjadi di clarification plant pada skala laboratorium. Dalam skala laboratorium, memungkinkan untuk dilakukannya enam tes individual yang dijalankan secara bersamaan. Jar test memiliki variabel kecepatan putar pengaduk yang dapat mengontrol energi yang diperlukan untuk proses.
(Nurhidayah, 2012)
Gambar 1. Gambar 1. Alat Jar Test
2.4
2.4 Faktor-Faktor yang Mempengaruhi Metode Koagulasi-FlokulasiFaktor-Faktor yang Mempengaruhi Metode Koagulasi-Flokulasi Adapun faktor-faktor yang mempengaruhi kinerja kogulasi dan flokulasiadalah sebagai berikut :
1. Kualitas air
Kualitas air ditentukan oleh tingkat kekeruhan, pH, COD (Chemical Oxygen Demand ), BOD ( Biochemical Oxygen Demand ), DO ( Dissolved Oxygen), dan kandungan logam terlarut.
2. Suhu air
Koagulasi lebih cepat terbentuk pada suhu kamar. Pada suhu yang lebih tinggi, koagulasi yang terbentuk akan terlarut kembali karena kelarutan dipengaruhi suhu.
3. Jenis koagulan
Pemilihan jenis koagulan didasarkan pada pertimbangan segi ekonomis dan daya efektivitas daripadakoagulan dalam pembentukan flok.Koagulan dalam bentuk larutan lebih efektif dibandingkan koagulan dalam bentuk serbukatau butiran.
4. pH air
pH suatu larutan menunjukkan aktivitas ion hidrogen dalam larutan tersebut dan dinyatakan sebagai konsentrasi ion hidrogen (dalam mol per liter) pada suhu tertentu. Nilai pH suatu perairan menunjukkan keseimbangan antara asam dan basa dalam air.pH yang baik bagi air minum dan air limbah adalah netral yaitu 7. Untuk proses flokulasi dan koagulasi, limbah cair tergantung logam yang akan diendapkan. Logam diendapkan pada pH tinggi dengan penambahan kapur.Logam yang berbeda, mengendap pada tingkat pH yang berbeda antara 8 sampai 11, sehingga agar pengolahan berlangsung
efektif, perlu dilakukan dalam beberapa tahap.Masing-masing logam dalam satu tahap. Zat bantu penggumpal seperti feriklorida, tawas, dan polielektrolit sering digunakan untuk membantu pemisahan zat padat-cair.
5. Jumlah garam terlarut dalam air
Bermacam-macam garam yang terlarut membutuhkantreatment yang berbeda untuk memisahkan masing-masing garam terlarut tersebut. Oleh karena itu,diperlukan analisis garam terlarut terlebih dahulu untuk mengetahui proses koagulasi yang akan dilakukan.
6. Kecepatan pengadukan
Dengan adanya pengadukan, tumbukan antarpartikel koloid akan semakin besar, mempercepat terbentuknya flokulasi, sehingga memudahkan terjadinya pengendapan.
7. Waktu pengadukan
Semakin lama pengadukan, maka flok yang terbentuk semakin banyak sehingga endapan yang terbentuk semakin banyak.
8. Dosis koagulan
Banyak sedikitnya inti flok yang terbentuk tergantung pada banyak sedikitnya koagulan yang ditambahkan.
BAB III
BAB III
METODOLOGI
METODOLOGI
3.13.1 Alat dan BahanAlat dan Bahan 3.1.1
3.1.1 Alat yang DigunakanAlat yang Digunakan
Ketersediaan alat merupakan komponen utama yang harus diperhatikan dalam praktikum ini. Adapun alat yang digunakan adalah sebagai berikut:
1. Alat jar test(1 buah) 2. Corong Inhoff (1 buah) 3. pH meter (1 buah) 4. Turbidimeter (1 buah)
5. Alat pengukur DHL dan TDS (1 buah) 6. Gelas kimia 100 ml (6 buah) 7. Gelas kimia 1000 ml (6 buah) 8. Gelas ukur 100 ml (1 buah) 9. Gelas ukur 1000 ml (1 buah) 10.Pipet ukur 25 ml (2 buah) 11.Bola isap (1 buah) 12.Botol semprot (1 buah) 13.Pengaduk gelas (1 buah) 14.Ember (1 buah)
15.Gulungan kertas tisu (1 buah) 16.Lap (1 buah)
3.1.2
3.1.2 Bahan yang DigunakanBahan yang Digunakan
Adapun bahan yang digunakan dalam praktikum ini adalah sebagai berikut:
1. Limbah cair tahu* (±10 liter) 2. Tawas 1%
3. Aquaclear ** 4. NaOH 0,5 M
Keterangan:
*) limbah cair tahu untuk praktikum ini diambil dari salah satu industri tahu di Desa Cihanjuang, Kota Cimahi.
**) merupakan merek dagang flokulan.
3.2
3.2 Prosedur KerjaProsedur Kerja 3.2.1
3.2.1 Penetralan Limbah Cair TahuPenetralan Limbah Cair Tahu
Adapun langkah-langkahnya adalah sebagai berikut: 1. Menyiapkan ember berisi limbah cair tahu. 2. Menyiapkan larutan NaOH 0,5 M.
3. Memasukkan sekitar 50 ml larutan NaOH 0,5 M ke dalam ember berisi limbah cair tahu.
4. Mengecek pH limbah dengan pH meter.
5. Jika masih asam, menambahkan kembali larutan NaOH 0,5 M sampai limbah cair tahu mendekati pH netral.
3.2.2
3.2.2 Menentukan Dosis Optimum KoagulanMenentukan Dosis Optimum Koagulan
Adapun langkah-langkahnya adalah sebagai berikut:
1. Mengecek nilai pH, kekeruhan, TDS, dan DHL limbah cair tahu yang sudah netral untuk persiapan melakukan percobaan run ke-1. 2. Menyiapkan 6 buah gelas kimia 1000 ml.
3. Mengisinya dengan limbah cair tahu dan tawas 1% sampai volumenya 700 ml (volume tawas untuk masing-masing gelas kimia yaitu 24, 26, 28, 30, 32, dan 34 ml).
4. Menempatkan 6 gelas kimia berisi limbah dan juga koagulan pada alat jar test.
5. Melakukan pengadukan pada unit jar test dengan kecepatan 100 rpm sampai konstan sekitar 1 menit.
6. Mengurangi putaran rotor sampai 40 rpm dan langsung menambahkan flokulan berupa aquaclear masing-masing 0,5 ml (secara bersamaan) selama 10 menit. Untuk run ke-2 digunakan flokulan sebanyak 1 ml untuk setiap gelas kimia.
7. Setelah 10 menit, memindahkan air limbah dari gelas kimia ke dalam 6 coronginhoff (secara bersamaan).
8. Menunggu coronginhoff yang berisi limbah yang sudah dilakukan proses koagulasi dan flokulasi selama 1 jam.
9. Setelah 1 jam, mengukur tinggi endapan pada corong inhoff. 10.Mengecek sampel limbah pada corong inhoff berupa analisis pH,
kekeruhan, TDS, dan DHL.
11.Membuat grafik hubungan dosis koagulan terhadaptinggi endapan, pH, kekeruhan, TDS, dan DHL.
3.2.3
3.2.3 Flow ChartFlow Chart
Sedimentasi
Corong/kerucut inhoff
endapan
pengukuran
Jar Test
Aquaclear, yang ditambahkan:
-Untuk run 1 = 0,5 ml
-Untuk run 2= = 1 ml
(pada 40 rpm, tambahkan secara bersamaan) Pengadukan Pengadukan cepat ± 100 rpm selama 1 menit Pengadukan lambat ± 40 rpm selama 10 menit Limbah 676 ml + tawas 1% 24 ml Limbah 674 ml + tawas 1% 26 ml Limbah 672 ml + tawas 1% 28 ml Limbah 670 ml + tawas 1% 30 ml Limbah 668 ml + tawas 1% 32 ml Limbah 666 ml + tawas 1% 34 ml DHL Ember Pengadukan Air 10 l Setelah netral, lakukan pengukuran pH Kekeruhan TDS Penambahan NaOH 0,5 M
untuk penetralan limbah cair tahu (sekitar 220 ml)
BAB IV
BAB IV
DATA PENGAMATAN
DATA PENGAMATAN
Data Praktikum Pengolahan Limbah Cair Tahu Data Praktikum Pengolahan Limbah Cair TahuJenis Limbah : Limbah Cair Tahu Jenis Koagulan :Tawas
Kualitas Awal Konsentrasi koagulan :10.000 ppm
pH : 3,95 Kecepatan putaran :100rpm/1menit
Kekeruhan : 124,5NTU Jenis Flokulan : Aquaclear
TDS : 1201 mg/l Konsentrasi Flokulan :0,1 %
DHL : 1,96 ms Kecepatan putaran :40rpm/10menit
Vol. NaOH 0,5 M : 220 ml
pH setelah penambahan NaOH 0,5 M : 6,51
Run 1 (dengan flokulan 0,5 ml) Run 1 (dengan flokulan 0,5 ml)
Volume Volume Koagulan(ml) Koagulan(ml) Dosis Koagulan Dosis Koagulan (mg/l) (mg/l) Kekeruhan Kekeruhan (NTU) (NTU) pHpH Tinggi Endapan Tinggi Endapan (cm) (cm) DHL DHL (ms) (ms) TDS TDS (mg/l)(mg/l) 24 342.8 88.34 5.92 9.5 1.041 608 26 371.4 89.02 5.99 9.7 1.2 809 28 400 92.8 6.1 11.3 1.072 715 30 428.5 91.45 5.92 11.6 1.15 769 32 457.1 88.89 5.93 12 1.027 685 34 485.7 83.83 5.83 12.5 1.202 764
Run 2 (dengan flokulan 1 ml) Run 2 (dengan flokulan 1 ml)
Volume Volume Koagulan(ml) Koagulan(ml) Dosis Koagulan Dosis Koagulan (mg/l) (mg/l) Kekeruhan Kekeruhan (NTU) (NTU) pHpH Tinggi Endapan Tinggi Endapan (cm) (cm) DHL DHL (ms) (ms) TDS TDS (mg/l)(mg/l) 24 342.8 77.21 5.99 9 0.999 661 26 371.4 82.92 5.94 12 1.01 675 28 400 71.55 5.95 13 0.821 550 30 428.5 71.12 5.94 13.1 1.071 735
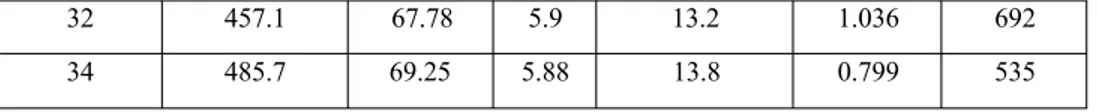
32 457.1 67.78 5.9 13.2 1.036 692 34 485.7 69.25 5.88 13.8 0.799 535
Tabel 1. Data pengamatan pengolahan limbah cair tahu Tabel 1. Data pengamatan pengolahan limbah cair tahu
BAB V
BAB V
PENGOLAHAN DATA
PENGOLAHAN DATA
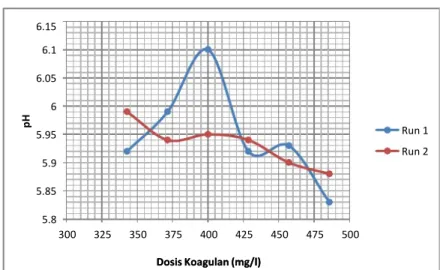
5.15.1Grafik Hubungan Antara Dosis Koagulan dan pHGrafik Hubungan Antara Dosis Koagulan dan pH
Grafik 1. Hubungan Antara Dosis Koagulan dan pH Grafik 1. Hubungan Antara Dosis Koagulan dan pH
5.2
5.2Grafik Hubungan Antara Dosis Koagulan dan KekeruhanGrafik Hubungan Antara Dosis Koagulan dan Kekeruhan
Grafik 2. Hubungan Antara Dosis Koagulan dan Kekeruhan Grafik 2. Hubungan Antara Dosis Koagulan dan Kekeruhan
65 70 75 80 85 90 95 300 325 350 375 400 425 450 475 500 K e k e r u h a n ( N T U ) Dosis Koagulan (mg/l) Dosis Koagulan (mg/l) Run 1 Run 2 5.8 5.85 5.9 5.95 6 6.05 6.1 6.15 300 325 350 375 400 425 450 475 500 p H Dosis Koagulan (mg/l) Dosis Koagulan (mg/l) Run 1 Run 2
5.3
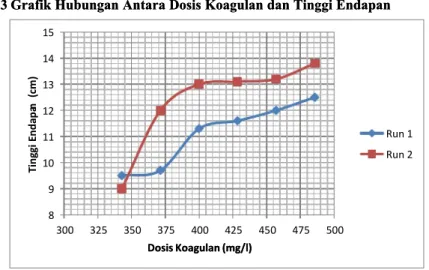
5.3Grafik Hubungan Antara Dosis Koagulan dan Tinggi EndapanGrafik Hubungan Antara Dosis Koagulan dan Tinggi Endapan
Grafik 3. Hubungan Antara Dosis Koagulan dan Tinggi Endapan Grafik 3. Hubungan Antara Dosis Koagulan dan Tinggi Endapan
5.4
5.4Grafik Hubungan Antara Dosis Koagulan dan DHLGrafik Hubungan Antara Dosis Koagulan dan DHL
Grafik 4. Hubungan Antara Dosis Koagulan dan DHL Grafik 4. Hubungan Antara Dosis Koagulan dan DHL
8 9 10 11 12 13 14 15 300 325 350 375 400 425 450 475 500 T i n g g i E n d a p a n ( c m ) Dosis Koagulan (mg/l) Dosis Koagulan (mg/l) Run 1 Run 2 0.7 0.8 0.9 1 1.1 1.2 1.3 300 325 350 375 400 425 450 475 500 D H L ( m s ) Dosis Koagulan (mg/l) Dosis Koagulan (mg/l) Run 1 Run 2
5.5
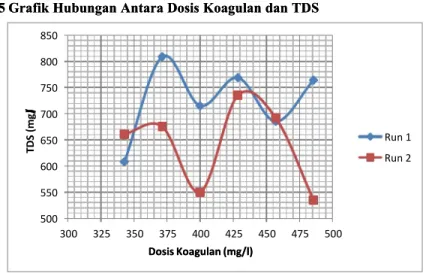
5.5Grafik Hubungan Antara Dosis Koagulan dan TDSGrafik Hubungan Antara Dosis Koagulan dan TDS
Grafik 5. Hubungan Antara Dosis Koagulan dan TDS Grafik 5. Hubungan Antara Dosis Koagulan dan TDS
500 550 600 650 700 750 800 850 300 325 350 375 400 425 450 475 500 T D S ( m g / l ) Dosis Koagulan (mg/l) Dosis Koagulan (mg/l) Run 1 Run 2
BAB VI
BAB VI
PEMBAHASAN
PEMBAHASAN
1. Oleh Ugi Muhammad Apriyanto (111411028) 1. Oleh Ugi Muhammad Apriyanto (111411028)2. Oleh Wina Puspita Asih (111411029) 2. Oleh Wina Puspita Asih (111411029) 3. Oleh Wina Septianawati (111411030) 3. Oleh Wina Septianawati (111411030) Tolong nanti susun
Tolong nanti susun
BAB V
BAB V
KESIMPULAN
KESIMPULAN
Adapun kesimpulan dari praktikum pengolahan limbah cair tahu menggunakan metode koagulasi dan flokulasi ini adalah sebagai berikut:
1. Aaa 2. Bbb 3. Ccc
Tolong Isi ya Win Tolong Isi ya Win
DAFTAR PUSTAKA
DAFTAR PUSTAKA
Anonim. 2010. http://id.wikipedia.org/koagulasi [diakses 26 Oktober 2013, pada pukul 13.00 WIB]
Anonim. 2010. http://id.wikipedia.org/flokulasi [diakses 26 Oktober 2013, pada pukul 13.14 WIB]
Anonim. 2013. http://greenkompasiana.com/polusi/2013/05/16/limbah-industri-tahu [diakses pada 27 Oktober 2013, pada pukul 11.15 WIB]
Fatha, A. 2007. Pemanfaatan Zeolit Aktif untuk Menurunkan BOD dan COD Limbah Cair Tahu.Semarang: Universitas Negeri Semarang
Goelanzaw. 2013. http://goelanzsaw.blogspot.com/2013/02/jart-test.html [diakses 27 Oktober 2013, pada pukul 14.30 WIB]
Herlambang.2002. Pengolahan Limbah Cair Industri Tahu Menggunakan Biji Kelor (Moringa Oleifera seeds) Sebagai Koagulan. Medan: Fakultas Teknik USU Nurhidayah, E. 2012. http:// evynurhidayah.wordpress.com/2012/01/17/jartest/