PENGARUH pH, SUHU HIDROLISIS ENZIM α-AMILASE DAN KONSENTRASI RAGI ROTI UNTUK PRODUKSI ETANOL
MENGGUNAKAN PATI BEKATUL
Skripsi
Untuk memenuhi sebagian persyaratan guna memperoleh gelar Sarjana Sains
Oleh :
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi ini adalah hasil penelitian saya sendiri dan tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, serta tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Apabila di kemudian hari dapat ditemukan adanya unsur penjiplakan maka gelar kesarjanaan yang telah diperoleh dapat ditinjau dan/atau dicabut.
Surakarta, Januari 2011
iv
PENGARUH pH, SUHU HIDROLISIS ENZIM α-AMILASE DAN KONSENTRASI RAGI ROTI UNTUK PRODUKSI ETANOL
MENGGUNAKAN PATI BEKATUL
Risha Tiara Jayanti
Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sebelas Maret, Surakarta
ABSTRAK
Selama ini bekatul hanya digunakan untuk pakan ternak. Sebagai sumber biomassa, bekatul berpotensi sebagai alternatif sumber energi berbasis etanol karena karbohidratnya yang tinggi. Karbohidrat melalui proses fermentasi dapat diubah menjadi etanol. Untuk mempercepat proses fermentasi karbohidrat, dibutuhkan katalis untuk mengubahnya menjadi gula sederhana (monosakarida), yaitu dengan menggunakan enzim α-amilase. Penelitian ini bertujuan untuk mengetahui pH dan suhu optimum yang dapat menghasilkan gula reduksi paling tinggi pada proses hidrolisis pati bekatul oleh enzim α-amilase dan mengetahui kadar etanol tertinggi yang dihasilkan setelah difermentasikan dengan menggunakan variasi konsentrasi ragi roti.
Penelitian ini dilakukan menggunakan Rancangan Acak Lengkap (RAL) dengan tiga faktor yaitu suhu hidrolisis (700C, 800C dan 900C), pH (5,2; 5,4 dan 5,6) dan konsentrasi ragi roti (0,5 mg, 1 mg dan 1,5 mg) dengan 3 ulangan. Bekatul dihidrolisis menggunakan enzim α-amilase dengan variasi pH dan suhu hidrolisis, dilanjutkan dengan fermentasi menggunakan ragi roti dalam botol fermentor. Waktu fermentasinya yaitu 3 hari. Kadar etanol dianalisis dengan AOAC tabel kadar etanol metode destilasi. Data dianalisis dengan ANAVA, dan jika terdapat beda nyata antar perlakuan variasi ketersediaan air dilanjutkan dengan Duncan’s Multiple Range Test (DMRT) taraf 5%.
Hasil penelitian menunjukkan bahwa perlakuan variasi pH dan suhu hidrolisis tidak berpengaruh terhadap konsentrasi gula reduksi. Kadar etanol tertinggi sebesar 2,84% ditunjukkan dengan penambahan ragi roti 1,5 mg pada suhu hidrolisis 700C dan pH 5,6. Tetapi dari uji statistik (α=0,05) hasil tersebut di atas tidak berbeda nyata dengan kadar etanol dengan penambahan ragi roti 1 mg. Sehingga ditinjau dari segi efisiensinya, penggunaan 1 mg ragi roti lebih ekonomis.
EFFECT OF pH, HYDROLISIS TEMPERATURE α-AMYLASE ENZYME AND BREAD YEAST CONCENTRATION FOR ETHANOL
PRODUCTION USING RICE POLISH STARCH
Risha Tiara Jayanti
Department of Biology, Faculty of Mathematics and Natural Science, Sebelas Maret University, Surakarta
ABSTRACT
All this time rice polish have been use only for cattle food. As a biomass source, rice polish is potential to be used as alternative ethanol based energi source cause it contains high carbohydrate. The carbohydrate through the fermentation process can be converted into ethanol. To accelerate the fermentation process of carbohydrate, α-amylase enzyme is need to catalyzed fermentation of simple sugar (monosaccharide). This research were aimed at studying pH and temperature optimum to produce the highest reduction sugar through hydrolysis of rice polish starch using α-amylase enzyme and to asses the highest ethanol concentration after fermentation by varying bread yeast concentration.
Completely Randomized Design was used in this research with three factorial : hydrolisis temperature (700C, 800C and 900C), pH (5,2;, 5,4 and 5,6) and bread yeast concentration (0,5 mg, 1 mg and 1,5 mg) each with 3 repetition. Rice polish was hidrolyzed using α-amylase enzyme by varying pH and hydrolisis temperature, followed by fermentation using bread yeast on fermentor bottle. The fermentation time was 3 days. Ethanol concentration was analyzed with a distillation method AOAC table-ethanol level. Data were analyzed with ANAVA, and if found a significant different from the treatments would be continued with Duncan’s Multiple Range Test (DMRT) at level of 5%.
vi MOTTO
Buah paling manis dari berani bermimpi adalah kejadian-kejadian menakjubkan
PERSEMBAHAN
Skripsi ini kupersembahkan dengan segenap cinta untuk Allah SWT
Ayah dan ibuku terima kasih untuk segalanya
Karina Dwi Jayanti dan Shakira Tika Jayanti jangan berhenti untuk meraih mimpi
Pebriana Nurcahyani, Andika Paramita, Iis Mucharomah,Dian Oktaviana, Ida Liana, Asti Mayasari, Yoga Sandi Perdana dan Hiba Rahmad Budiman terima kasih untuk segala dukungan dan perhatian yang memberikan semangat
viii
KATA PENGANTAR
Segala puji syukur penulis panjatkan ke hadirat Allah SWT atas segala limpahan rahmat, karunia serta hidayah-Nya yang tak tehingga sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul : “Pengaruh pH, Suhu Hidrolisis Enzim α-Amilase dan Konsentrasi Ragi Roti untuk Produksi Etanol menggunakan Pati Bekatul”. Penyusunan skripsi ini merupakan suatu syarat untuk memperoleh gelar kesarjanaan strata 1 (S1) pada Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sebelas Maret Surakarta.
Dalam pelaksanaan penelitian maupun penyusunan skripsi ini penulis mendapatkan banyak masukan, bantuan dan bimbingan dari berbagai pihak yang sangat bermanfaat baik secara langsung maupun tidak langsung. Oleh karena itu pada kesempatan ini penulis ingin menyampaikan terima kasih yang setulusnya kepada:
Prof. Drs. Sutarno, M.Sc. Ph.D., selaku Dekan FMIPA Universitas Sebelas Maret Surakarta yang telah memberikan arahan serta ijin penelitian skripsi.
Dra. Endang Anggarwulan, M.Si., selaku Ketua Jurusan Biologi FMIPA Universitas Sebelas Maret Surakarta atas ijin penelitian untuk keperluan skripsi.
Tjahjadi Purwoko, M.Si., selaku dosen pembimbing I yang telah memberikan bimbingan, arahan serta dukungan selama penelitian hingga selesainya penyusunan skripsi.
Elisa Herawati, M.Eng., selaku dosen pembimbing II yang telah memberikan bimbingan, arahan serta dukungan selama penelitian hingga selesainya penyusunan skripsi.
Sunarto, M.S., selaku dosen penelaah I yang telah memberikan bimbingan dan petunjuk selama penelitian sampai selesainya penyusunan skripsi.
Seluruh dosen, karyawan, staf Laboratorium Jurusan Biologi FMIPA Universitas Sebelas Maret Surakarta yang telah dengan sabar dan tiada henti-hentinya memberikan dorongan baik spiritual maupun materil sehingga penulis dapat menyelesaikan skripsi ini.
Kepala dan staf Laboratorium Pusat MIPA Universitas Sebelas Maret Surakarta yang telah mengijinkan dan membantu penulis untuk melakukan penelitian di laboratorium.
Keluarga besar Harjoko atas doa, dukungan dan perhatian yang memberikan semangat bagi penulis.
Keluarga besar Biologi 2006, terutama kepada Lilin Indah, Mita Mutia, Nina Kurnianingrum, Cintya Sandra, Ikke Irmawati, Idhyas Ayu, Pramesti Dwi A, Siska, Hartini, Rhosid Fajar, Prasasti Wahyu, Rianita, Nur Ana Fiatun, Galih Septia, Septiana W dan Setyabudi, untuk semangat, kebersamaan, dan persaudaraan yang luar biasa. Serta semua pihak yang telah memberikan dukungan yang tidak dapat disebutkan satu persatu.
Dengan kerendahan hati penulis menyadari bahwa dalam penelitian dan penyusunan skripsi ini masih jauh dari sempurna, oleh karena itu saran dan kritik yang membangun dari para pembaca akan sangat membantu. Semoga skripsi ini dapat bermanfaat bagi kita semua.
x
DAFTAR ISI
Halaman HALAMAN JUDUL ...
HALAMAN PENGESAHAN ... HALAMAN PERNYATAAN ... ABSTRAK ... ABSTRACT... HALAMAN MOTTO ... HALAMAN PERSEMBAHAN ... KATA PENGANTAR... DAFTAR ISI... DAFTAR TABEL ... DAFTAR GAMBAR ... DAFTAR LAMPIRAN ... DAFTAR SINGKATAN ... BAB I. PENDAHULUAN ... A. Latar Belakang... B. Rumusan Masalah ... C. Tujuan Penelitian... D. Manfaat Penelitian ... BAB II. LANDASAN TEORI ... A. Tinjauan Pustaka ... 1. Bekatul ... 2. Pati ... 3. Ragi roti ... 4. Enzim α-amilase ... 5. Fermentasi etanol ... B. Kerangka Pemikiran ... BAB III. METODE PENELITIAN ... A. Waktu dan Tempat Penelitian ... B. Alat dan Bahan ...
C. Cara Kerja ... 1. Penyiapan Alat dan Bahan... 2. Pembuatan Bubur Bekatul ... 3. Proses Hidrolisis... 4. Proses Fermentasi ... 5. Pengukuran Kadar Etanol ... E. Analisis Data... BAB IV. HASIL DAN PEMBAHASAN ... A. Pemecahan Pati Bekatul menjadi Gula Reduksi oleh Enzim α-amilase dengan Menggunakan Variasi Suhu dan pH ... B. Fermentasi Etanol oleh Ragi Roti ... BAB V. KESIMPULAN DAN SARAN... A. Kesimpulan ... B. Saran... DAFTAR PUSTAKA ... LAMPIRAN... RIWAYAT HIDUP PENULIS ...
xii
DAFTAR TABEL
Halaman Tabel 1. Konsentrasi gula reduksi (mg / ml) pada bubur bekatul
dengan variasi suhu hidrolisis dan pH ... Tabel 2. Kadar etanol pada konsentrasi ragi roti yang berbeda ... Tabel 3. Absorbansi gula reduksi standar ...
DAFTAR GAMBAR
Halaman Gambar 1. Amilosa ...
Gambar 2. Amilopektin... Gambar 3. Cara kerja α-amilase ... Gambar 4. Fase pertumbuhan bakteri pada kultur curah ... Gambar 5. Jalur fermentasi etanol oleh S. Cerevisiae ... Gambar 6. Alur Kerangka Pemikiran ... Gambar 7. Kurva standar gula reduksi ... Gambar 8. Konsentrasi gula reduksi (mg/ml) pada bubur bekatul
dengan variasi suhu hidrolisis dan pH ... Gambar 9. Kadar etanol pada konsentrasi ragi roti yang berbeda... Gambar 10. Bekatul... Gambar 11. Ragi roti ... Gambar 12. Proses hidrolisis ... Gambar 13. Enzim α-amilase ... Gambar 14. Uji gula reduksi ... Gambar 15. Proses fermentasi ... Gambar 16. Destilasi ... Gambar 17. Etanol ...
xiv
DAFTAR LAMPIRAN
Halaman Lampiran 1. Penyediaan Reagen ...
Lampiran 2. Pengukuran Parameter ... Lampiran 3. Hasil pengukuran parameter ... Lampiran 4. Hasil analisis ANAVA perlakuan suhu hidrolisis dan pH terhadap hasil konsentrasi gula reduksi ... Lampiran 5. Hasil analisis ANAVA perlakuan konsentrasi ragi roti terhadap kadar etanol ... Lampiran 6. Tabel etanol ... Lampiran 7. Gambar ...
37 38 41
45
DARTAR SINGKATAN
Singkatan Keterangan
ºC ANAVA ATP CO2 DMRT g H H2O
J. Biosci. Bioeng J. Biotechnol J. Sci. & Technol l mg ml nm O2 RAL derajat celcius analisis varian
adenosine tri phospphate gas karbondioksida
Duncan’s multiple range test gram
hidrogen
dihidrogen oksida
Jurnal Bioscience Bioenergy Jurnal Biotechnology
Jurnal Science and Technology liter
mili gram mili liter nanometer gas oksigen
1 BAB I PENDAHULUAN
A. Latar Belakang Masalah
Energi sangat dibutuhkan oleh masyarakat tetapi cepat atau lambat cadangan minyak bumi dunia akan habis. Ini disebabkan oleh persediaan bahan bakar fosil yang terbatas dan tidak dapat diperbaharui. Indonesia merupakan salah satu negara yang sedang menghadapi persoalan energi yang serius akibat ketergantungan yang sangat besar terhadap energi fosil. Etanol merupakan salah satu bahan bakar alternatif yang dapat diperoleh dari proses fermentasi biomassa yang mengandung karbohidrat dengan bantuan mikroorganisme (Yetty, 2007).
Indonesia adalah negara agraris, karena tanahnya subur dan dapat ditumbuhi berbagai tanaman. Padi, singkong dan jagung merupakan tanaman yang paling banyak ditanam di Indonesia dan tanaman tersebut merupakan sumber karbohidrat tinggi.
Pada proses pengolahan padi menjadi beras, dihasilkan limbah berupa jerami, dedak, dan bekatul. Bekatul merupakan lapisan sebelah dalam butiran beras (lapisan aleuron/kulit ari) dan sebagian kecil endosperma berpati. Bekatul mengandung karbohidrat cukup tinggi, yaitu 51-55 g / 100 g (Kompas, 2009). Tingginya kandungan karbohidrat ini sangat menguntungkan karena dapat digunakan sebagai sumber energi alternatif.
2
dikonversi menjadi glukosa dengan katalisis enzim α-amilase. Pada tahap kedua yaitu fermentasi, glukosa yang terbentuk dikonversi menjadi etanol dan karbondioksida oleh khamir Saccharomyces cerevisiae (Banati dkk., 2007).
Secara umum S.cerevisiae di Indonesia digunakan untuk pembuatan tape dan roti. Oleh karena itu, isolat S.cerevisiae dapat dijumpai pada ragi tape dan ragi roti. Ragi roti dapat menjadi salah satu alternatif pengganti penggunaan isolat S.cerevisiae dalam proses fermentasi produksi etanol. Hal ini disebabkan ragi roti mudah diperoleh di pasaran dan tidak memerlukan perlakuan yang spesifik (Reed, 1991).
Ketidakmampuan S.cerevisiae memfermentasi pati / amilum menjadi etanol karena tidak memiliki enzim amilase yang cukup. Fardiaz (1988) melaporkan bahwa pati dapat dipecah oleh enzim amilase menjadi komponen dengan berat molekul lebih rendah dan lebih larut. Enzim tersebut memecah ikatan α-1,4-glikosida dari molekul pati.
3
B. Rumusan Masalah
1. Berapakah pH dan suhu optimum yang dapat menghasilkan gula reduksi paling tinggi pada proses hidrolisis pati bekatul oleh enzim α-amilase ?
2. Berapakah kadar etanol tertinggi yang dihasilkan setelah difermentasikan dengan menggunakan variasi konsentrasi ragi roti ?
C. Tujuan Penelitian
1. Mengetahui pH dan suhu optimum yang dapat menghasilkan gula reduksi paling tinggi pada proses hidrolisis pati bekatul oleh enzim α-amilase.
2. Mengetahui kadar etanol tertinggi yang dihasilkan setelah difermentasikan dengan menggunakan variasi konsentrasi ragi roti.
D. Manfaat Penelitian
1. Dapat menambah informasi ilmiah dan pengetahuan kepada penulis dan masyarakat luas terutama dalam pemanfaatan bekatul untuk produksi etanol. 2. Dapat meningkatkan nilai ekonomi hasil samping penggilingan padi yang
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka 1. Bekatul
Bekatul merupakan salah satu hasil samping proses penggilingan padi yang jumlahnya cukup banyak. Pada proses penggilingan beras pecah kulit diperoleh hasil samping dedak 8-9% dan bekatul sekitar 2-3%. Ketersediaan bekatul di Indonesia cukup banyak dan mencapai 4.5-5 juta ton setiap tahunnya (Damayanthi dan Listyorini, 2006).
5
2. Pati
Karbohidrat yang tersusun atas lebih dari delapan satuan monosakarida disebut polisakarida. Pati merupakan polisakarida yang banyak ditemukan pada tanaman. Senyawa ini disimpan dalam bentuk granula dengan ukuran dan karakteristik yang spesifik untuk setiap spesies tanaman (van der Maarel, dkk., 2002). Beberapa contoh tanaman yang memiliki kandungan pati dengan konsentrasi tinggi yaitu jagung, sorghum, beras, dan singkong, masing-masing sebesar 72,4%; 73%; 78,9% dan 34,7% (Endah dkk., 2009).
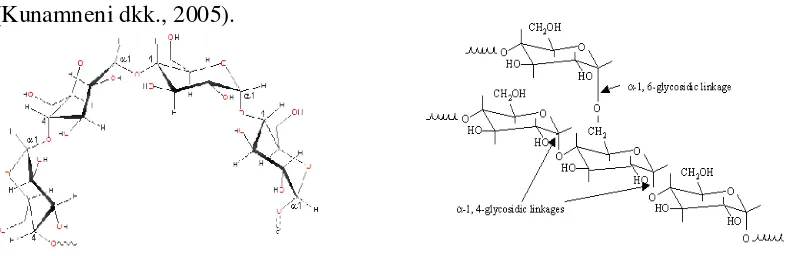
Pati merupakan polimer yang tersusun dari unit satuan α-D-glukosa yang dihubungkan oleh ikatan α-1,4 glikosidik dan ikatan α-1,6 glikosidik pada percabangan rantainya. Secara alami, pati merupakan campuran dari amilosa dan amilopektin yang kedua-duanya merupakan suatu polimer dari α-D-glukosa. (Kunamneni dkk., 2005).
Amilosa merupakan suatu polimer rantai tunggal tidak bercabang, terbentuk dari 500-20.000 monomer α-D-glukosa yang dihubungkan oleh ikatan α-1,4 glikosidik. Amilopektin merupakan suatu polimer rantai bercabang,
terbentuk dari 100.000 monomer glukosa yang dihubungkan oleh ikatan α-1,4 glikosidik pada rantai utama dan α-1,6 glikosidik pada percabangannya (Kunamneni dkk., 2005).
6
3. Ragi roti
Ragi roti terdiri atas 3 jenis yaitu (a) Ragi basah (fresh yeast) yaitu ragi
yang mengandung 70% air, harus disimpan pada suhu 2-40C dan bisa langsung digunakan pada saat pengadukan dengan jumlah pemakaian 2-5% dari jumlah
tepung. Contoh merk dagang : Red Star dan Fleishcmann’s; (b) Ragi koral (active dry yeast) yaitu ragi yang mengandung 7% air dan daya simpannya lama. Jika
akan digunakan, harus diaktifkan dengan cara mencampur satu bagian ragi dengan empat bagian air hangat (suhu 400C) selama 10-30 menit. Jumlah pemakaiannya sebesar 1,5-3% dari jumlah terigu. Contoh merk dagang : Red Star, Fleishcmann’s dan Rize; (c) Ragi instan (instant yeast) yaitu ragi yang mengandung air 1-2% dan
daya simpannya lama. Penggunaannya langsung pada saat pengadukan dengan jumlah pemakaian 0,75-3% dari jumlah tepung. Contoh merk dagang : Fermipan
dan Saf instant (Chan, 2009).
Ketiga jenis ragi roti tersebut sudah beredar di Indonesia. Akan tetapi ragi
instan lebih sering digunakan karena menghasilkan fermentasi yang lebih
konsisten dan penyimpanannya yang sangat mudah (pada suhu ruang normal)
(Stefanie and Nicko, 2008).
7
dalam kemasannya (Pelczar dan Chan, 1988). Selain itu, dapat juga diketahui dari
kemasannya, komposisi ragi roti terdiri dari ragi (S.cerevisiae) dan pengemulsi (sorbitan monostearate).
Fungsi utama ragi roti adalah memfermentasikan glukosa yang ada di dalam tepung menghasilkan etanol dan CO2. Karbondioksida yang dihasilkan akan terperangkap sebagai gelembung-gelembung kecil sehingga adonan roti dapat mengembang pada saat dipanaskan (Stefanie dan Nicko, 2008).
Pada pembuatan roti secara modern, biakan murni galur-galur S.cerevisiae terpilih dicampur dengan adonan roti untuk menghasilkan perubahan-perubahan yang dikehendaki dalam hal tekstur, rasa dan aroma. Galur-galur S.cerevisiae yang dipilih untuk memproduksi ragi roti secara komersial memiliki kemampuan untuk memfermentasi gula dengan baik di dalam adonan dan tumbuh dengan cepat. Karbondioksida yang dihasilkan selama fermentasi itulah yang membuat adonan mengembang. Mutu produk bergantung pada seleksi khamir yang baik, keadaan inkubasi dan pemilihan bahan mentah (Pelczar dan Chan, 1988).
Fungsi alternatif ragi roti antara lain dapat digunakan dalam pembuatan etanol, produksi minyak kelapa fermentasi (Hariawanty dan Nita, 2010) dan induksi tunas pisang Cavendish. (Ikasari, 2004).
8
4. Enzim α-amilase
Hidrolisis adalah suatu proses antara reaktan dengan air agar suatu senyawa pecah terurai. Pada reaksi hidrolisis pati dengan air, air akan menyerang pati pada ikatan α-1,4-glukosida menghasilkan dextrin, sirup atau glukosa tergantung pada derajat pemecahan rantai polisakarida dalam pati. Reaksi antara air dan pati ini berlangsung sangat lambat sehingga diperlukan bantuan katalisator untuk memperbesar kereaktifan air. Katalisator ini bisa berupa asam maupun enzim. Katalisator asam yang biasa digunakan adalah asam klorida, asam nitrat dan asam sulfat. Dalam industri umumnya digunakan asam klorida sebagai katalisator. Pemilihan ini didasarkan bahwa garam yang terbentuk setelah penetralan hasil merupakan garam yang tidak berbahaya yaitu garam dapur. Faktor – faktor yang berpengaruh pada reaksi hidrolisa pati adalah suhu reaksi, waktu reaksi , dan konsentrasi katalisator (Endah dkk., 2009).
9
lainnya. Enzim dapat diisolasi dari hewan, tumbuhan dan mikroorganisme (Azmi, 2006).
Pati dapat dipecah oleh enzim amilase menjadi komponen dengan berat molekul lebih rendah dan lebih larut. Enzim tersebut memecah ikatan α -1,4-glikosida dari molekul pati (Fardiaz, 1988).
Amilase terdiri atas 3 jenis yaitu a-amilase, b-amilase, dan glukoamilase.
Enzim a-amilase bekerja dengan memutus ikatan α-1,4-glikosidik pada rantai lurus amilum sehingga menghasilkan glukosa dalam konfigurasi alpha, maltosa dan dekstrin. Enzim β-amilase bekerja dengan memecah ikatan α-1,4 glikosidik dan tidak mampu melewati ikatan percabangan α-1,6 glikosidik sehingga menghasilkan maltosa dalam konfigurasi beta. Enzim glukoamilase bekerja dengan menghidrolisis ikatan α-1,4 dan α-1,6 glikosidik dari gugus non pereduksi sehingga menghasilkan D-glukosa (Moo Yong, 1985).
10
kisaran pH 5,2 –5,6 (Novozyme, 2010). Hal ini didukung oleh Fogarty (1983), enzim α-amilase umumnya stabil pada kisaran pH 5 - 8.
Mikroorganisme yang paling banyak menghasilkan enzim α-amilase dan paling banyak digunakan adalah jamur dan bakteri seperti Aspergillus oryzae, Bacillus amyloliquefaciens, dan Bacillus licheniformis (Sivaramakrishnan, 2006). Sejumlah ragi dapat memproduksi amilase dengan menggunakan media pati sebagai sumber karbon dan energi. Kebanyakan α-amilase adalah calcium metallo-enzyme yang mengandung minimal satu atom kalsium per molekul enzim (Moo Young, 1985). Aktivitas atau kinerja enzim amilase dipengaruhi oleh banyak faktor. Terdapat lima faktor utama yang mempengaruhi aktivitas enzim yaitu pH, temperatur, konsentrasi enzim, dan konsentrasi substrat (Sukandar dkk., 2009). Skema kerja α-amilase dapat dilihat pada gambar 3.
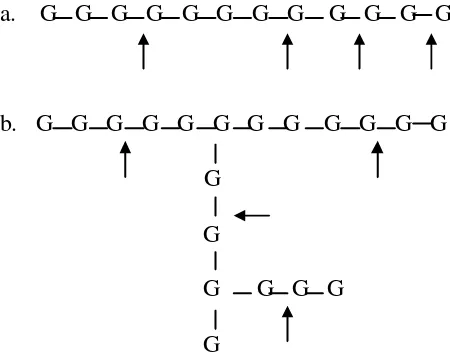
a. G G G G G G G G G G G G
b. G G G G G G G G G G G G G
G
11
G : glukosa.
Cara kerja α-amilase terjadi melalui dua tahap yaitu pertama degradasi amilosa menjadi maltosa dan maltotriosa yang terjadi secara acak. Degradasi ini terjadi sangat cepat dan diikuti dengan menurunnya viskositas dengan cepat. Tahap kedua relatif lambat yaitu pembentukan glukosa dan maltosa sebagai hasil akhir secara tidak acak. Keduanya merupakan kerja enzim α-amilase pada molekul amilosa saja. Kerja α-amilase pada molekul amilopektin akan menghasilkan glukosa, maltosa dan berbagai jenis limit dekstrin yaitu oligosakarida yang terdiri dari empat atau lebih residu gula yang semuanya mengandung α-1,6-glikosidik (Norman, 1980).
5. Fermentasi Etanol
Menurut Judoamidjojo (1992), fermentasi adalah peruraian senyawa organik menjadi senyawa sederhana dengan bantuan mikroorganisme sehingga menghasilkan energi. Kebanyakan fermentasi etanol skala komersial dilakukan oleh khamir, salah satunya S.cerevisiae yang menghasilkan etanol.
Penggunaan S.cerevisiae dalam produksi etanol secara fermentasi telah banyak dikembangkan di beberapa negara, seperti Brasil, Afrika Selatan, dan Amerika Serikat. Hal ini disebabkan S.cerevisiae dapat memproduksi etanol dalam jumlah besar (Basso dkk., 2008).
12
semua bahan dimasukkan sekaligus di awal proses dan dikeluarkan secara sekaligus pula setelah proses, kecuali oksigen atau udara dialirkan secara kontinyu (Crueger and Crueger, 1988). Keuntungan metode ini yaitu produktivitas tinggi, waktu fermentasi cepat dan efek toksik direduksi pada komponen media (Stanbury and Whitaker, 1984).
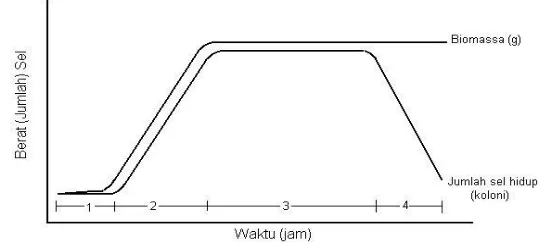
Gambar 4. Fase pertumbuhan bakteri pada kultur curah; 1 fase adaptasi; 2 fase perbanyakan; 3 fase statis; 4 fase kematian (Purwoko, 2007).
13
Produksi etanol melalui proses sakarifikasi dan fermentasi simultan. Proses konversi pati menjadi etanol dilakukan melalui dua tahap yang berjalan secara simultan di dalam satu reaktor. Tahap pertama adalah tahap sakarifikasi, yaitu pati dikonversi menjadi glukosa dengan katalisis amilase. Pada tahap kedua, setiap glukosa yang terbentuk sebagai hasil sakarifikasi, langsung secara simultan dikonversi menjadi etanol dan karbondioksida oleh ragi S.cerevisiae yang sudah ada dalam reaktor yang sama. Dengan proses ini, hambatan substrat dalam produksi etanol dan hambatan produk dalam hidrolisis pati secara enzimatik dapat diminimalkan (Rendra dan Ginanjar, 2007).
Reaksi yang terjadi pada proses produksi etanol secara sederhana ditujukkan pada reaksi :
(C6H10O5)n N C6H12O6
(pati) enzim amilase (glukosa)
(C6H12O6)n 2 C2H5OH + 2 CO2
(glukosa) yeast (ragi) (etanol)
14
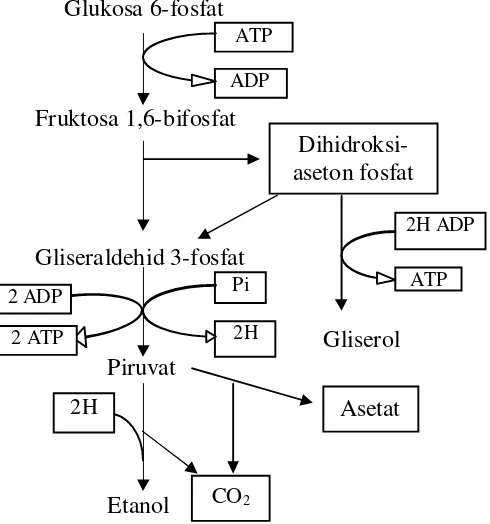
Saccharomyces cerevisiae menggunakan jalur EMP (Embden Meyerhoff Parnas) untuk memfermentasi glukosa menjadi etanol pada kondisi netral atau sedikit asam dan anaerob. Pada kondisi mikroaerofil, S.cerevisiae mampu merespirasi 10% glukosa menjadi CO2. Fermentasi etanol oleh S.cerevisiae dapat menghasilkan etanol kurang dari 50% (Purwoko, 2007).
Glukosa 6-fosfat
Fruktosa 1,6-bifosfat
Gliseraldehid 3-fosfat
Gliserol Piruvat
Etanol
Gambar 5. Jalur fermentasi etanol oleh S. cerevisiae
Pada konsentrasi yang rendah, laju hidrolisis pati menjadi glukosa
ATP
ADP
Dihidroksi-aseton fosfat
2H ADP
ATP Pi
2H
2H
CO2
Asetat
15
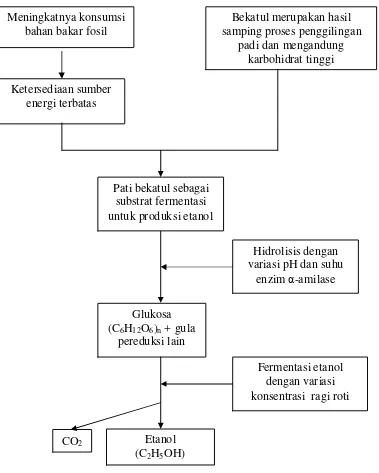
B. Kerangka Pemikiran
16
Meningkatnya konsumsi bahan bakar fosil
Bekatul merupakan hasil samping proses penggilingan
padi dan mengandung karbohidrat tinggi
Glukosa (C6H12O6)n + gula
pereduksi lain
Hidrolisis dengan variasi pH dan suhu
enzim α-amilase
Etanol (C2H5OH)
Fermentasi etanol dengan variasi konsentrasi ragi roti Pati bekatul sebagai
substrat fermentasi untuk produksi etanol Ketersediaan sumber
energi terbatas
[image:31.595.133.512.107.580.2]17 BAB III
METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan selama 3 bulan, pada bulan Agustus – Oktober 2010 di Laboratorium Pusat MIPA Universitas Sebelas Maret Surakarta.
B. Alat dan Bahan Penelitian
Alat yang digunakan dalam penelitian ini meliputi erlenmeyer, hot plate, pipet volum, spektrofotometer, pH meter, cawan petri, tabung reaksi, laminary air flow, autoclave, inkubator, rotary evaporator, gelas ukur, beaker glass, piknometer, labu alas bulat, hemasitometer Levy dan oven.
Bahan yang digunakan dalam penelitian ini antara lain adalah bekatul, akuades, larutan HCl 0,1%, larutan arsenomolybdat, reagen Nelson, alkohol, enzim α-amilase (Novozyme)0,09 gram dan ragi roti (Fermipan) 0,5 mg; 1 mg dan 1,5 mg.
C. Cara kerja 1. Penyiapan alat dan bahan
Alat dan bahan yang digunakan disterilisasi dengan autoclave pada suhu 1210C selama 15 menit.
18
Bekatul sebanyak 20 gram dimasukkan ke dalam erlenmeyer 250 ml kemudian dilarutkan dengan akuades 100 ml dan dibuat tiga ulangan setiap proses. Selanjutnya bubur bekatul disterilisasi dengan menggunakan autoclave.
3. Proses hidrolisis
Bubur bekatulyang sudah disterilisasi, diatur pH-nya menjadi 5,2; 5,4 dan 5,6 dengan penambahan HCl 0,1%. Enzim α-amilase sebanyak 0,09 gram (Banati dkk., 2007) ditambahkan ke dalam erlenmeyer kemudian dipanaskan di atas hot plate. Proses pemanasan berlangsung ± 1 jam dengan variasi suhu pemanasan 700C, 800C dan 900C. Proses hidrolisis selesai ditandai dengan parameter dimana bubur yang diproses menjadi lebih cair seperti sup. Setelah dihidrolisis, dilakukan pengukuran konsentrasi gula reduksi berdasarkan metode Nelson-Somogyi (lampiran 2). Selanjutnya diinkubasi pada suhu kamar.
4. Proses fermentasi
19
Sementara dilakukan destilasi, piknometer dikalibrasi. Piknometer diisi akuades destilasi dan ditutup. Piknometer dan akuades ditimbang, berat yang didapat adalah C. Piknometer dikosongkan kemudian dikeringkan dengan oven. Piknometer yang telah kering ditimbang, berat yang didapatkan adalah B. Berat akuades (W) dihitung dengan cara C-B.
Distilat dipindahkan ke dalam gelas beaker kering. Distilat diaduk supaya homogen sebelum diisikan ke piknometer. Piknometer kering diisi dengan distilat, permukaan luar piknometer dikeringkan dan ditimbang. Hasil yang didapat adalah A.
Berat distilat adalah A - B = L. Berat distilat (L) dihitung dengan “specific gravity” atau spg = L/W. Nilai spg ditentukan dengan menggunakan tabel AOAC (Analysis of the Association of Official Analitical Chemists) dan selanjutnya persentase etanol dihitung (Horwits and Franklin, 1975).
D. Analisis Data
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL). Masing-masing perlakuan dilakukan dengan 3 ulangan. Data dianalisis secara statistik dengan menggunakan ANAVA pada taraf kepercayaan 95% (α = 0,05) kemudian dilanjutkan dengan Duncan Multiple Range Test (DMRT) untuk mengetahui beda
BAB IV
HASIL DAN PEMBAHASAN
A. Pemecahan pati bekatul menjadi gula reduksi oleh enzim α-amilase dengan menggunakan variasi suhu dan pH.
Produk etanol dari hasil fermentasi dapat dipengaruhi oleh penambahan enzim α-amilase, dimana enzim α-amilase dapat menghidrolisis amilum dengan memutus ikatan α-1,4-glukosida menjadi monomer-monomer glukosa sebagai gula sederhana yang digunakan untuk fermentasi alkohol. Tanpa adanya penambahan enzim α-amilase, dapat menyebabkan proses hidrolisis amilum menjadi glukosa kurang sempurna sebab tidak ada pemutusan ikatan spesifik pada homopolimer rantai ikatan α-1,4-glikosida amilum sehingga glukosa (monosakarida) yang dihasilkan dari hidrolisis, secara mekanis tidak optimal (Banati dkk., 2007).
Enzim α-amilase yang digunakan berasal dari Bacillus licheniformis yang dapat menghidrolisis pati dengan hasil utama maltoheksosa, malopentosa dengan jumlah glukosa yang lebih tinggi (8 – 10%). Enzim ini berupa cairan
21
Dalam proses hidrolisis, pati dipecah menjadi gula reduksi dengan menggunakan enzim α-amilase.
(C6H10O5)n N C6H12O6
(pati) enzim amilase (glukosa)
Proses setelah hidrolisis adalah fermentasi dengan menggunakan ragi. Glukosa hasil hidrolisis diubah oleh ragi menjadi etanol. Kemampuan ragi menghasilkan etanol bergantung pada kadar glukosa, pH, kadar oksigen dan faktor lingkungan lainnya (Wulan dkk., 2007). Pentingnya pra fermentasi menyebabkan pengaturan kondisi optimum untuk lingkungan ragi dilakukan pada penelitian ini. Salah satunya adalah kadar glukosa sebagai media pertumbuhan ragi.
Pengukuran kadar glukosa dilakukan pada hasil hidrolisis bubur bekatul yang sudah diberi 0,09 gr enzim α-amilase. Pada penelitian ini digunakan variasi suhu hidrolisis (700C, 800C dan 900C) dan pH (5,2; 5,4 dan 5,6) untuk mengetahui konsentrasi gula reduksi paling tinggi.
Enzim memperlihatkan aktivitas katalitik maksimum pada kisaran pH tertentu yang disebut pH optimum kerja enzim. Enzim umumnya aktif pada rentang pH yang sempit. Oleh karena enzim merupakan protein, perubahan pH akan mempengaruhi gugus-gugus amino dan karboksilat dari protein enzim. Di luar pH optimumnya, aktivitas katalitik enzim dapat menjadi rendah atau bahkan dapat kehilangan aktivitas katalitiknya (Sukandar dkk., 2009).
22
terlebih dulu ditambah HCl 0,1%. Dalam hal ini penambahan HCl bertujuan untuk menurunkan pH awal bubur bekatul yang ber-pH 6.
Suhu dapat menentukan laju suatu reaksi. Pada reaksi yang melibatkan biokatalis, suhu juga dapat mempengaruhi kestabilan enzim yang merupakan suatu protein. Kenaikan suhu sampai sedikit di atas suhu optimumnya dapat menurunkan aktivitas enzim sedangkan suhu jauh di atas suhu optimumnya enzim akan mengalami denaturasi sehingga enzim akan kehilangan aktivitas katalitiknya (Sukandar dkk., 2009). Hasil pengukuran konsentrasi gula reduksi pada tiap perlakuan dapat dilihat pada tabel 1.
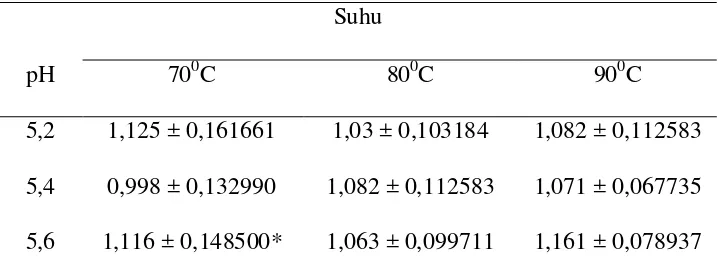
Tabel 1. Konsentrasi gula reduksi (mg/ml) pada bubur bekatul dengan variasi suhu hidrolisis dan pH.
Suhu
pH 700C 800C 900C
5,2 5,4 5,6
1,125 ± 0,161661 0,998 ± 0,132990 1,116 ± 0,148500*
1,03 ± 0,103184 1,082 ± 0,112583 1,063 ± 0,099711
1,082 ± 0,112583 1,071 ± 0,067735 1,161 ± 0,078937
[image:37.595.133.492.416.553.2]23
α-amilase semakin naik. Sedangkan pada suhu >1000C, aktivitas enzim α-amilase
menurun.
Selanjutnya dengan menggunakan analisis anava antara pH dan suhu hidrolisis terhadap konsentrasi gula reduksi menunjukkan tidak signifikan, dimana p > 0,05 yang artinya tidak berbeda nyata antar perlakuan yaitu 0,815. Hal ini menunjukkan bahwa perbedaan suhu dan pH yang diberikan tidak berpengaruh besar terhadap kadar gula reduksi yang dihasilkan. Tetapi jika berdasarkan efisiensinya, perlakuan suhu hidrolisis 700C dengan pH 5,6 lebih efisien dalam proses hidrolisis.
Glikolisis merupakan pengubahan glukosa menjadi dua molekul piruvat. Pada kondisi anaerobik, piruvat direduksi menjadi etanol dan CO2. Menurut Wulan dkk. (2007), kadar glukosa yang dibutuhkan untuk fermentasi berada pada konsentrasi 10-18%. Konsentrasi glukosa di atas 25% akan memperlambat fermentasi sedangkan di atas 70% proses fermentasi akan berhenti. Hal ini disebabkan adanya tekanan osmotik. Pada konsentrasi gula substrat sekitar 16% akan mempercepat pertumbuhan ragi pada awal fermentasi. Dari perhitungan kadar glukosa, gulareduksi bubur bekatulsebesar9,98-11,61% maka gula reduksi hasil hidrolisis bubur bekatul dapat digunakan sebagai substrat pada proses fermentasi.
B. Fermentasi etanol oleh ragi roti
24
dkk., 2008). Ada tiga komponen yang terlibat dalam proses fermentasi yaitu substrat, mikroba dan produk. Dalam penelitian ini, substrat yang digunakan
adalah larutan hasil sakarifikasi pati bekatul 20% yang diberi enzim α-amilase dengan perlakuan suhu 700C dan pH 5,6. Hal ini karena energi yang digunakan pada proses hidrolisis dengan suhu 700C lebih sedikit daripada suhu 800C atau 900C. Selain itu digunakan pH 5,6 karena mendekati pH awal bubur bekatul
sebelum dihidrolisis yaitu pH 6.
Fermentasi oleh yeast (S. cerevisiae) dapat menghasilkan etil alkohol (etanol) dan CO2. Untuk memisahkan alkohol dan air dapat dilakukan penyulingan atau destilasi sehingga dapat diperoleh alkohol dengan kadar kurang lebih 90% (Fessenden and Fessenden, 1991). Destilasi adalah suatu proses penguapan dan pengembunan kembali, yaitu untuk memisahkan campuran dua atau lebih zat cair ke dalam fraksi-fraksinya berdasarkan perbedaan titik didihnya (Bustaman, 2008).
25
Etanol merupakan produk metabolit primer karena dalam fermentasi etanol, produk etanol dihasilkan bersamaan dengan pertumbuhan sel. Gula reduksi
dipakai oleh ragi untuk pertumbuhannya dan selama metabolisme berlangsung akan dihasilkan etanol. Besarnya etanol yang dihasilkan dan pertumbuhan sel sangat dipengaruhi oleh besarnya substrat yang tersedia (Wulan dkk., 2007).
Tinggi rendahnya konsentrasi etanol selain ditentukan oleh mikroba juga ditentukan oleh tinggi rendahnya konsentrasi gula reduksi yang digunakan sebagai substrat dalam fermentasi (Wen and Cheng, 2000). Sehingga semakin tinggi konsentrasi gula reduksi yang digunakan sebagai substrat maka semakin tinggi juga konsentrasi yang dihasilkan dalam fermentasi oleh ragi.
Dalam fermentasi kadar gula total semakin lama akan semakin menurun. Hal ini dapat terjadi karena gula-gula tersebut akan di metabolisme oleh Saccharomyces cerevisiae yang tumbuh dalam media sebagai nutrisi untuk pertumbuhan sehingga semakin lama waktu fermentasi gula akan diubah menjadi etanol (Isnawati, 1997).
Konsentrasi etanol dapat diketahui dengan menggunakan rumus sebagai berikut :
A - B Konsentrasi etanol = X 1
C - B
Keterangan :
A = berat destilat (gr)
26
[image:41.595.142.475.279.385.2]Kadar etanol ditentukan dengan menggunakan tabel AOAC (Analysis of the Association of Official Analitical Chemists) dan selanjutnya persentase etanol dapat diketahui (Horwits and Franklin, 1975).
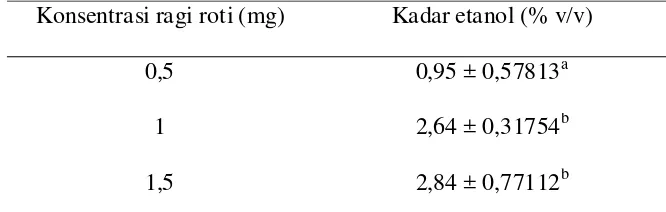
Tabel 2. Kadar etanol pada konsentrasi ragi roti yang berbeda Konsentrasi ragi roti (mg) Kadar etanol (% v/v)
0,5 0,95 ± 0,57813a
1 2,64 ± 0,31754b
1,5 2,84 ± 0,77112b
Keterangan : Angka yang diikuti huruf sama tidak berbeda nyata (α=0,05).
Dari data tabel 2, dapat diketahui bahwa ragi roti 1,5 mg menghasilkan kadar etanol tertinggi yaitu sebesar 2,84 %. Selanjutnya dengan menggunakan analisis anava antara kadar etanol dengan perlakuan penambahan ragi roti, menunjukkan hasil yang signifikan yaitu p < 0,05. Artinya perbedaan konsentrasi ragi roti berpengaruh terhadap hasil etanol yang diperoleh, dengan tingkat signifikan sebesar 0,013.
27
kemampuan yeast untuk fermentasi menjadi berkurang. Begitupula jika ragi yang digunakan berlebihan akan menghambat proses fermentasi dimana akan terjadi fase pertumbuhan lag (lambat). Disamping itu, adanya penambahan biomasa dapat terjadi jika botol untuk fermentasi tidak tertutup rapat sehingga udara masuk ke dalam botol dan mengakibatkan pertumbuhan biomassa yang mengakibatkan berkurangnya kadar alkohol. Fermentasi haruslah dalam keadaan anaerob sehingga biomassa tidak bertambah tetapi mengkonversi glukosa menjadi etanol. Penurunan kadar etanol dapat juga diakibatkan karena berubahnya alkohol menjadi senyawa lain (senyawa asam).
Pada penelitian ini juga dilakukan uji sampling berdasarkan jumlah sel khamir untuk mengetahui apakah jumlah ragi roti yang digunakan sudah mencukupi untuk proses fermentasi. Jumlah sel khamir ragi roti pada 1 jam fermentasi diperoleh sebesar 1,4 x 107 sel/mg. Hasil yang diperoleh ini menunjukkan bahwa jumlah ragi roti yang digunakan sudah mencukupi untuk fermentasi. Hal ini didukung oleh penelitian Elevri dan Surya (2006), 1 jam fermentasi pada kurva pertumbuhan sel S.cerevisiae, diperoleh jumlah sel khamir sebesar 1,1 x 107 sel/ml.
28
menyebabkan glukosa dapat terkonversi dengan maksimal dan mulai terbentuknya produk.
Glukosa dimanfaatkan untuk metabolisme oleh mikroba dengan mengeluarkan hasil samping berupa alkohol dan karbon dioksida. Ditunjukkan dalam reaksi berikut ini :
(C6H12O6)n 2 C2H5OH + 2 CO2
(glukosa) yeast (ragi) (etanol)
Ragi roti mengandung nutrisi tambahan (additive nutrition) yang menunjang viabilitas sel S. cerevisiae yang diawetkan dalam kemasan. Sumber karbohidrat dalam bentuk monosakarida (sukrosa, fruktosa, dan glukosa) di dalam ragi roti berfungsi sebagai agen nutrisi untuk pertumbuhan. Sodium karbonat untuk kontrol pH, dan vitamin B sebagai pembawa gugus asetaldehida (Reed, 1991).
29
dihasilkan melebihi 15% maka etanol akan merusak dinding sel dan membekukan plasma sehingga mikroorganisme mati.
Bioetanol merupakan salah satu alternatif bahan bakar nonfosil bagi kendaraan bermotor. Sumber bahan baku bioetanol merupakan limbah pertanian yang tidak bernilai ekonomis dan berasal dari hasil pertanian budidaya yang dapat diperoleh dengan mudah. Oleh karena itu, biaya produksi bioetanol cenderung lebih rendah daripada BBM. Hal yang terpenting dalam penggunaan bioetanol sebagai bahan bakar adalah penghematan sumber daya alam tak terbarui yang semakin lama semakin menipis cadangannya di bumi. Keuntungan penggunaan bioetanol sebagai bahan bakar adalah meningkatkan efisiensi dan emisi gas buang yang lebih ramah lingkungan. Selain itu, penggunaan bioetanol yang bersumber dari limbah serta produk pertanian membuka peluang bagi para petani.
Interaksi etanol dengan hidrogen bisa dimanfaatkan sebagai sumber energi fuel cell ataupun pada mesin pembakaran dalam (internal combustion engine) konvensional (Endah dkk., 2009). Bioetanol dapat digunakan sebagai pengganti bahan bakar minyak (BBM) tergantung dari tingkat kemurniannya. Bioetanol dengan kadar 95-99% dapat dipakai sebagai bahan substitusi premium (bensin), sedangkan kadar 40% dipakai sebagai bahan substitusi minyak tanah (Bustaman, 2008).
30
(gasohol) (Endah dkk., 2007). Penambahan beberapa persen etanol dalam air akan menurunkan tegangan permukaan air secara drastis. Campuran etanol dengan air yang lebih dari 50% etanol bersifat mudah terbakar dan mudah menyala (Sukandar, 2009).
31 BAB V
KESIMPULAN DAN SARAN
A. KESIMPULAN
1. Pada proses hidrolisis oleh enzim α-amilase, suhu hidrolisis 900C dan pH 5,6 menghasilkan gula reduksi paling tinggi yaitu 1,161 mg/ml.
2. Konsentrasi ragi roti 1,5 mg (suhu hidrolisis 700C dan pH 5,6) menghasilkan kadar etanol tertinggi yaitu sebesar 2,84%.
B. SARAN
1. Kebutuhan akan etanol semakin besar karena itu perlu penelitian lebih lanjut yang
berkaitan dengan bioetanol pada substrat yang berbeda.
2. Dilakukan penelitian lebih lanjut mengenai penambahan konsentrasi ragi roti untuk