BAB 2
TINJAUAN PUSTAKA
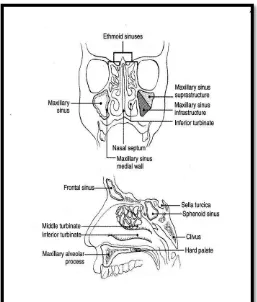
2.1 Anatomi Sinus Paranasal
Sinus frontal, maksila dan etmoid anterior merupakan kelompok sinus paranasal bagian anterior. Ketiga sinus ini bermuara pada meatus media. Sedangkan sel-sel etmoid posterior dan sinus sfenoid merupakan kelompok sinus paranasal bagian posterior. Sinus etmoid posterior dan sinus sfenoid bermuara ke meatus superior (Barnes,2005;Soetjipto 2007;Leung,2014).
2.1.1 Sinus maksila
Sinus maksila merupakan sinus paranasal terbesar. Pada saat lahir rongga sinus maksila berbentuk tabung dengan ukuran 7 x 4 x 4 mm, ukuran posterior lebih panjang daripada anterior, sedangkan ukuran tinggi dan lebar hampir sama panjang. Pada usia 10-12 tahun dasar sinus maksila telah mencapai tinggi yang sama dengan dasar kavum nasi. Diatas umur 12 tahun pertumbuhan sinus maksila ke arah inferior, berhubungan erat dengan erupsi gigi permanen, sehingga ruang yang semula ditempati oleh tugas-tugas gigi permanen akan mengalami pneumatisasi yang mengakibatkan volume sinus maksila bertambah besar kearah inferior (Ballenger,1994; Leung,2014).
oleh dinding lateral rongga hidung. Dinding superior dibentuk oleh dasar orbita dan dinding inferior oleh prosesus alveolaris dan palatum (Ballenger, 1994; Leung,2014).
Dasar sinus maksila berdekatan dengan tempat tumbuhnya gigi premolar kedua, gigi molar ke satu dan ke dua, bahkan kadang-kadang gigi tumbuh ke dalam rongga sinus dan hanya tertutup oleh mukosa.Proses supuratif yang terjadi sekitar gigi-gigi ini dapat menjalar ke mukosa sinus melalui pembuluh darah atau limfe, sedangkan pencabutan gigi ini dapat menimbulkan hubungan dengan rongga sinus melalui fistel
oroantral yang akan mengakibatkan sinusitis (Ballenger,1994;
Leung,2014). 2.1.2 Sinus frontal
Sinus frontal mulai berkembang sepanjang bulan keempat masa kehamilan yang merupakan suatu perluasan ke arah atas dari sel etmoidal anterosuperior. Sinus frontal jarang tampak pada pemeriksaan foto polos sebelum umur 5 atau 6 tahun, setelah itu pelan-pelan tumbuh, total volume 6-7 ml. Sinus frontal mengalirkan sekretnya ke dalam resesus frontalis (Ballenger,1994).
2.1.3 Sinus etmoid
2.1.4 Sinus sfenoid
Sinus sphenoid mulai tumbuh sepanjang bulan keempat masa
kehamilan yang merupakan invaginasi mukosa dari bagian
superoposterior rongga hidung. Sinus ini berupa suatu takikan kecil di dalam os sphenoid sampai umur 3 tahun ketika pneumatisasi mulai lebih lanjut. Pertumbuhan cepat untuk menjangkau tingkatan sella tursica pada umur 7 tahun dan menjadi ukuran orang dewasa setelah berumur 18 tahun, total volume 7,5 ml. Sinus sphenoid mengalirkan sekretnya ke dalam meatus superior bersama dengan etmoid posterior (Ballenger, 1994; Leung,2014).
2.2 Epidemiologi
Tumor sinus paranasal dijumpai sekitar 3% dari seluruh tumor kepala dan leher, dan 1% dari seluruh tumor ganas di tubuh. Dengan insidensi pada pria 2:1 dibandingkan pada wanita. Dimana 60% tumor sinonasal berkembang didalam sinus maksilaris, 20-30% didalam rongga nasal,10-15% didalam sinus ethmoidalis, dan 1% didalam sinus sfenoidalis dan frontalis. Apabila hanya melibatkan sinus-sinus paranasal tersendiri, 77% tumor maligna muncul didalam sinus maksilaris, 22% didalam sinus ethmoidalis dan 1% didalam sinus sfenoidalis dan frontalis. Neoplasma maligna pada tempat-tempat ini dapat mengakibatkan kematian dan kecacatan dalam jumlah yang signifikan ( Barnes,2005; Roezin,2007).
Di India, tumor ganas dan sinus paranasal berkisar sekitar 0,44% dari seluruh tumor ganas (0,57% pada pria dan 0,44% pada wanita). Paling banyak ditemukan pada sinus maksilaris dan diikuti pada sinus etmoidalis, sinus frontal sinus sfenoidalis (Dingra, 2010).
Insidensi tertinggi keganasan sinonasal ditemukan di Jepang yaitu 2 sampai 3,6 per100.000 penduduk pertahun. Di Departemen THT FKUI RSCM Jakarta keganasan ini ditemukan 10-15% dari seluruh tumor ganas THT( Roezin,2007).
Di Departemen THT-KL FK USU/RSUP.HAM Medan, kasus tumor ganas sinonasal pada periode bulan januari 2005 hingga bulan desember 2009 terdapat 51 kasus tumor ganas sinonasal, sebagian besar ditemukan 44 kasus (86,3%) pada stadium lanjut (Salim,2010).
2.3 Etiologi
Alkohol, asap rokok, makanan yang diasinkan atau diasap diduga meningkatkan kemungkinan terjadi keganasan, sebaliknya buah-buahan dan sayuran mengurangi keganasan ( Roezin,2007; Dingra, 2010).
Lebih dari 80% tumor ganas adalah karsinoma sel skuamosa. sisanya adalah adenokarsinoma, adenoid kistik karsinoma, melanoma dan berbagai jenis sarkoma. Karsinoma sel skuamous merupakan tumor sinonasal yang terbanyak. Dilaporkan pada pria kulit putih dengan umur dekade 5-6. Prognosis berhubungan dengan luas dan letak tumor (Roezin,2007; Dingra, 2010).
Adenokarsinoma sebanyak 10-20% dari seluruh tumor sinonasal. Awalnya kebanyakan di sinus etmoid dan rongga hidung, dihubungkan dengan paparan serbuk kayu (Roezin,2007; Leivo,2007;Dingra, 2010). Karsinoma kistik adenoid pada sinonasal sebanyak 14-20% dari seluruh karsinoma kistik adenoid di kepala dan leher. Karakteristiknya adalah perluasan yang cepat ke struktur neurovaskular, submukosa dan didiagnosa pertama kali pada stadium yang sudah lanjut (Roezin,2007; Dingra, 2010).
Melanoma pada sinonasal bisa berupa primer maupun metastase. Walaupun 20% dari melanoma yang ada di kepala dan leher, kurang dari 1% timbul dari sinonasal. Kebanyakan pada rongga hidung, kemudian di sinus maksilaris, etmoid, dan frontal (Roezin,2007; Dingra, 2010).
Sarkoma neurogenik jarang di kepala dan leher dan umumnya berhubungan denga neurofibromatosis. Sifatnya agresif dan sering muncul dengan metastase jauh ( Dingra, 2010;Leung,2014).
2.4 Gejala Klinis
penyakit. Gejala orbital, seperti diplopia, proptosis, hilang penglihatan dan epipora, dapat timbul dengan adanya invasi atau ekspansi ke mata. Memasuki dasar tengkorak hingga fossa kranial anterior menimbulkan nyeri kepala, neuropati kranial, bahkan sindrom lobus frontalis. Tumor juga bisa menembus maksila dan timbul massa di palatum (Roezin,2007;Lalwani,2008;Dingra,2010).
2.5Diagnosis
Diagnosis ditegakkan berdasarkan anamnesis, pemeriksaan fisik dan pemeriksaan penunjang, diagnosis pasti ditegakkan berdasarkan pemeriksaan histopatologi (Roezin,2007;Lalwani,2008; Dingra,2010). 2.5.1 Anamnesis
Penting untuk dilakukan anamnesis yang teliti, biasanya perlu ditanyakan apakah ada obstruksi hidung, hidung berdarah, diplopia, pasien mengeluh apakah gigi palsunya tidak pas lagi atau gigi geligi goyah (Ballenger,1994;Roezin,2007).
2.5.2 Pemeriksaan fisik
2.5.3 Pemeriksaan radiologi
Pemeriksaan radiologi merupakan bagian sangat penting pada diagnosis, staging dan follow up keganasan sinonasal. Foto polos berfungsi sebagai diagnosis awal, terutama jika ada erosi tulang dan perselubungan padat unilateral, harus dicurigai keganasan. CT scan merupakan sarana terbaik karena lebih jelas memperlihatkan tumor dan destruksi tulang. MRI dapat membedakan jaringan tumor dari jaringan normal tetapi kurang baik dalam memperlihatkan destruksi tulang (Roezin,2007;Ziemmer,2014).
Pemeriksaan dengan Positron emission tomography (PET) digunakan untuk staging dan mengamati tumor ganas pada leher dan kepala. Kombinasi PET dan CT scan menunjukkan secara detail anatomi serta perluasan dari tumor dan membantu dalam rencana pembedahan. Angiography dengan carotid flow study digunakan untuk pasien yang akan menjalani operasi dengan tumor yang berada disekeliling arteri carotis atau dapat juga digunakan untuk mendapatkan batas tumor dengan jelas. Foto polos paru diperlukan untuk melihat adanya metastase tumor secara hematogen seperti sarkoma, melanoma dan adenoid kistik karsinoma. Evaluasi metastase penting bila akan melakukan reseksi secara luas. Apabila tumor telah meluas ke meningen atau otak dapat dilakukan
pemeriksaan lumbal dan brain puncture serta spine imaging
(Roezin,2007;Ziemmer,2014).
2.5.4 Pemeriksaan histopatologi
dilakukan. Biopsi tumor maksila, dapat dilakukan melalui tindakan sinoskopi atau melalui operasi Caldwell-Luc yang insisinya melalui sulkus gingivo-bukal. Jika dicurigai tumor vaskuler, misalnya hemangioma atau angiofibroma, jangan dilakukan biopsi karena akan sangat sulit menghentikan perdarahan yang terjadi (Roezin,2007; Ziemmer,2014).
2.6 Klasifikasi TNM dan Stadium
Stadium tumor ganas sinonasal menurut American Joint Committee on Cancer (AJCC) tahun 2010 yaitu: (NCCN 2010)
Tumor Primer (T)
Tx : Tumor primer tidak bisa ditentukan TO : Tidak tampak tumor primer
Tis : Karsinoma insitu
2.6.1 Sinus maksilaris
T1 : Tumor terbatas pada mukosa sinus maksilaris tanpa erosi dan destruksi tulang
T2 : Tumor menyebabkan erosi atau destruksi tulang hingga palatum atau meatusmedia tanpa melibatkan dinding posterior sinus maksilaris,jaringan subkutaneus. T3 : Tumor menginvasi dinding posterior tulang sinus maksilaris, subkutaneus jaringan dinding dasar dan medial orbita, fossa pteriogoid,sinus etmoidalis.
T4a :Tumor menginvasi bagian anterior orbita, kulit pipi, fossa pterigoid, fossa infra temporal,fossa kribriformi, sinus sphenoidalis atau frontal.
2.6.2 Kavum nasi dan sinus etmoidalis
T1 : Tumor terbatas pada salah satu bagian dengan atau tanpa invasi tulang
T2 : Tumor berada didua bagian dalam satu region atau tumor meluas dan melibatkan daerah nasoetmoidal kompleks, dengan atau tanpa invasi tulang. fossa kranial medial, Nervus kranialis selain dari V2,nasofaring atau klivus.
Kelenjar getah bening regional (N)
Nx : Pembesaran kelenjar limfe regional tidak dapat ditentukan NO : Tidak ada metastasis kekelenjar limfe regional
N1 : Metastasis kelenjar limfe ipsilateral diameter ≤ 3 cm
N2 : Metastasis tunggal kelenjar limfe ipsilateral diameter 3-6 cm, atau 6cm multipel kelenjar limfe ipsilateral < 6 cm atau metastasis bilateral atau kontralateral diameter ≤ 6 cm
2.6.3 Stadium karsinoma sinus maksila dan sinus ethmoid (NCCN 2010)
Stadium I T1 N0 M0
Stadium II T2a N0 M0
Stadium III T3 N0 M0
T1 N1 M0
T2 N1 M0
T3 N1 M0
Stadium IV T4a N0 M0
T4a N1 M0
T1 N2 M0
T2 N2 M0 T3 N2 M0
T4a N2 M0
Stadium IVB Semua T N3 M0
T4a Setiap N M0
Stadium IVC Semua T Semua N M1 2.7 Penatalaksanaan
Penatalaksanaan dari tumor sinus paranasal ialah pembedahan atau lebih sering bersama dengan modalitas terapi lainnya seperti terapi radiasi dan kemoterapi sebagai adjuvant, dimana sampai saat ini masih merupakan pengobatan utama untuk keganasan hidung dan sinus
paranasal, penyakit stadium lanjut jika diobati, membutuhkan
pasien yang diobati dengan radioterapi saja adalah 49%. Kemoterapi sebagai tambahan radioterapi dan pembedahan telah menunjukkan peningkatan hasil pengobatan pada satadium III/IV (Roezin,2007;Glesson, 2008).
Pembedahan masih diiindikasikan walaupun menyebabkan
morbiditas yang tinggi bila terbukti dapat mengangkat tumor secara lengkap. Pembedahan dikontraindikasikan pada kasus yang telah bermetastasis jauh, sudah meluas kesinus kavernosus bilateral atau tumor sudah mengenai kedua orbita. Untuk tumor ganas, tindakan operasi seradikal mungkin. Biasanya dilakukan maksilektomi, dapat berupa maksilektomi medial, total atau radikal (Roezin,2007;Glesson,2008).
Maksilektomi radikal dilakukan pada tumor yang sudah mengenai seluruh dinding sinus maksila dan sering juga masuk kerongga orbita, sehingga pengangkatan maksila dilakukan secara en bloc disertai eksenterasi orbita. Jika tumor sudah masuk kerongga intrakranial dilakukan reseksi kraniofasial atau kalau perlu kraniotomi, tindakan dilakukan dalam tim bersama dokter bedah saraf (Roezin,2007).
Penatalaksanaan setelah operasi adalah rehabilitasi yang bertujuan untuk penyembuhan luka primer, memelihara atau rekonstruksi bentuk wajah dan pemulihan oronasal yang terpisah kemudian memperlancar proses bicara dan menelan. Rehabilitasi setelah reseksi pembedahan dapat dicapai dengan dental prosthesis atau reconstructive flap seperti flap otot temporalis dengan atau tanpa inklusi tulang kranial, pedicled atau microvascular free mycutaneous dan cutaneous flap (Ziemer,2014).
banyak lagi faktor lain yang dapat berpengaruh terhadap agresifitas penyakit dan hasil pengobatan yang tentunya berpengaruh juga terhadap prognosis penyakit ini. Walaupun demikian pengobatan yang agresif secara multimodalitas akan memberikan hasil yang terbaik dalam mengontrol tumor primer dan akan meningkatkan angka bertahan hidup selama 5 tahun sebesar 75% untuk seluruh stadium tumor (Roezin,2007 ).
2.8 Karsinoma Sel Skuamosa
Karsinoma sel skuamosa (SCC) merupakan bagian dari tumor sinonasal yang berasal dari epitelium mukosa kavum nasi atau sinus paranasal dimana etiologinya berhubungan dengan faktor lingkungan, merokok, alkohol dan terpapar dengan bidang industri seperti nikel,kromium dan debu kayu termasuk tipe keratinizing dan non keratinizing( Barnes,2005;Thompson,2006).
Enam puluh persen tumor sinonasal berkembang di dalam sinus maksilaris, diikuti didalam kavum nasi 22%, di dalam sinus etmoidalis 15%, dan <3% dijumpai dalam sinus sfenoidalis dan frontalis. Dengan mayoritas dijumpai SCC dan variannya (55%), diikuti oleh non-epithelial neoplasms(20%), glandular tumours (15%), undifferentiated carcinoma (7%) dan miscellneous tumours (3%). (Dhingra, 2008;Thompson 2006).
Secara makroskopik, KSS kemungkinan berupa exophytic,
fungating atau papiler. Biasanya rapuh, mudah berdarah, terutama berupa nekrotik, atau indurated, demarcated atau infiltratif (Barnes, 2005).
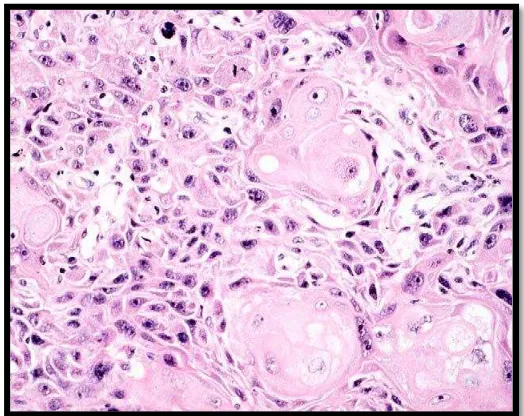
2.8.1 Mikroskopik keratinizing squamous cell carcinoma
Gambar 2.2 Karsinoma sel skuamosa, keratinizing Pulau-pulau sel-sel
tumor dengan invasi yang tidak beraturan
(Thompson,2006).
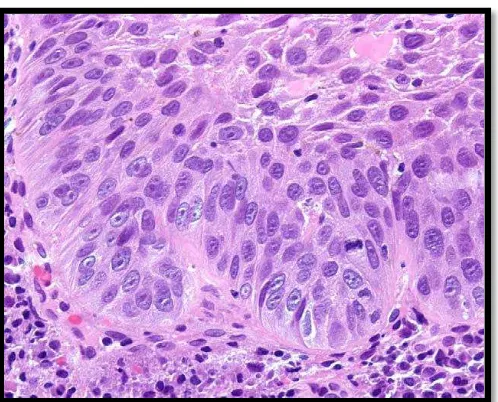
2.8.2 Mikroskopik non-keratinizing (cylindrical cell, transitional) carcinoma
Gambar 2.3 Karsinoma sel skuamosa, non-keratinizing. Pulau-pulau sel-sel tumor kohesif menginvasi ke dalam stroma dibawahnya (Thompson,2006).
2.9 Protein p53
Gen p53 dijumpai pertama kali pada tahun 1979 sebagai
transformation-related protein53 yang pada manusia terletak pada lengan pendek kromosom 17, terentang sepanjang 2,8 kb mRNA, terdiri atas 11 ekson dan diekspresikan pada hampir semua jaringan tubuh, p53 merupakan bagian dari gen supresor tumor, dimana fungsi dari p53 adalah untuk menghambat siklus sel, diferensiasi ,apoptosis penuaan sel dan angiogenesis (Fearon,2000;Macdonal,2004;Bai,2006).
Dalam keadaan sehat protein p53 secara terus menerus diproduksi dan didegradasi.Jika gen p53 mengalami kerusakan, misalnya akibat mutagen (kimia, radiasi dan virus), maka fungsi sebagai supresor akan berkurang, sehingga terjadi pembelahan yang tidak terkontrol. Pada keganasan sel, gen p53 adalah gen yang paling banyak bermutasi (ditemukan >50% dari seluruh kasus kanker) Waktu paruh p53 wild type kurang dari 30 menit dan merupakan protein yang labil dan terdiri atas region yang tidak terstruktur sedangkan p53 mutan mempunyai waktu paruh lebih panjang sehingga dapat terdeteksi dengan pulasan imunohistokimia (Handayani, 2011).
Wild-typep53 protein berisi 393 asam amino dan terdiri dari domain struktur dan fungsional, dimana gen p53 homolog dengan p63 dan p73 yang memiliki domain struktur yang sama dan termasuk domain oligomerisasi dan ketiga protein ini dapat menginduksi apoptosis. Kerusakan DNA yang mengarah untuk penggandaan DNA, ATM (Ataxia Telangiectasia Mutasi), protein kinase serta CHK2 kinase diaktifkan kemudian p53 difosforilasi kelokasi yang berbeda yang mengarah ke siklus dependent, dimana kerusakan DNA menyebabkan penghambatan replikasi sehingga ATR (ATM dan Rad3-related) kinase menjadi aktif akibatnya ATR dan Chk 1 phosphorylate diaktifkan dan p53 menjadi aktif (Bai,2006).
Peran utama p53 sebagai tumor suppressor gen adalah kemampuannya untuk mentranskripsi urutan spesifik, mengatur ekspresi gen seluler yang berbeda. Target p53 downstrem adalah mengaktifkan jenis sel yang berbeda, tingkat kerusakan yang mempengaruhi aktivitas p53 dan berbagai variasi parameter lainnya yang belum teridentifikasi (Handayani, 2011).
Pasien yang resisten terhadap obat memperlihatkan ekspresi p53 mutan lebih tinggi dibanding pasien yang responsif terhadap obat, sehingga ada indikasi bahwa adanya p53 mutan dapat mempengaruhi resistensi terhadap obat dibanding dengan petanda-petanda lain. Penelitian lain menyatakan bahwa mutasi p53 berhubungan dengan
perbedaan staging, tetapi tidak signifikan untuk prognostik
(Handayani,2011).
Ada dua jenis bentuk stres seluler yang dapat mengaktivasi p53 yaitu:
1. Kerusakan DNA, yang dapat disebabkan oleh ionisasi radiasi, obat-obatan kemoterapi, sinar ultraviolet atau inhibitor protein kinase, protein checkpoints yang memberikan sinyal pada p53 bahwa kerusakan telah terjadi dan siklus sel harus dihentikan sampai DNA diperbaiki oleh protein kinase.
2. Deregulasi ekspresi onkogen, dimana terjadi kegagalan mekanisme untuk mengeliminasi sel yang mengalami proliferasi abnormal.
Protein onkogen akan berinteraksi dengan MDM2 dan
menghambat aktifitas MDM2 tersebut sehingga kadar p53
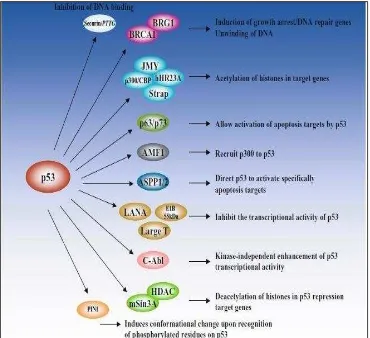
Gambar 2.4 skema protein p53 ( Zanbeeti,2005).
Respon p53 yang teraktivasi terdiri dari dua yaitu:
1. Inhibisi siklus sel
2. Apoptosis
Merupakan suatu proses aktif yang memerlukan induksi ekspresi gen. Sel limfoid dan sel myeloid dengan cepat mengalami apoptosis setelah mengalami kemoterapi atau radiasi, tetapi pada jenis sel lain diperlukan ekspresi gen-gen lain untuk membantu apoptosis, diantaranya bcl2 dan bax, dimana bax merupakan gen proapoptotik yang pertama diidentifikasikan sebagai target dari p53, dan dikuti oleh gen yang lainnya seperti NOXA, PUMA dan p53AIPI. Produk protein yang dihasilkan oleh gen-gen ini berada
pada mitokondria dan menyebabkan hilangnya potensial
membrane dan pelepasan sitokrom C. Integritas mitokondria juga dapat terganggu oleh gen yang disebut dengan p53-inducible genes (PIG). P53 juga terlibat dalam death receptor-induced pathway dan ekspresi dari paling sedikit dua resptor seperti FAS/APO1 dan DR5/KILLER yang diinduksi oleh p53. Menurunnya ketahanan protein oleh karena tertekannya gen antiapoptosis seperti BCL2 yang diinduksi oleh p53 juga berperan penting untuk terjadinya apoptosis (Macdonal,2004;Kresno,2011;Shahib,2012).
2.9.1 Peran p53 pada apoptosis
Tumor protein p53 memegang peranan penting dalam mengatur proses dalam sel sebagai respon terhadap berbagai stress, baik genotoksik (perubahan DNA akibat iradiasi, UV, karsinogen, obat sitotoksik) maupun non-genotoksik (hipoksia, deplesia nukleitida, aktivasi okogen, disrupsi mikrotubuli,gangguan kontak antar sel). Protein p53 dapat dipandang sebagai tanda adanya sinyal stress yang kemudian ditransduksi melalui kemampuan p53 untuk bertindak sebagai faktor transkripsi (Kresno,2011).
Gen p53 juga menghasilan 53-kDa fosforotein nuclear yang berlokasi pada kromosom 17p dan memiliki peranan penting dalam pertumbuhan sel. p53 dengan p73 dan p63 merupakan bagian dari family dariTSGs, dimana gen p53 ini berperan sebagai transkripsi beberapa target gen, mengendalikan perjalanan siklus sel, sebagai kontrol checkpoint pada G1, dan meregulasi perbaikan DNA, apoptosis dan diferensiasi (Scully,2003).
Hilangnya 17p13 terjadi pada hampir 60% pada kasus squamous cell carcinoma (SCC). Perubahan gen p53 oleh karena kehilangan alel, point mutation, delesi dan inaktifasi mengganggu perannya sebagai Guardian of the Genome dengan cara menurunkan kemampuan sel untuk memperbaiki DNA dan mengalami apoptosis sebagai respon terhadap kerusakan DNA tersebut sehingga menyebabkan instabilitas genomik. Sebuah penelitian mengenai tumor-tumor invasif, mutasi p53 terjadi
sebanyak 40-50% dan lebih banyak ditemukan pada penderita squamous
2.9.2 Ekspresi p53 mutan pada karsinoma sel skuamosa sinonasal
Gangguan fungsi p53 yang terjadi pada tumor disebabkan oleh mutasi gen p53 itu sendiri maupun mutasi gen yang mengatur p53. Mutasi dari protein p53 dapat dijumpai hampir 50% dari kanker. Sedangkan pada kanker mulut dan kanker kepala dan leher dijumpai hampir dua-pertiga (dari 12-100%) yang disebabkan mutasi dari p53. Di Negara barat, overekspresi skuamous sel karsinoma pada kepala dan leher dikatakan berhubungan dengan komsumsi alkohol dan tembakau. Beberapa penelitian juga menunjukkan adanya mutasi p53 pada perokok atau mantan perokok (Scully,2003).
Poeta dalam penelitian di Inggris menyatakan bahwa p53 mutan dapat digunakan sebagai faktor stratifikasi dalam prospektif uji klinis khususnya pada karsinoma sel skuamosa (Poeta,2007).
Ekspresi p53 lebih tinggi pada jaringan maligna dibandingkan dengan jaringan normal, dan karsinoma diferensiasi jelek menunjukkan jumlah sel p53 positif lebih banyak dengan karsinoma diferensiasi baik. P53 kuat terekspresi pada karsinoma sel skuamosa, tetapi negatif pada smallcellcarcinoma dan adenokarsinoma ( Scully,2003;Oncel,2011).
2.10 Kerangka Konsep
Z
Gambar 2.5 Skema kerangka konsep Zat hasil industri
(industrial Fumos)
Paparan karsinogen lingkungan
Infeksi bakteri dan inflamasi
Mutasi gen supressor p53
Protein p53 mutan Pasien Ca