UJI EFEK KOMBINASI EKSTRAK ETANOL KULIT KAYU
MANIS ((Cinnamomum burmannii (Nees & T.Nees) Blume))
DAN MADU TERHADAP PENURUNAN KADAR
GLUKOSA DARAH TIKUS JANTAN
SKRIPSI
OLEH: YOLIN HARTIKA
NIM 111524052
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI EFEK KOMBINASI EKSTRAK ETANOL KULIT KAYU
MANIS ((Cinnamomum burmannii (Nees & T.Nees) Blume))
DAN MADU TERHADAP PENURUNAN KADAR
GLUKOSA DARAH TIKUS JANTAN
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: YOLIN HARTIKA
NIM 111524052
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI EFEK KOMBINASI EKSTRAK ETANOL KULIT KAYU
MANIS ((Cinnamomum burmannii (Nees & T.Nees) Blume))
DAN MADU TERHADAP PENURUNAN KADAR
GLUKOSA DARAH TIKUS JANTAN
OLEH: YOLIN HARTIKA
NIM 111524052
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: 21 Desember 2013
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa yang telah melimpahkan
rahmat dan anugerah-Nya sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini yang berjudul “Uji Efek Kombinasi Ekstrak Etanol
Ku-lit Kayu Manis ((Cinnamomum burmannii (Nees & T.Nees) Blume)) dan Madu
Terhadap Penurunan Kadar Glukosa Darah Tikus Jantan”. Skripsi ini diajukan
sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi Universitas
Sumatera Utara.
Penulis menyampaikan terimakasih kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU yang telah
memberi-kan bantuan dan fasilitas selama masa pendidimemberi-kan. Bapak Prof. Dr. Urip
Hara-hap, Apt., dan Ibu Marianne, S.Si., M.Si., Apt., yang telah membimbing
penu-lis dengan penuh kesabaran, tulus dan ikhlas selama penelitian hingga
sele-sainya penulisan skripsi ini. Bapak Ginda Haro, M.Sc., Ph.D., Apt., selaku
do-sen wali yang telah membimbing penulis selama masa pendidikan. Ibu Prof.
Dr. Rosidah, M.Si., Apt., Bapak Drs. Saiful Bahri, M S., Apt., dan Ibu Poppy
Anjelisa Z. Hasibuan, S.Si., M.Si., Apt., sebagai dosen penguji yang telah
memberikan saran dan kritikan kepada penulis hingga selesainya penulisan
skripsi ini. Ibu Marianne, S.Si., M.Si., Apt., selaku kepala Laboratorium
Far-makologi dan Toksikologi dan Ibu Dra. Suwarti Aris, M.Si., Apt., selaku
Kepa-la Laboratorium Farmakognosi yang teKepa-lah memberika fasilititas dan bantuan
Ucapan terimakasih dan penghargaan yang tulus tiada terhingga kepada
Ayah Drs. Demmu Karo-karo, M.Pd., dan Ibu Suhartinah Pinem tercinta serta
Abang Niko Efrada, SE atas doa, dorongan dan semangat baik moril maupun
materil kepada penulis selama perkuliahan hingga selesainya penyusunan
skripsi ini. Kepada seluruh Staf Pengajar, Pegawai Tata Usaha dan
sahabat-sahabat (Irawinata Situmorang, Fery Nelsa Siahaan, Maria Susanti Manalu,
Novalya Frisley, dan Tri Ika Sinaga) yang telah membantu selama penelitian
hingga selesainya penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih
me-miliki banyak kekurangan, olehkarena itu sangat diharapkan kritikan dan saran
yang menyempurnakan skripsi ini.
Medan, Desember 2013
Penulis
Uji Efek Kombinasi Ekstrak Etanol Kulit Kayu Manis ((Cinnamomum burmannii (Nees & T.Nees) Blume)) dan Madu
Terhadap Penurunan Kadar Glukosa Darah Tikus Jantan ABSTRAK
Semua orang dapat mengidap diabetes melitus. Oleh karena itu, banyak penderita berusaha mengendalikan kadar glukosa darahnya menggunakan ba-han alam seperti kayu manis dan madu karena lebih murah dan mudah dipero-leh. Tujuan penelitian ini adalah mengetahui karakteristik simplisia, kandungan metabolit sekunder, dan efek kombinasi ekstrak etanol kayu manis-madu seba-gai penurunan kadar glukosa darah (KGD) dengan metode uji toleransi gluko-sa.
Penelitian ini meliputi karakterisasi dan skrining fitokimia simplisia dan ekstrak, pengujian pada hewan dan pengukuran KGD dengan metode uji tole-ransi glukosa. Pada uji toletole-ransi glukosa, hewan uji dibagi dalam 9 kelompok perlakuan yaitu kelompok suspensi Na-CMC 1% bb; kelompok uji EEKKM dengan dosis 50; 100; dan 200 mg/kg bb; Madu 0,75; 1,5; 3 ml/kg bb; kombi-nasi EEKKM dan Madu (50 mg/kg bb dan 0,75 ml/kg bb) dan kelompok gli-benklamid dosis 0,45 mg/kg bb.
Hasil makroskopik kulit kayu manis yaitu: menggulung membujur, berwarna coklat kemerahan, dan berbau khas aromatik. Hasil mikroskopik simplisia kulit kayu manis adalah sklerenkim dan sel minyak, sel batu, serabut sklerenkim dan hablur kalsium oksalat. Hasil penetapan kadar air kulit kayu manis 7,98%; kadar sari larut air 6,39%; kadar sari larut etanol 22,15%; kadar abu total 3,25%; dan kadar abu tidak larut asam 0,31%. Hasil skrining kulit kayu manis menunjukkan flavonoid, glikosida, saponin, dan tanin. Hasil ma-kroskopik madu berupa cairan kental menyerupai sirup, berwarna coklat keme-rahan, memiliki bau dan rasa yang khas. Hasil mikroskopik madu adalah ser-buk sari. Hasil penetapan kadar madu terhadap kadar air 27,94%; kadar sari larut air 17,79%; kadar sari larut etanol 5,93%; kadar abu total 0%; dan kadar abu tidak larut asam 0%. Hasil skrining madu yaitu flavonoid dan glikosida.
Hasil analisis ANAVA menunjukkan bahwa pemberian EEKKM dosis 50; 100; dan 200 mg/kg bb, Madu 0,75; 1,5; dan 3 ml/kg bb memberikan penu-runkan KGD yang berbeda bermakna dengan kelompok kontrol dan gliben-klamid dan kombinasi EEKKM dan Madu (50 mg/kg bb dan 0,75 ml/kg bb) berbeda bermakna dengan kelompok kontrol dan tidak memberikan perbedaan yang nyata dengan glibenklamid dosis 0,45 mg/kg bb (p < 0,05).
Berdasarkan hasil di atas, dapat disimpulkan bahwa EEKKM dosis 50; 100; 200 mg/kg bb; Madu 0,75; 1,5; 3 ml/kg bb mampu menurunkan KGD dan kombinasi EEKKM dan Madu mampu menurunkan KGD secara sinergis dan lebih baik jika dibandingkan dengan masing-masing kelompok EEKKM 50 mg/kg bb maupun madu 0,75 ml/kg bb dengan metode uji toleransi glukosa.
Effect of Ethanol Extract of Cinnamon Cortex
((Cinnamomum burmannii (Nees & T.Nees) Blume)) and Honey Combina-tion in Decreasing Blood Glucose Levels in Male Rats
ABSTRACT
Everyone can ail from diabetes mellitus. Therefore, many patient try to control their blood glucose level with natural products such as cinnamon and honey because they are cheaper and can be obtained easily. The objective of this research is to understand the characterization of symplicia, second metabo-lites content, and the effect combination of ethanol extract of cinnamon-honey in decreasing blood glucose level using glucose tolerance test method.
This research includes the characterization and phytochemical screening of simplicia and extracts, experiment in animals and measurement KGD with methods glucose tolerance test. In glucose tolerance test, male mice divided into group used Na-CMC suspension 1% bw, ethanol extract of cinna-mon cotex (EEKKM) with 50; 100; and 200 mg/kg bw; honey with 0.75; 1.5; and 3 ml/kg bw; combination of ethanol extract of cinnamon and honey (50 mg/kg bw and 0.75 mg/kg bw) and glibenclamide 0.45 mg/kg bw.
Result of cinnamon symplicia macroscopic is stretch roll, reddish-brown colour and aromatic odor. Microscopic of cinnamon showed scleren-chyma and oil cells, stone cells, and free sclerenscleren-chyma. The result of characte-rization in cinnamon symplicia obtained 7.98% water content; 6.39% water-soluble extract content; 22.15% ethanol-water-soluble extract content; 3.25% total ash content; and 0.31% acid-insoluble ash content. Phythochemical screening of cinnamon showed the presence of flavonoids, glycoside, saponins and tan-nins. Result of honey macroscopic is thick liquid, reddish brown colour and has a particular odor and taste. Result of honey microscopic showed pollen. The result of characterization of honey obtained 27.94% water content; 17,79% wa-ter-soluble extract content; 5.93% ethanol-soluble extract content; 0% total ash content and 0% acid-insoluble ash content. Phythochemical screening of honey showed the presence of flavonoids and glycosides.
ANOVA analysis showed ethanol extract of cinnamon (EEKKM) 50; 100; 200 mg/kg bw and honey with 0.75; 1.5 and 3 ml/kg bw gave significant decreasing of blood glucose level compared to control group and glibenclamide group and the combination of ethanol extract of cinnamon and honey (50 mg/kg bw and 0.75 ml/kg bw) gave significant difference results compared to control group but not significant to glibenclamide 0.45 mg/kg bw (p < 0.05).
According to above results, the conclusion is EEKKM with 50; 100; and 200 mg/kg bw; honey 0.75; 1.5; and 3 ml/kg bw can decrease blood glu-cose level and combination of EEKKM and honey can decrease blood gluglu-cose level synergically and it is way better compared to ethanol extract of cinnamon with 50 mg/kg bw and honey 0.75 ml/kg bw.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 5
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 6
1.6 Kerangka Pikir Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 8
2.1 Kayu Manis ... 8
2.1.1 Morfologi Tumbuhan Kayu Manis ... 8
2.1.3 Kandungan Kayu Manis ... 9
2.2 Madu ... 9
2.2.1 Kandungan Madu ... 10
2.3 Ekstrak ... 10
2.4 Metabolisme glukosa ... 12
2.5 Diabetes Melitus ... 14
2.5.1 Klasifikasi diabetes melitus ... 15
2.5.2 Diagnosis diabetes melitus ... 16
2.5.3 Manajemen pengobatan diabetes melitus ... 17
2.5.4 Monitoring diabetes melitus ... 20
BAB III METODE PENELITIAN ... 21
3.1 Alat-alat ... 21
3.2 Bahan-bahan ... 21
3.3 Prosedur Pembuatan Simplisia ... 22
3.3.1 Pengambilan Bahan ... 22
3.3.2 Identifikasi Tumbuhan ... 22
3.3.3 Pembuatan Simplisia ... 22
3.4 Pemeriksaan Karakteristik Simplisia ... 22
3.4.1 Pemeriksaan Makroskopik dan Organoleptik ... 23
3.4.2 Pemeriksaan Mikroskopik ... 23
3.4.3 Penetapan Kadar Air ... 23
3.4.4 Penetapan Kadar Sari Larut dalam Air ... 24
3.4.6 Penetapan Kadar Abu Total ... 25
3.4.7 Penetapan Kadar Abu Tidak Larut dalam Asam ... 25
3.5 Skrining Fitokimia Simplisia ... 26
3.5.1 Pemeriksaan Flavanoid ... 26
3.5.2 Pemeriksaan Alkaloid ... 26
3.5.3 Pemeriksaan Saponin ... 27
3.5.4 Pemeriksaan Tanin ... 27
3.5.5 Pemeriksaan Glikosida ... 27
3.5.6 Pemeriksaan Steroid/Triterpenoid ... 28
3.6 Proses Pembuatan Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 28
3.7 Pemeriksaan Karakteristik EEKKM ... 29
3.8 Skrining Fitokimia EEKKM ... 29
3.9 Penyiapan Hewan Percobaan ... 29
3.10 Pembuatan Pereaksi ... 30
3.10.1 Pembuatan Larutan Glukosa 50% ... 30
3.10.2 Pembuatan Suspensi Na-CMC 0,5% b/v ... 30
3.10.3 Pembuatan Suspensi Glibenklamid Dosis 0,45 mg/kg bb ... 30
3.10.4 Pembuatan Suspensi Ekstrak Etanol Kulit Kayu Manis ... 30
3.11 Pengujian Penurunan Kadar Glukosa Darah EEKKM-Madu 31 3.11.1 Penggunaan Blood Glucose Test Meter “EasyTouch® GCU” ... 31
3.11.3 Pengujian Penurunan KGD EEKKM dan Madu
dengan Metode Toleransi Glukosa ... 32
3.12 Analisis Data ... 33
BAB IV HASIL DAN PEMBAHASAN ... 34
4.1 Karakteristik Simplisia ... 34
4.2 Skrining Fitokimia ... 35
4.3 Hasil Uji Farmakologi ... 36
4.3.1 Hasil Pengujian Efek dengan Metode Uji Toleransi Glukosa ... 36
BAB V KESIMPULAN DAN SARAN ... 47
5.1 Kesimpulan ... 47
5.2 Saran ... 48
DAFTAR PUSTAKA ... 49
DAFTAR TABEL
Halaman
Tabel 2.1 Kategori Status Glukosa ... 17
Tabel 4.1 Hasil Penetapan Kadar Simplisia Kulit Kayu Manis,
Madu, dan Ekstrak Etanol Kayu Manis (EEKKM) ... 35
Tabel 4.2 Hasil Skrining Fitokimia Simplisia Kulit Kayu Manis,
Madu dan Ekstrak Etanol Kayu manis (EEKKM) ... 36
Tabel 4.3 Kadar Glukosa Darah Rata–rata Metode Uji
DAFTAR GAMBAR
Halaman
Gambar 1.1 Skema Kerangka Penelitian ... 7
Gambar 2.1 Pelepasan Insulin Secara Skematis ... 14
DAFTAR LAMPIRAN
Halaman Lampiran 1 Hasil Determinasi Tumbuhan Kulit Kayu
Manis Cinnamomum burmannii (Nees &
T.Nees) Blume . ... 52
Lampiran 7 Perhitungan Hasil Penetapan Kadar Air Serbuk Simplisia Kulit Kayu Manis ... 59
Lampiran 8 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Air Serbuk Simplisia Kulit Kayu Manis ... 60
Lampiran 9 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Etanol Serbuk Simplisia Kulit Kayu Manis .... 61
Lampiran 10 Perhitungan Hasil Penetapan Kadar Abu Total Serbuk Simplisia Kulit Kayu Manis ... 62
Lampiran 11 Perhitungan Hasil Penetapan Kadar Abu Tidak Larut Asam Serbuk Simplisia Kulit Kayu Manis ... 63
Lampiran 12 Perhitungan Hasil Penetapan Kadar Air Simplisia Madu . ... 64
Lampiran 13 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Air Simplisia Madu ... 65
Lampiran 14 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Etanol Simplisia Madu ... 66
Lampiran 15 Perhitungan Hasil Penetapan Kadar Abu Total Simplisia Madu ... 67
Larut Asam Simplisia Madu ... 68
Lampiran 17 Perhitungan Hasil Penetapan Kadar Air Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 69
Lampiran 18 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Air Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 70
Lampiran 19 Perhitungan Hasil Penetapan Kadar Sari Larut dalam Etanol Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 71
Lampiran 20 Perhitungan Hasil Penetapan Kadar Abu Total Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 72
Lampiran 21 Perhitungan Hasil Penetapan Kadar Abu Tidak Larut Asam Ekstrak Etanol Kulit Kayu Manis (EEKKM) ... 73
Lampiran 22 Tabel Maksimum Larutan Sediaan Uji untuk Hewan 74
Lampiran 23 Tabel Konversi Dosis Hewan dengan Manusia ... 75
Lampiran 24 Contoh Perhitungan Dosis ... 76
Lampiran 25 Data Pengukuran KGD Uji Toleransi Glukosa ... 81
Lampiran 26 Tabel hasil uji normalitas data ... 86
Lampiran 27 Tabel hasil analisis statistik ANOVA ... 87
Uji Efek Kombinasi Ekstrak Etanol Kulit Kayu Manis ((Cinnamomum burmannii (Nees & T.Nees) Blume)) dan Madu
Terhadap Penurunan Kadar Glukosa Darah Tikus Jantan ABSTRAK
Semua orang dapat mengidap diabetes melitus. Oleh karena itu, banyak penderita berusaha mengendalikan kadar glukosa darahnya menggunakan ba-han alam seperti kayu manis dan madu karena lebih murah dan mudah dipero-leh. Tujuan penelitian ini adalah mengetahui karakteristik simplisia, kandungan metabolit sekunder, dan efek kombinasi ekstrak etanol kayu manis-madu seba-gai penurunan kadar glukosa darah (KGD) dengan metode uji toleransi gluko-sa.
Penelitian ini meliputi karakterisasi dan skrining fitokimia simplisia dan ekstrak, pengujian pada hewan dan pengukuran KGD dengan metode uji tole-ransi glukosa. Pada uji toletole-ransi glukosa, hewan uji dibagi dalam 9 kelompok perlakuan yaitu kelompok suspensi Na-CMC 1% bb; kelompok uji EEKKM dengan dosis 50; 100; dan 200 mg/kg bb; Madu 0,75; 1,5; 3 ml/kg bb; kombi-nasi EEKKM dan Madu (50 mg/kg bb dan 0,75 ml/kg bb) dan kelompok gli-benklamid dosis 0,45 mg/kg bb.
Hasil makroskopik kulit kayu manis yaitu: menggulung membujur, berwarna coklat kemerahan, dan berbau khas aromatik. Hasil mikroskopik simplisia kulit kayu manis adalah sklerenkim dan sel minyak, sel batu, serabut sklerenkim dan hablur kalsium oksalat. Hasil penetapan kadar air kulit kayu manis 7,98%; kadar sari larut air 6,39%; kadar sari larut etanol 22,15%; kadar abu total 3,25%; dan kadar abu tidak larut asam 0,31%. Hasil skrining kulit kayu manis menunjukkan flavonoid, glikosida, saponin, dan tanin. Hasil ma-kroskopik madu berupa cairan kental menyerupai sirup, berwarna coklat keme-rahan, memiliki bau dan rasa yang khas. Hasil mikroskopik madu adalah ser-buk sari. Hasil penetapan kadar madu terhadap kadar air 27,94%; kadar sari larut air 17,79%; kadar sari larut etanol 5,93%; kadar abu total 0%; dan kadar abu tidak larut asam 0%. Hasil skrining madu yaitu flavonoid dan glikosida.
Hasil analisis ANAVA menunjukkan bahwa pemberian EEKKM dosis 50; 100; dan 200 mg/kg bb, Madu 0,75; 1,5; dan 3 ml/kg bb memberikan penu-runkan KGD yang berbeda bermakna dengan kelompok kontrol dan gliben-klamid dan kombinasi EEKKM dan Madu (50 mg/kg bb dan 0,75 ml/kg bb) berbeda bermakna dengan kelompok kontrol dan tidak memberikan perbedaan yang nyata dengan glibenklamid dosis 0,45 mg/kg bb (p < 0,05).
Berdasarkan hasil di atas, dapat disimpulkan bahwa EEKKM dosis 50; 100; 200 mg/kg bb; Madu 0,75; 1,5; 3 ml/kg bb mampu menurunkan KGD dan kombinasi EEKKM dan Madu mampu menurunkan KGD secara sinergis dan lebih baik jika dibandingkan dengan masing-masing kelompok EEKKM 50 mg/kg bb maupun madu 0,75 ml/kg bb dengan metode uji toleransi glukosa.
Effect of Ethanol Extract of Cinnamon Cortex
((Cinnamomum burmannii (Nees & T.Nees) Blume)) and Honey Combina-tion in Decreasing Blood Glucose Levels in Male Rats
ABSTRACT
Everyone can ail from diabetes mellitus. Therefore, many patient try to control their blood glucose level with natural products such as cinnamon and honey because they are cheaper and can be obtained easily. The objective of this research is to understand the characterization of symplicia, second metabo-lites content, and the effect combination of ethanol extract of cinnamon-honey in decreasing blood glucose level using glucose tolerance test method.
This research includes the characterization and phytochemical screening of simplicia and extracts, experiment in animals and measurement KGD with methods glucose tolerance test. In glucose tolerance test, male mice divided into group used Na-CMC suspension 1% bw, ethanol extract of cinna-mon cotex (EEKKM) with 50; 100; and 200 mg/kg bw; honey with 0.75; 1.5; and 3 ml/kg bw; combination of ethanol extract of cinnamon and honey (50 mg/kg bw and 0.75 mg/kg bw) and glibenclamide 0.45 mg/kg bw.
Result of cinnamon symplicia macroscopic is stretch roll, reddish-brown colour and aromatic odor. Microscopic of cinnamon showed scleren-chyma and oil cells, stone cells, and free sclerenscleren-chyma. The result of characte-rization in cinnamon symplicia obtained 7.98% water content; 6.39% water-soluble extract content; 22.15% ethanol-water-soluble extract content; 3.25% total ash content; and 0.31% acid-insoluble ash content. Phythochemical screening of cinnamon showed the presence of flavonoids, glycoside, saponins and tan-nins. Result of honey macroscopic is thick liquid, reddish brown colour and has a particular odor and taste. Result of honey microscopic showed pollen. The result of characterization of honey obtained 27.94% water content; 17,79% wa-ter-soluble extract content; 5.93% ethanol-soluble extract content; 0% total ash content and 0% acid-insoluble ash content. Phythochemical screening of honey showed the presence of flavonoids and glycosides.
ANOVA analysis showed ethanol extract of cinnamon (EEKKM) 50; 100; 200 mg/kg bw and honey with 0.75; 1.5 and 3 ml/kg bw gave significant decreasing of blood glucose level compared to control group and glibenclamide group and the combination of ethanol extract of cinnamon and honey (50 mg/kg bw and 0.75 ml/kg bw) gave significant difference results compared to control group but not significant to glibenclamide 0.45 mg/kg bw (p < 0.05).
According to above results, the conclusion is EEKKM with 50; 100; and 200 mg/kg bw; honey 0.75; 1.5; and 3 ml/kg bw can decrease blood glu-cose level and combination of EEKKM and honey can decrease blood gluglu-cose level synergically and it is way better compared to ethanol extract of cinnamon with 50 mg/kg bw and honey 0.75 ml/kg bw.
BAB I PENDAHULUAN
1.1 Latar Belakang
Banyak orang yang masih menganggap penyakit diabetes merupakan
penyakit orang tua atau penyakit yang timbul karena faktor keturunan. Padahal
diabetes merupakan penyakit yang tidak pandang bulu. Semua kalangan dapat
mengidap penyakit ini, baik kaya, miskin, muda, ataupun tua (Hembing, 2004).
Sebelum zaman kemerdekaan, angka penderita diabetes melitus
cenderung rendah karena pola makan masyarakat masih sederhana. Saat ini,
angka penderita diabetes melitus cenderung meningkat signifikan. Kondisi ini
didukung oleh pola makan yang berubah menjadi makanan cepat saji, makanan
berlemak dan berkarbohidrat tinggi yang melebihi jumlah kalori makanan yang
dibutuhkan oleh tubuh dan faktor genetik juga dapat memicu timbulnya
penyakit diabetes melitus. Jika tidak ditangani secara serius, akan
mengakibatkan komplikasi bahkan dapat menimbulkan kematian. Pengobatan
secara medis dengan obat-obatan modern dan suntikan kadang sulit dilakukan
karena tingginya biaya pengobatan dan membutuhkan pengobatan jangka
panjang. Untuk itu, sebagai salah satu alternatifnya adalah dengan
menggunakan obat tradisional (Hembing, 2004).
Indonesia merupakan negara yang kaya sumber bahan alam, beragam
tumbuhan hidup di Indonesia, termasuk tumbuhan yang berkhasiat obat.
terutama untuk keperluan obat-obatan dalam rangka mengatasi
masalah-masalah kesehatan (Dalimartha, 2000). Organisasi Kesehatan Dunia (WHO)
juga telah merekomendasi penggunaan obat tradisional termasuk obat herbal
dalam pemeliharaan kesehatan masyarakat, pencegahan, dan pengobatan
pe-nyakit.
Bahan alam yang memiliki efek antidiabetes diantaranya adalah kayu
manis dan madu. Kombinasi madu dan kayu manis telah digunakan dalam
pengobatan India dan Cina selama berabad-abad. Kedua bahan dengan
kemampuan penyembuhan yang unik tersebut memiliki sejarah panjang
sebagai obat tradisional. Keduanya tidak hanya digunakan sebagai minuman
penyedap dan obat, melainkan juga sebagai zat pembalseman dan digunakan
sebagai alternatif pengawet makanan tradisional karena adanya sifat
antimikroba yang efektif. Masyarakat telah mengklaim bahwa campuran
tersebut adalah obat alami untuk berbagai penyakit dan menjadi formula untuk
berbagai manfaat kesehatan seperti: penyakit jantung, kerontokan rambut, sakit
gigi, demam, pencernaan, anti-penuaan, jerawat, obesitas, diabetes dan
pernafasan yang buruk (Nurmalina, 2012).
Berdasarkan hasil penelitian yang dilakukan oleh Hananti, dkk.,
(2012), menyatakan bahwa ekstrak etanol kulit kayu manis dosis 50, 100, dan
200 mg/kg bb mampu menurunan kadar glukosa darah pada mencit jantan yang
diinduksi glukosa 2 g/kg bb dengan metode uji toleransi glukosa. Penurunan
kadar glukosa darah diduga disebabkan oleh adanya senyawa tanin yang
Selain itu, Anderson, et al., (2004), mendeterminasikan komponen bioaktif
dari kayu manis yaitu doubly-linked procyanidin type-A polymers yang
meru-pakan bagian dari epicatechin/catechin yang selanjutnya disebut sebagai
me-thylhydroxychalcone polymer (MHCP). MHCP merupakan senyawa aktif pada
kayu manis memiliki sifat meningkatkan insulin, meningkatkan metabolisme
glukosa dalam hal penyerapan glukosa, transpor glukosa ke seluruh sel, dan
sintesis glikogen (Roy, et al., 2009). Kayu manis juga memiliki senyawa kafeat
dan sinamat memberikan khasiat inhibitor α-glukosidase. Penghambatan α
-glukosidase pada usus mamalia mampu menurunkan kadar glukosa darah
(Ngadiwiyana, dkk., 2011).
Para ilmuwan juga sependapat khasiat kayu manis dan madu
menak-jubkan dalam penyembuhan berbagai penyakit. Madu yang ditambahkan kayu
manis selain menjadi obat, memberi rasa harum, rasa manis dan hangat juga
merupakan pasangan yang cocok untuk dikonsumsi (Nurmalina, 2012).
Mere-kapun menyatakan walaupun madu itu manis akan tetapi jika dikonsumsi
den-gan tepat, tidak membahayakan penderita diabetes. Menurut Sakri, (2012),
untuk mendapatkan khasiat dari madu harus mengonsumsi secara teratur pagi,
siang dan malam yaitu pada orang dewasa 30 gram atau 1 sendok makan dan
pada anak-anak 15 gram atau ½ sendok makan madu. Glukosa yang terdapat
dalam madu akan terserap langsung oleh darah sehingga menghasilkan energi
secara cepat bila dibandingkan dengan gula biasa. Di samping kandungan
gu-lanya yang tinggi (fruktosa 41,0%; glukosa 35%; sukrosa 1,9%) madu juga
seperti: enzim diastase (Sakri, 2012) serta kandungan nutrisi yang berfungsi
sebagai antioksidan seperti vitamin C, vitamin A, vitamin E, asam organik,
dan flavonoid (Anonim, 2010).
Berdasarkan latar belakang permasalahan di atas, maka peneliti tertarik
untuk melakukan karakterisasi simplisia, ekstrak dan mengukur kadar glukosa
darah dosis kombinasi antara ekstrak etanol kulit kayu manis dan madu
terha-dap efek penurunan kadar glukosa darah dengan menggunakan tikus jantan
se-bagai hewan coba.
1.2 Perumusan Masalah
Berdasarkan latar belakang diatas, maka perumusan masalah dalam
pene-litian adalah:
a. apakah dengan melakukan karakterisasi simplisia kulit kayu manis dan
madu diperoleh karakteristik simplisia?
b. apakah golongan senyawa kimia yang terkandung dalam simplisia kulit
kayu manis dan madu?
c. apakah ekstrak etanol kulit kayu manis (EEKKM) memiliki efek
penuru-nan kadar glukosa darah (KGD) dengan metode uji toleransi glukosa?
d. apakah madu memiliki efek penurunan kadar glukosa darah (KGD)
dengan metode uji toleransi glukosa?
e. apakah kombinasi ekstrak etanol kulit kayu manis (EEKKM) dan madu
memiliki efek penurunan kadar glukosa darah (KGD) dengan metode uji
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis dalam penelitian
ini adalah:
a. karakteristik simplisia kulit kayu manis dan madu dapat diperoleh dengan
melakukan karakterisasi simplisia.
b. kandungan golongan senyawa kimia yang terdapat dalam simplisia kulit
kayu manis dan madu adalah golongan alkaloid, flavonoid, glikosida,
saponin, tanin dan steroid.
c. ekstrak etanol kulit kayu manis (EEKKM) memiliki efek penurunan
ka-dar glukosa ka-darah (KGD) dengan metode uji toleransi glukosa.
d. madu memiliki efek penurunan kadar glukosa darah (KGD) dengan
metode uji toleransi glukosa.
e. kombinasi ekstrak etanol kulit kayu manis (EEKKM) dan madu memiliki
efek penurunan kadar glukosa darah (KGD) dengan metode uji toleransi
glukosa.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. untuk mengetahui karakteristik simplisia kulit kayu manis dan madu
b. untuk mengetahui golongan senyawa kimia yang terdapat dalam
c. untuk mengetahui efek ekstrak etanol kulit kayu manis (EEKKM) sebagai
penurunan kadar glukosa darah (KGD)
d. untuk mengetahui efek madu sebagai penurunan kadar glukosa darah
(KGD)
e. untuk mengetahui efek kombinasi ekstrak etanol kulit kayu manis
(EEKKM) dan madu sebagai penurunan kadar glukosa darah (KGD)
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah memberi informasi kepada masyarakat
tentang efek penurunan kadar glukosa darah (KGD) dari kombinasi ekstrak
etanol kulit kayu manis (EEKKM) dan madu.
1.6 Kerangka Pikir Penelitian
Penelitian dilakukan terhadap tikus jantan dengan metode uji toleransi
glukosa. Terdapat lima variabel yaitu suspensi Na-CMC 0,5% b/v dosis 1% bb,
variasi dosis ekstrak kulit kayu manis, variasi dosis madu, dosis kombinasi
ek-strak etanol kulit kayu manis-madu dan obat pembanding yaitu glibenklamid
sebagai variabel bebas dan kadar glukosa darah tikus (mg/dl) sebagai variabel
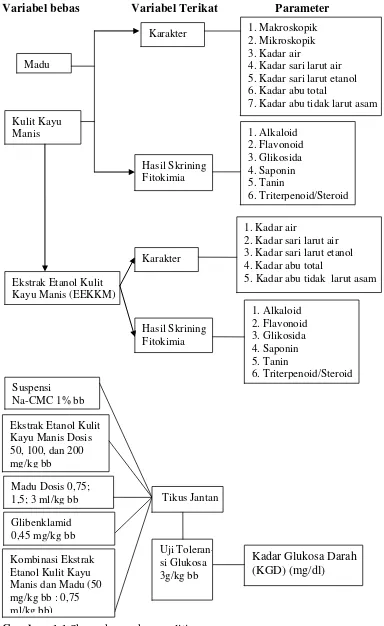
Variabel bebas Variabel Terikat Parameter
Gambar 1.1 Skema kerangka penelitian
Kulit Kayu 5. Kadar sari larut etanol 6. Kadar abu total
BAB II
TINJAUAN PUSTAKA
2.1 Kayu Manis
Pada pasar luar negeri terdapat dua jenis minyak kayu manis. Pertama,
minyak kayu manis asal Sri Langka yang disebut Cinnamon bark oil, diperoleh
dari penyulingan kulit kayu manis (Cinnamomum zeylanicum/Ceylon
cinnamon). Kedua, minyak kayu manis asal Cina, dihasilkan dari penyulingan
kulit manis (C. cassia/Chinese cinnamon), disebut cassia oil. Kayu manis yang
banyak dibudidayakan di Indonesia terutama di Sumatera Barat, Jambi dan
Sumatera Utara adalah jenis C. burmanii (Batavia cinnamon). Kayu manis
jenis ini belum banyak diproduksi minyaknya, tetapi masih diekspor sebagai
kulit kering yang disebut cassia vera. Namun hasil pengujian menunjukkan
bahwa karakteristik minyak C. burmanii hampir sama dengan minyak C.
zeylanicum dan C. cassia (Hapsoh, dkk., 2011).
2.1.1 Morfologi tumbuhan kayu manis
Kayu manis dapat ditemukan tumbuh liar di hutan pada ketinggian
0-2.000 m dpl. Namun, tumbuh baik pada tanah yang subur, gembur, agak
berpa-sir. Pohon memiliki tinggi 5 - 15 m, kulit berwarna abu-abu tua, berbau khas,
kayu berwarna merah atau coklat muda. Bentuk daun elips memanjang, ujung
meruncing, pangkal runcing, tepi rata. Daun muda berwarna merah pucat,
2.1.2 Sistematika tumbuhan kayu manis
Berikut adalah sistematika tumbuhan (Ditjen POM, 2000):
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledonae
Bangsa : Ranales
Suku : Lauraceae
Marga : Cinnamomum
Jenis : Cinnamomum burmani Bl.
2.1.3 Kandungan kayu manis
Kulit batang dan daun Cinnamomum burmani mengandung minyak
at-siri, saponin dan flavonoida. Di samping itu, kulit batangnya mengandung
tan-nin, daunnya mengandung alkaloida dan polifenol (Depkes RI, 2000).
Penelitian terhadap minyak atsiri dari Cinnamomum burmannii yang berasal
dari Guangzhou, Cina yang dilakukan oleh Wang, dkk pada tahun 2009
melaporkan bahwa komponen mayor minyak atsiri yang terkandung adalah
transsinamaldehid (60,72%), eugenol (17,62%) dan kumarin (13,39%)
(Hapsoh, dkk., 2011).
2.2 Madu
Madu merupakan sebuah cairan yang menyerupai sirup yang dihasilkan
pemanis lainnya. Rasa manis itu berasal dari cairan manis (nektar) yang
terda-pat pada bunga maupun ketiak daun yang dihisap lebah. Madu dihasilkan dari
dua jenis lebah, yaitu lebah liar dan lebah budidaya. Madu lebah liar berasal
dari pohon yang berbatang tinggi yang disebut oleh masyarakat dengan nama
pohon sialang. Warna madunya juga cenderung pekat. Sedangkan madu lebah
budidaya berasal dari tanaman rendah seperti tanaman buah-buahan maupun
tanaman pertanian, warna madu yang cenderung cerah (Sakri, 2012).
2.2.1 Kandungan madu
Madu memiliki kandungan gula yang tinggi, yaitu fruktosa (41 persen),
glukosa (35 persen), sukrosa (1,9 persen), serta unsur kandungan lain seperti
tepung sari yang ditambah berbagai enzim pencernaan (Sakri, 2012). Madu
memang merupakan campuran dari gula dan senyawa lainnya seperti vitamin
C, vitamin A, vitamin E, asam organik, flavonoid serta mineral. (Anonim,
2010). Semua kandungan tersebut dapat digunakan sebagai pengobatan
tradisional, antibodi, antioksidan dan antikanker. Oleh karena itu madu banyak
digunakan untuk pengobatan alternatif (Sakri, 2012).
2.3 Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang
Metode ekstraksi menurut Ditjen POM (2000) dan Syamsuni (2007)
ada beberapa cara, yaitu: cara dingin dan cara panas.
2.3.1 Cara Dingin
a. Maserasi
Maserasi merupakan suatu proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada
temperatur ruangan (kamar).
b. Perkolasi
Perkolasi merupakan suatu cara penyarian simplisia dengan menggunakan
per-kolator dimana simplisianya terendam dalam pelarut yang selalu baru dan
umumnya dilakukan pada temperatur kamar. Prosesnya terdiri dari tahapan
pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya
(pe-netesan dan penampungan ekstrak) terus-menerus sampai diperoleh ekstrak
(perkolat).
2.3.2 Cara Panas
a. Refluks
Refluks merupakan suatu cara ekstraksi dengan pelarut pada temperatur titik
didihnya selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik.
b. Sokletasi
Sokletasi merupakan suatu cara ekstraksi kontinu dengan menggunakan alat
soklet, dimana pelarut akan terkondensasi dari labu menuju pendingin,
sifon juga terisi dengan larutan ekstraksi dan ketika mencapai bagian atas
ta-bung sifon, larutan tersebut akan kembali ke dalam labu.
c. Digesti
Digesti merupakan maserasi kinetik (dengan pengadukan kontinu) pada
tempe-ratur yang lebih tinggi dari tempetempe-ratur kamar, umumnya dilakukan pada suhu
40-50oC.
d. Infus
Infus merupakan suatu cara ekstraksi dengan menggunakan pelarut air pada
tem-peratur 90oC selama 15 menit.
e. Dekok
Dekok merupakan suatu cara ekstraksi pada suhu 90oC dengan menggunakan
pelarut air selama 30 menit.
2.4 Metabolisme Glukosa Berperan Dalam Pelepasan Insulin
Insulin dihasilkan oleh pankreas yaitu sel β pankreas. Pelepasan insulin
dirangsang oleh sejumlah besar zat endogen dan eksogen. Glukosa merupakan
salah satu zat eksogen yang menjadi penentu utama fungsi sel β dalam
mensintesis maupun melepaskan insulin (Lawrence, 2005).
Setelah adanya rangsangan oleh molekul glukosa, proses sekresi insulin
diperngaruhi beberapa tahap. Tahap pertama adalah proses glukosa melewati
membran sel. Untuk dapat melewati membran sel β dibutuhkan bantuan
terdapat di dalam berbagai sel yang berperan dalam proses metabolisme
glukosa. Fungsinya sebagai “ kendaraan” pengangkut glukosa masuk dari luar
ke dalam sel jaringan tubuh. Glucose tansporter 2 (GLUT 2) yang terdapat
dalam sel beta, misalnya diperlukan dalam proses masuknya glukosa dari
dalam darah, melewati membran, ke dalam sel. Proses ini penting bagi tahapan
selanjutnya yakni molekul glukosa akan mengalami fosforilasi di dalam sel dan
kemudian membebaskan molekul ATP. Molekul ATP yang terbentuk,
dibutuhkan untuk tahapan selanjutnya yakni proses mengaktifkan penutupan K
channel pada membran sel. Penutupan kanal ini berakibat terhambatnya
pengeluaran ion K dari dalam sel yang menyebabkan terjadinya tahap
depolarisasi membran sel, yang diikuti kemudian oleh tahap pembukaan Ca
channel. Keadaan inilah yang memungkinkan masuknya ion Ca sehingga
meningkatkan kadar ion Ca intrasel. Suasana ini dibutuhkan bagi proses sekresi
insulin (Manaf, 2010).
Insulin kemudian berikatan dengan reseptor di permukaan sel pada
jaringan target. Adapun jaringan target yang penting untuk pengaturan
homeostatis glukosa adalah hati, otot dan lemak. Selain itu, insulin juga bekerja
pada sel darah, sel otak dan sel gonad. Interaksi antara insulin dan reseptor
menghasilkan sinyal yang ditransmisikan kedalam sel untuk mengaktifasi
berbagai jalur anabolik dan menghambat prose katabolik. Kerja anabolik
insulin ini mencakup transpor glukosa, sintesis glikogen, lipid dan protein.
Transpor glukosa ke dalam sel otot rangka dan adiposa diperantarai oleh
Glukosa dalam sel selanjutnya dapat dimetabolisme dengan berbagai cara.
Dalam otot rangka dan hati, glukosa disimpan dalam bentuk glikogen
(glikogenesis) untuk dapat dipakai kembali (glikogenolisis). Di dalam sel
lemak, glukosa dimetabolisme menjadi asetil koA yang kemudian digunakan
untuk mensintesis asam lemak. Pengesteran asam lemak dengan gliserol
menghasilkan trigliserida yang merupakan bentuk penyimpanan energi (Manaf,
2010).
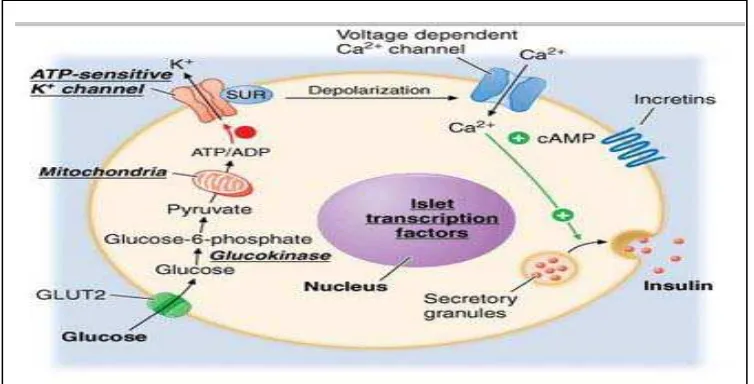
Sistematika pelepasan insulin dapat ditunjukkan pada Gambar 2.1
(Powers, 2008).
Gambar 2.1 Pelepasan Insulin secara skematis dikutip dari: Powers, A.C.
(2008). Diabetes Mellitus. Editor: Fauci, S.A., Braunwald, E.,
Kasper, D.L., Hauser, S.L., Longo, D.L., Jameson, J.L dan
Los-calzo, J. Dalam: Harrison’s Principles Of Internal Medicine.
Edi-si Ketujuh Belas. New York: The Mc Graw-Hill Companies, Inc.
2.5 Diabetes Melitus
Diabetes Melitus (DM) merupakan suatu kelompok penyakit metabolik
dimana adanya gangguan dalam metabolisme lemak, karbohidrat, dan protein
yang ditandai dengan karakteristik hiperglikemia yang terjadi karena akibat
penurunan dalam sekresi insulin, sensitivitas insulin, atau keduanya (Triplitt,
dkk., 2008).
Sindroma resistensi insulin adalah suatu kondisi dimana terjadi
penurunan sensitivitas insulin terhadap jaringan sehingga terjadi peningkatan
sekresi insulin sebagai bentuk kompensasi sel beta pankreas. Intoleransi
glukosa merupakan salah satu manifestasi sindrom metabolik yang dapat
menjadi awal suatu diabetes melitus (Soegondo, 2010).
Diabetes melitus (DM) mempunyai sindroma klinik yang ditandai
adanya poliuria, polidipsia, dan polifagia, disertai peningkatan kadar glukosa
darah atau hiperglikemia (kadar glukosa puasa ≥ 126 mg/dl atau postprandial ≥
200 mg/dl atau glukosa sewaktu ≥ 200 mg/dl) (Suherman, 2007).
2.5.1 Klasifikasi diabetes melitus
Berdasarkan Triplitt, dkk., 2008, diabetes melitus dapat dibagi menjadi:
a. Diabetes melitus tipe 1 (DM 1), merupakan diabetes yang mengalami
kerusakan sel β pankreas yang menyebabkan kekurangan insulin absolut.
Diabetes Melitus tipe 1 dikenal dengan nama Insulin Dependent Diabetes
Mel-litus (IDDM), terjadi karena adanya kerusakan sel pankreas (reaksi autoimun)
menyebabkan defisiensi absolut fungsi sel beta pankreas. Bila kerusakan sel
Peru-sakan sel beta ini lebih cepat terjadi pada anak-anak daripada dewasa. Sebagian
besar penderita diabetes melitus tipe 1 mempunyai antibodi yang menunjukkan
adanya proses autoimun, dan sebagian kecil tidak terjadi proses autoimun.
Kondisi ini digolongkan sebagai type 1 idiopathic. Sebagian besar (75%) kasus
terjadi < 20 tahun, tetapi dapat juga terjadi pada setiap usia. Prevalensi DM tipe
1 ini masih sedikit dalam populasi.
b. Diabetes melitus tipe 2, merupakan diabetes yang disebabkan oleh
resis-tensi insulin dan sekresi insulin yang abnormal. Diabetes Melitus tipe 2
meru-pakan 90% dari kasus DM dikenal sebagai Non Insulin Dependent Diabetes
Mellitus (NIDDM). Pada diabetes ini terjadi penurunan kemampuan insulin
be-kerja di jaringan perifer (insulin resistance) dan disfungsi sel beta. Akibatnya,
pankreas tidak mampu memproduksi insulin yang cukup untuk
mengkompen-sasi insulin resistance. Kedua hal ini menyebabkan terjadinya defisiensi insulin
relatif. DM tipe 2 ini sering dijumpai pada individu yang obesitas. Kasus ini
umumnya dijumpai pada usia > 30 tahun.
c. Diabetes tipe lain, merupakan diabetes yang disebabkan oleh adanya
ke-lainan genetik pada fungsi sel beta pankreas, keke-lainan insulin, infeksi,
pankrea-titis, pankreatomi, obat-obatan dan kelainan genetik lainnya.
d. Diabetes gestasional (diabetes kehamilan) merupakan diabetes yang timbul
selama kehamilan.
2.5.2 Diagnosis diabetes melitus
Diagnosis DM harus didasarkan atas pemeriksaan kadar glukosa
darah plasma vena. Langkah-langkah untuk menegakkan diagnosis DM dan
gangguan toleransi glukosa dapat juga dilihat dari keluhan khas DM
berupa poliuria, polidipsia, polifagia, dan penurunan berat badan. Keluhan
lain yang mungkin dikemukakan pasien berupa lemas, kesemutan, luka yang
sulit sembuh, gatal-gatal, mata kabur (Purnamasari, 2009).
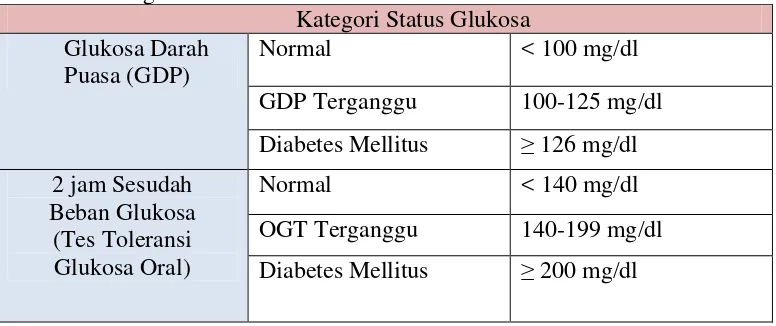
Kategori status glukosa darah puasa (GDP) dan tes toleransi glukosa oral
(OGTT) menurut Triplitt, et al., (2008) dapat dilihat pada Tabel 2.1.
Tabel 2.1 Kategori Status Glukosa
Kategori Status Glukosa Glukosa Darah
Puasa (GDP)
Normal < 100 mg/dl
GDP Terganggu 100-125 mg/dl
Diabetes Mellitus ≥ 126 mg/dl
OGT Terganggu 140-199 mg/dl
Diabetes Mellitus ≥ 200 mg/dl
2.5.3 Manajemen pengobatan diabetes melitus
Manajemen pengobatan diabetes melitus bertujuan untuk mengurangi
resiko terjadinya komplikasi, mengurangi mortalitas, dan meningkatkan
kuali-tas hidup (Triplitt, dkk., 2008). Langkah pertama dalam mengelola diabetes
melitus selalu dimulai dengan pendekatan non farmakologi, yaitu berupa
pemberian edukasi, perencanaan makan/terapi nutrisi medik, kegiatan jasmani
dan penurunan berat badan bila di dapat berat badan lebih atau obesitas. Bila
dengan langkah tersebut sasaran terapi pengendalian diabetes melitus belum
diperhatikan titik kerja obat sesuai dengan macam penyebab terjadinya
hiperglikemia (Soegondo, 2010).
Obat antidibetika oral dibagi dalam 7 kelompok, sebagai berikut:
a. Sulfonilurea, misalnya: tolbutamid, klorpropamida, glibenklamida,
gliklazida, glipizida, glikidon dan glimepirida.
Mekanisme kerja sulfonilurea dengan menstimulasi insulin dari sel beta
pankreas. Sulfonilurea berikatan dengan reseptor sulfonilurea yang memiliki
afinitas tinggi yang berkaitan dengan saluran K-ATP pada sel beta pankreas,
akan menghambat efluks kalium sehingga terjadi depolarisasi kemudian
membuka saluran Ca dan menyebabkan influks Ca sehingga meningkatkan
pelepasan insulin. Di samping itu, sulfonilurea juga dapat meningkatkan
kepekaan reseptor terhadap insulin di hati dan di perifer.
b. Penghambat kanal kalium, misalnya: repaglinida, nateglinida.
Golongan ini mempunyai mekanisme kerja yang sama dengan sulfonilurea,
hanya pengikatan reseptornya terjadi di tempat lain dan kerjanya lebih
singkat.
c. Biguanida, misalnya: metformin.
Berbeda dengan sulfonilurea, obat ini tidak bekerja dengan menstimulasi
pelepasan insulin, akan tetapi melalui pengaruhnya terhadap kualitas kerja
insulin pada tingkat seluler dengan meningkatkan kemampuan insulin dalam
memindahkan glukosa ke dalam sel (insulin sensitizers) dan menurunkan
produksi glukosa hati. Metformin meningkatkan pemakaian glukosa oleh sel
absorpsi glukosa di usus sesudah asupan makan. Golongan obat ini bukan
obat hipoglikemik tetapi suatu antihiperglikemik sebab tidak menyebabkan
rangsangan sekresi insulin dan umumnya tidak menyebabkan hipoglikemia.
d. Penghambat enzim α-Glukosidase, misalnya: akarbose dan miglitol.
Obat golongan ini bekerja dengan merintangi enzim alfa-glukosidase di
mukosa duodenum, sehingga reaksi penguraian polisakarida menjadi
monosakarida terhambat. Dengan demikian glukosa dilepaskan lebih
lambat dan absorpsinya ke dalam darah juga kurang cepat, lebih rendah dan
merata, sehingga puncak kadar gula darah dapat dihindarkan.
e. Thiazolidiendion, misalnya: rosiglitazon dan pioglitazon.
Obat golongan ini bekerja dengan mengurangi resistensi insulin dan
meningkatkan sensitivitas jaringan perifer untuk insulin (insulin sensitizers).
f. Mimetik Inkretin, misalnya : Exenatide, Liraglutide dan Taspoglutide
Mimetik inkretin adalah kelompok antidiabetes baru dengan daya kerja
me-nyerupai efek hormon inkretin endogen. Pada akhirnya obat ini mampu
menstimulasi sekresi insulin sekaligus menghambat pelepasan glukagon,
sehingga terjadi penurunan kadar glukosa darah.
g. Penghambat DPP-4 (dipeptidylpeptidase-4 blockers), misalnya : vildagliptin,
sitagliptin, saxagliptin.
Obat golongan baru ini bekerja dengan menghambat enzim DPP-4 sehingga
produksi hormon incretin tidak menurun. Adanya hormon incretin berperan
utama dalam produksi insulin di pankreas dan pembentukan hormon GLP-1
polypeptide) di saluran cerna yang juga berperan dalam produksi insulin.
Dengan penghambatan enzim DPP-4 akan mengurangi penguraian dan
inaktivasi incretin, GLP-1 dan GIP, sehingga kadar insulin akan meningkat.
(Tan dan Rahardja, 2007; Suherman, 2007).
2.5.4 Monitoring diabetes melitus
Monitoring diabetes melitus dapat dilakukan dengan pemeriksaan yang
dilakukan antara lain kadar glukosa darah puasa, 2 jam postprandial, dan
pe-meriksaan glycated haemoglobin, khususnya HbA1C. Pemeriksaan lain yang
bisa dilakukan ialah urinalisa rutin. Nilai HbA1C normal menurut ACA (
Amer-ican College of Endocrinology) dan AACE (American Association of Clinical
Endocrinologists) adalah < 6,5%, sedangkan menurut ADA (American
Di-abetes Assosiation) adalah < 7% (Triplitt, dkk., 2008).
Dari dalam sirkulasi darah, terdapat sel darah merah yang membentuk
molekul hemoglobin. Glukosa yang melekat pada hemoglobin ini membentuk
molekul glycated haemoglobin yang disebut hemoglobin A1c atau HbA1C.
HbA1C digunakan untuk memonitoring penatalaksanaan terapi obat dan
kepa-tuhan pasien dalam penggunaan obat. Oleh karena itu, penentuan HbA1C ini
dilakukan secara rutin tiap 3 bulan sekali untuk dapat mengontrol terapi
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental. Penelitian
meliputi pengumpulan dan penyiapan bahan, karakterisasi simplisia, skrining
fitokimia, pembuatan ekstrak, penyiapan hewan percobaan dan pengujian
pen-garuh kombinasi ekstrak etanol kulit kayu manis dan madu terhadap penurunan
kadar glukosa darah pada tikus jantan.
3.1 Alat
Alat-alat yang digunakan terdiri dari: lemari pengering, blender (
Phi-lip), oven (Memmert), neraca listrik (Mettler Toledo), neraca hewan (
GW-1500), rotary evaporator (Heidolph WB 2000), glukometer (EasyTouch ®
GCU) dan strip glukotest (EasyTouch ® GCU strip test), spuit, oral sonde,
mor-tir dan stamfer, alat-alat gelas lainnya, dan kertas filter.
3.2 Bahan
Bahan tumbuhan yang digunakan pada penelitian ini adalah kulit kayu
manis ((Cinnamomum burmannii (Nees & T.Nees) Blume)) dan madu. Bahan
kimia yang digunakan adalah etanol 96% (destilasi), pereaksi bouchardat,
Dra-gendorff, Mayer, besi (III) klorida 4,5% b/v, Molish, timbal (II) asetat 0,4 M,
Lieber-man-Burchard, toluen, kloroform, glukosa 50%, Na-CMC (natrium carboxy
methyl cellulose), glibenklamid dan akuades.
3.3 Prosedur Pembuatan Simplisia 3.3.1 Pengambilan bahan
Pengambilan sampel dilakukan secara purposif tanpa membandingkan
dengan tumbuhan yang sama dari daerah lain. Sampel kulit kayu manis diambil
dari Tiga Dolok Kecamatan Dolok Panribuan Kabupaten Simalungun,
Sumatera Utara dan Sampel madu diambil dari PTP V Sei Rokan Kecamatan
Kunto Darussalam Kabupaten Rokan Hulu, Riau.
3.3.2 Identifikasi tumbuhan
Identifikasi sampel kulit kayu manis dilakukan di Herbarium
Bogo-riense, Bidang Botani Pusat Penelitian Biologi-LIPI Bogor.
3.3.3 Pembuatan simplisia
Bahan baku kulit kayu manis dikumpulkan, dicuci bersih di bawah air
mengalir, ditiriskan, dan ditimbang beratnya (2,276 kg). Kulit kayu manis
se-lanjutnya dikeringkan di lemari pengering hingga kering, dibuang benda asing
yang masih tertinggal pada simplisia, kemudian ditimbang beratnya (1,714 kg)
dan disimpan dalam wadah plastik yang tertutup rapat.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
peneta-pan kadar sari larut dalam etanol, penetapeneta-pan kadar abu total, dan penetapeneta-pan
ka-dar abu tidak larut dalam asam.
3.4.1 Pemeriksaan makroskopik dan organoleptik
Pemeriksaan makroskopik dan organolepik dilakukan dengan
menga-mati bentuk, bau dan rasa dari kayu manis, serbuk simplisia kulit kayu manis
dan simplisia madu.
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia kulit
kayu manis dan simplisia madu. Serbuk simplisia kulit kayu manis diletakkan
di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup
dengan kaca penutup, selanjutnya diamati di bawah mikroskop. Simplisia
madu diletakkan di atas kaca objek lalu ditetesi dengan aquadest dan ditutup
dengan kaca penutup, selanjutnya diamati di bawah mikroskop.
3.4.3 Penetapan kadar air
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi
to-luena). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung,
tabung penerima 5 mL berskala 0,05 ml, alat penampung dan pemanas listrik.
Cara kerja:
Dimasukkan 200 ml toluena dan 2 ml air suling ke dalam labu alas
bu-lat, lalu didestilasi selama 2 jam. Setelah itu, toluena dibiarkan mendingin
se-lama 30 menit, dan dibaca volume air pada tabung penerima dengan ketelitian
0,05 ml. Kemudian ke dalam labu tersebut dimasukkan 5 g serbuk simplisia
Se-telah toluena mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik
sampai sebagian besar air terdestilasi, kemudian kecepatan tetesan dinaikkan
hingga 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin
dibilas dengan toluena. Destilasi dilanjutkan selama 5 menit, kemudian tabung
penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluena
memi-sah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua
vo-lume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan
yang diperiksa. Kadar air dihitung dalam persen (Depkes RI, 1977).
3.4.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu
bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan
selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai
kering dalam cawan penguap yang berdasar rata yang telah ditara dan sisa
di-panaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang
larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes RI,
1977).
3.4.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam
per-tama, kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk
menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering
Si-sa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari
yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan
(Depkes RI, 1977).
3.4.6 Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia dimasukkan dalam krus porselin yang
telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan
sam-pai arang habis, jika arang masih tidak dapat dihilangkan, ditambahkan air
pa-nas, saring melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring
da-lam krus yang sama. Masukkan filtrat ke dada-lam krus, uapkan, pijarkan hingga
bobot tetap, timbang. Kadar abu dihitung terhadap bahan yang telah
dikering-kan (Depkes RI, 1977).
3.4.7 Penetapan kadar abu tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikum-pulkan, disaring melalui kertas saring bebas abu, cuci dengan air panas,
dipi-jarkan, kemudian didinginkan dan ditimbang sampai bobot tetap. Kadar abu
yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan
(Depkes RI, 1977).
3.5 Skrining Fitokimia Simplisia
Skrining fitokimia serbuk simplisia kulit kayu manis dan simplisia
madu meliputi pemeriksaan senyawa golongan flavonoid, alkaloid, saponin,
3.5.1 Pemeriksaan flavanoid
Sebanyak 10 g serbuk simplisia ditambahkan 10 ml air panas,
dididih-kan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat
ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml
amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi
warna merah, kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.5.2 Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2
menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk tes
alka-loid. Diambil 3 tabung reaksi, lalu ke dalamnya dimasukkan 0,5 ml filtrat. Pada
masing-masing tabung reaksi:
a. Ditambahkan 2 tetes pereaksi Mayer
b. Ditambahkan 2 tetes pereaksi Bouchardat
c. Ditambahkan 2 tetes pereaksi Dragendorff
Alkaloid positif jika terjadi endapan atau kekeruhan pada dua dari tiga
perco-baan diatas (Depkes RI, 1977).
3.5.3 Pemeriksaan saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan ke dalam
tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan, kemudian
sta-bil tidak kurang dari 10 menit dan buih tidak hilang dengan penambahan 1
tetes asam klorida 2 N menunjukkan adanya saponin (Depkes RI, 1977).
3.5.4 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling lalu
dis-aring, filtratnya diencerkan dengan air suling sampai tidak berwarna. Diambil 2
ml larutan dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi
warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin
(Depkes RI, 1977).
3.5.5 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g, lalu disari dengan 30 ml
campuran etanol 96%-air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2
jam, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 25 ml air
suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit,
lalu disaring. Filtrat disari dengan 20 ml campuran kloroform-isopropanol (3:2)
sebanyak 3 kali. Pada kumpulan sari lapisan isopropanol diuapkan pada suhu
tidak lebih dari 50oC. Sisanya dilarutkan dengan 2 ml metanol untuk larutan
percobaan. 0,1 ml larutan percobaan diuapkan diatas penangas air, pada sisa
ditambahkan 2 ml air dan 5 tetes Molish, kemudian ditambahkan hati-hati 2 ml
asam sulfat, terbentuk cincin berwarna ungu pada batas cairan, menunjukkan
adanya ikatan gula (Depkes RI, 1977).
3.5.6 Pemeriksaan steroid/triterpenoid
Serbuk simplisia ditimbang sebanyak 1 g, dimaserasi dengan 20 ml
pada sisanya ditambahkan pereaksi Liebermann-Burchard melalui dinding
ca-wan. Apabila terbentuk warna ungu atau merah yang berubah menjadi biru
un-gu atau biru hijau menunjukkan adanya triterpenoid/steroid (Harborne, 1987).
3.6 Proses Pembuatan Ekstrak Etanol Kulit Kayu Manis (EEKM)
Metode: Maserasi
Cara Kerja: Masukkan 10 bagian (500 g) simplisia atau campuran simplisia
dengan derajat halus yang cocok dalam bejana, dituangi dengan 75 bagian
cai-ran penyari etanol 96% (3,75 liter), ditutup dan dibiarkan selama 5 hari
terlin-dung dari cahaya sambil sering diaduk, lalu diserkai, diperas, di remaserasi
ampas dengan cairan penyari secukupnya hingga diperoleh 100 bagian (5 liter),
maserat dipindahkan kedalam bejana tertutup, dibiarkan di tempat yang sejuk,
terlindung dari cahaya selama 2 hari, lalu di enaptuangkan atau disaring.
Maserat yang diperoleh dipekatkan dengan alat rotary evaporator. Kemudian
dikeringkan dengan freeze dryer selama lebih kurang 24 jam (Ditjen POM,
1979).
3.7 Pemeriksaan Karakteristik EEKKM
Pemeriksaan karakteristik ekstrak etanol kulit kayu manis meliputi,
pe-netapan kadar air, pepe-netapan kadar sari larut dalam air, pepe-netapan kadar sari
larut dalam etanol, penetapan kadar abu total, dan penetapan kadar abu tidak
larut dalam asam. Prosedur pemeriksaan karakterisasi ekstrak etanol kulit kayu
3.8 Skrining Fitokimia EEKM
Skrining terhadap ekstrak etanol kulit kayu manis dilakukan untuk
mengetahui metabolit sekunder yang terkandung di dalam ekstrak. Prosedur
pemeriksaan ekstrak etanol kulit kayu manis sama seperti prosedur skrining
fitokimia terhadap simplisia kulit kayu manis.
3.9 Penyiapan Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian adalah tikus putih
jantan galur Wistar dengan berat badan 150 – 200 g. Pada metode uji toleransi
glukosa, sebanyak 54 ekor tikus dibagi dalam 9 kelompok, setiap kelompok
terdiri dari 6 ekor tikus. Sebelum pengujian dikondisikan terlebih dahulu
sela-ma 1 minggu dengan kondisi lingkungan, makanan, dan minuman yang sama.
Setelah 1 minggu, dipilih tikus yang sehat ditandai dengan berat badan yang
stabil atau meningkat.
3.10 Pembuatan Pereaksi
Pembuatan pereaksi mencakup larutan glukosa 50% b/v, pembuatan
suspensi Na-CMC 0,5% b/v, pembuatan suspensi glibenklamid dosis 0,45
mg/kg bb, pembuatan suspensi EEKM dosis 50 mg/kg bb, 100 mg/kg bb, dan
200 mg/kg bb.
3.10.1 Pembuatan larutan glukosa 50% b/v
3.10.2 Pembuatan suspensi Na-CMC 0,5% b/v
Sebanyak 0,5 g Na-CMC ditaburkan dalam lumpang yang berisi 10 ml
air suling panas. Didiamkan selama 15 menit lalu digerus hingga diperoleh
massa yang transparan, lalu digerus sampai homogen, diencerkan dengan air
suling, dihomogenkan dan dimasukkan ke labu tentukur 100 ml, dicukupkan
volumenya dengan air suling hingga 100 ml.
3.10.3 Pembuatan suspensi glibenklamid dosis 0,45 mg/kg bb Se-banyak 1 tablet glibenklamid 5 mg, diambil dan dimasukkan ke dalam lumpang
dan ditambahkan suspensi Na-CMC 0,5% b/v sedikit demi sedikit sambil
dige-rus sampai homogen, volume dicukupkan hingga 50 ml.
3.10.4 Pembuatan suspensi ekstrak etanol kulit kayu manis (EEKKM)
Dalam pengujian akan digunakan 3 variasi dosis yakni dosis 50 mg/kg
bb, 100 mg/kg bb, 200 mg/kg bb. Sejumlah 50 mg, 100 mg, dan 200 mg
ek-strak etanol kulit kayu manis dimasukkan ke dalam lumpang dan ditambahkan
suspensi Na-CMC 0,5% b/v sedikit demi sedikit sambil digerus sampai
homo-gen hingga 10 ml.
3.11 Pengujian Penurunan Kadar Glukosa Darah Ekstrak Etanol Kulit Kayu Manis dan Madu
3.11.1 Penggunaan blood glucose test meter “EasyTouch ® GCU”
Kadar glukosa darah diukur dengan alat glukometer menggunakan strip
tes yang bekerja secara enzimatis.
Alat yang digunakan untuk mengukur kadar glukosa darah adalah
Ea-syTouch ® GCU . Glukometer ini secara otomatis akan hidup ketika strip tes
EasyTouch ® GCU dimasukkan ke alat EasyTouch ®GCU sehingga glukometer
ini akan hidup secara otomatis, kemudian dicocokkan kode nomor yang
mun-cul pada layar dengan yang ada pada vial strip tes EasyTouch ® GCU. Tes strip
yang dimasukkan pada glukometer pada bagian layar akan tertera angka yang
harus sesuai dengan kode vial strip tes EasyTouch ® GCU, kemudian pada
layar monitor glukometer muncul tanda siap untuk diteteskan darah. Caranya
dengan menyentuh 1 tetes darah yang keluar ke tes strip dan ditarik sendirinya
melalui aksi kapiler. Ketika wadah terisi penuh oleh darah, alat mulai
mengu-kur kadar glukosa darah.
3.11.2 Pengukuran kadar glukosa darah (KGD)
Sebelum percobaan dilakukan, diukur KGD tikus dimana KGD yang
diukur adalah KGD puasa yaitu tikus dipuasakan (tidak diberi makan tetapi
tetap diberi minum) selama 12 jam sebelum percobaan (Frode, 2008).
Masing-masing tikus diukur dengan diambil darah tikus melalui pembuluh darah vena.
Darah yang keluar diteteskan pada glukometer. Angka yang tampil pada layar
dicatat sebagai KGD (mg/dL).
3.11.3 Pengujian penurunan kadar glukosa darah ekstrak etanol kulit kayu manis (EEKKM) dan madu dengan metode toleransi gluko-sa
Tikus jantan galur Wistar sebanyak 54 ekor dengan berat badan
150-200 g yang telah dipuasakan ditimbang berat badannya, diukur kadar glukosa
darah (KGD) puasa, dikelompokkan secara acak menjadi 9 kelompok, yang
masing –masing kelompok terdiri dari 6 ekor tikus dan diberi perlakuan secara
Kelompok I : Tikus diberikan suspensi Na-CMC 0,5% b/v dosis 1% bb
Kelompok II : Tikus diberikan suspensi EEKKM dosis 50 mg/kg bb
Kelompok III : Tikus diberikan suspensi EEKKM dosis 100 mg/kg bb
Kelompok IV : Tikus diberikan suspensi EEKKM dosis 200 mg/kg bb
Kelompok V : Tikus diberikan Madu dosis 0,75 ml/kg bb
Kelompok VI : Tikus diberikan Madu dosis 1,5 ml/kg bb
Kelompok VII : Tikus diberikan Madu dosis 3 ml/kg bb
Kelompok VIII: Tikus diberikan EEKKM 50 mg/kg bb dan Madu 0,75 ml/kg bb
Kelompok IX : Tikus diberikan suspensi glibenklamid dosis 0,45 mg/kg bb
Setiap kelompok yang telah diberikan sediaan uji, 30 menit kemudian
diberikan larutan glukosa 50% b/v dengan dosis 3 g/kg bb. Setelah pemberian
glukosa, dilakukan pengukuran KGD pada menit ke-30, 60, 90 dan 120 dengan
menggunakan alat ukur glukometer.
3.12 Analisis Data
Data hasil penelitian dianalisis dengan metode analisis variansi
(ANA-VA) dengan tingkat kepercayaan 95% dan dilanjutkan dengan uji post Tukey
untuk melihat perbedaan nyata antar perlakuan. Analisis Statistik ini
BAB IV
HASIL DAN PEMBAHASAN
4.1 Karakteristik Simplisia
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense
Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia, Cibinong
me-nyebutkan bahwa tumbuhan yang digunakan adalah kulit kayu manis
Cinna-momum burmannii (Nees & T.Nees) Blume famili Lauraceae (Lampiran 1).
Hasil makroskopik kulit kayu manis berbentuk kayu batangan, agak
menggulung membujur, tebal kulit 1mm-3mm atau lebih, berwarna coklat
ke-merahan, bergaris-garis pucat, bekas patahan tidak rata dan berbau khas
aroma-tik. Hasil makroskopik madu berupa cairan kental menyerupai sirup, berwarna
coklat kemerahan, memiliki bau dan rasa yang khas (Lampiran 2).
Hasil mikroskopik simplisia kulit kayu manis adalah sklerenkim dan sel
minyak, sel batu, sklerenkim lepas dan hablur kalsium oksalat. Hasil
mi-kroskopik madu adalah memiliki serbuk sari (Lampiran 3).
Hasil penetapan kadar air simplisia madu cukup tinggi yakni sebesar
27,94%. Hal tersebut dikarenakan madu memiliki sifat higroskopis yaitu
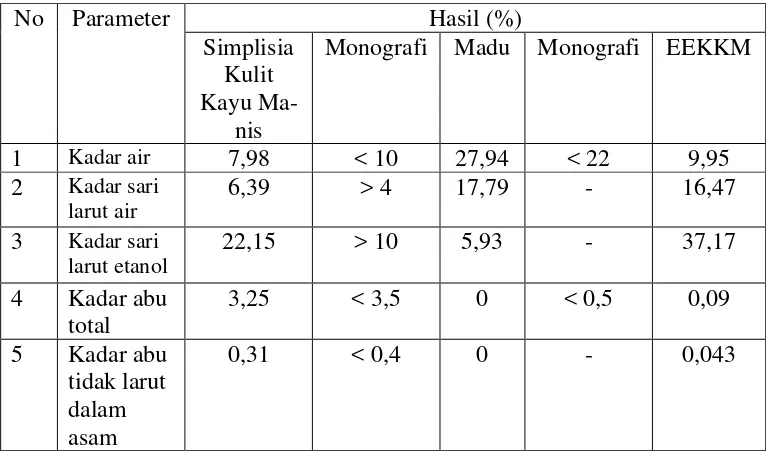
mu-dah menarik air (Tabel 4.1).
Tabel 4.1 Hasil penetapan kadar simplisia kulit kayu manis, madu, dan ek-strak etanol kulit kayu manis (EEKKM)
No Parameter Hasil (%)
Simplisia Kulit Kayu
Ma-nis
Monografi Madu Monografi EEKKM
1 Kadar air 7,98 < 10 27,94 < 22 9,95
Standarisasi simplisia untuk kulit kayu manis memenuhi syarat yang
tertera pada monografi buku Materi Medika Indonesia Jilid I dan Farmakope
Herbal Indonesia Edisi I, Madu memenuhi syarat yang tertera pada SNI 2010
kecuali parameter kadar air, dan EEKKM kering belum tertera pada monografi
buku Materi Medika Indonesia dan Farmakope Herbal Indonesia Edisi I,
se-hingga diharapkan untuk hasil karakterisasi ini dapat digunakan sebagai
pem-banding dalam pembuatan ekstrak.
4.2 Skrining Fitokimia
Tujuan dilakukannya skrining fitokimia adalah untuk mengetahui
se-nyawa metabolit sekunder yang terdapat dalam simplisia (Harborne, 1996).
Hasil skrining fitokimia terhadap simplisia kulit kayu manis mengandung
mengandung saponin. Hal ini mungkin senyawa golongan saponin rusak
selama proses ekstraksi. Hasil skrining fitokimia dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia simplisia kulit kayu manis, madu dan ek-strak etanol kulit kayu manis (EEKKM)
No Skrining Simplisia Kulit Kayu Manis
Ekstraksi serbuk kayu manis dilakukan dengan cara maserasi
menggu-nakan etanol 96%, dengan maksud agar kandungan kimia yang terdapat dalam
kulit kayu manis dapat tersari dengan sempurna dalam cairan penyari. Ekstrak
cair (maserat) dari 500 g serbuk simplisia kulit kayu manis yang dimaserasi,
dipekatkan dengan menggunakan rotary evaporator sehingga diperoleh ekstrak
kental lalu di keringkan dengan menggunakan freeze dryer sehingga diperoleh
ekstrak kering sebanyak 148 gram (rendemen 29,60%)
4.3 Hasil Uji Farmakologi
4.3.1 Hasil pengujian efek dengan metode uji toleransi glukosa
Pada penelitian ini subjek yang digunakan adalah tikus putih jantan
ga-lur Wistar dengan metode uji toleransi glukosa. Sebelum percobaan tikus
dipu-asakan selama 12 jam, tetapi air minum tetap diberi (Frode, 2008) lalu diukur
KGD puasa tikus. Berdasarkan hasil pengukuran KGD puasa rata-rata setiap
0) diperoleh nilai signifikansi (0,271) pada α = 0,05 yang menunjukkan tidak
terdapat perbedaan yang signifikan di antara kelompok kontrol, kelompok uji,
dan kelompok pembanding. Hal ini menunjukkan bahwa tikus yang digunakan
dalam kondisi fisiologis adalah homogen, yakni dalam kadar glukosa darah
puasa normal, sehingga dapat digunakan sebagai hewan uji. Hasil pengukuran
KGD puasa rata-rata dapat dilihat pada Tabel 4.3 dan hasil analisis statistik
ANAVA dapat dilihat pada Lampiran 27. Hewan uji kemudian dibagi menjadi
8 kelompok yaitu: kelompok suspensi Na-CMC 0,5% b/v sebanyak 1% bb;
suspensi EEKKM dosis 50 mg/kg bb; 100 mg/kg bb; 200 mg/kg bb; Madu 0,75
ml/kg bb; 1,5 ml/kg bb; 3 ml/kg bb dan suspensi glibenklamid 0,45 mg/kg bb.
Berdasarkan hasil pengukuran KGD rata-rata setiap kelompok tikus dan hasil
analisis statistik ANAVA setelah perlakuan (menit ke-30, 60, 90 dan 120)
di-peroleh nilai signifikansi (0,000) pada α = 0,05; ini berarti terdapat perbedaan
yang signifikan di antara setiap kelompok perlakuan terhadap penurunan kadar
glukosa darah yaitu di antara kelompok kontrol, kelompok uji dan kelompok
pembanding. Hasil pengukuran KGD rata-rata dapat dilihat pada Tabel 4.3 dan
Hasil analisis statistik ANAVA dapat dilihat pada Lampiran 27.
Berdasarkan hasil pengukuran KGD rata-rata setiap kelompok variasi
EEKKM maupun madu, diperoleh standar deviasi (SD) yang tidak jauh
berbeda pada masing-masing kelompok variasi mulai menit ke-30 sampai
menit ke-120. Begitu juga dari hasil uji Posthoc Tukey, kelompok variasi
EEKKM baik dosis 50; 100; maupun 200 mg/kg bb; kelompok variasi madu