HUBUNGAN PERDARAHAN INTRAVENTRIKEL
TERHADAP MORTALITAS 30 HARI PENDERITA
PERDARAHAN INTRASEREBRAL SPONTAN
TESIS
MICHAEL NORMAN JUSMAN
NIM. 097116002
PROGRAM MAGISTER KEDOKTERAN KLINIK
DEPARTEMEN ILMU BEDAH SARAF
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
LEMBAR PENGESAHAN
Judul Penelitian : Hubungan Perdarahan Intraventrikel Terhadap Mortalitas 30 Hari Penderita Perdarahan Intraserebral Spontan
Peneliti : Michael Norman Jusman
NIM : 097116002
Program Studi : Ilmu Bedah Saraf Hari/Tanggal :
Pembimbing 1 Pembimbing 2
DR. dr. Rr. Suzy Indharty, SpBS Prof. Dr. Iskandar Japardi, SpBS(K) NIP. 1944 0507 1977 031001 NIP. 1949 0331 1977 111001
Mengetahui / Mengesahkan :
Ketua Departemen Ilmu Bedah Saraf Ketua Program Studi Ilmu Bedah Saraf FK. USU / RSUP. HAM Medan FK. USU/ RSUP. HAM Medan
Sudah diperiksa hasil penelitian :
Judul Penelitian : Hubungan Perdarahan Intraventrikel Terhadap Mortalitas 30 Hari Penderita Perdarahan Intraserebral Spontan
Peneliti : Michael Norman Jusman
NIM : 097116002
Program Studi : Ilmu Bedah Saraf
Institusi : Fakultas Kedokteran Universitas Sumatera Utara
Medan, Oktober 2013 Konsultan Metodologi Penelitian
Fakultas Kedokteran Universitas Sumatera Utara
ABSTRAK
Tujuan: Studi ini mengkaji hubungan perdarahan intraventrikel dengan mortalitas tiga puluh hari penderita SICH
Metode: Penelitian ini merupakan penelitian analitik dengan pendekatan potong lintang (cross sectional) yang dilakukan mulai Januari 2011 sampai Agustus 2013 yang dilakukan di RSUP. H. Adam Malik Medan. Penderita yang menderita SICH
dengan perdarahan intraventrikel dengan onset kurang dari 48 jam dan memenuhi
kriteria inklusi, akan dinilai perdarahan intraventrikelnya berdasarkan gambaran
CT scan kepala. Sistim penilaian yang digunakan adalah sistim penilaian IVH,
Graeb dan LeRoux yang masing-masing dianalisis dengan hasil akhir mortalitas
30 hari.
Hasil: Dari analisis data diperoleh bahwa variabel volume perdarahan dan sistim penilaian Graeb yang memiliki nilai p (p value) mendekati 0.005 yaitu 0.06 yang menunjukan bahwa terdapat perbedaan bermakna antara pasien yang memiliki volume perdarahan yang besar dengan terjadinya kematian pada pemantauan 30 hari. Kemaknaan ini diikuti oleh sistim penilaian IVH (p=0.09) dan GCS (p=0,09).
ABSTRACT
Objective: This study evaluate the relationship between intraventricular hemorrhage with 30 day mortality rate in SICH patients.
Methods: This is an analytic study which used cross sectional method. This study was held in January 2011 until August 2013 in Adam Malik General Hospital. SICH patients were included in this study if the onset before 48 hours. Selected patients were evaluated based on they head CT scan appearance. We used three different scoring system, IVH score, Graeb score and LeRoux score to evaluate the severity of intraventricular hemorrhage. The result were analyzed with patient outcome by 30 day mortality rate.
Results: The study shows that bleeding volume and Graeb score had the closest significancy with p value 0.06 when analyzed with 30 day mortality rate. This significancy were followed with IVH score and GCS (p=0.09).
DAFTAR ISI
LEMBAR PENGESAHAN ... i
ABSTRAK ... iii
DAFTAR ISI ... vi
BAB 1 PENDAHULUAN A. LATAR BELAKANG PENELITIAN ... 1
B. RUMUSAN MASALAH ... 3
C. TUJUAN PENELITIAN ... 3
D. MANFAAT PENELITIAN ... 4
BAB II TINJAUAN PUSTAKA A. PERDARAHAN INTRASEREBRAL ... 5
B. PATOFISIOLOGI SICH ... 8
C. SISTEM VENTRIKEL ... 10
D. DINAMIKA CSF PADA IVH ... 11
E. MEKANISME KERUSAKAN OTAK AKIBAT IVH ... 12
F. PENATALAKSANAAN IVH ... 13
G. HIPERTENSI DAN HASIL AKHIR PENDERITA ICH ... 15
H. SICH DAN KOAGULOPATI ... 16
I. TINDAKAN OPERASI KRANIOTOMI EVAKUASI PADA PENDERITA SICH ... 20
K. CEDERA OTAK SEKUNDER PADA SICH ... 21
BAB III KERANGKA TEORI, KONSEP, HIPOTESIS A. KERANGKA TEORI ... 25
B. KERANGKA KONSEP ... 26
C. HIPOTESIS ... 26
BAB IV METODE PENELITIAN A. RANCANGAN PENELITIAN ... 27
B. WAKTU DAN TEMPAT PENELITIAN ... 27
C. POPULASI DAN SAMPEL PENELITIAN ... 27
D. KRITERIA SAMPEL PENELITIAN ... 28
E. BESAR SAMPEL PENELITIAN ... 29
F. ALUR PENELITIAN ... 30
G. CARA KERJA ... 30
H. BATASAN OPERASIONAL ... 33
I. ANALISIS DATA ... 38
BAB V HASIL PENELITIAN A. DISTRIBUSI BERDASARKAN USIA, GCS, JENIS KELAMIN DAN MORTALITAS ... 39
C. PERBEDAAN GCS, USIA, DAN VOLUME PERDARAHAN
TERHADAP MORTALITAS 30 HARI ... 42
BAB VI PEMBAHASAN ... 44
BAB VII SIMPULAN DAN SARAN A. SIMPULAN ... 47
B. SARAN ... 47
DAFTAR PUSTAKA ... 49
ABSTRACT
Objective: This study evaluate the relationship between intraventricular hemorrhage with 30 day mortality rate in SICH patients.
Methods: This is an analytic study which used cross sectional method. This study was held in January 2011 until August 2013 in Adam Malik General Hospital. SICH patients were included in this study if the onset before 48 hours. Selected patients were evaluated based on they head CT scan appearance. We used three different scoring system, IVH score, Graeb score and LeRoux score to evaluate the severity of intraventricular hemorrhage. The result were analyzed with patient outcome by 30 day mortality rate.
Results: The study shows that bleeding volume and Graeb score had the closest significancy with p value 0.06 when analyzed with 30 day mortality rate. This significancy were followed with IVH score and GCS (p=0.09).
BAB I PENDAHULUAN
A.Latar Belakang Penelitian
bermakna (Hallevi et al., 2009). Tindakan operasi dengan mengangkat bekuan darah yang berada didalam ventrikel dapat mengurangi inflamasi, hidrosefalus dan defisit fungsional pada penderita yang mengalami ICH (Hanley, 2009; Mayfrank et al., 2000; Pang et al, 1986; Wagner et al., 1999). Pemasangan External Ventricular Drain (EVD) dapat memberikan manfaat pada penderita
yang memiliki IVH yang berat, meskipun masih kontroversial (Nishikawa et al., 2009). Penderita yang dipasang EVD memiliki mortalitas dan hasil akhir yang sama dengan penderita yang tidak dipasang EVD (Tuhrim et al., 1991). Skor IVH, Graeb dan Le Roux digunakan untuk memperkirakan berat ringannya IVH berdasarkan gambaran perdarahan pada CT scan dan ada tidaknya dilatasi pada setiap ventrikel. Sistem penilaian ini bermanfaat untuk menilai IVH pada saat penderita datang ke Rumah Sakit, dan telah digunakan untuk menentukan berat ringannya IVH dan seleksi penderita dalam penelitian (Ruscalleda et al., 1986; Graeb et al., 1982; Le Roux et al., 1992; Nieuwkamp et al., 2000; Mayfrank et al., 2000). Ketiga sistem penilaian di atas memiliki ketepatan yang sama baik dalam memprediksi hasil akhir penderita ICH yang disertai IVH apabila digunakan pada saat penderita datang ke Rumah Sakit dan dalam 6 hari setelah onset serangan (Tuhrim et al., 1991)
ini memiliki pengaruh yang bermakna terhadap hasil akhir dan cedera sekunder yang akan terjadi (Tuhrim et al., 1991).
B.Rumusan Masalah
Berdasarkan uraian dalam latar belakang masalah tersebut diatas, dapat dirumuskan pertanyaan penelitian sebagai berikut:
Bagaimanakan hubungan IVH terhadap mortalitas tiga puluh hari penderita SICH?
C.Tujuan Penelitian 1. Tujuan Umum
Untuk mengkaji hubungan derajat IVH dan GCS awal dengan mortalitas tiga puluh hari penderita SICH
2. Tujuan Khusus
a. Melihat hubungan sistem penilaian IVH dengan mortalitas tiga puluh hari penderita SICH
b. Melihat hubungan sistem penilaian Graeb dengan mortalitas tiga puluh hari penderita SICH
c. Melihat hubungan sistem penilaian Le Roux dengan mortalitas tiga puluh hari penderita SICH
D. Manfaat Penelitian
1. Dampak dari IVH telah dilaporkan oleh beberapa penelitian sebagai prediktor independen hasil akhir yang buruk dan meningkatkan risiko kematian. Beberapa sistem penilaian berat ringannya IVH telah dikenal dan digunakan secara terpisah. Dalam penelitian ini penulis ingin mengetahui hubungan antara berat ringannya IVH terhadap mortalitas tiga puluh hari dengan menggunakan ketiga sistem penilaian yang berbeda.
BAB II
TINJAUAN PUSTAKA
A. Perdarahan Intraserebral (SICH)
Selain beberapa faktor prognosis diatas, dikenal juga istilah END (early neurological deterioration), yang terjadi pada 20% hingga 40% penderita SICH,
dan berhubungan dengan prognosis yang buruk (Lisk et al., 1994). Prediktor independen dari END antara lain suhu tubuh, hitung neutrofil, dan kadar fibrinogen plasma yang tinggi. Hipertermia merupakan dampak dari reaksi fase akut dan inflamasi. Kadar fibrinogen mencerminkan aktivasi mekanisme inflamasi yang menyebabkan kerusakan jaringan di sekitar hematoma.
Secara klinis mayoritas penderita SICH datang dengan penurunan kesadaran akibat peningkatan ICP dan atau penekanan langsung atau distorsi thalamus atau RAS (Reticular Activating System) di batang otak. Presentasi klinis penderita SICH disamping penurunan kesadaran tergantung dari lokasi hematoma.
Tabel 1. Tabel karakteristik klinis penderita SICH berdasarkan lokasi perdarahan Jenis
perdarahan
Lokasi Tampilan klinis
Supratentorial Putaminal
Thalamic
Hemiparesis dan hemisensory loss, hemianopia & disfasia (apabila hemisfer dominan terlibat), deviasi konjugat ke sisi yang mengalami perdarahan)
Infratentorial
Occipital: nyeri bola mata ipsilateral & defisit lapangan pandang; temporal: disfasia, ganguan lapangan pandang & nyeri telinga; frontal: nyeri kepala & hemiparesis; parietal: nyeri kepala di temporal anterior & hemisensory loss
Mual muntah yang mendadak, ataksia, nistagmus, dismetria, kelemahan otot wajah Bila berukuran kecil, dapat menyebabkan paralisis dan dapat berhubungan dengan pergerakan bola mata (lock-in state), bila berukuran besar dapat menyebabkan koma, kuadriplegia, rigiditas deserebrasi & pupil yang pinpoint
Meningismus & penurunan kesadaran
hematoma intraventrikel akan mengurangi respons inflamasi, hidrosefalus dan defisit fungsional jangka panjang.
B. Patofisiologi SICH
Efek ICH terhadap jaringan otak bersifat bifasik. Pada fase awal, cedera terjadi akibat efek massa dari hematoma (Aronowski et al., 2005). ICH menyebabkan peningkatan tekanan intrakranial/ intracranial pressure (ICP), yang kemudian akan menyebabkan herniasi transtentorial (Badjatia et al., 2005). Pada fase berikutnya melibatkan faktor-faktor komponen darah yang sifatnya merusak, infiltrasi sel-sel imun sistemik ke dalam jaringan otak, aktivasi mikroglia, dan proses apoptosis yang diinduksi oleh hematoma, kerusakan progresif dari sawar darah otak/ blood brain barrier (BBB) dan meningkatnya edema otak (Xi et al., 1998; Xue et al., 2003; Wang et al., 2005; Felberg et al., 2002; Qureshi et al., 2001).
Respons inflamasi pada SICH ditandai dengan aktivasi sel-sel imun lokal seperti sel mikroglia. Proses inflamasi akut dapat terlihat dalam 4 jam setelah ICH pada model hewan coba, dan reaksi inflamasi lokal ini berperan dalam kerusakan otak (Wang et al., 2007). Leukosit yang berasal dari sirkulasi darah merupakan sumber utama dari kerusakan yang terjadi. Infiltrasi dari sel-sel imun yang bersirkulasi sistemik ini memperburuk kerusakan BBB. Hal ini menyebabkan terjadinya edema (Aronowski et al., 2005; Gong et al., 2000; Ma et al., 2011).
molecule-1 (sICAM-1), soluble endothelial selectin (sE-selectin), dan soluble platelet selectin (sP-selectin) yang mengikat leukosit-leukosit yang ada didalam
sirkulasi sehingga leukosit-leukosit tersebut melakukan migrasi kedalam daerah otak yang telah mengalami iskemia (Yilmaz et al., 2008). Molekul adhesi seperti sICAM-1 dan soluble vascular cell adhesion molecule-1 (sVCAM-1) merupakan parameter pro-inflamasi terhadap terjadinya aktivasi sistem imun (Bevilacque et al., 1993). Peranan molekul-molekul adhesi ini sebenarnya dalam kondisi fisiologis adalah mengatur kontak antar sel (Springer, 1990). Pengerahan dari sel-sel mononuklear yang berada di sirkulasi perifer merupakan langkah penting pada awal terjadinya inflamasi di otak (Hafler & Weiner, 1989). Molekul-molekul adhesi ini juga berperan dalam kondisi patologis seperti pada penyakit serebrovaskular (Endres et al., 1997). sICAM-1 dan sVCAM-1 dilaporkan meningkat kadarnya didalam cairan serebrospinal/ cerebrospinal fluid (CSF) yang diperoleh dari dalam ventrikel pada penderita SICH, yang berhubungan dengan hasil akhir yang buruk (Kraus et al., 2002).
Meskipun EVD dianggap sebagai pertolongan pertama pada kelompok penderita IVH yang mengalami hidrosefalus akut, ternyata tidak didapatkan hubungan antara peningkatan ICP atau kontrol ICP terhadap perburukan atau perbaikan neurologis (Adams et al., 1998). Peningkatan ICP pada IVH kemungkinan juga disebabkan oleh hal-hal lain disamping akibat hidrosefalus akut (Coplin et al., 1998).
Seringkali terdapat asumsi bahwa koma ataupun kematian yang terjadi pada penderita IVH merupakan akibat dari peningkatan ICP yang akut yang kemudian mencederai reticular activating system (RAS) atau menyebabkan gangguan perfusi otak. Meskipun volume IVH yang lebih besar dan derajat dilatasi ventrikel yang lebih berat pada pemeriksaan CT scan awal berhubungan dengan hasil akhir yang buruk, tidak dijumpai hubungan antara ICP terhadap hasil akhir penderita IVH (Diringer et al., 1998).
C. Sistem Ventrikel
lokasinya cukup dalam dari permukaan otak yang berdekatan dengan ventrikel juga dapat ruptur mengisi ke ruang ventrikel dan mengganggu regulasi tekanan intrakranial. Rupturnya darah ke dalam ventrikel akan menimbulkan penurunan kesadaran secara klinis dan seringkali menyebabkan kematian (Qureshi et al., 1995).
Fasilitas pemeriksaan CT scan dan ICP monitoring kini memungkinkan pengukuran IVH baik secara kuantitatif serta efeknya terhadap ICP (Graeb et al., 1982; Naff et al., 2000; Zimmerman et al., 2006; Janny et al., 1982). Meskipun penatalaksanaan IVH secara akademis dilakukan dengan melakukan kontrol ICP dan drainase IVH hingga sistem ventrikel lancar kembali, hingga saat ini belum ada penelitian randomized control trial (RCT) dalam skala besar yang menguji manfaat dari tindakan tersebut (Broderick et al., 2007; Steiner et al., 2006).
D. Dinamika CSF pada IVH
utama dalam terjadinya hidrosefalus, tetapi ada faktor-faktor lain seperti komposisi biokimiawi jaringan periventrikel terhadap proses terjadinya dilatasi sistim ventrikel.
E. Mekanisme Kerusakan Otak Akibat IVH
F. Penatalaksanaan IVH: Alasan Rasional dan Evidence Based
Usaha mengobati IVH pada awalnya difokuskan untuk mengurangi ICP yang meningkat. Alasan pengobatan IVH ini cukup beralasan, karena ICP yang tinggi akan mengakibatkan herniasi dan iskemia, yang merupakan dua dampak yang sering terjadi pada IVH. Meskipun demikian, beberapa laporan menunjukan bahwa pengelolaan ICP yang dilakukan tidak memberikan perbaikan kesadaran dan fungsional ataupun mortalitas (Adams & Diringer, 1998; Misra et al., 2005). Sementara itu, penelitian lain melaporkan bahwa pengendalian ICP mampu memperbaiki gejala-gejala herniasi dan memperbaiki hasil akhir (Qureshi et al., 2000). Penelitian yang dilakukan dalam skala besar seperti STICH dan FVIIa, NovoSeven tidak memberikan pernyataan spesifik mengenai tindakan evakuasi IVH maupun target pengendalian ICP. Pada CLEAR IVH trial dilaporkan bahwa pengobatan IVH dengan memberikan r-TPA melalui kateter mampu mengurangi mortalitas. Evakuasi hematoma diharapkan mampu mengurangi cedera sekunder akibat efek negatif dari hematoma tersebut. Secara biologis diperkirakan tindakan tersebut mampu memblokir aktivasi inflamasi dan kematian sel yang diperantarai oleh aktivasi trombin, pembersihan dari sisa-sisa besi bebas, dan meningkatkan fagositosis dari eritrosit yang mengalami pembekuan (Xi et al., 1998; Xi et al., 2006; Zhao et al., 2007).
menyuntikan obat-obat trombolitik. Metode langsung adalah dengan melakukan kraniotomi untuk menciptakan akses ke ventrikel lateralis untuk mengangkat hematoma dibawah visualisasi langsung. Metode tidak langsung merupakan metode yang kurang invasif, tetapi cukup sulit untuk mengidentifikasi sumber perdarahan. Akses transkortikal untuk mencapai ventrikel lateralis terdiri dari beberapa approach: frontal, temporal, parietal dan occipital (Piepmeier et al., 1993; Timurkaynak et al., 1986). Pengangkatan hematoma menggunakan frontal approach menuju kornu inferior sangat sulit. Jarak antara kornu posterior melalui parietal approach cukup jauh dan cukup sulit untuk melakukan pengangkatan hematoma melalui kornu anterior dan inferior. Temporal approach sangat bermanfaat untuk pengangkatan hematoma di kornu inferior, tetapi tidak dapat mengkonfirmasi lesi yang berada di kornu anterior. Occipital approach cukup baik untuk mencapai kornu posterior karena pada ventrikel yang dilatasi, jarak tersebut cukup pendek dan memungkinkan untuk menilai seluruh bagian dari ventrikel lateralis. Dikenal juga high occipital approach yang dinilai lebih baik karena jarak dengan kornu posterior lebih dekat dibandingkan dengan occipital approach (Onoda et al., 2001).
membeku (clotting). Untuk menghindari hal tersebut, beberapa ahli menggunakan obat-obat fibrinolitik seperti urokinase.
Disamping pemasangan EVD dan tindakan operasi, dikenal juga metode lain untuk melakukan pengangkatan IVH, yakni aspirasi dengan endoskopi (Chen et al., 2011; Hamada et al., 2008; Longatti et al., 2005; Nishikawa et al., 2007; Nishikawa et al., 2008; Zhang et al., 2007). Dengan tehnik ini juga dikenal penggunaan rigid dan flexible instument dengan segala kelebihan dan kekurangannya masing-masing. Pada tehnik ini, keberhasilan atau hasil akhir sangat dipengaruhi oleh ada tidaknya sisa IVH di akuaduktus syilvii dan ventrikel IV (Saphiro et al., 1994).
G. Hipertensi dan Hasil Akhir Penderita ICH
Tekanan darah seringkali mengalami peningkatan pada penderita yang mengalami ICH. Mekanisme patofisiologi yang melandasi terjadinya peningkatan tekanan darah ini adalah akibat respons stress tubuh melalui sistem neuroendokrin (sistem saraf simpatik, aksis renin-angiotensin, atau sistem glukokortikoid) dan akibat respons peningkatan tekanan intrakranial. Secara teoritis, hipertensi juga berperan dalam meluasnya hematoma intraserebral, edema perihematoma, dan terjadinya perdarahan ulang yang pada akhirnya memberikan hasil akhir yang buruk bagi penderita SICH.
sistolik antara 150 hingga 220 mm Hg cukup aman apabila dilakukan penurunan tekanan darah yang akut hingga 140 mm Hg (Class IIa; Level of Evidence: B).
Apabila tekanan darah sistolik > 200 mm Hg atau MAP diatas 150 mm Hg, maka penurunan tekanan darah yang agresif menggunakan antihipertensi intravena yang diberikan melalui infus kontinyu dapat diberikan dengan melakukan pemantauan tekanan darah setiap 5 menit. Apabila tekanan darah sistolik > 180 mm Hg atau MAP diatas 130 mm Hg kemungkinan besar terjadi peningkatan ICP yang perlu dimonitor dan dilakukan penurunan tekanan darah dengan antihipertensi intravena yang diberikan secara intermiten untuk
mempertahankan CPP ≥ 60 mm Hg. Apabila tekanan darah sistolik > 180 mm Hg
atau MAP diatas 130 mm Hg kemungkinan besar terjadi peningkatan ICP yang perlu dimonitor dan dilakukan penurunan tekanan darah dapat diberikan lebih bertahap misalnya dengan target MAP 110 mm Hg atau tekanan darah 160/ 90 mm Hg menggunakan antihipertensi intravena kontinyu dengan melakukan pengukuran ulang setiap 15 menit (Class C).
H. SICH dan Koagulopati
Koagulopati atau gangguan perdarahan hanya terjadi pada sebagian kecil penderita, tetapi merupakan faktor risiko yang bermakna terhadap terjadinya SICH. Kondisi seperti hemofilia dan leukemia akut berhubungan dengan trombositopenia, perdarahan intrakranial masif yang sering menjadi penyebab utama kematian (Kerr, 1964; McCormick & Rosenfield, 1973).
Proses koagulasi dan hemostasis yang dimediasi trombosit merupakan dua mekanisme pertahanan terhadap perdarahan. Kaskade koagulasi segera dikerahkan setelah terjadi kontak langsung antara darah dengan lapisan endotel yang mengalami cedera. Respons kaskade koagulasi idealnya berkoordinasi dengan pembentukan plak trombosit yang awalnya menutup lesi pada pembuluh darah. Di susunan saraf pusat, ketidakseimbangan antara sistim yang pro- dengan anti-koagulan akibat faktor yang didapat maupun yang diturunkan dapat menyebabkan kelainan trombosis ataupun perdarahan.
Koagulopati dapat menyebabkan perdarahan intrakranial dibagi menjadi kelainan yang didapat dan kelainan kongenital. Koagulopati yang didapat pada umumnya merupakan akibat dari obat-obat seperti aspirin, antikoagulan, dan agen trombolitik. Koagulopati yang didapat yang lain antara lain akibat: 1) neoplasma; 2) ITP (Idiopathic Trombositopenic Purpura) dan 3) Trombositopenia yang disebabkan oleh alkohol, kelainan hepar dan ginjal, maupun obat-obat yang lain. Kelainan kongenital yang dapat menyebabkan SICH antara lain hemofilia A, hemofilia B, dan penyakit jarang yang lainnya.
irreversible sehingga mengurangi produksi platelet agreggant alami thromboxane A2 (Vane, 1971). Inhibisi ini membuat aspirin menjadi agen antiplatelet yang sangat baik secara klinis. Pada pasien-pasien yang menderita infark miokard akut dan penyakit oklusi kardiovaskular, obat aspirin mengurangi risiko infark miokard non fatal, stroke non fatal, dan kematian yang disebabkan oleh penyakit vaskular. Aspirin juga dapat mengurangi serangan infark miokard pertama pada pria (Gaziano et al, 2000).
Physician’s Health Study melaporkan terdapat 23 kasus stroke hemoragik
pada 11,037 penderita yang mengkonsumsi aspirin dosis rendah (325 mg setiap harinya) dibandingkan dengan 12 stroke hemoragik pada 11,034 pasien yang
menerima plasebo ( Steering Committee of the Physicians’ Health Study Research
Group, 1996).
SICH yang disebabkan oleh antikoagulan terjadi sekitar 10% hingga 20% ( Kase, 1986; Mohr et al., 1978; Yarnell & Earnest, 1976)
Lokasi perdarahan pada penderita yang mengkonsumsi antikoagulan sebagaian terjadi di intraserebral, dan hanya sebagian kecil bermanifestasi sebagai perdarahan subdural (Subdural hemorrhage/ SDH). Target INR 2.5 hingga 4.5 pada pengobatan antikoagulan meningkatkan risiko tahunan SICH sebesar tujuh hingga sepuluh kali pilat (Hart et al, 1995)
radiologi pertama kali (Hart et al., 1995). Angka mortalitas SICH akibat antikoagulan adalah 60% (Hart et al., 1995).
Mekanisme terjadinya SICH akibat antikoagulan masih belum jelas. Pada pemeriksaan autopsi pada penderita lansia yang memiliki riwayat hipertensi sering didapati pengumpulan hemosiderin yang menunjukan adanya vaskulopati pembuluh darah berkaliber kecil (Cole & Yates, 1967).
Tabel 2. Uji Tapis Laboratorium untuk kelainan perdarahan
Pemeriksaan Laboratorium Kelainan Perdarahan
Interaksi antara trombosit dan pembuluh darah
Penggunaan warfarin, defisiensi faktor I, II, V, VII dan X
Penggunaan heparin; defisiensi seluruh faktor koagulasi, terutama faktorVIII & IX, kecuali faktor VII
I. Tindakan Operasi Kraniotomi Evakuasi Pada Penderita SICH
Hingga saat ini manfaat tindakan operasi dikatakan belum jelas terlihat (Class IIb; Level of Evidence: C), kecuali pada penderita yang mengalami perdarahan di serebelum yang mengalami deteriorasi neurologis atau mengalami penekanan batang otak dan/ atau yang mengalami hidrosefalus akibat obstruksi sistem ventrikel, perlu dilakukan evakuasi hematoma sesegera mungkin (Class I; Level of Evidence: B). Tindakan pertolongan pertama pada kelompok penderita diatas hanya dengan melakukan pemasangan EVD saja tanpa melakukan evakuasi hematoma, tidak dianjurkan (Class III; Level of Evidence: C). Pada penderita yang mengalami perdarahan lobar > 30 mL dan lokasinya 1 cm dari permukaan korteks maka perlu dipertimbangkan untuk kraniotomi evakuasi hematoma (Class IIb; Level of Evidence: B).
J. Tindakan Hemikraniektomi Dekompresi pada SICH
dengan melakukan pembukaan tulang kepala dan tulang tersebut tidak dikembalikan/ disimpan untuk sementara waktu untuk memberikan waktu bagi otak yang sedang mengalami edema untuk mendapatkan penambahan ruang, sehingga tidak terjadi pergeseran jaringan otak didalam kranium yang dapat menyebabkan herniasi yang mengancam jiwa. Disamping memberikan manfaat untuk mengurangi ICP yang tinggi, prosedur ini juga dapat meningkatkan compliance jaringan otak, cadangan oksigen otak, dan perfusi otak (Aarabi, 2006;
Kontopoulos, 2002; Schaller, 2003). Prosedur ini lebih banyak digunakan pada kasus cedera kepala berat, perdarahan subarachnoid yang hebat akibat ruptur aneurisma dan pada infark serebri yang berat. Sedangkan penggunaan prosedur in ipada kasus SICH masih jarang. Meskipun demikian, hemikraniektomi dekompresi dilaporkan dapat meningkatkan hasil akhir pada model ICH hewan (tikus), dan beberapa penelitian juga melaporkan manfaat prosedur ini pada SICH yang luas (Marinkovic, 2009; Dierssen, 1983; Fung, 2012; Kim, 2009; Ma, 2010; Maira, 2002; Murthy, 2005; Ramnarayan, 2009; Shimamura, 2011; Takeuchi, 2013).
K. Cedera Otak Sekunder pada SICH
perluasan hematom (Anderson, 2010; Anderson, 2008; Qureshi, 2007; Qureshi, 2011).
Pada hitungan jam setelah terjadinya perdarahan intraserebral, efek massa dari hematoma secara mekanik merusak struktur neuron dan membran sel glia yang berada di sekitarnya, sehingga terjadi influks ion kalsium dan pelepasan neurotransmiter eksitatorik (Xi, 2006). Hal ini menyebabkan nekrosis dan edema sitotoksik (Keep, 2005). Homeostasis menjadi terganggu pada tingkat selular dan proses kerusakan terus berlanjut. Cedera otak sekunder akibat SICH diakibatkan oleh efek toksik selular, disrupsi BBB, edema vasogenik, dan upregulation dari mediator inflamasi (Hwang, 2011).
Aktivasi kaskade koagulasi akan mencetuskan pembentukan trombin (Hwang, 2011). Trombin pada awalnya membatasi perluasan hematoma dan pada konsentrasi yang rendah merangsang heat shock protein dan iron scavanger. Pada konsentrasi yang tinggi seperti pada SICH, trombin akan menginisiasi beberapa jalur yang sifatnya destruktif (Hua, 2009).
Trombin merangsang sel glia untuk memproduksi sitokin-sitokin inflamasi. Upregulation TNF-α akibat disrupsi integritas BBB, apoptosis, dan recruitment mediator-mediator pro-inflamasi (Barone, 1999; Hua, 2007).
Upregulation beberapa MMP menyebakan terjadinya degradasi matriks
ekstraselular (Giancotti, 1999; Hwang, 2011).
hipoperfusi regional akibat penekanan pembuluh-pembuluh darah disekitarnya (Thiex, 2007). Hal ini akan menyebabkan gangguan pembentukan adenosine triphosphate, gangguan regulasi ion dan neurotransmiter, dan pembentukan radikal bebas (Siesjo, 1988).
kaskade komplemen yang diinisiasi oleh trombin meningkatkan migrasi sel inflamasi melalui anafilatoksin dan destruksi selular secara langsung melalui membrane attack complex. Lisis sel-sel endotel melalui membrane attack complex
pada akhirya menyebabkan disrupsi BBB lebih lanjut (Hua, 2000). Besi yang dilepaskan dari lisis sel darah merah dan radikal bebas yang dihasilkan oleh sel-sel inflamasi akan menghasilkan stres oksidatif, yang kemudian menyebabkan kematian sel dan kerusakan BBB lebih lanjut (Babu, 2012; Hwang, 2011).
klinis dan menunjukan bukt-bukti pemulihan spontan (Leonardo, 2012; Grasso, 2009; Hua, 2006; Hua, 2000).
BAB III
KERANGKA TEORI, KERANGKA KONSEP, HIPOTESIS PENELITIAN
B. Kerangka Konsep
C. Hipotesis
1. Hipotesis mayor
Derajat IVH dan nilai GCS awal pada penderita SICH
berhubungan dengan mortalitas tiga puluh hari.
2. Hipotesis minor
a. Skor IVH berhubungan dengan mortalitas tiga puluh hari
penderita SICH
b. Skor Graeb berhubungan dengan mortalitas tiga puluh hari
penderita SICH
c. Skor Le Roux berhubungan dengan mortalitas tiga puluh hari
penderita SICH
d. Nilai GCS penderita pada awal masuk rumah sakit berhubungan
dengan mortalitas tiga puluh hari penderita SICH
Variabel Bebas Variabel Tergantung
Mortalitas tiga puluh hari Skor Graeb
Skor IVH
Skor Le Roux
Volume ICH
BAB IV
METODE PENELITIAN
A. Rancangan Penelitian
Penelitian ini merupakan penelitian analitik dengan pendekatan
potong lintang (cross sectional). Pada subjek penelitian dilakukan pengamatan pada saat subjek tersebut datang berobat ke RSUP. H. Adam
Malik dan dilakukan seleksi berdasarkan kriteria inklusi dan eksklusi.
Subjek penelitian yang terpilih kemudian dilakukan pengamatan mengenai
GCS, beberapa variabel yang dapat dinilai dari gambaran CT scan kepala
dan pengamatan selama 30 hari masa perawatan di RS.
B. Waktu dan Tempat Penelitian
Waktu penelitian mulai Januari 2011 sampai Agustus 2013.
Tempat peneltian adalah Departemen Ilmu Bedah Saraf RSUP H Adam
Malik Medan.
C. Populasi dan Sampel Penelitian
1. Populasi Target
Populasi yang dilakukan generalisasi/inferensialnya yaitu seluruh
2. Populasi Terjangkau
Kumpulan dari satuan/unit yang dilakukan pengambilan sampel
penelitian, yaitu penderita SICH yang dirawat di RSUP H. Adam
Malik Medan.
3. Sampel Penelitian
Bagian dari populasi terjangkau yang diambil untuk dilakukan
pengukuran, yaitu penderita SICH yang mengalami IVH yang
dirawat di RSUP H. Adam Malik Medan. Sampel penelitian
diambil dengan cara consecutive sampling dengan penetapan kriteria inklusi dan kriteria eksklusi.
D. Kriteria Sampel Penelitian
1. Kriteria Inklusi
a. Penderita perdarahan intraserebral spontan yang dirawat di
RSUP. H. Adam Malik
b. Usia penderita diatas 30 tahun
c. Mengalami serangan dalam kurun waktu 48 jam
d. Merupakan serangan perdarahan intraserebral yang pertama
kali
e. Sedang menderita atau dengan riwayat hipertensi
2. Kriteria eksklusi
intraserebral akibat penyakit primer seperti AVM,
aneurisma dan sebagainya
b. Adanya riwayat penggunaan antikoagulan atau koagulopati
3. Kriteria drop-out
a. Pasien pulang atas permintaan sendiri selama waktu
pemantauan dilakukan
b. Tidak dapat menyelesaikan prosedur penelitian karena
ketidaklengkapan data
E. Besar Sampel Penelitian
Besar sampel dihitung berdasarkan rumus uji hipotesis satu
populasi sebagai berikut:
P0 : 0,5
Pα : 0.75
Berdasarkan rumus di atas, didapat bahwa besar sampel satu
kelompok minimal 29 orang.
n
(P0 - P )2
F. Alur Penelitian
G. Cara Kerja
1. Dimulai dengan identifikasi karakteristik subjek penderita SICH dengan
onset > 48 jam berdasarkan anamnesis, baik secara autoanamnesis maupun
secara aloanamnesis.
2. Kemudian dilakukan evaluasi terhadap airway, breathing dan circulation. a. Airway: bila airway tidak paten, dilakukan pemasangan
oropharyngeal atau nasopharyngeal airway. Pemasangan dilakukan oleh Peserta Program Pendidikan Dokter Spesialis
Anestesi dan Perawatan Intensif yang memiliki telah terlatih
b. Breathing: respirasi dinilai dengan laju respirasi dan saturasi oksigen, apabila laju respirasi > 20 kali/ menit dengan atau tanpa
disertai penurunan saturasi oksigen < 98% maka akan diberikan
suplementasi oksigen dengan nasal kanula atau face mask sesuai dengan kebutuhan (dengan target RR: 20 kali/ menit atau saturasi
Penderita masuk (seleksi kriteria)
Subjek penelitian:
1. Penanganan SICH secara komprehensif (tindakan operatif sesuai indikasi)
2. Dokumentasi variabel bebas
Penilaian mortalitas tiga puluh hari
oksigen > 98%). Pemasangan alat bantu nafas mekanik (ventilator) bila memenuhi kriteria gagal nafas.
c. Circulation: Sirkulasi dinilai berdasarkan frekuensi nadi, tekanan darah, dan tekanan vena sentral apabila diperlukan. Tekanan darah
diukur dengan spigmomanometer secara manual pada Korotkoff I
dan IV. Frekuensi nadi dinilai secara manual berdasarkan palpasi
arteri radialis. Tekanan vena sentral dinilai jika penderita berada di
ICU. Target tekanan darah adalah 140/ 90 mm Hg. Pada keadaan
krisis hipertensi, tekanan darah diturunkan dengan memberikan
perdipine intravena.
3. Kemudian dilakukan pemeriksaan laboratorium, radiologi dan
elektrokardiografi (EKG)
4. Pemeriksaan laboratorium standar yang dilakukan antara lain adalah darah
lengkap, analisis gas darah, kadar gula darah sewaktu, elektrolit darah,
fungsi hati, fungsi ginjal, dan skrining fungsi pembekuan darah.
Pemeriksaan radiologi yang standar dilakukan adalah X-ray Thoraks AP
dan CT Scan Kepala. CT Scan yang digunakan adalah Hitachiseri W 450. Pemeriksaan penunjang, baik radiologi dan laboratorium dapat bertambah
jika memang diindikasikan. Penilaian Thoraks AP dilakukan oleh seorang
ahli radiologi yang berpengalaman. EKG dinilai oleh Peserta Program
Pendidikan Dokter Spesialis Kardiologi yang berpengalaman. Penilaian
bedah saraf yang berpengalaman. Beberapa hal yang dinilai pada
gambaran CT Scan kepala adalah sebagai berikut: a. Volume dan lokasi SICH
b. Derajat IVH menurut skor IVH, skor Graeb dan skor Le Roux
c. Ada tidaknya hidrosefalus menurut rasio Evan
5. Riwayat penggunaan antikoagulan dan koagulopati disingkirkan melalui
anamnesis
6. Penatalaksanaan konservatif terhadap penderita SICH meliputi:
a. Pemberian Mannitol 20% secara bolus dengan dosis 0,5-1 gram dalam 10 menit. Sebelumnya dilakukan pemeriksaan osmolaritas
serum dengan batas maksimal 320 mmol/l untuk mencegah gagal
ginjal. Osmolaritas dihitung berdasarkan kadar ureum, elektrolit,
dan kadar gula sewaktu.
b. Pemberian Gastric Mucosal Protector dan Acid Supressor Agent
dengan H2 Blocker, PPI (proton Pump Inhibitor) dan gastric mucosal protector.
c. Nutrisi diberikan sesegera mungkin dengan target 120% dari BMR
dengan kebutuhan protein 1,5 gram/kgBB. Diet diberikan dalam
bentuk makanan cair melalui selang nasogastrik, empat sampai
lima kali sehari.
7. Bila penderita memenuhi indikasi operasi, maka dilakukan tindakan
operasi. Indikasi operasi ditetapkan berdasarkan kriteria sebagai berikut
(Morgenstern, 2010):
a. Perdarahan serebelum dengan perburukan neurologis atau
penekanan batang otak dengan atau tanpa hidrosefalus
akibat obstruksi ventrikel
b. Perdarahan lobar dengan volume > 30 cc dengan jarak 1 cm
dari permukaan
8. Penderita dinyatakan boleh pulang apabila memiliki Glasgow Outcome Scale (GOS) setidaknya empat.
9. Jika penderita meninggal dalam tiga puluh hari pertama, penderita
dimasukkan ke dalam kelompok mortalitas dalam tiga puluh hari
10. Setelah penderita pulang, dilakukan pencatatan lama rawatan.
H. Batasan Operasional
1. GCS awal sesudah resusitasi
a) Definisi : merupakan tingkat kesadaran penderita cedera kepala setelah
dilakukan resusitasi (stabilisasi patensi airway, breathing dan
b) Alat ukur : Glasgow Coma Scale (GCS)
c) Cara ukur : Ada tiga komponen dalam GCS, yaitu respon bukan mata,
respon motorik, dan respon verbal. GCS merupakan penjumlahan dari
ketiga komponen tersebut.
kata-kata tidak teratur 3
tidak jelas 2
tidak ada 1
Berdasarkan GCS, penderita kemudian dikelompokkan
menjadi tiga, yaitu: kelompok cedera kepala ringan (GCS 14-15),
kelompok cedera kepala sedang ( GCS 9-13), dan kelompok cedera
kepala berat (GCS 3-8)
2. Skor IVH
a. Definisi: Sistim penilaian untuk menentukan derajat berat
ringannya IVH
b. Alat ukur: Skor IVH
c. Cara ukur: Skor IVH berkisar antara 0 hingga 23. Untuk ventrikel
lateralis kanan dan kiri masing masing menggunakan nilai 0-4. 0:
tidak dijumpai perdarahan pada sistim ventrikel lateralis. 1: kurang
dari 1/3 ventrikel lateralis terisi darah. 2: 1/3 hingga 2/3 ventrikel
lateralis terisi darah. 3: lebih dari 2/3 ventrikel lateralis terisi darah.
4: seluruh ventrikel lateralis penuh terisi darah. Berdasarkan ada
tidaknya hidrosefalus, nilai 0: tidak dijumpai gambaran
hidrosefalus pada sistim ventrikel. 1: dijumpai gambaran
hidrosefalus pada sistim ventrikel. Untuk ventrikel tiga dan empat,
nilai 0: tidak dijumpai perdarahan sedangkan nilai 1: dijumpai
perdarahan. Kalkulasi skor IVH mengikuti rumus sebagai berikut:
3 x (skor ventrikel lateralis kanan + skor ventrikel lateralis kiri +
ada tidaknya hidrosefalus) + skor pada ventrikel 3 + skor pada
ventrikel 4
d. Skala ukur: skala nominal (variabel kategorik)
3. Skor Graeb
a. Definisi: Salah satu sistim penilaian untuk menentukan derajat
berat ringannya IVH
c. Cara ukur: Skor Graeb berkisar antara 0 – 12. Untuk ventrikel
lateralis kanan dan kiri, nilai 0: tidak dijumpai adanya perdarahan
pada sistim ventrikel lateralis, 1: dijumpai sedikit perdarahan pada
sistim ventrikel lateralis, 2: < 50% ventrikel lateralis terisi darah, 3:
> 50% ventrikel lateralis terisi darah, 4: ventrikel lateralis penuh
terisi darah dan melebar. Untuk ventrikel tiga dan empat, nilai 0:
tidak dijumpai adanya perdarahan pada ventrikel, 1: dijumpai
perdarahan pada ventrikel tetapi tidak melebar, 2: dijumpai
perdarahan pada ventrikel dan ventrikel tampak melebar.
d. Skala ukur: skala nominal (variabel kategorik)
4. Skor Le Roux
a. Definisi: Salah satu sistim penilaian untuk menentukan derajat berat
ringannya IVH
b. Alat ukur: Skor Le Roux
c. Cara ukur: Skor Le Roux berkisar antara 0 – 16. Untuk seluruh sistim
ventrikel, nilai 0: tidak dijumpai adanya perdarahan pada sistim
ventrikel, 1: dijumpai sedikit perdarahan pada sistim ventrikel, 2:
kurang dari 50% ventrikel terisi perdarahan, 3: lebih dari 50%
ventrikel terisi perdarahan, 4: seluruh ventrikel terisi darah dan
melebar
5. Hidrosefalus
a. Definisi: pelebaran sistim ventrikel yang disertai dengan gejala
peningkatan tekanan intrakranial seperti pandangan kabur, penurunan
kesadaran, nyeri kepala persisten serta tanda-tanda klinis seperti edema
papil dan trias Cushing (hipertensi, takikardia dan pola pernafasan
yang tidak teratur)
b. Alat ukur: CT Scan
c. Cara ukur: formula Evan: (a + b)/ 2 > 50% dimana a adalah diameter
kedua tepi kornu anterior ventrikel lateralis dan b adalah diameter
biparietal yang terluas pada potongan CT scan aksial yang sama.
d. Skala ukur: skala nominal (variabel kategorik)
6. Volume ICH
a. Definisi: volume perdarahan intraserebral
b. Alat ukur: CT Scan kepala
c. Cara ukur: formula dari Broderick: (a x b x c)/ 2, dimana a =
panjang, b = lebar (tegak lurus dengan sumbu panjang) dan c =
banyaknya potongan pada CT Scan kepala aksial yang masih menunjukan perdarahan.
d. Skala ukur: skala rasio (variabel numerik)
7. Mortalitas tiga puluh hari pertama
a. Definisi : kematian subjek penelitian dalam hari ketiga puluh setelah
c. Cara ukur : Kematian ditegakkan setelah terjadi henti nafas dan henti
jantung pada subjek penelitian. Kematian batang otak dimasukkan ke
dalam batasan operasional kematian yang ditegakkan berdasarkan
kriteria American Academy of Neurology (1994) d. Skala ukur : Skala nominal (variabel kategorik).
I. Analisis Data
Variabel kategorik dianalisis dalam bentuk frekuensi dan persentase yang
disajikan baik dalam bentuk tabel maupun grafik. Analisis deskriptif variabel
numerik dilakukan dalam bentuk ukuran pemusatan (mean, median) dan ukuran
penyebaran (standar deviasi, minimum-maksimum). Jika sebaran data normal,
digunakan pasangan mean dan standar deviasi. Jika sebaran data tidak normal,
digunakan median dengan minimum-maksimum.
Untuk uji normalitas, digunakan uji Kolmogorov-Smirnov dengan batas
kemaknaan p<0,05. Untuk Analisis data tidak berpasangan dengan sebaran
normal digunakan uji One Way ANOVA dengan Bonferoni sebagai uji post hoc. Bila sebaran data tidak normal, digunakan uji Kruskal Wallis.
Korelasi variabel numerik dengan numerik menggunakan uji korelasi
Pearson bila sebaran data normal. Bila sebaran data tidak normal, digunakan uji
BAB V
HASIL PENELITIAN
Subjek penelitian diambil dari bulan Februari 2010 sampai dengan bulan Februari 2013. Dalam kurun waktu tersebut diperoleh 46 penderita intraserebral spontan yang disertai dengan perdarahan intraventrikel yang memenuhi kriteria inklusi penelitian. Hasil pemeriksaan CT scan kepala dari tiap penderita dilakukan analisis hubungannya terhadap hasil akhir berupa mortalitas 30 hari. Hasil lengkap data penderita dapat dilihat pada lampiran.
A. Distribusi Berdasarkan Usia, GCS, Jenis Kelamin dan Mortalitas
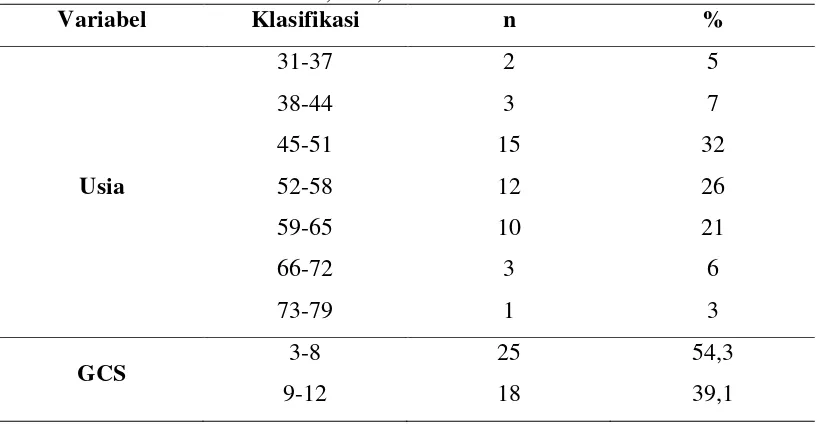
Pertama kali dilakukan pembagian subjek penelitian berdasarkan usia, GCS, jenis kelamin, dan mortalitas (tabel 3). Masing-masing variabel tersebut kemudian diklasifikasikan menjadi beberapa kelompok.
Setelah dilakukan pendataan dan memasukkan data tersebut kedalam tabel, didapatkan subjek berjenis kelamin perempuan lebih banyak dibandingkan dengan subjek laki-laki, dimana subjek perempuan sebanyak 25 (54,3%) kasus dan laki-laki sebanyak 21 (45,7%) kasus.
Berdasarkan tingkat kesadaran penderita yang dikelompokan berdasarkan GCS, diperoleh data bahwa mayoritas subjek penelitian datang dengan GCS 3-8, dengan jumlah 25 subjek (54,3%), diikuti dengan kelompok penderita dengan GCS 9-12 (39,1%) dan hanya sebagian kecil penderita saja masuk dalam kelompok GCS 13-15, yakni sebanyak 3 subjek (6,6%).
Distribusi jenis kelamin dalam penelitian ini tidak jauh berbeda yakni laki-laki berjumlah 21 subjek (45,7%) dan wanita berjumlah 25 subjek (54,3%).
Berdasarkan mortalitas 30 hari, diperoleh hanya 4 subjek penelitian yang hidup (8,7%) dan 42 subjek penelitian yang meninggal selama observasi 30 hari (91,3%).
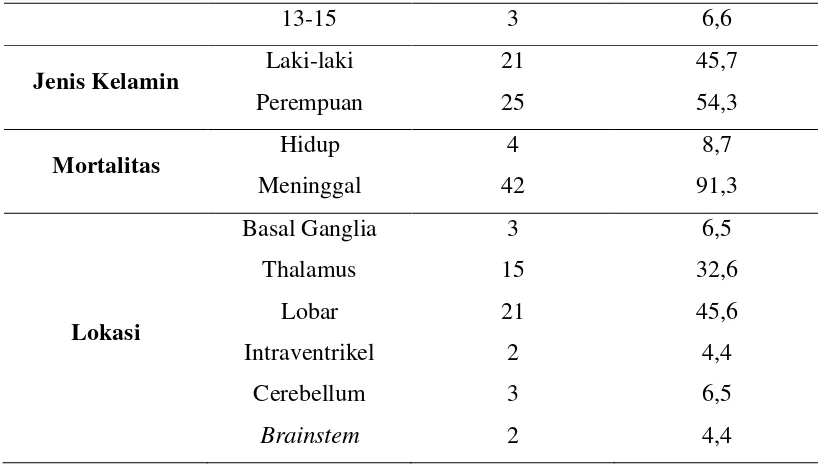
Berdasarkan lokasi perdarahan, didapatkan lokasi terbanyak adalah perdarahan lobar, sebanyak 21 subjek (45,6%), diikuti dengan perdarahan di thalamus sebanyak 15 subjek (32,6%), basal ganglia hanya didapati pada 3 subjek penelitian (6,5%).
Tabel 3. Distribusi berdasarkan Usia, GCS, Jenis Kelamin dan Mortalitas
13-15 3 6,6
B. Karateristik Volume Perdarahan dan Sistim Skoring IVH
Setelah seluruh data CT scan kepala dikumpulkan, diperoleh beberapa data yang bisa dikelompokan menjadi volume perdarahan dan menurut masing-masing sistim skoring IVH. (Tabel 4)
Tabel 4. Nilai Rerata Volume dan Sistim Skoring
Mean ±SD
Volume 31,22 ± 33,22 (median 18)
Sistim penilaian IVH 14,87±5,32
Sistim penilaian Graeb 6,93±2,94
Sistim penilaian LeRoux 9,04±4,22
Berdasarkan sistim skoring, didapatkan rerata berat ringannya perdarahan
C. Perbedaan GCS, Usia, dan Volume Perdarahan terhadap Mortalitas 30 hari
Dari data karateristik yang telah diuraikan diatas, maka dilakukan analisis terhadap perbedaan mortalitas 30 hari terhadap nilai GCS, usia dan volume. Dari analisis diperoleh variabel volume yang paling memiliki kemaknaan yang mendekati normal (p=0,063), diikuti oleh variabel GCS (p=0,09) dan usia (p=0,293). Adapun variabel volume dianalisis menggunakan Mann Whitney u-test, sedangkan GCS dan usia dianalisis menggunakan independent t-test (tabel 5).
Tabel 5. Tabel Perbedaan GCS, Usia dan Volume Terhadap Mortalitas 30 Hari
Mortalitas 30 hari Hidup P SD Median
GCS 7,95±2,12 12,75±3,86 0,090a 2,63 8,00
Usia 53,74±9,73 54,5±5,91 0,293a 9,41 52,00
Volume 24,64 11,5 0,063b 18 33,21
a
Independent t-test b Mann Whitney u-test; CI 95%
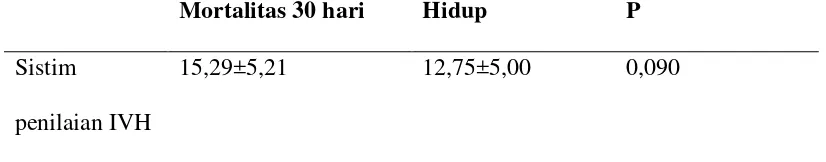
Setelah melakukan analisis adanya perbedaan bermakna antara masing-masing sistim skoring terhadap mortalitas 30 hari, didapatkan sistim penilaian Graeb memiliki perbedaan yang paling mendekati bermakna (p=0,063), diikuti dengan sistim penilaian IVH (p=0,09) dan sistim penilaian LeRoux (p=0,293), tabel 6.
Tabel 6. Tabel Perbedaan Sistim Penilaian IVH, Graeb dan LeRoux Terhadap Mortalitas 30 Hari
Mortalitas 30 hari Hidup P
Sistim
penilaian IVH
Sistim
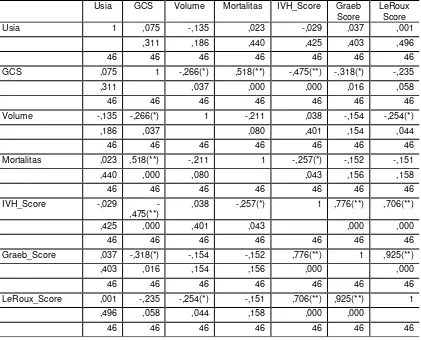
Tabel 7. Tabel korelasi Penilaian IVH, Graeb dan LeRoux Terhadap Mortalitas 30 Hari
Usia GCS Volume Mortalitas IVH_Score Graeb
BAB VI PEMBAHASAN
Perdarahan intraventrikel terjadi pada 30-45% penderita SICH dan telah banyak penelitian yang membuktikan bahwa perdarahan intraventrikel ini merupakan prediktor independen terhadap hasil akhir yang buruk. Adanya perdarahan intraventrikel juga dilaporkan secara bermakna meningkatkan risiko kematian dan volume IVH berhubungan langsung terhadap terjadinya kematian.
Sistim penilaian IVH, Graeb dan LeRoux dilaporkan memiliki kemampuan untuk memprediksi hasil akhir penderita SICH dengan IVH dengan tingkat akurasi yang sama baiknya pada waktu penderita masuk Rumah Sakit dan dalam periode 6 hari setelah perdarahan. Dalam penelitian ini peneliti mengambil batasan waktu 48 jam pertama setelah perdarahan/ onset serangan SICH sehingga diharapkan ketiga sistim penilaian tersebut masih memiliki tingkat akurasi dalam memprediksi hasil akhir.
Hasil akhir pada penelitian sebelumnya menggunakan modified Rankin Scale/ mRS, sedangkan dalam penelitian ini dilakukan pengukuran hasil akhir menggunakan mortalitas 30 hari. Sepengetahuan peneliti, penelitian ini merupakan penelitian pertama yang mengukur kemampuan ketiga sistim penilaian berat ringannya perdarahan intraventrikel dengan metode pengukuran hasil akhir menggunakan mortalitas 30 hari.
penderita perdarahan intraserebral spontan dan intraventrikel dinilai berat ringannya IVH berdasarkan sistim penilaian IVH, sistim penilaian Graeb dan sistim penilaian LeRoux. Dari seluruh karateristik data yang ada, didapati bahwa hanya variabel volume perdarahan saja yang terdistribusi normal sedangkan variabel yang lain meliputi usia, GCS, sistim penilaian IVH, sistim penilaian Graeb dan sistim penilaian LeRoux terdistribusi tidak normal. Berdasarkan hal tersebut, maka variabel volume perdarahan dianalisis dengan Mann-Whitney test sedangkan variabel yang lain dianalisis menggunakan Independent t-test.
Kelemahan Penelitian
Penelitian ini memiliki beberapa kelemahan, diantaranya adalah mayoritas subjek penelitian memiliki nilai skor GCS yang rendah (3-8) dengan jumlah 25 penderita (54,3%). Hal ini akan mempengaruhi mortalitas yang diperoleh karena skor GCS awal merupakan salah satu prognosis yang buruk terhadap penderita SICH.
Kelemahan berikutnya adalah bahwa penelitian ini menunjukan gambaran hidrosefalus pada seluruh subjek penderita. Hidrosefalus telah dilaporkan sebagai salah satu faktor prognosis yang buruk terhadap penderita SICH.
Dalam penelitian sebelumnya dikatakan bahwa volume IVH secara langsung berhubungan dengan risiko terjadinya kematian. Dalam penelitian ini tidak dinilai berapa volume IVH, tetapi berat ringannya hanya diukur berdasarkan sistim penilaian yang sifatnya semikuantitatif.
tindakan operatif dapat memberikan hasil akhir yang lebih baik dibandingkan dengan tindakan konservatif.
BAB VII
SIMPULAN DAN SARAN
A. SIMPULAN
Dalam penelitian ini didapatkan 46 kasus perdarahan intraserebral spontan yang disertai dengan perdarahan intraventrikel pada RSUP. H. Adam Malik Medan dalam kurun waktu penelitian sekitar tiga tahun dengan rata-rata umur 46,20 ± 16,3 tahun dan dengan dominasi jenis kelamin perempuan terhadap laki-laki. Berdasarkan lokasi terjadinya perdarahan intraserebral, urutan paling sering adalah perdarahan lobar sebanyak 45,7% dengan nilai GCS pada awal masuk rata-rata adalah 7 (21,7%).
Dari ketiga sistim skoring yakni IVH score, Graeb score dan LeRoux score, didapati perbedaan yang mendekati bermakna terhadap mortalitas 30 hari berturut-turut LeRoux score (p=0.254), Graeb’s score (p=0.256) dan IVH score. Dari variabel-variabel yang diteliti didapati variabel volume perdarahan yang memiliki kemaknaan yang paling tinggi (p=0.34) terhadap mortalitas 30 hari.
B. SARAN
DAFTAR PUSTAKA
Adams R. E, Diringer M. N; Response to external ventricular drainage in spontaneous intracerebral hemorrhage with hydrocephalus. 1998. Neurology 50:519-523
Ahn C. S., Lee S.K., Kim H.S., Kang M.H., Song M.Y., Kang D.S.; Surgical outcome of spontaneous intracerebral hemorrhage in less than stuporous status. 2004. J Korean Neurosurg Soc 35:290-296
Anderson C. S., Chakera T. M., Stewart-Wynne E. G., Jamrozik K. D.; Spectrum of Primary Intracerebral Haemorrhage in Perth, Western Australia, 1959-90: Incidence and Outcome. 1994. J Neurol Neurosurg Psychiatry 57(8): 936-940
Aronowski J, Hall C. E.; New horizons for primary intracerebral hemorrhage treatment: experience from preclinical studies. 2005. Neurol Res 27:268-279
Bamford, J., Sandercock P, Dennis M, Burn J, Warlow C; A Prospective Study of Acute Cerebrovascular Disease in the Community: The Oxfordshire Community Stroke Project, 1981-86. 2. Incidence, Case Fatality Rates and Overall Outcome at One Year of Cerebral Infarction, Primary Intracerebral and Subarachnoid Hemorrhage. 1990. J Neurol Neurosurg Psychiatry 53(1): 16-22
Bevilacqua MP; Endothelial-leukocyte adhesion molecules. 1993. Annu Rev Immunol 11:767-804
Broderick J, Connolly S, Feldmann E, Hanley D, Kase C, Krieger D, Mayberg M, Morgenstern L, Ogilvy C. S., Vespa P., Zuccarello M; Guidelines for the Management of Spontaneous Intracerebral Hemorrhage in Adults: 2007 Update: A Guideline From the American Heart Association/ American Stroke Association Stroke Council High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group: The American Academy of Neurology affirms the value of this guideline as an educational tool for neurologists. 2007. Stroke 38: 2001-2023
M. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage: A Statement for Healthcare Professionals From a Special Writing Group of the Stroke Council, American Heart Association. 1999. Stroke 30: 905-915
Broderick J. P., Brott T. G., Duldner J.E., et al; Volume of intracerebral hemorrhage. A powerful and easy-to-use predictor of 30-day mortality. 1993. Stroke 24:987-93
Coplin W. M., Vinas F. C., Agris J. M., Biciuc R, Michael D.B., Diaz F.G., Muizelaar J. P.; A cohort study of the safety and feasibility of intraventricular urokinase for nonaneurysmal spontaneous intraventricular hemorrhage. 1998. Stroke 29:1573-1579
Counsell C, Boonyakarnkul S, Dennis M, Sandercock P, Bamford J, Burn J, Warlow C; Primary Intracerebral Haemorrhage in the Oxfordshire Community Stroke Project 2. Prognosis. 1995. Cerebrovasc Dis 5(1): 26-34
Daverat P, Castel JP, Dartigues JF, et al. 1991. Death and functional outcome after spontaneous intracerebral hemorrhage. A prospective study of 166 cases using multivariate analysis. Stroke 22:1-6
Endres M, Laufs U, Merz H, Kaps M. Focal expression of intercelular adhesion molecule-1 in the human carotid bifurcation.. 1997. Stroke 28:77-82
Felberg R, Grotta C, Shirzadi A, Strong R, Narayana P, Hill-Felberg S, Aronowski J. Cell death in experimental intracerebral hemorrhage: the
“black hole” model of hemorrhagic damage. 2002. Ann Neurol
51:517-524
Fieschi C, Carolei A, Fiorelli M, Argentino C, Bozzao L, Fazio C, Salvetti M, Bastianello S. Changing Prognosis of Primary Intracerebral Hemorrhage: Results of a Clinical and Computed Tomographic Follow-Up Study Of 104 Patients. 1988. Stroke 19:192-195
Franke C. L., van Swieten J. C., Algra A, van Gijn J. Prognostic factors in patients with intracerebral haematoma.. 1992. J Neurol Neurosurg Psychiatry 55:653-657
Gebel J. M., Jauch E. C., Brott T. G., Khoury J, Sauerbeck L, Salisbury S, Spilker J, Tomsick T. A., Duldner J, Broderick J. P.; Natural History of Perihematomal Edema in Patients With Hyperacute Spontaneous Intracerebral Hemorrhage. 2002a. Stroke 33: 2631-2635
Gong C, Hoff J.T., Keep R.F.; Acute inflammatory reaction following experimental intracerebral hemorrhage in rat. 2000. Brain Research 71:57-65
Graeb D. A., Robertson W. D., Lapointe J. S., Nugent R. A., Harrison P. B.; Computed tomographic diagnosis of intraventricular hemorrhage. Etiology and prognosis. 1982. Radiology 143:91-96
Hafler D. A., Weiner H. L.; CNS and systemic autoimmune disease. 1989. Immunol Today 10:104-107
Janny P, Papo I, Chazal J, Colnet G, Barretto L. C.; Intracranial hypertension and prognosis of spontaneous intracerebral haematomas: A correlative study of 60 patients. 1982. Acta Neurochir (Wien) 61:181-186
Kase C. S., Crowell R.M.; Prognosis and treatment of patients with intracerebral hemorrhage. In: Kase CS, Caplan LR, eds. Intracerebral hemorrhage. Boston: Butterworth-Heinemann, 1994:467-89
Kraus J, Oschmann P, Leis S, Neundorfer B, Heckmann J.G.; High concentrations of sVCAM-1 and sICAM-1 in the cerebrospinal fluid of patients with intracerebral haemorrhage are associated with poor outcome. 2002. J Neurol Neurosurg Psychiatry 73:346-347
Lisk D. R., Pasteur W, Rhoades H, Putnam R. D., Grotta J. C.; Early presentation of hemispheric intracerebral hemorrhage: prediction of outcome and guidelines for treatment allocation. 1994. Neurology 44: 133-139
Ma Q, Manaenko A, Khatibi N. H., Chen W, Zhang J. H., Tang J. Vascular adhesion protein-1 inhibition provides antiinflammatory protection after an intracerebral hemorrhagic stroke in mice. 2011. J Cereb Blood Flow Metab 31:881-893
Mayfrank L, Kim Y, Kissler J, Delsing P, Gilsbach J. M., Schroder J.M., Weis J. Morphological changes following experimental intraventricular haemorrhage and intraventricular fibrinolytic treatment with recombinant tissue plasminogen activator. 2000. Acta Neuropathol (Berl) 100:561-567
Mayfrank L, Kissler J, Raoofi R.; Ventricular dilatation in experimental intraventricular hemorrhage in pigs. Characterization of cerebrospinal fluid dynamics and the effects of fibrinolytic treatment. 1997. Stroke 28:141-148
Mayfrank L, Lippitz B, Groth M, Bertalanffy H, Gilsbach J. M.; Effect of recombinant tissue plasminogen activator on clot lysis and ventricular dilatation in the treatment of severe intraventricular haemorrhage. 1993. Acta Neurochir 122:32-38
International Surgical Trial in Intracerebral Haemorrhage (STICH): a randomised trial. 2005. Lancet 365:387-397
Misra U. K., Kalita J, Ranjan P, Mandal S. K.; Mannitol in intracerebral hemorrhage: A randomized controlled study. 2005. J Neurol Sci 234:41-45
Naff N. J., Carhuapoma J. R., Williams M. A., Bhardwaj A, Ulatowski J. A., Bederson J, Bullock R, Schmutzhard E, Pfausler B, Keyl P. M., Tuhrim S, Hanley D. F.; Treatment of intraventricular hemorrhage with urokinase: Effect on 30-day survival. 2000. Stroke 31:841-847
Nieuwkamp D. J., de Gans K, Rinkel G. J., Algra A.; Treatment and outcome of severe intraventricular extension in patients with subarachnoid or intracerebral hemorrhage: A systematic review of the literature. 2000. J Neurol 247:117-121
Pang D, Sclabassi R. J., Horoton J. A.; Lysis of intraventricular blood clot with urokinase in a canine model: Part 2: In vivo safety study of intraventricular urokinase. 1986. Neurosurgery 19:547-552
Pang D, Sclabassi R. J., Horton J. A.; Lysis of intraventricular blood clot with urokinase in a canince model: Part 1: Canince intraventricular blood cast model. 1986. Neurosurgery 19:540-546
Portenoy R. K., Lipton R.B., Berger A. R., et al.; Intracerebral haemorrhage: a model for the prediction of outcome. 1987. J Neurol Neurosurg Psychiatry 50:976-9
Qureshi A, Ling G, Khan J, Suri M, Misholczi L, Guterman L, Hopkins L.; Quantitative analysis of injured, necrotic, and apoptotic cells in a new experimental model of intracerebral hemorrhage. 2001. Crit Care Med 29:152-157
Qureshi A. I., Geocadin R. G., Suarez J. l., Ulatowski J. A.; Long-term outcome after medical reversal of transtentorial herniation in patients with supratentorial mass lesions. 2000. Crit Care Med 28:1556-1564
Qureshi A. I., Safdar K, Weil J. Predictors of early deterioration and mortality in black americans with spontaneous intracerebral hemorrhage. 1995. Stroke 26(10):1764-1767
Qureshi A. I., Tuhrim S, Broderick J, Batjer H. H., Hondo H, Hanley D. Spontaneous intracerebral hemorrhage. 2001. N Engl J Med 344:1450-1460
with malignant brain edema. 2005. Acta Neurochir (Wien) 147:947-951; discussion 952,
Rincon F, Mayer S. A.; Clinical Review: Critical Care Management of Spontaneous Intracerebral Hemorrhage. 2008. Critical Care 12: 237
Springer T. A.; Leucocyte adhesion to cells. 1990. Scand J Immunol 32:211-216
Steiner T, Kaste M, Forsting M, Mandelow D, Kwiecinski H, Szikora I, Juvela S, Marchel A, Chapot R, Cognard C, Utenberg A, Hacke W.; Recommendations for the management of intracranial haemorrhage – part i: Spontaneous intracerebral haemorrhage. The european stroke initiative writing committee and the writing committee for the eusi executive committee. 2006. Cerebrovasc Dis 22:294-316
Steinke W, Sacco R. L., Mohr J. P., Foulkes M. A., Tatemichi T. K., Wolf P. A., Price T. R., Hier D. B.; Thalamic stroke. Presentation and prognosis of infarcts and hemorrhages. 1992. Arch Neurol 49:703-710
Tuhrim S, Dambrosia J. M., Price T. R., e al. Intracerebral hemorrhage: external validation and extension of a model for prediction of 30-day survival. 1991. Ann Neurol 29:658-63
Tuhrim S, Horowitz D. R., Sacher M, Godbold J. H.; Volume of ventricular blood is an important determinant of outcome in supratentorial intracerebral hemorrhage. 1992. Crit Care Med 27:617-621
Wagner K. R., Xi G, Hua Y, Zuccarello M, de Courten-Myers G. M., Broderick J. P., Brott T. G.; Ultra-early clot aspiration after lysis with tissue plasminogen activator in a porcine model of intracerebral hemorrhage: Edema reduction and blood-brain barrier protection. 1999. J Neurosurg 90:491-498
Wang J, Dore S: Inflammation after intracerebral hemorrhage. 2007. J Cereb Blood Flow Metab 27:894-908
Wang J, Tsirka S. E.; Tuftsin fragment 1-3 is beneficial when delivered after the induction of intracerebral hemorrhage. 2005. Stroke 36(3):613-618
Xi G, Keep R. F, Hoff J. T. Erythrocytes and delayed brain edema formation following intracerebral hemorrhage in rats. 1998. J Neurosurg 89:991-996
Xi G, Keep R. F, Hoff J. T.; Mechanisms of brain injury after intracerebral haemorrhage. 2006. Lancet Neurol 5:53-63
Xue M, Del Bigio M. Comparison of brain cell death and inflammatory reaction in three models of intracerebral hemorrhage in adult rats. 2003. J Stroke Cerebrovasc Dis 12(3):152-159
Yilmaz G, Granger D. N.; Cell adhesion molecules and ischemic stroke. 2008. Neurol Res 30:783-793
Yuzawa H, Higano S, Mugikura S, Umetsu A, Murata T, Nakagawa A, et al. Pseudo-subarachnoid hemorrhage found in patients with postresuscitation encephalopathy: characteristics of CT findings and clinical importance. 2008. AJNR Am J Neuroradiol 29:1544-1549
Zhao X, Sun G, Zhang J, Strong R, Song W, Gonzales N, Grotta J. C., Aronowski J. Hematoma resolution as a target for intracerebral hemorrhage treatment: Role for peroxisome proliferation activated receptor gamma in microglia/macrophages. 2007. Ann Neurol 61:352-362