SINTESISN,N (DI-2 ETIL FTALAT) LAURAMIDA YANG
DIHASILKAN DARI ESTERIFIKASI ANTARA
N,N ( DI -2-ETANOL ) LAURAMIDA
DENGAN ANHIDRIDA FTALAT
SKRIPSI
DIAN M SITINJAK
100802043
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
SINTESISN,N( DI-2 ETIL FTALAT) LAURAMIDA YANG DIHASILKAN DARI ESTERIFIKASI ANTARA
N,N ( DI -2- ETANOL ) LAURAMIDA DENGAN ANHIDRIDA FTALAT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
DIAN M SITINJAK 100802043
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Sintesis N,N (Di-2-Etil Ftalat) Lauramida
yang Dihasilkan dari Esterifikasi antara
N,N (Di-2-Etanol) Lauramida dengan Anhidrida Ftalat
Kategori : Skripsi
Nama : Dian M Sitinjak
NIM : 100802043
Program Studi : Sarjana (S1) Kimia
Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan
Alam ( FMIPA) Universitas Sumatera Utara
Disetujui di,
Medan, Oktober 2014
Komisi Pembimbing :
Dosen Pembimbing 2, Dosen Pembimbing 1,
Dr.Adil Ginting, M.Sc Dra.Herlince Sihotang, M.Si
NIP. 195307041980031002 NIP.195503251986012002
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
SINTESISN,N ( DI - 2 - ETIL FTALAT ) LAURAMIDA YANG DIHASILKAN DARI ESTERIFIKASI ANTARA
N,N ( DI -2-ETANOL) LAURAMIDA DENGANANHIDRIDA FTALAT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Oktober 2014
PENGHARGAAN
Segala puji dan syukur penulis ucapkan kepada Tuhan Yesus Kristus atas kasihNya sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini dengan tidak kekurangan suatu apapun.
Teristimewa penulis mengucapkan terimakasih kepada orang tua penulis (Arpagus Sitinjak dan Erika Purba) yang selalu mengasihi dan bersabar, memberikan dukungan moril maupun materi dan selalu berdoa untuk kesuksesan penulis.
Penulis sadar banyak pihak-pihak yang turut serta dalam penyelesaian penelitian dan penyusunan skripsi ini. Untuk itu pada kesempatan ini penulis mengucapkan terima kasih kepada:
• Ibu Dra.Herlince Sihotang,M.Si sebagai pembimbing I dan Bapak Dr.Adil Ginting,MSc sebagai pembimbing II dan juga Kepala Laboratorium Kimia Organik FMIPA USU Bapak Dr. Mimpin Ginting,MS yang dengan sabar telah memberikan bimbingan dan saran kepada penulis
• Ibu DR.Rumondang Bulan,M.S dan Bapak Drs.Albert Pasaribu,M.sc sebagai Ketua dan Sekretaris Departemen Kimia FMIPA USU.
• Bapak Prof.Dr.Jamaran Kaban,M.sc selaku Ketua Bidang Kimia Organik FMIPA USU beserta Dosen dan Staff Laboratorium Kimia Organik FMIPA USU.
• Seluruh Dosen Departemen Kimia FMIPA USU yang telah memberikan
bimbingan selama penulis mengikuti kuliah di Departemen Kimia FMIPA USU, terkhusus kepada Bapak Prof.Dr.Seri Bima Sembiring,MSc sebagai dosen wali yang telah memberikan pengarahan dalam menyelesaikan studi selama perkuliahan dan penelitian berlangsung.
• Seluruh Asisten Laboratorium Kimia Organik FMIPA USU (Bang Egitarius, KakNaomi,KakDespita,KakRimenda,Yabes,Sophia,Lianta,Daniel,Hotlan,Bern ard,Friska,Yulia, Oesrima,Hardi,Ebenezer,Sevty).
• Seluruh teman-teman stambuk 2010 serta seluruh kakak dan adik Stambuk. • Seluruh adik-adik kelompokku (Robert,Betria,Eka,Yohana,Anna,Rina)
Akhirnya, penulis mengucapkan rasa terimakasih kepada keluarga EUNIKE (Kak Adelina, Rahel,Hotnida,Yabes,Doni,dan Zulfandri,) yang selalu menghibur dan memberi semangat kepada penulis saat menyelesaikan penelitian dan skripsi ini. Tuhan Yesus Memberkati
SINTESISN,N (DI-2-ETIL FTALAT) LAURAMIDA YANG DIHASILKAN DARIESTERIFIKASI ANTARA
N,N (DI-2-ETANOL) LAURAMIDA DENGAN ANHIDRIDA FTALAT
ABSTRAK
Telah dilakukan sintesisN,Netil ftalat) lauramida hasil esterifikasi N,N (di-2-etanol) lauramida dengan anhidrida ftalat menggunakan pelarut xylena:aseton (2:1) pada suhu 140-1500C menghasilkan rendemen sebesar 53,24%. N,N (di-2-etanol) lauramida diperoleh dari hasil amidasi metil laurat dengan dietanolamina menggunakan katalis NaOCH3pada suhu 110-1200C. Senyawa N,N(di-2-etil ftalat)
SYNTHESIS N,N (DI-2 ETHYL PTHALIC) LAURAMIDE PRODUCED FROM ESTERIFICATION OF N,N (DI-2-ETHANOL)
LAURAMIDE WITH PTHALIC ANHYDRIDE
ABSTRACT
It has been synthesized N,N( di-2-ethyl pthalic)lauramideby esterification of N,N (di-2-ethanol) lauramide with pthalic anhydride by using solvents xylene-acetone (2:1) at 140-1500C make 53,24% yield. N,N (di-2-ethanol) lauramide obtained from amidation of methyl lauric with diethanolamine using NaOCH3 as catalyst at 110-1200 C. N,N(
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Tabel ix
Daftar Gambar x
Daftar Lampiran xi
BAB 1. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Permasalahan 3
1.3. Pembatasan Masalah 4
1.4. Tujuan Penelitian 4
1.5. Manfaat Penelitian 4
1.6. Lokasi Penelitian 5
1.7. Metode Penelitian 5
BAB 2. TINJAUAN PUSTAKA
2.1. Lemak dan Minyak 6
2.2. Oleokimia 7
2.3. Asam Lemak dan Turunannya 8
2.3.1. Asam Laurat 11
2.4. Ester 12
2.4.1. Esterifikasi 13
2.5. Amida 15
2.5.1. Reaksi Amidasi 16
2.5.2. Etanolamina 18
2.5.3. Dietanolamina 19
2.5.4. Alkanolamida 20
2.5.5. Monoetanolamida 21
2.5.6. Dietanolamida 21
2.6. Anhidrida Asam 22
2.6.1. Tatanama Anhidrida 23
2.6.2. Pembuatan Anhidrida 23
2.6.3. Reaksi Anhidrida 24
2.6.4. Anhidrida Ftalat 25
2.7. Surfaktan 25
BAB 3. METODE PENELITIAN
3.1.1. Alat-alat 29
3.1.2. Bahan-bahan 30
3.2. Prosedur Penelitian 31
3.2.1. Esterifikasi Asam Laurat dengan Metanol 31
3.2.2. Amidasi Metil Laurat dengan Dietanolamina 31
3.2.3. Esterifikasi N,N (di-2-etanol) lauramida dengan 32 Anhidrida Ftalat
3.2.4. Analisis Hasil Reaksi 33
3.2.4.1. Penentuan Titik Lebur 33
a. Zat padat 33
b. Zat cair 33
3.2.4.2. Penentuan Nilai Hydrophylic Lypophylic 33
Balance (HLB)
a. Penentuan Bilangan Penyabunan 34
b. Penentuan Bilangan Asam 34
3.2.4.3. Analisis dengan Spektrofotometer FT-IR 34 3.2.4.4. Analisis dengan Spektrofotometer 1H-NMR 35
3.3. Bagan Penelitian 36
3.3.1. Esterifikasi Asam Laurat dengan Metanol 36
3.3.2. Amidasi Metil Laurat dengan Dietanolamina 37
3.3.3. Esterifikasi N,N (di-2-etanol) Lauramida dengan 38 Anhidrida Ftalat
3.3.4. Penentuan Nilai Hydrophylic Lypophylic Balance (HLB) 39
3.3.4.1. Penentuan Bilangan Penyabunan 39
3.3.4.2. Penentuan Bilangan Asam 39
BAB 4. HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 40
4.1.1. Esterifikasi Asam Laurat dengan Metanol 40
4.1.2. Amidasi Metil Laurat dengan Dietanolamina 41
4.1.3. Esterifikasi N,N (di-2-etanol) Lauramida dengan 41 Anhidrida Ftalat
4.1.4. Penentuan Titik Lebur 44
4.1.5. Penentuan Nilai Hydrophylic Lypophylic Balance (HLB) 44
4.2. Pembahasan 45
4.2.1. Esterifikasi Asam Laurat dengan Metanol 45
4.2.2. Amidasi Metil Laurat dengan Dietanolamina 46
4.2.3. Esterifikasi N,N (di-2-etanol) Lauramida dengan 48 Anhidrida Ftalat
4.2.4. Penentuan Titik Lebur 51
4.2.5. Penentuan Nilai Hydrophylic Lypophylic Balance (HLB 52 BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 54
5.2. Saran 54
DAFTAR TABEL
Nomor Judul Halaman
Tabel
2.1. Diagram Alur Proses Oleokimia dari Bahan Dasar Minyak 8
Atau Lemak menjadi Oleokimia dan Turunan Oleokimia
2.2. Asam Lemak Jenuh yang Terdapat dalam Lemak dan 10
Minyak
2.3. Asam Lemak Tidak Jenuh yang Terdapat dalam Lemak dan 11
Minyak
4.1. Data Kromatografi Lapis Tipis 42
4.2 Data Spektrometer 1H-NMR 43
4.3. Data Titik Lebur 44
4.4. Data Penentuan Bilangan Penyabunan 44
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1. Hasil Hidrolisa Trigliserida menjadi Asam Lemak dan 6
Gliserol
2.2 Struktur Asam Laurat 12
2.3. Rumus Umum Ester 12
2.4. Reaksi Pembentukan Maleanised Albizia Benth Oil 15
Polyesteramida
2.5. Bentuk-Bentuk Amida 16
2.6. Contoh Amida siklik 16
2.7. Reaksi Pembentukan Etanolamina 19
2.8. Reaksi Pembentukan Dietanolamina 19
2.9. Reaksi Pembentukan Monoetanolamida 21
2.10. Reaksi Pembentukan Dietanolamida 22
2.11. Anhidrida Asam 22
2.12. Reaksi-Reaksi Anhidrida Asam 25
2.13. Anhidrida Ftalat 25
2.14. Lambang Umum Surfaktan 26
2.15. Skala Rentang Nilai HLB untuk Beberapa Zat Aktif Permukaan 28
4.1. Spektrum FT-IR Metil Laurat 40
4.2. Spektrum FT-IRN,N (di-2-etanol) lauramida 41
4.3. Spektrum FT-IR N,N (di-2-etil ftalat) lauramida 43
4.4. Spektrum 1H-NMR N,N (di-2-etil ftalat) lauramida 43
4.5. Mekanisme Reaksi Esterifikasi Asam Laurat dengan Metanol 46
4.6. Mekanisme Reaksi Amidasi Metil Laurat dengan 47
Dietanolamina
DAFTAR LAMPIRAN
Nomor Judul Halaman
lampiran
1. Gambar Metil Ester Asam Laurat 58
2. Gambar N,N (Di-2-Etanol) Lauramida 58
3. Gambar N,N (Di-2-Etil Ftalat) Lauramida 58
Sebelum Pemurnian dengan Kromatografi Kolom
4. GambarN,N (Di-2-Etil Ftalat) Lauramida 59
Sesudah Pemurnian dengan Kromatografi Kolom
5. Tabel Analisa KLT Terhadap N,N (Di-2-etanol) 59
SINTESISN,N (DI-2-ETIL FTALAT) LAURAMIDA YANG DIHASILKAN DARIESTERIFIKASI ANTARA
N,N (DI-2-ETANOL) LAURAMIDA DENGAN ANHIDRIDA FTALAT
ABSTRAK
Telah dilakukan sintesisN,Netil ftalat) lauramida hasil esterifikasi N,N (di-2-etanol) lauramida dengan anhidrida ftalat menggunakan pelarut xylena:aseton (2:1) pada suhu 140-1500C menghasilkan rendemen sebesar 53,24%. N,N (di-2-etanol) lauramida diperoleh dari hasil amidasi metil laurat dengan dietanolamina menggunakan katalis NaOCH3pada suhu 110-1200C. Senyawa N,N(di-2-etil ftalat)
SYNTHESIS N,N (DI-2 ETHYL PTHALIC) LAURAMIDE PRODUCED FROM ESTERIFICATION OF N,N (DI-2-ETHANOL)
LAURAMIDE WITH PTHALIC ANHYDRIDE
ABSTRACT
It has been synthesized N,N( di-2-ethyl pthalic)lauramideby esterification of N,N (di-2-ethanol) lauramide with pthalic anhydride by using solvents xylene-acetone (2:1) at 140-1500C make 53,24% yield. N,N (di-2-ethanol) lauramide obtained from amidation of methyl lauric with diethanolamine using NaOCH3 as catalyst at 110-1200 C. N,N(
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Asam laurat merupakan asam lemak jenuh yang paling besar jumlahnya di dalam minyak kelapa sawit, yaitu sebesar 46,3-51.1%. Asam laurat juga terdapat pada berbagai minyak yang bersumber dari bahan nabati lainnya. Pada minyak kelapa 45,9-50,3%,minyak canola 37%.(Richard, 2009).
Turunan asam laurat telah banyak dihasilkan. Salah satunya adalah metil ester asam lemak. Metil ester asam lemak merupakan hasil transesterifikasi dari suatu minyak dengan metanol (Noureddini and Medikonduru,1997). Metil ester asam lemak selain digunakan sebagai pengganti solar, juga digunakan dalam pembuatan kosmetik, detergen, aditif pada tekstil dan kertas (Kimmel, 2004).
Senyawa alkanolamida juga dapat dihasilkan dari asam laurat. Pembuatan senyawa alkanolamida dilakukan dengan mereaksikan asam lemak dengan amina pada suhu 120oC-180oC. Sintesis senyawa alkanolamida yang telah dilakukan adalah melalui reaksi antara asam lemak dengan etanolamina ataupun dietanolamina, sering terjadi persaingan antara terbentuknya amida dan ester apabila kondisi reaksi tidak diatur dengan baik (Maag,1984). Lubis,(2012) juga telah melakukan penelitian mengenai sintesis senyawa alkanolamida yang dihasilkan melalui amidasi antara metil palmitat campuran dengan etanolamina dan dietanolamina.
sebagai agen pengontrol busa, aditif bahan bakar, corrosion inhibitors (Rosen, 2004).
Pemanfaatan surfaktan juga terdapat pada bidang polimer. Belakangan ini salah satu jenis polimer sintetik yang banyak dikembangkan adalah polimer emulsi yang memanfaatkan surfaktan sebagai penghasil misel untuk tempat nukleasi dan penstabil partikel polimer. Salah satu bentuk struktur polimer emulsi adalah polimer core shell yang banyak dikembangkan untuk aplikasi
coating. Jenis polimer yang biasa digunakan adalah polimer akrilik karena memiliki daya tahan, toughness dan kestabilan UV yang kuat (Helmiyati dkk,2009).
Poliester tak jenuh merupakan produk serbaguna yang dapat digunakan sebagai resin untuk enkapsulasi komponen elektronik dan komponen penguat plastik. Dalam pembuatan poliester tersebut asam dikarboksilat yang biasa digunakan adalah anhidrida ftalat. Penggantian anhidrida ftalat dengan menggunakan anhidrida azelat menghasilkan poliester dengan dampak ketahanan dan kekuatan yang lebih baik (Smith,1985).
Lestari,(2014) ,mensintesis poliester dari shellac dan anhidrida ftalat, dimana dengan penambahan anhidrat ftalat untuk meningkatkan sifat mekanis bahan misalnya sifat kekuatan tarik,kekerasan bahan dan daya serap terhadap air,sehingga nantinya akan memberikan nilai tambah pada aplikasi produknya yaitu sebagai coating.
Telah dilakukan sintesis senyawa hidroxylethyl albizia benth oil dengan anhidrida maleat dengan bantuan katalis HCl menghasilkan maleanised hydroxyethyl albizia benth oil amide. Dimana hidroxyethyl albizia benth oil
merupakan hasil reaksi dari albizia benth oil dengan dietanolamina. Reaksi esterifikasi dilanjutkan terhadap maleanised hydroxyethyl albizia benth oil amide dengan penambahan anhidrida ftalat yang menghasilkan senyawa
oil dengan anhidrida maleat yang bermanfaat dalam material polimer sehingga memberikan dorongan untuk melakukan penelitian dari bahan yang tersedia, dapat diperbaharui, harga murah dan alami. (Akintayo et al,2012).
Sheyla,(2014), membuat senyawa N-2-etanol-N-etil maleat palmitamida dari reaksi esterifikasi antara senyawa N,N (di-2-etanol) palmitamida dengan anhidrida maleat dengan menggunakan pelarut xylena-aseton (3:1) pada suhu 140-150oC menghasilkan senyawa N-2-etanol-N-etil maleat palmitamida sebanyak 1,4 gram (45,35%).
Berdasarkan hal-hal tersebut, peneliti tertarik untuk melakukan penelitian mengenai esterifikasi antara alkanolamida dengan anhidrida ftalat yang berbeda dari peneliti terdahulu,baik dalam asam lemak yang digunakan maupun ratio pencampuran,yaitu sintesis senyawa N,N(di-2-etil ftalat) lauramida hasil esterifikasi N,N (di-2-etanol) lauramida dengan anhidrida ftalat dimana N,N (di-2-etanol) lauramida diperoleh dari amidasi metil laurat dengan dietanolamina,sedangkan metil laurat diperoleh dari esterifikasi asam laurat dengan metanol menggunakan katalis H2SO4(p).
1.2. Permasalahan
1. Apakah senyawa N,N(di-2-etil ftalat) lauramida dapat disintesa melalui reaksi esterifikasi antara senyawa N,N ( di-2-etanol ) lauramida dengan anhidrida ftalat dengan menggunakan pelarut xylena-aseton pada suhu 140-150oC.
2. Berapakah nilai Hydrophilic Lipophilic Balance
1.3. Pembatasan Masalah
1. Pembuatan metil laurat yang diperoleh dari hasil reaksi esterifikasi antara asam laurat dengan metanol menggunakan katalis H2SO4(p).
2. Penentuan titik lebur dari senyawa yang dihasilkan dengan menggunakan melting point apparatus, penentuan nilai HLB menggunakan metode titrasi.
1.4. Tujuan Penelitian
1. Untuk menghasilkan senyawa N,N(di-2-etil ftalat) lauramida melalui reaksi esterifikasi antara senyawa N,N ( di-2-etanol ) lauramida dengan anhidrida ftalat dengan menggunakan pelarut xylena-aseton pada suhu 140-150oC.
2. Untuk mengetahui nilai Hydrophilic Lipophilic Balance ( HLB ) dari senyawa N,N (di-2-etanol) lauramida dan N,N(di-2-etil ftalat) lauramida yang dihasilkan melalui metode titrasi.
1.5. Manfaat Penelitian
Diharapkan hasil penelitian ini dapat memberikan informasi tentang perkembangan sintesa organik dalam bidang oleokimia, dimana senyawa alkanolamida turunan asam laurat yang diesterifikasi dengan anhidrida ftalat, diharapkan dapat dimanfaatkan sebagai bahan pelapis pada bidang industri.
Penelitian ini dilakukan di Laboratorium Kimia Organik FMIPA USU Medan. Analisa spektroskopi FT-IR dilakukan di Laboratorium Kimia Organik FMIPA UGM. Analisis spektrofotometer 1H-NMR dilakukan di Pusat Penelitian LIPI – Serpong.
1.7. Metodologi Penelitian
Penelitian ini dilakukan melalui ekperimen laboratorium, dimana semua zat-zat kimia yang digunakan merupakan p.a E’merck. Asam laurat diesterifikasi dengan metanol menggunakan katalis H2SO4(p) dalam kondisi refluks menghasilkan metil laurat.
Selanjutnya metil laurat diamidasi dengan dietanolamina pada suhu 110-120oC menggunakan katalis NaOCH3 yang dilarutkan dalam metanol menghasilkan senyawa
BAB 2
TINJAUAN PUSTAKA
2.1. Lemak dan Minyak
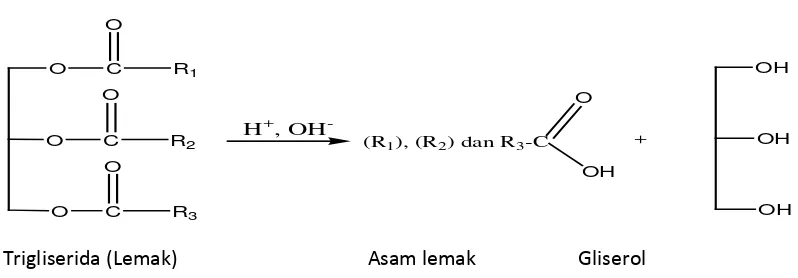
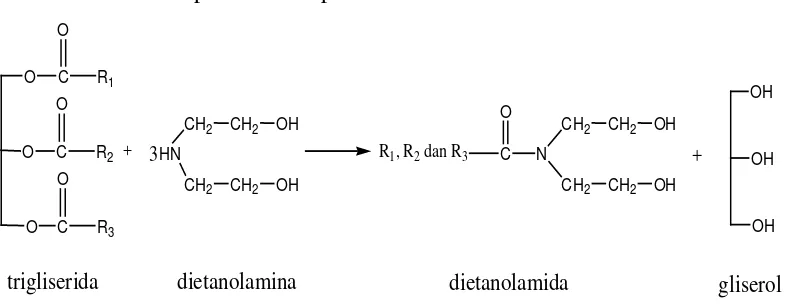
Lemak dan minyak merupakan salah satu kelompok yang termasuk golongan lipida. Satu sifat yang khas dan mencirikan golongan lipida (termasuk lemak dan minyak) adalah daya larutnya dalam pelarut organik (misalnya eter, benzen, chloroform) atau sebaliknya ketidak larutannya dalam pelarut air. Lemak dan minyak secara kimiawi adalah trigliserida yang merupakan bagian terbesar dari kelompok lipida. Trigliserida ini merupakan senyawa hasil kondensasi satu molekul gliserol dengan tiga molekul asam lemak (Sudarmadji dan Haryono, 1989).
O
O C
C O
O
R1
R2
H+, OH
-(R1), (R2) dan R3-C +
OH
OH
OH
O C
O
R3
O
OH
Trigliserida (Lemak) Asam lemak Gliserol
Gambar 2.1. Hasil Hidrolisis Trigliserida menjadi Asam Lemak dengan Gliserol (Bahl, 2004).
pelarut-pelarut organik lainnya. Kelarutan minyak atau lemak dalam suatu pelarut-pelarut ditentukan oleh sifat polaritas asam lemaknya. Asam lemak yang bersifat polar cenderung larut dalam pelarut polar, sedangkan asam lemak non polar larut dalam pelarut non polar. Sebagai contoh ialah asam lemak berantai pendek (misalnya asam butirat) pada lemak susu bersifat polar cenderung larut dalam air sedangkan asam lemak berantai karbon panjang tidak larut dalam air. Sifat dan daya kelarutan ini digunakan sebagai dasar praktek pada pengujian-pengujian analitis dan ekstraksi minyak dengan pelarut. Sifat minyak dan lemak yang larut dalam pelarut tertentu dipergunakan dalam pengolahan minyak secara komersil. Daya kelarutan asam asam lemak biasanya lebih tinggi dari komponen gliseridanya dan dapat larut dalam pelarut organik yang bersifat polar dan non polar. Semakin panjang rantai karbon maka minyak dan lemak tersebut semakin sukar larut (Ketaren, 2008).
2.2 Oleokimia
Oleokimia pada dasarnya merupakan cabang ilmu kimia yang mempelajari trigliserida menjadi asam lemak dan gliserin serta turunan asam lemak baik dalam bentuk ester, amida, sulfat, sulfonat, alkohol, alkoksi, maupun sabun. Asam lemak bersama-sama dengan gliserol merupakan penyusun utama minyak nabati atau lemak dan merupakan bahan baku untuk semua lipida pada makhluk hidup. Asam lemak ini mudah dijumpai dalam minyak masak (minyak goreng), margarin atau lemak hewan dan dapat menentukan nilai gizinya. Secara alami, asam lemak bisa berbentuk bebas (karena lemak yang terhidrolisis) maupun yang terikat dari gliserida. Asam lemak merupakan salah satu dasar oleokimia (Tambun, 2006).
(hampir mencapai 40% dari total penggunaannya). Penggunaan terbesar berikutnya sebesar 30% untuk dijadikan sabun, detergen, kosmetik. Asam lemak juga digunakan sebagai bahan dasar pembuatan resin dan cat sekitar 15% sisanya digunakan dalam industri pembuatan ban, tekstil, kulit kertas, pelumas dan lilin (Richtler and Knaut, 1984). Diagram alur oleokimia dapat digambarkan pada tabel 2.1. dibawah ini!
Tabel 2.1. Diagram Alur Proses Oleokimia dari Bahan Dasar Minyak atau Lemak menjadi Oleokimia dan Turunan Oleokimia
Bahan Dasar Bahan Dasar Oleokimia Turunan
Oleokimia
Minyak / Lemak
Asam Lemak Diikuti reaksi-reaksi
seperti : Aminasi Klorinasi Dimerisasi Epoksidasi Etoksidasi Guebetisasi Hidrogenasi Kuarternisasi Sulfasi
Transesterifikasi Esterifikasi Saponifikasi Amina Asam Lemak
Alkohol Asam Lemak
Amina Asam Lemak
Metil Ester Asam Lemak
Propilen,
ParafindanEtilen
Sumber : Richtler and Knaut, 1984 : Alami
: Sintesis
Gliserol
2.3.Asam Lemak dan Turunannya
reaktif. Hingga dapat dimengerti bahwa asam lemak mempunyai pengaruh besar terhadap lemak dan minyak. Asam lemak yang menyusun lemak ini dapat dibedakan antara asam lemak jenuh dan tak jenuh. Asam lemak disebut jenuh bila semua atom C dalam rantainya diikat tidak kurang daripada dua atom H, hingga dengan demikian tidak ada ikatan rangkap. Asam-asam lemak jenuh yang telah dapat diidentifikasi sebagai bagian dari lemak mempunyai atom C4 hingga C26. Adapun struktur umum rantai karbon dari asam lemak jenuh
adalah sebagai berikut:
R C H H C C H H H H C O OH
Asam-asam lemak yang didalamnya rantai karbonnya mengandung ikatan rangkap. Derajat ketidakjenuhan dari minyak tergantung pada jumlah rata-rata dari ikatan rangkap didalam asam lemak.Pada asam lemak tak jenuh, masih dibedakan antara asam lemak yang mempunyai bentuk “non-conjugated” yaitu ikatan rangkap dalam rantai C selalu dipisahkan oleh dua ikatan tunggal. Bentuk yang lain adalah asam yang “conjugated”, dimana antara atom-atom C tertentu terdapat ikatan tunggal dan ikatan rangkap berganti-ganti.
C
H
H
R C C C
H H O
OH
Rantai karbon dari asam lemak tak jenuh
R C C
H
H
C
H H
C C C
H H H C H C H H C C H C H H C H C C H O OH C R H O OH
Rantai asam lemak yang “non-conjugated” Rantai asam lemak yang
(tak terkonjugasi) “conjugated” (terkonjugasi)
Hampir semua asam lemak yang terdapat dalam alam mempunyai jumlah atom karbon yang genap karena asam ini dibiosintesis dari gugus asetil berkarbon dua dalam asetil koenzim A.
dua atom karbon
CH3C
O
SCoA
8
asetil koenzim A
banyak tahap
CH3(CH2)14CO2H asam palmitat
jumlah atom karbon genap
(Fessenden dan Fessenden, 1986).
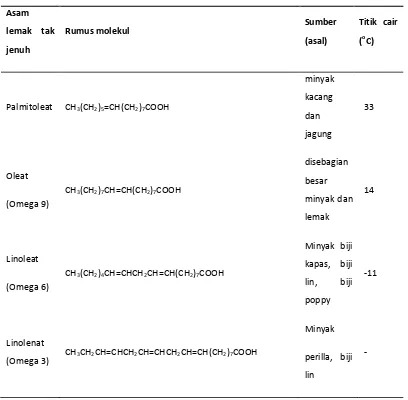
Asam lemak jenuh dan tidak jenuh yang penting, terdapat dalam minyak dan lemak dapat dilihat dalam tabel 2.2 dan 2.3 berikut:
Tabel 2.2. Asam Lemak Jenuh yang Terdapat dalam Lemak dan Minyak
Asam lemak jenuh Rumus molekul Sumber (Asal)
Titik cair (oC)
n- Butirat CH3(CH2)2COOH lemak susu sapi, mentega -7,6
n-Kaproat CH3(CH2)4COOH
mentega, minyak kelapa, minyak kelapa sawit -1,5 n-Kaprilat CH3(CH2)6COOH Domba 1,6
Kaprat CH3(CH2)8COOH
susu sapi dan kambing, minyak kelapa, minyak kelapa sawit
31,5
Laurat CH3(CH2)10COOH
susu, minyak inti sawit, spermaseti, mnyak laural, minyak kelapa
44
Miristat CH3(CH2)12COOH minyak pala, susu ternak, dan lemak
ikan hiu Palmitat CH3(CH3)14COOH
sebagian besar terdapat dalam lemak hewani dan minyak nabati
64
Stearat CH3(CH3)16COOH Domba 69,4
Tabel 2.3. Asam Lemak Tidak Jenuh yang Terdapat dalam Lemak dan Minyak
Asam lemak tak jenuh Rumus molekul Sumber (asal) Titik cair (oC)
Palmitoleat CH3(CH2)5=CH(CH2)7COOH
minyak kacang dan jagung 33 Oleat (Omega 9)
CH3(CH2)7CH=CH(CH2)7COOH
disebagian besar minyak dan lemak 14 Linoleat (Omega 6)
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH
Minyak biji kapas, biji lin, biji poppy -11 Linolenat (Omega 3)
CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH
Minyak perilla, biji lin
(Ketaren, 2008).
2.3.1 Asam Laurat
Asam laurat atau disebut juga dengan asam dodekanoat merupakan asam lemak jenuh yang tersusun dari 12 atom karbon. Asam laurat mengandung hidrokarbon non Polar pada bagian ekornya dan gugus karboksilat yang Polar pada bagian kepala sehingga dapat berinteraksi dengan air. Asam laurat merupakan satu diantara tiga asam lemak jenuh yang paling banyak dijumpai daripada asam miristat,asam palmitat dan asam stearat. Asam laurat paling banyak dijumpai pada cinnamon (80-90%),minyak kelapa (40-60%) dan minyak inti sawit(40-50%). Asam laurat banyak digunakan pada pembuatan sabun,sampo,kosmetik dan bahan aktif permukaan lainnya.
Adapun struktur dari asam laurat adalah sebagai berikut.
C11H23C O
OH
Gambar 2.2. Struktur Asam Laurat
Sifat-sifat asam laurat adalah sebagai berikut:
-rumus molekul : C12H24O2
-Berat molekul : 200,31 gr/mol
-Densitas : 0,869 gr/cm3
- Titik didih : 225 oC
-Titik lebur : 44oC
- tidak larut dalam air,1 gram larut dalam 1ml alkohol, 2,5 ml dalam propil alkohol dan larut sempurna dalam benzena dan eter (Anonimous,1976).
2.4. Ester
Ester adalah turunan asam karboksilat yang gugus OH dari karboksilnya diganti gugus OR dari alkohol. Ester mengandung gugus karbonil dan satu ikatan eter dengan karbon karbonil (Wilbraham dan Matta, 1992).
Rumus Umum
R C
O
O R
Gambar 2.3. Rumus Umum Ester
Ester dapat diperoleh dari asam organik yang di reaksikan dengan alkohol. Pembentukan air pada reaksi esterifikasi, selalu OH nya berasal dari asam, sebab reaksi senyawa organik bersifat molekular, meskipun asam karboksilat terionisasi sedikit, tetapi alkohol tidak terionisasi.
Ester dari asam organik memiliki sifat:
• Berupa larutan bila massa rumusnya tidak terlalu besar
• Larutan yang netral, tidak berwarna, lebih mengkilat dibandingkan air dan berbau harum
• Senyawa yang massa rumusnya rendah dapat larut dalam air tapi sangat sedikit, lebih banyak larut dalam alkohol dan eter
• Titik didih relatif rendah, dibandingkan titik didih asam atau alkohol yang menyusunnya (Besari dkk, 1982).
Reaksi esterifikasi adalah suatu reaksi antara asam karboksilat dan alkohol membentuk ester. Turunan asam karboksilat membentuk ester asam karboksilat. Ester asam karboksilat ialah suatu senyawa yang mengandung gugus –CO2R dengan R dapat
berupa alkil maupun aril. Esterifikasi dikatalisis asam dan bersifat dapat balik (Fessenden dan Fessenden ,1986).
Menurut Besari dkk (1982), reaksi esterifikasi dapat dilakukan dengan reaksi-reaksi berikut ini:
1. Asam karboksilat ditambah dengan alkohol
H3C C O
OH + C2H5OH H3C C
O
OC2H5 + H2O
Asam asetat etanol etil asetat air
2. Alkil halida ditambah garam dari suatu asam karboksilat
CH3I + AgOC CH3
O
H3C C
O
OCH3 + AgI
Metil Iodida garam argentum metil asetat argentum iodida
3. Anhidrida asam ditambah dengan alkohol
CH3 C
O
O
C
O CH3
+ C2H5OH CH3 C
O
OH
+ CH3 C
O
OC2H5
Anhidrida asetat etanol asam asetat etil asetat
4. Asil halida ditambah dengan alkohol
H3C C
O
Cl + C2H5OH H3C C
O
OC2H5 + HCl
5. Alkohol ditambah dengan amida
C2H5OH + H3C C
O
NH2 NH3 + H3C C
O
OC2H5
Etanol amida amoniak etil asetat
Salah satu contoh dari reaksi pembuatan ester adalah reaksi esterifikasi antara
hidroxylethyl albizia benth oil dengan anhidrida maleat dengan bantuan katalis HCl menghasilkan maleanised hydroxyethyl albizia benth oil amide. Dimana hidroxyethyl albizia benth oil merupakan hasil reaksi dari albizia benth oil dengan dietanolamina. Reaksi esterifikasi dilanjutkan terhadap maleanised hydroxyethyl albizia benth oil amide dengan penambahan anhidrida ftalat yang menghasilkan senyawa maleanised albizia benth oil polyesteramide, seperti reaksi berikut ini : (Akintayo et al,2012).
+ O O C C O O R1 R2 O C O R3 HN CH2 CH2
CH2 CH2
OH
OH
3
H3C(CH2)3CH2 CH CH CH2 CH CH CH2 (CH2)4 CH2CH2 C
O
N CH2 CH2
CH2 CH2
OH
OH
+
O O
O
H3C(CH2)3CH2CH CH CH2CH CHCH2 (CH2)4CH2CH2 C
O
N CH2CH2
CH2CH2
O
OH
C COOH
O
Albizia Benth Oil dietanolamina
Hidroksietil Albizia Benth Oil Amida (HEABOA) anhidrida maleat HCl Maleanised HEABOA C C O O O anhidrida ftalat +
H3C(CH2)3CH2CH CH CH2CH CHCH2 (CH2)4CH2CH2 C
O
N
CH2CH2
CH2CH2
O O C COOH O C O COOH
Gambar 2.4. Reaksi pembentukan maleanised albizia benth oil polyesteramide
2.5. Amida
Amida umumnya dibuat dengan jalan mereaksikan suatu klorida asam dengan amina, amonia, amina monosubstitusi atau amina disubstitusi. Pemberian nama senyawa amida yaitu dengan mengganti akhiran –oat atau –at dari asam karboksilat dengan –amida. Jika atom nitrogen suatu amida berikatan dengan gugus alkil atau aril, maka gugus yang berikatan pada amida ditunjukkan dengan N- (Riswiyanto,2009).
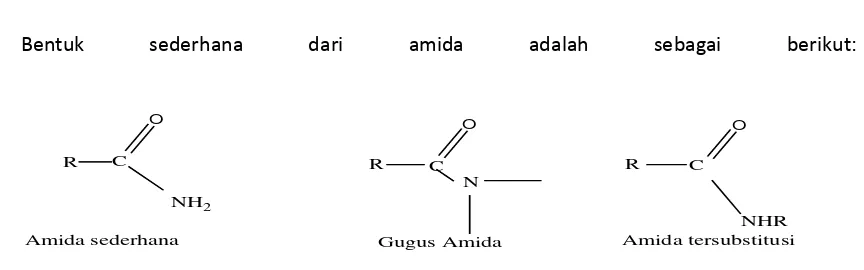
Bentuk sederhana dari amida adalah sebagai berikut:
Amida sederhana C
O
NH2
C
O
N
Gugus Amida
NHR C
O
Amida tersubstitusi
[image:30.595.103.535.312.447.2]R R R
Gambar 2.5. Bentuk-Bentuk Amida
(Fessenden dan Fessenden,1986).
Amida juga dapat dibuat dari reaksi ammonia atau amina dengan turunan asam karboksilat, ester terutama metil ester dan anhidrida asam. Jika ester digunakan sebagai bahan baku, terbentuk alkohol sebagai hasil samping reaksi. Jika digunakan anhidrida, hasil sampingnya adalah asam karboksil (Wilbraham,1992).
Amida siklik mempunyai nama khusus, yaitu diberi akhiran –laktam sebagai pengganti dari gugus lakton yang di dalam cincinnya mengandung atom nitrogen(Riswiyanto, 2009).
NH H3C
NH O O α β γ ε α
[image:31.595.122.496.284.511.2]β−butirolaktam ε−kaprolaktam
Gambar 2.6. Contoh Amida Siklik
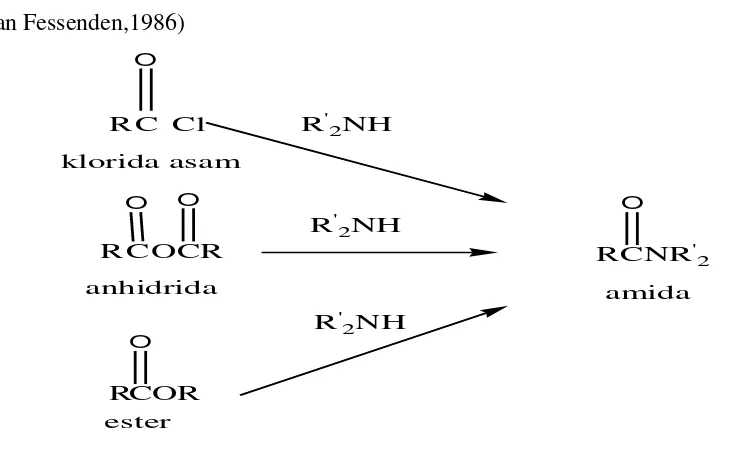
2.5.1. Reaksi Amidasi
Amida disintesis dari derivat asam karboksilat dan amonia atau amina yang sesuai. Reaksi pembuatan amida secara umum dapat digambarkan sebagai berikut: (Fessenden dan Fessenden,1986) C O Cl R CR O CO R O COR O R
CNR'2
O
R R'2NH
R'2NH
R'2NH
klorida asam
anhidrida
ester
amida
Reaksi antara monoetanolamin dengan metil ester asam lemak untuk membentuk alkanolamida telah banyak dikembangkan untuk pembuatan Stearamida (amida asam lemak) yang banyak digunakan dalam kosmetik dan sabun kecantikan (Urata and Takaishi, 1998).
Apabila senyawa amina direaksikan dengan ester, reaksi akan terjadi pada suhu tinggi, tetapi sangat lambat sekali apabila dilakukan pada suhu rendah dan tanpa bantuan katalis basa Lewis seperti NaOCH3yang lebih kuat dari trietilamin. Reaksi
amidasi antara amina dan ester dengan bantuan katalis NaOCH
pada suhu 100o-120oC, sedangkan apabila tidak menggunakan katalismaka reaksi dapat berlangsung pada suhu 150o-250o C (Gabriel, 1984).
Pembuatan amida antara lain : 1. Reaksi asam karboksilat dengan amoniak
HOH CH3 C
O
OH
+ NH3 CH3 C
OH
OH NH2
CH3 C O
NH2
+
asam
asetat amoniak asetamida air
2. Dalam perdagangan didapat dari garam amoniumnya dipanaskan pada temperatur 100 -200 oC
100-200 oC
H2O +
CH3 C O
ONH4
CH3 C O
NH2
amonium asetat asetamida air
3. Dengan mereaksikan anhidrida asam dengan amoniak
H NH2
+ H3C C
O
NH2
+ CH3 C
O
OH H3C C
O
O C
O H3C
anhidrida asetat amoniak asetamida asam asetat
4. Dengan menghidrolisa senyawa nitril, yakni pada reaksi sebelum terbentuknya asam karboksilat, terbentuk dahulu amida sebagai salah satu hasil antara.
+ H2O
CH3 C CH
3 C
O NH2
N
Metil sianida Air asetamida
H2O +
CH3 C
O NH2
CH3 C O OH
+ NH3
(Besari dkk, 1982)
2.5.2.Etanolamina
Etanolamina (NH2-(CH2)2-OH) merupakan cairan yang higroskopis, kental, berbau
amoniak, mampu mengabsorpsi CO2 dan larut dalam air, metanol serta
aseton.Etanolamina dikenal juga dengan nama 2-Aminoethanol, Monoethanolamine,
Ethylolamine,β-Amino Ethyl alcohol dan β–Hydroxylethylamine. Etanolamina dapat digunakan untuk menghilangkan CO2, H2S dari gas alam ataupun gas lainnya. Etanolamina
dapat juga digunakan sebagai sintesis pembuatan surfaktan (Anonimous,1976).
Reaksi dari etilen oksida dengan amonia menghasilkan etanolamina yang digunakan untuk menghilangkan hidrogen sulfida dan karbon dioksida dan gas alam.
H2C CH2 O
NH3 + H2N-CH2-CH2OH
Etanolamina
Gambar 2.7. Reaksi Pembuatan etanolamina (Bailey,1985).
2.5.3.Dietanolamina
Dietanolamina adalah senyawa yang terdiri dari gugus amina dan dialkohol. Dialkohol menunjukkan adanya dua gugus hidroksil pada molekulnya. Dietanolamina juga dikenal dengan nama bis(hydroxyethyl)amine, diethylolamine, hydroxtdiethylamine, diolamine dan 2,2-iminodiethanol.
H2C CH2
O
NH3 + H2N-CH2CH2OH
Dietanolamina HN-CH2CH2OH
CH2CH2OH
HOH2CH2C-N
CH2CH2OH CH2CH2OH
Trietanolamina Etanolamina
+ +
[image:34.595.117.305.394.514.2]Amoniak Etilen Oksida
Gambar 2.8. Reaksi pembuatan dietanolamina (Bailey, 1985).
Sifat-sifat dietanolamina adalah sebagai berikut :
a. Rumus molekul : C4H11NO2
b. Berat molekul : 105,1364 g/mol c. Densitas : 1,090 g/cm3 d. Titik leleh : 28ºC (1atm) e. Titik didih : 268,8ºC (1atm)
f. Kelarutan : H2O, alcohol, eter
Dietanolamina banyak digunakan dalam produk kosmetik dan detergen karena mampu menciptakan tekstur yang lembut dan foaming agent (Wikipedia,2007).
2.5.4. Alkanolamida
Alkanolamida digunakan sebagai bahan pembusa (foom boosting) dalam pembuatan shampoo (Nuryanto,2002).
Untuk membuat senyawa alkanolamida dengan menggunakan dietanolamina melalui reaksi amidasi langsung dengan trigliserida akan menghasilkan senyawa alkanolamida yang memiliki dua gugus hidroksi (poliol) seperti yang telah dilakukan oleh penelitian sebelumnya (Anasri, 2009).
Alkanolamida adalah surfaktan bukan ionik dimana gugus hidroksil yang dimilikinya tidak cukup hidrofilik untuk membuat alkanolamida larut dalam air dengan sendirinya. Alkanolamida digunakan sebagai bahan pembusa (foom boosting) dalam pembuatan shampoo.
Jenis alkanolamida yang paling penting adalah dietanolamida. Senyawa N-etanol alkil amida adalah senyawa yang termasuk dalam golongan asam lemak yang dapat dimanfaatkan sebagai surfaktan dalam produk detergen, kosmetik dan tekstil. Senyawa ini dapat dibuat dengan mereaksikan asam lemak sawit destilat dengan senyawa yang mengandung gugus atom Nitrogen seperti alkanolamina (Nuyanto, dkk, 2002). Sifat kimia dari suatu senyawa alkanolamida sangat bervariasi, tergantung dari panjang cincin hidrokarbon dan sifat substituen pada atom nitrogen (Bilyk et al, 1992).
2.5.5. Monoetanolamida
+ O O C C O O R1 R2 O C O R3 OH OH OH C O N
CH2 CH2 OH
+
H
R1, R2 dan R3
OH
H2C
H2C
3 H2N
[image:36.595.113.523.81.228.2]Trigliserida Monoetanolamina Monoetanolamida Gliserol
Gambar 2.9. Reaksi Pembentukan Monoletanolamida (Hughes and Lew, 1970)
2.5.6. Dietanolamida
Dietanolamida pertama kali diperoleh dengan mereaksikan dua mol dietanolamina dengan satu mol asam lemak. Senyawa ini diberi nama kritchevsky sesuai dengan nama penemunya. Bahan baku yang digunakan dalam produksi dietanolamida dapat berupa asam lemak, trigliserida atau metil ester. Dietanolamida biasanya diproduksi secara kimia konvensional pada temperature 150oC selama 6-12 jam (Herawan,1999).
Berikut merupakan reaksi pembuatan dietanolamida:
+ O O C C O O R1 R2 O C O R3 OH OH OH C O N
CH2 CH2
CH2 CH2
OH
OH
+
R1, R2 dan R3
HN
CH2 CH2
CH2 CH2
OH
OH
3
trigliserida dietanolamina dietanolamida gliserol
[image:36.595.115.509.581.734.2]2.6. Anhidrida Asam
Anhidrida asam berasal dari dua asam karboksilat yang melepaskan satu molekul air. Anhidrida berarti tanpa air. Anhidrida dinamai dengan menambahkan kata anhidrida di depan nama asamnya. Anhidrida dari asam monokarboksilat berwujud cair, sedangkan asam dikarboksilat dan asam karboksilat aromatik berwujud padat (Wilbraham dan Matta, 1992).
CH3COCCH3 O O
Gambar 2.11. Anhidrida Asam
IUPAC : anhidrida asam etanoat
Trivial : anhidrida asam asetat (Fessenden dan Fessenden, 1986).
Asam anhidrida lebih reaktif dibandingkan dengan ester, tetapi reaksinya dengan nukleofil kurang reaktif dibandingkan dengan asil halida. Air menghidrolisis anhidrida kembali menjadi asam. Reaksinya dengan alkohol menghasilkan ester, sedangkan dengan amonia menghasilkan asam (Hart, 1990).
2.6.1. Tatanama Anhidrida
Anhidrida dinamai dengan menambahkan kata anhidrida di depan nama asamnya. Salah satu anhidrida asam ialah anhidrida asetat :
H3C C O
O C CH3 O
2.6.2. Pembuatan Anhidrida
Dengan sedikit kekecualian, anhidrida asam tidak dapat dibentuk langsung dari asam karboksilat induknya, tetapi harus dibuat dari derivat asam karboksilat yang lebih reaktif. Satu jalur ke anhidrida ialah dari klorida asam dan suatu karboskilat.
R-C-Cl + -O-C-R' R-C-O-C-R' + Cl
-O O O O
suatu klorida asam suatu ion karboksilat suatu anhidrida
Jalur lain pembuatan anhidrida ialah dengan mereaksikan asam karboskilat dan anhidrida asetat. Suatu reaksi reversible terjadi antara suatu asam karboskilat dan suatu anhidrida. Letak kesetimbangan dapat digeser ke kanan dengan menyuling asam asetat segera setelah asam ini terbentuk (Fessenden dan Fessenden, 1986).
2.6.3. Reaksi Anhidrida
Beberapa asam dikarboksilat tertentu mudah melepas air dalam pemanasan apabila dapat membentuk cincin beranggota lima atau enam. Misalnya :
H2C
H2C OH
OH C O
C
O
kalor H2C H2C
O C O
C
O
H2O
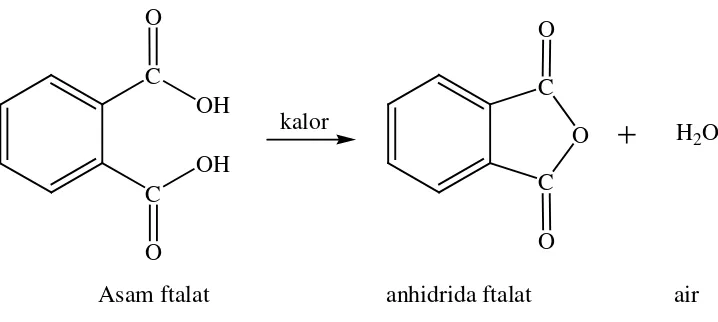
OH OH C O C O kalor O C O C O
H2O
Asam ftalat anhidrida ftalat air
Anhidrida asam dari asam monokarboksilat berwujud cair, sedangkan asam dikarboksilat dan asam karboksilat aromatik berwujud padat (Wilbraham dan Matta, 1992).
Reaksi pembuatan anhidrida asam umumnya berlangsung antara asil klorida dengan garam dari asam karboksilat. Sifat kimia anhidrida asam sama dengan klorida asam, namun anhidrida bereaksi sedikit lebih lambat daripada klorida asam. Anhidrida bereaksi dengan air menghasilkan asam, dengan amina menjadi amida, dengan alkohol membentuk ester, dan dengan LiAlH4 menghasilkan alkohol primer.
R O R
C O C O anhidrida asam R C OH O R C NH2 O R C OR' O R C H O LiAlH4 R C H OH H
H2O NH3 R'OH LiAlH4
[image:39.595.141.500.84.245.2]asam amida ester aldehida alkohol primer
2.6.4 Anhidrida Ftalat
Anhidrida ftalat disebut juga 1,3-Isobenzofurandione. Dengan rumus molekul C8H4O3,
berat molekul 148,11 dan titik lebur 130,8oC. Larut dalam alkohol.
O O
O
Gambar 2.13. Anhidrida Ftalat (Anonimous, 1967)
2.7.Surfaktan
Surfaktan atau surface active agent merupakan senyawa yang dapat menurunkan tegangan permukaan air. Molekul surfaktan apa saja mengandung suatu ujung hidrofobik (satu rantai hidrokarbon atau lebih) dan suatu ujung hidrofilik (biasanya, namun tidak harus, ionik). Jumlah hidrokarbon dari suatu molekul surfaktan harus mengandung 12 atau lebih atom karbon agar efektif.
O
[image:40.595.189.402.470.540.2]Ekor hidrofobik Ekor hidrofilik
Gambar 2.14. Lambang Umum Surfaktan (Fessenden dan Fessenden,1986).
Berdasarkan gugus hidrofiliknya, surfaktan diklasifikasikan menjadi 4 golongan yaitu (Rosen,2004) :
a. Surfaktan anionik
- Jenis surfaktan yang paling besar
- Sensitif terhadap air sadah atau hard water. Derajat sensitifitasnya : asam karboksilat > pospat > sulfat (sulfonat).
- Rantai pendek polioksietilen antara gugus anionik dan hidrokarbon meningkatkan kemampuan untuk bereaksi terhadap garam.
- Rantai pendek polioksipropilen antara gugus anionik dan hidrokarbon meningkatkan kelarutan dalam pelarut organik.
- Jenis sulfat mudah terhidrolisa oleh asam-asam dalam proses autokatalitik.
Contohnya adalah
- Sabun karboksilat RCOO
-- Sulfonat RSO3
-- Sulfat RO SO3
-- Phospat ROPO(OH)2O-
b. Surfaktan kationik
- Jenis surfaktan yang banyak jumlahnya setelah anionik dan nonionik. - Pada umunya tidak bereaksi dengan jenis anionik.
- Mempunyai sifat indeks bias yang lebih tinggi dibanding surfaktan jenis lain.
- Mempunyai sifat adsorpsi permukaan yang baik.
Contohnya adalah
- Heksa decil trimetilamonium bromida CH3(CH2)15N+(CH3)3Br
-- Dodecilamina hidroklorida CH3(CH2)11NH3+Cl
-c. Surfaktan non-ionik
- Merupakan surfaktan kedua terbesar.
- Dapat bereaksi dengan semua jenis surfaktan. - Sensitif terhadap air sadah.
- Berbeda dengan surfaktan ionik, sifat fisik-kimia surfaktan ini tidak terpengaruh oleh penambahan elektrolit.
- Sifat fisik-kimia senyawa etoksilat sangat tergantug pada temperatur.
- Polioksietilen-p-tertocyl phenyleter C8H17C6H4O(CH2CH2O)10H
d. Surfaktan ampoterik ( Zwitter ion)
Surfaktan zwitter ion mengandung muatan yang berbeda dan dapat membentuk surfaktan amfoter. Perubahan muatan terhadap pH pada surfaktan ampoterik mempengaruhi pembentukan busa, pembasahan, sifat detergen dan lainnya. Contohnya adalah :
N-Dodesil-N,N-Dimetil C12H25N+(CH3)2CH2COO- ( Porter, 1994).
Senyawa yang mengandung bagian hidrofilik dan hidrofobik, umumnya disebut sebagai zat amphiphilic. Keseimbangan hidrofilik-lipofilik (HLB =
hidrophilic-lipophilic balance) dari suatu zat amphiphilic cukup penting dalam fenomena kelarutan dan emulsifikasi (Winsor, 1956).
Nilai HLB dapat dihitung dengan menggunakan rumus sebagai berikut :
HLB = 20 1 S
A
Dimana S adalah bilangan penyabunan dan A adalah bilangan asam (Martin, 1960).
Griffin (1949), merancang sebuah skala sembarang nilai sebagai ukuran keseimbangan hidrofilik-lipofilik (HLB = Hydrophilic-Lipophilic Balance) dari zat aktif permukaan. Dengan sistem nomor ini, kemungkinan untuk membuat berbagai rentang HLB yang optimal untuk setiap kelas surfaktan dapat dilihat pada gambar berikut:
0
3
6 15 18
12
9
H
id
ro
fi
li
k
L
ipof
il
ik
Zat pelarut
Detergen
Zat pengemulsi o/w
Zat penyebar dan pembasah
Zat pengemulsi w/o
Kebanyakan zat antibusa
[image:43.595.192.450.82.462.2]Skala HLB
Gambar 2.15. Skala Rentang Nilai HLB untuk Beberapa Zat Aktif Permukaan
BAB 3
3.1. Alat dan Bahan
3.1.1. Alat-alat
- Neraca analitis MettlerPM480
- Spatula -
- Labu leher dua 250 ml Pyrex
- Labu leher dua 500 ml Pyrex
- Labu leher tiga 250 ml Pyrex
- Stopper -
- Pipet tetes -
- Gelas ukur 100 ml Pyrex
- Gelas ukur 10 ml Pyrex
- Hotplate stirrer Thermolyne
- Kondensor bola Pyrex
- Tabung CaCl2 Pyrex
- Corong penetes 50 ml Pyrex
- Termometer 300oC Pyrex
- Pengaduk magnetik -
- Gelas Beaker 250 ml Pyrex
- Corong pisah 500 ml Pyrex
- Statif dan klem -
- Kertas saring biasa -
- Corong Pyrex
- Kaca arloji Pyrex
- Rotarievaporator Heidolph
- Melting point apparatus Gallenkamp
- Alat vakum Fisons
- Tabung gas nitrogen -
- Gelas Erlenmeyer Pyrex
- Botol vial -
- Teflon Onda
- Pipa kapiler Blaubrand
- Spektrofotometer FT-IR Shimadzu
- Spektrofotometer 1H-NMR Delta2-NMR500MHz
3.1.2. Bahan-bahan
- Asam laurat p.a E’merck
- Metanol p.a E’merck
- Benzena p.a E’merck
- CaCl2 anhidrous p.a E’merck
- Asam sulfat p.a E’merck
- n-Heksana p.a E’merck
- Akuades -
- Natrium sulfat anhidrous p.a E’merck
- Dietanolamina p.a E’merck
- Natrium metoksida p.a E’merck
- Dietil eter p.a E’merck
- Natrium klorida p.a E’merck
- Xylena p.a E’merck
- Aseton p.a E’merck
- Asam klorida p.a E’merck
- Anhidrida ftalat p.a E’merck
- Gas nitrogen -
- Kalium hidroksida pellet p.a E’merck
- Indikator fenolftalein -
- Alkohol netral p.a E’merck
- NaOH p.a E’merck
3.2.Prosedur Penelitian
3.2.1.Esterifikasi asam laurat dengan metanol
Ke dalam labu leher dua volume 250 ml dimasukkan 50 gram (0,2496 mol) asam laurat
kemudian ditambahkan 100 ml metanol dan 100 ml benzena diaduk dengan menggunakan
pengaduk magnet. Dirangkai alat refluks yang dihubungkan dengan tabung CaCl2anhidrous,
dalam keadaan dingin sambil diaduk diteteskan H2SO4(p) sebanyak 2 ml melalui corong
penetes. Direfluks selama 5 jam, hasil reaksi kemudian diuapkan dengan menggunakan
rotarievaporator. Selanjutnya residu diekstraksi dengan 100 ml n-heksana, kemudian dicuci
dengan 10 ml akuades sebanyak dua kali. Lapisan atas dikeringkan dengan CaCl2anhidrous
dan disaring. Selanjutnya dilanjutkan pengeringan dengan Na2SO4 anhidrouskemudian
disaring. Filtrat diuapkan mengunakan rotarievaporator, residu yang diperoleh diukur
volumenya kemudian di ukur titik lebur dan di analisis dengan spektroskopi FT-IR.
3.2.2.Amidasi metil laurat dengan dietanolamina
Ke dalam labu leher dua volume 250 ml dimasukkan 15 gram (0,05 mol) metil laurat kemudian ditambahkan 10 ml (0,103 mol) dietanolamina diaduk dengan menggunakan pengaduk magnet. Dirangkai alat refluks yang dihubungkan dengan tabung CaCl2anhidrous, ditambahkan 5 gram natrium metoksida dalam 20 ml metanol
melalui corong penetes. Dipanaskan pada suhu 110-120oC selama 5 jam sambil diaduk. Hasil reaksi diuapkan menggunakan rotarievaporator. Residu yang diperoleh diekstraksi dengan menggunakan 100 ml dietil eter dan di cuci dengan 25 ml larutan NaCl jenuh sebanyak 3 kali. Lapisan atas yang diperoleh, diuapkan menggunakan rotarievaporator kemudian residu di keringkan didalam oven pada suhu 50oC dalam keadaan vakum selanjutnya didinginkan dalam desikator. Hasil yang diperoleh diukur titik leburnya, dilanjutkan analisis dengan spektroskopi FT-IR dan diukur nilai HLB dengan menggunakan metode titrasi.
Ke dalam labu leher tiga 250 ml dimasukan 2,4 gram (0,021 mol) alkanolamida (hasil amidasi metil palmitat dengan dietanolamina) dan ditambahkan 50 ml campuran xylena:aseton (2:1) v/v. Dirangkai alat refluks yang dihubungkan dengan tabung berisi CaCl2anhidrous, diaduk dengan pengaduk magnet pada suhu 100oC sambil di aliri gas
nitrogen. Ditambahkan 4 tetes HCl 1N melalui corong penetes. Kemudian ditambahkan 1,5 gram (0,05 mol) anhidrida ftalat yang dilarutkan dalam campuran xylena-aseton secara perlahan melalui corong penetes. Dilanjutkan pemanasan pada suhu 140-150oC selama 4 jam diikuti pemantauan hasil reaksi menggunakan analisis KLT. Hasil yang diperoleh diuapkan pelarutnya dengan menggunakan destilasi vakum, kemudian residu dicuci dengan metanol lalu disimpandidalam desikator. Senyawa yang diperoleh dianalisis menggunakan kromatografi lapis tipis (KLT) dengan beberapa pelarut organik sebagai developer selanjutnya dilakukan pemurnian menggunakan kolom kromatografi dengan adsorben silika gel 60G menggunakan eluen n-heksan : dietil eter 8:2 v/v. Hasil yang diperoleh diukur titik leburnya, dianalisis dengan spektrometer FT-IR dan1H-NMR kemudian diukur nilai HLB dengan menggunakan metode titrasi.
3.2.4. Analisa hasil reaksi
Senyawa N,N (di-2-etanol) lauramida dan N,N (di-2-etil ftalat) lauramida yang diperoleh, diambil sedikit mungkin dengan spatula kemudian diletakkan diatas melting point apparatus lalu dicatat perubahan titik leburnya.
b. Zat cair
Metil laurat dimasukkan kedalam pipa kapiler setinggi 1 cm kemudian dimasukkan kedalam freezerselama satu malam. Setelah disimpan satu malam, dikeluarkan pipa kapiler lalu diikatkan pada thermometer sehingga ujung pipa kapiler sama letaknya dengan ujung tempat air raksa dari thermometer. Bersama dengan thermometer, pipa kapiler tersebut dicelupkan kedalam gelas Beaker yang diisi campuran air dengan es. Kemudian dinaikkan suhu secara perlahan sambil diaduk dan diamati perubahan yang terjadi (Ketaren,2008).
3.2.4.2. Penentuan nilai Hidrophilic Lipophilic Balance (HLB)
Penentuan nilai HLB ini dilakukan pada senyawa N,N ( di-2- etanol ) lauramida dan N,N (di-2-etil ftalat) lauramida.
Nilai HLB = 20 ( 1 – S/A )
Dimana : S = Bilangan penyabunan A = Bilangan Asam
a.Penentuan Bilangan Penyabunan
menggunakan indikator fenolftalein sebanyak 3 tetes hingga warna merah hilang, lalu dicatat volume HCl 0,05 N yang dipakai.
Hal yang sama dilakukan untuk larutan blanko.
Bilangan Penyabunan =(V Blanko-V.titrasi) x N.HCl x BM KOH Berat sampel (gram)
b. Penentuan Bilangan Asam
Sebanyak 0,1 gram sampel dimasukkan kedalam gelas Erlenmeyer, kemudian ditambahkan 10 ml alkohol netral, lalu ditutup dengan plastik dan dipanaskan hingga larut kemudian didinginkan dan dititrasi dengan KOH 0,02 N menggunakan indikator fenolftalein sebanyak 3 tetes sampai tepat warna merah lembayung, lalu dicatat volume KOH 0,02 N yang dipakai (Ginting, 2011).
Bilangan Asam = V KOH x N KOH x BM KOH Berat sampel (gram)
3.2.4.3. Analisa dengan spektrofotometer FT-IR
Untuk masing-masing cuplikan yaitu untuk metil laurat yang berwujud cair dioleskan pada plat NaCl.N,N (di-2-etanol) lauramida dan N,N (di-2-etil ftalat) lauramidayang berwujud padat dicetak hingga terbentuk pellet KBr kemudian diukur spektrumnya dengan alat spektrofotometer FT-IR.
3.2.4.4. AnalisisSpektrofotometer1H-NMR
CuplikansenyawaN,N (di-2-etil ftalat) lauramidahasilsintesisdilarutkandalam CDCl3
model Delta2-NMR 500 MHz, dengan menggunakan tetra metilsilan (TMS) sebagaipembanding.
3.3. Bagan Penelitian
50 gram asam laurat
dimasukkan ke dalam labu leher dua 250 ml ditambahkan 100 ml metanol
ditambahkan 100 ml benzena
ditambahkan 2 ml H2SO4 (p) secara perlahan-lahan dalam keadaan dingin melalui corong penetes
direfluks sambil diaduk selama 5 jam
campuran
didinginkan pada suhu kamar
diuapkan dengan rotarievaporator
residu
diekstraksi dengan 100 ml n-heksana
dicuci dengan 10 ml akuades sebanyak 2 kali
destilat
lapisan atas lapisan bawah
ditambahkan dengan CaCl2 anhidrous selama 1 jam disaring
ditambahkan dengan Na2SO4 anhidrous selama 1 jam disaring
diuapkan dengan rotarievaporator
filtrat residu
filtrat residu
HASIL
dirangkai alat refluks yang dihubungkan dengan tabung CaCl2
penentuan titik lebur analisis FT-IR
15 gram metil laurat
dimasukkan kedalam labu leher dua 250ml
ditambahkan 10 ml dietanolamina
dirangkai alat refluks
ditambahkan 5 gram natrium metoksida dalam 20 ml metanol
dipanaskan pada suhu 110-120
oC sambil diaduk selama 5 jam
campuran
diuapkan dengan rotarievaporator
residu
destilat
diekstraksi dengan 100 ml dietil eter
dicuci dengan larutan NaCl jenuh sebanyak 3 kali masing-masing 25 ml
lapisan atas
lapisan bawah
diuapkan dengan rotarievaporator
residu
destilat
dikeringkan didalam oven pada suhu 50
oC dalam keadaan vakum
HASIL
penentuan titik lebur
analisis FT-IR
penentuan nilai HLB
KLT
2,4 gram N,N (di-2-etanol) lauramida
dimasukkan kedalam labu leher tiga 250ml
ditambahkan 50 ml campuran xylena-aseton dengan perbandingan 2:1 (v/v)
dirangkai alat refluks
ditambahkan 4 tetes HCl 1 N melalui corong penetes
ditambahkan 1,5 gram anhidrida ftalat yang telah dilarutkan dalam 50 ml xylena-aseton secara perlahan melalui corong penetes
dilanjutkan pemanasan pada suhu 140-150oC selama 4 jam yang diikuti pemantauan menggunakan analisis KLT
dipanaskan pada suhu 100oC sambil dialiri gas nitrogen dan diaduk hingga larut
Campuran
diuapkan dengan destilasi vakum
residu destilat
dicuci dengan metanol
disaring
residu filtrat
didiamkan di dalam desikator selama 1 malam
HASIL
KLT penentuan
nilai HLB penentuan
titik lebur
analisis
FT-IR analisis
H-NMR
dilakukan pemurnian dengan dengan kromatografi kolom dengan adsorben silika gel 60G dan eluen n-heksana:dietil eter 8:2 (v/v)
3.3.4.1. Penentuan bilangan penyabunan
0,1 gram sampel
dimasukkan kedalam gelas erlenmeyer
ditutup dengan plastik dipanaskan hingga larut campuran
didinginkan
ditambahkan 3 tetes indikator fenolftalein
dicatat volume HCl 0,05 N yang terpakai
HASIL
ditambahkan KOH alkohol 0,5 N sebanyak 5 ml
dititrasi dengan HCl 0,05 N hingga warna merah hilang
3.3.4.2. Penentuan bilangan asam
0,1 gram sampel
dimasukkan kedalam gelas erlenmeyer
ditutup dengan plastik dipanaskan hingga larut
campuran
didinginkan
ditambahkan 3 tetes indikator fenolftalein
dicatat volume KOH 0,02 N yang terpakai
HASIL
ditambahkan alkohol netral 95% sebanyak 10 ml
BAB 4
HASIL DAN PEMBAHASAN
4.1.Hasil Penelitian
4.1.1. Esterifikasi asam laurat dengan metanol
Pembuatan metil laurat secara esterifikasi terhadap 50,14 gram asam laurat dengan metanol dalam pelarut benzena menggunakan katalis asam sulfat pekat diperoleh metil laurat sebanyak 62,36 gram (97,16%) dan berbentuk cairan bening tidak berwana.
[image:55.595.116.509.490.694.2]Hasil yang diperoleh dianalisis dengan spektroskopi FT-IR memberikan spektrum dengan puncak-puncak serapan pada daerah bilangan gelombang 3749 cm-1, 3626 cm-1, 3464 cm-1, 3332 cm-1, 2924 cm-1, 2854 cm-1, 2731 cm-1, 2677 cm-1, 2368 cm-1, 2337 cm-1, 2052 cm-1, 1743 cm-1, 1550 cm-1, 1442 cm-1, 1365 cm-1, 1172 cm-1, 1118 cm-1,1010 cm-1, 840 cm-1, 725 cm-1, 408 cm-1, 300 cm-1(Gambar 4.1).
Gambar 4.1 Spektrum FT-IR metil laurat.
Pembuatan N,N (di-2-etanol) lauramida secara amidasi antara senyawa metil laurat dengan dietanolamina dalam pelarut metanol dengan bantuan katalis natrium metoksida diperolehalkanolamida sebanyak 17,12 gram(92,27%) berbentuk padatan berwarna putih.
[image:56.595.116.503.318.543.2]Hasil yang diperoleh dianalisis dengan spektroskopi FT-IR memberikan spektrum dengan puncak-puncak serapan pada daerah bilangan 3842 cm-1, 3410 cm-1, 2916 cm-1, 2846 cm-1, 2708 cm-1, 2368 cm-1, 2337 cm-1, 1851 cm-1, 1620 cm-1, 1566 cm-1, 1442 cm-1, 1365 cm-1, 1265 cm-1, 1188 cm-1, 1064 cm-1, 925 cm-1, 871 cm-1, 717 cm-1, 594 cm-1, 540 cm-1, 447 cm-1, 354 cm-1(Gambar 4.2).
Gambar 4.2 Spektrum FT-IRN,N (di-2-etanol) lauramida.
4.1.3Esterifikasi N,N (di-2-etanol) lauramida dengan anhidrida ftalat
Uji kromatografi lapis tipis N,N(di-2 etil ftalat)lauramidahasil dari pemurnian senyawa menggunakan kromatografi kolom dimana fase diam yang digunakan adalah silika gel 60G dan fase gerak n-neksana : dietil eter dengan perbandingan 8:2 v/v menunjukkan hasil sebagai berikut:
Tabel 4.1. Data Kromatografi Lapis Tipis
No Fraksi Jumlah noda Harga Rf
1. 1-10 0 -
2 11-27 1 0,22
3. 28-53 2 0,24
0,48
Hasil yang diperoleh yaitu fraksi 11-27 dianalisis dengan spektroskopi FT-IR memberikan spektrum dengan puncak-puncak serapan pada daerah bilangan 3520 cm
-1
, 2951 cm-1, 2924 cm-1, 2852 cm-1, 2671 cm-1, 2316 cm-1, 1710 cm-1, 1614 cm-1, 1460 cm-1, 1371 cm-1, 1259 cm-1, 1201 cm-1, 1168 cm-1, 1116 cm-1, 1080 cm-1, 970 cm-1, 908 cm-1, 887 cm-1, 815 cm-1, 723 cm-1, (Gambar 4.3).
Gambar 4.4Spektrum 1H-NMRN,N(di-2 etil ftalat)lauramida.
4.1.4PenentuanTitik Lebur
Penentuan titik lebur pada senyawa metil laurat, N,N (di-2-etanol) lauramida, dan N,N(di-2 etil ftalat)lauramida menunjukkan data sebagai berikut:
Tabel 4.2. Data Penentuan Titik Lebur
NO Nama senyawa Titik Lebur (0C)
1. Metil laurat 13,8-14
2. N,N (di-2-etanol) lauramida 87-89
3. N,N (di-2-etil ftalat)lauramida 54-56
[image:59.595.122.489.582.642.2]Harga HLB (Hydrophylic Lypophylic Balance) dari N,N (di-2-etanol) lauramida dan N,N(di-2 etil ftalat) lauramida yang dilakukan berdasarkan metode titrasi melalui penentuan bilangan penyabunan yang dilanjutkan penentuan bilangan asam memberikan data dan perhitungan sebagai berikut :
Tabel 4.3. Data Penentuan Bilangan Penyabunan
No Sampel Massa
sampel (gram) Massa sampel rata-rata (gram) Volume titrasi (ml) Volume titrasi rata-rata (ml) Bilangan penyabunan
1. Blanko - - 16,54 16,54 -
- 16,54
- 16,54
2. N,N(di-2-etanol) lauramida
0,1003 0,1002 16,18 16,18 10,079
0,1002 16,20
0,1002 16,18
3. N,N(di-2 etil
ftalatlauramida
0,1002 0,1002 15,38 15,38 32,47
0,1002 15,36
0,1003 15,36
Tabel 4.4. Data Penentuan Bilangan Asam
No Sampel Massa
sampel (gram) Massa sampel rata-rata (gram) Volume titrasi (ml) Volume titrasi rata-rata (ml) Bilangan asam
1. N,N (di-2-etanol) lauramida
0,1004 0,1003 4,22 4,24 47,43
0,1002 4,26
0,1003 4.24
2. N,N(di-2etil ftalat)lauramida
0,1002 0,1002 7,64 6,64 85,56
0,1003 7,66
0,1002 7,64
4.2. Pembahasan
[image:60.595.112.535.489.633.2]Pembuatan metil laurat secara esterifikasi antara asam laurat dengan metanol dalam pelarut benzena menggunakan katalis asam sulfat pekat pada kondisi refluks. Hasil yang diperoleh dianalisis dengan spektrofotometer FT-IR pada gambar 4.1, memberikan puncak serapan pada daerah bilangan gelombang 1742 cm-1yang merupakan pita serapan khas dari gugus C=O ester dan juga didukung oleh munculnya pita serapan pada daerah bilangan gelombang 1169 cm-1yang menunjukkan serapan khas C-O dari C-C(=O)-O ester. Sedangkan puncak serapan pada daerah bilangan gelombang diatas 3000 cm-1 yang merupakan serapan khas gugus O-H tidak lagi muncul. Hal ini membuktikan bahwa senyawa metil laurat yang diharapkan telah terbentuk. Puncak serapan pada daerah gelombang 2924 cm-1menunjukkan vibrasi streching asimetrik dari CH (sp3) dan puncak serapan pada daerah bilangan gelombang 2854 cm-1menunjukkan vibrasi streching simetrik dari CH (sp3) yang didukung oleh vibrasi bending CH (sp3) pada bilangan gelombang 1169 cm-1. Spektrum pada daerah bilangan gelombang 722 cm-1adalah vibrasi rocking gugus metilena (CH2)n dari alkena
berantai lurus yang terdiri dari tujuh atom karbon atau lebih (Silverstein,1984)
Mekanisme reaksi yang terjadi diperkirakan seperti pada gambar berikut:
CH3(CH2)10C
O
OH CH3(CH2)10C
+OH
OH
CH3OH
CH3(CH2)10C
OH OH O H3C H+
CH3(CH2)10C
OH OH O CH3
HSO4
-CH3(CH2)10C
OH O O CH3
H H
CH3(CH2)10C
O+ OCH3
CH3(CH2)10C
O
OCH3 + H
2SO4 HSO4
-+
Metil Laurat Asam Laurat
H+ HSO4
-H+ HSO4 --H2O
Gambar 4.5. Mekanisme reaksi esterifikasi asam laurat dengan metanol
Dalam media asam, pasangan elektron bebas atom oksigen karbonil dapat terprotonasi menghasilkan atom oksigen karbonil bermuatan positif, sehingga dengan demikian atom karbon karbonil dapat diserang oleh nukleofil yang lemah seperti metanol (Riswiyanto,2002)
4.2.2 Amidasi metil laurat dengan dietanolamina
Pembuatan N,N (di-2-etanol) lauramida dari hasil amidasi metil laurat dengan menggunakan dietanolamina dengan katalis natrium metoksida pada suhu 110-1200C. Hasil analisis yang diperoleh dengan spektrofotometer FT-IR pada gambar 4.2, memberikan spektrum dengan puncak pita serapan yang kuat pada daerah bilangan gelombang 3410 cm-1yang merupakan vibrasi streching dari gugus O-H. Selain itu, pita khas spektrum alkohol juga ditunjukkan oleh vibrasi streching dari C-O yang berada pada daerah bilangan gelombang 1064 cm-1. Munculnya puncak serapan pada bilangan gelombang 1566 cm-1yang merupakan serapan khas dari amida tersier, puncak serapan dari gugus C=O amida pada daerah bilang gelombang 1620 cm-1 menunjukkan bahwa senyawa yang telah terbentuk merupakan senyawa amida tersier. Hal ini didukung oleh adanya perubahan bilangan gelombang gugus C=O dari ester pada daerah bilangan gelombang 1743 cm-1, menjadi munculnya bilangan gelombang dari gugus C=O amida yaitu 1620 cm-1. Puncak serapan pada daerah gelombang 2916 cm-1menunjukkan vibrasi streching asimetrik dari CH (sp3) dan puncak serapan pada daerah bilangan gelombang 2846 cm-1menunjukkan vibrasi streching simetrik dari CH (sp3) yang didukung oleh vibrasi bending CH (sp3) pada bilangan gelombang 1442 cm
-1
. Spektrum pada daerah bilangan gelombang 717 cm-1adalah vibrasi rocking gugus metilena (CH2)n dari alkena berantai lurus yang terdiri dari tujuh atom karbon atau
lebih (Silverstein,1984)
CH3(CH2)10 C O
OCH3 + H N
CH2CH2OH
CH2CH2OH
CH3O- Na+
-CH3OH
CH3(CH2)10 C O
O Na
N
CH3
CH2CH2OH
CH2CH2OH
CH3(CH2)10 C O
O Na
N
CH3
CH2CH2OH
CH2CH2OH
-NaOCH3
CH3(CH2)10 C O
N
CH2CH2OH
CH2CH2OH
+ + -+ -H + dietanolamina
N,N (di-2-etanol) lauramida
CH3(CH2)10 C+
O
N
CH2CH2OH
CH2CH2OH
-Gambar 4.6. Mekanisme reaksi amidasi metil laurat dengan dietanolamina
Berdasarkan konsep HSAB (Hard Soft Acid Base), dimana H+ dari dietanolamina HN-(CH2CH2OH)2 merupakan asam keras yang mudah bereaksi
dengan basa keras CH3O- dari metil laurat sehingga membentuk metanol. Sebaliknya
nitrogen dengan sepasang elektron bebasnya merupakan basa lunak yang akan terikat pada asam lunak ion karboksilat R-C+=O dan membentuk senyawa alkanolamida.
4.2.3. EsterifikasiN,N (di-2-etanol) lauramida dengan anhidrida ftalat
[image:63.595.121.506.85.354.2]ini berada pada bilangan gelombang 1735 yang merupakan serapan khas dari gugus C=O ester dan didukung dengan vibrasi bending C-O dari (C-(C=O)-O) menunjukkan bahwa senyawa yang diharapkan telah terbentuk yang didukung juga dengan munculnya bilangan gelombang pada 3363 cm-1yang merupakan vibrasi streching
gugus O-H dari COOH. Puncak serapan pada daerah gelombang 2924 cm
-1
menunjukkan vibrasi streching asimetrik dari CH (sp3) dan puncak serapan pada daerah bilangan gelombang 2852 cm-1menunjukkan vibrasi streching simetrik dari CH (sp3) yang didukung oleh vibrasi bending CH (sp3) pada bilangan gelombang 1168 cm
-1
. Spektrum pada daerah bilangan gelombang 723 cm-1adalah vibrasi rocking gugus metilena (CH2)n dari alkena berantai lurus yang terdiri dari tujuh atom karbon atau
lebih (Silverstein,1984).
Hasil analisis spektroskopi FT-IR tersebut didukung juga oleh hasil spektrometer 1H-NMR. Dimana hasil tersebut menunjukkan puncak-puncak
[image:64.595.107.509.444.561.2]pergeseran kimia (δ) pada daerah-daerah berikut:
Tabel 4.5. Data Spektrometer 1H-NMR
No Daerah pergeseran kimia (ppm) Puncak Proton
1. 6,7446-6,7615 doublet-doublet CH=CH
2. 4,9377-4,9403 Triplet –CH2-O-C=O
3. 4,1530-4,1660 Triplet –CH2-O-
4. 2,2968-2,3189 Triplet –N-CH2
5. 2,0309-2,0439 Triplet –CH2-C=O
6. 1,1904-1,2994 Multiplet –CH2-
7. 0,8661-0,8934 Triplet CH3-
H3C (CH2)10 CH2 C
O N
CH2
CH2
CH2 O
CH2 O C
O
C C
C OH
O 0,8661 (T)
1,1904 (M)
2,0309 (T)
2,2968 (T)
4,1530 (T)
4,9377 (T)
6,7446 (D,D) C
C C
HC C
H CH
CH
C OH
HC CH
C
H CH
[image:65.595.117.510.82.303.2]O O
Gambar 4.7. Senyawa N,N(di-2-etil ftalat) Lauramida dengan pergeseran kimia
Dalam hal ini proton –OH dari COOH tidak terdeteksi pada spektrum 1H-NMR yang biasanya muncul pada pergeseran kimia 10-12 ppm, disebabkan pergeseran kimia yang dideteksi pada senyawa ini hanya pada 0-8 ppm. Tetapi spektrum FT-IR dapat memberikan dukungan adanya gugus OH dari COOH pada senyawa yang dihasilkan dengan munculnya puncak gelombang pada daerah 3363 cm-1 yang merupakan serapan khas gugus OH dari COOH. Hal ini juga didukung dari hasil penentuan bilangan asam maupun bilangan penyabunan. Meningkatnya bilangan asam dan bilangan penyabunan senyawa N,N(di-2 etil ftalat)lauramida dibandingkan N,N (di-2-etanol) lauramida menunjukan adanya kehadiran gugus OHdari COOH pada senyawa N,N(di-2 etil ftalat)lauramida yang dihasilkan.
O
O
O H+
Cl
-C C
O
CH3(CH2)10 C
O
N CH2CH2
CH2CH2
+
CH3(CH2)10 C O
N
CH2CH2 O C
CH2CH2 O C
O C O OH 2 anhidrida ftalat
N,N(di-2 etil ftalat) lauramida - HCl
O OH
O H O H+
O C O OH + :
Gambar 4.8. Mekanisme reaksi esterifikasi N,N (di-2-etanol) lauramida dengan anhidrida ftalat
Pada reaksi esterifikasi diatas, digunakan katalis HCl 1N sebanyak 4 tetes untuk membuka rantai siklik dari anhidrida ftalat. Dalam hal ini, reaksi tidak dapat berlangsung tanpa penggunaan katalis, tetapi dengan adanya molekul air dalam reaksi tersebut maka reaksi bersifat reversibel, sehingga dari hasil yang diharapkan dengan ratio pencampuran antara N,N (di-2-etanol) lauramida dengan anhidrida ftalat (1:2).
hidroksietil albizia benth oil amida dan kemudian melanjutkan reaksi esterifikasi dengan menggunakan anhidrida ftalat untuk dapat menggantikan gugus OH kedua yang tidak dapat digantikan oleh anhidrida maleat. Reaksi tersebut menghasilkan senyawa maleanised albizia benth oil poliesterami