UJI AKTIVITAS ANTIOKSIDAN EKSTRAK DAUN
RAMBUTAN (
Nephelium lappaceum
Linn) DENGAN METODE
DPPH (2,2-DIFENIL-1-PIKRILHIDRAZIL)
SKRIPSI
SONIA ULFAH
1111102000116
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
UIN SYARIF HIDAYATULLAH JAKARTA
UJI AKTIVITAS ANTIOKSIDAN EKSTRAK DAUN
RAMBUTAN (
Nephelium lappaceum
Linn) DENGAN METODE
DPPH (2,2-DIFENIL-1-PIKRILHIDRAZIL)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
SONIA ULFAH
1111102000116
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
ABSTRAK
Nama : Sonia Ulfah
Jurusan : Farmasi
Judul : Uji Aktivitas Antioksidan Ekstrak Daun Rambutan
(Nephelium lappaceum Linn) dengan Metode DPPH
(2,2-Difenil-1-Pikrilhidrazil)
Penelitian ini dilakukan untuk menguji aktivitas antioksidan ekstrak
daun rambutan (Nephelium Lappaceum Linn) dengan metode DPPH. Ekstrak
daun rambutan diekstraksi secara maserasi langsung dengan etanol 70%
sehingga diperoleh ekstrak etanol total (E1) daun rambutan dan dilanjutkan
dengan pemisahan secara partisi sehingga diperoleh ekstrak fraksi
n-Heksana (NH), fraksi etil asetat (EA) dan fraksi etanol (E2). Pengujian aktivitas
antioksidan ekstrak daun rambutan ini dilakukan menggunakan metode
DPPH (2,2-difenil-1-pikrilhidrazil) dengan vitamin C sebagai kontrol positif.
Hasil uji aktivitas antioksidan yang dilakukan menunjukkan nilai AAI
(Antioksidant Activity Index) ekstrak etanol total (E1), fraksi n-Heksana (NH),
fraksi etil asetat (EA), fraksi etanol (E2), dan vitamin C berturut-turut
2,1488 (sangat kuat); 0,1401 (lemah); 0,8488 (sedang); 1,5767 (kuat); dan
10,6383 (sangat kuat).
ABSTRACT
Name : Sonia Ulfah
Departement : Pharmacy
Title : Antioxidant Activity Test of Rambutan Leave
(Nephelium lappaceum Linn) Extract Using the DPPH
(2,2-Diphenyl-1-Picryhidrazyl) Method
This study aimed to find out antioxidant activity leave extract
of rambutan (Nephelium lappaceum Linn). Leave extract of rambutan
(Nephelium lappaceum Linn) extracted by maceration with ethanol 70% to obtain
the total ethanol leave extract (E1) of rambutan and continued with
the separation partition thus obtained n-hexane fraction extract (NH), ethyl
acetate fraction (EA) and the ethanol fraction (E2). Antioxidant activity
testing was tested by DPPH (2,2-diphenyl-1-picrylhydrazyl) method
with vitamin C as a positive control. The results of antioxidant activity
showed that AAI (Antioxidant Activity Index) value of total ethanol
extract (E1), n-hexane fraction (NH), ethyl acetate fraction (EA), ethanol
fraction (E2) and vitamin C were 2,1488 (very strong); 0,1401 (weak);
0,8488 (moderate); 1,5767 (strong); and 10,6383 (very strong).
KATA PENGANTAR
Bismillahirrahmanirrahim.
Alhamdulillahirabbil’alamin, puji syukur ke hadirat Allah SWT yang telah melimpahkan segala rahmat dan karunia-Nya, sehingga penulis dapat
menyelesaikan penulisan skripsi dengan judul “Uji Aktivitas Antioksidan Ekstrak
Daun Rambutan dengan Metode DPPH (2,2-Difenil-1-Pikrilhidrazil)”. Shalawat
serta salam semoga senantiasa tercurah limpahkan pada Nabi Muhammad SAW
beserta para keluarga dan sahabatnya.
Skripsi ini disusun sebagai salah satu syarat kelulusan tingkat sarjana
di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas
Islam Negeri Syarif Hidayatullah Jakarta. Penelitian ini tidaklah dapat
terselesaikan tanpa dukungna dan bantuan dari berbagai pihak. Dalam kesempatan
ini, penulis ingin mengucapkan terima kasih terkhususkan kepada:
1. Prof. Dr. Atiek Soemiati, M.Si., Apt. dan Ibu Eka Putri, M.Si., Apt.
selaku pembimbing yang telah meluangkan banyak waktu untuk
memberikan bimbingan, motivasi, serta dorongan kepada penulis dari
awal hingga skripsi ini dapat terselesaikan.
2. Bapak Dr. H. Arif Sumantri, SKM., M. Kes. selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan, UIN Syarif Hidayatullah Jakarta.
3. Bapak Yardi, M.Si., Ph.D., Apt. selaku Ketua Program Studi Farmasi
UIN Syarif Hidayatullah Jakarta dan Ibu Nelly Suryani, Ph.D., Apt.
selaku sekretaris Program Studi Farmasi UIN Syarif Hidayatullah
Jakarta.
4. Seluruh dosen di Program Studi Farmasi Fakultas Kedokteran dan
Ilmu Kesahatan UIN Syarif Hidayatullah Jakarta atas ilmu
pengetahuan selama penulis menempuh pendidikan.
5. Kepada orang tuaku tercinta, Ayahanda A. Syamsuryana dan Ibunda
non materil, motivasi, dan juga kepada penulis untuk menyelesaikan
skripsi ini.
6. Adik-adikku tersayang Dian Mayasanti, M. Regi Saputra dan
M. Rachel Jabar Winara yang senantiasa memberikan semangat dan
keceriaan kepada penulis.
7. Untuk orang spesial Al Kahfi yang selalu memberikan semangat dan
bantuan kepada penulis.
8. Untuk kakak kelasku tersayang Ka Oni Maria Sari yang selalu
memberikan bantuan, semangat kepada penulis.
9. Teman-teman seperjuangan Farmasi Angkatan 2011 khususnya
Farmasi BD yang selalu memberikan semangat dan kekompakannya
semasa kuliah.
10. Kak Lisna, Kak Tiwi, Kak Eris, Mba Rani, Kak Yaenap, Kak Rahmadi
dan Kak Walid yang telah membantu keseharian penulis selama
penelitian di laboratorium.
11. Serta semua pihak yang telah membantu penulis selama ini yang tidak
dapat penulis sebutkan satu per satu.
Semoga Allah SWT memberikan balasan yang berlipat ganda atas segala
bantuan dan dukungannya kepada penulis. Penulis menyadari bahwa dalam
penulisan skripsi ini masih banyak kelemahan dan kekurangan. Maka dari itu,
dengan segala kerendahan hati penulis sangat mengharapkan kritik dan saran
pembaca agar lebih sempurnanya skripsi ini.
Jakarta, 14 Januari 2016
DAFTAR ISI
2.1.2.2 Daerah Asal dan Penyebaran ... 5
2.1.2.3 Kandungan Kimia ... 5
2.1.2.4 Khasiat dan Kegunaan ... 6
2.2 Simplisia ... 6
2.3 Ekstraksi ... 6
2.4 Pemisahan secara Partisi ... 9
2.5 Penapisan Fitokimia ... 9
2.6 Kromatografi Lapis Tipis ... 10
2.7 Radikal Bebas... 12
2.8 Antioksidan ... 13
2.9 Uji Aktivitas Antioksidan dengan Metode DPPH ... 15
BAB 3 METODOLOGI PENELITIAN ... 18
3.3.5 Pemisahan secara Partisi Ekstrak Etanol Total (E1) Daun Rambutan (Nephelium lappaceum Linn) dengan Pelarut n-Heksan, Etil Asetat dan Etanol ... 21
3.3.6 Pengujian Antioksidan secara Kualitatif dengan Metode Kromatografi Lapis Tipis (KLT) ... 22
3.3.7 Pengujian Antioksidan secara Kuantitatif dengan Metode DPPH ... 22
3.3.7.1 Pembuatan Larutan DPPH 0,1 mM ... 22
3.3.7.2 Penentuan Panjang Gelombang Serapan Maksimum DPPH ... 22
3.3.7.3 Pembuatan Larutan Blanko ... 23
3.3.7.4 Pembuatan Larutan Pembanding Vitamin C ... 23
3.3.7.5 Pembuatan Larutan Uji Ekstrak Daun Rambutan .. 23
3.3.8 Analisa Data ... 24
BAB 4 Hasil dan Pembahasan ... 26
4.1 Determinasi Tanaman ... 26
4.2 Penyiapan Sampel ... 26
4.3 Ekstraksi ... 27
4.4 Penapisan Fitokimia Ekstrak Etanol Total (E1) Daun Rambutan . 28 4.5 Pemisahan secara Partisi Ekstrak Etanol Total (E1) Daun Rambutan ... 29
4.6 Uji Aktivitas Antioksidan secara Kualitatif ... 30
4.7 Uji Aktivitas Antioksidan secara Kantitatif ... 31
BAB 5 Kesimpulan dan Saran ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40
DAFTAR GAMBAR
Gambar 2.1 Daun Rambutan (Nephelium lappaceum Linn)... 4 Gambar 2.2 Reduksi DPPH dari Senyawa Peredam Radikal Bebas... 15 Gambar 4.1 Kurva Hubungan Konsentrasi dan % Inhibisi Ekstrak Etanol Total
(E1) Daun Rambutan... 35
Gambar 4.2 Kurva Hubungan Konsentrasi dan % Inhibisi Ekstrak Fraksi n-Heksana (NH) Daun Rambutan ... 35
Gambar 4.3 Kurva Hubungan Konsentrasi dan % Inhibisi Ekstrak Fraksi Etil Asetat (EA) Daun Rambutan ... 36
Gambar 4.4 Kurva Hubungan Konsentrasi dan % Inhibisi Ekstrak Fraksi Etanol (E2) Daun Rambutan ... 36
DAFTAR TABEL
Tabel 4.1 Hasil Ekstraksi Daun Rambutan ... 27
Tabel 4.2 Hasil Penapisan Fitokimia Ekstrak Etanol Daun Rambutan ... 28
Tabel 4.3 Hasil Partisi Ekstrak Etanol Total (E1) Daun Rambutaan ... 29
Tabel 4.4 Hasil Uji Kualitatif Antioksidan Ekstrak Daun Rambutan ... 30
Tabel 4.5 Hasil Uji Aktivitas Antioksidan Ekstrak Etanol Total (E1) Daun Rambutan ... 32
Tabel 4.6 Hasil Uji Aktivitas Antioksidan Ekstrak Fraksi n-Heksan (NH) Daun Rambutan ... 33
Tabel 4.7 Hasil Uji Aktivitas Antioksidan Ekstrak Fraksi Etil Asetat (EA) Daun Rambutan ... 33
Tabel 4.8 Hasil Uji Aktivitas Antioksidan Ekstrak Fraksi Etanol (E2) Daun Rambutan ... 33
DAFTAR LAMPIRAN
Lampiran 1 Alur Penelitian ... 44
Lampiran 2 Hasil Determinasi Daun Rambutan ... 45
Lampiran 3 Penapisan Fitokimia Ekstrak Etanol Total (E1) Daun Rambutan (Nephelim lappaceum Linn) ... 46
Lampiran 4 Perhitungan Rendemen Ekstrak Daun Rambutan ... 47
Lampiran 5 Sertifikat Analisa DPPH ... 48
Lampiran 6 Panjang Gelombang Maksimum DPPH ... 49
Lampiran 7 Data Absorbansi Ekstrak Etanol Total (E1) Daun Rambutan ... 50
Lampiran 8 Data Absorbansi Ekstrak Fraksi n-Heksana (NH) Daun Rambutan ... 51
Lampiran 9 Data Absorbansi Ekstrak Fraksi Etil Asetat (EA) Daun Rambutan ... 52
Lampiran 10 Data Absorbansi Ekstrak Fraksi Etanol (E2) Daun Rambutan ... 53
Lampiran 11 Data Absorbansi Vitamin C ... 54
Lampiran 12 Perhitungan dalam Uji Antioksidan ... 55
Lampiran 13 Perhitungan Persen Inhibisi ... 58
Lampiran 14 Perhitungan IC50 ... 63
Lampiran 15 Perhitungan Nilai AAI ... 65
BAB I PENDAHULUAN
1.1 Latar Belakang
Penggunaan senyawa antioksidan semakin berkembang baik untuk
makanan maupun pengobatan seiring dengan bertambahnya pengetahuan
tentang radikal bebas (Boer, 2000). Radikal bebas merupakan salah satu
bentuk senyawa yang mempunyai elektron tidak berpasangan
(Winarsi, 2007). Adanya elektron tidak berpasangan menyebabkan
senyawa tersebut sangat reaktif mencari pasangan. Radikal bebas ini akan
merebut elektron dari molekul lain yang ada di sekitarnya untuk
menstabilkan diri. Radikal bebas erat kaitannya dengan kerusakan sel,
kerusakan jaringan, dan proses penuaan (Fessenden dan Fessenden, 1986).
Radikal bebas yang merusak tubuh ini dapat dinetralisir oleh
senyawa antioksidan. Antioksidan merupakan senyawa yang dapat
menghambat oksigen reaktif dan radikal bebas dalam tubuh. Senyawa
antioksidan ini akan menyerahkan satu atau lebih elektron bebas sehingga
menjadi bentuk molekul yang normal kembali dan menghentikan berbagai
kerusakan yang ditimbulkan (Sashikumar, et al., 2009). Tubuh manusia
tidak mempunyai cadangan antioksidan dalam jumlah berlebih, sehingga
jika terjadi paparan radikal bebas berlebih maka tubuh membutuhkan
antioksidan eksogen (Rohdiana, 2001).
Pemanfaatan bahan alam yang mempunyai aktivitas biologis
menjadi motivasi dilakukannya penelitian lebih lanjut, setelah
senyawa-senyawa sintetik yang mempunyai aktivitas biologis seperti
senyawa antioksidan sintetik butylated hydroxytoluen (BHT),
butylated huydroxyanisole (BHA) dan terbutylhydroxyquinone (TBHQ)
dibatasi penggunannnya karena bersifat karsinogenik. Berbagai studi
mengenai BHA dan BHT menunjukkan bahwa komponen ini dapat
menimbulkan tumor pada hewan percobaan pada penggunaan dalam
jangka panjang (Andarwulan, 1996). Adanya kekhawatiran akan
antioksidan alami menjadi alternatif yang sangat dibutuhkan
(Rohdiana, 2001).
Antioksidan alami mampu melindungi tubuh terhadap kerusakan
yang disebabkan senyawa oksigen reaktif, yang mampu menghambat
terjadinya penyakit degeneratif seperti diabetes, kanker,
inflamasi jaringan, kelainan imunitas, infark jantung dan penuaan dini
(Middleton, et al., 2000).
Rambutan (Nephelium lappaceum Linn) merupakan salah satu
tanaman yang banyak terdapat di Indonesia. Secara tradisional tanaman
rambutan digunakan untuk pengobatan berbagai penyakit, antara lain kulit
buahnya untuk mengatasi sariawan, daun untuk mengatasi diare dan
menghitamkan rambut, akar untuk mengatasi demam dan serat bijinya
untuk mengatasi diabetes mellitus (Tjandra, et al., 2011).
Kulit dan biji rambutan yang tumbuh di Thailand memiliki sifat
antioksidan dan antibakteri (Thitilertdecha, et al., 2008). Kulit buah
rambutan mengandung senyawa golongan tanin, polifenol, dan saponin
(Tjandra, et al., 2011). Daun rambutan (Naphelium lappaceum Linn)
mengandung senyawa saponin, tanin (Dalimarta, 2003).
Ekstrak etanol daun rambutan (Nephelium lappaceum Linn)
efektif untuk membunuh larva Aedes aegypti instar III (Asiah, 2008).
Menurut Maradona (2013) ekstrak etanol daun rambutan
(Nephelium lappaceum Linn) yang tumbuh di taman Fakultas Kedokteran
dan Ilmu Kesehatan memiliki aktivitas antibaketri terhadap bakteri
Staphylococcus aureus ATCC 25925 serta mengandung metabolit
sekunder yaitu flavonoid, saponin, tanin dan hidrokuinon.
Berdasarkan laporan penelitian-penelitian tersebut, maka
dilakukan pengujian aktivitas antioksidan ekstrak daun rambutan yang
diekstraksi secara maserasi langsung dengan pelarut etanol 70% dan
pemisahan secara partisi dengan pelarut n-Heksana, etil asetat, dan etanol
menggunakan metode DPPH (2,2-difenil-1-pikrilhidrazil). Metode DPPH
memerlukan sedikit sampel dan dapat mengukur aktivitas total antioksidan
baik dalam pelarut polar maupun nonpolar (Prakash, 2001).
1.2 Rumusan Masalah
a. Apakah ekstrak daun rambutan (Nephelium lappaceum Linn) memiliki
aktivitas antioksidan?
b. Berapakah nilai IC50 (Inhibitory Concentration) dan nilai AAI
(Antioxidant Activity Index) dari masing masing ekstrak daun
rambutan (Nephelium lappaceum Linn)?
1.3 Tujuan Penelitian
Untuk menguji aktivitas antioksidan dari ekstrak daun
rambutan (Nephelium lappaceum Linn) dengan metode DPPH
(2,2-difenil-1-pikrilhidrazil).
1.4 Manfaat Penelitian
Untuk memberikan informasi yang dapat dipertanggungjawabkan
secara ilmiah kepada masyarakat mengenai aktivitas antioksidan dari
ekstrak daun rambutan (Nephelium lappaceum Linn), sehingga daun ini
dapat digunakan sebagai antioksidan alami.
BAB 2
TINJAUAN PUSTAKA
2.1 Daun Rambutan
2.1.1 Sistematika Daun Rambutan
Daun rambutan (Nephelium lappaceum Linn) memiliki sistematika
tanaman sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Sapindales
Famili : Sapindaceae
Genus : Nephelium
Spesies : Nephelium lappaceum Linn
(Rukmana, et al., 2002)
2.1.2 Uraian Tanaman 2.1.2.1Morfologi
Rambutan merupakan tanaman tahunan. Secara alami, pohon
rambutan dapat mencapai ketinggian 5m-9m. Batang rambutan berkayu
keras, berbentuk gilig, tumbuh kokoh dan berwarna kecoklat-coklatan
sampai putih kecoklatan. Percabangan tumbuh secara horizontal, namun
kadang-kadang sedikit miring ke arah atas. Daun rambutan berbentuk
bulat panjang dengan ujung tumpul atau meruncing, dan pada umumnya
Nikolai Ivanovich Vavulov, sentrum utama asal tanaman rambutan adalah
daerah Indo-Malaya, yang meliputi Indo-Cina, Malaysia, Indonesia dan
Filipina. Di wilayah ini ditemukan sumber genetik rambutan. Para ahli
botani kemudian memastikan bahwa daerah asal tanaman rambutan adalah
Malaysia dan Indonesia. Di Indonesia, tanaman rambutan tersebar di
berbagai wilayah, terutama di Jawa, Kalimantan, dan Sumatera
(Rukmana, 2002).
2.1.2.3 Kandungan Kimia
Daun rambutan (Naphelium lappaceum Linn) mengandung
senyawa saponin, tannin (Dalimarta, 2003). Kulit buah rambutan
mengandung senyawa senyawa golongan tanin, polifenol, dan saponin
(Tjandra, et al., 2011). Kulit batang rambutan mengandung tanin, saponin,
flavonoid, dan zat besi. Buahnya mengandung karbohidrat, protein,
lemak, fosfor, besi, kalsium dan vitamin C. Kulit buah rambutan
mengandung tanin dan saponin. Ekstrak etanol daun rambutan
(Nephelium lappaceum Linn) memiliki kandungan kimia flavonoid,
2.1.2.4 Khasiat dan Kegunaan
Tanaman rambutan digunakan untuk pengobatan berbagai
penyakit, antara lain kulit buahnya untuk mengatasi sariawan, daun untuk
mengatasi diare dan menghitamkan rambut, akar untuk mengatasi demam
dan serat bijinya untuk mengatasi Diabetes mellitus (Tjandra, et al., 2011).
Kulit dan biji rambutan yang tumbuh di Thailand memiliki sifat
antioksidan dan antibakteri (Thitilertdecha, et al., 2008). Ekstrak etanol
daun rambutan (Nephelium lappaceum Linn) efektif untuk membunuh
larva Aedes aegypti instar III (Asiah, 2008) serta memiliki aktivitas
antibaketri terhadap bakteri Staphylococcus aureus ATCC 25925
(Maradona, 2013).
2.2 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai bahan
obat yang belum mengalamai pengolahan apapun kecuali dinyatakan lain,
berupa bahan yang telah dikeringkan. Simplisia dibedakan menjadi tiga,
yaitu simplisia nabati, simplisia hewani, dan simplisia pelikan (mineral).
Simplisia nabati adalah simplisia yang berupa tanaman utuh, bagian
tanaman atau eksudat tanaman. Eksudat tumbuhan ialah isi sel yang secara
spontan keluar dari tumbuhan atau isi sel yang dengan cara tertentu
dipisahkan dari tumbuhannya dan belum berupa senyawa kimia murni
(Anonim, 2000).
2.3 Ekstrak dan Ekstraksi
Ekstrak adalah sediaan kental yang diperoleh dengan
mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani
menggunakan pelarut yang sesuai, kemudian semua atau hampir semua
pelarut dan massa atau serbuk yang tersisa diperlakukan sehingga
memenuhi baku yang telah ditetapkan (Soesilo, 1995). Ekstrak adalah
sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati
atau hewani menurut cara yang sesuai, diluar pengaruh cahaya matahari
Parameter yang mempengaruhi kualitas dari ekstrak adalah bagian
dari tumbuhan yang digunakan, pelarut yang digunakan untuk ekstraksi,
dan prosedur ekstraksi (Tiwari, et al., 2011).
Ekstraksi adalah pemisahan bagian aktif sebagai obat dari jaringan
tumbuhan ataupun hewan menggunakan pelarut yang sesuai melalui
prosedur yang telah ditetapkan (Tiwari, et al., 2011). Selama proses
ekstraksi, pelarut akan berdifusi sampai ke material padat dari tumbuhan
dan akan melarutkan senyawa dengan polaritas yang sesuai dengan
pelarutnya (Tiwari, et al., 2011).
Beberapa metode ekstraksi dengan menggunakan pelarut dibagi
menjadi dua cara, yaitu cara panas dan cara dingin (Ditjen POM, 2000).
Ekstraksi cara dingin dapat dibedakan sebagai berikut:
1. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut
dengan beberapa kali pengocokan atau pengadukan pada temperatur
kamar (Ditjen POM, 2000). Keuntungan ekstraksi dengan cara
maserasi adalah pengerjaan dan peralatan yang digunakan sederhana,
sedangkan kerugiannya yakni cara pengerjaannya lama, membutuhkan
pelarut yang banyak dan penyarian kurang sempurna. Dalam maserasi
(untuk ekstrak cairan), serbuk halus atau kasar dari tumbuhan obat
yang kontak dengan pelarut disimpan dalam wadah tertutup untuk
periode tertentu dengan pengadukan yang sering, sampai zat tertentu
dapat terlarut. Metode ini cocok digunakan untuk senyawa yang
termolabil (Tiwari, et al., 2011).
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
terjadi penyarian sempurna yang umumnya dilakukan pada temperatur
kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap
perendaman, tahap perkolasi antara, tahap perkolasi sebenarnya
(penampungan ekstrak) secara terus menerus sampai diperoleh
ekstrak (perkolat). Untuk menentukan akhir dari pada perkolasi dapat
akhir. Ini adalah prosedur yang paling sering digunakan untuk
mengekstrak bahan aktif dalam penyusunan tincture dan ekstrak cairan
(Tiwari, et al., 2011).
Ekstraksi cara panas dapat dibedakan sebagai berikut:
1. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru,
dengan menggunakan alat soklet sehingga terjadi ekstraksi continue
dengan jumlah pelarut relatif konstan dengan adanya pendingin balik
(Ditjen POM, 2000).
2. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada
temperatur titik didihnya, selama waktu tertentu dan jumlah
pelarut terbatas yang relatif konstan dengan adanya pendingin balik
(Ditjen POM, 2000).
3. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur 900C selama
15 menit. Infus adalah ekstraksi menggunakan pelarut air pada
temperatur penangas air dimana bejana infus tercelup dalam penangas
air mendidih, temperatur yang digunakan (96-980C) selama waktu
ekstraksi dengan pelarut air pada temperatur 900C selama 30 menit.
Metode ini digunakan untuk ekstraksi konstituen yang larut dalam
air dan konstituen yang stabil terhadap panas (Tiwari, et al., 2011).
5. Digesti
Digesti adalah maserasi kinetik pada temperatur lebih tinggi dari
temperatur suhu kamar, yaitu secara umum dilakukan pada temperatur
pengadukan continue pada temperatur lebih tinggi dari temperatur
ruang (umumnya 25-300C). Ini adalah jenis ekstraksi maserasi di mana
suhu sedang digunakan selama proses ekstraksi (Tiwari, et al., 2011).
2.4 Pemisahan secara Partisi (Pemisahan Cair-cair)
Pemisahan dengan cara partisi atau dikenal juga dengan pemisahan
cair-cair pelarut merupakan metode pemisahan suatu senyawa berdasarkan
tingkat kelarutannya di dalam campuran dua pelarut yang tidak bercampur.
Dalam proses isolasi kandungan kimia dari bahan alam, penggunaan
metode partisi dimaksudkan untuk memisahkan campuran komponen
kimia yang terdapat dalam ekstrak dengan menggunakan dua pelarut yang
tidak saling bercampur. Komponen kimia yang ada pada ekstrak tumbuhan
akan larut ke dalam pelarut yang sesuai dengan tingkat kepolaran yang
dimiliki oleh senyawa tersebut (Hostettmann, 2007).
Satu hal yang penting dalam proses memisahkan senyawa dengan
menggunakan metode partisi ini adalah langkah dalam pemilihan
pelarutnya. Dimana pelarut yang dipilih merupakan campuran dua
pelarut yang tidak saling bercampur. Beberapa contoh campuran pelarut
yang digunakan adalah air-diklorometana, air-eter, air-heksana
(Hostettmann, 2007).
2.5 Penapisan Fitokimia
Penapisan fitokimia merupakan tahap pendahuluan dalam suatu
penelitiain fitokimia yang bertujuan untuk memberikan gambaran tentang
golongan senyawa yang terkandung dalam tanaman yang sedang diteliti.
Metode skrining fitokimia dilakukan untuk melihat reaksi pengujian warna
dengan menggunakan suatu pereaksi warna. Hal yang paling berperan
penting dalam penapisan fitokimia adalah pemilihan pelarut dan
2.6 Kromatografi Lapis Tipis (KLT)
Kromatografi lapis tipis (KLT) merupakan salah satu metode
pilihan kromatografi secara fisikokimia (Gandjar dan Rohman, 2007).
Kromatografi lapis tipis (KLT) merupakan bentuk kromatografi planar, selain kromatografi kertas dan elektroforesis. Pada KLT fase diamnya
berupa lapisan yang seragam (uniform) pada permukaan bidang datar yang
didukung oleh lempeng kaca, plat aluminium atau plat plastik. Meskipun
demikian, kromatografi planar ini merupakan bentuk terbuka dari
kromatografi kolom (Gritter, et al., 1991).
Kromatografi lapis tipis (KLT) dapat dipakai dengan dua
tujuan. Pertama, dipakai untuk mencapai hasil kualitatif, kuantitatif
atau preparatif. Kedua dipakai untuk menjajaki sistem pelarut dan
sistem penyangga yang akan dipakai dalam kromatografi kolom
(Gritter, et al., 1991).
Kromatografi lapis tipis (KLT) dapat digunakan untuk tujuan
analitik dan preparatif. KLT analitik digunakan untuk menganalisa
senyawa-senyawa organik dalam jumlah kecil misalnya, menentukan
jumlah komponen dalam campuran dan menentukan pelarut yang tepat
untuk pemisahan dengan KLT preparatif sedangkan KLT preparatif
digunakan untuk memisahkan campuran senyawa dari sampel dalam
jumlah besar berdasarkan fraksinya, yang selanjutnya fraksi-fraksi
tersebut dikumpulkan dan digunakan untuk analisa berikutnya
(Townshend, 1995).
Kromatografi lapis tipis (KLT) merupakan teknik yang benar-benar
menguntungkan karena tingkat sensitivitasnya sangat besar dan
konsekuensinya jumlah sampel lebih sedikit. Fase gerak yang dikenal
sebagai pelarut pengembang atau cairan pengelusi akan bergerak
sepanjang fase diam karena pengaruh kapiler pada pengembangan secara
mekanik (ascending), atau karena pengaruh gravitasi pada pengembangan
menurun (descending) (Gritter, et al., 1991).
Jumlah volume fase gerak harus mampu mengelusi lempeng
terelusi, dilakukan deteksi bercak (Gandjar dan Rohman, 2007).
Laju pergerakan fase gerak terhadap fase diam dihitung sebagai
retardation farctor (Rf). Nilai Rf diperoleh dengan membandingkan jarak
yang ditempuh oleh zat terlarut dengan jarak yang ditempuh oleh fase
gerak (Gandjar dan Rohman, 2007).
Fase gerak harus memiliki kemurnian yang tinggi. Fase gerak yang
digunakan adalah pelarut organik yang memiliki tingkat polaritas
tersendiri, melarutkan senyawa contoh, dan tidak bereaksi dengan
penjerap. Adsorben umumnya digunakan dalam KLT meliputi partikel
silika gel ukuran 12 µm, alumina, mineral oksida, silika gel dengan
ikatan kimia, selulosa, poliamida, polimer penukar ion, silika gel, dan
fase kiral (Gritter, et al., 1991).
Ada beberapa cara untuk mendeteksi senyawa yang tidak berwarna
pada kromatogram. Deteksi paling sederhana adalah jika senyawa
menunjukkan penyerapan di daerah UV gelombang pendek
(radiasi utama kira-kira 254 nm) atau jika senyawa itu dapat dieksitasi
pada radiasi UV gelombang pendek dan gelombang panjang (365 nm).
Pada senyawa yang mempunyai dua ikatan rangkap atau lebih dan
senyawa aromatik seperti turunan benzena, mempunyai serapan
kuat ± di daerah 230-300 nm (Stahl, 1985).
Identifikasi dari senyawa-senyawa yang terpisah dari lapisan tipis
menggunakan nilai Rf. Polaritas fase gerak perlu diperhatikan pada analisa
dengan KLT, sebaiknya digunakan campuran pelarut organik yang
mempunyai polaritas serendah mungkin. Campuran pelarut yang baik
memberikan fase gerak yang mempunyai kekuatan bergerak sedang.
Secara umum dikatakan bahwa fase diam yang polar akan mengikat
senyawa polar dengan kuat sehingga bahan yang kurang sifat
kepolarannya akan bergerak lebih cepat dibandingkan bahan-bahan polar
2.7 Radikal Bebas
Radikal bebas merupakan salah satu bentuk senyawa yang
mempunyai elektron tidak berpasangan (Winarsi, 2007). Adanya elektron
tidak berpasangan menyebabkan senyawa tersebut sangat reaktif mencari
pasangan. Radikal bebas ini akan merebut elektron dari molekul lain yang
ada di sekitarnya untuk menstabilkan diri. Radikal bebas erat kaitannya
dengan kerusakan sel, kerusakan jaringan, dan proses penuaan
(Fessenden dan Fessenden, 1986). Radikal bebas juga dapat mengubah
suatu molekul menjadi suatu radikal (Winarsi, 2007).
Radikal bebas akan menyerang biomakromolekul penting dalam
tubuh seperti komponen penyusun sel, yaitu protein, asam nukleat, lipid
dan polisakarida. Target utama radikal bebas adalah protein, asam lemak
tak jenuh dan lipoprotein serta DNA termasuk polisakaridanya. Asam
lemak tak jenuh adalah yang paling rentan. Radikal bebas akan merusak
lemak tak jenuh ganda pada membran sel sehingga dinding sel menjadi
rapuh, merusak pembuluh darah dan menimbulkan aterosklerosis. Radikal
bebas juga merusak basa DNA sehingga mengacaukan sistem informasi
genetika dan membentuk sel kanker. Jaringan lipid juga akan dirusak oleh
senyawa radikal bebas sehingga terbentuk peroksida dan menimbulkan
penyakit degeneratif (Winarsi, 2007).
Serangan radikal bebas terhadap molekul sekelilingnya dapat
menyebabkan reaksi berantai dan kemudian menghasilkan senyawa radikal
baru. Hal ini akan menimbulkan kerusakan sel atau jaringan, penyakit
degeneratif hingga kanker. Berbagai gangguan akibat kerja radikal bebas
adalah gangguan fungsi sel, kerusakan struktur sel, molekul yang tidak
teridentifikasi oleh sistem imun bahkan mutasi. Semua gangguan tersebut
memicu timbulnya berbagai macam penyakit (Winarsi, 2007).
Secara umum, tahapan reaksi pembentukan reaksi radikal bebas
melalui 3 tahapan reaksi yaitu inisiasi, propagasi dan terminasi. Tahap
inisiasi merupakan awal pembentukan radikal bebas, tahap propagasi
merupakan pemanjangan rantai dan tahap terminasi merupakan
radikal sehingga potensi propagasinya rendah. Reaktivitas radikal bebas
dapat dihambat dengan cara (Winarsi, 2007):
a. Mencegah (prevention) atau menghambat (inhibition)
pembentukan radikal bebas baru.
b. Menginaktivasi (inactivation) atau menangkap radikal
bebas (free radical scavenger) dan memotong propagasi
(pemutusan rantai).
c. Memperbaiki (repaire) kerusakan yang diakibatkan oleh
radikal bebas.
2.8 Antioksidan
Antioksidan merupakan substansi penting yang mampu melindungi
tubuh dari serangan radikal bebas dan meredamnya. Konsumsi antioksidan
dalam jumlah memadai mampu menurunkan resiko terkena penyakit
degeneratif seperti kardiovaskuler, kanker, aterosklerosis, osteoporosis dan
lain-lain. Konsumsi makanan yang mengandung antioksidan dapat
meningkatkan status imunologi dan menghambat timbulnya penyakit
degeneratif akibat penuaan. Kecukupan antioksidan secara optimal
dibutuhkan oleh semua kelompok umur (Winarsi, 2007).
Antioksidan merupakan substansi nutrisi maupun non-nutrisi yang
terkandung dalam bahan pangan, yang mampu mencegah atau
memperlambat terjadinya kerusakan oksidatif dalam tubuh. Antioksidan
merupakan senyawa pemberi elektron (elektron donor) atau
reduktan/reduktor. Antioksidan mampu menghambat reaksi oksidasi
dengan cara mengikat radikal bebas dan molekul yang sangat reaktif
sehingga kerusakan sel dapat dicegah. Senyawa ini mempunyai berat
molekul kecil tapi mampu menginaktivasi reaksi oksidasi dengan
mencegah terbentuknya radikal (Winarsi, 2007).
Tubuh manusia mempunyai sistem antioksidan yang diproduksi
secara continue untuk menangkal atau meredam radikal bebas, seperti
enzim superoksida dismutase (SOD), katalase dan glutation peroksidase.
dalam tubuh maka radikal bebas akan menyerang komponen lipid, protein
dan DNA. Sehingga tubuh kita membutuhkan asupan antioksidan yang
mampu melindungi tubuh dari serangan radikal bebas tersebut
(Winarsi, 2007).
Antioksidan penting untuk kesehatan dan kecantikan serta
mempertahankan mutu produk pangan. Di bidang kesehatan dan
kecantikan, antioksidan berfungsi untuk mencegah penyakit kanker dan
tumor, penyempitan pembuluh darah, penuaan dini, dan lain-lain
(Tamat, et al. 2007). Antioksidan juga mampu menghambat reaksi
oksidasi dengan cara mengikat radikal bebas dan molekul yang sangat
reaktif sehingga kerusakan sel dapat dicegah. Reaksi oksidasi dengan
radikal bebas sering terjadi pada molekul protein, asam nukleat, lipid dan
polisakarida (Winarsi, 2007).
Konsumsi antioksidan dalam jumlah memadai mampu menurunkan
resiko terkena penyakit degeneratif seperti kardiovaskuler, kanker,
aterosklerosis, osteoporosis, dan lain-lain. Konsumsi makanan yang
mengandung antioksidan dapat meningkatkan status imunologi dan
menghambat timbulnya penyakit degeneratif akibat penuaan. Kecukupan
antioksidan secara optimal dibutuhkan oleh semua kelompok umur
(Winarsi, 2007).
Antioksidan dapat berupa enzim (misalnya superoksida dismutase
atau SOD, katalase dan glutation peroksidase), vitamin (misalnya
vitamin E, C, A dan beta-karoten), dan senyawa non enzim (misalnya
flavanoid, albumin, bilirubin, seruloplasmin dan lain-lain) (Winarsi, 2007).
Menurut Winarsi (2007) antioksidan berdasarkan fungsinya
dibedakan menjadi tiga macam yaitu :
a. Antioksidan primer
Berfungsi untuk mencegah terbentuknya radikal bebas baru.
yang ada dalam tubuh yang sangat terkenal adalah enzim
superoksida dismutase (SOD) yang dapat melindungi
b. Antioksidan sekunder
Berfungsi untuk menangkal radikal bebas serta mencegah
terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang
lebih besar, misalnya vitamin E, vitamin C, Cod Liver Oil,
Virgin Coconut Oil dan betakaroten.
c. Antioksidan tersier
Berfungsi untuk memperbaiki sel-sel dan jaringan yang rusak
karena serangan radikal bebas, yang termasuk dalam kelompok
ini adalah jenis enzim, misalnya metionin sulfoksida reduktase
yang dapat memperbaiki DNA pada penderita kanker.
2.9 Uji Aktivitas Antioksidan dengan Metode DPPH
Metode DPPH (2,2-difenil-1-pikrilhidrazil) digunakan secara luas
untuk menguji kemampuan senyawa yang berperan sebagai pendonor
elektron atau atom hidrogen. Metode DPPH merupakan metode yang
dapat mengukur aktivitas total antioksidan baik dalam pelarut polar
maupun nonpolar. Beberapa metode lain terbatas mengukur komponen
yang larut dalam pelarut yang digunakan dalam analisa. Metode DPPH
mengukur semua komponen antioksidan, baik yang larut dalam lemak
maupun dalam air (Prakash, 2001).
DPPH DPPH-H
(2,2-difenil-1-pikrilhidrazil) (2,2-difenil-1-pikrilhidrazin)
Gambar 2.2
Reduksi DPPH dari senyawa peredam radikal bebas
Metode DPPH (2,2-diefnil-1-pikrilhidrazil) merupakan metode
yang sederhana, mudah, cepat peka, serta hanya memerlukan sedikit
sampel. DPPH adalah senyawa radikal bebas stabil kelompok nitrit oksida.
Senyawa ini mempunyai ciri-ciri padatan berwarna ungu kehitaman, larut
dalam pelarut DMF atau etanol/metanol 394,3 g/mol, rumus molekul
C18H12N5O6 (Prakash, 2001).
Radikal bebas DPPH yang memiliki elektron tidak berpasangan
memberikan warna ungu dan menghasilkan absorbansi maksimum pada
panjang gelombang 517 nm. Warna akan berubah menjadi kuning saat
elektronnya berpasangan. Pengurangan intensitas warna yang terjadi
berhubungan dengan jumlah elektron DPPH yang menangkap atom
hidrogen. Sehingga pengurangan intensitas warna mengindikasikan
peningkatan kemampuan antioksidan untuk menangkap radikal bebas
(Prakash, 2001).
Aktivitas antioksidan dapat dinyatakan dengan satuan % aktivitas.
Nilai ini diperoleh dengan rumus sebagai berikut (Molyneux, 2004).
% Inhibisi =
x 100% Berdasarkan rumus tersebut, semakin tinggi tingkat diskolorisasi
(absorbansi semakin kecil) maka semakin tinggi nilai aktivitas
penangkapan radikal bebas (Molyneux, 2004).
Aktivitas antioksidan pada metode DPPH dinyatakan dengan
IC50 (Inhibition Concentration). IC50 adalah bilangan yang menunjukkan
konsentrasi ekstrak yang mampu menghambat aktivitas DPPH sebesar
50%. Semakin kecil nilai IC50 berarti semakin tinggi aktivitas antioksidan
(Blois, 1958).
AAI (Antioxidant Activity Index) adalah nilai yang menunjukkan
besarnya aktivitas antioksidan yang dimiliki suatu ekstrak atau bahan uji.
Nilai AAI dapat ditentukan dengan cara menghitung konsentrasi
DPPH yang digunakan dalam uji (ppm) dibagi dengan nilai IC50 yang
diperoleh (ppm). Penggolongan nilai AAI ini dilakukan oleh Scherer dan
Godoy (2009). Nilai AAI <0,5 menandakan antioksidan lemah,
antioksidan kuat, dan AAI >2 menandakan antioksidan yang sangat kuat
(Vasic, et al., 2011).
2.10 Spektrofotometer UV-Vis
Spektrum UV-Vis merupakan hasil interaksi antara radiasi
elektromagnetik (REM) dengan molekul. Radiasi elektromagnetik
merupakan bentuk energi radiasi yang mempunyai sifat gelombang dan
partikel (foton). Karena bersifat sebagai gelombang, maka ada
parameter-parameter yang perlu diketahui, antara lain panjang gelombang (λ), frekuensi (υ), bilangan gelombang (v), dan serapan (A). REM memiliki vektor listrik dan magnet yang bergetar dalam bidang yang
tegak lurus satu sama lain dan masing-masing tegak lurus pada arah
perambatan radiasi (Harmita, 2006).
Spektrofotometer dapat digunakan untuk mengukur besarnya
energi yang diabsorpsi atau diteruskan. Jika radiasi monokromatik
melewati larutan yang mengandung zat yang dapat menyerap, maka
radiasi ini akan dipantulkan, diabsorpsi oleh zatnya, dan sisanya akan
ditransmisikan. Lambert dan Beer telah menurunkan secara empiris
hubungan antara intensitas cahaya yang ditransmisikan dengan tebalnya
larutan dan hubungan antara intensitas dengan konsentrasi zat.
Hukum Lambert-Beer (Harmita, 2006):
Keterangan : A = serapan
Io = intensitas sinar yang dating
It = intensitas sinar yang diteruskan
= absorbtivitas molekuler (mol.cm.It-1)
a = daya serap (g.cm. It-1)
BAB 3
METODOLOGI PENELITIAN
3.1 Tempat dan Waktu
Penelitian ini dilakukan di Laboratorium Penelitian I dan
Laboratorium Farmakognosi dan Fitokimia Fakultas Kedokteran dan Ilmu
Kesehatan UIN Jakarta, Ciputat. Penelitian ini dilakukan pada bulan
April 2015 sampai dengan Desember 2015.
3.2 Alat dan Bahan 3.2.1 Alat
Blender (Philips), vacuum rotary evaporator (Eyela), pipet volum
(Iwaki Pyrex), mikropipet (Metler Toledo), batang pengaduk, gelas beker
(Pyrex), corong pisah (Iwaki), cawan penguap, kapas, timbangan digital
(GH-202), timbangan kasar (Wiggen Haser), vortex (Thermolyne),
pipa kapiler, chamber, tabung reaksi, spatula, gelas ukur (Pyrex),
labu ukur (Pyrex), Erlenmeyer, penangas air, lampu ultraviolet
(Parkin Elmer), dan spektrofotometer UV-Vis (Hitachi U-2900).
3.2.3 Bahan
Daun rambutan (Nephelium lappaceum Linn) yang diambil dari
taman Fakultas kedokteran dan Ilmu Kesehatan, UIN Syarif Hidayatullah
Jakarta, Etanol 70%, n-Heksana, etil asetat, aluminium foil, kertas saring,
plat KLT, asam klorida, reagen Mayer, reagen Dragendorff, asam sulfat
pekat, asam asetat anhidrat, NaOH, asam sulfat, asam klorida,
ammonia 30%, eter, FeCl3, natrium klorida, metanol p.a (Merck),
DPPH (2,2-diefnil-1-pikrilhidrazil) (Sigma Aldrich), kloroform, asam
3.3 Prosedur Penelitian 3.3.1 Pengambilan Bahan
Daun rambutan diambil dari taman Fakultas Kedokteran dan Ilmu
Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Selanjutnya daun dideterminasi di Lembaga Ilmu Penelitian Indonesia
(LIPI) Cibinong, Bogor.
3.3.2 Penyiapan Simplisia
Sampel daun rambutan (Nephelium lappaceum Linn) yang
diperoleh disortasi basah kemudian ditimbang. Sampel daun rambutan
selanjutnya dicuci bersih dengan air mengalir lalu dikeringkan pada
suhu ruangan dengan cara dikering-anginkan. Sampel daun rambutan
yang telah kering disortasi kering dan ditimbang kemudian
dihaluskan menggunakan blender hingga diperoleh serbuk daun rambutan
(Nephelium lappaceum Linn). Serbuk daun rambutan kemudian disimpan
dalam wadah yang bersih untuk dilakukan langkah selanjutnya.
3.3.3 Pembuatan Ekstrak Etanol
Serbuk simplisia daun rambutan (Nephelium lappaceum Linn)
dimaserasi dengan etanol 70% selama 2 sampai 3 hari dengan beberapa
kali pengadukan kemudian disaring. Maserasi dilakukan sampai filtrat
terakhir mendekati jernih. Filtrat yang terkumpul kemudian dipekatkan
dengan vacuum rotary evaporator pada suhu 45-500C hingga diperoleh
ekstrak kental etanol.
ammonia 30%. Dikocok kuat kemudian ditambahkan 20 mL kloroform
dan dikocok kembali dengan kuat (larutan A). Setengah larutan A
diperoleh larutan B. Larutan B dibagi dalam dua tabung reaksi,
ditambahkan masing masing pereaksi Dragendorff dan Mayer. Bila
terbentuk endapan merah bata dengan pereaksi Dragendorff dan
endapan putih dengan pereaksi Mayer menunjukkan adanya senyawa
alkaloid (Farnsworth, 1996).
b. Identifikasi Flavonoid
Sebanyak 0,5 gram ekstrak dilarutkan dengan 2 mL etanol 70%
dan ditambahkan 3 tetes larutan NaOH. Terjadinya perubahan
intensitas warna pada penambahan asam sulfat mengindikasikan
adanya senyawa flavonoid (Tiwari, et al., 2011).
c. Identifikasi Saponin
Sebanyak 0,5 gram ekstrak kental ditambahkan 2 mL
aquadest, kemudian dikocok selama 10 detik. Hasil positif
ditunjukkan dengan terbentuknya buih yang stabil selama tidak
kurang dari 10 menit (Tiwari, et al., 2011).
d. Identifikasi Triterpenoid dan Steroid
Sebanyak satu gram ekstrak kental dimasukkan dengan
20 mL eter selama dua jam (dalam wadah tertutup rapat). Disaring
dan diambil filtratnya. Kemudain 5 mL dari filtrat diuapkan dalam
cawan penguap hingga diperoleh residu atau sisa. Ke dalam residu
ditambahakan 2 tetes asam asetat anhidrat dan 2 tetes asam sulfat
pekat. Terbentuknya warna hijau atau merah menunjukkan adanya
senyawa golongan steroid dan triterpenoid (Farnsworth, 1996).
e. Tanin
Sebanyak 0,5 gram ekstrak kental diekstraksi dengan etanol.
Diuapkan sampai kering diatas penangas air. Selah kering dilarutkan
dengan 20 mL air panas dan didinginkan. Ditambahkan 10 tetes
natrium klorida 10% dan disaring. Larutan yang diperoleh
merupakan larutan percobaan. Pada larutan percoban ditambahkan
3 tetes FeCl3 1%. Bila terjadi perubahan warna biru hitam atau
hijau coklat menunjukkan adanya senyawa golongan tanin
3.3.5 Pemisahan secara Partisi Ekstrak Etanol Total (E1) Daun Rambutan (Nephelium lappaceum Linn) dengan Pelarut n-Heksana, Etil Asetat dan Etanol
Sebanyak 10 gram ekstrak etanol total (E1) daun rambutan
(Nephelium lappaceum Linn) dilarutkan dengan 100 mL etanol
kemudian dimasukkan ke dalam corong pisah. Ke dalam corong
tersebut kemudian dimasukann pelarut n-Heksana sebanyak 100 mL
untuk dilakukan proses pemisahan secara partisi. Corong pisah
tersebut kemudian dikocok dengan kuat sehingga tercampur dan
didiamkan hingga memisah menjadi dua fraksi, yaitu fraksi etanol dan
fraksi n-Heksana. Fraksi n-Heksana kemudian dikeluarkan dari corong
pisah sedangkan fraksi etanol dipartisi kembali dengan pelarut
n-Heksana. Partisi dengan pelarut n-Heksana dilakukan berulang kali
hingga fraksi n-Heksana mendekati berwarna bening. Fraksi etanol
selanjutnya dipartisi kembali menggunakan pelarut etil asetat sebanyak
100 mL lalu dikocok dengan kuat sehingga tercampur dan didiamkan
hingga memisah menjadi dua fraksi, yaitu fraksi etanol dan fraksi etil
asetat. Fraksi etil asetat kemudian dikeluarkan dari corong pisah
sedangkan fraksi etanol dipartisi kembali dengan etil asetat. Partisi
dengan pelarut etil asetat dilakukan berulang kali hingga fraksi etil
asetat mendekati berwarna bening. Dari proses partisi ini didapatkan
tiga fraksi yaitu fraksi n-Heksana, fraksi etil asetat dan fraksi air. Ketiga
fraksi ini masing-masing diuapkan dengan vacuum rotary evaporator
sampai didapatkan ekstrak kental fraksi n-Heksana (NH), fraksi
etil asetat (EA) dan fraksi etanol (E2). Masing-masing ekstrak kental
yang diperoleh diuji aktivitas antioksidannya dengan metode
3.3.6 Pengujian Antioksidan secara Kualitatif dengan Metode KromatografiLapis Tipis (KLT)
Ekstrak daun rambutan [ekstrak etanol total (E1), ekstrak fraksi
n-Heksana (NH), ekstrak fraksi etil asetat (EA), dan ekstrak fraksi
etanol (E2)] masing-masing ditimbang 50 mg dilarutkan dengan
etanol 50 mL (1000 ppm). Silika gel pada lempeng aluminium
digunakan sebagai fase diam. Setelah itu chamber yang berisi eluen
dijenuhkan (Ghasal dan Mandal, 2012).
Ekstrak daun rambutan (Nephelium lappaceum Linn) ditotolkan
pada plat KLT menggunakan pipa kapiler. Proses elusi dilakukan
dengan cara plat KLT dimasukkan ke dalam chamber yang berisi eluen
dan telah dijenuhkan. Eluen dibiarkan terelusi hingga mencapai batas
plat yang telah ditandai sebelumnya. Setelah selesai, plat KLT
dikeluarkan dari chamber, plat KLT kemudian dikeringkan dan
disemprot dengan larutan DPPH 0,1 mM (Ghasal dan Mandal, 2012).
Bercak pada plat KLT yang memiliki aktivitas antioksidan akan
berubah menjadi warna kuning dengan latar belakang ungu
(Kuntorini dan Astuti, 2010).
3.3.7 Pengujian Antioksidan secara Kuantitatif dengan Metode DPPH 3.3.7.1Pembuatan Larutan DPPH 0,1 mM
Sebanyak 1,98 mg DPPH (BM 394,32) dilarutkan dengan
metanol p.a dan dimasukkan kedalam labu ukur 50 mL. Volume
dicukupkan dengan metanol p.a hingga tanda batas, kemudian
ditempatkan dalam botol gelap (Molyneux, 2004)
3.3.7.2Penentuan Panjang Gelombang Serapan Maksimum DPPH
Sebanyak 2 mL larutan DPPH 0,1 mM dimasukkan ke dalam
tabung reaksi lalu ditambahkan metanol p.a sebanyak 2 mL, tutup
dengan aluminium foil, dihomogenkan dengan vortex lalu dituang ke
dalam kuvet dan diukur pada panjang gelombang 400-700 nm
3.3.7.3Pembuatan Larutan Blanko
Dipipet 2 mL larutan DPPH (0,1 mM) ke dalam tabung
reaksi dan ditambahkan metanol p.a sebanyak 2 mL. Tutup dengan
aluminium foil. Kemudian dihomogenkan dengan vortex dan diinkubasi
dalam ruangan gelap selama 30 menit (Molyneux, 2004). Serapan
larutan blanko diukur dengan spektrofometer UV-Vis pada panjang
gelombang maksimum.
3.3.7.4Pembuatan Larutan Pembanding Vitamin C a. Pembuatan larutan pembanding vitamin C
Sebanyak 50 mg serbuk vitamin C dilarutkan dengan metanol
p.a dan dimasukkan ke dalam labu ukur 50 mL sehingga diperoleh
larutan induk vitamin C dengan konsentrasi 1000 ppm. Kemudian
dari larutan induk dibuat seri konsentrasi 2 ppm, 4 ppm, 6 ppm,
8 ppm, dan 10 ppm.
b. Pengukuran serapan dengan menggunakan spekrofotometer UV-Vis
Masing-masing konsentrasi larutan pembanding vitamin C
sebanyak 2 mL dimasukkan kedalam tabung reaksi. Ditambahkan
larutan DPPH 0,1 mM sebanyak 2 mL, dihomogenkan dengan
vortex. Selanjutnya diinkubasi dalam ruangan gelap selama 30 menit
(Molyneux, 2004). Serapan diukur pada panjang gelombang
maksimum.
3.3.7.5 Pembuatan Larutan Uji Ekstrak Daun Rambutan a. Pembuatan larutan uji ekstrak daun rambutan
Ekstrak etanol daun rambutan etanol total (E1), ekstrak
fraksi n-Heksana (NH), ekstrak fraksi etil asetat (EA), dan ekstrak
fraksi etanol (E2) masing-masing ditimbang 50 mg, kemudian
dilarutkan dengan metanol p.a. Larutan dimasukkan ke dalam labu
ukur 50 mL. Volume dicukupkan dengan metanol p.a sampai
tanda batas (1000 ppm). Dari larutan induk dibuat seri konsentrasi
b. Pengukuran serapan dengan menggunakan spekrofotometer
UV-Vis
Masing-masing konsentrasi larutan uji sebanyak 2 mL
dimasukkan ke dalam tabung reaksi. Ditambahkan larutan DPPH
0,1 mM sebanyak 2 mL, dihomogenkan dengan vortex. Selanjutnya
diinkubasi dalam ruangan gelap selama 30 menit (Molyneux, 2004).
Lalu diukur absorbansinya pada panjang gelombang maksimum (λ maks) DPPH 0,1 mM.
3.3.8 Analisis Data
a. Penentuan Nilai IC50 (Inhibitory Concentration)
Parameter yang biasa digunakan untuk menginterpretasikan
hasil dari uji aktivitas antioksidan dengan metode DPPH adalah
dengan nilai efficient concentration (EC50) atau sering disebut nilai
IC50, yaitu konsentrasi yang menyebabkan hilangnya 50% aktivitas
DPPH (Molyneux, 2004). Untuk menghitung nilai IC50 diperlukan
data persen inhibisi dari pengujian yang dilakukan. Persen inhibisi
dapat dihitung dengan menggunakan rumus sebagai berikut:
% inhibisi =
x 100% (Ghosal dan Mandal, 2012)
Konsentrasi sampel dan persen inhibisi yang diperoleh diplot
masing-masing pada sumbu x dan y pada persamaan regresi linear.
Persamaan tersebut digunakan untuk menentukan nilai IC50 dari
masing-masing sampel dinyatakan dengan nilai y sebesar 50 dan
nilai x yang akan diperoleh sebagai IC50 (Nurjanah, et al., 2011).
b. Penentuan nilai AAI (Antioxidant Activity Index)
Nilai AAI dapat ditentukan dengan cara konsentrasi
DPPH yang digunakan dalam uji (ppm) dibagi dengan nilai
aktivitas antioksidan lemah, AAI >0,5-1 menandakan aktivitas
antioksidan sedang, AAI >1-2 menandakan aktivitas antioksidan
kuat, dan AAI >2 menandakan aktivitas antioksidan sangat kuat
BAB 4
HASIL DAN PEMBAHASAN
4.1 Determinasi Tanaman
Determinasi tanaman terlebih dahulu dilakukan untuk
mengetahui identitas tanaman yang digunakan. Determinasi tanaman ini
dilakukan di Herbarium Bogoriense, Pusat Penelitian Biologi LIPI
(Lembaga Ilmu Pengetahuan Indonesia) Cibinong, Bogor. Hasil
determinasi menunjukkan bahwa sampel yang digunakan merupakan
Nephelium lappaceum Linn dari famili Sapindaceae (lampiran 2).
4.2 Penyiapan Sampel
Sampel yang digunakan pada penelitian ini adalah daun rambutan
(Nephelium lappaceum Linn) yang diambil dari taman Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
Daun yang diambil merupakan daun muda dan daun tua. Pengambilan
daun dilakukan pada bulan Januari 2015.
Sebanyak 2 kg daun rambutan yang telah di sortasi basah dicuci
dengan air bersih. Sortasi basah dilakukan untuk memisahkan pengotor
dan bagian tanaman yang tidak digunakan dalam penelitian dan
terbawa pada saat proses pengambilan daun rambutan. Pencucian daun
rambutan menggunkan air mengalir untuk membersihkan kotoran yang
menempel pada daun. Daun yang telah dicuci kemudian dikeringkan
selama 6 hari sehingga didapatkan sampel kering daun rambutan
(Nephelium lappaceum Linn) dengan bobot 618 gram. Pengeringan
dilakukan dengan cara dikering-anginkan pada suhu ruangan. Pengeringan
dilakukan untuk menghentikan reaksi enzimatik yang dapat menyebabkan
penguraian atau perubahan kandungan kimia yang terdapat pada daun.
Selain itu, pengeringan dilakukan di tempat yang terlindung dari cahaya
matahari langsung. Hal ini dilakukan untuk menghindari kemungkinan
terjadinya kerusakan pada kandungan kimia daun akibat pemanasan. Daun
pengotor-pengotor yang masih terbawa pada saat proses pengeringan.
Daun yang telah disortasi kering kemudian dihaluskan dengan blender
hingga diperoleh serbuk simplisia kering dengan bobot 600 gram.
4.3 Ekstraksi
Proses ekstraksi daun rambutan dilakukan dengan metode
maserasi. Maserasi langsung dilakukan dengan mengekstraksi langsung
simplisia daun rambutan dengan etanol 70%. Maserasi dipilih karena
proses pengerjaan yang mudah dan peralatan yang cukup sederhana. Pada
maserasi ini, digunakan simplisia sebanyak 600 gram. Proses maserasi
dilakukan selama 2 sampai 3 hari. Prosedur diulangi hingga 15 kali proses
maserasi. Total pelarut etanol yang digunakan sebanyak 12 L yang
sebelumnya telah didestilasi terlebih dahulu. Filtrat hasil maserasi disaring
dengan kapas dan kertas saring yang kemudian dipekatkan dengan
vacuum rotary evaporator pada suhu 45-500C hingga diperoleh ekstrak
kental sebanyak 110 gram dengan rendemen 18,33%.
Tabel 4.1 Hasil ekstraksi daun rambutan Bobot
Prinsip maserasi adalah pelarut yang digunakan dalam proses
maserasi akan masuk ke dalam sel tanaman melewati dinding sel, isi sel
akan larut karena adanya perbedaan konsentrasi antara larutan didalam
dengan di luar sel melalui proses difusi hingga terjadi keseimbangan
antara larutan di dalam sel dan larutan di luar sel (Ansel, 1989). Maserasi
merupakan metode ekstraksi dingin yang banyak digunakan dan paling
sederhana diantara metode lain, yaitu hanya dengan merendam sampel
dalam pelarut yang sesuai. Sampel dibuat dalam serbuk dengan tujuan
memperluas permukaan bidang sentuh antara etanol dan serbuk simplisia,
dengan demikian penyarian dapat lebih efektif. Pada saat maserasi,
sel, sehingga isi sel termasuk zat aktifnya akan keluar dan terlarut dalam
pelarut (Anonim, 1993 dalam Yulianty, 2011).
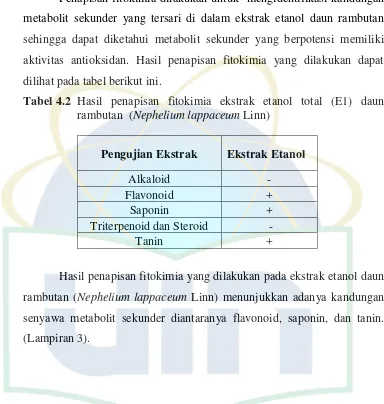
4.4 Penapisan Fitokimia Ekstrak Etanol Total (E1) Daun Rambutan Penapisan fitokimia dilakukan untuk mengidentifikasi kandungan
metabolit sekunder yang tersari di dalam ekstrak etanol daun rambutan
sehingga dapat diketahui metabolit sekunder yang berpotensi memiliki
aktivitas antioksidan. Hasil penapisan fitokimia yang dilakukan dapat
dilihat pada tabel berikut ini.
Tabel 4.2 Hasil penapisan fitokimia ekstrak etanol total (E1) daun rambutan (Nephelium lappaceum Linn)
Pengujian Ekstrak Ekstrak Etanol
Alkaloid -
Flavonoid +
Saponin +
Triterpenoid dan Steroid -
Tanin +
Hasil penapisan fitokimia yang dilakukan pada ekstrak etanol daun
rambutan (Nephelium lappaceum Linn) menunjukkan adanya kandungan
senyawa metabolit sekunder diantaranya flavonoid, saponin, dan tanin.
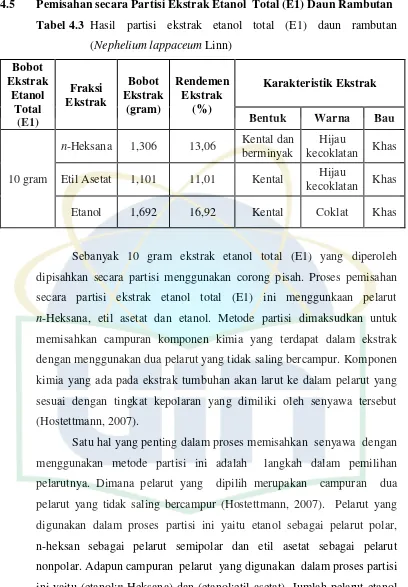
4.5 Pemisahan secara Partisi Ekstrak Etanol Total (E1) Daun Rambutan
dipisahkan secara partisi menggunakan corong pisah. Proses pemisahan
secara partisi ekstrak etanol total (E1) ini menggunkaan pelarut
n-Heksana, etil asetat dan etanol. Metode partisi dimaksudkan untuk
memisahkan campuran komponen kimia yang terdapat dalam ekstrak
dengan menggunakan dua pelarut yang tidak saling bercampur. Komponen
kimia yang ada pada ekstrak tumbuhan akan larut ke dalam pelarut yang
sesuai dengan tingkat kepolaran yang dimiliki oleh senyawa tersebut
(Hostettmann, 2007).
Satu hal yang penting dalam proses memisahkan senyawa dengan
menggunakan metode partisi ini adalah langkah dalam pemilihan
pelarutnya. Dimana pelarut yang dipilih merupakan campuran dua
pelarut yang tidak saling bercampur (Hostettmann, 2007). Pelarut yang
digunakan dalam proses partisi ini yaitu etanol sebagai pelarut polar,
n-heksan sebagai pelarut semipolar dan etil asetat sebagai pelarut
nonpolar. Adapun campuran pelarut yang digunakan dalam proses partisi
ini yaitu (etanol:n-Heksana) dan (etanol:etil asetat). Jumlah pelarut etanol
yang digunakan pada proses partisi ini yaitu etanol 100 mL, n-Heksana
4.4 Uji Aktivitas Antioksidan secara Kualitatif
Tabel 4.4 Hasil uji aktivitas antioksidan secara kualitatif Eluen n-Heksana : Etil Asetat (3:7)
Sinar Biasa Sinar UV366 Sinar UV254 Sebelum disemprot DPPH
Sinar Biasa Sinar UV366 Sinar UV254 Setelah disemprot DPPH
Pengujian kualitatif antioksidan ekstrak daun rambutan dilakukan
dengan metode kromatografi lapis tipis (KLT). Uji antiksidan secara
kualitatif ini dilakukan untuk mengetahui ada atau tidaknya aktivitas
antioksidan dari ekstrak daun rambutan (Nephelium lappaceum Linn).
Ekstrak daun rambutan [Ekstrak etanol total (E1), fraksi n-Heksana (NH),
fraksi etil asetat (EA), dan fraksi etanol (E2) dengan konsentrasi
1000 ppm ditotolkan pada plat KLT kemudian dielusi dengan eluen
n-Heksana:etil asetat (3:7) dan disemprot dengan larutan DPPH kemudian
diiamkan selama 30 menit. Berdasarkan hasil uji antioksidan secara
kualitatif dapat diketahui bahwa ekstrak ekstrak etanol (E1), fraksi
n-Heksana (NH), ekstrak fraksi etil asetat (EA), dan ekstrak fraksi
etanol (E2) memiliki aktivitas antioksidan karena pada keempat ekstrak ini
terlihat bercak berwarna kuning dengan latar belakang ungu. E1 NH EA E2
E1 NH EA E2
E1 NH EA E2
E1 NH EA E2
E1 NH EA E2
4.7 Uji Aktivitas Antioksidan secara Kuantitatif
Uji aktivitas antioksidan ekstrak daun rambutan
(Nephelium lappaceum Linn) dilakukan dengan menggunakan metode
penangkapan radikal bebas DPPH (2,2-difenil-1-pikrilhidrazil). Metode
DPPH dipilih karena merupakan metode sederhana, mudah, cepat dan
peka serta hanya memerlukan sedikit sampel untuk mengevaluasi aktivitas
antioksidan dari senyawa bahan alam (Molyneux, 2004).
Prinsip pengukuran aktivitas antioksidan secara kuantitatif
menggunakan metode DPPH ini adalah adanya perubahan intensitas warna
ungu DPPH yang sebanding dengan konsentrasi larutan DPPH tersebut.
Radikal bebas DPPH yang memiliki elektron tidak berpasangan akan
memberikan warna ungu. Warna akan berubah menjadi kuning saat
elektronnya berpasangan. Perubahan intensitas warna ungu ini terjadi
karena adanya peredaman radikal bebas yang dihasilkan oleh bereaksinya
molekul DPPH dengan atom hidrogen yang dilepaskan oleh molekul
senyawa sampel sehingga terbentuk senyawa difenil pikrilhidrazin
dan menyebabkan terjadinya peluruhan warna DPPH dari ungu menjadi
kuning. Perubahan warna ini akan memberikan perubahan absorbansi
pada panjang gelombang maksimum DPPH menggunakan
spektrofotometer UV-Vis sehingga akan diketahui nilai aktivitas
peredaman radikal bebas yang dinyatakan dengan nilai IC50
(Inhibitory Concentration) (Molyneux, 2004).
Nilai IC50 didefinisikan sebagai besarnya konsentrasi senyawa uji
yang dapat meredam radikal bebas sebanyak 50%. Semakin kecil nilai IC50
maka aktivitas peredaman radikal bebas semakin tinggi (Molyneux, 2004).
AAI (Antioxidant Activity Index) adalah nilai yang menunjukkan besarnya
aktivitas antioksidan yang dimiliki suatu ekstrak atau bahan uji. Nilai AAI
(Antioxidant Activity Index) ditentukan untuk menggolongkan sifat
antioksidan ekstrak sebagaimana yang dilakukan oleh Scherer dan
Godoy (2009). Nilai AAI diperoleh dengan membandingkan konsentrasi
Pengujian aktivitas antioksidan secara kuantitatif ekstrak ekstrak
etanol total (E1), ekstrak fraksi n-Heksana (NH), ekstrak fraksi etil asetat
(EA), ekstrak fraksi etanol (E2), beserta kontrol positif vitamin C
dilakukan dengan berbagai seri konsentrasi menggunakan metode DPPH
yang selanjutnya absorbansinya diukur menggunakan spektrofotometer
UV-Vis.
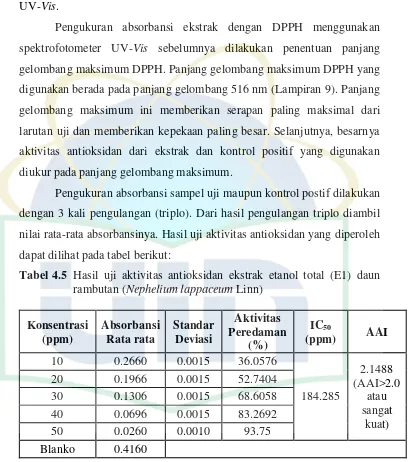
Pengukuran absorbansi ekstrak dengan DPPH menggunakan
spektrofotometer UV-Vis sebelumnya dilakukan penentuan panjang
gelombang maksimum DPPH. Panjang gelombang maksimum DPPH yang
digunakan berada pada panjang gelombang 516 nm (Lampiran 9). Panjang
gelombang maksimum ini memberikan serapan paling maksimal dari
larutan uji dan memberikan kepekaan paling besar. Selanjutnya, besarnya
aktivitas antioksidan dari ekstrak dan kontrol positif yang digunakan
diukur pada panjang gelombang maksimum.
Pengukuran absorbansi sampel uji maupun kontrol postif dilakukan
dengan 3 kali pengulangan (triplo). Dari hasil pengulangan triplo diambil
nilai rata-rata absorbansinya. Hasil uji aktivitas antioksidan yang diperoleh
dapat dilihat pada tabel berikut:
Tabel 4.5 Hasil uji aktivitas antioksidan ekstrak etanol total (E1) daun rambutan (Nephelium lappaceum Linn)
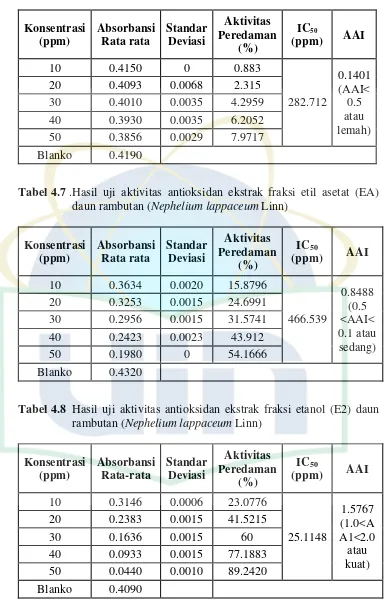
Tabel 4.6 Hasil uji aktivitas antioksidan ekstrak fraksi n-Heksana (NH) daun rambutan (Nephelium lappaceum Linn)
Konsentrasi daun rambutan (Nephelium lappaceum Linn)
Konsentrasi rambutan (Nephelium lappaceum Linn)
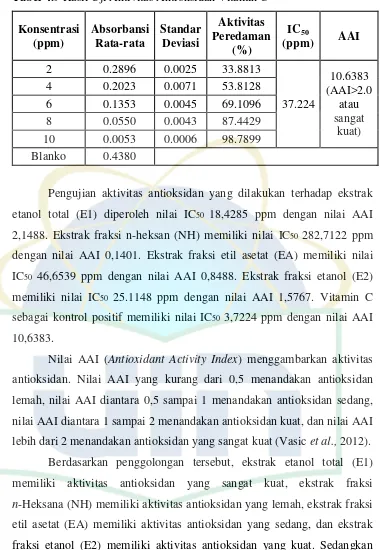
Tabel 4.9 Hasil Uji Aktivitas Antioksidan Vitamin C
Pengujian aktivitas antioksidan yang dilakukan terhadap ekstrak
etanol total (E1) diperoleh nilai IC50 18,4285 ppm dengan nilai AAI
Nilai AAI (Antioxidant Activity Index) menggambarkan aktivitas
antioksidan. Nilai AAI yang kurang dari 0,5 menandakan antioksidan
lemah, nilai AAI diantara 0,5 sampai 1 menandakan antioksidan sedang,
nilai AAI diantara 1 sampai 2 menandakan antioksidan kuat, dan nilai AAI
lebih dari 2 menandakan antioksidan yang sangat kuat (Vasic et al., 2012).
Berdasarkan penggolongan tersebut, ekstrak etanol total (E1)
memiliki aktivitas antioksidan yang sangat kuat, ekstrak fraksi
n-Heksana (NH) memiliki aktivitas antioksidan yang lemah, ekstrak fraksi
etil asetat (EA) memiliki aktivitas antioksidan yang sedang, dan ekstrak
fraksi etanol (E2) memiliki aktivitas antioksidan yang kuat. Sedangkan
vitamin C sebagai kontrol positif memiliki aktivitas antioksidan yang
sangat kuat.
Vitamin C merupakan antikosidan yang bekerja sebagai oxygen
scavengers, yaitu mengikat oksigen sehingga tidak mendukung reaksi
oksigen yang berada dalam sistem sehingga jumlah oksigen
akan berkurang. Selain vitamin C, senyawa yang bekerja sebagai
oxygen scavengers diantaranya askorbil palminat, asam eritorbat, dan
sulfit (Gordon, 1990).
Peningkatan konsentrasi senyawa mempengaruhi aktivitas
antioksidannya. Kurva hubungan konsentrasi ekstrak terhadap persen
inhibisi sebagai persen penghambatan radikal bebas DPPH dari
ekstrak etanol total (E1), ekstrak fraksi n-Heksana (NH), ekstrak fraksi
etil asetat (EA), ekstrak fraksi etanol (E2), dan kontrol positif vitamin C
dapat dilihat pada gambar berikut:
Gambar 4.1. Kurva hubungan konsentrasi dan % inhibisi ekstrak etanol total (E1) daun rambutan (Nephelium lappaceum Linn)
Gambar 4.2. Kurva hubungan konsentrasi dan % inhibisi Inhibisi Ekstrak Etanol Total (E1)
Gambar 4.1. Kurva hubungan konsentrasi dan % inhibisi
Gambar 4.5. Kurva hubungan konsentrasi dan % inhibisi vitamin C y = 0.9579x + 5.3102
Inhibisi Fraksi Etanol (E1)