PENETAPAN POTENSI NEOMISIN SULFAT DALAM KRIM
BETASON-N SECARA MIKROBIOLOGI
TUGAS AKHIR
OLEH :
NURUL FAHMI
NIM 122410123
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ii
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan rahmat dan karunia-Nya yang telah memberikan pengetahuan, kekuatan, kesehatan dan kesempatan kepada penulis sehingga penulis dapat menyelesaikan tugas akhir ini, serta sholawat beriring salam untuk Rasulullah Nabi Muhammad SAW sebagai contoh tauladan dalam kehidupan. Tugas akhir ini berjudul ”PENETAPAN POTENSI NEOMISIN SULFAT DALAM KRIM BETASON-N SECARA MIKROBIOLOGI”. Tugas akhir ini disusun untuk memenuhi salah satu syarat untuk menyelesaikan Program Diploma III Analis Farmasi Dan Makanan di Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak, penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya, untuk itu penulis mengucapkan terima kasih yang sebesar–besarnya kepada berbagai pihak antara lain:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., sebagai Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai Kordinator Program Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara.
iii
5. Bapak Dr. Kasmirul Ramlan Sinaga, MS., Apt., sebagai Dosen Pembimbing Tugas Akhir yang telah membimbing penulis dalam menyusun tugas akhir ini. 6. Bapak Beben Budiman, Apt., selaku Plant Manager PT. Kimia Farma
(Persero) Tbk. Plant Medan beserta stafnya.
7. Bapak Yogi Sugianto, S.Farm., Apt., sebagai Pembimbing Lapangan di Industri Farmasi PT. Kimia Farma (Persero) Tbk. Plant Medan.
8. Bapak, Ibu dosen staf pengajar Fakultas Farmasi Universitas Sumatera Utara. 9. Pihak-pihak lainnya yang tidak dapat disebutkan namanya satu-persatu.
Penulis ingin menyampaikan penghargaan yang sebesar-besarnya kepada kedua orang tua penulis yaitu Ayahanda Selamat, Ibunda Siti Fatimah, Abangda M. Fadlan, Abangda M. Fajar, Kakanda Lia yang telah memberikan dukungan dan segenap doa kepada penulis sehingga dapat menyelesaikan tugas akhir ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan maupun penyajian tugas akhir ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima saran dan keritik yang sifatnya membangun demi kesempurnaan tugas akhir ini. Akhir kata semoga Allah SWT melimpahkan rahmat dan karunia-Nya kepada kita semua dan semoga tugas akhir ini dapat bermanfaat bagi kita semua. Aamiin.
Medan, Mei 2015 Penulis,
iv
PENETAPAN POTENSI NEOMISIN SULFAT DALAM KRIM
BETASON-N SECARA MIKROBIOLOGI
ABSTRAK
Betason-N krim merupakan salah satu sediaan farmasi berbentuk krim yang sering digunakan untuk mengobati penyakit kulit. Tiap gram krim mengandung Betametason valerat dan Neomisin sulfat. Betametason adalah suatu 9-fluorokortikosteroid yang paling efektif untuk obat kulit, sedangkan neomisin dikenal sebagai suatu antibiotik yang aktif terhadap sejumlah besar bakteri yang umumnya menyertai radang kulit. Tujuan pemeriksaan ini adalah untuk mengetahui apakah potensi Neomisin sulfat dalam krim Betason-N yang di produksi PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi persyaratan Farmakope Indonesia Edisi IV Tahun 1995, sehingga dengan potensi yang tepat dapat memberikan efek terapi yang diinginkan.
Penetapan potensi Neomisin sulfat dalam Betason-N krim dilakukan secara mikrobiologi menggunakan metode lempeng silinder. Metode ini berdasarkan difusi antibiotik dari silinder yang dipasang tegak lurus pada lapisan agar padat dalam cawan petri atau lempeng, sehingga mikroba yang ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” di sekeliling silinder yang berisi larutan antibiotik. Media yang digunakan adalah media antibiotik no.1 dan menggunakan bakteri Staphylococcus epidermidis.
Hasil yang diperoleh menunjukkan bahwa potensi Neomisin sulfat dalam Betason-N krim dengan no. betsB50187 T produksi PT. Kimia Farma (Persero) Tbk. Plant Medan sebesar 745.91 mcg/mg massa. Farmakope Indonesia Edisi IV Tahun 1995 memberi persyaratan potensi Neomisin sulfat setara dengan tidak kurang dari 600 mcg neomisin per mg. Sehingga hasil penetapan potensi yang dilakukan memenuhi persyaratan.
v
THE POTENTIAL DETERMINATION OF NEOMYCIN
SULFATE IN BETASON-N CREAM BY MICROBIOLOGY
ABSTRACT
Betason-N cream is one of pharmaceutical preparation shaped of a cream that is often used to treat skin diseases. One grams of cream contains Bethametason valerate and Neomycin sulfate. Bethametason is a 9-fluorokortikosteroid the most effective drug for the skin, while the neomycin is known as an antibiotic that is active against a large number of bacteria that commonly accompany skin inflammation. The purpose of this examination is to determine whether the potential of Neomisin sulfate in cream Betason-N production of PT. Kimia Farma (Persero) Tbk. Plant Medan meet the requirements Indonesian Pharmacopeia 4th edition 1995, so with the right potential can provide the desire therapeutic effect.
Potency determination of Neomycin sulfate in Betason-N cream by microbiology using cylindrical plate method. This method is based on antibiotics diffusion of cylinders mounted perpendicular to the layers so solid in petri dish or plate, so that inhibited growth of microbes are added to the area of a circle or zone around the cylinder containing the antibiotics solution. The medium using is antibiotic medium no.1 and using the bacteria Staphylococcus epidermidis.
The results obtained show that the potency of Neomisin sulfate in Betason-N cream with batch number B50187 T production of PT. Kimia Farma (Persero) Tbk. Plant Medan of 745.91 mcg/mg masses. Indonesian Pharmacopoeia 4thedition 1995 gives the requirements potential of Neomycin sulfate equivalent not less than 600 mcg/mg. So that the result of the potential determination that do meet the requirements.
vi DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujuan dan Manfaat ... 2
1.2.1. Tujuan ... 2
1.2.2. Manfaat ... 2
BAB II TINJAUAN PUSTAKA ... 4
2.1. Obat Kulit ... 4
2.2. Krim ... 5
2.2.1. Betason-N krim ... 7
2.2.2. Betametason valerat ... 8
vii
kimianya ... 10
2.3.2. Penggolongan antibiotik berdasarkan spektrum atau kisaran kerja ... 11
2.3.3. Penggolongan antibiotik berdasarkan mekanisme kerjanya ... 11
2.3.4. Bahaya pemakaian antibiotik ... 12
2.3.5. Resistensi ... 13
2.3.6. Neomisin sulfat ... 14
2.4. Metode Pengujian ... 16
2.5. Medium Biakan Mikroba ... 18
2.6. Bakteri ... 19
BAB III METODOLOGI PENGUJIAN ... 22
3.1. Tempat Pelaksanaan Penetapan Potensi ... 22
3.2. Alat-alat ... 22
3.3. Bahan ... 22
3.4. Prosedur Kerja ... 22
3.4.1. Pembuatan media uji ... 22
3.4.2. Pembuatan larutan dapar fosfat III ... 23
3.4.3. Pembuatan larutan pembanding kerja ... 23
3.4.4. Pembuatan larutan uji ... 24
3.4.5. Penandaan cawan petri ... 24
3.4.6. Pembuatan inokulum ... 24
viii
3.4.8. Penetapan potensi ... 25
3.5. Perhitumgan Potensi ... 25
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1. Hasil ... 27
4.2. Pembahasan ... 28
BAB V KESIMPULAN DAN SARAN ... 30
5.1. Kesimpulan ... 30
5.2 Saran ... 30
DAFTAR PUSTAKA ... 31
ix
DAFTAR TABEL
Halaman Tabel 4.1. Hasil pengamatan penetapan potensi Neomisin sulfat dalam
krim Betason-N produksi PT. Kimia Farma (Persero) Tbk.
Plant Medan ... 27
Tabel 4.2. Hasil pengolahan data dari penentuan garis tengah hambat
x
DAFTAR GAMBAR
Halaman
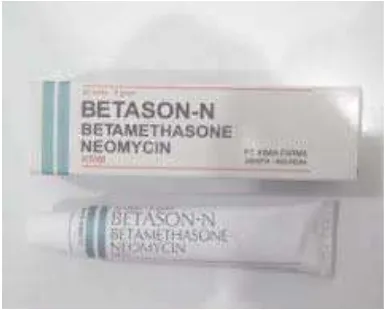
Gambar 2.1. Betason-N krim ... 7
Gambar 2.2. Struktur kimia Betametason valerat ... 8
Gambar 2.3. Struktur kimia Neomisin sulfat ... 14
Gambar 2.4. Staphylococcus epidermidis ... 20
xi
DAFTAR LAMPIRAN
Halaman Lampiran 1. Hasil perhitungan potensi antibiotik ... 33 Lampiran 2. Perhitungan penetapan potensi Neomisin sulfat dalam
krim Betason-N ... 34
iv
PENETAPAN POTENSI NEOMISIN SULFAT DALAM KRIM
BETASON-N SECARA MIKROBIOLOGI
ABSTRAK
Betason-N krim merupakan salah satu sediaan farmasi berbentuk krim yang sering digunakan untuk mengobati penyakit kulit. Tiap gram krim mengandung Betametason valerat dan Neomisin sulfat. Betametason adalah suatu 9-fluorokortikosteroid yang paling efektif untuk obat kulit, sedangkan neomisin dikenal sebagai suatu antibiotik yang aktif terhadap sejumlah besar bakteri yang umumnya menyertai radang kulit. Tujuan pemeriksaan ini adalah untuk mengetahui apakah potensi Neomisin sulfat dalam krim Betason-N yang di produksi PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi persyaratan Farmakope Indonesia Edisi IV Tahun 1995, sehingga dengan potensi yang tepat dapat memberikan efek terapi yang diinginkan.
Penetapan potensi Neomisin sulfat dalam Betason-N krim dilakukan secara mikrobiologi menggunakan metode lempeng silinder. Metode ini berdasarkan difusi antibiotik dari silinder yang dipasang tegak lurus pada lapisan agar padat dalam cawan petri atau lempeng, sehingga mikroba yang ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” di sekeliling silinder yang berisi larutan antibiotik. Media yang digunakan adalah media antibiotik no.1 dan menggunakan bakteri Staphylococcus epidermidis.
Hasil yang diperoleh menunjukkan bahwa potensi Neomisin sulfat dalam Betason-N krim dengan no. betsB50187 T produksi PT. Kimia Farma (Persero) Tbk. Plant Medan sebesar 745.91 mcg/mg massa. Farmakope Indonesia Edisi IV Tahun 1995 memberi persyaratan potensi Neomisin sulfat setara dengan tidak kurang dari 600 mcg neomisin per mg. Sehingga hasil penetapan potensi yang dilakukan memenuhi persyaratan.
v
THE POTENTIAL DETERMINATION OF NEOMYCIN
SULFATE IN BETASON-N CREAM BY MICROBIOLOGY
ABSTRACT
Betason-N cream is one of pharmaceutical preparation shaped of a cream that is often used to treat skin diseases. One grams of cream contains Bethametason valerate and Neomycin sulfate. Bethametason is a 9-fluorokortikosteroid the most effective drug for the skin, while the neomycin is known as an antibiotic that is active against a large number of bacteria that commonly accompany skin inflammation. The purpose of this examination is to determine whether the potential of Neomisin sulfate in cream Betason-N production of PT. Kimia Farma (Persero) Tbk. Plant Medan meet the requirements Indonesian Pharmacopeia 4th edition 1995, so with the right potential can provide the desire therapeutic effect.
Potency determination of Neomycin sulfate in Betason-N cream by microbiology using cylindrical plate method. This method is based on antibiotics diffusion of cylinders mounted perpendicular to the layers so solid in petri dish or plate, so that inhibited growth of microbes are added to the area of a circle or zone around the cylinder containing the antibiotics solution. The medium using is antibiotic medium no.1 and using the bacteria Staphylococcus epidermidis.
The results obtained show that the potency of Neomisin sulfate in Betason-N cream with batch number B50187 T production of PT. Kimia Farma (Persero) Tbk. Plant Medan of 745.91 mcg/mg masses. Indonesian Pharmacopoeia 4thedition 1995 gives the requirements potential of Neomycin sulfate equivalent not less than 600 mcg/mg. So that the result of the potential determination that do meet the requirements.
1 BAB I PENDAHULUAN
1.1Latar Belakang
Kulit adalah lapisan tubuh yang paling luar dan paling sensitif terhadap berbagai macam benda asing yang dating dari luar dan dapat menyebabkan penyakit. Penyakit kulit biasa disebabkan oleh banyak faktor, diantaranya faktor lingkungan dan pola tingkah laku sehari-hari (Faulkner, 2008). Penyakit kulit sangat beragam dikalangan masyarakat, seringkali sulit membedakan penyakit kulit yang satu dengan penyakit kulit yang lain. Penyakit kulit merupakan kelainan yang diakibatkan oleh adanya infeksi bakteri, jamur, kuman-kuman, parasit maupun virus (Widodo, 2004).
Bentuk sediaan farmasi yang dipakai untuk kulit adalah salep, krim, pasta dengan basis bermacam-macam, baik yang hidrofil atau hidrofob. Sediaan-sediaan tersebut digunakan pada kulit untuk memberikan aksi lokal dan aksinya dapat berlangsunglama padatempat yang sakit dan sedikit mungkin diabsorbsi (Anief, 2007).
2
Salah satu krim yang mengandung antibiotik dan beredar di pasaran adalah Betason-N krim produksi PT. Kimia Farma (Persero) Tbk. Plant Medan. Sebelum krim tersebut dipasarkan terlebih dahulu dilakukan serangkaian pengujian, salah satunya adalah uji potensi terhadap antibiotik yang terdapat dalam krim tersebut, hal ini bertujuan untuk melindungi masyarakat dari penggunaan obat yang tidak memenuhi mutu dan efek terapi yang tidak baik, sehingga penulis tertarik untuk mengambil tugas akhir dengan judul “PENETAPAN POTENSI NEOMISIN SULFAT DALAM KRIM BETASON-N SECARA MIKROBIOLOGI”.
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
Adapun tujuan dari penetapan potensi Neomisin sulfat dalam krim Betason-N secara mikrobiologi adalah untuk mengetahui:
• Metode yang digunakan dalam penetapan potensi Neomisin sulfat
cocok untuk krim Betason-N produksi PT. Kimia Farma (Persero) Tbk. Plant Medan.
• Potensi Neomisin sulfat dalam krim Betason-N yang di produksi oleh
PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi syarat Farmakope Indonesia Edisi IV Tahun 1995.
1.2.2 Manfaat
3
4 BAB II
TINJAUAN PUSTAKA
2.1 Obat Kulit
Penyakit kulit dikenal bermacam-macam, seperti kudis, eksema, kutu air, biang keringat, koreng dan sebagainya. Untuk mengobati penyakit-penyakit kulit tersebut digunakan bahan-bahan yang sifatnya mampu melindungi kulit yang luka, mampu menghaluskan dan melemaskan kulit, mengurangi rasa gatal dan mempunyai kerja khusus serta bersifat antiseptika (Widjajanti, 1988).
Sediaan farmasi yang digunakan pada kulit adalah untuk memberikan aksi lokal, berlangsung lama pada tempat yang sakit dan sedikit mungkin diabsorpsi. Oleh karena itu sediaan pada kulit biasanya digunakan sebagai antiseptik, antifungi, antiinflamasi, anestetik lokal, emolien, pelindung terhadap sinar matahari, udara dan iritasi zat kimia. Biasanya bentuk sediaannya berupa salep, krim dan pasta, sedangkan sediaan lain yang juga digunakan adalah berupa serbuk tabur, aerosol, larutan dan losio (Anief, 2007).
Contoh obat-obatan yang sering digunakan pada pengobatan penyakit kulit:
1. Obat antibakteri dan germisida, seperti fenol, kresol, timol alkohol dan lain-lain.
2. Antibiotik topikal, terdiri dari Penisilin, Neomisin, Framisetin, Gramisidin, Gentamisin, Polimixin B, Tetrasiklin HCl, Eritromisin dan lainnya.
5 2.2Krim
Krim adalah bentuk sediaan setengah padat mengandung satu atau lebih bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai (Depkes RI, 1995). Sediaan ini memiliki konsistensi relatif cair yang diformulasikan sebagai air dalam minyak (A/M) atau minyak dalam air (M/A).Krim dapat disimpan dalam wadah tertutup dan diletakkan ditempat sejuk (Jas, 2004).
Krim merupakan obat yang digunakan sebagai obat luar yang dioleskan ke bagian kulit badan. Yang dimaksud dengan “obat luar” adalah obat yang pemakaiannya tidak melalui mulut, kerongkongan dan ke arah lambung. Menurut definisi tersebut yang termasuk obat luar adalah obat luka, obat kulit (salep, krim, jelly, serbuk tabur), obat hidung, obat mata, obat tetes telinga dan sebagainya (Widjajanti, 1988). Secara umum obat-obat luar memiliki keamanan yang lebih baik karena hanya digunakan secara lokal pada lokasi tertentu diluar tubuh. Efek samping yang mungkin terjadi adalah iritasi kulit, atau kadang-kadang rasa terbakar (Widodo, 2004).
Sebagai obat luar, krim harus memenuhi beberapa persyaratan berikut: a. Stabil selama masih dipakai untuk mengobati. Oleh karena itu krim harus
stabil pada suhu kamar.
b. Lunak. Semua zat dalam keadaan halus, lunak serta homogen.
c. Mudah dipakai. Umumnya, krim tipe emulsi adalah yang paling mudah dipakai dan dihilangkan dari kulit.
6 Basis krim
Seperti salep, krim juga mengandung basis atau bahan dasar tertentu. Ada beberapa bahan dasar yang sering digunakan dalam pembuatan krim, diantaranya sebagai berikut:
a. Fase minyak
b.
, yaitu bahan obat yang larut dalam minyak dan bersifat asam. Contohnya asam stearat, adeps lanae, paraffin liquidum, stearil alkohol dan sebagainya.
Fase air
c.
, yaitu bahan obat yang larut dalam air dan bersifat basa. Contohnya, Na tetraborat, Trietanolamin/TEA, NaOH, KOH, Gliserin, Polietilenglikol/PEG, propilen glikol, surfaktan dan sebagainya.
Pengemulsi
d.
, bahan pengemulsi yang digunakan dalam sediaan krim disesuaikan dengan jenis dan sifat krim yang akan dibuat. Misalnya: emulgide, lemak bulu domba, setaseum, setearil alkohol dan lainnya.
Pengawet
e.
, yaitu bahan yang digunakan untuk meningkatkan stabilitas sediaan. Bahan pengawet yang sering digunakan adalah metil paraben (nipagin) 0,12-0,18%, propil paraben (nipasol) 0,02-0,05% dan lainnya. Pendapar
f.
, yaitu bahan yang digunakan untuk mempertahankan pH sediaan.
Antioksidan
7
kerja berlangsung pada jaringan setempat, tidak lengket, memberikan rasa dingin dan lain-lain. Adapun kerugian dari penggunaan sediaan krim antara lain, susah dalam pembuatannya karena harus dalam keadaan panas, gampang pecah, mudah kering dan rusak khususnya tipe a/m karena terganggunya sistem campuran yang disebabkan oleh perubahan suhu dan perubahan komposisi (Widodo, 2013).
Salah satu krim yang beredar di pasaran adalah Betason-N krim yang di produksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan. Betason-N krim merupakan salah satu krim yang sering digunakan untuk mengobati penyakit kulit. Tiap gram krim mengandung Betametason valerat 0.1% dan Neomisin sulfat 0.5%.
2.2.1 Betason-N krim
Gambar 2.1 Betason-N Krim
8
mengobati penyakit kulit dengan radang akut maupun sub-akut seperti eksema, dermatitis atopik, neurodermatitis, alergi terhadap bubuk sabun atau zat-zat kimia. Adanya Neomisin dalam Betason-N krim menjamin penyembuhan infeksi sekunder yang umumnya disertai radang-radang kulit.
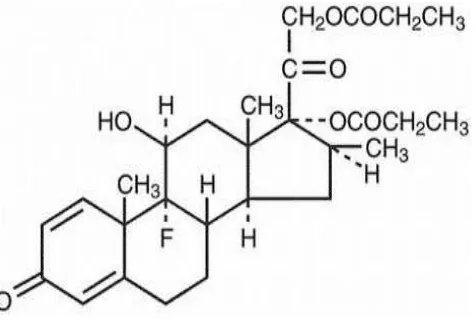
2.2.2 Betametason valerat
Gambar 2.2 Struktur kimia Betametason valerat
Betametason valerat mengandung tidak kurang dari 97.0% dan tidak lebih dari 103.0% C27H37FO6, dihitung terhadap zat yang dikeringkan. Pemeriannya serbuk, putih sampai praktis putih, tidak berbau, melebur pada suhu lebih kurang 190oC disertai peruraian. Kelarutan, praktis tidak larut dalam air, mudah larut dalam aseton dan kloroform, larut dalam etanol, sukar larut dalam benzen dan dalam eter (Depkes RI, 1995). Betametason sering digunakan pada salep sebagai valerat 0,1 % atau dipropionat 0.05 % yang dua kali lebih kuat (Tan dan Raharja, 2007).
2.3 Antibiotik
9
toksisitasnya bagi manusia relatif kecil. Turunan zat-zat ini yang dibuat secara semi-sintesis juga termasuk kelompok ini, begitu pula semua senyawa sintetis dengan khasiat antibakteri (Tan dan Raharja, 2007).
Kata antibiotik diberikan pada produk metabolik yang dihasilkan suatu organisme tertentu, yang dalam jumlah amat kecil bersifat merusak atau menghambat mikroorganisme lain. Dengan perkataan lain antibiotik merupakan zat kimia yang dihasilkan oleh suatu mikroorganisme yang mengahambat mikroorganisme lain (Pelczar, 1988). Pada awalnya istilah yang digunakan adalah antibiosis, yang berarti substansi yang dapat menghambat pertumbuhan organisme hidup yang lain dan berasal dari mikroorganisme. Namun pada perkembangannya antibiosis ini disebut sebagai antibiotik (Pratiwi, 2008).
Penghambatan mikroba yang disebabkan oleh suatu antibiotik mungkin bersifat tetap atau sementara. Apabila penghambatan itu hanya bersifat sementara maka keaktifan antibiotik itu disebut sebagai bakteriostatik. Walaupun antibiotik ini menghambat pertumbuhan sel bakteri, mikroba terus berkembang jika pemberian antibiotik dihentikan. Sedangkan agen bakterisid mekanisme tindakannya adalah memusnahkan mikroba (Hadisahputra dan Harahap, 1994).
10
Antibiotik dapat digolongkan menjadi beberapa golongan antara lain sebagai berikut:
2.3.1 Penggolongan antibiotik berdasarkan struktur kimianya a. Golongan Beta laktam
b.
, antara lain golongan sefalosporin (sefaleksin, sefazolin, sefuroksin, sefadroksil, seftazidim) golongan monosiklik dan golongan penisilin (penisilin, amoksisilin). Penisilin adalah suatu agen antibakterial alami yang dihasilkan dari jamur jenis Penicillium chrysogenum.
Antibiotik golongan Aminoglikosida
c.
, aminoglikosida dihasilkan oleh jenis-jenis fungi Streptomyces dan Micromonospora. Semua senyawa dan turunan semi sintetisnya mengandung dua atau tiga gula amino di dalam molekulnya yang saling terikat secara glikosidis. Spektrum kerjanya luas, aktifitasnya adalah bakterisid. Contohnya neomisin, streptomisin, amikasin, gentamisin dan paranomisin.
Antibiotik golongan Tetrasiklin
d.
, khasiatnya bersifat bakteriostatis. Mekanisme kerjanya berdasarkan diganggunya sintesa protein kuman. Spektrum antibakterinya luas dan meliputi banyak cocci Gram positif dan Gram negatif. Contohnya tetrasiklin, doksisiklin dan monosiklin.
11 e. Antibiotik golongan Linkomisin
f.
, dihasilkan oleh Streptomyces lincolnensis. Khasiatnya bakteriostatis, spektrum kerjanya lebih sempit dari pada makrolida terutama terhadap kuman Gram positif dan anaerob. Contohnya linkomisin.
Antibiotik golongan Kuinolon
g.
, senyawa-senyawa kuinolon berkhasiat bakterisid pada fase pertumbuhan kuman. Golongan ini hanya dapat digunakan pada infeksi saluran kemih (ISK) tanpa komplikasi.
Antibiotik golongan Kloramfenikol
2.3.2 Penggolongan antibiotik berdasarkan spektrum atau kisaran kerja , kloramfenikol mempunyai spektrum luas. Bersifat bakteriostatis terhadap hampir semua kuman Gram positif dan sejumlah kuman Gram negatif. Mekanisme kerjanya berdasarkan perintangan sintesa polipeptida kuman. Contohnya kloramfenikol (Tan dan Rahardja, 2007).
Berdasarkan spektrum atau kisaran kerjanya antibiotik dapat dibedakan menjadi dua yaitu :
a. Berspektrum sempit (narrow spectrum)
b.
, hanya mampu menghambat segolongan jenis bakteri saja, contohnya hanya mampu menghambat atau membunuh bakteri Gram positif atau Gram negatif saja.
Berspektrum luas (broad spectrum)
2.3.3 Penggolongan antibiotik berdasarkan mekanisme kerjanya
, dapat menghambat atau membunuh bakteri dari golongan Gram positif maupun Gram negatif (Pratiwi, 2008).
12
a. Antibiotik yang menghambat sintesis dinding sel
Antibiotik yang termasuk kelompok ini ialah penisilin, sefalosporin, basitrasin dan vankomisin.
b. Antibiotik yang merusak membran plasma
Antibiotik yang termasuk kelompok ini ialah polimiksin, nistatin dan amfoterisin B.
c. Antibiotik yang menghambat sintesis protein
Antibiotik yang termasuk kelompok ini adalah golongan aminoglikosida, makrolida, kloramfenikol, linkomisin dan tetrasiklin.
d. Antibiotik yang menghambat sintesis asam nukleat (DNA/RNA)
Antibiotik yang termasuk kelompok ini ialah rifampisin dan golongan kuinolon.
e. Antibiotik yang menghambat sintesis metabolit esensial
Antibiotik yang termasuk kelompok ini ialah sulfonamid, kotrimoksazol dan asam p-amino salisilat (PAS) (Pratiwi, 2008).
2.3.4 Bahaya pemakaian antibiotik
Beberapa bahaya yang dapat diakibatkan pada pemakaian antibiotik antara lain:
13
menjadi berkurang atau tidak berkhasiat sama sekali. Bila sudah terjadi resistensi antibiotik ini sudah tidak efektif lagi melawan kuman dan pada pengobatan selanjutnya harus diganti dengan antibiotik lain yang mempunyai khasiat yang sama.
b. Gejala kepekaan yang disebut alergi
c.
, misalnya gatal-gatal. Sebagai contoh, penisilin bila diberikan kepada seseorang yang tidak tahan (peka) dapat menimbulkan bintik-bintik merah, gatal-gatal bahkan pingsan.
Supra infeksi
2.3.5 Resistensi
, yaitu seseorang yang telah ketularan suatu kuman, ketularan kuman sekali lagi dengan kuman yang sama. Ini terutama terjadi pada pemakaian antibiotik broad spectrum, karena kegiatannya demikian luasnya sehingga flora bakteri usus juga dimatikan dan keseimbangan bakteri normal juga terganggu (Widjajanti, 1988).
Resistensi terhadap obat antibiotik, ialah obatnya tidak mampu membunuh kuman atau kumannya menjadi kebal terhadap obat. Beberapa jenis resistensi yaitu:
• Resistensi bawaan (primer)
•
, terjadi secara alamiah. Pada kuman sudah terdapat resistensi secara alamiah, misalkan adanya enzim penisilinase
yang merusak penisilin dan sefaloridin.
Resistensi yang diperoleh (sekunder)
•
, disebabkan kontak kuman dengan antibiotik.
14
• Resistensi silang
Salah satu contoh antibiotik yang beredar dipasaran adalah Neomisin sulfat yang terdapat dalam krim Betason-N produksi PT. Kimia Farma (Persero) Tbk. Plant Medan. Neomisin dikenal sebagai suatu antibiotik yang aktif terhadap sejumlah besar bakteri yang umumnya menyertai radang kulit.
, ialah kejadian dimana bakteri resisten terhadap suatu antibiotika dan semua derivatnya. Contohnya Penisilin dengan Ampisilin dan sebagainya (Anief, 1996).
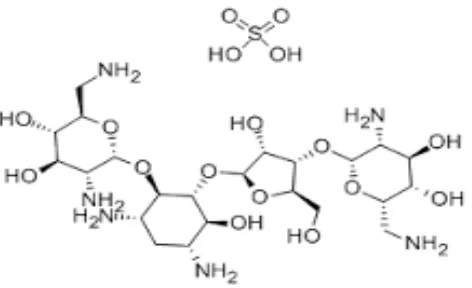
2.3.6 Neomisin sulfat
Gambar 2.3 Struktur kimia Neomisin sulfat
Neomisin sulfat adalah garam sulfat dari neomisin, zat antibakteri yang dihasilkan oleh pertumbuhan Streptomyces fradiae (1949) Waksman (Familia
Streptomycetaceae) atau campuran dari dua atau lebih bentuk garam. Mempunyai potensi setara tidak kurang dari 600 mcg neomisin per mg, dihitung terhadap zat yang telah dikeringkan (Depkes RI, 1995).
15
luas untuk penggunaan topikal dan berbagai infeksi kulit dan membran mukus yang disebabkan oleh mikroorganisme yang rentan terhadap obat ini. Pemberian oral neomisin biasanya dalam kombinasi dengan eritromisin basa. Neomisin diabsorpsi dengan buruk dari saluran gastrointestinal dan diekskresikan oleh ginjal sebagaimana aminoglikosida lainnya (Goodman dan Gilman, 2012).
Neomisin merupakan antibiotik golongan aminoglikosida. Aminoglikosida adalah golongan antibiotik bakterisidal yang terkenal toksik terhadap saraf otak (ototoksik) dan terhadap ginjal (nefrotoksik). Antibiotik ini merupakan produk berbagai spesies streptomyces atau fungus lainnya (Istiantoro dan Gan, 2011). Aminoglikosida merupakan kelompok antibiotik yang gula aminonya tergabung dalam ikatan glikosida. Antibiotik ini memiliki spektrum luas dan bersifat bakterisidal dengan mekanisme penghambatan pada sintesis protein. Antibiotik ini berikatan pada subunit 30S ribosom bakteri (beberapa terikat juga pada subunit 50S ribosom) dan menghambat translokasi peptidil-tRNA dari situs A ke situs P dan menyebabkan kesalahan pembacaan mRNA dan mengakibatkan bakteri tidak mampu menyintesis protein vital untuk pertumbuhannya (Pratiwi, 2008).
Secara in vitro neomisin aktif terhadap organisme Gram negatif termasuk
Eschericia coli, Enterobacter aerogenes, Klebsiella pneumonia, Proteus vulgaris
dan Haemophilus influenza. Neomisin aktif terhadap Gram positif yaitu
16
Efek merugikan dari penggunaan neomisin sulfat adalah reaksi hipersensitivitas, terutama ruam kulit, terjadi pada 6% hingga 8% pasien jika diberikan secara topikal. Efek toksis neomisin yang paling penting adalah kerusakan ginjal dan ketulian akibat kerusakan saraf pendengaran. Pada pemakaian oral efek merugikannya adalah malabsorpsi dan superinfeksi usus (Goodman dan Gilman, 2012).
Resistensi terhadap aminoglikosida
Resistensi terhadap antibiotik golongan aminoglikosida muncul karena sel bakteri memproduksi enzim-enzim yang dapat menambahkan fosfat, asetat, atau gugus adenil pada berbagai macam tempat pada antibiotik aminoglikosida. Antibiotik aminoglikosida yang telah dimodifikasi tersebut nantinya tidak akan mampu terikat pada subunit 30S ribosom sehingga tidak lagi dapat menghambat sintesis protein (Pratiwi, 2008).
2.4 Metode Pengujian
17
Keampuhan biologis dinyatakan dalam mikrogram (atau satuan lain) sebagaimana ditetapkan dengan cara membandingkan jumlah sel yang mati atau keadaan bakteriostatis organisme uji yang disebabkan oleh substansi uji, dengan yang disebabkan oleh siapan baku. Meskipun satuan pengukuran bagi beberapa antibiotik itu sembarang, bagi antibiotik-antibiotik lain hal tersebut ditetapkan menurut perjanjian internasional atau peraturan FDA (Food and Drug Administration). Misalnya unit internasional (“International Unit” atau IU) (Pelczar, 1988).
Untuk menentukan aktivitas antibiotik ada dua metode umum yang dapat digunakan, yaitu penetapan dengan lempeng silinder atau “lempeng” dan penetapan dengan cara “tabung” atau turbidimetri (Depkes RI, 1995).
a. Metode Lempeng Silinder
Metode ini berdasarkan difusi antibiotik dari silinder yang dipasang tegak lurus pada lapisan agar padat dalam cawan petri atau lempeng, sehingga mikroba yang ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” di sekeliling silinder yang berisi larutan antibiotik. b. Metode Turbidimetri
Metode ini berdasarkan atas hambatan pertumbuhan biakan mikroba dalam larutan serba sama antibiotik, dalam media cair yang dapat menumbuhkan mikroba dengan cepat bila tidak terdapat antibiotik.
2.5 Medium Biakan Mikroba
18
dalamnya. Medium dapat digunakan untuk isolasi, perbanyakan, pengujian sifat-sifat fisiologis dan perhitungan jumlah mikroorganisme (Waluyo, 2010).
Berdasarkan sifat keheterotrofan mikroba, medium dapat digolongkan beberapa kelompok besar yaitu :
1. Media hidup
2.
, pada umumnya media hidup dipakai dalam laboratorium virologi untuk pembiakan berbagai virus, sedangkan dalam laboratorium bakteriologi hanya beberapa kuman tertentu saja. Contoh media hidup adalah hewan percobaan, manusia, telur berembrio, biakan jaringan dan lainnya.
Media mati
Media mati dapat digolongkan berdasarkan konsistensinya yaitu :
, pada media mati juga dikenal media sintetis. Media sintetis merupakan media yang mempunyai kandungan dan isi bahan yang telah diketahui secara terperinci. Media sintetis sering digunakan untuk mempelajari sifat faali dan genetika mikroorganisme (Waluyo, 2010).
• Media padat
dari ganggang atau alga yang berfungsi sebagai bahan pemadat.
, diperoleh dengan cara menambah agar-agar. Agar berasal
• Media setengah padat
•
, media ini dibuat dengan bahan sama dengan media padat, akan tetapi yang berbeda adalah komposisi agarnya.
19
Media yang digunakan pada penetapan potensi Neomisin sulfat dalam krim
Betason-N produksi PT. Kimia Farma (Persero) Tbk. Plant Medan secara mikrobiologi yaitu media antibiotik no. 1.
Media antibiotik no. 1
Komposisi media antibiotik no.1 ini adalah campuran dari pepton, Tripton, ekstrak ragi, lab-lemco powder, glukosa dan agar. Untuk membuat media tersebut dapat melarutkan bahan-bahan diatas dengan air hingga 1 L dan atur pH nya dengan menggunakan Natrium hidroksida 1 N atau Asam klorida 1 N, hingga sesudah sterilisasi uap air pH 6,6 ± 0,1 (Depkes RI,1995).
2.6 Bakteri
Bakteri merupakan organisme mikroskopik yang memiliki peran besar dalam kehidupan di bumi. Beberapa kelompok bakteri dikenal sebagai agen penyebab infeksi dan penyakit, sedangkan kelompok lainnya dapat memberikan manfaat dibidang pengobatan, pangan, industri dan lain-lain (Wikipedia, 2015).
Berdasarkan struktur kimia dinding selnya, bakteri dapat dibedakan menjadi dua yaitu bakteri Gram positif dan bakteri Gram negatif. Bakteri Gram positif yaitu bakteri yang dinding selnya banyak mengandung peptidoglikan, sedangkan bakteri Gram negatif dinding selnya banyak mengandung lipopolisakarida (Pratiwi, 2008). Contoh bakteri Gram positif antara lain genus
20
Pada penetapan potensi Neomisin sulfat dalam Betason-N krim produksi PT. Kimia Farma (Persero) Tbk. Plant Medan, bakteri yang digunakan adalah
Staphylococcus epidermidis. Bakteri ini merupakan salah satu jenis bakteri yang sering menyertai radang kulit.
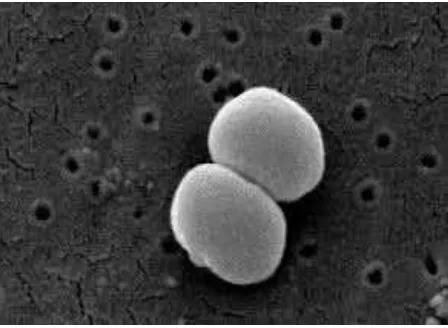
Staphylococcus
Staphylococcus adalah bakteri gram positif berbentuk bulat, biasanya tersusun dalam rangkaian tak beraturan seperti anggur. Bakteri ini mudah tumbuh pada berbagai pembenihan dan mempunyai metabolisme aktif, meragikan karbohidrat, serta menghasilkan pigmen yang bervariasi dari putih sampai kuning tua. Beberapa diantaranya tergolong flora normal pada kulit dan selaput mukosa manusia. Staphylococcus patogen sering menghemolisis darah, mengkoagulasi plasma, serta menghasilkan berbagai enzim ekstraseluler dan toksin.
Staphylococcus cepat menjadi resisten terhadap banyak zat antimikroba sehingga menimbulkan masalah pengobatan yang sulit (Nasution, 2014).
Staphylococcus epidermidis
21
Klasifikasi ilmiah bakteri Staphylococcus epidermidis Kingdom : Bacteria
Filum : Firmicutes
Class : Bacili
Ordo : Bacillales
Family : Staphylococcaceae
Genus : Staphylococcus
Spesies : S. epidermidis
Nama binomial : Staphylococcus epidermidis (Wikipedia, 2013)
Staphylococcus epidermidis adalah salah satu spesies bakteri dari genus
Staphylococcus yang diketahui dapat menyebabkan infeksi oportunistik (menyerang individu dengan sistem kekebalan tubuh yang lemah). Secara klinis bakteri ini menyerang orang-orang yang rentan atau imunitas rendah (Wikipedia, 2013). Staphylococcus epidermidis merupakan bakteri koagulase negatif dan katalase negatif. Mempunyai karakteristik dengan bentuk koloni putih pada manitol salt agar dan ini dapat digunakan untuk membedakannya dengan
22 BAB III
METODOLOGI PENGUJIAN
3.1 Tempat Pelaksanaan Penetapan Potensi
Penetapan potensi ini dilakukan di ruang Laboratorium Quality Control
yang terdapat di Industri PT. Kimia Farma (Persero) Tbk. Plant Medan yamg beralamat di Jl. Tanjung Morawa Km. 9 No. 59 Medan.
3.2 Alat-alat
Alat-alat yang digunakan adalah autoklaf, batang pengaduk, beaker gelas (50 ml dan 100 ml), benang wol, Bio Safety Cabinet Class II, botol roux, bunsen, cawan petri, erlenmeyer (250 ml, 500 ml dan 1000 ml), gelas ukur (100 ml dan 250 ml), gunting, hot plate, inkubator, jangka sorong, kain kasa, kapas, kertas perkamen, labu tentukur (10 ml, 25 ml dan 50 ml), oven, pinset, pipet mikro, pipet tetes, pipet volum 2 ml, ring stainless stell, spatula, timbangan analitik elektrik,
Ultrasonic digital. 3.3 Bahan-bahan
Bahan-bahan yang digunakan adalah aquadem, baku pembanding sekunder Neomisin sulfat, biakan bakteri Staphylococcus epidermidis nomor ATCC 12228, krim Betason-N no. bets B50187T, larutan dapar fosfat (LDF) III, larutan NaCl 0,9%, media Antibiotik no.1, media Tryptone Soya Agar (TSA). 3.4 Prosedur Kerja
3.4.1 Pembuatan media uji
23
dengan 1000 ml aquadem, dipanaskan di atas hot plate sampai mendidih, di sterilkan di dalam autoklaf dengan pH 6,6 ± 0,1.
3.4.2 Pembuatan larutan dapar fosfat III
Dilarutkan 8,36 g kalium dihidrogen fosfat dalam 500 ml aquadem. Atur pH hingga syarat 8,0 ± 0,1 dengan kalium hidroksida 10 N dan asam fosfat 18 N. 3.4.3 Pembuatan larutan baku pembanding kerja
Ditimbang baku pembanding sesuai dengan potensi yang ada pada etiket setara dengan 1000 mcg/ml. Masukkan kedalam labu 50 ml, tambahkan pelarut ±25 ml diletakkan diatas Ultrasonic selama 15 menit lalu tambahkan pelarut sampai garis tanda.
Untuk larutan standar 1 (S1) dipipet sebanyak 0,64 ml, S2 dipipet sebanyak 0,8 ml, S3 dipipet sebanyak 1 ml, S4 dipipet sebanyak 1,25 ml, S5 dipipet sebanyak 1,56 ml, larutan diatas, masukkan ke dalam labu tentukur 10 ml cukupkan dengan Larutan Dapar Fosfat (LDF) III sampai garis tanda lalu homogenkan. Dimasukkan kedalam vial yang berbeda untuk setiap larutan standar.
3.4.4 Pembuatan larutan uji
Timbang 1 g krim Betason-N dalam beker gelas 50 ml. Tambahkan 5 ml larutan dapar fosfat (LDF) III, panaskan diatas hot plate, biarkan hingga larut. Masukkan ke dalam labu 10 ml lalu tambahkan pelarut sampai garis tanda. Saring dan ambil filtratnya.
3.4.5 Penandaan cawan petri
24
dari 3 cawan petri. Pada bagian bawah bagian luar cawan petri beri tanda titik 6 buah ring dengan 3 titik untuk S1 dan 3 titik untuk S3 secara selang-seling. Pada bagian bawah sebelah luar cawan petri kelompok 2, beri tanda titik 6 buah ring dengan 3 buah untuk S2 dan 3 buah untuk S3 secara berselang-seling. Seterusnya sampai S4, S5 dan U.
3.4.6 Pembuatan inokulum
Bakteri Staphylococcus epidermidis dengan nomor ATCC 12228 di biakkan ke dalam media non selektif. Digariskan ke dalam tabung reaksi, inkubasi selama 24 jam pada suhu 35°C. Siapkan media antibiotik no.1 sebanyak 250 ml masukkan kedalam botol roux. Pada biakan bakteri ditambahkan 3 ml NaCl 0,9% dikocok sampai larut lalu masukkan ke dalam tabung reaksi. Inkubasi selama 1 minggu pada suhu 35-37oC. Setelah 1 minggu ke dalam botol roux ditambahkan 40 ml larutan NaCl 0,9%, kocok sampai semua bakteri terlarut. Pindahkan suspensi bakteri ke dalam erlenmeyer 250 ml. Simpan di dalam lemari pendingin suhu 2-8°C dengan masa simpan 1 bulan.
3.4.7 Penyiapan media
Tuangkan 15 ml larutan media antibiotik no.1 kedalam cawan petri, ratakan lalu diamkan hingga memadat. Tambahkan 5 ml suspensi bakteri ke dalam cawan petri, homogenkan lalu diamkan.
3.4.8 Penetapan potensi
25
ke dalam ring sesuai dengan penandaan untuk ketiga cawan petri pada kelompok 1. Begitu seterusnya untuk S2 dan S3 kelompok 2, S4 dan S3 kelompok 3, S5 dan S3 kelompok 4 dan U dan S3 kelompok 5. Inkubasi selama 24 jam pada suhu 35-37°C. Ukur zona hambatnya dengan menggunakan jangka sorong.
3.5Perhitungan Potensi
Korektor = rata-rata baku S3 – diameter hambat S3 Diameter hambat S3 = jumlah rata-rata baku S3 / 4 Hasil koreksi = rata-rata baku S3 + korektor
a = (∑�
a : Garis tengah rata-rata daerah hambatan yang telah dikoreksi pada kadar U b : Kemiringan garis
26
y : Garis tengah rata-rata daerah hambatan yang telah dikoreksi Yu : Garis tengah rata-rata daerah hambatan uji yang telah dikoreksi Xu : Garis tengah rata-rata daerah hambatan larutan uji
Dosis U : Dosis sampel Potensi U : Potensi sampel
n : Jumlah variasi kadar larutan baku ∑x2
27 BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL
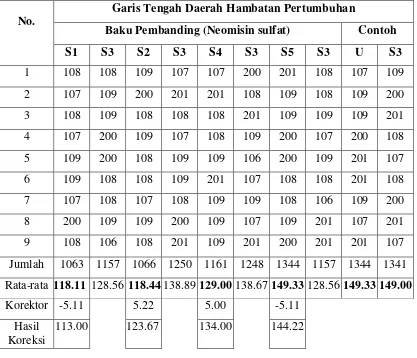
Hasil pengamatan penetapan potensi Neomisin sulfat dalam krim Betason-N yang diproduksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan dengan menggunakan metode Lempeng silinder dapat dilihat pada tabel 4.1 berikut ini: Tabel 4.1 Hasil pengamatan penetapan potensi Neomisin sulfat dalam krim
Betason-N produksi PT. Kimia Farma (Persero) Tbk. Plant Medan
No.
Garis Tengah Daerah Hambatan Pertumbuhan
Baku Pembanding (Neomisin sulfat) Contoh
S1 S3 S2 S3 S4 S3 S5 S3 U S3 Rata-rata 118.11 128.56 118.44 138.89 129.00 138.67 149.33 128.56 149.33 149.00 Korektor -5.11 5.22 5.00 -5.11
Hasil Koreksi
113.00 123.67 134.00 144.22
28
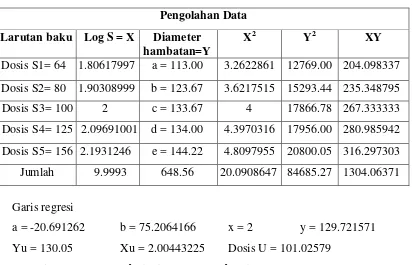
Tabel 4.2 Hasil pengolahan data dari penentuan garis tengah hambat dan garis regresi
Pengolahan Data Larutan baku Log S = X Diameter
hambatan=Y
X2 Y2 XY
Dosis S1= 64 1.80617997 a = 113.00 3.2622861 12769.00 204.098337 Dosis S2= 80 1.90308999 b = 123.67 3.6217515 15293.44 235.348795 Dosis S3= 100 2 c = 133.67 4 17866.78 267.333333 Dosis S4= 125 2.09691001 d = 134.00 4.3970316 17956.00 280.985942 Dosis S5= 156 2.1931246 e = 144.22 4.8097955 20800.05 316.297303 Jumlah 9.9993 648.56 20.0908647 84685.27 1304.06371
Garis regresi
a = -20.691262 b = 75.2064166 x = 2 y = 129.721571 Yu = 130.05 Xu = 2.00443225 Dosis U = 101.02579
Potensi U = 101.03 % 5.05 mg/g massa745.91 mcg/mg massa
4.2 PEMBAHASAN
Krim Betason-N yang di produksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan sebelum diedarkan kepasaran terlebih dahulu harus dilakukan serangkaian pengujian yang merupakan bagian dari pengawasan mutu, yang bertujuan untuk melindungi konsumen dari penggunaan obat yang tidak memenuhi mutu dan efek terapi yang tidak baik. Salah satu pengujian yang dilakukan adalah uji potensi terhadap antibiotik yang terdapat dalam krim tersebut secara mikrobiologi.
29
ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” di sekeliling silinder yang berisi larutan antibiotik (Depkes RI, 1995). Media yang digunakan yaitu media antibiotik no.1 dan bakteri yang digunakan adalah bakteri Staphylococcus epidermidis. Pengujian ini juga bertujuan untuk mengatasi keraguan atas kemungkinan hilangnya aktivitas (potensi) antibiotik terhadap efek daya hambatnya pada mikroba.
Dari hasil penetapan potensi Neomisin sulfat yang terdapat dalam krim Betason-N produksi PT. Kimia Farma (Persero) Tbk. Plant Medan dengan no. bets B50187T didapatkan potensi sampel sebesar 101.03 % atau 5.05 mg/g massa atau setara dengan 745.91 mcg/mg massa. Berdasarkan Farmakope Indonesia Edisi ke-IV Tahun 1995 potensi neomisin sulfat setara dengan tidak kurang dari 600 mcg/mg massa. Maka dengan hasil pengujian ini dapat dinyatakan bahwa potensi Neomisin sulfat yang terdapat dalam krim Betason-N dengan no. bets B50187T produksi PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi persyaratan, sehingga krim tersebut layak untuk dipasarkan.
Gambar 4.1 Zona hambat Neomisin sulfat pada Betason-N krim dalam menghambat pertumbuhan bakteri Staphylococcus epidermidis. Keterangan:
30 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
• Metode yang digunakan pada penetapan potensi Neomisin sulfat dalam
krim Betason-N secara mikrobiologi produksi PT. Kimia Farma (Persero) Tbk. Plant Medan, yaitu metode Lempeng silinder. Metode ini berdasarkan difusi antibiotik dari silinder yang dipasang tegak lurus pada lapisan agar padat dalam cawan petri atau lempeng, sehingga mikroba yang ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau “zona” di sekeliling silinder yang berisi larutan antibiotik.
• Berdasarkan pengujian yang telah dilakukan di PT. Kimia Farma (Persero)
Tbk. Plant Medan di dapatkan hasil potensi dari Neomisin sulfat yaitu 101.03 % atau 5.05 mg/g massa atau sama dengan 745.91 mcg/mg massa. Dari hasil yang diperoleh, dapat disimpulkan bahwa potensi Neomisin sulfat yang terdapat dalam krim Betason-N telah memenuhi syarat Farmakope Indonesia Edisi IV tahun 1995 yaitu mempunyai potensi setara dengan tidak kurang dari 600 mcg neomisin per mg massa.
5.2 Saran
31
DAFTAR PUSTAKA
Anief, M. (1996). Penggolongan Obat Berdasarkan Khasiat dan Penggunaan. Yogyakarta: Gadjah Mada University Press. Hal: 20-21.
Anief, M. (1997). Formulasi Obat Topical Dengan Dasar Penyakit Kulit. Yogyakarta: Gadjah Mada University Press. Hal: 61-62.
Anief, M. (2007). Farmasetika. Yogyakarta: Gadjah Mada University Press. Hal: 116-117.
Depkes RI, (1995). Farmakope Indonesia Edisi IV. Jakarta: Departemen Kesehatan RI. Hal: 142, 606, 891-892.
Faulkner. (2008). What About Scabies. Ohio online dot com. Di unggah pada 24 April 2015 pukul: 05:45.
Goodman dan Gilman. (2012). Dasar Farmakologi Terapi Edisi 10, Vol. 3.
Jakarta: EGC. Hal: 1209-1210
Hadisahputra, S dan Harahap, U. (1994). Biokimia dan Farmakologi Antibiotika. Medan: USU Press. Hal: 4.
Istiantoro, Y dan Gan, V. (2011). Farmakologi dan Terapi Edisi 5 (Cetak Ulang dengan Tambahan). Jakarta: Badan Penerbit FK UI.Hal: 705.
Jas, A. (2004). Perihal Obat dan Berbagai Sediaannya. Medan: USU Press. Hal: 60.
Nasution, M. (2014). Pengantar Mikrobiologi. Medan: USU Press. Hal: 74-79 Pelczar, J. (1988). Dasar-dasar Mikrobiologi. Jakarta: UI Press. Hal: 511,
535-536.
Pratiwi, T. (2008). Mikrobiologi Farmasi. Jakarta: Penerbit Erlangga. Hal: 150-160.
Tan. T. H, dan Rahardja. K (2007). Obat-obat Penting. Jakarta: Elex media. Hal: 65, 78, 734.
Volk, A. dan Wheeler, F. (1988). Mikrobiologi Dasar. Jakarta: Penerbit Erlangga. Hal: 3.
Waluyo, L. (2010). Teknik dan metode dasar Mikrobiologi. Malang: UMM Press. Hal: 127-129, 195-196.
32
Widjajanti, V. (1988). Obat-obatan. Yogyakarta: Kanisius. Hal: 76-77, 90, 95. Widodo, H. (2013). Ilmu Meracik Obat Untuk Apoteker. Yogyakarta: D-Medika.
Hal: 168-172.
Widodo, R. (2004). Panduan Keluarga Memilih dan Menggunakan Obat.
Yogyakarta: Kreasi Wacana. Hal: 96.
Wikipedia. (2013). http://id.m.wikipedia.org/wiki/Staphylococcus_epidermidis. diunggah pada 20 Februari 2015 pukul: 23:09.
33 LAMPIRAN
34
Lampiran 2. Perhitungan penetapan potensi Neomisin sulfat dalam krim Betason-N
Korektor = rata-rata baku S3 – diameter hambat S3
Diameter hambat S3 = jumlah rata-rata baku S3 / 4
= 128,56+138,89+138,67+128,56
4
= 133,67
Korektor S1 = 128,56 – 133,67 = -5,11 Korektor S2 = 138,89 – 133,67 = 5,22 Korektor S4 = 138,67 – 133,67 = 5,00 Korektor S5 = 128,56 – 133,67 = -5,11
Hasil koreksi = rata-rata baku S3 + korektor Hasil koreksi S1 = 118,11 + (-5,11) = 113,00 Hasil koreksi S2 = 118,44 + 5,22 = 123,67 Hasil koreksi S4 = 129,00 + 5,00 = 134,00 Hasil koreksi S5 = 149,33 + (-5,11) = 144,22
a = (∑�
2 .∑�)− (∑� .∑��)
� .∑�2−(∑�)2
=(20,0908647 .648,56)− (9,9993 .1304 ,06371 ) 5 .20,0908647−(9,9993)2
35 Lampiran 2. (Lanjutan)
b = (� .∑��)− (∑� .∑�)
� .∑�2− (∑�)2
=(5 .1304 ,06371 )− (9,9993 .648,56) 5 .20,0908647−(9,9993)2
= 75.2064166
x = Log S dari S3
= Log 100= 2
y = a + bx
= -20.691262 + 75.2064166 . 2
= 129.721571
Yu = {�+ (� − �3�)}
= {(129.721571 + (149,33−149,00}= 130.05
Xu = ��−�
�
= 130.05−(−20.691262 ) 75.2064166
= 2.00443225
Dosis U = (10)Xu
36 Lampiran 2. (Lanjutan)
Potensi U = (dosisU / S3) x 100 %
= (101.02579 )
100
�
100%
= 101.03 % 5.05 mg/g massa
Potensi = ������� �
100 ������������������������������
= 101.03 %
100 � 738.31 ���/�
37
Lampiran 3. Beberapa alat yang digunakan dalam penetapan potensi
a. Bio Safety Cabinet Class II b.Otoklaf