DETEKSI VIRUS AVIAN INFLUENZA (H5N1)
PADA UNGGAS AIR DI PROPINSI LAMPUNG
DENGAN UJI
HAEMAGGLUTINATION INHIBITION
(HI)
DAN
REVERSE TRANSCRIPTASE -POLYMERASE CHAIN
REACTION
(RT-PCR)
DWI DESMIYENI PUTRI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa Deteksi Virus Avian Influenza (H5N1) pada Unggas Air di Propinsi Lampung dengan Uji Haemagglutination Inhibition (HI) dan Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR) merupakan gagasan atau hasil penelitian saya sendiri dengan arahan komisi pembimbing. Tesis ini belum pernah diajukan untuk memperoleh gelar pada program sejenis di Perguruan Tinggi lain. Sumber informasi dari karya yang diterbitkan maupun tidak diterb itkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2006
ABSTRAK
DWI DESMIYENI PUTRI. Deteksi Virus Avian Influenza (H5N1) pada Unggas Air di Propinsi Lampung dengan Uji Haemagglutination Inhibition (HI) dan Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR). Dibimbing oleh Retno D Soejoedono dan Ekowati Handharyani
Avian Influenza (AI) atau lebih dikenal oleh masyarakat sebagai “Flu Burung” adalah penyakit infeksi pada unggas yang disebabkan oleh virus influenza tipe A. Di Indonesia virus AI telah ditemukan sejak September 2003, dan menyebabkan kematian yang tinggi pada peternakan ayam komersil. Unggas air seperti itik, entok, dan angsa merupakan reservoir dari semua tipe influenza A, tetapi unggas yang terinfeksi oleh virus ini tidak menunjukkan gejala klinis. Lampung merupakan salah satu propinsi dimana semua Kabupaten/Kota di Propinsi ini berstatus sebagai daerah tertular AI. Pada tahun 2003 virus AI menyebabkan kematian 977.718 ekor unggas, dan pada tahun 2004 kasus kematian unggas karena AI meningkat menjadi 2 kalinya. Namun belum ada informasi mengenai keberadaan virus AI pada unggas air di Propinsi Lampung. Tujuan dari penelitian ini adalah untuk mengetahui keberadaan antibodi terhadap virus Avian Influenza (H5) dan untuk mendeteksi dan menentukan subtipe virus AI (H5N1) pada unggas air di Propinsi Lampung dengan metode RT-PCR.
Pada penelitian ini sampel yang digunakan berupa serum dan usap kloaka yang masing-masing berjumlah 673 sampel. Berdasarkan hasil uji serologis, antibodi terhadap AI (H5) ditemukan pada semua Kabupaten/Kota di Propinsi Lampung dan pada semua jenis unggas air (itik, entok, dan angsa) yang diperiksa dengan persentase tertinggi ditemukan pada Kabupaten Tulang Bawang (69.41 %). Rata-rata titer antibodi terhadap virus AI (H5) masih rendah, yaitu dibawah 24 (kecuali Lampung Selatan), dan rata-rata titer antibodi paling rendah ditemukan pada Kabupaten Tulang Bawang (20.92). Pada pemeriksaan keberadaan materi genetik virus H5N1 secara individu tidak ditemukan virus AI subtipe H5N, tetapi ditemukan virus AI dengan subtipe H5Nx dan HxN1 pada unggas air di Propinsi Lampung.
DETEKSI VIRUS AVIAN INFLUENZA (H5N1)
PADA UNGGAS AIR DI PROPINSI LAMPUNG
DENGAN UJI
HAEMAGGLUTINATION INHIBITION
(HI)
DAN
REVERSE TRANSCRIPTASE -POLYMERASE CHAIN
REACTION
(RT-PCR)
DWI DESMIYENI PUTRI
Tesis
Sebagai salah satu syarat memperoleh gelar Magister Sains pada
Program Studi Sains Veteriner
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Deteksi Virus Avian Influenza (H5N1) pada Unggas Air di Propinsi Lampung dengan Uji Haemagglutination Inhibition (HI)dan Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR)
Nama : Dwi Desmiyeni Putri
NIM : B053040011
Program Studi : Sains Veteriner
Disetujui Komisi Pembimbing
Dr. drh. Retno D Soejoedono, M.S. Dr. drh. Ekowati Handharyani, M.S.
Ketua Anggota
Diketahui
Ketua Program Studi Sains Veteriner Dekan Sekolah Pascasarjana
Dr. drh. Bambang Pontjo P, M.S. Dr. Ir. Khairil Anwar Notodiputro, M.S.
PRAKATA
Segala puji dan syukur penulis panjatkan kepada Allah SWT atas rahmat yang telah dilimpahkan sehingga penulis dapat menyelesaikan penelitian dan penulisan tesis yang berjudul Deteksi Virus Avian Influenza (H5N1) pada Unggas Air di Propinsi Lampung dengan Uji Haemagglutination Inhibition (HI) dan Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR)
Ucapan terima kasih penulis sampaikan kepada :
1. Dr. drh Retno D Soejoedono, M.S. selaku ketua komisi pembimbing dan Dr. drh. Ekowati Handharyani, M.S. selaku anggota komisi pembimbing, atas waktu, saran, kesempatan, nasehat, serta bimbingannya.
2. Dr. drh. Bambang Pontjo P, MS selaku Ketua Program Studi Sains Veteriner.
3. Dr. drh. Agus Setiyono, M.S. selaku dosen penguji luar.
4. drh. Sri Murtini, M.S. dan Ir. Etih Sudarnika M.S. atas saran dan informasinya.
5. Teman-teman Program Studi Sains Veteriner.
6. Teman-teman grup AI dan IgY (mb santi, okti, mas rizal, ika) 7. Orang tua dan keluarga, atas segala doa dan perhatiannya.
8. Anak -anak (Faatih dan Nabil) serta suami tercinta atas kesempatan, doa dan kasih sayangnya.
.
Bogor, Agustus 2006
RIWAYAT HIDUP
Penulis dilahirkan di Tanjungkarang, 5 Desember 1973 dari ayah Kamaruddin BN dan ibu Dra. H. Emmy Alidar. Penulis merupakan anak kedua dari tiga bersaudara.
DAFTAR TABEL
Halaman 1 Fungsi protein Virus Influenza A ………... 7 2 Distribusi jumlah sampel pada tiap
kabupaten/kota di Propinsi Lampung ……… 22 3 Distribusi hasil serologis menurut wilayah dan jenis ternak …………... 24 4 Nilai rata-rata titer antibodi terhadap H5 virus Avian Influenza ……… 25 5 Hasil pemerikasaan materi genetik dengan RT-PCR
pada pool sampel unggas air serologis positif ………. 28 6 Hasil pemeriksaan materi genetik pada
sampel serologis positif pool 14 secara individu ………... 30 7 Hasil pemerikasaan materi genetik dengan RT-PCR
DAFTAR GAMBAR
Halaman
1 Virus Influenza Tipe A, B, dan C ………. 4
2 Ilustrasi antigenic drift virus influenza ………. 6
3 Ilustrasi antigenic shift virus influenza ……… 6
4 Replikasi virus influenza ………... 13
5 Contoh hasil RT-PCR pada gen HA dielektroforesis pada gel agarose 1,5 %, diwarnai dengan ethidium bromide …………... 27
6 Contoh hasil RT-PCR pada gen H5 dielektroforesis pada gel agarose 1,5 %, diwarnai dengan ethidium bromide …………... 27
DAFTAR LAMPIRAN
Halaman 1 Alur Penelitian ………... 37 2 Hasil Pemeriksaan Materi Genetik dengan RT-PCR
PENDAHULUAN
Latar Belakang
Avian Influenza (AI) atau lebih dikenal oleh masyarakat sebagi “Flu Burung” adalah penyakit infeksi pada unggas yang disebabkan oleh virus influenza tipe A. Penyakit yang pertama diidentifikasi di Italia lebih dari 100 tahun yang lalu, kini muncul di seluruh dunia (Capua et al. 1999). Seluruh unggas diketahui rentan terhadap infeksi AI, walaupun beberapa spesies lebih tahan terhadap virus ini dibandingkan dengan yang lain. Infeksi oleh virus AI dapat menyebabkan gejala yang sangat bervariasi pada unggas, mulai dari gejala yang ringan hingga ke penularan yang sangat tinggi dan cepat menjadi penyakit yang fatal (Murphy et al. 1999; Swayne dan Suarez 2000).
Avian Infuenza telah meresahkan dunia karena penyakit in i menyebar sangat cepat dan mengakibatkan kematian unggas dalam jumlah yang sangat besar. Di Asia, wabah virus AI mulai merebak sekitar tahun 90-an di Hongkong, dan selanjutnya virus ini telah menyebar ke beberapa negara yaitu Thailand, Malaysia, China, Korea, Kamboja, Jepang, Vietnam, dan termasuk Indonesia (OIE 2005; Meines et al. 2005). Di Indonesia virus AI telah ditemukan sejak September 2003, dan secara resmi baru diumumkan pemerintah pada 25 Januari 2004. Penyakit ini menyebabkan kematian yang tinggi pada ayam komersial petelur di Indonesia (6.2 juta ekor). Kerugian lain yang ditimbulkan adalah efek psikologis masyarakat, yang secara nyata mengimbas perekonomian negara, khususnya yang berkaitan dengan unggas dan produk-produk asal unggas. Unggas yang terserang pada umumnya adalah ayam petelur, pedaging, bebek dan puyuh (Soejoedono dan Handharyani 2005)
Unggas air adalah unggas yang biasa atau dapat hidup di air. Namun pada penelitian ini yang dimaksud dengan unggas air adalah unggas yang biasa hidup di air dan dipelihara bersamaan dengan ayam, seperti itik, entok, dan angsa. Unggas air yang hidup berdamp ingan dengan ayam diduga sebagai reservoir virus AI yang dapat menjadi sumber penularan bagi ayam dan dapat berakibat fatal.
Pada Januari 2004, di beberapa daerah di Indonesia, terutama di Bali, Lombok, Jawa Timur, Jawa Tengah, Kalimantan Barat, dan Jawa Barat dilaporkan adanya kasus kematian ternak ayam yang luar biasa. Awalnya kematian tersebut diduga disebabkan karena virus Newcastle, namun konfirmasi terakhir oleh Departemen Pertanian disebabkan oleh virus flu burung atau AI. Departemen Pertanian menyatakan bahwa, sepanjang tahun 2004 telah dimusnahkan sekitar 5 juta ekor ayam yang diidentifikasi terserang flu burung.
Selain beberapa propinsi di Pulau Jawa dan Kalimantan yang telah menjadi daerah tertular AI, beberapa propinsi di Sumatra juga telah menjadi daerah tertular. Lampung merupakan propinsi yang letaknya di ujung selatan Pulau Sumatra. Daerah ini merupakan tempat yang menjadi lalu lintas perdagangan ternak dari Pulau Sumatra ke Jawa atau sebaliknya. Sehingga berbagai agen penyakit sangat mungkin dan mudah sekali untuk masuk ke daerah ini termasuk virus AI.
Berdasarkan data dari Dinas Peternakan dan Kesehatan Hewan Propinsi Lampung, AI pertama kali di temukan pada bulan September 2003 dan menyebabkan kematian 977 718 ekor unggas (ayam dan puyuh) dan pada tahun 2004 tingkat kematian meningkat menjadi dua kali lipat. Belum ada data yang menyebutkan adanya kematian pada unggas-unggas air yang disebabkan oleh virus tersebut. Oleh karena itu perlu dilakukan identifikasi virus AI pada unggas air di Propinsi Lampung.
Metode ini lebih sensitif dan spesifik dibandingkan prosedur konvensional lainnya (Daum et al. 2002 ; Poddar 2002 ; Stockton et al. 1998).
Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui keberadaan antibodi terhadap virus Avian Influenza (H5) pada unggas air di Propinsi Lampung dengan uji serologis.
TINJAUAN PUSTAKA
Virus Influenza A, B dan C
Virus influenza merupakan virus RNA memiliki amplop (envelope) yang termasuk anggota dari famili Orthomyxoviridae. Genomnya terdiri dari negative single strand RNA. Virus ini terdiri atas tiga tipe yaitu A, B, dan C. Virus Influenza tipe A dan B memiliki 8 segmen RNA, tetapi virus influenza tipe C hanya memiliki 7 segmen (Murphy et al.
1999) (Gambar 1).
Gambar 1 Virus influenza tipe A, B dan C
Virus influenza A merupakan virus yang menyebar luas dan menginfeksi banyak spesies hewan seperti babi, kuda, kucing, harimau, macan tutul, mamalia laut serta jenis unggas; dan termasuk manusia. Virus tipe A dibagi atas beberapa subtipe yang disusun berdasarkan dua (2) jenis glikoprotein pada permukaannya. Protein ini disebut Hemaglutinin (HA) dan Neuraminidase (NA) (Lipatov et al. 2004; Murphy et al. 1999).
misalnya H7N7 dan H3N8 yang menyebabkan penyakit flu pada kuda (Murphy et al. 1999).
Virus Influenza tipe B umumnya ditemukan di manusia. namun, infeksi virus influenza B baru-baru ini ditemukan pada anjing laut. Tidak seperti Virus tipe A, Virus ini tidak diklasifikasi berdasar subtipe. Virus influenza tipe B belum memberikan susunan HA dan NA yang sama dan merupakan populasi minor pada peredaran virus influenza pada manusia. Virus Influenza tipe C secara umum hanya menyebabkan gangguan sedang pada saluran pernafasan manusia dan tidak menyebabkan epidemi atau pandemi. Virus influenza tipe C tidak memiliki protein permukaan HA dan NA seperti yang dimiliki oleh virus influenza A dan B akan tetapi kedua segmen tersebut digantikan oleh glikoprotein tunggal yang disebut dengan haemagglutinin-esterase-fusion (HEF) (Sturm-Ramirez et al. 2004).
Gambar 2 Ilustrasi antigenic drift virus influenza (Anonim 2005).
Virus Avian Influenza
Avian Influenza atau “Fowl Plaque” dis ebabkan oleh virus influenza tipe A dengan diameter 90 sampai 120 nm (Murphy et al. 1999). Virus ini memiliki 8 segmen RNA negatif-sense yang menghasilkan 10 protein dengan fungsi yang berbeda. Kedelapan segmen genom tersebut berturut-turut menyandi protein polimerase B2 (PB2; segmen 1), polimerase B1 (PB1; segmen 2), polimerase A (PA; segmen 3), hemaglutinin (HA; segmen 4), nukleoprotein (NP; segmen 5), neuraminidase (NA; segmen 6), protein matriks (M1 dan M2; segemen 7) serta protein non struktural (NS1 dan NS2; seg men 8). Tabel 1 menunjukkan fungsi dari 10 protein yang dihasilkan oleh virus influenza A. Semua virus Influenza mempunyai komponen internal (PB1, PB2, PA, NP, M1 dan NS) yang serupa, tetapi komponen amplopnya sangat bervariasi (Whittaker 2005).
Tabel 1 Fungsi protein dari virus influenza A
PROTEIN FUNGSI
PB1 Transkrip tase
PB2 Endonuklease
PA Replikasi RNA virus ; aktivitas proteolitik
HA (Hemaglutinin) Attachment virus pada reseptor sel inang ; fusi amplop virus ; netralisasi virus berperantara antibodi NP (Nukleoprotein) Transport RNP virus dari sitoplasma ke inti ;
sintesis RNA virus full legth ; target bagi limfosit T sitotoksik
NA (Neurominidase) Enzim yang melepaskan ikatan v irus dengan reseptor sel inang; netralisasi virus berperantara antibodi M1 (Matrix 1) Berperan dalam proses budding ; mencegah RNP
virus kembali ke inti M2 (Matriks 2) Ion channel
NS1 (Non Struktural 1) Menghambat proses mRNA sel inang ; meningkatkan translasi RNA virus ; menghambat interferon pathways
NS 2 (Non struktural 2) Keluar dari inti
memperlihatkan gejala klinis. Angka kematian hewan yang terinfeksi virus LPAI sangat kecil bila tidak terjadi infeksi sekunder. Beberapa strain LPAI mampu bermutasi dibawah kondisi lapang menjadi virus HPAI. Virus HPAI bersifat sangat infeksius dan fatal pada unggas dan dapat menyebabkan kematian hingga 90 sampai 100% dalam waktu yang cepat dengan atau tanpa memperlihatkan gejala klinis, dan ketika ini terjadi, maka penyakit dapat menyebar dengan cepat antar flock (Swayne dan Suarez 2003).
Pada bulan April 1983 di Pennsylvania, USA terjadi wabah AI yang disebabkan oleh virus LPAI subtipe H5N2 dengan angka kematian antara 0 sampai 15%. Namun demikian pada bulan Oktober 1983 wabah tersebut menjadi HPAI dengan angka kematian sangat tinggi. Hasil tes laboratorium mengidentifikasi bahwa wabah tersebut disebabkan oleh virus HPAI, subtipe H5N2 sebagai hasil mutasi dari virus LPAI. Demikian juga wabah AI di Meksik o pada tahun 1994 diawali dengan LPAI, kemudian mutasi menjadi HPAI yang menimbulkan angka kematian tinggi dan disebabkan oleh virus AI subtipe H5N2 (Li 2005 ). Dengan demikian potensi terjadinya mutasi dari virus LPAI menjadi HPAI atau sebaliknya yang masih dalam satu subtipe sangat mungkin terjadi pada virus AI.
Unggas yang menderita AI dapat mengeluarkan virus dengan jumlah yang besar dalam kotorannya. Virus tersebut dapat bertahan hidup di air sampai 4 hari pada suhu 22 0C dan lebih dari 30 hari dalam suhu 30 0C. Di dalam tinja unggas dan dalam tubuh unggas yang sakit dapat bertahan lebih lama, tetapi akan mati pada pemanasan 60 0C selama 30 menit (Soejoedono dan Handharyani 2005).
Prevalensi Avian Influenza
Prevalensi subtipe virus AI pada unggas bervariasi tergantung umur, musim dan spesies . Umur merupakan faktor utama penentu infeksi oleh virus AI. Prevalensi infeksi virus AI lebih tinggi terjadi pada unggas usia muda dari pada unggas dewasa terutama pada musim panas dan semi (Weaver 2005).
2.4% dari sampel, H9 0.9%, dan virus AI selain H5 dan H9 sebanyak 2.7% (Shortridge 1997). Pada pasar ternak di Nanchang, Cina pada tahun 2000 menunjukkan virus AI ditemukan hanya pada 1% dari 6360 sampel, virus paling banyak dijumpai pada itik (1.3%), ayam (1.2%), puyuh (0.8%) dan merpati (0.5%) (Liu et al. 2003).
Penelitian tentang keb eradaan virus AI pada itik di Maryland Amerika Serikat tahun 1998 menunjukkan bahwa virus hanya dapat ditemukan pada itik pada periode yang sangat singkat yaitu dari pertengahan Juli sampai akhir Agustus. Subtipe virus yang diisolasi adalah H2, H3, H6, H9, dan H12 sebanyak 13.9% dari 209 sampel usap klo aka (Slemonts et al. 2003). Prevalensi virus HPAI H5 (0.4%), H7 (0.7%) dan H9 (0.4%) lebih kecil jika dibandingkan dengan virus H3, H4, dan H6 yang mencapai 63.8% (Weaver 2005).
Phuong (2005) berhasil mengisolasi virus AI subtipe H12 dari 587 usap kloaka yang berasal dari pasar unggas di Propinsi Thai binh, Vietnam. Namun keberadaan antibodi terhadap H5, H3 dan H12 ditemukan dengan prevalensi yang tinggi. Prevalensi antibodi terhadap H5 paling tinggi dijumpai pada itik yang mencapai 77.63%.
Avian Influenza di Propinsi Lampung
bulan Mei 2005 menunjukkan hasil yang negatif terhadap virus AI (Dinas Peternakan dan Kesehatan Hewan Propinsi Lampung 2006).
Virus Avian Influenza pada Unggas Air
Unggas air terutama yan g termasuk dalam orde Anseriformis (bebek dan angsa) dan Caridiformis (burung camar dan burung-burung pantai) merupakan inang alami dari semua subtipe virus influenza A. Beberapa spesies unggas domestik seperti ayam, kalkun, puyuh dan merak rentan terhadap infeksi dari virus Avian Influenza. Virus Influenza A biasanya tidak menimbulkan penyakit pada inang alami, dimana pada hewan tersebut virus berada dalam keadaan seimbang dan tidak menimbulkan penyakit (Webster 1992; Fouchier 2003). Virus bereplikasi di gastrointestinal itik, sehingga shedding virus bersama feses ditransmisikan ke unggas atau mamalia lain melalui fecal-oral (Sturm-Ramirez et al. 2004). Secara periodik virus influenza disebarkan ke inang lain, termasuk mamalia, dan menyebabkan infeksi yang sifatnya sementara dan kadang-kadang menimbulkan kematian. Jarang sekali, virus influenza ditularkan ke spesies lain dan menimbulkan infeksi terus-menerus yang permanen pada inang tersebut. Namun demikian, infeksi permanen dari virus influenza dapat terjadi pada manusia, babi, kuda dan unggas domestik (Nguyen et al. 2005).
Virus H5N1 pertama kali di deteksi pada unggas air di Hongkong pada November 2002, yang menyebabkan kematian pada angsa (Sturm-Ramirez et al. 2004). Namun HPAI H5N1 juga dapat diisolasi dari itik yang sehat di Cin a dari tahun 1999 sampai 2002 (Chen et al. 2004). Penelitian menunjukkan bahwa 15% itik dan 2% angsa merupakan reservoir virus AI, selain unggas air, burung liar juga dilaporkan sebagai reservoir virus AI (Khawaja et al. 2005).
Pada bulan Mei 2001, virus Avian Influenza diisolasi dari daging itik yang diimport oleh Korea Selatan dari Cina. Berdasarkan analis a filogeni pada gen HA-nya menunjukkan bahwa virus tersebut satu cluster dengan H5 Goose/Guandong/1/96 dan memiliki urutan basa yang identik pada HA cleavage site-nya dengan virus yang diisolasi pada manusia di Hong Kong tahun 1997 (Tumpey et al. 2002). Itik yang terinfeksi oleh virus AI biasanya akan mengeluarkan virus dalam jumlah besar pada feses, sekresi hidung, dan salivanya. Shedding virus terjadi dalam 2 minggu post infeksi. Puncak shedding biasanya terjadi sesudah hari ke-3 post infeksi (WHO 2006). Dari beberapa isolat virus H5N1 yang diinokulasi pada itik, walaupun itik tidak menunjukkan gejala klinis namun virus dapat dideteksi pada paru-paru pada hari ke-2 dan ke-4 post infeksi, usap kloaka (sesudah hari ke 5 post infeksi) dan usap orofaring pada hari ke 2 post infeksi. Isolat DK/Anyang /AVL-1/01 dapat juga did eteksi pada otot dan otak itik (Tumpey et al. 2002).
Faktor Virulensi Virus AI
Faktor virulen virus AI yang paling berperan adalah hemaglutinin (HA) yang tersusun dari 560 asam amino. Asam amino yang menyusun regio cleavage site sangat menentukan keganasan virus ini. Virus HPAI memiliki multi basic amino acid (arginin dan lisin) pada cleavage site-nya sedangkan virus avirulen hanya memiliki arginin tunggal (Whittaker 2005; Capua et al. 2004).
Perjalanan Virus Influenza Intraseluler
Tipe sel target dari virus influenza adalah sel-sel pada lapisan epitel mukosa saluran pernafasan, yang merupakan epitel yang terpolarisasi (memiliki permukaan apikal dan basoleteral). Virus yang terhirup dari udara akan masuk sel epitel saluran pernafasan dari permukaan apikal. Setelah bereplikasi pada sel virus dapat dikeluarkan melalui permukaan apikal sel, hal ini yang dapat menyebabkan penyebaran virus ke individu lain. Namun virus juga dapat menembus permukaan basolateral sel dan menyebabkan penyebaran secara sistemik dari sel ke sel (Whittaker 2005).
Pada saat viru s masuk ke tubuh inang, virus mengawali perlekatannya ke reseptor pada permukaan sel. Virus influenza pada manusia akan melekat pada bagian yang mengandung 5-N-acetyl neurominic acid (asam sialik) pada permukaan sel inang, namun pada babi dan kuda N-glycolyl neurominic acid dapat digunakan. Beberapa virus lebih menyukai menempel pada terminal asam sialik yang berisi α-(2,6), dan yang lainnya lebih menyukai melekat pada asam sialik α-(2,3) (Chu dan Whittaker 2004). Spesifisitas perlekatan reseptor berhubungan dengan asam amino spesifik pada posisi 226 pada HA. HA yang memiliki leusin pada posisi 226 secara selektif melekat ke α-(2,6) asam sialik, dan terjadi paling banyak pada strain manusia. Namun HA yang mempunyai glutamin pada posisi 226, spesifik untuk α-(2,3) asam sialik, dan terjadi hampir sebagin besar pada strain unggas dan kuda (Zhou et al. 1999). Baik asam sialik yang berhubungan dengan α-(2,6) dan α-(2,3) terdapat pada trakhea babi, yang menyebabkan babi dapat diinfeksi dengan strain manusia dan strain unggas (Whittaker 2005) dan berperan sebagai “ mixing vessel” untuk transmisi dari unggas ke manusia (Webster et al. 1992). Informasi terakhir manyatakan bahwa babi bukanlah satu-satunya hewan yang memiliki kedua reseptor tersebut, burung puyuh dan ayam juga memiliki reseptor α-(2,6) dan α-(2,3). Hal ini memungkinkan burung puyuh dan ayam dapat juga berfungsi sebagai “ mixing vessel” virus influenza strain manusia dan unggas (Wan dan Perez 2005).
dan melakukan uncoating. Ribonukleoprotein (RNP) virus yang sudah uncoating kemudian masuk ke inti dari sel inang untuk melakukan replikasi, Sesudah replikasi virus, ribonukleoprotein meninggalkan inti dan pindah ke membran sitoplasma bergabung dengan glikoprotein virus sebelum akhirnya budding dan dilepaskan. Pelepasan virus dari permukaan sel terinfeksi didasarkan pada aktivitasi dari NA virus. NA (sialidase) berperan sebagai enzim yang merusak reseptor, dengan memindahkan asam sialik dari permukaan sel inang. Tanpa tahapan ini partikel virus yang baru dibentuk akan kembali melekat pada reseptornya dan tidak dapat dilepaskan ke ekstraseluler (Gambar 4) (Whittaker 2005).
Penularan Virus Avian Influenza
Virus AI dapat menyebar dengan cepat diantara populasi unggas, namun penularan virus AI dari unggas ke unggas lain dapat dipengaruhi oleh banyak faktor yaitu, strain virus, strain unggas, dan faktor lingkungan (Wetsbury at al. 1981). Sumber penularan virus AI adalah ekskreta yang berasal dari hidung, mulut, dan konjungtiva serta feses unggas yang menderita. Virus AI dikeluarkan dari hidung, konjungtiva, dan kloaka unggas yang terinfeksi ke lingkungan karena virus bereplikasi di saluran pernafasan, pencernaan, ginjal, dan/atau organ reproduksi (Swayne dan Suarez 2000). Namun bahan-bahan lain seperti litter, pakan, air minum, peralatan, atau kendaraan yang tercemar virus AI dapat menjadi sumber penularan virus tersebut.
Penularan virus AI dapat terjadi secara langsung dan tidak langsung. Penularan secara langsung terjadi melalui kontak antara unggas yang peka dengan unggas yang terinfeksi virus AI melalui pernafasan. Penularan virus secara tidak langsung dapat terjadi secara oral melalui pakan dan air minum yang terc emar oleh virus AI (Soejoedono dan Handharyani 2005).
Air danau atau sungai dapat juga menjadi sumber virus AI. Menurut Web ster et al. (1978), itik yang terinfeksi AI dapat mencemari air danau dengan mengeluarkan virus lebih dari 108.7 EID per gram feses. Berdasarkan hasil observasi kasus AI di Vietnam pada tahun 2004, munculnya wabah AI terjadi pada Propinsi yang memiliki banyak populasi itik seperti di Long An, Tien Giang, dan Vietnam Selatan. Pemeliharaan berbagai spesies unggas domestik secara bersama-sama serta kesulitan dalam melakukan kontrol terhadap burung migrasi merupakan faktor utama munculnya wabah AI di Vietnam pada tahun 2004 (Phuong 2005).
Gejala Klinis AI pada Unggas
Masa inkubasi virus AI berlangsung beberapa jam sampai 3 hari. Masa inkubasi virus AI tergantung pada jumlah virus, subtipe virus dan spesies unggas yang terserang (Elbers et al. 2005). Sebagian besar infeksi oleh virus AI (LPAI) pada unggas liar tidak menimbulkan gejala klinis (Capua dan Mutinelli 2001). Berdasarkan hasil penelitian pada itik mallard infeksi oleh virus LPAI akan menekan fungsi sel T dan menyebabkan penurunan produksi telur (Takizawa et al. 1995). Pada unggas-unggas domestik seperti ayam dan kalkun, gejala klinis yang dapat diamati berupa bersin, batuk serta produksi air mata yang berlebihan . Namun beberapa strain LPAI separti H9N2, dapat beradaptasi pada unggas dan dapat menimbulkan gejala yang lebih nyata dan juga mengakibatkan kematian (Li 2005). Infeksi LPAI H7N1 tahun 1999 di Italia yang menyerang peternakan kalkun menimbulkan gejala klinis seperti batuk, bersin, kebengkakan pada sinus infraorbitalis, menurunnya produksi telur (30% sampai 80%) serta kematian 5% sampai 20% dari populasi (Capua et al. 2003).
Infeksi oleh Virus AI yang patogenitasnya tinggi (HPAI) pada burung dan unggas air hanya menyebabkan sedikit gejala klinis. Hal ini disebabkan karena pada spesies hewan tersebut replikasi virus menjadi terbatas (Swayne dan Halvorson dalam Phuong 2005). Pada unggas domestik seperti ayam dan kalkun, gejala klinis yang ditimbulkan oleh infeksi virus HPAI menggambarkan replikasi virus dan kerusakan pada berbagai organ pencernaan, jantung dan pembuluh darah serta sistem syaraf. Gejala klinis yang dapat diamati berupa jengger dan pial yang berwarna biru keunguan, pembengkakan disekitar kepala dan muka, cairan yang keluar dari hidung dan mata, pendarahan titik (ptechie) pada daerah dada, kaki dan telapak kaki, batuk, bersin , dan ngorok (Soejoedono dan Handharyani 2005).
Perubahan Patologis Anatomis
yang kadang -kadang disertai dengan ptechie pada konjungtiva, dapat ditemukan eksudat (serues sampai kaseus) pada trakhea, serta airsacculitis yang bersifat fibrinous sampai fibrinopurulen (Swayne dan Halvorson dalam Phuong 2005).
Pada infeksi HPAI dapat ditemukan berbagai perubahan patologis anatomis. Pada ayam dapat ditemukan kebengkakan pada kepala, wajah, leher bagian atas, dan kaki sebagai akibat dari adanya edema subkutan yang dapat diikuti dengan ptechie sampai hemoragi. Fokal nekrotik, hemoragi dan sianosis juga dapat dijumpai pada kulit yang tidak ditumbuhi bulu seperti pada pial dan jengger. Fokal nekrotik juga dapat dijumpai pada pankreas, limpa, dan jantung, dan kadang-kadang juga dijumpai pada ginjal dan hati. Pada paru -paru dapat ditemukan pneumonia interstesialis dan edema (Swayne dan Halvo rson dalam Puong 2005).
Diagnosis Avian Influenza
Penyakit Avian Infuenza memberikan gambaran gejala klinis dan perubahan patologik yang bervariasi, oleh karena itu diagnosa definitif dari penyakit ini didasarkan atas isolasi dan identifikasi virus. Pemeriksaan serologis dapat dilakukan untuk mengetahui adanya pembentukan antibodi terhadap virus AI yang dapat diamati pada hari ke-7 sampai hari ke-14 pasca infeksi. Pemerikasaan serologis yang sering digunakan adalah uji Haemagglutination Inhibition (HI) untuk mengetahui keberadaan antibodi terhadap hemaglutinin. Seekor ayam dapat dinyatakan kebal terhadap penyakit AI jika memiliki titer antibodi HI serendah-rendahnya 4 (log2) (D arminto 2006). Selain untuk mengetahui keberadaan antibodi terhadap hemaglutinin, uji HI juga dapat digunakan untuk identifikasi HA dari virus AI dengan menggunakan serangkaian antibodi terhadap 16 subtipe HA (Lee et al. 2001). Namun sekarang sudah dikembangkan suatu teknik yang cepat dan akurat untuk identifikasi virus AI yaitu dengan Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR) (WHO 2003; OIE 2005)
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan November 2005 sampai Juli 2006. Pengambilan sampel lapangan dilaksanakan pada bulan November 2005 sampai Januari 2006, dan pemeriksaan laboratorium dilaksanakan pada bulan Februari sampai Juli 2006 di Laboratorium Terpadu, Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat (IPHK), Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Metode Penelitian Pengumpulan Sampel
Sampel usap kloaka (cloacal swab) dan darah (serum) diperoleh dari unggas air (itik, entok, dan angsa) pada peternakan tradisional yang tidak divaksinasi di 6 kabupaten dan 2 kota di Propinsi Lampung meliputi Kabupaten Lampung Timur, Lampung Utara, Lampung Selatan, Lampung Tengah, Tulang Bawang, Tanggamus, Kota Bandar Lampung dan Metro. Metode pengambilan sampel yang digunakan adalah Multistage sampling. Penentuan lokasi pengambilan sampel dilakukan berdasarkan daerah di Propinsi Lampung yang sudah dinyatakan tertular AI. Media Transport yang digunakan adalah PBS gliserol (WHO 2003). Alur penelitian dapat dilihat pada Lampiran 1.
Uji Serologis
Selanjutnya dilakukan pencampuran serum dengan suspensi virus dengan cara mengambil dan mengeluarkan cairan tersebut dengan mikropipet (paling sedikit 5 kali). Campuran itu dikocok dengan menggoyang-goyangkannya microplate dan kemudian diinkubasikan pada suhu ruang selama 15 menit, dan kemudian ditambahkan 25 µl suspensi sel darah merah ayam 0.5 % ke dalam seluruh sumur. Tahap terakhir dilakukan pengocokan microplate dengan menggoyang-goyangkannya, kemudian diinkubasikan pada suhu ruang selama kurang lebih 30 menit. Pembacaan hasil uji dapat dilakukan apabila eritrosit pada tabung kontrol telah mengendap ke dasar sumur. Sampel dinyatakan positif apabila sel darah merah pada sumur sampel mengendap.
Ekstraksi RNA virus
6 000 g selama 1 menit. Selanjutnya sampel disimpan pada suhu -20 0C atau -70 0C sampai akan digunakan.
Amplifikasi Gen Virus dengan RT-PCR
Amplifikasi gen virus dilakukan dengan teknik Reverse Transcriptase – Polymerase Chain Reaction menggunakan GeneAmp PCR System 9700. Pada penelitian ini digunakan primer HAR, HA-1144F, dan H5-1735R (WHO 2003) serta primer CU-N1F dan CU-N1R (Payungporn et al. 2004) dengan urutan basa sbb :
RT-PCR dilakukan dengan SuperScriptTM III One-Step RT-PCR System dengan Platinum Taq (Invitrogen). Reaksi RT-PCR dibuat sebanyak 50 µl dengan komposisi : 25 µl 2X Reaction Mix, pasangan primer masing -masing (10 µM) 1 µl, 2 µl Superscript III RT/Platinum Taq Mix, 3 µl sampel RNA, dan distilated water RNAsefree hingga volume 50 µl. Program RT-PCR yang digunakan adalah sebagai berikut 45 oC selama 60 menit (reverse transcription), 94 oC selama 5 menit (predenaturasi) dan kemudian 94 oC selama 30 detik (denaturasi), 54 oC selama 1 menit (annealing), 68 oC selama 1 menit (ekstensi). Siklus amplifikasi yang digunakan adalah 40 siklus dan selanjutnya 68 oC selama 5 menit (ekstensi final).
Analisa DNA Hasil RT-PCR pada Agarose Gel Elektroforesis 1.5 %
HASIL DAN PEMBAHASAN
Pada penelitian ini jenis sampel diambil berupa serum dan usap kloaka yang diperoleh dari unggas air yang belum pernah mendapat vaksinasi AI dan dipelihara bersama dengan unggas lain (ayam). Unggas air (waterfowl) adalah anggota dari ordo Anseriformes seperti, itik, entok dan angsa yang dapat hidup baik di air maupun di darat (Blood dan Studdert 1988). Unggas air merupakan reservoir semua subtipe virus Influenza A, tetapi infeksi pada spesies ini secara umum tidak menunjukkan gejala klinis, namun unggas air dapat menularkan virus ke ayam dan menyebabkan akibat yang fatal (Tumpey et al. 2002).
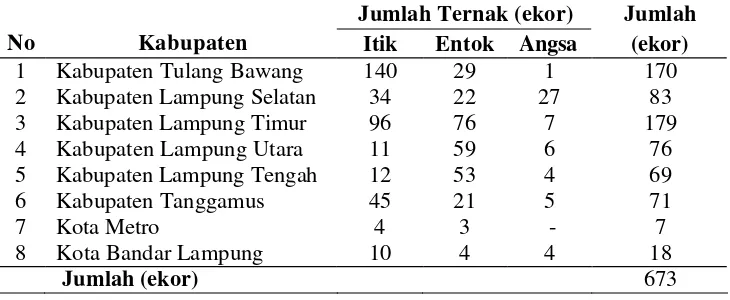
Sampel usap kloaka dan serum yang digunakan pada penelitian ini masing-masing berjumlah 673 yang terdiri dari 352 sampel itik, 267 sampel entok dan 54 sampel angsa. Sampel unggas air d iperoleh dari 8 daerah tertular AI di Propinsi Lampung dengan distribusi jumlah sampel pada tiap- tiap dae rah dapat dilihat pada Tabel 2.
Tabel 2 Distribusi jumlah sampel pada tiap kabupaten/kota di Propinsi Lampung Jumlah Ternak (ekor) Jumlah
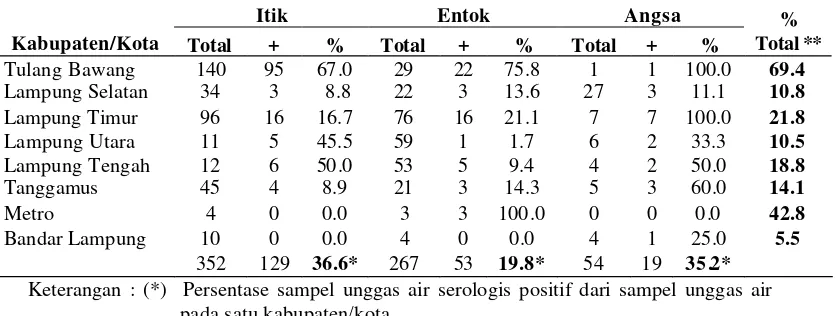
sampel serum yang diperoleh. Uji mikrotiter HI bertujuan untuk mengetahui titer antibodi pada serum yang diuji, dan selanjutnya dapat digunakan untuk mengetahui rata-rata titer antibodi pada suatu populasi. Hasil uji HI cepat juga digunakan untuk menentukan/mengelompokkan sampel yang berupa usap kloaka menjadi kelompok HI positif (seropositif) dan kelompok HI negatif (seronegatif). Dari uji HI cepat didapatkan hasil keberadaan antibodi terhadap H5 pada unggas air di Kabupaten Tulang Bawang adalah itik (67%), entok (75.86%) dan angsa (100%); untuk Kabupaten Lampung Selatan, itik (8.82%), entok (13.63%) dan angsa (11.11); untuk Kabupaten Lampung Timur, itik (16.67%), entok (21.05%) dan angsa (100%); untuk Kabupaten Lampung Utara, itik (45.45%), entok (1.69%) dan angsa (33.33%); untuk Kabupaten Lampung Lampung Tengah, itik (50%), entok (9.43%) dan angsa (50%); untuk Kabupaten Tanggamus, itik (8.88%), entok (14.28%), dan angsa (60%); untuk Kota Metro, itik (0%), entok (100%), dan angsa (0%); untuk Kota Bandar Lampung, itik (0%), entok (0%), dan angsa (25%) (Tabel 3).
Persentase keberadaan antibodi terhadap H5 berdasarkan wilayah, yang paling tinggi terdapat di Kabupaten Tulang Bawang yaitu 69.41%. Hal ini menunjukkan bahwa unggas air yang telah terpapar oleh virus AI (H5) pada daerah tersebut lebih banyak dibandingkan dengan 7 kabupaten/kota lainnya di Propinsi Lampung. Kabupaten Tulang Bawang merupakan tempat pertama kali kasus AI ditemukan d i Propinsi Lampung yaitu pada bulan September 2003 (Dinas Peternakan dan Kesehatan Hewan Propinsi Lampung 2006). Berdasarkan data dari Kajian Seroepidemiologi Penyakit Avian Influenza serta Strategi Penanggulangannya di Sumatra dan Kalimantan (2005), keberadan antibodi terhadap H5 pada ayam kampung di Kabupaten Tulang Bawang paling tinggi diantara 7 daerah lainnya yaitu 57.29%, berarti adanya hubungan yang berbanding lurus pada antibodi terhadap H5 antara unggas air dan ayam kampung. Berdasarkan hasil observasi kasus AI di Vietnam pada tahun 2004, munculnya wabah AI terjadi pada Propinsi yang memiliki banyak populasi itik seperti di Long An, Tien Giang, dan Vietnam Selatan (Phuong 2005).
35.18% dan 19.85%. (Tabel 3). Hasil uji serologis tersebut mengindikasikan bahwa kelompok unggas tersebut pernah kontak dengan virus AI walaupun hewan tersebut tidak harus menunjukkan gejala klinis (sakit). Hasil ini akan lebih bermakna dan dapat digunakan sebagai indikator adanya infeksi AI, apabila dilakukan uji serologis ulangan yang dilakukan 3 minggu setelah uji pertama (WHO 2003).
Tabel 3 Distribusi hasil serologis menurut wilayah dan jenis ternak
Itik Entok Angsa
Keterangan : (*) Persentase sampel unggas air serologis positif dari sampel unggas air pada satu kabupaten/kota
(**) Persentase sampel jenis unggas air tertentu serologis positif dari seluruh sampel unggas air sejenis di Propinsi Lampung
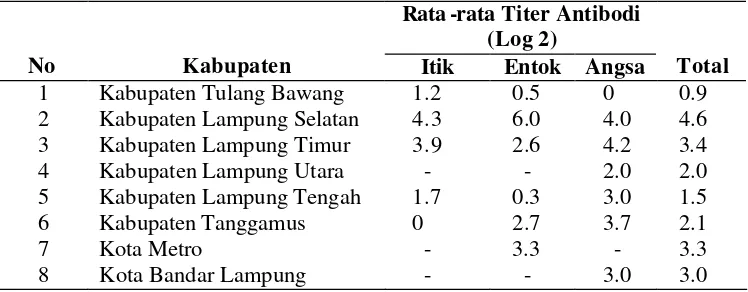
AI. Seekor ayam dapat dinyatakan kebal terhadap penyakit AI jika memiliki titer antibodi HI serendah-rendahnya 4 (log 2) (Darminto 2006). Dari hasil uji mikrotiter HI juga banyak ditemukan sampel yang positif HI cepat tetapi nilai titernya hanya 20. Hal ini disebabkan karena kandungan antibodi pada sampel serum tersebut sangat sedikit sekali. Pada penelitian ini virus standar yang dugunakan 4 HAU (setara dengan 4 x 106 partikel virus), jika antibodi yang ada pada serum tidak dapat menetralisir semua virus standar, maka virus yang tidak ternetralisasi akan mengaglutinasi sel darah merah sehingga pada sumur tersebut kita tetap akan menemukan sel darah merah yang teraglutinasi.
Tabel 4 Nilai Rata-rata Titer Antibodi terhadap H5 Virus Avian Influenza Rata -rata Titer Antibodi
Deteksi Virus AI (H5N1) dengan RT-PCR
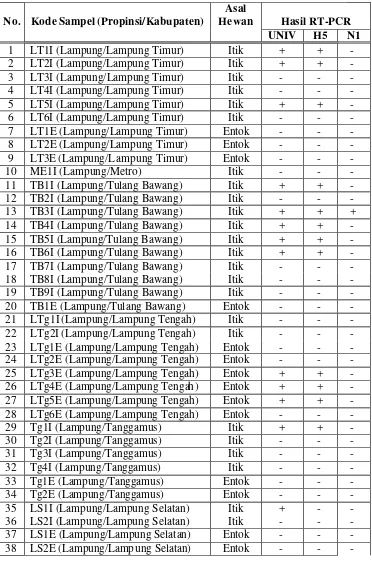
Dari hasil uji serologis dapat diperoleh sebanyak 201 sampel HI positif dan 472 sampel yang HI negatif. Sampel usap kloaka, baik yang berasal dari HI positif dan HI negatif masing-masing di pool 10 sampai 11 sampel untuk diuji keberadaan materi genetik virus AI (H5N1) pada sampel tersebut. Sehingga diperoleh 64 pool yang terdiri dari 19 pool HI positif dan 45 pool HI negatif.
Sampel usap kloaka yang berasal dari unggas air yang menunjukkan reaksi HI positif dan HI negatif d igunakan untuk mendeteksi keberadaan virus AI (H5N1). Deteksi dilakukan dengan teknik RT-PCR terhadap gen HA, H5 dan N1 dengan menggunakan rancangan primer HAR dan HA-1144F, HA-1144F dan H5-1735R , CU-N1F dan CU-N1R. Keberadaan virus AI (H5N1) dalam sampel akan ditunjukan dengan adanya pita fragmen yang berukuran ~600 bp untuk gen HA (universal), ~591 bp untuk gen H5 , dan ~131 bp untuk gen N1. Deteksi virus AI dilakukan secara bertahap, dari deteksi gen HA (universal), dan apabila menunjukk an reaksi yang positif maka dilanjutkan dengan penentuan subtipe dengan deteksi gen H5 dan N1.
Dari 19 pool sample yang HI positif diperoleh 14 pool yang positif RT-PCR terhadap gen HA, dan dari 14 pool yang positif HA tersebut hanya 1 pool yang menunjukkan reaksi RT-PCR yang negatif terhadap gen H5 (Tabel 5). Sampel dari HI positif dan RT-PCR positif gen H5 virus AI ditemukan pada jenis unggas itik, entok, dan angsa dari pool sampel yang berasal dari 7 kabupaten/kota di Propinsi Lampung (kecuali Metro) (Tabel 5). Hasil RT-PCR dapat dilihat pada Gambar 5 dan 6.
Tidak ditemukannya reaksi positif RT-PCR pada sebagian sampel unggas air yang HI positif dapat disebabkan oleh beberapa hal antara lain, 1) antibodi yang ada sebagai akibat unggas pernah terpapar dengan virus AI dan tidak menimbulkan sakit, atau terpapar virus pada waktu yang sudah lama sehingga virus tidak ditemukan lagi dalam feses, 2) jumlah virus yang ada pada usap kloaka sangat kecil sehingga tidak terdeteksi pada saat melakukan uji RT-PCR. Menurut Tumpey (2002), virus AI dapat ditemukan pada kloaka 1 minggu post infeksi, namun sangat sedikit virus yang dapat ditemukan dari usap kloaka.
Untuk diketahui dengan pasti urutan nukleotida pada daerah yang dapat teramplifikasi oleh primer spesifik tersebut perlu dilakukan sequensing terhadap sampel tersebut.
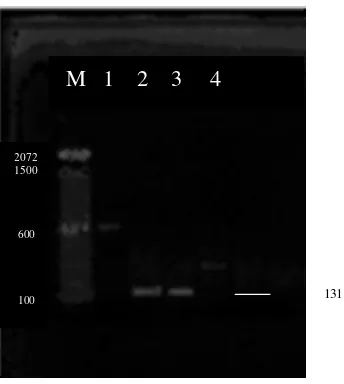
Gambar 5 Contoh hasil RT-PCR dielektroforesis pada gel agarose 1.5%, diwarnai dengan ethidium bromida. Hasil Positif ditunjukkan dengan adanya pita hasil amplifikasi fragmen gen HA sebesar ~600bp. M= Marker, 1: kontrol positif (HA), 2: swab entok Lampung Timur, 3 : swab itik Lampung Timur, 4: swab itik Lampung Utara.
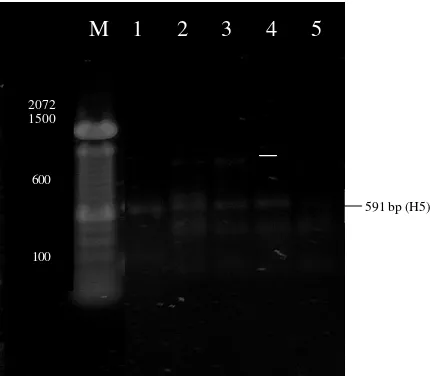
Gambar 6 Contoh hasil RT-PCR dielektroforesis pada gel agarose 1.5%, diwarnai dengan ethidium bromida. Hasil Positif ditunjukkan dengan adanya pita hasil amplifikasi fragmen gen H5 sebesar ~591bp. M= Marker, 1: kontrol positif (H5), 2: swab entok Lampung Timur, 3 : swab itik Lampung Timur, 4: swab itik Lampung Utara.
M 1 2 3 4 5
M 1 2 3 4 5
2072 1500
600
100
600 bp (HA)
2072 1500
600
100
Dari 45 pool sampel usap kloaka yang HI negatif, terdapat 13 pool yang menunjukkan reaksi RT-PCR positif terhadap gen HA, dan dari 13 pool yang positif HA terdapat 1 pool yang negatif H5 (Lampiran 2). Ditemukannya materi genetik AI pada unggas yang HI negatif dapat disebabkan oleh beberapa hal antara lain, 1) materi genetik dari virus AI dapat dijumpai pada unggas sehat dan tidak harus menunjukkan respon pembentukan antibodi spesifik, sehingga hewan sehat potensial sebagai reservoir virus AI, 2) Awal infeksi. Dimana pada tahap ini belum terb entuk antibodi atau masih dalam jumlah yang sedikit. Menurut Bellanti (1993), antibodi dapat dideteksi empat sampai lima hari sesudah infeksi.
Sampel yang menunjukkan hasil RT-PCR terhadap HA yang positif tetapi negatif terhadap gen H5 menunjukkan bahwa unggas tersebut terinfeksi atau terpapar oleh virus AI selain subtipe H5. Unggas air dan burung pantai merupakan reservoir untuk semua subtipe HA, tetapi infeksi pada spesies ini biasanya tidak menimbulkan gejala klinis (Tumpey et al. 2002). Balitvet (Balai Penelitian Veteriner) pernah mengisolasi virus Influenza A dari itik dan berbagai jenis burung, namun semua isolat yang diperoleh pada saat itu semuanya tergolong LPAI dengan subtipe H4N2 dan H4N6 (Ronohardjo diacu dalam Darminto 2006).
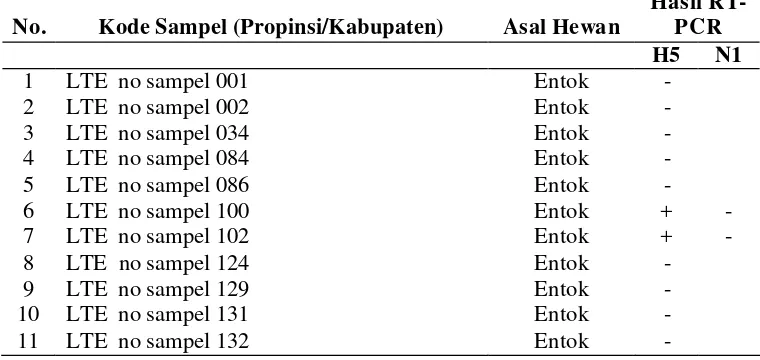
Dari pool yang menunjukkan reaksi positif secara konsisten terhadap gen HA dan H5 dilanjutkan RT-PCR terhadap gen N1. Dari 13 pool yang HI positif dan menunjukkan reaksi positif terhadap gen HA dan H5, hanya ditemukan 1 pool yang positif terhadap N1 (Tabel 6). Hasil RT-PCR yang menunjukkan hasil positif gen H5N1 dilihat pada Gambar 7. Hasil N1 yang negatif pada pool yang positif gen HA dan H5 menunjukkan bahwa adanya H5 selain N1 yang terdapat pada unggas air tersebut. Pada pool yang menunjukkan hasil RT-PCR yang konsisten terhadap gen HA, H5, dan N1, dilanjutkan dengan pemeriksaan sampel secara individu terhadap gen H5 dan N1 (Tabel 6).
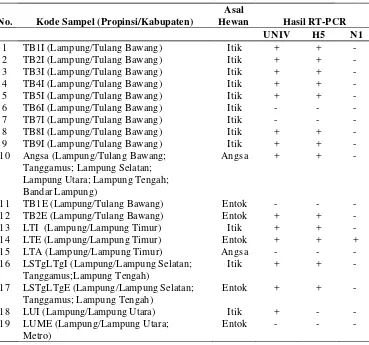
Tabel 6 Hasil pemeriksaan material genetik dengan RT-PCR pada sampel serologis positif pool 14 secara individu
No. Kode Sampel (Propinsi/Kabupaten) Asal Hewan
Hasil
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian tentang deteksi keberadaan virus avian influenza pada unggas air di Propinsi Lampung disimpulkan :
1 Antibodi terhadap H5 virus Avian Influenza ditemukan pada semua jenis unggas air di 8 kabupaten/kota di Propinsi Lampung.
2 Materi genetik virus Avian Influenza (H5N1) tidak ditemukan pada sampel unggas air di Propinsi Lampung.
3 Materi genetik virus Avian Influenza H5Nx dan HxN1 ditemukan pada unggas air di Propinsi Lampung.
Saran
1 Perlu dilakukan penelitian lebih lanjut mengenai keberadaan virus Avian Influenza selain subtipe H5N1 pada unggas Air .
DAFTAR PUSTAKA
[Anonim] 2005. Antigenic Drift and Antigenic Shift. http://www.niaid.gov/antigenic_drift-shift.html [15-10-2005]
Bellanti JA. 1993. Imunologi III. Waholo AS penerjemah; Soeripto N editor. Gadjah Mada University Press. Terjemahan dari : Immunology III. Blood DC, Studdert VP. 1998. Bailliere’s Comprehensive Veterinary Dictionary.
Bailliere Tindall. Philadelphia.
Capua I et al. 1999. Outbreaks of highly pathogenic avian influenza (H5N2) in Italy during October 1997 to January 1998. Avian Pathol 28: 455-460. Capua I, Alexander DJ, 2004. Review article avian influenza: Recent
developments.http://www.scielo.br/pdf/jpbneu/v31n5/en_27161 [07-02-2006]
Capua I, Mutinelli F. Low pathogenicity (LPAI) and highly pathogenic (HPAI) avian influenza in turkeys and chicken. Avian Pathol 29: 537-543.
Capua I, Marangon S, Pozza MD, Terregino C, Cattoli G. 2003. Avian influenza in Italy 1997-2001. Avian dis. 47:839-843.
Chen H et al. 2004. The evolution of H5N1 influenza viruses in ducks in southern Chine. PNAS. 101: 10452-10457.
Chu VC, Whittaker GR. 2004. Influenza viruses entry and infection require host cell N -linked glycoprotein. PNAS. 101: 18153-18158.
Cwhaane T. 2006. Bird Flu now is South Africa. http://www.mmegi.bw/2006/July/Friday7/.html [07-5-2006]
Darminto. Mengenal penyakit Flu Burung dan strategi pengendaliannya. http://www.jatim.litbang.go.id/template/prosiding/flu%20burungpdf [07-5-2006]
Daum LT et al. 2002. A rapid, single-step multiplex reverse transcription-PCR assay for detection of human H1N1, H3N2 and B influenza. J Clin Virol 25: 345-350.
Direktorat Jenderal Peternakan. Departemen Pertanian. 2006. Populasi Unggas menurut Propinsi. http://www.deptan.go.id/infoeksekutif/nak/2005/pop-itik.htm. [24-02-2006]
Donatelli et al. 2001. Characterization of H5N2 influenza viruses from Italian poultry. J Gen Virol. 2001: 635-640.
Elbers AR, Koch G, Bouma A. 2005. Performance of clinical signs in poultry for detection of outbreaks during the avian influyenza A (H7N7) epidemic in Netherlands in 2003. Avian pathol 33: 418-422.
Fouchier RA, Munster V, Wallensten A, Bestebroar TM. 2005. Characterization of a novel influenza A virus hemaglu tinin subtype (H16) obtained from black-headed gulls. J Virol. 79: 2814 -2822.
Fouchier RA, Olsen B, Bestebroer TM et al. 2003. Infuenza A virus surveilllance in wild birds in Northern Erophe in 1999 and 2000Avian Dis 47: 857-860.
Horimoto T, Kawaoka Y. 2001. Pandemic th reat posed by avian influenza a viruses. Clinical Microbiology Reviews 14:129-149.
Khawaja JZ, Naeem K, Ahmed Z, Ahmad S. 2005. Surveillance of avian influenza viruses in wild birds in areas adjacent to epicenter of an outbreak in federal capital territory of Pakistan. International Journal of Poultry Science 4: 39-43.
Lee MS, Chang PC, Shien JH, Cheng MC, and Shieh HK. 2001. Identification and subtyping of avian influenza viruses by reverse transcription-PCR. J Virol Methods 97: 13-22.
Lee CW, Swayne DE, Linares JA, Senne DA, Suarez DL. 2005. H5N2 avian influenza outbreak in Texas in 2004 : the first highly pathogenic strain in the United States in 20 years. J Virol 79: 11412-11421.
Lipatov AS et al. 2004. Influenza: Emergence and control. J Virol 78: 8951-8959.
Li Z et al. 2005. Molecular basis of replication of duck H5N1 influenza viruses in a mammalian mouse model. J Virol 76:12078-12086.
Liu M et al. 2003. The quest of influenza A viruses for new host. Avian Dis 47:849-856.
Murphy FA, Gibbs EP, Horzinek MC, Studdert MJ. 1999. Veterinary Virology. Academic Press. San Diego. California.
Munch M, Neilsen LP, Handberg KJ, Jorgensen PH. 2001. Detection and subtyping (H5 and H7) of avian type A influenza virus by reverse transcription-PCR and PCR-ELISA. Arch Virol 146:87 -97.
Nguyen DC et al. 2005. Isolation and characterization of avian influenza viruses, including highly pathogenic H5N1 from poultry in live bird markets in Hanoi, Vietnam, in 2001. J Virol 79: 4201-4212.
Office international des Epizooties (OIE), 2005. Update on avian influenza in animals in Asia (type H5) http://www.oie.int/eng/en.index.htm [07-12-2005]
Payungporn S et al. 2004. Singel step multiplex RT-PCR for influenza A virus subtype H5N1 detection. J Immunol 17: 588-593.
Poddar SK. 2002. Influenza virus types and subtypes detection by single step tube multyplex reverse transcription-polymerase chain reactio n (RT-PCR) and agarose gel electrophoresis. J Virol 99: 63-70.
Puong DQ. 2005. Seroprevalence study on avian influenza in rural poultry of Thaibinh Province and characterization of the environmental survival of the agents involved [Thesis]. Vietnam. Department of Veterinary and Pathobiology. The Royal Veterinary and Agricultural University.
Shortridge KF. 1999. Poultry and the influenza H5N1 outbreak in Hong Kong, 1997: abridged chronology and virus isolation. Vaccine 17:826-829. Slemons RD, Hansen WR, Converse KA, Senne DA. 2003. Type A influenza
virus surveillance in free-flying, non-migratory ducks residing on Eastern Shore Maryland. Avian Dis 47:1107-1110.
Soejoedono RD, Handharyani E. 2005. Flu Burung. Jakarta. Penebar Swadaya. Swayne DE, Suarez LD. 2000. High pathogenic avian influenza. Rev. Sci. Tech.
19: 463-482.
Swayne DE, Suarez DL. 2003. Biology of avian Influenza especially the change of low pathogenicity virus to high pathogenicity. Proc Lathin American Poultry Congres.
Stockton J et al. 1998. Multiplex PCR for typing and subtyping influenza and respiratory syncytial viruses. J Clin Microbiol 36: 2990-2995.
Sturm-Ramirez KM. 2004. Re-emerging H5N1 influenza viruses in Hong Kong in 2002 are highly pathogen ic to ducks. J Virol 78:4892-4901.
Takizawa T, Fukuda R, Miyawaki T, Ohashi K, Nakanishi Y. 1995. Activation of the apoptotic fast antigen-encoding gene upon influenza virus infection involving spontaneously produced beta-interferon. Virology 209:288-296.
Tim AI FKH IPB. 2006. Seroepidemiologi virus avian influenza serta strategi penanggulangannya di Sumatra dan Kalimantan. Laporan Akhir Penelitian Kerjasama Departemen Pertanian dan FKH IPB.
Tumpey TM et al. 2002. Characterization of highly pathogenic H5N1 avian influenza A virus isolated from duck meat. J Virol 76:6344 -6355.
Wan H, Perez DR. 2005. Quail carry sialic acid reseptors compatible with binding of avian and human influenza viruses . http://amadeo.com/lit.php . [07-6-2006]
Weaver T. 2005. Avian influenza surveys in waterfowl part I: The role wild and domestic waterfowl in avian influenza outbreaks in domestic poultry. NAHSS Outlook February 2005 www.aphis.usda.gov/vs/nsu/outlook Webster RG, Bean WJ, Gorman OT, Chambers TM, Kawaoka Y. 1992. Evolution
and ecology of influenza A viruses. Microbiol Rev 56:152-179.
Whittaker GR. Intracellular trafficking of influenza virus : Clinical implications for molecular medecine. http://www.expertreviews.org/ [08-02-2005] [WHO] World Health Organization. 2003. Technical Report Series –
Recommendations for production and control of influenza vaccine (Inactivated).
[WHO] World Health Organization. 2006. Review o f latest available evidence on risks to human health through potential transmission of avian influenza (H5N1) through water and sewage.
Lampiran 1 Alur Penelitian
PENGAMBILAN SAMPEL
Serum Usap Kloaka
Uji HI cepat (+) pool @ 10 sampel
(-) pool @ 10 sampel
Uji mikrotiter HI
(+) PCR Universal (gen HA)
PCR gen H5
(+) PCR gen N1
(+)
Pemeriksaan sampel individu
Lampiran 2
No. Kode Sampel (Propinsi/Kabupaten)
Asal
Hewan Hasil RT-PCR
UNIV H5 N1
39 LSA (Lampung/Lampung Selatan) Angsa - - - 40 LU1I (Lampung/Lampung Utara) Itik - - - 41 LU2I (Lampung/Lampung Utara) Itik - - - 42 LU3I (Lampung/Lampung Utara) Itik - - - 43 LU4I (Lampung/Lampung Utara) Itik - - - 44 BL1I (Lampung/Bandar Lampung) Itik - - - 45 BL1E (Lampung/Bandar Lampung) Entok - - - 46
BLLUTgLTgA (Lampung/Bandar
Lampung; Angsa - - -
Tanggamus; Lampung Tengah;