BAB III
METODE PEMBUATAN
3.1 FORMULA DAN PENIMBANGAN
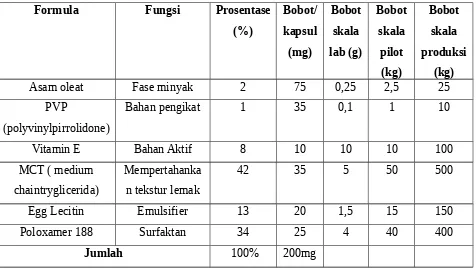
Tabel 3.1 Formula mikroemulsi vitamin E dan Bobot Penimbangan
Formula Fungsi Prosentase
Asam oleat Fase minyak 2 75 0,25 2,5 25
PVP
(polyvinylpirrolidone)
Bahan pengikat 1 35 0,1 1 10
Vitamin E Bahan Aktif 8 10 10 10 100
MCT ( medium chaintryglicerida)
Mempertahanka n tekstur lemak
42 35 5 50 500
Egg Lecitin Emulsifier 13 20 1,5 15 150
Poloxamer 188 Surfaktan 34 25 4 40 400
Jumlah 100% 200mg
Skala lab 1.000 tablet Skala pilot 10.000 tablet Skala produksi 100.000 tablet
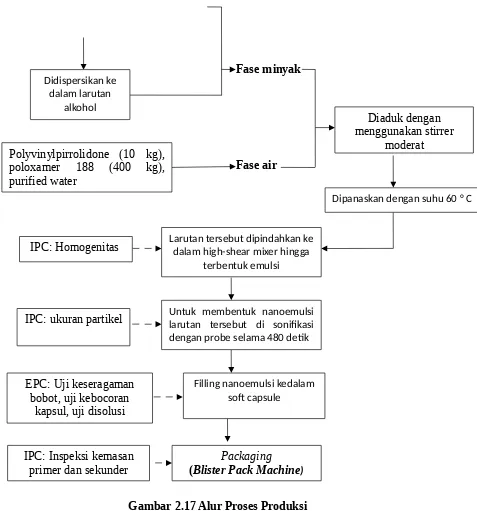
3.2 SKEMA KERJA SKALA PRODUKSI 3.2.1 NANOEMULSION
Fase minyak
Fase air
Gambar 2.17 Alur Proses Produksi
3.3 Pengukuran Ukuran Partikel dan Zeta Potensi Alam
Vitamin E Nanoemulsi Ukuran partikel rata-rata dari vitamin E nanoemulsion diukur dengan analisa partikel (Zetasizer-3000 HSA, Malvern Instrumen, Inggris). Sebelum pengukuran,vitamin E nanoemulsion diencerkan sepuluh kali lipat dengan air purified water. Sampel diencerkan dilakukan pada suhu 25 ° C.
Didispersikan ke dalam larutan
alkohol
Polyvinylpirrolidone (10 kg), poloxamer 188 (400 kg), purified water
Diaduk dengan menggunakan stirrer
moderat
Dipanaskan dengan suhu 60 ° C
Larutan tersebut dipindahkan ke dalam high-shear mixer hingga
terbentuk emulsi IPC: Homogenitas
Untuk membentuk nanoemulsi larutan tersebut di sonifikasi dengan probe selama 480 detik IPC: ukuran partikel
Filling nanoemulsi kedalam soft capsule
Packaging (Blister Pack Machine) EPC: Uji keseragaman
bobot, uji kebocoran kapsul, uji disolusi
Potensi zeta vitamin E nanoemulsion dianalisis menggunakan analisa partikel. Potensial zeta dihitung dari mobilitas elektroforesis oleh persamaan Helmholtz-Smoluchowski. pengukuran,vitamin E nanoemulsion diencerkan sepuluh kali lipat dengan air purified water. Sampel diencerkan dilakukan pada suhu 25 ° C. Pengukuran diulang tiga kali tiap sample.
3.4 Studi Stabilitas Awal
Stabilitas sterilisasi dilakukan dengan memonitor perubahan dalam ukuran partikel, potensial zeta, nilai pH, dan konsentrasi vitamin E nanoemulsion pra dan pasca aliran uap sterilisasi pada 100 ° C selama 30 menit.
Sentrifugasi Stabilitas dilakukan evaluasi dengan pemisahan fasa vitamin E nanoemulsion setelah sentrifugasi pada 4.000 rpm selama 15 menit.
3.5 UJI STABILITAS PRODUK
Stabilitas merupakan kemampuan suatu produk untuk mempertahankan sifat dan karakteristiknya selama waktu penyimpanan dan penggunaan (Departemen Kesehatan RI, 1995). Stabilitas merupakan syarat sediaan bermutu selain aman, efektif, dan dapat diterima. Stabilitas sediaan meliputi stabilitas kimia, stabilitas fisika, stabilitas mikrobiologi, stabilitas farmakologi, dan stabilitas toksikologi (USP 36, 2013). Pada penelitian ini uji stabilitas Softkapsul vitamin E nanoemulsi yang dilakukan seperti yang ada pada Tabel 3.2. Softkapsul Vitamin E nanoemulsi disimpan dalam climatic chamber.
Tabel 3.2 Uji Stabilitas Softkapsul Vitamin E nanoemulsi
Penelitian Kondisi Penyimpanan
24 bulan (12, 18, 24), ditambah bulan ke 36
Waktu dipercepat 40º C ± 2º C RH 75% ± 5%
6 bulan ( 0, 1 , 3, dan 6)
3.3 UJI BIOAVAILABILITAS-BIOEKIVALENSI (BA-BE)
obat yang dibandingkan pada subyek manusia. Karena itu desain dan pelaksanaan studi BE harus mengikuti Pedoman Cara Uji Klinik yang Baik (CUKB) termasuk harus lolos Kaji Etik (BPOM, 2004).
Uji Bioekivalensi (BPOM, 2004)
Desain dan pelaksanaan studi bioekivalensi: 1. Kaji etik
2. Desain
3. Subyek (kriteria seleksi, jumlah subyek, standardisasi kondisi studi, genetik phenotyping)
4. Produk obat uji (Paracetamol ODT) 5. Dosis obat uji
6. Uji disolusi in vitro (UDT)
7. Pengambilan sampel darah (12-18 sampel darah) 8. Kadar yang diukur
9. Metode bioanalitik
10. Parameter bioavailabilitas dari sampel darah (AUCt, AUC∞, Cmax, tmax, t1/2)
11. Analsisi data (analisis statistik, kriteria bioekivalen, catatan untuk bioekivalen individual dan populasi)
Studi Farmakokinetik
Pemilihan Subyek : Tikus laki-laki Sprague Dawley sehat dengan berat 250±10 g, yang dibeli dari Eksperimental Hewan Pusat Cina Farmasi Universitas.
Rancangan Penelitian
Sebelum digunakan penelitian tikus disimpan dalam suhu 250Cdan kelembaban
55-60% yang terkontrol untuk ruang observasi hewan dengan tujuan supaya tikus dapat beradaptasi dengan kondisi laboratotium selama 5 hari. Semua tikus disimpan untuk dipuasakan semalam (selama 24 jam) tetapi memungkinkan diberi asupan air.
Macam Cuplikan dan waktu pengambilan sampel Tikus secara acak dibagi menjadi 3 kelompok yaitu
Masing-masing tikus kelompok nanoemulsi dan kapsul lunak diberikan vitamin-e alami dosis tunggal 40mg/kg. Sekitar 0,5 ml sampel darah dari vena jugularis dimasukkan tabung sampai 1,0 ml untuk disentrifuge dengan rentang waktu 0,5, 1, 1,5, 2, 3, 4, 6, 8, 10, dan 12 jam setelah pemberian oral. Kemudian 0,5 ml sampel darah dikumpulkan dalam tabung sampai 1,0 ml untuk disentrifuge dengan rentang waktu 0,083, 0,25, 0,5, 1, 2, 4, 6, 8, dan 12 jam setelah pemberian intravena. Plasma darah dipisahkan segera dengan sentrifugasi pada 4.000 rpm, selama 15 menit dan disimpan dibawah suhu -200C
sampai sampel dianalisis.
Penentuan Konsentrasi Vitamin-E alami dalam plasma
Semua analisis vitamin E alami dilakukan pada system kromatografi cair kinerja tinggi Shimadzu Promience (HPLC) (Shimadzu, Kyoto, Jepang), yang termasuk unit pengiriman pelarut LC-20A dengan tekanan tinggi katup pilihan flowline, sampler auto SIL -20A, dan kolom oven CTO-20A, terhubung dengan perangkat lunak solusi LC. Vitamin E alami dideteksi menggunakan Waters Symmetry C18 (4,6 mm x 150 mm, 5 mm) kolom terhubung dengan kolom 4,6 × 20 mm guard (Waters, USA), dan suhu dijaga pada 30°C.
Seratus mikroliter (100 µl) sampel plasma deproteinized dengan penambahan 300 ml etil alkohol. Sampel kemudian divortex dicampur selama 2 menit, diikuti dengan penambahan 500 ml heksana. Setelah sentrifugasi selama 10 menit pada 15.000 rpm, supernatan dipindahkan ke vial-botol kaca. Proses ekstraksi heksana diulang. Bagian organik dipisahkan dan diuapkan sampai kering di bawah aliran dari nitrogen pada suhu kamar. Sebelum analisis HPLC residu kemudian dilarutkan dalam 100 ml metanol. Sebuah alikuot (20 µl) sampel diinjeksikan ke dalam kolom HPLC untuk analisis (14, 15).
Analisis Statistik
Untuk perbandingan statistik, semua data dinyatakan sebagai mean ± standar deviasi dan dianalisis untuk perbedaan yang signifikan secara statistik menggunakan uji independent sample T.
Hasil
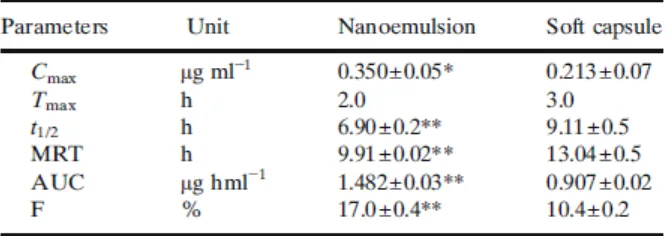
Profil konsentrasi-waktu plasma vitamin E alami pada tikus setelah pemberian oral pada bentuk sediaan dari kedua nanoemulsi dan kapsul lunak yang ditunjukkan pada Gambar. dan parameter farmakokinetik yang dirangkum dalam Tabel. Perbedaan yang nyata antara profil farmakokinetik dari vitamin E alami nanoemulsi dan kapsul lunak. Hasil menunjukkan Cmax yang lebih tinggi dan Tmax pendek untuk pemberian oral dari nanoemulsion dan kapsul lunak. Daerah di bawah kurva (AUC) nilai dari vitamin E alami nanoemulsi dan kapsul lunak yang masing-masing 1,482 ± 0,03 dan 0,907 ± 0,02 mg hml-1. Dengan demikian, ada peningkatan 1,6 kali lipat dalam AUC
alami vitamin E menggunakan teknik emulsifikasi yang dimodifikasi.