PEMANFAATAN KITOSAN SEBAGAI KOAGULAN UNTUK
MEMPEROLEH KEMBALI PROTEIN YANG DIHASILKAN DARI
LIMBAH CAIR INDUSTRI PEMINDANGAN IKAN
DISUSUN OLEH
DEWI MURNIATI (037022001)
SEKOLAH PASCA SARJANA
MAGISTER TEKNIK KIMIA
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMANFAATAN KITOSAN SEBAGAI KOAGULAN UNTUK
MEMPEROLEH KEMBALI PROTEIN YANG DIHASILKAN DARI
LIMBAH CAIR INDUSTRI PEMINDANGAN IKAN
TESIS
Untuk Memperoleh Gelar Magister Teknik
Dalam Program Studi Magister Teknik Kimia
Pada Sekolah Pascasarjana Universitas Sumatera Utara
DEWI MURNIATI
037022001/MTK
SEKOLAH PASCA SARJANA
MAGISTER TEKNIK KIMIA
UNIVERSITAS SUMATERA UTARA
MEDAN
HALAMAN PENGESAHAN
Judul Tesis : PEMANFAATAN KEMBALI PROTEIN YANG
DIHASILKAN DARI LIMBAH CAIR INDUSTRI
PEMINDANGAN IKAN DENGAN MENGGUNAKAN
KITOSAN SEBAGAI KOAGULAN.
Nama Mahasiswa : DEWI MURNIATI
Nomor Pokok : 037022001
Program Studi : Magister Teknik Kimia
Menyetujui,
Komisi Pembimbing:
Prof. DR. Ir. Setiaty Pandia Zuhrina Masyithah, ST, M.Sc Pembimbing Utama Pembimbing Kedua
Mengetahui
Ketua Program Studi Direktur Sekolah Pascasarjana Magister Teknik Kimia Universitas Sumatera Utara
TELAH DIUJI PADA
Tanggal : 5 Oktober 2007
____________________________________________________________________
PANITIA PENGUJI TESIS
Ketua : Prof.DR. Ir. Setiaty Pandia
Anggota : Zuhrina Masyithah, ST, MSc
Prof. DR. Zul Alfian, MSc
DR. Rumondang Bulan, MS
DR. Halimatuddahliana, ST, MSc.
ABSTRAK
Kitosan merupakan kitin yang dihilangkan gugus asetilnya dengan menggunakan basa kuat. Kitosan memiliki banyak kandungan nitrogen daripada kitin. Gugus amina dan hidroksil menjadikan kitosan bersifat lebih aktif dan bersifat polikationik. Sifat tersebut dapat dimanfaatkan sebagai koagulan dalam pengolahan limbah cair industri pemindangan ikan.
Dalam penelitian ini, di kaji proses koagulasi ion organik dalam larutan limbah cair dengan penambahan kitosan sebagai koagulan dengan memvariasikan konsentrasi kitosan dan pH koagulasi.
Penelitian ini menggunakan rancangan acak kelompok faktorial dengan 2 faktor, masing-masing diulang 2 kali yaitu: penambahan dosis kitosan (200, 400, 600, 800, 1000 mg/L) dan pH (4, 5, 6, 7, 8). Penelitian ini dilakukan dengan pengadukan dengan menggunakan magnetic stirrer dan sentrifuse. Setelah ini dilakukan analisa kadar protein, lemak, serat,air, abu dari limbah cair industri pemindangan ikan.
Hasil dari penelitian ini dapat diketahui bahwa dengan penambahan kitosan 1000 mg/L pada pH 7 kedalam limbah cair industri pemindangan ikan dapat mengkoagulasi limbah cair tersebut sehingga didapat kadar proteinnya 50,56%,sedangkan pada penambahan kitosan 800 mg/L dan pH 7 didapat kadar lemaknya 4,75 % , serat 3,08% dan penambahan kitosan 1000 mg/L pada pH 8 didapat kadar airnya 11,87 % dan kadar abu sebesar 6,36 %.
ABSTRACT
Chitosan is chitin which its acetyl group part has been vanished by using strong alkali. Chitosan contens more nitrogen than chitin. Amino and hydroxyl group made chitosan become more active and polycationic. Those nature able to use as coagulant in fish meal processing wastewater industry.
In this research, ion organic coagulation was tested in wastewater with addition of chitosan as coagulant by varied chitosan concentration and coagulation pH. By using factorial random design with 2 (two) factors, when each of The factor repeated twice to : add chitosan dosage (200, 400, 600, 800, 1000 mg/L) and pH (4, 5, 6, 7, 8). This reseach performed by strirring with magnetic stirrer and centrifuge. After analysis of protein level, fat, fiber, water and ash from fish meal processing wastewater industry.
The results informed that by chitosan amount adding 1000 mg/L at pH 7 into fish meal processing wastewater industry able to coagulated the wastewater until emerge its protein level about 50,56% and for chitosan amount 800 mg/L at pH 7 its fat 4,75 %, fiber 3,08% and chitosan amount 1000 mg/L at pH 8 its water 11,87%, ash 6,36% .
KATA PENGANTAR
Puji dan Syukur Saya Panjatkan kepada Allah SWT yang memberikan Saya
kemampuan telah dapat menyelesaikan tesis penelitian ini. Tesis ini ditulis
berdasarkan hasil penelitian yang berjudul “Pemanfaatan Kitosan Sebagai
Koagulan Untuk Memperoleh Kembali Protein Yang Dihasilkan Dari Limbah
Cair Industri Pemindangan Ikan”.
Pada kesempatan ini penulis menyampaikan terima kasih kepada Ibu Prof. Dr.
Ir. Setiaty Pandia sebagai ketua komisi pembimbing dan kepada Ibu Zuhrina
Masyithah , ST, M.Sc sebagai anggota komisi pembimbing yang telah memberikan
pengarahan dan bimbingan sehingga tesis terwujud.
Ucapan terima kasih tak lupa pula penulis sampaikan kepada :
1. Prof. Dr. Ir. T Chairun Nisa B., M.Sc., selaku Direktur Sekolah Pascasarjana
Universitas Sumatera Utara.
2. Staf Pengajar serta karyawan / ti Sekolah Pascasarjana Unversitas Sumatera
Utara.
3. Keluarga besar, yang telah memberikan dorongan dan dukungan yang besar
kepada Saya.
4. Rekan – rekan mahasiswa, yang telah memberikan masukan dan saran – saran
kepada saya.
Akhirnya penulis berharap semoga hasil penelitian yang dituangkan dalam
tesis ini dapat memberikat manfaat.
Hormat Saya,
Penulis
DAFTAR ISI
ABSTRAK i
KATA PENGANTAR ii
DAFTAR ISI iii
DAFTAR TABEL iv
DAFTAR GAMBAR v
DAFTAR LAMPIRAN vi
BAB I. PENDAHULUAN 1.1. Latar Belakang 1
1.2. Perumusan Masalah 3
1.3. Tujuan Penelitian 3
1.4. Manfaat Penelitian 4
1.5. Ruang Lingkup Penelitian 4
BAB II. TINJAUAN PUSTAKA 2.1. Kitosan 6
2.1.1. Sumber Kitosan 8
2.1.2. Sifat-sifat Kitosan 9
2.2. Kegunaan Kitosan 11
2.3. Metode Penyediaan Kitin 12
2.4. Metode Penyediaan Kitosan 14
2.5. Limbah Cair Industri Pemindangan Ikan 19
2.6. Protein 21
2.7. Lemak 23
2.8. Serat Kasar 23
2.7. Koagulasi 24
BAB III. METODELOGI PENELITIAN
3.1. Lokasi Penelitian 28
3.2. Bahan 28
3.3. Alat 29
3.4. Pelaksanaan Penelitian 29
3.4.1. Proses Perlakuan Limbah Cair Tanpa Diolah Dengan Koagulan kitosan 29
3.4.2. Proses Perlakuan Limbah cair Dengan Menggunakan Koagulan Kitosan 30
3.5. Rancangan Statistik 30
BAB IV. HASIL DAN PEMBAHASAN 4.1. Penentuan Komposisi Kimia Limbah Cair Pemindangan Ikan 35
4.2. Pengaruh Variasi Dosis Kitosan dan pH Koagulasi Terhadap Kadar Protein Limbah Cair Pemindangan Ikan 36
4.3. Pengaruh Variasi Dosis Kitosan dan pH Koagulasi Terhadap Kadar Lemak Limbah Cair Pemindangan Ikan 38
4.4. Pengaruh Variasi Dosis Kitosan dan pH Koagulasi Terhadap Kadar Serat Limbah Cair Pemindangan Ikan 39
4.5. Pengaruh Variasi Dosis Kitosan dan pH Koagulasi Terhadap Kadar Air Limbah Cair Pemindangan Ikan 41
4.6. Pengaruh Variasi Dosis Kitosan dan pH Koagulasi Terhadap Kadar Abu Limbah Cair Pemindangan Ikan 42
4.7. Pengujian Statistik 44
BAB V. KESIMPULAN DAN SARAN 5.1. Kesimpulan 51
DAFTAR PUSTAKA
53
LAMPIRAN A 56
LAMPIRAN B 64
LAMPIRAN C 69
DAFTAR TABEL
Tabel 2.1. Sumber – Sumber Kitin dan KItosan 8
Tabel 2.2. Karateristik Kitosan 10
Tabel 2.3. Penggunaan Kitin dan Kitosan 12
Tabel 2.4. Kondisi Perlakuan Dengan NaOH pada Proses Deproteinisasi 16
Tabel 2.5. Kondisi Perlakuan Dengan HCl pada Proses Demineralisasi 17
Tabel 2.6. Komposisi Beberapa Komponen Limbah Cair Pemindangan Ikan 20
Tabel 2.7. Komponen Kandungan Asam amino Limbah Cair pemindangan ikan 20
Tabel 2.8. Komposisi Beberapa Kandungan Nutrisi Bahan Baku Pakan 21
Tabel 3.1. Bentuk Tranformasi Data Rancangan Acak Kelompok Lengkap (RAKL) 31
Tabel 4.1. Komposisi Kimia Limbah Cair Pemindangan ikan 35
Tabel 4.2. Analisis Varian Untuk Parameter Kadar Protein 44
Tabel 4.3. Analisis Varian Untuk Parameter Kadar Lemak 46
Tabel 4.4. Analisis Varian Untuk Parameter Kadar Serat 47
Tabel 4.5. Analisis Varian Untuk Parameter Kadar Air 48
DAFTAR GAMBAR
Gambar 2.1. Struktur Kitin dan Kitosan 6
Gambar 4.1. Grafik Hubungan Variasi Dosis Kitosan (mg/L) dan pH Koagulasi
Terhadap Kadar Protein limbah Cair Industri Pemindangan Ikan 36
Gambar 4.2. Grafik Hubungan Variasi Dosis Kitosan (mg/L) dan pH Koagulasi
Terhadap Kadar Lemak limbah Cair Industri Pemindangan Ikan 38
Gambar 4.3. Grafik Hubungan Variasi Dosis Kitosan (mg/L) dan pH Koagulasi
Terhadap Kadar Serat limbah Cair Industri Pemindangan Ikan 40
Gambar 4.4. Grafik Hubungan Variasi Dosis Kitosan (mg/L) dan pH Koagulasi
Terhadap Kadar air limbah Cair Industri Pemindangan Ikan 41
Gambar 4.5. Grafik Hubungan Variasi Dosis Kitosan (mg/L) dan pH Koagulasi
DAFTAR LAMPIRAN
L.A.1. Prosedur Analisa Limbah Cair Industri Pemindangan Ikan 56
L.A.2. Contoh Perhitungan Perhitungan Analisa Protein dan Lemak Limbah Cair Industri Pemindangan Ikan 60
L.B.1. Data Hasil Pengukuran Penentuan Kadar Protein Dari Koagulasi Limbah Cair Industri Pemindangan Ikan 64
L.B.2. Data Hasil Pengukuran Penentuan Kadar Lemak Dari Koagulasi Limbah Cair Industri Pemindangan Ikan 65
L.B.3. Data Hasil Pengukuran Penentuan Kadar Serat Dari Koagulasi Limbah Cair Industri Pemindangan Ikan 66
L.B.4. Data Hasil Pengukuran Penentuan Kadar Air Dari Koagulasi Limbah Cair Industri Pemindangan Ikan 67
L.B.5. Data Hasil Pengukuran Penentuan Kadar Abu Dari Koagulasi Limbah Cair Industri Pemindangan Ikan 68
L.C.1. Perhitungan Data Statistik Dengan Program SPSS. 11 69
L.D.1. Proses Koagulasi Protein Limbah Cair Pemindangan Ikan 76
BAB I
PENDAHULUAN
1.1. Latar Belakang
Meningkatnya perkembangan sektor industri di Indonesia merupakan sarana
untuk memperbaiki taraf hidup rakyat, tetapi dilain pihak muncul masalah
pencemaran lingkungan akibat limbah industri yang dihasilkan. Sehingga dapat
merusak kelestarian lingkungan, keseimbangan sumber daya alam dan
berkembangbiaknya bibit penyakit.
Industri pengolahan udang merupakan salah satu industri yang berkembang
pesat pada saat ini dan memiliki potensi menghasilkan limbah yang dapat mencemari
lingkungan. Selama ini limbah kulit udang belum dimanfaatkan secara maksimal,
padahal limbah ini masih bisa dimanfaatkan menjadi produk lanjut yang mempunyai
nilai ekonomi yang tinggi, misalnya: kitin dan kitosan , tepung udang, pakan ternak
dan flavor udang (Suhardi, 1993).
Limbah udang hasil samping pengolahan udang beku merupakan sumber yang
potensial untuk pembuatan kitin dan kitosan, yakni biopolimer yang secara komersil
potensial untuk berbagai bidang kesehatan dan industri seperti: industri tekstil,
industri kosmetik, industri farmasi, industri fungisida, industri pengolahan pangan,
Kitosan yang diperoleh dari limbah pengolahan udang dapat dimanfaatkan
untuk penanganan limbah sebagai penyerap logam-logam beracun seperti : merkuri,
timah, tembaga, plutonium dan uranium karena sifat polikationiknya kitosan dapat
dimanfaatkan sebagai bahan penggumpal dalam penanganan limbah berprotein dan
memiliki potensi digunakan untuk pakan ternak.
Industri pemindangan ikan merupakan industri kecil yang mengolah dan
mengawetkan ikan yang mampu meningkatkan masa simpan ikan segar. Produksi
pemindangan ikan yang dihasilkan pada tahun 2005 mencapai 1,4 juta ton. Dari total
produksi tersebut limbah yang tidak dimanfaatkan mencapai 118.868 – 158.025 ton
(DKP, 2005).
Dalam proses pengolahan pemindangan ikan menghasilkan limbah cair yang
dapat menyebabkan pencemaran lingkungan terutama bau yang dikeluarkan akibat
dari pembusukan protein. Limbah cair pengolahan pemindangan ikan mengandung
nilai gizi yang cukup tinggi yang dapat dimanfaatkan untuk pangan dan pakan dengan
cara membuat produk protein konsentrat (Kementerian Lingkungan Hidup, 2005).
Penggunaan kitosan sebagai koagulan dalam penanganan limbah cair
pengolahan pangan dapat memudahkan terjadinya pemisahan protein dari filtratnya,
sehingga mengurangi beban limbah hasil samping yang terkoagulasi dari limbah
pengolahan pangan pada umumnya mengandung protein antara 30% - 75% dan
memiliki potensi untuk digunakan sebagai pakan (Bough dan Landes, 1976).
rajungan dapat digunakan untuk perolehan kembali protein dari limbah cair
precooking tuna kaleng sebesar 69,9 %, Harnentis (1998) yang meneliti tentang
pemanfaatan kitosan dari kulit beberapa jenis udang untuk memperoleh kembali
protein dalam penanganan limbah cair hasil samping pengolahan limbah udang,
Kennedy (1994) yang menyatakan kitosan sebagai koagulan untuk memperoleh
kembali protein dari limbah cair pabrik keju sebesar 40 %, Knorr (1991) meneliti
tentang perolehan kembali dan pemanfaatan kitin dan kitosan dalam penanganan
limbah pabrik pengolahan bahan makanan, Holland (1986) yang meneliti tentang
proses pemanfaatan kitosan dalam limbah pengolahan pangan.
Berdasarkan uraian diatas, peneliti tertarik untuk melakukan penelitian
terhadap pemanfaatan limbah cair dari industri pemindangan ikan untuk
dimanfaatkan proteinnya dengan menggunakan kitosan dari kulit udang sebagai
koagulan dengan variasi pH dan jumlah pemberian kitosan. Diharapkan limbah cair
industri pemindangan ikan yang terkoagulasi ini akan mempunyai kandungan protein
yang cukup tinggi dan memiliki potensi untuk digunakan sebagai pakan.
1.2. Perumusan Masalah
Adapun yang menjadi permasalahan dalam penelitian ini adalah sejauh mana
pengaruh penggunaan kitosan sebagai koagulan untuk mendapatkan kembali protein
yang dihasilkan dari limbah cair industri pemindangan ikan.
Penelitian ini bertujuan untuk mengetahui konsentrasi kitosan dan pH yang
optimum pada rentang penelitian untuk memperoleh kembali protein dalam limbah
cair industri pemindangan ikan dengan mutu terbaik.
1.4. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat sebagai berikut:
- Sebagai masukan berupa informasi baru dan teknologi alternatif dalam
mengolah limbah cair bagi industri pemindangan ikan dan industri lain yang
menghasilkan limbah sejenis.
- Sebagai informasi aplikatif mengenai penggunaan kitosan sebagai koagulan
untuk mendapatkan protein pada limbah cair industri pemindangan ikan.
1.5. Ruang Lingkup Penelitian
Adapun ruang lingkup dalam penelitian ini adalah;
a. Bahan baku yang digunakan:
• Kitosan dari limbah kulit udang dari industri pengolahan udang.
b. Variabel yang digunakan:
• pH koagulasi : 4, 5, 6, 7, 8.
• Dosis kitosan : 200, 400, 600, 800, 1000 mg/ L asam asetat 1%.
c. Limbah cair adalah limbah cair industri pemindangan ikan dengan volume 500
ml
Beberapa parameter yang diamati dan diuji pada penelitian ini adalah:
1. Pemberian kitosan sebagai koagulan pada limbah cair terhadap:
• Kadar air
• Kadar abu • Kadar protein
• Kadar lemak
BAB II
TINJAUAN PUSTAKA
2.1. Kitosan
Kitosan ditemukan oleh Routget pada tahun 1959. Kitosan merupakan turunan
(derivat) dari kitin. Kitosan memiliki struktur (1-4) – 2 – Amino – 2 – Deoksi - β - D
– Glukosa . Pembuatan kitosan dari kitin diperoleh melalui jalan melakukan proses
pemasakan dengan alkil kuat (NaOH). Sumber kitin yang sangat potensial adalah
kerangka crustacea (kepiting, lobstar, udang) dan dinding struktural fungi serta
hewan tingkat rendah. Kitosan mengandung gugus amina lebih besar 60%, sebaliknya
amina lebih kecil dari 60% adalah kitin (Whistler, 1973).
Rudall (1969) menjelaskan bahwa kitin adalah salah satu senyawa molekular
selain sellulosa dan kolagen. Senyawa ini merupakan suatu mikopolisakarida yang
berkonjugasi dengan protein dan sering berada pada dinding sel dalam tanaman
menggantikan sellulosa atau kadang-kadang terjadi bersama sellulosa.
Kitosan merupakan senyawa yang tidak larut dalam air, larutan basa kuat,
sedikit larut dalam HCl dan HNO3, 0,5 % H3PO4 sedangkan dalam H2SO4 tidak larut. Kitosan juga tidak larut dalam beberapa pelarut organik seperti alkohol, aseton,
dimetil formamida dan dimetilsulfida tetapi kitosan larut baik dalam asam formiat
mudah terbiodegradasi. Berat molekul kitosan adalah sekitar 1,2 x 105, bergantung degradasi yang terjadi selama proses.
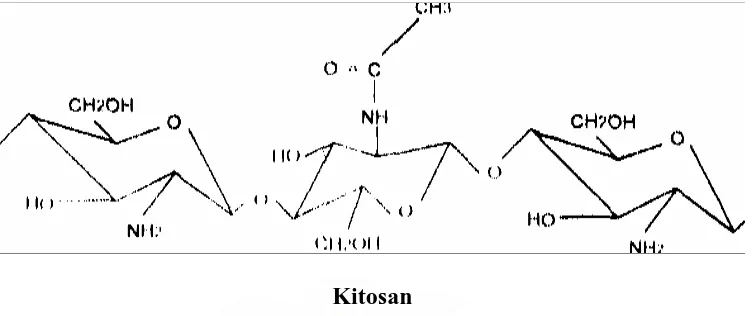
Perbedaan antara kitin dan kitosan terletak pada
kumpulan asetamida dari karbon dari karbon ke dua pada
strukturnya. Pada kitosan sebagian dari kumpulan gugus
asetil diganti dengan atom hidrogen melalui reaksi hidrolisis
dengan alkali pekat. Kitosan secara umum merupakan
kopolimer yang mengandung unit ulang kitin dengan
kandungan nitrogennya melebihi 7% (Muzzarelli, 1977).
Kitosan mempunyai sifat menyerap dan menggumpal yang baik, sifat ini
dapat meninggikan kreaktifannya dalam pembuatan turunannya. Satu sifat yang
spesifik adalah kitosan mudah mengurai didalam pelarut yang sesuai. Disamping itu
kitosan berintegrasi dengan zat-zat organik lainnya seperti protein (Bastaman,1989).
Oleh karena itu kitosan relatif lebih banyak digunakan pada berbagai bidang industri
terapan dan kesehatan (Knorr , 1991).
Kitosan
Gambar 2.1. Struktur Kitin dan Kitosan (sumber:Brine, 1984)
Pada Gambar 2.1, terlihat bahwa kitin murni mengandung gugus asetamida
(NH-COCH3), kitosan murni mengandung gugus amino (NH2). Perbedaan gugus ini akan mempengaruhi sifat-sifat kimia senyawa tersebut.
2.1.1. Sumber Kitosan
Pada Tabel 2.1 dapat dilihat beberapa sumber kitin kitosan:
Tabel 2.1.Sumber-sumber kitin dan kitosan
Jamur/ cendawan 5 – 20%
Tulang cumi-cumi 3 – 20%
Kalajengking 30%
Laba-laba 38%
Kecoa 35%
Kumbang 37%
Ulat sutra 44%
Kepiting 69%
Udang 70%
Dari Tabel 2.1 di atas terlihat bahwa sumber kitin dan kitosan yang terbanyak adalah
terdapat pada jenis udang-udangan (70%).
Sebenarnya kitin dan kitosan yang diproduksi secara komersial memiliki
gugus asetamida dan gugus amida pada rantai polimernya, dengan beragam
komposisi gugus tersebut. Perbedaan antara keduanya juga berdasarkan kandungan
nitrogennya. Bila nitrogen kurang dari 7% maka polimer disebut kitin dan apabila
kandungan total nitrogennya lebih dari 7% maka disebut kitosan (Roberts, 1992).
2.1.2. Sifat-sifat Kitosan
Sifat kationik biologi dan sifat larutan kitosan adalah sebagai berikut :
1. Sifat kationik
a. Linear polielektrolit pada pH asam.
b. Jumlah muatan positif tinggi: satu muatan per unit gugus glukosamin, jika
banyak material bermuatan negatif (seperti protein) maka muatan positif
kitosan berinteraksi kuat dengan permukaan negatif.
c. Flokulan yang baik : gugus NH3+ berinteraksi dengan muatan negatif dari koloid.
d. Mengikat ion-ion logam (Fe, Cu, Cd, Hg, Pb, Cr, Ni, Pu dan U).
2. Sifat biologi :
a. Dapat terdegradasi secara alami.
b. Polimer alami
c. Non toksis.
a. Linear oliamin (poli D-glukosamin) yang memiliki gugus amino yang baik untuk
reaksi kimia dan pembentukan garam dengan asam.
b. Gugus amino yang reaktif.
c. Gugus hidroksil yang reaktif (C3-OH, C6 – OH) yang dapat membentuk senyawa
turunannya.
Aplikasi kitosan dalam berbagai bidang tergantung sifat kationik, biologi dan
sifat kimianya (Sandford dan Hutchins, 1978).
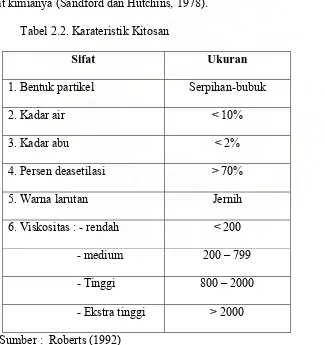
Tabel 2.2. Karateristik Kitosan
Sifat Ukuran
1. Bentuk partikel Serpihan-bubuk
2. Kadar air < 10%
3. Kadar abu < 2%
4. Persen deasetilasi > 70%
5. Warna larutan Jernih
6. Viskositas : - rendah < 200
- medium 200 – 799
- Tinggi 800 – 2000
- Ekstra tinggi > 2000
Sumber : Roberts (1992)
b. Berbentuk gel dengan polianion
c. Larut dalam campuran alkohol-air.
2.2. Kegunaan Kitosan
Kitosan memiliki sifat unik yang dapat digunakan dalam berbagai cara serta
memilki kegunaan yang beragam, antara lain sebagai bahan perekat, aditif untuk
kertas dan tekstil, penjernih air minum, serta untuk mempercepat penyembuhan luka
dan memperbaiki sifat pengikatan warna (Cho Kyun Rha,1980).
Kitosan dapat digunakan untuk mengolah limbah, seperti pengolahan limbah
dari industri pengolahan pangan dan untuk memisahkan protein dari limbah. Padatan
yang diperoleh dapat dimanfaatkan sebagai sumber protein dalam makanan ternak
(Bough dan Landes, 1976).
Kualitas kitosan tergantung pada penggunaannya, misalnya untuk kitosan yang
dipakai dalam proses permurnian air limbah tidak dibutuhkan kualitas yang
tinggi tetapi untuk penggunaan dalam bidang kesehatan dibutuhkan bahan dengan
kemurnian yang tinggi (Bastaman, 1989).
Tabel 2.3. Penggunaan Kitin dan Kitosan
1. Klasifikasi (penjernihan)
Limbah industri pangan
Industri sari buah
Pengolahan wine dan
minuman beralkohol
Penjernihan air minum
Penjernihan kolam renang
Penjernihan zat warna
Penjernihan tannin
Koagulasi/flokulan
Flokulan pektin/protein
Flokulan protein/mikroba
Koagulasi
Flokulan mikroba
Pembentuk kompleks
Pembentuk kompleks
2. Pengambilan Protein Mengendapkan bahan protein
3. Detoksifikasi limbah industri Membentuk senyawa kompleks dengan
logam dan bahan kimia berbahaya
4. Biomedis Menurunkan kadar kolesterol
Mempercepat penyembuhan luka
5. Bioteknologi Imobilisasi enzim
6. Industri tekstil Meningkatkan ketahanan warna
7. Kosmetik Substantive ketahanan warna
8. Fotografi Melindungi film dari kerusakan
9. Pertanian Bersifat sebagai Fungistatik
Sumber:Bastaman,1989
2.3. Metode Penyediaan Kitin
Kitin secara komersial umumnya diekstraksi dari kulit
udang, cangkang kepiting dan tulang rawan cumi yang
diperoleh dari limbah industri pengolahan hasil laut. Proses
tulang rawan cumi secara kimia merupakan proses yang
relatif sederhana. Ada beberapa metode dasar ekstraksi
kitin yang banyak dikembangkan dalam berbagai
penelitian,seperti metode Hackman dan Goldberg,
Blumberg dan Rigby (Muzzarelli,1977), dan juga dapat
digunakan metode Alimuniar sebagai metode penyediaan
kitin (Alimuniar, 1992).
Metode Rigby
Sisa kulit krustacea dengan larutan sodium karbonat 1
% panas dicampur dengan asam klorida 1 - 5% dan
kemudian sodium karbonat 0,4%.
Metode Blumberg
Kitin dari kulit udang dicampur dengan larutan
sodium hidroksida 5 % panas, larutan HCl dingin dan
larutan HCl 5 % panas.
Metode Hackman dan Goldberg
dengan HCl 1 M selama 24 jam lalu disaring. Hasil saringan
direfluks dengan NaOH 1 M pada suhu 100
oC selama 5 jam
dan kemudian dicuci dengan air suling dan dikeringkan.
Metode Alimuniar, A dan Zainuddin, R
Kitin udang yang telah bersih dan kering direndam dengan HCl 2 M selama
24 jam untuk menghilangkan mineral yang terkandung dalam kulit. Untuk
menghilangkan protein dilakukan dengan merendam selama 24 jam dengan NaOH 2
M, kemudian dicuci dengan air bersih lalu dikeringkan dengan penyinaran matahari.
2.4. Metode Penyediaan Kitosan
Metode penyediaan kitosan yang pertama dilakukan oleh Hope Seyler pada
tahun 1984 yaitu dengan merefluks kitin dalam kalium hidroksida pada suhu 180oC. Terdapat beberapa metode penyediaan kitosan lainnya antara lain (Muzzarelli,1977):
Metode Wolfrom dan Rigby
Kitin dicampur dengan 40% larutan NaOH dan direfluks pada suhu 115oC selama 4 jam, kemudian didinginkan dan seterusnya dicuci dengan air.
Kitin dicampur dengan NaOH 50% dan larutan paraffin selama 2 jam pada
suhu 120oC, campuran tersebut dituangkan dalam air dan seterusnya disaring dan dibilas dengan air suling.
Metode Horowitz
Kitin dicampur dengan larutan KOH dan campuran logam nikel dibawah
aliran gas nitrogen. Campuran dipanaskan pada suhu 180oC selama 30 menit, setelah itu dimasukkan kedalam etanol dan akan mengendap kemudian hasil yang diperoleh
dicuci dengan air suling.
Metode Alimuniar dan Zainuddin
Kitin dicampur dengan NaOH 40% dan dibiarkan selama 6 hari, dan setiap
harinya dilakukan pengadukan kemudian dicuci dengan air. Kitosan yang diperoleh
lalu dijemur.
Pembuatan kitosan yang menggunakan metode Alimuniar dan Zainuddin
(1992) lebih ekonomis penyediaannya dibandingkan dengan metode lainnya karena:
1. Proses deasetilasi kitin terjadi tanpa pemanasan pada temperatur 30oC.
2. Pada umumnya metode lain menggunakan vessel khusus dengan kontrol
atmosfir selama waktu tertentu, sedangkan pada metode ini hanya
menggunakan vessel sederhana.
3. Pada metode lain untuk mengontrol reaksi pembentukan produk dibutuhkan
sejumlah bahan aditif, sedangkan pada metode ini tidak menggunakan
Kitin yang terdapat pada kulit atau cangkang ini masih terikat dengan protein,
CaCO3 pigmen dan lemak. Berbagai teknik dilakukan untuk memisahkannya, tetapi pada umumnya melalui tiga tahapan yaitu demineralisasi dengan HCl encer,
deproteinisasi dengan NaOH encer (setelah tahap ini diperoleh kitin dan selanjutnya
deasitilasi kitin menggunakan NaOH pekat (Brine, 1981 dan Shahidi dkk, 1999).
Deproteinisasi
Proses deproteinisasi menggunakan berbagai pereaksi seperti NaOH yang
lebih banyak. Perlakuan dengan larutan NaOH bervariasi antara 0,25 N hingga 2,5 N
dan berbagai suhu serta lama perendaman seperti yang ditunjukkan pada Tabel 2.4
(Roberts,1992).
Tabel 2.4. Kondisi Perlakuan dengan NaOH pada proses Deproteinisasi
Sumber Kosentrasi NaOH (N)
Suhu (oC)
Lama Reaksi (jam)
Tulang rawan cumi
0,125 0,25 0,75 1,25 100 65 100 100 0,5 1 2 0,5
Udang / kepiting
0,5 1,0 1,0 1,0 1,25 1,25 65 80 100 100 85-90 100 2 3 36 72 1,5-2,25 24
Lobster 1,0
1,25
2,5
100
80-85
100
60
1
2,5
Sumber : Roberts, 1992
Keterangan : sk = suhu kamar
Penggunaan enzim untuk memisahkan protein juga
dilakukan dalam beberapa penelitian diantaranya dengan
pepsin, tripsin, enzim proteolitik seperti tuna proteinase dan
papain, setelah didemineralisasi sebelumnya dengan HCl.
Perlakuan dengan enzim ini masih menyisakan protein
sekitar 5 % yang memerlukan proses lanjutan (Roberts,
1992).
Demineralisasi
Proses
demineralisasi
menggunakan HCl dengan
konsentrasi 0,275 – 1 N, dengan kisaran suhu perendaman –
20
oC sampai dengan 22
oC (Tabel 2.5). Perendaman pada
suhu kamar lebih banyak dilakukan untuk meminimalkan
hidrolisis pada rantai polimer (Roberts, 1992). Proses
demineralisasi bertujuan untuk memisahkan CaCO
3dari
[image:30.612.114.511.112.183.2]kitin .
Tabel 2.5. Kondisi Perlakuan dengan HCl pada proses Demineralisasi
Sumber Konsentrasi HCl (N)
Suhu (oC)
Lama Reaksi (jam)
0,5 1,25 1,57
sk sk 20 – 22
1 1 1 – 3 Udang / kepiting 0,65
1,0 1,0 1,57 2,0 11,0 sk sk sk sk sk -20 24 12 8 5 48 4 Lobster 1,57 2,0 2,0 sk sk sk 11 –14 5 48 Sumber : Roberts (1992)
Keterangan : sk = suhu kamar
Deasetilasi
Kitin yang diperoleh dari proses deproteinisasi dan demineralisasi tidak dapat
larut dalam sebagian besar pereaksi kimia. Untuk memudahkan kelarutannya, maka
kitin di deasetilasi dengan pelarut alkali menjadi kitosan. Setelah melalui proses
deasetilasi maka daya adsorbsi kitin akan meningkat dengan bertambahnya gugus
amina (NH2) yang terdapat didalamnya, proses ini terjadi tanpa pemutusan rantai polimernya. Perbedaan antara kitin dan kitosan terletak pada gugus asetamida pada
karbon (C-2) di dalam strukturnya. Pada kitosan sebagian dari gugus asetil digantikan
dengan atom hidrogen melalui reaksi hidrolisis dengan basa kuat (Muzzarelli, 1977).
Proses deasetilasi kimiawi dilakukan untuk menghilangkan gugus asetil kitin
melalui perebusan dalam larutan alkali konsentrasi tinggi. Hwang dan Shin (2000)
deasetilasi kitosan tergantung dari konsentrasi alkali yang digunakan, lama reaksi,
ukuran partikel kitin dan berat jenis.
Makin tinggi konsentrasi alkali yang digunakan, makin rendah suhu atau
makin singkat waktu yang diperlukan dalam proses ini. Rigby dan Dupont dalam
Roberts (1992) membuat beberapa variasi deasetilasi seperti 5 % NaOH, 150 oC, 24 jam; 40 % NaOH,100 oC,1 jam.
Menurut Yunizal, dkk. (2001) ekstraksi kitosan dari
kepala udang putih (Penaeus merguensis) dengan kondisi
perlakukan yang tepat adalah deproteinase dengan NaOH 3
%, demineralisasi dengan HCl 1,25 N dan proses deasetilasi
menggunakan NaOH 50 %.
2.5. Limbah Cair Industri Pemindangan Ikan
Pengolahan pindang ikan sangat berperan dalam
usaha pemanfaatan hasil perikanan di Indonesia, karena
hampir 50 % dari hasil tangkapan memberikan hasil devisa
yang cukup besar. Dalam proses pengolahannya ikan segar
yang di pindang dengan bantuan air dan garam akan
menghasilkan pindang ikan dan hasil sampingan berupa
ikan, baik dalam volume maupun nilai perdagangannya.
(Moelyanto, 1992).
Pemindangan adalah merebus ikan dalam air dengan garam di bawah tekanan
udara normal, tanpa perlakuan lanjutan sehingga kegiatan enzim dan autolisis serta
bakteri pembusuk dapat dicegah. Pada pemindangan ikan dan garam yang telah
tersusun dalam wadah kedap air dimasak pada bak pemasakan yang telah berisi air
selama 2 jam. Setelah masak pindang diangkat dan ditiriskan. Limbah cair didapatkan
berupa air sisa dari bekas memasak dan hasil meniriskan ikan, dimana limbah
[image:33.612.137.510.521.700.2]tersebut mengandung protein terlarut (Afrianto dan Liviawaty, 1991).
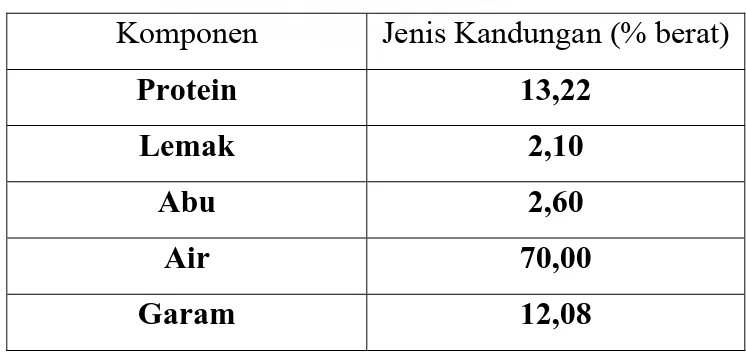
Tabel 2.6. Komposisi beberapa komponen limbah cair
pemindangan ikan
Komponen
Jenis Kandungan (% berat)
Protein 13,22
Lemak 2,10
Sumber : Deptan, 1995
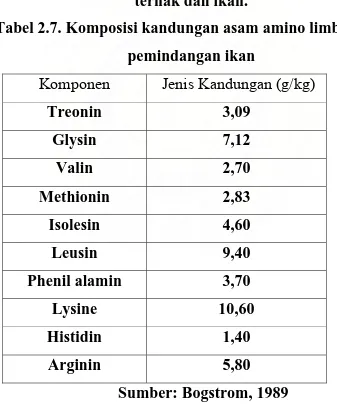
Protein yang terlarut dalam limbah cair pemindangan
ikan dapat dimanfaatkan dengan mengkoagulasi dengan
kitosan. Dalam kandungan limbah cair pemindangan ikan
terkandung asam amino berupa methionin dan lysine yang
[image:34.612.129.466.288.697.2]dapat digunakan sebagai bahan pencampur untuk pakan
ternak dan ikan.
Tabel 2.7. Komposisi kandungan asam amino limbah cair
pemindangan ikan
Komponen
Jenis Kandungan (g/kg)
Treonin 3,09
Glysin 7,12
Valin 2,70
Methionin 2,83
Isolesin 4,60
Leusin 9,40
Phenil alamin
3,70
Lysine 10,60
Histidin 1,40
Arginin 5,80
Limbah cair pengolahan perikanan yang mengandung sumber protein selama
ini belum dimanfaatkan sehingga dapat menimbulkan masalah di lingkungan bila
tidak diolah terlebih dahulu, sedangkan limbah cair tersebut yang berasal dari hasil
bekas memasak dan hasil meniriskan dapat dimanfaatkan untuk pakan. Dengan
pengolahan lebih lanjut pemanfaatan limbah cair untuk pakan harus memenuhi
[image:35.612.131.453.306.453.2]kriteria pada Tabel 2.8.
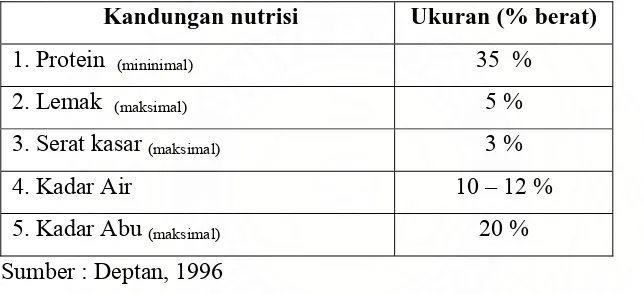
Tabel 2.8. Komposisi beberapa kandungan nutrisi bahan baku pakan
Kandungan nutrisi Ukuran (% berat)
1. Protein (mininimal) 35 %
2. Lemak (maksimal) 5 %
3. Serat kasar (maksimal) 3 %
4. Kadar Air 10 – 12 %
5. Kadar Abu (maksimal) 20 %
Sumber : Deptan, 1996
Dengan mengetahui komposisi limbah cair pemindangan ikan dan kandungan
nutrisi bahan baku pakan, maka diharapkan penelitian yang direncanakan ini dapat
memberikan masukan yang berguna sebagai upaya pengolahan limbah cair
pemindangan ikan.
2.6. Protein
Protein merupakan molekul organik komplek yang mengandung karbon,
persentasenya cukup konstan (berkisar antara 15-18 % atau rata-rata 16 %). Pada
umumnya protein juga mengandung sulfur, fosfor dan besi.
Senyawa organik protein ini sangat dibutuhkan oleh hewan untuk kepentingan
struktur (membentuk kolagen dalam tulang dan kartilago atau kepentingan fungsional
misalnya membentuk enzim atau protein khusus lain seperti hemoglobin).
Apabila protein di hidrolisis dengan larutan asam atau basa atau dengan enzim
akan menghasilkan lebih kurang 20 asam amino yang berbeda. Dari 20 jenis asam
amino tersebut telah diketahui sejumlah 10 asam amino merupakan jenis asam amino
yang sangat penting dan harus tersedia dalam pakan, kesepuluh asam amino tersebut
adalah leucine, methionine, isoleusine, tripthopban, valine, arginin, theonine,
bistidine, phenylalamine dan lysine (Tabel 2.7).
Protein merupakan komponen bahan baku pakan ternak yang sangat penting
bagi pertumbuhan ternak misalnya :
1. Memperbaiki jaringan
2. Untuk pertumbuhan dari jaringan baru
3. Metabolisme untuk energi
4. Untuk enzim yang essensial bagi fungsi tubuh yang normal
Protein dapat berasal dari tumbuhan (protein nabati) dan hewan (protein hewani).
Berdasarkan hasil penelitian protein hewani lebih mudah dicerna daripada protein
nabati. Kandungan asam amino essensialnya pun lebih lengkap daripada protein
nabati.
Lemak adalah senyawa organik kompleks yang tidak larut dalam air tetapi
larut dalam ester, chloroform dan benzena. Lemak merupakan nama umum yang
meliputi unsur sterol, wates, ester, phospolipid dan sphyngomyelin. Lemak
mengandung asam lemak yang diklasifikasikan sebagai asam lemak jenuh dan asam
lemak tak jenuh ditandai dengan adanya ikatan rangkap (PUFA) sedangkan asam
lemak jenuh ditandai dengan tidak adanya ikatan rangkap. Beberapa jenis asam lemak
sangat dibutuhkan dalam bahan baku pakan ternak dan sering disebut asam lemak
essensial.
Lemak dalam bahan baku pakan berfungsi sebagai sumber asam lemak dan
energi atau sumber tenaga yang sangat penting untuk pertumbuhan dan kelangsungan
hidup ternak, dan juga dapat membantu penyerapan vitamin yang larut dan minyak,
membantu pembentukan tekstur membran, serta mempengaruhi aroma dan tekstur
dari pakan.
2.8. Serat Kasar
Serat kasar termasuk golongan karbohidrat yang berfungsi untuk mengisi dan
menjaga agar alat pencernaan bekerja dengan baik, serta mendorong kelenjar-kelenjar
pencernaan untuk mengeluarkan enzim-enzim pencernaan. Dengan adanya
kandungan serat kasar yang cukup digunakan untuk bahan baku pakan dapat menekan
jumlah kebutuhan pakan yang akan dikonsumsi.
Koagulasi merupakan penyerapan bagian-bagian dari suatu koloid menjadi
berbagai bentuk yang lebih besar sehingga mampu mengendap. Biasanya dari suatu
koloid dapat diperoleh endapan melalui pemanasan, sehingga bagian-bagian yang
lebih besar menjadi berkembang dan mendesak bagian-bagian yang kecil (Reynolds,
1982).
Ukuran partikel cenderung mempengaruhi pengendapan partikel dalam suatu
media air tenang. Koloid sering memerlukan koagulan untuk mencapai ukuran
partikel agar dapat terbentuk suatu endapan dan juga memerlukan waktu yang cukup
lama untuk mengendap. Bila waktu pengendapan tidak cukup dapat dilakukan dengan
perlakuan lain untuk menggeser padatan suspensi, koagulasi dan flokulasi bisa
menyebabkan perbesaran ukuran dan pengendapan dengan cukup cepat (Sawyer and
McCarty, 1987).
Koloid dikategorikan hidrofobik dan hidrofilik. Koloid yang hidrofobik tidak
bereaksi dengan air, sedangkan hidrofilik bereaksi dengan air. Dalam pengolahan air
koloid hidrofilik bisa bereaksi dengan koagulan yang digunakan dalam proses
pengolahan limbah.
Pengadukan diperlukan untuk memperbesar koagulasi agar dapat merusak
stabilitas sistem koloid dengan terjadinya penggumpalan partikel. Penambahan energi
pengadukan sangat diperlukan agar dapat memberikan intensitas pengadukan yang
tinggi sehingga koagulan terdistribusi secara merata yang akan memperbesar
Proses koagulasi untuk pengolahan air dipengaruhi oleh beberapa faktor
antara lain : efek pH, efek garam, efek koagulan yang digunakan, efek suhu dan efek
pencampuran (pengadukan). Umumnya partikel-partikel tersuspensi/koloid dalam air
buangan memperlihatkan gerak Brownian. Permukaan partikel-partikel tersebut
bermuatan listrik negatif. Partikel-partikel itu menarik ion-ion negatif. Ion-ion positif
tersebut kemudian menyelubungi partikel koloid dan membentuk lapisan rapat
muatan didekat permukaannya.
Proses terjadinya koagulasi menurut Farooq dan Velioglu dalam
Cheremisinoff, 1989 adalah sebagai berikut:
1. Partikel koloid (suspensi) yang bermuatan negatif menarik partikel koagulan
(polimer) yang bermuatan positif.
2. ion-ion positif kemudian menyelubungi partikel koloid dan membentuk lapisan
rapat muatan didekat permukaannya yang disebut lapisan kokoh/tetap (fixed
layer)
3. Lapisan kokoh dikelilingi lagi oleh sejumlah ion-ion yang berlawanan muatan
yang disebut difusi (difussed layer).
4. Di dalam lapisan diffusi terdapat bidang geser (shear plane) batas dimana ion-ion
yang berlawanan muatan dapat tersapu dari permukaan partikel karena gerakan
fluida.
5. Kumpulan ion-ion berlawanan didalam air yang mengelilingi partikel koloid dan
6. Potensial listrik diantara bidang geser (shear plane) dan badan cairan dapat
ditentukan dengan pengukuran elektroforesis (pengukuran laju partikel dalam
suatu medan listrik) dan disebut potensial zeta ( ). Potensial zeta berhubungan
dengan muatan partikel dan ketebalan lapisan ganda. Ketebalan lapisan
tergantung pada konsentrasi ion didalam cairan, semakin besar konsentrasi ion
semakin kecil ketebalan lapisan ganda dan berarti semakin rapat muatan.
Potensial zeta sering digunakan sebagai suatu ukuran stabilitas partikel koloid
karena semakin tinggi potensial zeta semakin stabil partikel koloid. Potensial zeta
dinyatakan dengan persamaan :
= 4 q d D Keterangan :
= zeta potensial
q = muatan partikel persatuan luas (Coulombs/m2) d = ketebalan lapisan ganda disekitar bidang geser (m)
D = konstanta dielektrik cairan.
Jika ion-ion atau koloid bermuatan positif (kation) ditambahkan ke dalam
target koagulasi, maka kation tersebut akan masuk ke dalam lapisan difusi karena
tertarik oleh muatan negatif yang ada pada permukaan partikel koloid. Hal ini
menyebabkan konsentrasi ion-ion dalam lapisan difusi akan meningkat. Akibatnya
ketebalan lapisan difusi akan berkurang (termampatkan ke arah permukaan partikel).
Pemampatan lapisan difusi ini akan mempengaruhi potensial permukaan partikel
kation hingga mencapai suatu jumlah tertentu, akan merubah besar potensial zeta ke
suatu tingkat dimana gaya tarik menarik Van der waals antar partikel dapat
melampaui gaya tolak menolak yang ada. Dengan demikian partikel koloid dapat
saling mendekati dan menempel satu sama lain serta membentuk mikroflok.
Mekanisme destabilisasi partikel koloid ini disebut pemampatan lapisan ganda listrik.
Dalam hal ini jenis muatan permukaan partikel koloid tidak berubah (Farooq dan
Velioglu dalam Cheremisinoff, 1989).
Menurut Davis dan Cornwell (1991) ada dua faktor penting dalam
pertambahan koagulan yakni pH dan dosis. Dosis dan pH optimum harus ditentukan
dalam test laboratorium. Untuk mengatur pH air atau limbah cair ke dalam range
optimal koagulasi, diperlukan bahan penolong (coagulan aid) berupa asam atau
alkali. Asam paling umum digunakan untuk menurunkan pH adalah asam sulfat dan
untuk menaikkan pH biasanya digunakan lime [Ca(OH)2], soda abu (Na2CO3) dan NaOH.
BAB III
METODOLOGI PENELITIAN
3.1. Lokasi Penelitian
Penelitian ini dilaksanakan di laboratorium Penelitian Fakultas MIPA dan
Laboratorium sentral pertanian Fakultas Pertanian Universitas Sumatera Utara.
Waktu penelitian dilaksanakan selama enam bulan, mulai Januari 2006 hingga Juni
2006.
3.2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah sebagai berikut:
1. Kitosan
2. Sampel (limbah cair industri)
3. Asam asetat, CH3COOH (p.a. E Merck) 4. Asam klorida pekat, HCl
5. Asam formiat, CH2O2 6. Natrium Hidroksida, NaOH
7. Kalium Sulfat, K2SO4 8. Asam sulfat, H2SO4 9. Petroleum benzen
11. Kertas saring
3.3. Alat
Alat-alat yang digunakan adalah sebagai berikut:
1. Neraca Analitis
2. Sentrifuse
3. Magnetic stirrer
4. Sochlet
5. Kjedhal Term
6. Oven
7. Erlenmeyer
8. Beaker glass
9. Labu takar
10. Corong
11. Gelas ukur
12. Cawan porselen
3.4. Pelaksanaan Penelitian
Dalam penelitian ini ada dua tahapan yang dilakukan yaitu :
1. Proses perlakuan limbah cair tanpa diolah dengan koagulan kitosan
2. Proses perlakuan limbah cair dengan menggunakan koagulan kitosan.
Air limbah pemindangan ikan yang digunakan berasal dari salah satu industri
kecil pengolahan pemindangan ikan yang ada di Kampung Nelayan, Kec. Medan
Labuhan. Dibawa ke laboratorium, dimasukkan dalam suatu wadah dan disaring.
Kemudian dianalisa limbah cairnya meliputi : kadar protein, lemak, abu, air dan kadar
garam.
3.4.2. Proses perlakuan limbah cair dengan menggunakan koagulan kitosan
(Harnentis,1998)
Sebanyak 200, 400, 600, 800, 1000 mg kitosan yang masing-masing dilarutkan
dalam 1 L asam asetat 1 % .
Sebanyak 100 ml larutan kitosan dengan konsentrasi yang berbeda kemudian
ditambahkan ke dalam limbah cair industri pemindangan ikan sebanyak 500 ml
yang telah disaring terlebih dahulu.
Kemudian diaduk dengan magnetic stirrer pada kecepatan 100 rpm selama ± 30 menit dengan variasi pH 4 dengan penambahan 200, 400, 600, 800, 1000 mg/L ke
dalam beaker glass.
Dan selanjutnya dilakukan hal yang sama pada variasi pH 5, 6 ,7 dan 8.
Campuran tersebut kemudian disentrifuse pada kecepatan 1.200 rpm selama 5
menit.
Endapan yang diperoleh dikeringkan dalam oven pada suhu 40 oC selama ± 24 jam, kemudian dilakukan analisis kadar protein, lemak, serat, air dan abu
(Lampiran A).
Pengujian perbedaan varian sangat banyak kegunaannya dalam penelitian.
Pengujian menggunakan analisis varian dalam statistika parametric diantara
kelompok yang saling memiliki perbedaan sebagai akibat adanya perlakuan dilakukan
dengan menggunakan Analysis of Varian (ANOVA).
Uji ANOVA interaksi dua faktor (Two way ANOVA) dilakukan untuk
mengetahui perbedaan nyata rata-rata antara varian dari tiga kelompok sampel atau
lebih berdasarkan satu faktor dan dilihat interaksinya dengan faktor-faktor lain.
Analisis terhadap rancangan dalam penelitian ini adalah menggunakan Rancangan
Acak Kelompok Lengkap (RAKL) merupakan desain percobaan yang memiliki ciri
pada ditemukannya kelompok dengan jumlah yang sama dan masing-masing
kelompok memberikan perlakuan. Harapan atas dilakukannya pengelompokkan
dalam RAKL adalah makin berkurangnya galat perlakuan.
Dalam kasus penelitian ini uji yang dilakukan untuk mengetahui perbedaan
nyata rata-rata antar varian dari lima kelompok sampel berdasarkan satu faktor
perlakuan yang mempengaruhi masing-masing parameter Kadar air, abu, protein,
lemak dan serat kasar dari limbah cair.
Pada analisis kasus dalam penyelesaian RAKL dengan SPSS 11 tabel data
harus ditransformasikan dulu dalam bentuk seperti Tabel 3.1. Setelah pengisian data
maka data diolah dengan program SPSS 11 sehingga diperoleh output sebagai
berikut:
2. Output Test of Between subjects effects: merupakan uji ANOVA, yaitu uji yang
bertujuan untuk mengetahui apakah ada hubungan yang signifikan (jelas) antar
dua faktor, yaitu antara jumlah kitosan dan pH.
3. Output Test homogeneous subsets: merupakan uji yang bersifat menemukan
kelompok sampel manakah yang perbedaan rata-ratanya signifikan, dengan dasar
letak kelompok sampel pada subsets (grup).
Dari tabel ANOVA dapat diketahui perbedaan rata-rata kadar airnya
berdasarkan kelompok jumlah kitosan dan pH, dengan menentukan hipotesis (Ho dan
Hi), maka pengambilan keputusan adalah : jika probabilitas > 0,05 maka Ho diterima
dan bila probabilitas < 0,05 maka Ho ditolak (berbeda nyata).
Pengertian Corrected total adalah menyatakan jumlah kuadrat (sum of square)
dari variabel pH (sebagai variabel yang dependen). Corrected model adalah
menyatakan jumlah kuadrat (sum of square) yang dihitung oleh model ANOVA.
Pengertian Error adalah menyatakan jumlah kuadrat (sum of square) yang tidak
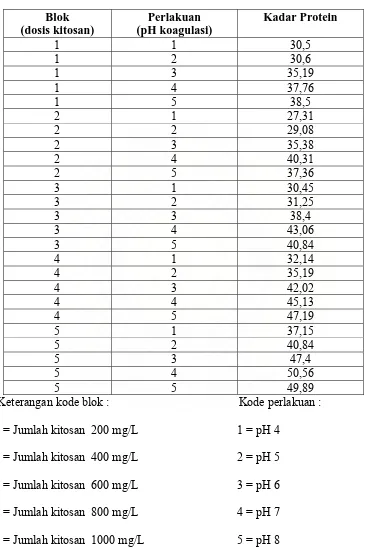
Tabel 3.1. Bentuk transformasi data Rancangan Acak Kelompok Lengkap (RAKL)
Blok (dosis kitosan)
Perlakuan (pH koagulasi)
Kadar Protein
1 1 30,5 1 2 30,6 1 3 35,19 1 4 37,76 1 5 38,5 2 1 27,31 2 2 29,08 2 3 35,38 2 4 40,31 2 5 37,36 3 1 30,45 3 2 31,25 3 3 38,4 3 4 43,06 3 5 40,84 4 1 32,14 4 2 35,19 4 3 42,02 4 4 45,13 4 5 47,19 5 1 37,15 5 2 40,84 5 3 47,4 5 4 50,56 5 5 49,89 Keterangan kode blok : Kode perlakuan :
1 = Jumlah kitosan 200 mg/L 1 = pH 4
2 = Jumlah kitosan 400 mg/L 2 = pH 5
3 = Jumlah kitosan 600 mg/L 3 = pH 6
4 = Jumlah kitosan 800 mg/L 4 = pH 7
Setelah data ditransformasikan akan diperoleh beberapa uji dari variabel yang akan
BAB IV
HASIL DAN PEMBAHASAN
4.1. Penentuan Komposisi kimia limbah cair pemindangan ikan
Penentuan komposisi kimia limbah cair pemindangan ikan yang digunakan pada
proses koagulasi dimana dapat diketahui kandungan komposisi kimianya yang
terdapat dalam limbah cair tersebut.
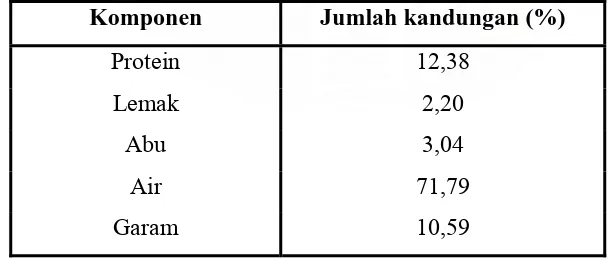
Dari hasil analisis limbah cair pemindangan ikan menunjukkan kandungan
komposisi kimianya cukup baik, yaitu dengan kadar proteinnya 12,38% (Tabel 4.2).
Hasil ini menggambarkan bahwa limbah cair pemindangan ikan cukup baik untuk
diolah selanjutnya dalam proses koagulasi dengan penambahan kitosan sebagai
[image:49.612.126.430.486.616.2]koagulan sehingga dapat dimanfaatkan sebagai bahan pakan.
Tabel 4.1. Komposisi kimia limbah cair pemindangan ikan.
Komponen Jumlah kandungan (%)
Protein 12,38
Lemak 2,20
Abu 3,04
Air 71,79
4.2. Pengaruh variasi dosis kitosan dan pH koagulasi terhadap kadar protein
limbah cair pemindangan ikan
Hasil pengujian penggunaan kitosan sebagai koagulan untuk menentukan
[image:50.612.117.522.257.528.2]kadar protein dalam limbah cair industri pemindangan ikan dapat dilihat pada
Gambar 4.1 berikut ini:
20 25 30 35 40 45 50 55
0 4 5 6 7 8
pH
Ka
da
r Pr
ot
e
in (
%
)
dosis kitosan 200 mg/L dosis kitosan 400 mg/L
dosis kitosan 600 mg/L dosis kitosan 800 mg/L
dosis kitosan 1000 mg/L
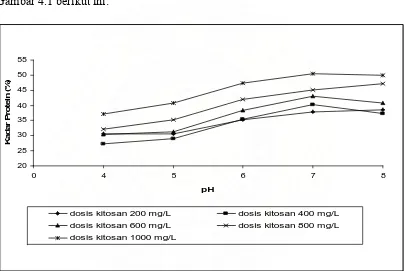
Gambar 4.1. Grafik hubungan pengaruh variasi dosis kitosan (mg/L) dan pH koagulasi terhadap kadar protein limbah cair industri pemindangan ikan
Dari Gambar 4.1 di atas terlihat bahwa perolehan kadar protein optimum
terjadi pada pH 7 dengan penambahan dosis kitosan 1000 mg/L. Pada pH 8 perolehan
kadar protein untuk dosis kitosan 400 mg/L, 600 mg/L dan 1000 mg/L mengalami
kitosan berkurang karena akan bersaing dengan ion H dalam larutan untuk menempati
grup amina bebas dari kitosan sehingga keaktifan gugus NH3+ dalam larutan berkurang untuk menggumpalkan protein. Knorr (1984) menyatakan bahwa pada pH
yang tinggi proses adsorbsi partikel-partikel koloid dalam larutan berkurang, dengan
demikian fungsi kitosan untuk mengadsorbsi dalam larutan semakin berkurang
sehingga kemampuan mengendapkan protein semakin kecil.
Kadar protein setelah proses koagulasi diperoleh sebesar 50,56 % (Lampiran
B) terjadi pada penambahan kitosan sebanyak 1000 mg/L dan pH 7. Hal ini
memenuhi standarisasi kadar protein untuk dapat digunakan sebagai bahan baku yang
diizinkan oleh pemerintah yaitu: minimal 35 % (Deptan, 1996). Dari penelitian yang
pernah dilakukan oleh Harnentis (1998) pada proses koagulasi limbah cair hasil
samping pengolahan limbah udang untuk menggumpalkan protein dengan kitosan
sebagai koagulan diperoleh kadar proteinnya sebesar 44,24 % dengan konsentrasi
kitosan 300 mg/L pada pH 7. Menurut Holland (1986) penggumpalan protein dalam
limbah cair dengan penambahan kitosan sebagai koagulan dapat meningkatkan gugus
NH3+ dalam larutan melalui mekanisme yaitu NH3+ NH2 + H+
Gugus amino dalam kesetimbangan yang bergantung pada konsentrasi kitosan
dan pH, dimana pada konsentrasi kitosan yang tinggi dan pH netral dapat
kemampuan gugus fungsional kitosan dalam menggumpalkan protein juga akan
meningkat.
4.3. Pengaruh variasi dosis kitosan (mg/L) dan pH koagulasi terhadap kadar
lemak limbah cair pemindangan ikan
Hasil pengujian penggunaan kitosan sebagai koagulan untuk menentukan
kadar lemak dalam limbah cair industri pemindangan ikan dapat dilihat pada Gambar
4.2 berikut ini:
3 3.2 3.4 3.6 3.8 4 4.2 4.4 4.6 4.8 5
0 4 5 6 7 8
pH
Kadar
Lem
a
k (
%
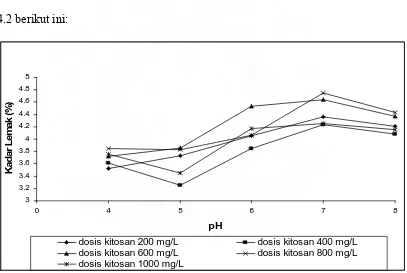
)
[image:52.612.116.523.295.568.2]dosis kitosan 200 mg/L dosis kitosan 400 mg/L dosis kitosan 600 mg/L dosis kitosan 800 mg/L dosis kitosan 1000 mg/L
Gambar 4.2. Grafik hubungan pengaruh variasi dosis kitosan (mg/L) dan pH koagulasi terhadap kadar lemak limbah cair industri pemindangan ikan
Dari Gambar 4.2 di atas terlihat bahwa perolehan kadar lemak optimum
terjadi pada penambahan kitosan 800 mg/L dan pH 7. Pada pH di atas pH 7
cair sudah jenuh dan tidak dapat lagi bereaksi lagi dengan partikel-partikel koloid
dengan sempurna. Pada pH 5 untuk penambahan kitosan 400 mg/L dan penambahan
kitosan 1000 mg/L terjadi penurunan perolehan kadar lemak hal ini disebabkan tidak
sempurnanya penggumpalan protein dalam larutan karena sebagian sisa polimer yang
berada dalam larutan tidak cukup untuk mengikat partikel lain sehingga jembatan
partikel tidak sempurna terbentuk. Bastaman (1989) menyatakan bahwa kitosan dapat
berinteraksi dengan bahan organik terutama protein dimana perolehan kadar protein
berpengaruh terhadap perolehan kadar lemak dalam limbah cair. Hal ini dilihat pada
penambahan kitosan sebanyak 800 mg/L dan pH 7 diperoleh kadar lemak sebesar
4,75 % (Lampiran B). Hal ini memenuhi standarisasi kadar lemak untuk dapat
digunakan sebagai bahan baku yang diizinkan oleh pemerintah yaitu: maksimal 5 %
(Deptan, 1996). Dari penelitian yang pernah dilakukan oleh Fadjar (2002) pada
proses koagulasi limbah cair precooking tuna kaleng untuk menggumpalkan protein
dengan kitosan sebagai koagulan diperoleh kadar lemaknya sebesar 2,54 % dengan
konsentrasi kitosan 300 mg/L pada pH 7.
4.4. Pengaruh Variasi dosis kitosan dan pH koagulasi terhadap kadar serat
limbah cair pemindangan ikan
Hasil pengujian penggunaan kitosan sebagai koagulan untuk menentukan
kadar serat dalam limbah cair industri pemindangan ikan dapat dilihat pada Gambar
1 1.2 1.4 1.6 1.8 2 2.2 2.4 2.6 2.8 3 3.2
0 4 5 6 7 8
pH
K
a
d
a
r S
e
ra
t (%
)
dosis kitosan 200 mg/L dosis kitosan 400 mg/L
dosis kitosan 600 mg/L dosis kitosan 800 mg/L
dosis kitosan 1000 mg/L
Gambar 4.3. Grafik hubungan variasi dosis kitosan (mg/L) dan pH koagulasi terhadap kadar serat limbah cair industri pemindangan ikan
Dari Gambar 4.3 di atas terlihat bahwa perolehan kadar serat optimum terjadi
pada penambahan kitosan 800 mg/L dan pH 7. Pada pH 5 untuk penambahan kitosan
200 mg/L dan 400 mg/L mengalami penurunan perolehan kadar serat hal ini
disebabkan tidak sempurnanya partikel-partikel koloid dalam larutan berinteraksi
dengan kitosan dalam menggumpalkan protein sehingga partikel-partikel padatan
yang terlarut dalam limbah cair semakin kecil. Pada pH 8 untuk penambahan 200
mg/L, 800 mg/L dan 1000 mg/L mengalami penurunan perolehan kadar serat hal ini
disebabkan partikel-partikel padatan yang terlarut dalam limbah cair sudah jenuh
sehingga kemampuan kitosan untuk mengkoagulasi limbah cair tidak sempurna. Hal
ini di lihat pada penambahan kitosan sebanyak 800 mg/L dan pH 7 terjadinya
kadar serat untuk dapat digunakan sebagai bahan baku yang diizinkan oleh
pemerintah yaitu: maksimal 3 % (Deptan, 1996). Maezaki (1993) menyatakan bahwa
penambahan kitosan pada limbah cair pengolahan pangan dapat menaikkan perolehan
kandungan serat dalam proses penggumpalan protein.
4.5. Pengaruh variasi dosis kitosan dan pH koagulasi terhadap kadar air limbah
cair pemindangan ikan
Hasil pengujian penggunaan kitosan sebagai koagulan untuk menentukan
kadar air dalam limbah cair industri pemindangan ikan dapat dilihat pada Gambar
4.4 berikut ini:
6 6.5 7 7.5 8 8.5 9 9.5 10 10.5 11 11.5 12
0 4 5 6 7 8
pH
K
a
d
a
r A
ir (
%
)
dosis kitosan 200 mg/L dosis kitosan 400 mg/L
dosis kitosan 600 mg/L dosis kitosan 800 mg/L
[image:55.612.115.526.338.642.2]dosis kitosan 1000 mg/L
Dari Gambar 4.4 di atas terlihat bahwa perolehan kadar air optimum terjadi
pada penambahan kitosan 1000 mg/L dan pH 8 hal ini disebabkan semakin besar
penambahan konsentrasi kitosan semakin besar kemampuan partikel-partikel padatan
yang tergumpal.dalam limbah cair sehingga kadar air yang di dapat semakin tinggi.
Hal ini di lihat pada penambahan kitosan sebanyak 1000 mg/L dan pH 7 diperoleh
kadar airnya sebesar 11,87 % (Lampiran B). Hal ini memenuhi standarisasi kadar air
untuk dapat digunakan sebagai bahan baku yang diizinkan oleh pemerintah yaitu: 10 -
12 % (Deptan, 1996). Pada pH 6 untuk penambahan 200 mg/L dan 600 mg/L
mengalami penurunan hal ini disebabkan partikel-partikel padatan yang tergumpalkan
tidak sempurna pada proses koagulasi sehingga kadar air yang didapat semakin kecil.
4.6. Pengaruh variasi dosis kitosan dan pH koagulasi terhadap kadar abu
limbah cair pemindangan ikan
Hasil pengujian penggunaan kitosan sebagai koagulan untuk menentukan
kadar abu dalam limbah cair industri pemindangan ikan dapat dilihat pada Gambar
0 1 2 3 4 5 6 7
0 4 5 6 7 8
pH
Ka
da
r Ab
u (
%
)
dosis kitosan 200 mg/L dosis kitosan 400 mg/L
dosis kitosan 600 mg/L dosis kitosan 800 mg/L
dosis kitosan 1000 mg/L
Gambar 4.5. Grafik hubungan pengaruh variasi dosis kitosan (mg/L) dan pH koagulasi terhadap kadar abu limbah cair industri pemindangan ikan.
Dari Gambar 4.5 di atas terlihat perolehan kadar abu optimum diperoleh pada
penambahan kitosan 1000 mg/L dan pH 8 hal ini disebabkan semakin besar jumlah
kitosan yang ditambahkan dalam limbah cair semakin besar kadar abu yang diperoleh
sehingga dapat menurunkan jumlah garam mineral yang tertinggal dalam
penggumpalan protein. Chandrakrachang (1998) menyatakan bahwa semakin besar
jumlah kitosan yang digunakan, semakin cepat dan banyak garam mineral yang dapat
dihilangkan. Hal ini dilihat pada penambahan kitosan sebanyak 1000 mg/L dan pH 8
terjadinya kenaikan dari kadar abu sebesar 6,36 % (Lampiran B). Hal ini memenuhi
pemerintah yaitu: maksimal 20 % (Deptan, 1996). Pada pH 6 terlihat adanya
penurunan perolehan kadar abu untuk penambahan 400 mg/L, 600 mg/L dan 800
mg/L disebabkan kitosan yang ditambahkan untuk mengkoagulasi limbah cair
industri pemindangan ikan terlarut tidak sempurna sehingga partikel-pertikel
padatannya tidak mampu mengurangi jumlah garam mineral yang tertinggal untuk
menggumpalkan protein.
4.7. Pengujian Statistik
Pada penelitian ini uji yang dilakukan untuk mengetahui perbedaan nyata
rata-rata antar varian dari lima kelompok sampel berdasarkan satu faktor perlakuan
yang mempengaruhi masing-masing parameter kadar protein, lemak, serat, air dan
abu dari limbah cair industri pemindangan ikan.
4.7.1 Pengaruh dosis kitosan dan pH koagulasi terhadap kadar protein dalam
limbah cair industri pemindangan ikan.
Hasil penelitian pengaruh penambahan dosis kitosan dan pH koagulasi untuk
menentukan kadar protein dari proses koagulasi limbah cair industri pemindangan
ikan dapat dilihat dari Tabel 4.2 dibawah ini:
Tabel 4.2. Analisis varian untuk parameter kadar protein
Sumber Varian Jumlah Kuadrat
Derajat Kebebasan
Rata-rata Kuadrat
F Hitung
F Tabel
Probabilitas
Model koreksi 1023,610 8 127,951 73,314 2,82 0,000
Intersep 363666,49 1 36366,49 20837,5 0,000 Perlakuan A (dosis) 436,292 4 109,073 62,497 0,000
Perlakuan B (pH) 587,317 4 146,829 84,131 0,000
[image:58.612.112.569.610.701.2]Total 37418,023 25
Total Koreksi 1051,533 24
Dari Tabel 4.2 di atas hipotesis yang dapat dirumuskan adalah:
Ho = semua perlakuan mempunyai pengaruh yang sama terhadap kadar protein.
Ha = tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar protein
Hipotesis di atas dapat menjadi dasar pengambilan keputusan berdasarkan
probabilitas yaitu apabila > 0,05 maka Ho diterima dan apabila probabilitas < 0,05
maka Ho ditolak.
Pada Tabel 4.2 di atas dapat dilihat bahwa nilai F hitung adalah 84,131
denagan probabilitas 0,000 karena probabilitas < 0,05 maka Ho ditolak dan Ha
diterima atau kesimpulan yang dapat diambil adalah terbukti secara meyakinkan
bahwa tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar
protein limbah cair industri pemindangan ikan, ini berarti terbukti secara meyakinkan
bahwa perlakuan B (pH) mempunyai pengaruh yang berbeda terhadap kadar protein
secara signifikan karena ada perbedaan nyata, maka uji lanjut perlu dilakukan.
Kesimpulan ini juga dapat digunakan untuk perlakuan A (dosis) karena nilai F hitung
adalah 62,497 dan probabilitas 0,000 < 0,05.
4.7.2. Pengaruh dosis kitosan dan pH koagulasi terhadap kadar lemak dalam
Hasil penelitian pengaruh penambahan dosis kitosan dan pH koagulasi untuk
menentukan kadar lemak dari proses koagulasi limbah cair industri pemindangan ikan
dapat dilihat dari Tabel 4.3. dibawah ini:
Tabel 4.3. Analisis varian untuk parameter kadar lemak
Sumber Varian Jumlah Kuadrat
Derajat Kebebasan
Rata-rata Kuadrat
F Hitung
F Tabel
Probabilitas
Model koreksi 3,326 8 0,416 20,345 2,82 0,000
Intersep 403,367 1 403,367 19738,063 0,000 Perlakuan A (dosis) 0,525 4 0,131 6,427 0,003
Perlakuan B (pH) 2,801 4 0,700 34,263 0,000
Error 0,327 16 2,044E-02
Total 407,020 25
Total Koreksi 3,653 24
Dari Tabel 4.3 di atas hipotesis yang dapat dirumuskan adalah:
Ho = semua perlakuan mempunyai pengaruh yang sama terhadap kadar lemak.
Ha = tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar lemak.
Hipotesis diatas dapat menjadi dasar pengambilan keputusan berdasarkan probabilitas
yaitu apabila > 0,05 maka Ho diterima dan apabila probabilitas < 0,05 maka Ho
ditolak.
Pada Tabel 4.3 di atas dapat dilihat bahwa nilai F hitung adalah 34,263
dengan probabilitas 0,000 karena probabilitas < 0,05 maka Ho ditolak dan Ha
diterima atau kesimpulan yang dapat diambil adalah terbukti secara meyakinkan
bahwa tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar lemak
limbah cair industri pemindangan ikan, ini berarti terbukti secara meyakinkan bahwa
[image:60.612.118.565.250.398.2]signifikan karena ada perbedaan nyata, maka uji lanjut perlu dilakukan. Kesimpulan
ini juga dapat digunakan untuk perlakuan A (dosis) karena nilai F hitung adalah
6,427 dan probabilitas 0,003 < 0,05.
4.7.3. Pengaruh dosis kitosan dan pH koagulasi terhadap kadar serat dalam
limbah cair industri pemindangan ikan.
Hasil penelitian pengaruh penambahan dosis kitosan dan pH koagulasi untuk
menentukan kadar serat dari proses koagulasi limbah cair industri pemindangan ikan
[image:61.612.116.565.329.507.2]dapat dilihat dari Tabel 4.4. dibawah ini:
Tabel 4.4. Analisis varian untuk parameter kadar serat
Sumber Varian Jumlah Kuadrat
Derajat Kebebasan
Rata-rata Kuadrat
F Hitung
F Tabel
Probabilitas
Model koreksi 7,630 8 0,954 84,829 2,82 0,000
Intersep 130,965 1 130,965 11648,075 0,000 Perlakuan A (dosis) 2,012 4 0,503 44,731 0,002
Perlakuan B (pH) 5,618 4 1,405 124,926 0,000
Error 0,180 16 1,124E-02
Total 138,775 25
Total Koreksi 7,810 24
Dari Tabel 4.4 di atas hipotesis yang dapat dirumuskan adalah:
Ho = semua perlakuan mempunyai pengaruh yang sama terhadap kadar serat.
Ha = tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar serat.
Hipotesis di atas dapat menjadi dasar pengambilan keputusan berdasarkan
probabilitas yaitu apabila > 0,05 maka Ho diterima dan apabila probabilitas < 0,05
Pada Tabel 4.4 di atas dapat dilihat bahwa nilai F hitung adalah 124,926
dengan probabilitas 0,000 karena probabilitas < 0,05 maka Ho ditolak dan Ha
diterima atau kesimpulan yang dapat diambil adalah terbukti secara meyakinkan
bahwa tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar serat
limbah cair industri pemindangan ikan, ini berarti terbukti secara meyakinkan bahwa
perlakuan B (pH) mempunyai pengaruh yang berbeda terhadap kadar serat secara
signifikan karena ada perbedaan nyata, maka uji lanjut perlu dilakukan. Kesimpulan
ini juga dapat digunakan untuk perlakuan A (dosis) karena nilai F hitung adalah
44,731 dan probabilitas 0,002 < 0,05.
4.7.4. Pengaruh dosis kitosan dan pH koagulasi terhadap kadar air dalam
limbah cair industri pemindangan ikan.
Hasil penelitian pengaruh penambahan dosis kitosan dan pH koagulasi untuk
menentukan kadar air dari proses koagulasi limbah cair industri pemindangan ikan
dapat dilihat dari Tabel 4.5. dibawah ini:
Tabel 4.5. Analisis varian untuk parameter kadar air
Sumber Varian Jumlah Kuadrat
Derajat Kebebasan
Rata-rata Kuadrat
F Hitung
F Tabel
Probabilitas
Model koreksi 33,260 8 4,157 52,934 2,82 0,000
Intersep 2222,180 1 2222,180 28293,603 0,000 Perlakuan A (dosis) 7,750 4 1,937 24,668 0,000
Perlakuan B (pH) 25,510 4 6,377 81,200 0,000
Error 1,257 16 7,854E-02
Total 2256,696 25
Total Koreksi 34,516 24
[image:62.612.116.564.541.659.2]
Ho = semua perlakuan mempunyai pengaruh yang sama terhadap kadar air.
Ha = tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar air.
Hipotesis di atas dapat menjadi dasar pengambilan keputusan berdasarkan
probabilitas yaitu apabila > 0,05 maka Ho diterima dan apabila probabilitas < 0,05
maka Ho ditolak.
Pada Tabel 4.5 di atas dapat dilihat bahwa nilai F hitung adalah 81,200
dengan probabilitas 0,000 karena probabilitas < 0,05 maka Ho ditolak dan Ha
diterima atau kesimpulan yang dapat diambil adalah terbukti secara meyakinkan
bahwa tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar air
limbah cair industri pemindangan ikan, ini berarti terbukti secara meyakinkan bahwa
perlakuan B (pH) mempunyai pengaruh yang berbeda terhadap kadar air secara
signifikan karena ada perbedaan nyata, maka uji lanjut perlu dilakukan. Kesimpulan
ini juga dapat digunakan untuk perlakuan A (dosis) karena nilai F hitung adalah
24,668 dan probabilitas 0,000 < 0,05.
4.7.5. Pengaruh dosis kitosan dan pH koagulasi terhadap kadar abu dalam
limbah cair industri pemindangan ikan.
Hasil penelitian pengaruh penambahan dosis kitosan dan pH koagulasi untuk
menentukan kadar abu dari proses koagulasi limbah cair industri pemindangan ikan
dapat dilihat dari Tabel 4.6. dibawah ini:
Sumber Varian Jumlah Kuadrat
Derajat Kebebasan
Rata-rata Kuadrat
F Hitung
F Tabel
Probabilitas
Model koreksi 14,973 8 1,872 49,762 2,82 0,000
Intersep 612,464 1 612,464 16283,943 0,000 Perlakuan A (dosis) 7,652 4 1,913 50,860 0,000
Perlakuan B (pH) 7,321 4 1,830 48,664 0,001
Error 0,602 16 3,761E-02
Total 628,038 25
Total Koreksi 15,575 24
Dari Tabel 4.6 di atas hipotesis yang dapat dirumuskan adalah:
Ho = semua perlakuan mempunyai pengaruh yang sama terhadap kadar abu.
Ha = tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar abu.
Hipotesis di atas dapat menjadi dasar pengambilan keputusan berdasarkan
probabilitas yaitu apabila > 0,05 maka Ho diterima dan apabila probabilitas < 0,05
maka Ho ditolak.
Pada Tabel 4.6 di atas dapat dilihat bahwa nilai F hitung adalah 48,664
dengan probabilitas 0,001 karena probabilitas < 0,05 maka Ho ditolak dan Ha
diterima atau kesimpulan yang dapat diambil adalah terbukti secara meyakinkan
bahwa tidak semua perlakuan mempunyai pengaruh yang sama terhadap kadar abu
limbah cair industri pemindangan ikan, ini berarti terbukti secara meyakinkan bahwa
perlakuan B (pH) mempunyai pengaruh yang berbeda terhadap kadar abu secara
signifikan karena ada perbedaan nyata, maka uji lanjut perlu dilakukan. Kesimpulan
ini juga dapat