SINTESIS DAN KARAKTERISASI KOMPOSIT
APATIT-KITOSAN DENGAN METODE
IN-SITU
DAN
EX-SITU
ASTRI LESTARI
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ASTRI LESTARI. Sintesis dan Karakterisasi Komposit Apatit-Kitosan dengan Metode In-situ dan Ex-situ. Dibimbing oleh KIAGUS DAHLAN DAN AKHIRUDDIN MADDU.
Sintesis komposit apatit-kitosan dilakukan dengan teknik presipitasi secara in-situ dan ex-situ pada
kondisi fisiologis tubuh manusia. Apatit-kitosan secara in-situ dihasilkan dari presipitasi
Na2HPO4.2H2O dan kitosan yang diteteskan dengan CaCl2.2H2O. Pada proses ex-situ, kitosan
diteteskan setelah proses presipitasi Na2HPO4.2H2O yang diteteskan dengan CaCl2.2H2O selesai dilakukan. Penambahan kitosan yang dilakukan diharapkan dapat meningkatkan kristanilitas dan kelenturan serta biokompatibilitas dari HAP sehingga dapat diaplikasikan untuk bidang medis terutama dalam implantasi tulang. Untuk mengetahui karakteristik komposit apatit-kitosan yang dihasilkan, dilakukan karakterisasi dengan XRD (X-Ray Diffraction), SEM (Scanning Electron Microscope), FTIR (Fourier Transform Infrared), EDXA (Energy Dispersive X-Ray Analysis) dan
uji mekanik. Hasil karakterisasi XRD pada sampel in-situ dan ex-situ memperlihatkan adanya
puncak milik hidroksiapatit (HAp), Apatit Karbonat tipe A (AKA), Apatit Karbonat tipe B (AKB), Okta Kalsium Fosfat (OKF) dan kitosan. Hadirnya puncak milik apatit dan kitosan menandakan bahwa komposit apatit-kitosan berhasil terbentuk. Hasil XRD juga menunjukkan adanya penurunan derajat kristanilitas pada sampel komposit apatit-kitosan yang disebabkan karena kitosan bersifat lebih amorf dibandingkan apatit. Terbentuknya komposit apatit-kitosan juga diperkuat dengan hasil karakterisasi FTIR dan SEM. Pada FTIR, gugus fosfat (PO4), hidroksil (OH) dan karbonat (CO3) yang merupakan milik apatit muncul bersama dengan gugus fungsi milik kitosan yaitu NH2, C-H, dan amida. Pada karakterisasi SEM, terbentuknya komposit apatit-kitosan ditandai dengan morfologi sampel in-situ dan ex-situ yang berbentuk bongkahan yang
menunjukkan bahwa kitosan telah berikatan dengan apatit.
IN-SITU
DAN
EX-SITU
ASTRI LESTARI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Menyetujui:
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Dr. Drh. Hasim, DEA
NIP. 19610328 198601 1 002
Tanggal Lulus:
Nama
: Astri Lestari
NRP
: G74051551
Pembimbing 1
Dr. Kiagus Dahlan
NIP. 19600507 198703 1 003
Pembimbing 2
karya ilmiah ini berhasil diselesaikan. Shalawat serta salam juga tak lupa tercurah kepada Rasulullah Muhammad SAW. Tema yang dipilih dalam penelitian ini adalah sintesis dan karakterisasi komposit apatit-kitosan dengan metode in-situ dan ex-situ. Penelitian yang
merupakan hibah dari PHK A2 ini dilaksanakan sejak bulan Agustus 2008 sampai dengan Mei 2009.
Ucapan terimakasih juga penulis haturkan kepada pihak-pihak yang telah membantu dalam penyelesaian skripsi ini:
1. Dr. Kiagus Dahlan selaku pembimbing pertama dan Dr. Akhiruddin Maddu selaku pembimbing kedua yang telah memberikan banyak masukan, bimbingan dan motivasi. 2. Drs. M. Nur Indro, M. Sc dan Drs. Sidikrubadi P selaku dosen penguji
3. Bapak dan Ibu serta keluarga besar yang telah memberikan dukungan yang luar biasa selama menempuh studi di IPB
4. Seluruh dosen fisika yang telah memberikan ilmu selama ini serta seluruh staf dan pegawai atas kerjasamanya
5. Pak Sulis, Pak Dadang, Pak Didik, Ibu Titis, dan Pak Wawan atas kerjasamanya selama karakterisasi
6. Seluruh teman-teman Fisika 42, 43, dan 44, BEM MIPA 2008, KAMMI, dan kru Puri Salwa atas semua yang telah diberikan
7. Dan semua pihak yang tidak mungkin penulis sebutkan satu persatu.
Bogor, September 2009
Penulis dilahirkan di Jakarta pada tanggal 17 Agustus 1987 dari ayah Sarto dan ibu Mujirah. Penulis merupakan putri ketiga dari tiga bersaudara.
Pada tahun 2005 penulis lulus dari SMA Negeri 31 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB). Penulis memilih Mayor Fisika dan Minor Keuangan Aktuaria, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Halaman
KATA PENGANTAR ... i
RIWAYAT HIDUP ... ii
DAFTAR ISI ... iii
DAFTAR GAMBAR ... v
DAFTAR TABEL ... vi
DAFTAR LAMPIRAN ... vii
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujuan Penelitian ... 1
1.3. Waktu dan Tempat Penelitian ... 1
2. TINJAUAN PUSTAKA ... 1
2.1. Struktur Tulang ... 1
2.2. Mineral Tulang ... 2
2.3. Mineral Apatit ... 2
2.4. Struktur Kristal Apatit ... 3
2.5. Kitosan ... 3
2.6. X-Ray Diffraction (XRD) ... 4
2.7. Spektroskopi Fourier Transform Infra Red (FTIR) ... 4
2.8. Scanning Electron Microscopy (SEM) ... 5
3. BAHAN DAN METODE ... 6
3.1. Bahan dan Alat ... 6
3.2. Metode Penelitian ... 6
3.2.1 Preparasi Sampel ... 6
3.2.2. Kontrol ... 6
3.2.3. In-situ ... 6
3.2.4. Ex-situ ... 6
3.2.5. Karakterisasi dengan XRD ... 7
3.2.6. Karakterisasi dengan FTIR... 7
3.2.7. Karakterisasi dengan SEM ... 7
4. HASIL DAN PEMBAHASAN... 7
4.1. Analisa XRD ... 7
4.2. Analisa FTIR ... 9
4.3. Analisa Morfologi SEM dan EDXA ... 10
4.4. Uji Kekerasan Vickers ... 11
1 Struktur Hidroksiapatit ... 3
2 Struktur Kimia Kitosan ... 4
3 Sinar-X Menumbuk Atom ... 4
4 Skema FTIR ... 5
5 Skema SEM ... 6
6 Pola XRD Kitosan Murni, Sampel Kontrol (A1 dan A2), Sampel In-situ (B1 dan B2) dan Sampel Ex-situ (C1 dan C2) ... 7
7 Pola Spektra FTIR Sampel ... 10
1 Kandungan Unsur Mineral dalam Tulang ... 2
2 Formula Kimia, Struktur dan Parameter Kisi Kristal Kalsium Fosfat ... 2
3 Spesifikasi Kitosan Niaga ... 4
4 Kode Sampel ... 7
5 Derajat Kristanilitas Sampel ... 8
6 Ukuran Kristal Sampel ... 8
7 Parameter Kisi Sampel ... 9
8 Pita Absorpsi Sampel ... 9
9 Rasio Molaritas Ca/P Sampel ... 11
SINTESIS DAN KARAKTERISASI KOMPOSIT
APATIT-KITOSAN DENGAN METODE
IN-SITU
DAN
EX-SITU
ASTRI LESTARI
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ASTRI LESTARI. Sintesis dan Karakterisasi Komposit Apatit-Kitosan dengan Metode In-situ dan Ex-situ. Dibimbing oleh KIAGUS DAHLAN DAN AKHIRUDDIN MADDU.
Sintesis komposit apatit-kitosan dilakukan dengan teknik presipitasi secara in-situ dan ex-situ pada
kondisi fisiologis tubuh manusia. Apatit-kitosan secara in-situ dihasilkan dari presipitasi
Na2HPO4.2H2O dan kitosan yang diteteskan dengan CaCl2.2H2O. Pada proses ex-situ, kitosan
diteteskan setelah proses presipitasi Na2HPO4.2H2O yang diteteskan dengan CaCl2.2H2O selesai dilakukan. Penambahan kitosan yang dilakukan diharapkan dapat meningkatkan kristanilitas dan kelenturan serta biokompatibilitas dari HAP sehingga dapat diaplikasikan untuk bidang medis terutama dalam implantasi tulang. Untuk mengetahui karakteristik komposit apatit-kitosan yang dihasilkan, dilakukan karakterisasi dengan XRD (X-Ray Diffraction), SEM (Scanning Electron Microscope), FTIR (Fourier Transform Infrared), EDXA (Energy Dispersive X-Ray Analysis) dan
uji mekanik. Hasil karakterisasi XRD pada sampel in-situ dan ex-situ memperlihatkan adanya
puncak milik hidroksiapatit (HAp), Apatit Karbonat tipe A (AKA), Apatit Karbonat tipe B (AKB), Okta Kalsium Fosfat (OKF) dan kitosan. Hadirnya puncak milik apatit dan kitosan menandakan bahwa komposit apatit-kitosan berhasil terbentuk. Hasil XRD juga menunjukkan adanya penurunan derajat kristanilitas pada sampel komposit apatit-kitosan yang disebabkan karena kitosan bersifat lebih amorf dibandingkan apatit. Terbentuknya komposit apatit-kitosan juga diperkuat dengan hasil karakterisasi FTIR dan SEM. Pada FTIR, gugus fosfat (PO4), hidroksil (OH) dan karbonat (CO3) yang merupakan milik apatit muncul bersama dengan gugus fungsi milik kitosan yaitu NH2, C-H, dan amida. Pada karakterisasi SEM, terbentuknya komposit apatit-kitosan ditandai dengan morfologi sampel in-situ dan ex-situ yang berbentuk bongkahan yang
menunjukkan bahwa kitosan telah berikatan dengan apatit.
IN-SITU
DAN
EX-SITU
ASTRI LESTARI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Menyetujui:
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Dr. Drh. Hasim, DEA
NIP. 19610328 198601 1 002
Tanggal Lulus:
Nama
: Astri Lestari
NRP
: G74051551
Pembimbing 1
Dr. Kiagus Dahlan
NIP. 19600507 198703 1 003
Pembimbing 2
karya ilmiah ini berhasil diselesaikan. Shalawat serta salam juga tak lupa tercurah kepada Rasulullah Muhammad SAW. Tema yang dipilih dalam penelitian ini adalah sintesis dan karakterisasi komposit apatit-kitosan dengan metode in-situ dan ex-situ. Penelitian yang
merupakan hibah dari PHK A2 ini dilaksanakan sejak bulan Agustus 2008 sampai dengan Mei 2009.
Ucapan terimakasih juga penulis haturkan kepada pihak-pihak yang telah membantu dalam penyelesaian skripsi ini:
1. Dr. Kiagus Dahlan selaku pembimbing pertama dan Dr. Akhiruddin Maddu selaku pembimbing kedua yang telah memberikan banyak masukan, bimbingan dan motivasi. 2. Drs. M. Nur Indro, M. Sc dan Drs. Sidikrubadi P selaku dosen penguji
3. Bapak dan Ibu serta keluarga besar yang telah memberikan dukungan yang luar biasa selama menempuh studi di IPB
4. Seluruh dosen fisika yang telah memberikan ilmu selama ini serta seluruh staf dan pegawai atas kerjasamanya
5. Pak Sulis, Pak Dadang, Pak Didik, Ibu Titis, dan Pak Wawan atas kerjasamanya selama karakterisasi
6. Seluruh teman-teman Fisika 42, 43, dan 44, BEM MIPA 2008, KAMMI, dan kru Puri Salwa atas semua yang telah diberikan
7. Dan semua pihak yang tidak mungkin penulis sebutkan satu persatu.
Bogor, September 2009
Penulis dilahirkan di Jakarta pada tanggal 17 Agustus 1987 dari ayah Sarto dan ibu Mujirah. Penulis merupakan putri ketiga dari tiga bersaudara.
Pada tahun 2005 penulis lulus dari SMA Negeri 31 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB). Penulis memilih Mayor Fisika dan Minor Keuangan Aktuaria, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Halaman
KATA PENGANTAR ... i
RIWAYAT HIDUP ... ii
DAFTAR ISI ... iii
DAFTAR GAMBAR ... v
DAFTAR TABEL ... vi
DAFTAR LAMPIRAN ... vii
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujuan Penelitian ... 1
1.3. Waktu dan Tempat Penelitian ... 1
2. TINJAUAN PUSTAKA ... 1
2.1. Struktur Tulang ... 1
2.2. Mineral Tulang ... 2
2.3. Mineral Apatit ... 2
2.4. Struktur Kristal Apatit ... 3
2.5. Kitosan ... 3
2.6. X-Ray Diffraction (XRD) ... 4
2.7. Spektroskopi Fourier Transform Infra Red (FTIR) ... 4
2.8. Scanning Electron Microscopy (SEM) ... 5
3. BAHAN DAN METODE ... 6
3.1. Bahan dan Alat ... 6
3.2. Metode Penelitian ... 6
3.2.1 Preparasi Sampel ... 6
3.2.2. Kontrol ... 6
3.2.3. In-situ ... 6
3.2.4. Ex-situ ... 6
3.2.5. Karakterisasi dengan XRD ... 7
3.2.6. Karakterisasi dengan FTIR... 7
3.2.7. Karakterisasi dengan SEM ... 7
4. HASIL DAN PEMBAHASAN... 7
4.1. Analisa XRD ... 7
4.2. Analisa FTIR ... 9
4.3. Analisa Morfologi SEM dan EDXA ... 10
4.4. Uji Kekerasan Vickers ... 11
1 Struktur Hidroksiapatit ... 3
2 Struktur Kimia Kitosan ... 4
3 Sinar-X Menumbuk Atom ... 4
4 Skema FTIR ... 5
5 Skema SEM ... 6
6 Pola XRD Kitosan Murni, Sampel Kontrol (A1 dan A2), Sampel In-situ (B1 dan B2) dan Sampel Ex-situ (C1 dan C2) ... 7
7 Pola Spektra FTIR Sampel ... 10
1 Kandungan Unsur Mineral dalam Tulang ... 2
2 Formula Kimia, Struktur dan Parameter Kisi Kristal Kalsium Fosfat ... 2
3 Spesifikasi Kitosan Niaga ... 4
4 Kode Sampel ... 7
5 Derajat Kristanilitas Sampel ... 8
6 Ukuran Kristal Sampel ... 8
7 Parameter Kisi Sampel ... 9
8 Pita Absorpsi Sampel ... 9
9 Rasio Molaritas Ca/P Sampel ... 11
2 Komposisi Massa untuk Menghasilkan Sampel ... 16
3 Proses Preparasi Sampel... 17
4 Metode Presipitasi Sampel ... 18
5 Probabilits Fase Sampel ... 19
6 Tabel Data JCPDS ... 22
7 Perhitungan Parameter Kisi Sampel ... 24
8 Perhitungan Ukuran Kristal Sampel ... 30
9 Spektra FTIR Sampel ... 31
1. PENDAHULUAN
1.1. Latar Belakang
Kerusakan pada organ tulang merupakan masalah kesehatan yang serius karena tulang merupakan salah satu organ tubuh yang sangat penting bagi manusia. Betapa pentingnya fungsi tulang sehingga apabila terjadi kerusakan maka fungsi kerja dari tubuh akan terhambat. Untuk menangani kerusakan pada tulang tersebut, maka dibutuhkan suatu material yang tepat untuk implantasi tulang. Material pengganti tulang yang umum digunakan adalah autograf (penggantian satu
bagian tubuh dengan bagian tubuh yang lainnya dalam satu individu), allograf
(penggantian tulang manusia dengan tulang yang berasal dari manusia lain), xenograf
(penggantian tulang manusia dengan tulang yang berasal dari hewan), exogemus
(penggantian atau implantasi dengan bahan sintetik atau yang biasa disebut dengan biomaterial) dan berbagai macam material sintetik lainnya seperti polimer, material logam, komposit dan biokeramik. Setiap material tersebut memiliki kekurangan dan kelebihan sebagai material untuk memperbaiki tulang, seperti stabilitas kimia, biokompatibilitas, biodegradasi dengan tubuh dalam waktu yang lama [1].
Adanya keterbatasan dalam setiap material tersebut memicu perkembangan riset di bidang biomaterial. Biomaterial merupakan bahan inert yang diimplantasi ke dalam sistem hidup sebagai pengganti fungsi jaringan hidup atau organ [2]. Pemilihan biomaterial yang tepat sangat diperlukan dalam proses implantasi. Tentunya biomaterial yang dipilih adalah yang mudah diperoleh, biokompatibel atau sesuai dengan jaringan keras dalam komposisi dan morfologi kandungannya, bioaktif dan tidak toksik [3].
Material komposit kalsium fosfat dibutuhkan untuk memperbaiki atau mengganti tulang yang rusak. Senyawa kalsium fosfat yang paling stabil adalah hidroksiapatit (HAP) yang memiliki formula Ca10(PO4)6(OH)2 dengan rasio Ca/P sekitar 1,67 [4]. HAp memiliki biokompatibilitas yang baik terhadap kontak langsung dengan tulang.
Salah satu sifat biokompatibilitas yang diharapkan adalah tidak mudah getas. Untuk mengoptimalisasikan sifat tersebut maka digunakan kitosan sebagai biopolimer yang diharapkan mampu meminimalisir sifat getas pada HAP.
Kitosan merupakan polisakarida dengan struktur yang mirip dengan selulosa. Kitosan (2-asetamida-deoksi-α-D-glukosa) memiliki gugus amina bebas yang membuat polimer ini bersifat polikationik, sehingga polimer ini potensial untuk diaplikasikan dalam pengolahan limbah, obat-obatan, pengolahan makanan dan bioteknologi. Kitosan merupakan salah satu matriks polimer yang dapat digunakan untuk modifikasi komposit [5]. Matriks polimer dari bahan alami ini diharapkan dapat meningkatkan bioaktivitas, biokompatibel dan sifat mekanik komposit.
1.2 Tujuan Penelitian
Penelitian ini bertujuan:
1. Membuat senyawa komposit apatit-kitosan melalui presipitasi dengan metode in-situ
dan ex-situ.
2. Melakukan karakterisasi dan menganalisis komposit apatit-kitosan hasil presipitasi dengan menggunakan XRD (X-Ray Diffraction), FTIR (Fourier Transform Infra Red) dan SEM (Scanning Electron Microscopy)
1.3. Waktu dan Tempat
Penelitian ini dilakukan pada bulan Agustus 2008 – Mei 2009 di Laboratoium Biofisika Departemen Fisika IPB. Karakterisasi XRD dilakukan di Litbang Kehutanan Bogor dan PTBIN Batan Serpong, SEM dilakukan di PPGL Bandung, dan FTIR dilakukan di Pusat Studi Biofarmaka LPPM IPB.
2. TINJAUAN PUSTAKA
2.1. Struktur Tulang
Tulang sebagai bagian dari kerangka manusia memiliki beberapa fungsi antara lain sebagai tempat melekatnya otot dan menyokong jaringan halus, memberikan perlindungan kepada organ-organ internal tubuh sehingga mengurangi resiko organ-organ tersebut terluka dan sebagai tempat memproduksi sel darah. Interaksi antar otot pada tulang menyebabkan tulang dapat digerakkan. Selain itu, jaringan tulang menyediakan beberapa mineral antara lain kalsium (Ca) dan fosfor (P). Ketika diperlukan, tulang akan melepaskan mineral ke dalam darah sehingga tercipta keseimbangan mineral di dalam tubuh [6].
dan posisi tulang. Tulang terdiri dari dua komponen utama yaitu rangka organik dan garam anorganik. Mineral tulang merupakan komponen anorganik tulang, sedangkan kolagen merupakan komponen organik tulang. Serat kolagen memberikan tulang kemampuan untuk meregang dan memutar. Kombinasi dari serat dan garam menjadikan tulang kuat tanpa menjadi rapuh [7].
Tulang merupakan jaringan hidup dan bersifat dinamis sehingga struktur tulang dapat berubah karena gaya luar yang didapat selama hidup. Tulang juga mengalami rekonstruksi internal atau remodelling. Remodelling adalah proses tulang lama akan
dihancurkan dan diganti oleh tulang baru. Proses ini berlangsung selama hidup manusia dan terjadi pada semua tulang. Selain itu tulang juga mengalami perkembangan atau osifikasi. Ada dua tipe osifikasi yaitu osifikasi intramembranus dan osifikasi endokondral [8].
Rangka berkembang dari transformasi jaringan embrionik yang menjadi tulang. Jaringan yang menjadi tulang tersebut berasal dari sel-sel yang terdapat pada lapisan mesodermal embrio. Jika jaringan embrionik langsung bertransformasi menjadi tulang disebut osifikasi intramembranus. Jika sel mesodermal bertransformasi menjadi kartilago dahulu sebelum menjadi tulang maka prosesnya disebut osifikasi endokondral.
2.2. Mineral Tulang
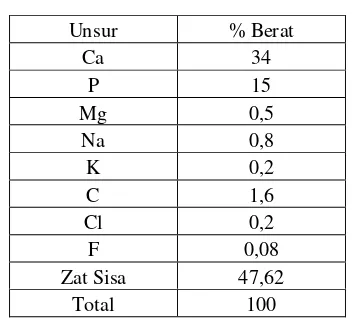
Jaringan keras tulang adalah material komposit alami, yang mengandung 60% mineral, 30% matriks, dan 10% air. Kombinasi yang demikian memberikan fungsi mekanik yang dibutuhkan oleh tulang untuk penyangga tubuh dan pendukung gerakan [9]. Komponen utama material anorganik adalah senyawa kalsium fosfat yang berhubungan erat dengan kristal stabil kalsium fosfat yang biasanya disebut dengan hidroksiapatit (HAP)[10]. Kandungan unsur mineral tulang dapat dilihat pada Tabel 1.
Apatit biologi yang hadir dalam tulang mempunyai karakteristik kristanilitas rendah dan nonstokiometri. Hal ini disebabkan oleh kehadiran ion asing selain ion kalsium dan fosfat. Sebagian ion ini masuk ke dalam kisi kristal apatit dan sebagian lain hanya diabsorpsi pada permukaan kristal [11].
Tabel 1. Kandungan unsur mineral dalam tulang
Unsur % Berat
Ca 34
P 15
Mg 0,5
Na 0,8
K 0,2
C 1,6
Cl 0,2
F 0,08
Zat Sisa 47,62
Total 100
2.3. Mineral Apatit
Apatit adalah istilah umum untuk kristal mineral dengan komposisi M10(ZO4)6X2. Elemen-elemen yang menempati M, Z, dan X adalah:
M = Ca, Mg, Sr, Ba, Cd, Pb, dst. Z = P<V<As, S, Si, Ge, CO3, dst. X = F, Cl, OH, O, Br, CO3, dst.
Hidroksiapatit adalah kalsium fosfat yang mengandung hidroksida, anggota dari kelompok mineral dalam tulang yang memiliki rasio Ca/P dicirikan sebesar 1,67.
Kalsium fosfat memiliki sifat alami yang komplek, seperti dapat hadir dalam berbagai fase, dapat dalam bentuk nonstoikiometri dengan hadirnya impuritas yang mengganti ion kisi dalam kristal, dan dapat pula dalam bentuk larutan padat [12].
Tabel 2. Formula kimia, struktur dan parameter kisi kristal kalsium fosfat [13].
Nama Ca/P Struktur kristal Parameter kisi
HAP 1,67 Heksagonal a = 9,42 Å c = 6,88 Å
DKFD 1,00 Monoklinik
a = 5,81 Å b = 15,18 Å c = 6,24 Å
= 116,4o
OKF 1,33 Triklinik
a = 19,87 Å b = 9,63 Å c = 6,88 Å
α = 8λ,γo = λβ,βo
= 108,9o
Pada umumnya, kalsium fosfat hadir dalam bentuk campuran amorf maupun berbagai kristal (dapat berada dalam berbagai fase).
Formula kimia, struktur dan parameter kisi kristal kalsium fosfat dari tiap fase diperlihatkan pada Tabel 2. Fase-fase tersebut terdiri dari satu fase amorf dan empat fase kristal, yaitu:
1. Kalsium fosfat amorf (KFA), memiliki rumus kimia yang bervariasi, kaya akan HPO42- dan mempunyai harga rasio molar unsur Ca dan P rendah. Selain ion kalsium dan fosfat, ion lain seperti CO32-, HCO3- , Mg2+ dan sebagainya juga dapat masuk dan mengganggu struktur KFA. 2. Dikalsium fosfat dihidrat (DKFD,
Ca2HPO4.2H2O), merupakan tahap awal proses pertumbuhan kristal hidroksiapatit. Kristal DKFD ini memiliki ukuran yang kecil sehingga dalam profil XRD masih tampak seperti amorf. DKFD dapat dihasilkan dari medium dengan pH di bawah 6,6 yang kemudian mengalami hidrolisis dan berubah menjadi OKF. 3. Oktakalsium fosfat (OKF,
Ca8H2(PO4)5H2O), mempunyai struktur yang mirip dengan hidroksiapatit.
4. Trikalsium fosfat (TKF, Ca3(PO4)2), kristal TKF mempunyai kemungkinan kecil dalam salah satu komponen mineral jaringan keras.
Hidroksiapatit (HAP, Ca10(PO4)6(OH)2), merupakan fase kristal yang paling stabil. [13].
2.4. Struktur Kristal Apatit
Struktur hidroksiapatit adalah heksagonal dengan a = b = 9,423 Å dan c = 6,881 Å. Struktur ini dapat dipandang sebagai struktur kristal ideal heksagonal (closed-packed) dari
ion PO43- yang mengalami distorsi akibat kehadiran unsur Ca2+ dan ion OH- di celah antara ion-ion PO43- [14].
Gambar 1. Struktur Hidroksiapatit [15]
Gambar 1. menunjukkan unit sel struktur hidroksiapatit. Unit sel terdiri dari 2 subsel prisma segitiga rombik. Atom Ca ditunjukkan oleh lingkaran hijau, atom O oleh lingkaran biru, dan atom P oleh lingkaran merah. Terdapat dua kaca datar horizontal yaitu pada z = ¼ dan z = ¾ dan sebagai tambahan terdapat bidang tengah inversi tepatnya di setiap tengah muka vertikal dari setiap subsel. Unit sel kristal hidroksiapatit memiliki 2 jenis atom Ca yang disebut Ca1 dan Ca2. Perbedaannya terletak pada lokasi atom Ca. Setiap subsel memiliki 3 pusat. Atom Ca1 puncak dan dasar masing-masing dihitung sebagai ½ Ca1, sementara Ca1 tengah dihitung sebagai satu Ca1 sehingga masing-masing subsel tersebut memiliki 2 atom Ca dari Ca1. Setiap unit sel memiliki 6 atom Ca2. Total atom Ca setiap unit sel adalah 10 yang terdiri dari 4 atom Ca1 dan 6 atom Ca2. Atom-atom Ca2 membentuk 2 segitiga normal hingga sumbu c dan berotasi sebesar 60o [15].
2.5. Kitosan
Kitosan adalah biopolimer natural, berpotensi dalam teknik jaringan. Kitosan banyak terdapat di alam, salah satunya dari kepiting [16]. Sebagai polimer alam keberadaan kitosan di alam kedua setelah selulosa. Kitosan merupakan polisakarida alam yang terdapat di biota laut, dengan strukturnya menyerupai glycosaminoglycansi
[17]. Senyawa ini tidak dapat disintesis secara kimia dan tersusun oleh satuan molekul N-asetil-D-glukosamin [18].
Karakteristik fisikokimia kitosan seperti fleksibilitas rantai dalam larutan, sifat reologi, ukuran kristal dan kristalinitas kitosan bergantung pada faktor intrinsik seperti derajat deasetilasi, distribusi grup asetil, bobot molekular, dan distribusinya [19]. Karakteristik fisikokimia kitosan dapat dilihat pada Tabel 3.
Derajat deasetilasi merupakan salah satu sifat kimia yang penting, yang dapat mempengaruhi kegunaannya dalam berbagai aplikasi. Derajat deasetilasi menyatakan banyaknya gugus amino bebas dalam polisakarida. Kitosan merupakan kitin dengan derajat deasetilasi lebih dari 70%. Deasetilasi adalah proses pengubahan gugus asetil (-NHCOCH3) dari rantai molekular kitin menjadi gugus amina lengkap (-NH2) pada kitosan dengan penambahan NaOH konsentrasi tinggi. Reaksi deasetilasi kitin pada dasarnya adalah suatu reaksi hidrolisis
bergantung pada derajat kimia reaktif yang tinggi gugus aminonya [20].
Kitosan memiliki karakter bioresorbabel, biokompatibel, non-toksik, non-antigenik, biofungsional, dan osteokonduktif. Karakter osteokonduktif yang dimiliki kitosan dapat mempercepat pertumbuhan osteoblas sehingga mempercepat pembentukkan sel-sel tulang [21]. Karakter lain yang dimiliki kitosan adalah tidak larut dalam air, alkali dan pelarut organic tetapi larut dalam larutan asam organikdan dapat terdegradasi oleh enzim dala tubuh. Komposit kitosan apatit dapat meningkatkan bioaktivitas.
2.6. X-Ray Diffraction (XRD)
Adanya struktur kristal dapat dibuktikan dengan percobaan difraksi sinar-X. Berkas gelombang elektromagnetik yang mengenai kristal mengalami difraksi sesuai dengan hukum fisika [22].
X-Ray Diffraction (XRD) digunakan untuk
mengetahui nilai parameter kisi, struktur kristal dan derajat kekristalan. Derajat kekristalan adalah besaran yang menyatakan banyaknya kandungan kristal dalam suatu materi dengan membandingkan luasan kurva puncak dengan total luasan amorf dan kristal [23].
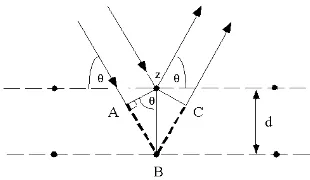
Gambar 3. Sinar-X Menumbuk Atom
Sinar-X berinteraksi dengan elektron di dalam atom. Ketika foton sinar-X menumbuk elektron, beberapa foton akan dihamburkan dengan arah yang berbeda dari arah datangnya seperti halnya bola biliar yang saling bertumbukkan. Gelombang difraksi dari atom yang berbeda-beda dapat saling berinterferensi maksimal yang tajam (puncak-puncak) dengan kesimetrian sama yang menggambarkan distribusi atom-atom. Pengukuran pola difraksi akan menggambarkan distribusi atom di dalam bahan [24].
Puncak-puncak pola difraksi sinar-X berhubungan dengan jarak antar bidang. Jika sinar-X dilewatkan pada atom-atom yang tersusun secara teratur dan periodik seperti diilustrasikan pada gambar secara dua dimensi dimana jarak antar bidang adalah d, maka
difraksi dapat dituliskan sebagai
2 d sin θ = n λ (1)
Persamaan tersebut dikenal sebagai hukum
Bragg. Pada persamaan, merupakan panjang gelombang sinar-x, θ adalah sudut hamburan dan n adalah orde difraksi.
Parameter kisi HAp telah diketahui memiliki sistem heksagonal, yakni dengan menggunakan persamaan [24]:
2 2 2 2 2 2 3 4 1 c l a k hk h d (2)
Ukuran kristal dihitung dengan menggunakan persamaan Scherrer sebagai berikut: k D C os
(3)
dimana β merupakan FWHM (Full width at half maximum) dari garis difraksi skala βθ,
merupakan panjang gelombang yang digunakan pada alat XRD yaitu 0,15406 nm dan k adalah konstanta untuk material biologi
yang nilainya adalah 0,94.
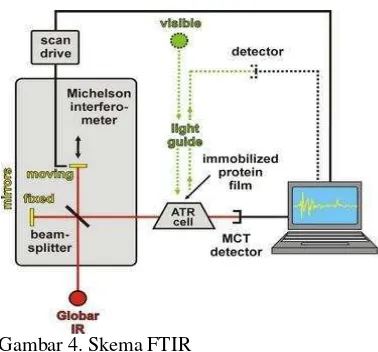
2.7. Spektroskopi Fourier Transform Infrared (FTIR)
FTIR merupakan salah satu teknik spektroskopi inframerah yang dapat mengidentifikasi kandungan gugus kompleks No Parameter Ciri
1 Ukuran partikel Serbuk sampai bubuk
2 Warna Putih kelabu
3 Kelarutan 97% dalam 1% asam asetat 4 Kadar abu (%) 2,0 5 Kadar air (%) 10,0 6 Warna larutan Tak berwarna 7 N-deasetilasi (%) 70,0
8 Ph 6,5 – 8,0
9 Viskositas (cPs)
- rendah 200 - medium 200 – 799 - tinggi 800 – 2000 - sangat tinggi 2000 Gambar 2 Struktur kimia kitosan
dalam senyawa kalsium fosfat, tetapi tidak dapat digunakan untuk menentukan unsur-unsur penyusunnya. Pada spektroskopi inframerah, spektrum inframerah terletak pada daerah dengan panjang gelombang 0,78
sampai 1000 m atau bilangan gelombang
dari 12800 sampai 1 cm-1. FTIR termasuk ke dalam kategori radiasi inframerah pertengahan (bilangan gelombang 4000-200 cm-1).
Plot antara presentase transmitansi dengan bilangan gelombang akan menghasilkan spektrum inframerah dan setiap tipe ikatan yang berbeda mempunyai frekuensi vibrasi yang sedikit berbeda, maka tidak ada dua molekul yang berbeda strukturnya akan mempunyai bentuk serapan inframerah atau spektrum inframerah yang sama [25]. FTIR memanfaatkan energi vibrasi gugus fungsi penyusun senyawa hidroksiapatit, yaitu gugus PO43-, gugus CO32-, serta gugus OH-.
Gugus PO43- mempunyai empat mode vibrasi yaitu:
1. Vibrasi simetri stretching (υ1) dengan
bilangan gelombang sekitar 956 cm-1 2. Vibrasi simetri bending (υ2) dengan
bilangan gelombang sekitar 430-460 cm-1 3. Vibrasi asimetri stretching (υ3) dengan
bilangan gelombang sekitar 1040-1090 cm-1
4. Vibrasi asimetri bending (υ4) dengan
bilangan gelombang sekitar 575-610 cm-1
Bentuk pita υ3 dan υ4 yang tidak simetri merupakan tanda bahwa senyawa hidroksiapatit tidak seluruhnya dalam bentuk amorf. Spektrum hidroksiapatit dapat diteliti
yaitu pada υ4 dalam bentuk belah dengan maksimum 562 cm-1 dan 602 cm-1. Pita
absorpsi υ3 mempunyai dua puncak maksimum yaitu pada bilangan gelombang 1090 cm-1 dan 1030 cm-1. Pita absorpsi υ1 dapat dilihat pada bilangan gelombang 960 cm-1 [26].
Puncak pada 633 cm-1 dan 3570 cm-1 menunjukkan vibrasi dari OH. Luas puncak pada 3500 cm-1 dan puncak pada 1660 cm-1 menunjukkan penyerapan air [15,17]. Ikatan karbonat teramati pada 870 dan 1430cm-1[27]. Kitosan murni ditunjukkan pada puncak 1255 cm-1 dan 1040 cm-1 menunjukkan amino primer yang bebas (-NH2) pada posisi C2 dari
glucoseamine, kelompok utama pada kitosan.
Puncak pada 1380, 1420, 2870 dan 2920 cm_1 berkaitan dengan C-H. Ikatan pada 280 dan 2920 cm-1 adalah
aliphatic C-H stretching.
Ada sebuah penyerapan ikatan amida pada 1565 cm-1. Bilangan gelombang 1605cm-1 berkaitan dengan C=O.
Gambar 4. Skema FTIR
Puncak pada 3420 cm-1 menunjukkan –OH
stretching. Ada sebuah amino asetil pada
puncak 1650 cm-1 yang diindikasikan sebagai kitosan tidak mengalami deacetylated secara
penuh.[28].
Spektra inframerah kitosan murni menginformasikan adanya pita serapan gugus fungsi –OH pada bilangan gelombang 3433,45 cm-1. Pita serapan yang lebar dan kuat pada daerah 3450-3200 cm-1 tersebut tumpang tindih dengan gugus N-H amina. Pita serapan utama lainnya antara 1220-1020cm-1 menunjukkan gugus amino bebas primer (-NH2), suatu gugus utama dalam kitosan serta mengindikasikan vibrasi regang C-O dari gugus alkohol. Serapan pada bilangan gelombang 2921,18 cm-1 mengindikasikan vibrasi regang -CH2- dari gugus –CH. Pita serapan antara 1640–1560 cm-1 menunjukkan vibrasi bending N-H dari gugus amina yang
merupakan serapan karakteristik kitosan. Selain itu, serapan dengan intensitas medium pada bilangan gelombang 1379,61 dan 1454,37cm-1 merupakan vibrasi
bending -CH3 dari gugus C-H [29].
2.8. Scanning Electron Microscopy (SEM)
Scanning Electron Microscopy (SEM)
merupakan alat yang dapat membantu mengatasi permasalahan analisis struktur mikro dan morfologi dalam berbagai bidang. Pemercepat elektron (electron gun)
Gambar 5. Skema SEM
koil penyearah untuk membentuk gambar dan diteruskan ke lensa akhir untuk difokuskan ke sampel. Interaksi pancaran elektron dengan sampel dan elektron yang dipantulkan diterima oleh detektor. Detektor akan menghitung elektron-elektron yang diterima dan menampilkan intensitasnya.
Energy Dispersive X-Ray (EDXA)
merupakan satu perangkat dengan dengan SEM. Pengukuran EDXA merupakan perangkat analisa sedara kuantitatif untuk menentukan kadar unsur dalam sampel.
3. BAHAN DAN METODE
3.1. Bahan dan Alat
Bahan yang digunakan yaitu CaCl2.2H2O(s) pro analis, Na2HPO4.2H2O(s) pro analis, kitosan, CH3COOH 2%, aquades, aquabides,
dan gas nitrogen (N2). Alat yang digunakan antara lain buret, beaker glass, statip, gelas
ukur, labu takar, corong, kertas saring,
furnace, incubator, magnetic stirrer, hot plate,
termometer digital, sudip, neraca analitik, dan sentrifuse.
Karakterisasi menggunakan X-Ray Diffraction (XRD), Scanning Electron Microscopy (SEM), Fourier Transform Infra Red (FTIR), dan Uji Mekanik.
3.2. Metode Penelitian 3.2.1. Preparasi Sampel
Senyawa Na2HPO4.2H2O dan CaCl2.2H2O masing-masing dilarutkan dengan aquabides sebanyak 50ml. Komposisi massa yang digunakan Na2HPO4.2H2O 1,7801g, CaCl2. 2H2O 2,4554g. Komposisi massa ini diperoleh dengan menggunakan perbandingan molaritas Ca/P sebesar 0,334:0,2.
Untuk larutan kitosan, komposisi massa kitosan yang digunakan yaitu menggunakan perbandingan 35:55 (massa kitosan:massa HAP). Massa HAP didapat dari hasil presipitasi sampel kontrol. Kitosan dilarutkan dengan asam asetat 2%.
Pada penelitian ini dilakukan dua metode pada sampel yaitu in-situ dan ex-situ.
Perbedaan kedua metode ini terletak pada proses penambahan kitosan saat presipitasi sampel berlangsung.
3.2.2. Kontrol
Pada kontrol dibuat HAP murni yang dihasilkan dari proses presipitasi tanpa menggunakan tambahan kitosan.
Larutan Na2HPO4.2H2O 50 ml disiapkan dalam beaker glass yang diletakkan di atas hot plate dalam kondisi atmosfir nitrogen.
Ketika suhu larutan Na2HPO4.2H2O 50 ml mencapai 70oC, larutan CaCl2.2H2O 50ml diteteskan ke dalamnya dengan kecepatan konstan menggunakan buret. Selama proses presipitasi berlangsung, suhu larutan tetap dikontrol pada 70oC dengan kecepatan stirring sekitar 400 rpm. Setelah proses presipitasi selesai, larutan di-agging selama 24 jam
kemudian dipanaskan dalam inkubator pada suhu 50oC selama 48 jam.
3.2.3. In-situ
Pada metode in-situ proses pembentukkan
mineral apatit dilakukan dalam matrik kitosan. Larutan Na2HPO4.2H2O 50 ml dalam beaker glass ditambahkan dengan larutan kitosan
kemudian diletakkan di atas hot plate dalam
kondisi atmosfir nitrogen.
Ketika suhu larutan Na2HPO4.2H2O 50 ml dan kitosan mencapai 70oC, larutan CaCl2.2H2O 50 ml diteteskan ke dalamnya dengan kecepatan konstan menggunakan buret. Selama proses presipitasi berlangsung, suhu larutan tetap dikontrol pada 70oC dengan kecepatan stirring sekitar 400 rpm. Setelah proses presipitasi selesai, larutan di-agging
selama 24 jam kemudian dipanaskan dalam inkubator pada suhu 50oC selama 48 jam.
3.2.4. Ex-situ
Pada metode ex-situ, penambahan larutan
kitosan dilakukan setelah proses presipitasi selesai dilakukan. Larutan Na2HPO4.2H2O 50 ml disiapkan dalam beaker glass yang
diletakkan di atas hot plate dalam kondisi
atmosfir nitrogen.
konstan menggunakan buret. Selama proses presipitasi berlangsung, suhu larutan tetap dikontrol pada 70oC dengan kecepatan
stirring
sekitar 400 rpm.
Setelah proses presipitasi selesai, larutan kitosan diteteskan dengan menggunakan pipet. Selama penetesan, suhu larutan dan kecepatan
stirring tetap dikontrol masing-masing pada
70oC dan 400 rpm. Larutan kemudian
di-agging selama 24 jam kemudian dipanaskan
dalam inkubator pada suhu 50oC selama 48 jam.
3.2.5. Karakterisasi XRD
Alat yang digunakan pada karakterisasi XRD ini adalah Shimidzu XRD 7000 dengan sumber target CuK α ( = 1.54056 Angstrom). Sampel yang akan dikarakterisasi berbentuk serbuk yang diletakkan dalam holder yang
berukuran 2x2 cm2 pada difraktometer.
3.2.6. Karakterisasi FTIR
Sampel yang akan diuji dengan FTIR dibuat dalam bentuk pelet inframerah (IR). Pelet dibuat dengan mencampurkan dua mg sampel dengan 100 mg KBr yang kemudian di IR dengan jangkauan bilangan gelombang 4000 – 400 cm-1. Pada setiap pengukuran, pelet KBr selalu dijadikan satu agar latar belakang absorpsi dapat dihilangkan.
3.2.7. Karakterisasi SEM/EDXA
Sampel diletakkan pada plat aluminium yang memiliki dua sisi. Sampel tersrbut kemudian dilapisi dengan lapisan emas setebal 48 nm. Sampel yang telah dilapisi tersebut dikarakterisasi SEM dengan tegangan 22 kV dan perbesaran 5000x, 10.000x dan 20.000x.
Tabel 4 Kode Sampel
Kode
Sampel Komposisi Penambahan Kitosan
A
(Kontrol) CaCl2.2H2O + Na2HPO4.2H2O -
B (In-situ)
CaCl2.2H2O +
Na2HPO4.2H2O Sebelum presipitasi
C (Ex-situ)
CaCl2.2H2O +
Na2HPO4.2H2O Setelah presipitasi
4. HASIL DAN PEMBAHASAN
4.1. Analisa XRD
Karakterisasi XRD dilakukan untuk mengetahui fasa yang terbentuk pada sampel, derajat kristanilitas sampel, parameter kisi kristal dan ukuran kristal sampel. Analisa yang dilakukan dengan mencocokkan data JCPDS (Joint Committee on Powder Diffraction Standards). Berikut ini adalah
pola XRD yang didapat dari masing-masing sampel.
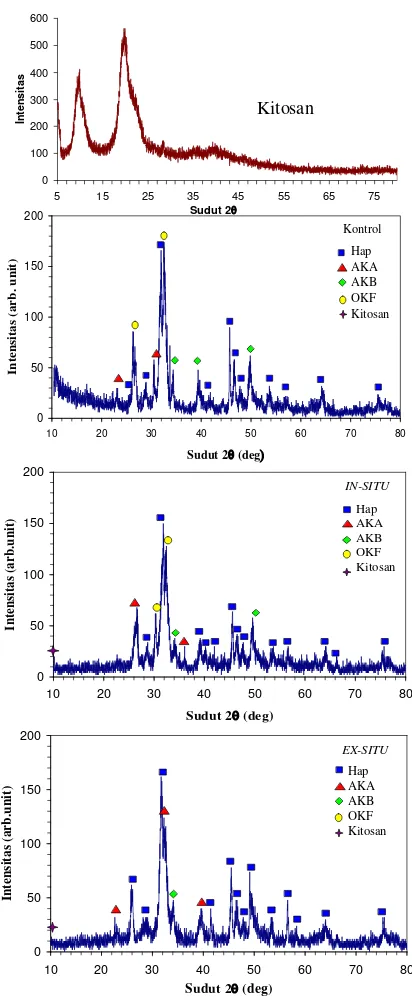
Gambar 6 Pola XRD Kitosan murni, sampel kontrol, In-situ dan Ex-situ
Kitosan 0 100 200 300 400 500 600
5 15 25 35 45 55 65 75
Sudut 2
Int e ns it a s Kitosan Kontrol 0 50 100 150 200
10 20 30 40 50 60 70 80
Sudut 2 (deg)
Intensita s (a rb. u nit) Hap AKA AKB OKF Kitosan 0 50 100 150 200
10 20 30 40 50 60 70 80
Sudut 2(deg)
Intensita s (a rb.un it) IN-SITU Hap AKA AKB OKF Kitosan 0 50 100 150 200
10 20 30 40 50 60 70 80
Sudut2 (deg)
Gambar 6 memperlihatkan pola XRD yang terbentuk pada kitosan murni dan ketiga sampel. Pola XRD kitosan murni memperlihatkan puncak-puncak karakteristik
pada βθ = λ,88o dan 19,86o. Dari pola tersebut juga terlihat bahwa kitosan murni memiliki struktur campuran antara kristalin dan amorf. Pola XRD untuk ketiga sampel memperlihatkan bahwa sebagian besar fasa yang terbentuk pada masing-masing sampel adalah HAP. Fasa lainnya yang terbentuk yaitu apatit karbonat tipe-A (AKA), apatit karbonat tipe-B (AKB), dan okta-kalsium fosfat (OKF). Pada sampel kontrol, puncak-puncak yang terbentuk tidak semuanya hadir dalam fasa HAP. Puncak tertinggi yang didapat pada sampel kontrol merupakan milik OKF. Puncak tertinggi HAP kontrol yaitu
pada sudut βθ = γ1,λ40. Pada sampel
in-situ,
puncak tertinggi yang terbentuk merupakan milik HAP yakni pada sudut βθ = γ1,840. Puncak tertinggi pada ex-situ, fase yang
terbentuk merupakan milik HAP yaitu pada
sudut βθ = γ1,740. Hadirnya fase karbonat pada sampel dapat terjadi karena pada struktur HAP karbonat dapat menggantikan ion OH -dengan membentuk AKA dan menggantikan ion PO4- dengan membentuk AKB. Pada umumnya presipitasi pada temperatur rendah akan membentuk AKB, sedangkan apatit yang dipresipitasi pada temperatur tinggi akan menghasilkan AKB.
Pola XRD sampel komposit apatit-kitosan baik pada in-situ maupun ex-situ,
memperlihatkan adanya puncak milik kitosan yang muncul di beberapa titik sudut. Pada sampel in-situ, puncak milik kitosan muncul
pada sudut βθ = 10,160. Sementara pada sampel ex-situ, memiliki puncak bersama
yaitu milik kitosan dan HAP yang terletak
pada sudut βθ = 10,8β0. Munculnya puncak milik kitosan pada komposit apatit-kitosan ini menandakan bahwa apatit telah mengisi matrik kitosan. Rendahnya intensitas yang dimiliki oleh puncak kitosan terjadi karena kitosan telah menyebar dalam sampel dan struktur dari kitosan yang lebih amorf dibandingkan kristal apatit.
Pengukuran derajat kristanilitas diperoleh langsung dari program karakterisasi XRD. Derajat kristanilitas merupakan besaran yang menyatakan banyaknya kandungan kristal dalam suatu material dengan membandingkan luasan kurva kristal dengan luasan amorf dan kristal. Penambahan kitosan baik pada metode
in-situ dan ex-situ mempengaruhi nilai derajat
kristanilitas pada sampel. Pada Tabel 5 terlihat perbedaan derajat kristanilitas yang diperoleh
pada sampel kontrol, in-situ, dan ex-situ. Dari
tabel tersebut memperlihatkan bahwa sampel kontrol memiliki derajat kristanilitas paling tinggi yaitu 84,26% dibandingkan dengan sampel in-situ (62,59%) dan sampel ex-situ
(73,89%). Hal ini menunjukkan bahwa penambahan kitosan pada komposit Apatit-kitosan mengakibatkan menurunnya nilai derajat kristanilitas dibandingkan sampel kontrol yang tanpa penambahan kitosan.
Sampel in-situ memiliki derajat
kristanilitas lebih rendah dibandingkan sampel
ex-situ. Hal ini dapat terjadi karena dalam
metode in-situ proses pembentukkan mineral
apatit dilakukan dalam matrik kitosan, sehingga kitosan lebih banyak menyebar dan mengakibatkan sampel bersifat lebih amorf.
Penambahan kitosan yang mengakibatkan turunnya nilai kristanilitas ini mengindikasikan bahwa kitosan telah berikatan dengan apatit.
Pada Tabel 6 memperlihatkan nilai ukuran kristal sampel yang dihitung menggunakan persamaan Scherrer. Ukuran kristal yang diperoleh pada sampel berkisar antara 23-25 nm. Ukuran kristal antara apatit dan komposit apatit-kitosan tidak menunjukkan perbedaan yang signifikan. Ukuran kristal yang diperoleh ini berbanding terbalik dengan nilai FWHM, sampel yang memiliki FWHM yang rendah akan menghasilkan ukuran kristal yang lebih besar.
Parameter kisi dapat dihitung dengan menggunakan jarak antar bidang pada geometri kristal heksagonal dengan menggunakan persamaan (1) dan (2).
Hasil parameter kisi dapat dilihat pada Tabel 7. Berdasarkan hasil perhitungan, parameter kisi sampel berada pada kisaran HAp dengan nilai akurasi mencapai 98-99%, sehingga dapat dikatakan bahwa fase yang terbentuk pada sampel adalah HAP.
Tabel 5. Derajat kristanilitas sampel Sampel Kristalinitas (%)
Kontrol 84,26
In-situ 62,59
Ex-situ 73,89
Tabel 6. Ukuran kristal sampel Kode
Tabel 7. Parameter kisi sampel
Kode Sampel
Parameter Kisi
a (Å) Accuracy c (Å) Accuracy
A 9,718 96,872 6,997 98.311
B 9,581 98,321 6,908 99,614
C 9,617 97,936 6,954 98,938
4.2. Analisa FTIR
Spektroskopi FTIR mengidentifikasi gugus fungsi yang terbentuk pada sampel. Gugus fungsi yang teridentifikasi pada HAP diantaranya adalah gugus fosfat (PO4), gugus karbonat (CO3), dan gugus hidroksil (OH). Pada komposit apatit-kitosan muncul gugus NH2, C-H, amida I dan amida II yang merupakan karakteristik dari kitosan.
Tabel 8 memperlihatkan peta absorpsi FTIR dari keseluruhan sampel. Spektrum IR pada ketiga sampel tersebut menunjukkan adanya pita absorpsi fosfat υ1, υ3, dan υ4, pita
absorpsi karbonat υ2 dan υ3, serta pita absorpsi hidroksil. Munculnya ketiga gugus tersebut menandakan bahwa pada sampel kontrol, in-situ dan ex-situ telah terbentuk HAP. Pada
sampel kontrol (A), pita absorpsi fosfat υ1 muncul pada bilangan gelombang 961 cm-1.
Sementara pita absorpsi fosfat υ3 muncul pada bilangan gelombang 1035 cm-1 dan 1085 cm-1.
Gugus fosfat υ4 pada sampel A muncul pada bilangan gelombang 563 cm-1 dan 607 cm-1. Gugus karbonat pada sampel A hadir pada kisaran bilangan gelombang 893 cm-1 dan 896 cm-1. Gugus hidroksil pada sampel A muncul
pada bilangan gelombang 1636 cm-1 dan
3439 cm-1. Pada sampel
in-situ (B) dan ex-situ
(C) telah terbentuk gugus NH2, C-H dan amida I yang merupakan karakteristik dari kitosan. Pada sampel B, gugus NH2 bertumpuk dengan gugus milik OH sehingga pada spektra FTIR terlihat lebih lebar pada daerah bilangan gelombang 3430 cm-1. Gugus C-H juga muncul pada sampel in-situ . Gugus
C-H muncul pada bilangan gelombang 2930 cm-1. Gugus amida I pada sampel B muncul pada bilangan gelombang 1634 cm-1. Gugus amida yang hadir ini bertumpukan dengan gugus OH sehingga pita serapan terlihat sedikit lebih lebar. Pada sampel ex-situ (C)
gugus NH2 terbentuk pada bilangan gelombang 3152 cm-1 dan 3404 cm-1. Gugus amida muncul pada sampel ex-situ (C).
Gugus ini terbentuk bertumpukan dengan gugus OH. Hadirnya gugus NH2, C-H, dan amida pada sampel B dan C yang merupakan karakteristik dari kitosan menandakan bahwa kitosan telah berikatan dengan apatit. Kemunculan gugus fungsi HAp dan gugus fungsi NH2, C-H, dan amida yang merupakan milik kitosan menandakan bahwa komposit apatit-kitosan pada sampel B dan C telah berhasil terbentuk. Penambahan kitosan dengan metode in-situ dan ex-situ tidak
memperlihatkan hasil yang terlalu signifikan. Gusus fungsi yang hadir pada kedua sampel sama hanya berbeda pada nilai transmisinya saja. Hal ini bisa dilihat dari bentuk spektra pada Gambar 7.
Kode Sampel
Pita Absorpsi (cm-1)
PO4 (υ1)
PO4 (υ3)
PO4 (υ4)
CO3 (υ2)
CO3
(υ3) OH NH2 C-H
Amida I
Amida II
A
961 1035 563 893 1636 - - - -
1085 607 3439
B
960 1032 562 894 1402 1634 3430 2930 1634 -
605 896 3430
C
960 1030 562 869 1403 1633 3404 1633
[image:30.595.108.514.535.719.2]605 3404 3152
a
b
c
d
4.3. Analisa Morfologi SEM dan EDXA
[image:31.595.133.503.49.242.2]Karakterisasi SEM dilakukan untuk mengetahui morfologi sampel pada skala mikro. Untuk mengetahui kandungan Ca dan P yang dimiliki pada sampel apatit dan komposit apatit-kitosan maka dilakukan karakterisasi EDXA. Gambar 8 memperlihatkan hasil analisa SEM pada keenam sampel dan morfologi kitosan murni.
Gambar 8. Struktur morfologi SEM sampel (a) Kontrol, (b) In-situ, (c) Ex-situ, dan (d) kitosan murni.
0 500 1000 1500 2000 2500 3000 3500 4000 4500
Bilangan Ge lombang (cm-1)
Tr
an
sm
ita
ns
i Kontrol
[image:31.595.319.503.279.664.2]In-situ Ex-situ Kitosan
[image:31.595.111.295.382.747.2]Partikel apatit dalam komposit menyebar seragam, dapat terlihat melalui matriks kitosan yang telah saling berhubungan antar sel. Bentuk pori-pori terlihat berubah dibandingkan sampel HAP sendiri, dalam sampel kitosan murni pori-pori lebih datar dan ketika HAP bergabung pori-pori terlihat lebih banyak membulat [30] .
Morfologi sampel kitosan murni pada Gambar 8d memperlihatkan struktur kitosan dengan pori-pori yang tampak kecil dan permukaan yang halus dan datar. Pada sampel kontrol (a) yang merupakan HAP tanpa penambahan kitosan, permukaannya terlihat datar dan butiran-butiran yang terbentuk berukuran relatif kecil dan halus. Sementara pada sampel in-situ (b) morfologi
permukaannya terlihat lebih kasar dan berbentuk bongkahan-bongkahan sehingga pori-pori yang terbentuk menjadi lebih besar. Pada sampel ex-situ (c), morfologi yang
terbentuk juga berupa bongkahan dan permukaannya terlihat kasar dibandingkan dengan kontrol.
Secara umum morfologi sampel (b) dan (c) tidak terlihat berbeda secara signifikan. Morfologi komposit apatit-kitosan yang berupa bongkahan pada sampel (b) dan (c) menunjukkan bahwa telah terbentuk komposit apatit-kitosan, dimana kitosan berperan sebagai matrik tempat apatit tumbuh.
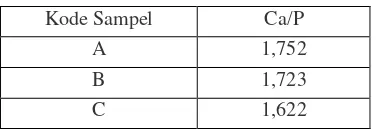
Rasio molaritas Ca/P diperoleh dengan pengukuran EDXA yang dilakukan bersamaan dengan karakterisasi SEM. Rasio Ca/P pada HAp adalah 1,67 [4]. Rasio Ca/P yang diperoleh relatif lebih besar, kecuali pada sampel ex-situ dimana rasio Ca/P sedikit lebih
kecil. Nilai rasio Ca/P yang diperoleh dapat dipengaruhi oleh munculnya gugus karbonat seperti yang terlihat dari hasil analisa FTIR dan XRD. Pada FTIR menunjukkan adanya pita absorpsi milik karbonat dan pada analisa XRD menunjukkan bahwa terdapat fasa lain yang terbentuk selain HAP yaitu AKA, AKB dan OKF. Kehadiran karbonat ini akan mempengaruhi jumlah Ca dan P pada sampel, sehingga rasio yang didapatkan tidak tepat 1,67.
Rasio Ca/P didapatkan dengan membandingkan persentasi massa dibagi dengan massa relatif Ca dan P, sehingga akan
didapatkan perbandingan molaritas antara Ca dan P.
4.4. Uji Kekerasan Vickers
Uji kekerasan sampel diukur dengan perangkat uji vickers. Alat yang digunakan
adalah shimadzu micro hardness tester tipe
M, Shimadzu Corporation Kyto-Jepang. Untuk melakukan uji kekerasan, sampel yang akan diuji permukaannya harus rata. Salah satu cara yang digunakan untuk mendapatkan sampel yang memiliki permukaan rata adalah dengan metode
molding. Proses molding dilakukan dengan
cara menambahkan epoxy resin dan hardener
pada sampel di suatu cetakan. Setelah itu cetakan sampel tersebut dibiarkan sampel mengering. Setelah mengering kemudian dipoles dengan ampelas hingga permukaannya rata dan sampel siap dikarakterisasi.
Uji kekerasan sampel dilakukan pada tiga titik yang berbeda posisi. Namun setelah dilakukan pengujian kekerasan ternyata sampel kontrol, in-situ dan ex-situ tidak dapat
terukur. Hal ini dikarenakan struktur sampel yang terlalu lunak.
4.5. Massa Komposit Apatit-Kitosan
Massa komposit merupakan massa yang dihasilkan dari penambahan massa apatit dan massa kitosan. Tabel 10 memperlihatkan massa komposit yang dihasilkan.
Massa sampel A (apatit) yang dihasilkan yaitu 1,8784 g. Sementara pada sampel B ( in-situ) dan C (ex-situ) yang merupakan
komposit apatit-kitosan dihasilkan massa yang lebih banyak. Massa sampel B yang dihasilkan yaitu 2,0257 g dan sampel C sebesar 2,2095 g. Hal ini menunjukkan telah terjadi ikatan antara apatit dan kitosan.
Kode Sampel Ca/P
A 1,752
B 1,723
C 1,622
Kode Sampel
Massa
(Na)2HPO4
(gram) CaCl2 (gram) Kitosan (gram) Komposit (gram)
A 3,5602 4,9108 - 1,8784
B 3,5599 4,9105 1,1950 2,0257
[image:32.595.113.301.91.156.2]C 3,5599 4,9103 1,1953 2,2095
[image:32.595.322.529.561.678.2]Tabel 9 Rasio Molaritas Ca/P Sampel
Apatit-5. SIMPULAN DAN SARAN
5.1. Simpulan
Pembuatan komposit apatit-kitosan dapat dilakukan dengan metode in-situ dan ex-situ.
Karakterisasi XRD menunjukkan bahwa baik pada sampel in-situ maupun ex-situ terdapat
puncak milik kitosan, selain itu hadirnya kitosan juga ditandai dengan menurunnya derajat kristanilitas dari sampel komposit apatit-kitosan menjadi lebih rendah dibandingkan dengan sampel apatit. Penurunan derajat kristanilitas ini dikarenakan fasa kitosan yang lebih amorf dibandingkan dengan apatit. Derajat kristanilitas yang dimiliki sampel ex-situ lebih besar
dibandingkan in-situ, hal ini dikarenakan
proses pembentukan apatit tidak dihalangi oleh kitosan, sehingga lebih kristal dibandingkan in-situ. Pada karakterisasi FTIR
terlihat adanya pita absorpsi NH2, C-H, dan amida yang merupakan karakteristik pada kitosan yang hadir pada sampel in-situ dan ex-situ. Baik in-situ maupun ex-situ tidak terlihat
perbedaan morfologi yang signifikan. Gugus fungsi yang hadir pada kedua sampel tersebut sama, hanya berbeda pada nilai transmisinya. Hal ini menunjukkan bahwa apatit telah berikatan dengan kitosan. Karakterisasi SEM juga memperlihatkan telah terbentuknya komposit apatit-kitosan yaitu morfologi in -situ dan ex-situ yang berbentuk bongkahan,
yang mengindikasikan bahwa apatit telah tumbuh dalam kitosan yang berperan sebagai matrik.
5.2. Saran
Untuk penelitian lebih lanjut dapat divariasikan konsentrasi Ca/P dan suhu presipitasi agar mendapatkan komposit apatit-kitosan yang lebih biokompatibel. Selain itu pH sampel saat presipitasi sebaiknya dikontrol tetap 7 agar sifat biokompatibel tercapai.
6. DAFTAR PUSTAKA
1. Tadic, A., Beckmann, F. et all. 2003. A novel Methode to Produce Hydroxyapatite Object with Interconnecting Porosity that Avoids Sintering. www.elsevier.com
2. Baht, Sujata V. 2002. Biomaterials.
Pangbone England: Alpha Science International Ltd.
3. Riyani, Esti. 2005. Karakterisasi Senyawa Kalsium Fosfat Karbonat Hasil Presipitasi Menggunakan XRD (X-Ray Diffraction),
SEM (Scanning Electron Microscopy) dan EDXA (Energy Dispersive X-Ray Analysis): Pengaruh Penambahan Ion F -dan Mg2+ [Skripsi]. Bogor: Institut Pertanian Bogor.
4. Aoki, Hideki. 1991. Science and Medical Application of Hydroxyapatite. JAAS:
Tokyo, Japan.
5. Wang YX, JL Robertson, WB Spillman, RO Claus. 2004. Effects of the Chemical Structure and the Surface Properties of Polymeric Biomaterials on Their Biocompatibility Pharmaceutical Research. 21(8): 1363-1372.
6. [Anonim]. The StructureFunction of Bones. http://www.ivy-rose.co.uk. [11
Januari 2009]
7. Spence, Alexander P. dan Mason, Elliot B. 1987. Human Anatomy and Physiology Third Edition. California: The Benjamin/
Cummings Publishing Company, Inc. 8. Swindler, Daris R. 1998. Introduction to
the Primates. USA: University of
Washington Press.
9. Betts F., NC. Blumenthal, A.S. Posner. 1981. Bone Mineralization, J. Cryst. Growth, 53: 63.73.
10. Mathew Mathai, Shozo Takagi. 2001.
Structure of Biological Minerals in Dental Research. Journal of Research of
The National of Standard and Technology. 106: 1035-1044.
11. Bigi A, E. Foresti, R. Gregorini, A. Ripamonti, N. Roveri, and J. S. Shah. 1992. The Role of Magnesium on the Structure of Biological Apatites. Calc.
Tiss. Int. 50: 439-444.
12. Soejoko S. D. 1999. Kajian Komposisi dan Struktur Senyawa Mineral dalam Kutikula Macrobrachium Rosenbergi dan Paneaus Monodon serta evolusinya
selama perioda molting. [Disertasi]. Bandung: Institut Teknologi Bandung. 13. Solechan A. 2001. Pengukuran Derajat
Kekristalan Tulang Tikus pada Berbagai umur dengan XRD. [Skripsi]. Depok. Universitas Indonesia Fakultas Matematika dan Ilmu Pengetahuan Alam. 14. Calderin L., M. J. Stott, A. Rubio. 2003.
Electronic and Crystallographic Structure of Apatite. Physical Review B
67, 134106.
15. Hanson, Bob. 2005. 150000000:1 Model of Hydroxyapatite.
www.stolaf.edu./people/hansonr [15 Januari 2009].
Nano-Sized Hydroxyapatite Particles and Hydroxyapatite/Chitosan Nano-Composite for Use in Biomedical Materials. Materials Letters: 57: 858-861.
17. TH Ang, FSA Sultana, DW Hutmacher, YS Wong, JYH Fuh, XM Mo, HT Loh, E Burdet, SH Teoh. 2002. Fabrication of 3D Chitosan Hydroxyapatite Scaffolds Using a Robotic Dispensing System.
Materials Science and Engineering C. 20:
35-42
18. Suhartono MT. 2006. Pemanfaatan Kitin, Kitosan, dan Kitooligosakarida.
http://www.wordpress.com. [21 Januari 2009].
19. Jin Li, Jun Cai, Lihong Fan. 2008. Effect of Sonolysis on Kinetics and Physicochemical Properties of Treated Chitosan. Journal of Applied Polymer Science, Vol. 109, 2417-2425.
20. Khan TA, Kok KP, Hung SC. 2002.
Reporting Degree of Deacetilation Values of Chitosan: The Influence of analytical Methods. J Pharm Pharmaceut Sci. 5:
205-212.
21. Lew H, DH Shin, SY Lee, SJ Kim, JW Jang. Osseous Metaplasia with Functioning Bone Marrow in Hydroxyapatite Orbital Implants.
Graefe’s Arch Clin Exp Ophthalmol. 2000; 238: 366-368.
22. Cullity BD., Stock, SR. 2001. Elements of X-Ray Diffraction. Prentice Hall:New
Jersey.
23. [Anonim]. 2005. Introduction to X-ray Diffraction. Materials Research Laboratory. University of California. http://www.mrl.ucsb.edu. [21 Januari 2009].
24. Vlack, Van. 1995. Ilmu dan Teknologi Bahan. Jakarta: PT. Gramedia Pustaka
Utama.
25. Koutsopoulus S. 2002. Syntesis and Characterization of Hydroxyapatite Crystals: A review on The Analytical
Methode. Departement of Chemistry, University of Patras, Greece.
26. Hidayat Y. 2005. Pengaruh Ion Karbonat, Magnesium dan Flour dalam Presipitasi
Senyawa Kalsium Fosfat : Karakterisasi dengan Menggunakan Atomic Absorption Spectroscopy (AAS), Spectroscopy UV-VIS, dan Fourier Transform Infrared
(FTIR) [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
27. Yamaguchi,I. Tokuchi. K, Fukuzaki, H, Koyama, Y, Takakuda K, Monma J, Tanaka, H. 2001. “Preparation and
microstructure analysis of chitosan/HA
nanocomposite”, ppβ0-27,Vol55,Journal of BiomedicalMaterial Research.
28. Saraswathy,.G, Pal.S.C, Rose.T.P.A. 2000. Novel Bio-Inorganic Bone Implant Containing Deglued Bone, Chitosan and Gelatin.pp.415-420.Vol.24. Buletin of Material Science.
29. Yildirim,Oktay.2004. Preparation and Characterization of Chitosan/Calsium Phosphate Based Composite Biomaterials.[disertasi]. Turki:
Lampiran 1. Diagram Alir Penelitian
Penyediaan alat dan bahan
Siap
Sintesis apatit sebagai
kontrol
Penentuan jumlah kitosan yang akan
digunakan dengan perbandingan
kitosan dengan apatit kontrol 35:55
Analisis Data
Tidak
Karakterisasi XRD, FTIR, SEM, dan
Uji Mekanik
Presipitasi komposit apatit-kitosan
dengan metode insitu dan eksitu
Aging selama 24 jam dan
dikeringkan pada suhu 50
oC
Lampiran 2. Komposisi massa untuk menghasilkan sampel
massa (Na)2HPO4 100ml dan massa CaCl2 100ml yang dibutuhkan untuk membuat senyawa apatit dengan perbandingan molaritas Ca/P (0.334/0.2) :
massa (Na)2HPO4 100ml = Mr (Na)2HPO4 x M x V = (177.99) x (0.2) x (100x10-3)
= 3.5598 gram massa CaCl2 100ml = Mr CaCl2 x M x V
= (147.02) x (0.334) x (100x10-3) = 4.9104 gram
massa komposit = massa apatit + massa kitosan massa kitosan yang digunakan:
perbandingan massa apatit : kitosan = 55 : 35 (55:35) = (1.8784:x)
x = 1.1953 gram
Kode
Sampel Massa (gram) (Na)2HPO4 Massa (gram)CaCl2 Massa Kitosan (gram) Massa Hasil (gram)
A1 3.5602 4.9108 - 1.8784
A2 3.5597 4.9106 - 2.1476
B1 3.5596 4.9107 1.1955 2.2856
B2 3.5599 4.9105 1.1950 2.0257
C1 3.5592 4.9103 1.1958 1.9499
Lampiran 3 Proses Preparasi Sampel
Na2HPO4.
2H2O
CaCl2.
Lampiran 4. Metode Presipitasi Sampel
Presipitasi kontrol: Presipitasi In-situ:
Presipitasi Ex-situ:
- - - - - - - - - -
HOT PLATE
CaCl2
SUHU 700 C Na2HPO4
- - - - - - - - - -
HOT PLATE
CaCl2
SUHU 700 C Na2HPO4
HOT PLATE
- - - - - - - - -
-HOT PLATE SUHU 370
C Na2HPO4
+ kitosan CaCl2
Lampiran 5 Probabilitas Fase Sampel
Kontrol 1 (A1)
2 int int-f HAP AKA AKB OKF Fase
2
% int %2 int %2 int %2 int
23.22 30 17.24 98.34515 10 99.41345 40 99.40213 80 AKA
26.38 85 48.85 98.06407 42 98.34688 35 97.45782 25 99.87095 80 OKF
28.92 36 20.69 99.92733 14 98.56547 17 97.17699 <2 98.51814 10 HAP
30.52 58 33.33 96.16233 100 99.88519 10 96.03134 10 99.18076 70 AKA
31.94 166 95.40 99.36354 100 99.23261 70 99.27888 100 98.88885 100 HAP
32.54 174 100.00 99.01412 55 99.91096 50 98.85615 100 99.97848 90 OKF
34.38 48 27.59 99.02491 24 98.55115 19 99.37954 10 AKB
39.38 48 27.59 99.46131 5 99.04427 13 99.9467 6b AKB
41.84 26 14.94 99.74492 5 98.38456 2b HAP
45.72 90 51.72 99.08844 3 98.86969 2b HAP
46.68 58 33.33 99.95928 24 99.16934 16 HAP
47.78 32 18.39 99.44636 12 98.49376 16 HAP
49.86 62 35.63 99.19534 26 99.38249 16 AKB
53.7 32 18.39 99.06584 12 98.06765 10b HAP
56.94 22 12.64 99.72503 3 HAP
64.18 32 18.39 99.90174 7 HAP
75.56 23 13.22 99.96957 4 HAP
In-situ 1 (B1)
2 int int-f
HAP AKA AKB OKF Kitosan
Fase
2
% int %2 int %2 int %2 int %2 int
10.22 64 27.00 94.42853 26 95.30915 96.13821 361 KITOSAN
13.18 53 22.36 97.97972 1 AKA
26.5 125 52.74 97.60037 42 98.78844 <1 96.99137 25 99.41547 80 OKF
26.68 128 54.01 96.90483 42 99.45946 <1 96.29169 25 99.43722 80 AKB
28.58 53 22.36 98.89616 14 99.75799 17 98.38584 <2 98.38584 80 AKA
30.22 135 56.96 95.21709 100 99.13072 10 97.05331 10 99.82822 70 OKF
31.78 237 100.00 99.86767 100 99.12072 100 98.78155 100 99.39536 100 HAP
32.42 114 48.10 99.26672 43 99.54251 50 99.22914 100 99.65266 90 AKA
36.06 41 17.30 98.19886 4 99.23223 10 99.77765 6 AKB
39.02 40 16.88 99.6196 5 99.57276 2 99.03302 6b HAP
40.08 41 17.30 99.21774 2 99.19517 13 99.21774 16 AKB
45.48 123 51.90 99.61816 3 99.40056 2b HAP
46.16 40 16.88 98.9263 24 97.89644 2b HAP
47.52 41 17.30 98.90522 12 99.04612 16 AKB
49.3 56 23.63 99.67248 26 99.48743 16 HAP
53.04 40 16.88 99.69363 12 99.32045 10b HAP
56.64 38 16.03 99.19961 3 HAP
64.24 24 10.13 99.80816 7 HAP
66.22 23 9.70 99.78151 2 HAP
69.2 15 6.33 99.40958 2 HAP
Ex-situ 1 (C1)
2 int int-f
HAP AKA AKB OKF Kitosan
Fase
2
% int %2 int %2 int %2 int %2 int
10.82 59 30.57 99.97228 26 99.0954 14 90.48583 361 HAP
26 77 39.90 99.53244 42 99.81118 35 98.93493 25 98.68671 80 HAP
26.44 92 47.67 97.83222 42 98.56477 <1 97.2246 25 99.64321 80 OKF
28.66 46 23.83 99.17298 14 99.47739 17 98.1014 <2 98.1014 80 AKA
30.22 79 40.93 95.42891 14 99.13072 10 97.05331 10 99.82822 70 OKF
31.7 177 91.71 99.88027 100 99.37466 100 98.53289 100 99.64861 100 HAP
32.26 193 100.00 99.76386 43 99.7732 70 99.72647 100 99.904 90 AKB
33.98 53 27.46 99.80028 24 99.73148 19 99.44978 10 HAP
36.02 27 13.99 98.31178 4 99.12216 10 99.88883 6 AKB
39.04 46 23.83 99.67066 5 99.08378 6b HAP
45.5 86 44.56 99.57402 3 99.35632 2b HAP
46.42 62 32.12 99.48351 24 98.61698 16 HAP
47.74 26 13.47 99.36311 12 98.57874 16 HAP
49.4 67 34.72 99.87465 26 99.68923 16 HAP
53.18 31 16.06 99.95677 12 99.05471 10b HAP
56.42 30 15.54 98.8143 3 HAP
64.1 34 17.62 99.97349 7 HAP
66.22 29 15.03 99.78151 2 HAP
Kontrol 2 (A2)
2 int int-f HAP AKA AKB OKF Fase
2
% int %2 int %2 int %2 int
19.14 18 9.57 98.1969 4 98.93007 10 96.22442 80 AKA
26.46 188 100.00 97.75494 42 98.63933 <1 97.14686 25 99.5673 80 OKF
28.56 34 18.09 98.82695 14 99.82814 17 98.45694 <2 98.45694 80 AKA
30.18 54 28.72 95.56732 14 98.99951 10 97.18958 10 99.69609 80 OKF
31.84 124 65.96 99.67862 100 98.93026 100 98.96805 100 99.20542 100 HAP
32.52 134 71.28 98.956 43 99.84955 50 98.91831 100 99.95979 90 OKF
33.96 38 20.21 99.74154 24 99.79049 19 99.39124 10 HAP
36.08 28 14.89 98.1424 4 99.28727 10 99.72207 6 AKB
39.14 52 27.66 99.92596 5 99.67403 19 99.33758 6b HAP
40.22 68 36.17 99.56431 2 98.84306 13 99.56431 16 HAP
45.64 48 25.53 99.26501 3 99.04665 2b HAP
46.52 46 24.47 99.69782 24 98.82943 16 HAP
49.6 52 27.66 99.721 26 99.90717 16 AKB
53.22 36 19.15 99.96805 12 98.97878 10b HAP
63.94 30 15.96 99.96092 6 HAP
In-situ 2 (B2)
2 int int-f
HAP AKA AKB OKF Kitosan
Fase
2
% int %2 int %2 int %2 int %2 int
10.16 20 13.33 93.87416 26 94.7496 14 95.73071 40 97.16599 361 KITOSAN
26.68 66 44.00 96.90483 42 99.45946 <1 96.29169 25 99.43722 80 AKA
28.74 34 22.67 99.44981 14 99.1968 2 97.90496 10 97.81697 80 HAP
30.36 62 41.33 95.6582 100 99.58996 10 96.57639 10 99.7093 70 OKF
31.84 150 100.00 99.67862 100 98.93026 100 98.96805 100 99.20542 100 HAP
32.46 128 85.33 99.14243 43 99.66533 50 99.10481 100 99.77561 90 OKF
34.12 38 25.33 99.78853 24 99.31836 19 99.85952 10 95.12188 90 AKB
36.08 30 20.00 98.1424 4 99.28727 10 99.72207 6 AKA
39.18 38 25.33 99.97192 5 99.7759 19 99.4391 6b HAP
40.26 28 18.67 99.66333 2 98.74245 13 99.66333 16 HAP
42 30 20.00 99.87365 5 98.76079 2b HAP
45.6 64 42.67 99.3533 3 99.13513 2b HAP
46.5 42 28.00 99.65496 24 98.7
![Tabel 2. Formula kimia, struktur dan parameter kisi kristal kalsium fosfat [13].](https://thumb-ap.123doks.com/thumbv2/123dok/687980.358116/23.595.328.504.112.271/tabel-formula-kimia-struktur-parameter-kristal-kalsium-fosfat.webp)
![Gambar 1. Struktur Hidroksiapatit [15]](https://thumb-ap.123doks.com/thumbv2/123dok/687980.358116/24.595.114.302.588.723/gambar-struktur-hidroksiapatit.webp)