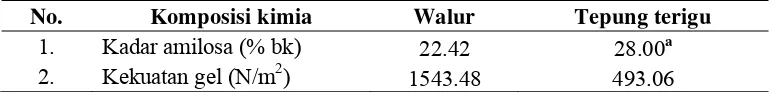KARAKTERISASI SERTA APLIKASI PATI WALUR PADA
COOKIES DAN MIE
RANI ANGGRAENI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ABSTRACT
ANGGRAENI. Oxalate Reduction in Walur (Amorphophallus Campanullatus
Var. Sylvestris), Characterizations and Applications of walur Starch on Cookies
and Noodles under direction of FERI KUSNANDAR, EKO HARI PURNOMO and RISFAHERI
Walur (Amorphophallus campanulatus var. sylvestris) is a type of tuber containing high oxalate content (36058.8375 ppm) causing itchiness and irritation owhen consumed. Walur can be easily found in iles-iles plantation as gulma and produced with the triple amount of iles-iles root, 3.6 ton/ha. The objective of this research is to study the reduction of total oxalic content in walur and the application of walur starch to cookies and noodles.
There are four main step in this research which are the characterization of physicochemical properties of walur tuber, reduction of oxalic content, characterization of physicochemical and functional properties of walur starch, and application of walur starch for cookies and noodle production.
Walur tuber has moisture content of 74.46%, ash of 4.89%, fat of 14.41%, protein of 6.42%, and carbohydrate of 74.28% in dry basis. Walur starch has ovale and polygonale shape with size of 10-22 μm. RVA analysis showed that walur starch had A type gelatinization pattern. Reduction of oxalic content up to 93.18% can be achieved by soaking in HCl 0.2 N solution for 30 minutes, 1% sodium bicarbonate solution for 5 minutes and washing. Walur starch could be applied for cookies and noodles production. Organoleptic test showed cookies with 25% of walur starch and noodle with 60% of walur starch are the same acceptance with the control.
RINGKASAN
ANGGRAENI. Penurunan kadar Oksalat Umbi Walur (Amorphophallus campanulatus var. sylvestris) dan Karakterisasi serta Aplikasi Pati Walur Pada
Cookies dan Mie. Dibimbing oleh FERI KUSNANDAR, EKO HARI PURNOMO dan RISFAHERI
Walur (Amorphophallus campanulatus Var. Sylvestris) adalah salah satu jenis umbi yang termasuk ke dalam keluarga Araceae. Salah satu hambatan dalam pemanfaatan umbi walur adalah rasa gatal dan iritasi apabila dikonsumsi yang disebabkan oleh kandungan oksalat yang terdapat pada umbi walur. Umbi walur, banyak tumbuh sebagai tanaman pengganggu (gulma) di sekitar lokasi kebun iles-iles dan dihasilkan dengan jumlah tiga kali lipat lebih banyak dari umbi iles-iles-iles-iles yaitu sekitar 3.6 ton/ha.
Tujuan dari penelitian ini adalah untuk menurunkan kandungan oksalat pada umbi walur agar dapat dikonsumsi tanpa menimbulkan rasa gatal dan iritasi serta mengaplikasikan pati walur sebagai pensubstitusi terigu pada pengolahan produk pangan (cookies dan mie).
Penelitian ini terdiri dari empat tahapan penelitian, yaitu karakterisasi sifat fisikokimia umbi walur, penurunan kandungan oksalat pada umbi walur hingga mencapai batas aman untuk dikonsumsi, produksi dan karakterisasi sifat fisikokimia dan fungsional pati walur dan aplikasi pati walur dalam pembuatan produk pangan (cookies dan mie).
Hasil analisis menunjukkan bahwa umbi walur mengandung kadar air, abu, lemak, protein dan karbohidrat berturut-turut sebesar 74.46% (bb); 4.89% (bk), 14.41%; 6.42% (bk) dan 74.28% (bk). Granula pati umbi walur berbentuk oval dan bersudut banyak (polygonal) dengan ukuran berkisar antara 10 hingga 22 μm. Hasil analisis RVA menunjukkan bahwa pati walur menunjukkan pola gelatinisasi tipe A. Berdasarkan hasil optimasi diketahui bahwa reduksi oksalat terbaik dilakukan dengan perendaman dalam larutan HCl 0.2 N selama 30 menit diikuti dengan larutan natrium bikarbonat 1% selama 5 menit dan pencucian. Dengan cara ini, dapat mereduksi kandungan oksalat sebsar 93.17 % dengan sisa oksalat sebsar 2462.1 ppm. Selanjutnya pati walur yang dihasilkan dapat diaplikasikan untuk pembuatan produk cookies dan mie. Hasil analisis menunjukkan bahwa produk yang memiliki karakteristik yang sama dengan produk tepung terigu adalah cookies 25% pati walur dan mie substitusi 10%. Namun, hasil analisis organoleptik menunjukkan bahwa produk cookies hingga 100% pati walur dan mie hingga 60% pati walur masih disukai oleh panelis. Kata kunci : Amorphophallus campanulatus var. sylvestris, Penurunan kadar
©Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
PENURUNAN KADAR OKSALAT UMBI WALUR
(Amorphophallus campanulatus var. Sylvestris) DAN
KARAKTERISASI SERTA APLIKASI PATI WALUR PADA
COOKIES DAN MIE
RANI ANGGRAENI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul tesis : Penurunan Kadar Oksalat Umbi Walur (Amorphophallus campanulatus var. Sylvestris) dan Karakterisasi serta Aplikasi Pati Walur pada Cookies dan Mie
Nama : Rani Anggraeni NIM : F251090221
Disetujui Komisi Pembimbing
Dr. Ir. Feri Kusnandar M. Sc Ketua
Dr. Eko Hari Purnomo, S.TP, M. Sc Prof. Dr. Ir. Risfaheri, MS Anggota Anggota
Mengetahui
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Pangan
Dr. Ir. Ratih Dewanti, M. Sc Dr. Ir. Dahrul Syah, M.Agr
RIWAYAT HIDUP
PRAKATA
Segala puji dan syukur, tak henti penulis panjatkan hanya ke hadirat Allah SWT, karena atas limpahan rahmat dan karunia Nya penulis dapat menyelesaikan tesis yang berjudul “Reduksi Oksalat Umbi Walur (Amorphophallus campanulatus var. sylvestris) dan Karakterisasi serta Aplikasi Pati Walur Pada
Cookies dan Mie”. Shalawat dan Salam semoga selalu tercurahkan pula kepada junjungan Nabi Besar, Muhammad SAW.
Terima kasih penulis ucapkan kepada Dr. Ir. Feri Kusnandar, M.Sc, Dr. Eko H. Purnomo, S. TP, M. Sc dan Bapak Prof. Dr. Ir. Risfaheri, M. S selaku komisi pembimbing serta Bapak Asep W. Permana, S. TP, M. Si yang telah banyak membantu dan memberikan saran selama pelaksanaan penelitian. Ungkapan terima kasih juga disampaikan kepada Mamah, Bapak serta seluruh keluarga atas segala doa dan kasih sayangnya. Juga kepada teman-teman seperjuangan, Eka dan Mba Devi juga Dede dan teman-teman IPN 2009 atas kebersamaan, dukungan serta bantuannya. Tak lupa penulis ucapkan terima kasih kepada seluruh staf di laboratorium kimia Balai Besar Litbang Pascapanen Pertanian yang senantiasa membantu selama penelitian ini berlangsung.
Tak lupa ucapan terima kasih yang sebesar-besarnya penulis ucapkan kepada Kementrian Pertanian yang telah memberikan dana untuk penelitian ini melalui program Kerja Sama Kemitraan Penelitian Pertanian dengan Perguruan Tinggi (KKP3T). Penelitian ini merupakan penelitian awal. Suatu penelitian akan semakin sempurna ketika setiap insan dapat berpartisipasi dalam mengisi kekosongan informasi yang diperlukan. Semoga penelitian ini bermanfaat tidak hanya untuk bidang keilmuan, tetapi juga bagi masyarakat luas khususnya para petani.
Bogor, Juni 2011
DAFTAR ISI
Halaman
DAFTAR TABEL ix
DAFTAR GAMBAR x
DAFTAR LAMPIRAN xii
1 PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Tujuan Penelitian 2
1.3 Hipotesis 3
1.4 Manfaat Penelitian 3
2 TINJAUAN PUSTAKA 4
2.1 Umbi Walur 4
2.2 Pati 5
2.3 Oksalat dalam Bahan Pangan 9
2.4 Reduksi oksalat 10
2.5 Cookies dan mie 12
2.6 Substitusi pati pada pembuatan cookies dan mie 14
3 BAHAN DAN METODE 16
3.1 Waktu dan tempat penelitian 16
3.2 Bahan dan Alat 16
3.3 Metodologi 16
3.4 Analisis data 24
3.5 Prosedur analisis 25
4 HASIL DAN PEMBAHASAN 38
4.1 Karakterisasi Sifat Fisikokimia Umbi Walur 38 4.2 Pengaruh Proses Perendaman Terhadap Kandungan Total Oksalat 42 4.3 Produksi dan Karakterisasi Pati Walur 49 4.4 Aplikasi Pati Walur dalam Produk Pangan 64
5 SIMPULAN DAN SARAN 84
DAFTAR PUSTAKA 86
DAFTAR TABEL
Halaman
1. Penetapan Gula menurut Luff Schoorl 30
2. Perbandingan data proksimat umbi walur dan umbi Suweg 38
3. Perbandingan data karakteristik umbi walur dan tepung terigu 40
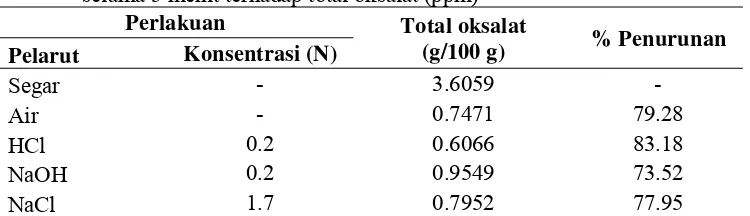
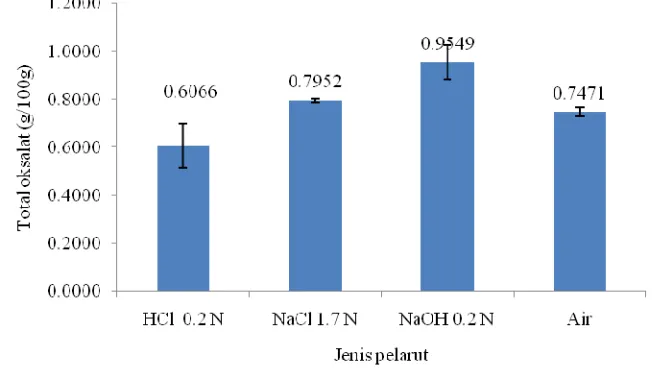
4. Pengaruh perlakuan perendaman irisan umbi walur dengan perlakuan pemanasan selama 3 jam dan perendaman pada berbagai jenis pelarut selama 5 menit terhadap total oksalat (ppm) 43
5. Rendemen pati umbi walur 50
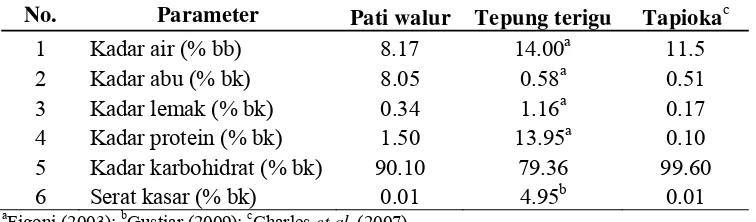
6. Perbandingan data proksimat pada pati walur dan tepung terigu 51
7. Perbandingan data analisis kimia pati walur dan tepung terigu 52
8. Pengaruh proses ekstraksi pati terhadap nilaitotal oksalat (ppm) 55
9. Perbandingan sifat fisik pati dan tepung terigu 57
10. Perbandingan sifat fungsional pati walur dan tepung terigu 59
11. Perbandingan data profil gelatinisasi pati walur dan tepung terigu 62
12. Kandungan kimia cookies 100% pati walur dan standar SNI 70
13. Pengaruh kandungan pati walur terhadap waktu pemasakan (menit) 75
14. Kandungan kimia dalam mie 30% pati walur 83
DAFTAR GAMBAR
Halaman 1. (a) Umbi walur; (b) Umbi suweg 4
2. Pohon walur (a); Batang tanaman umbi walur (b); Umbi suweg (c) 5 3. Struktur kimia amilosa (a); amilopektin (b) 7 4. Struktur kimia asam oksalat (a); kalsium oksalat (b) 10 5. Diagram alir penelitian 17 6. Diagram alir ekstraksi pati 20 7. Proses produksi produk cookies 21 8. Proses Produksi mie 23 9. Bentuk granula pati umbi walur mikroskop polarisasi (a); Scanning
Electron Microscop(b) 39
10. Reaksi kimia antara kalsium oksalat dengan pelarut NaOH (a); NaCl (b);
HCl (c) 44
11. Pengaruh jenis pelarut untuk perendaman irisan umbi walur terhadap kandungan total oksalat (ppm) 46 12. Pengaruh lama perendaman irisan umbi walur dalam pelarut HCl 0.2 N
terhadap total oksalat (ppm 48 13. Kristal oksalat hasil mikroskop polarisasi ekstrak umbi walur segar (a);
Ekstrak umbi walur hasil perendaman dengan pelarut HCl 0.2 N selama 30 menit Umbi rendaman (b). 49 14. Pengaruh proses ekstraksi terhadap kristal oksalat pati walur 56 15. Pengaruh proses reduksi oksalat terhadap granula pati walur 57 16. Perbandingan kurva gelatinisasi pati walur (a); tepung terigu (b) 61 17. Pengaruh substitusi pati walur terhadap kekerasan cookies (gf) 66 18. Produk cookies substitusi pati walur kontrol (a); 25 % pati (b); 50 % pati (c); 75 % pati (d); 100 % pati walur (e) 68 19. Pengaruh substitusi pati walur terhadap nilai kesukaan cookies 69 20. Pengaruh substitusi pati walur terhadap nilai kesukaan mie. 73 21. Produk mie substitusi pati walur kontrol (1); 10 % pati (2); 20 %
23.Pengaruh substitusi pati walur terhadap nilai KPAP mie 77 24. Pengaruh substitusi pati walur terhadap kekerasan mie (g) 79 25. Pengaruh substitusi pati walur terhadap nilai kelengketan (g) mie 80 26. Pengaruh substitusi pati walur terhadap nilai daya kunyah (g) mie 81 27. Pengaruh substitusi pati walur terhadap nilai kekuatan tarikan 82
Halaman
1. Kurva standar HPLC 95
2. Perhitungan konsentrasi total oksalat dalam sampel 95
3. Data analisis amilosa 98
4. Data analisis total pati 99
5. Data analisis daya cerna pati 99
6. Data analisis kemampuan pengembangan pati walur 100
7. Data analisis persen kelarutan pati walur 100
8. Kekuatan gel 101
9. Data analisis kekuatan cookies 101
10. Rekapitulasi data Uji Organoleptik Cookies pati walur 102
11. Kuisioner organoleptik cookies 106
12. Data analisis penyerapan air mie pati walur 107
13. Data analisis % KPAP mie pati walur 108
14. Data analisis tekstur mie pati walur 109
15. Rekapitulasi data Uji Organoleptik Mie pati walur 111
16. Format kuisioner uji organoleptik mie 115
1.1 Latar belakang
Walur (Amorphophallus campanulatus) adalah salah satu jenis umbi yang termasuk ke dalam keluarga Araceae. Menurut Ohtsuki (1967), di Jawa terdapat dua jenis varietas Amorphophallus campanulatus, yaitu varietas hortensis yang dikenal dengan nama suweg dan varietas sylvestris yang dikenal dengan nama walur. Berbeda dengan umbi suweg yang sudah banyak dimanfaatkan, umbi walur yang merupakan tanaman sejenis belum banyak dieksplorasi dan hanya dianggap sebagai tanaman pengganggu.
Penelitian terbaru oleh Das et al. (2009) menunjukkan bahwa spesies
Amorphophallus campanulatus mengandung 78.7% air; 1.2% protein; 0.1% lemak dan 18.4% karbohidrat. Berdasarkan data tersebut, diketahui bahwa spesies
Amorphophallus campanulatus memiliki kandungan karbohidrat yang cukup tinggi yang menunjukkan adanya potensi bagi spesies ini untuk dimanfaatkan sebagai bahan pangan alternatif.
Saat ini, umbi walur ditemukan di sekitar kebun iles-iles sebagai gulma, yaitu tanaman yang pertumbuhannya tidak diinginkan karena dapat menurunkan produktivitas tanaman lainnya. Pada lahan pertanian tersebut, umbi walur diproduksi dalam jumlah tiga kali lipat lebih banyak dari produksi umbi iles-iles yang dibudidayakan.
Potensi umbi walur yang cukup besar ini selanjutnya diharapkan dapat dijadikan sumber pangan alternatif. Selama ini baru 4 jenis tanaman yang dianggap sebagai pendamping padi atau beras sebagai makanan pokok yaitu jagung, ubi kayu, ubi jalar dan kentang (Sudiro 2005). Diharapkan, potensi umbi walur yang cukup baik ini, selanjutnya dapat dijadikan pula sebagai sumber pangan pendamping padi atau beras. Selain itu juga, dengan memanfaatkan umbi walur dapat mencegah terjadinya pengrusakan hutan dengan memberikan nilai tambah bagi petani di sekitar hutan.
bioavailibilitas kalsium dalam tubuh dan menyebabkan batu ginjal sedangkan kalsium oksalat yang tidak larut air menyebabkan rasa gatal dan iritasi jika dikonsumsi (Noonan dan Savage 1999).
Kandungan oksalat tidak hanya terdapat pada umbi walur. Hampir semua jenis tanaman talas-talasan mengandung oksalat di dalam umbinya, namun rasa gatal dari sebagian besar tanaman tersebut dapat hilang dengan proses pemasakan. Menurut Kriswidarti (1980), diketahui bahwa umbi walur memiliki kandungan oksalat yang jauh lebih tinggi dibandingkan dengan umbi suweg sehingga rasa gatalnya belum hilang meskipun telah dilakukan proses pemasakan. Untuk itu, perlu dilakukan proses penurunan kadar oksalat pada umbi walur agar selanjutnya dapat dikonsumsi tanpa menimbulkan rasa gatal dan juga aman dikonsumsi tanpa memberikan dampak negatif terhadap kesehatan
Penelitian ataupun informasi mengenai umbi walur belum banyak ditemukan hingga saat ini baik di dalam maupun di luar negeri. Untuk itu, perlu dilakukan penelitian mengenai umbi walur agar potensi besar yang dimilikinya dapat tereksplorasi sehingga selanjutnya dapat dimanfaatkan oleh masyarakat.
1.2 Tujuan
1.2.1 Tujuan Umum
Tujuan dari penelitian ini adalah untuk menghasilkan dan mengkarakterisasi pati walur sebagai sumber pangan alternatif
1.2.2 Tujuan khusus
1. Mempelajari karakteristik sifat fisikokimia umbi walur
2. Menurunkan kandungan oksalat dalam umbi walur agar dapat dikonsumsi tanpa menimbulkan rasa gatal dan iritasi
3. Mempelajari karakteristik sifat fisikokimia dan fungsional pati walur
4. Mengaplikasikan pati walur sebagai pensubstitusi terigu pada pengolahan produk pangan (cookies dan mie).
Proses perendaman umbi walur dalam berbagai jenis pelarut dan waktu perendaman dapat mereduksi kandungan oksalat pada umbi walur dan pati walur yang dihasilkan dapat digunakan untuk mensubstitusi terigu dalam produk cookies
dan mie.
1.4 Manfaat Penelitian
Pati walur dapat dijadikan sebagai sumber pangan alternatif yang memiliki sifat fungsional sebagai pensubstitusi terigu pada pengolahan produk pangan. Selanjutnya diharapkan dapat meningkatkan nilai tambah dan pendapatan bagi petani dan Lembaga Masyarakat Di sekitar Hutan (LMDH) serta akan mendorong berkembangnya agroindustri pengolahan produk pangan berbasis umbi walur serta agribisnis terkait lainnya.
2.1 Umbi Walur
Umbi walur merupakan tanaman yang termasuk ke dalam dunia Spermatophyta, sub dunia Angiospermae dan kelas Monokotiledon. Umbi walur juga termasuk ke dalam kelas talas-talasan (areceae), genus Amorphophallus, dan spesies Amorphophallus campanulatus. Menurut Ohtsuki (1967), di Jawa banyak berkembang dua varietas Amorphophallus campanulatus, yaitu varietas sylvestris,
yang dikenal dengan nama umbiwalur (Gambar 1a) dan varietas hortensis dengan nama umbi suweg (Gambar 1b).
(a) (b)
Gambar 1 Umbi walur (a); suweg (b) Sumber : Koleksi pribadi 2010
Amorphopallus campanulatus merupakan tanaman yang berbatang semu, mempunyai satu daun tunggal yang terpecah-pecah dengan tangkai daun tegak yang keluar dari umbinya (Gambar 2a). Tangkainya belang hijau putih, berbintil-bintil dengan panjang 50-150 cm. Perbungaannya muncul setelah daun hilang dari permukaan tanah, terdiri atas tangkai bunga, seludang dan tongkol. Tongkolnya berbau tidak enak dan terdiri atas tiga bagian, yaitu bagian bawah bunga betina, bagian tengah bunga jantan dan bagian atas bunga mandul. Spesies
(a) (b) (c) Gambar 2 Pohon walur (a); batang umbi walur (b); batang umbi suweg (c)
Sumber : Koleksi pribadi 2010
Perbedaan kedua jenis varietas tanaman ini terletak pada batang yang dimilikinya. Umbi walur memiliki batang yang kasar (Gambar 2b) sedangkan suweg memiliki batang yang halus (Gambar 2c). Namun, keduanya sangat mudah untuk dikembang biakan melalui anakan atau umbi. Selain mempunyai batang yang kasar, walur memiliki umbi yang sangat gatal jika dikonsumsi (Kriswidarti 1980). Oleh karena itu, walur belum dimanfaatkan penduduk dan masih merupakan tumbuhan liar sedangkan umbi suweg dapat dikonsumsi karena oksalat yang terdapat pada umbi suweg dapat dihilangkan dengan cara perebusan sehingga sudah cukup banyak dimanfaatkan dan banyak ditanam di pekarangan.
2.2 Pati
2.2.1 Sifat Fisikokimia pati
Pati merupakan bagian makanan utama yang terdapat dalam tanaman dan menyediakan 70-80% kalori yang dikonsumsi oleh manusia. Pati dan produk hidrolisisnya merupakan karbohidrat yang dapat dicerna yang tersedia dalam makanan. Selain itu, pati juga banyak digunakan untuk membuat berbagai produk makanan.
pati. Dengan demikian sifat fisik tersebut dapat digunakan sebagai variabel dalam identifikasi pati.
Dalam granula pati, campuran molekul yang berstruktur linier dan bercabang tersusun membentuk lapisan-lapisan tipis yang berbentuk cincin atau lamela, dimana lamela tersebut tersusun terpusat mengelilingi titik awal yang disebut dengan hilium. Penampakan hilium pada granula pati adalah akibat dari pengendapan lapisan molekul pati yang terjadi pada waktu yang berlainan dan tidak sama kadarnya (Campbell et al. 1999). Letak hilium dalam granula pati ada yang di tengah dan ada yang di tepi
Jane et al. (1996) melaporkan bahwa ukuran granula pati yang berasal dari biji-bijian lebih kecil dari tanaman sumber pati lainnya, yaitu berkisar antara 3-20 μm, sedangkan yang berasal dari akar dan umbi-umbian berkisar antara 10-100 μm dan yang berasal dari batang 50 μm. Bentuk granula pati bervariasi, yaitu mulai dari bentuk bulat, oval, elips, polgonal sampai bentuk yang tidak beraturan.
Pati merupakan polisakarida yang tersusun atas unit-unit glukosa dengan ikatan α-glikosidik (Winarno 1997). Tiap jenis pati memiliki sifat yang berbeda-beda bergantung pada panjang rantai karbonnya. Selain itu, perbandingan antara molekul amilosa dan amilopektin serta kandungan protein dan lemak juga menjadi faktor yang mempengaruhi sifat dari suatu jenis pati.
(a)
(b)
Gambar 3 Struktur kimia amilosa (a); amilopektin (b). Sumber : Tester dan Karkalas (2004)
Amilosa bersifat sangat hidrofilik karena banyak mengandung gugus hidroksil, oleh karena itu molekul amilosa cenderung membentuk susunan paralel satu sama lain melalui ikatan hidrogen dan gaya van der walls. Oleh karena itu, amilosa mampu membentuk struktur kristal karena adanya interaksi molekuler yang kuat. Kristalisasi sering pula disebut sebagai retrogradasi, proses yang menyebabkan molekul pati menjadi tidak larut dalam air yang bersifat dapat balik karena terjadi pembentukan ikatan intermolekuler yang kuat (Klucinec et al.
1999).
2.2.2 Sifat Fungsional Pati
Sifat fungsional pati merupakan sifat-sifat pati yang turut menentukan mutu produk akhir. Sifat fungsional pati antara lain penyerapan air, penyerapan minyak, kemampuan pengembangan dan kelarutan, pembentukan gel dan pola gelatinisasi. Karakteristik fungsional pati untuk aplikasi bahan pangan sangat ditentukan oleh karakteristik kimianya
secara berlebihan dan pemanasan pada waktu dan suhu tertentu, sehingga granula pati membengkak dan tidak dapat kembali pada kondisi semula. Mekanisme gelatinisasi dibedakan menjadi tiga fase (Fennema 2000), yaitu tahap awal, air secara perlahan-lahan dan secara bolak-balik masuk ke dalam granula, selanjutnya tahap kedua, yaitu suhu 60-85 °C granula akan mengembang dengan cepat dan polimer yang lebih pendek akan larut, sehingga pati akan kehilangan sifat birefringentnya. Pada tahap ketiga, jika suhu tetap naik, maka molekul-molekul pati akan berdifusi keluar granula.
Selama pemanasan dalam air, peregangan lamela granula berawal dari penyerapan molekul air di bagian amorf granula. Selanjutnya bagian ini akan menginduksi pengembangan bagian kristalin granula sehingga molekul amilopektin pada titik percabangan dapat terpisah. Bangun molekul dari amilopektin memungkinkan kemampuan untuk memerangkap air yang lebih besar daripada rantai linier yang membentuk heliks sehingga amilopektin mempunyai peran pada pengembangan granula pati yang lebh besar daripada amilosa (Jane et al. 1999). Pengembangan granula pati akan mencapai maksimal pada suhu gelatinisasi sehingga dapat meningkatkan viskositas secara drastis.
Pemanasan lebih lanjut di atas suhu akhir gelatinisasi akan menyebabkan dinding granula rusak sehingga isi granula terbebaskan ke medium dan menghasilkan pasta. Peningkatan kelarutan juga diikuti dengan peningkatan viskositas. Hal ini disebabkan air yang sebelumnya bebas bergerak di luar granula pati menjadi terperangkap dan tidak dapat bergerak bebas lagi setelah mengalami gelatinisasi.
asam dan pengadukan dapat meningkatkan atau menurunkan viskositas tergantung dari rasio amilosa dan amilopektin.
Scoch dan Maywald (1968) mengelompokkan pati ke dalam empat tipe pola gelatinisasi berdasarkan kemampuan pengembangan granula pati dan ketahanannya terhadap panas serta pengadukan. Keempat jenis pola viskositas tersebut adalah tipe A, B, C dan D. Tipe A adalah jenis pati yang memiliki kemampuan pengembangan yang tinggi. Granula pati dari tipe ini mengembang dengan mudah ketika dipanaskan dalam air dan ikatan internalnya menjadi lemah sehingga menjadi tidak tahan terhadap pengadukan. Kurva viskositas tipe ini menghasilkan puncak viskositas yang tinggi diikuti dengan pengenceran secara cepat selama pemasakan. Jenis pati yang memiliki pola viskositas tipe ini adalah pati kentang, tapioka, dan sereal jenis wax.
Tipe B adalah pati yang mengalami pengembangan yang moderat. Karena granula pati tidak mengembang secara sempurna sehingga menyebabkannya menjadi tidak mudah pecah, maka pati jenis ini menunjukkan puncak viskositas yang lebih rendah dan mengalami sedikit pengenceran selama pemasakan. Contohnya adalah pati sereal. Tipe C merupakan jenis pati yang mengalami pembengkakan terbatas. Kurva viskositasnya tidak menunjukkan adanya puncak viskositas tapi memiliki viskositas yang sangat tinggi dan meningkat selama pemasakan berlangsung.
Pola viskositas tipe D merupakan pati yang memiliki pengembangan yang sangat terbatas. Biasanya, pati yang memiliki pola viskositas ini adalah pati yang mengandung amilosa sangat tinggi. Hal ini karena kekakuan ikatan internal akibat interaksi molekul-molekul linier sehingga menyebabkan granula pati tidak memberikan pembengkakan yang cukup untuk meningkatkan viskositas selama pemasakan.
2.3 Oksalat dalam Bahan Pangan
yang larut dalam air (5-25%), sementara itu asam oksalat juga dapat berikatan dengan ion logam dan membentuk endapan tak larut, seperti kalsium oksalat (Gambar 4).
(a) (b)
Gambar 4 Struktur kimia asam oksalat (a); kalsium oksalat (b).
Oksalat banyak ditemukan di dalam tanaman. Lebih dari 215 keluarga tanaman mengakumulasi kristal ini di dalam jaringannya. Kandungan oksalat dalam tanaman sekitar 5-80% (b/b) dan 90% dari total oksalat tanaman berada dalam bentuk garam oksalat. Kristal kalsium oksalat dalam tumbuhan memiliki beberapa fungsi, diantaranya adalah sebagai pengatur kalsium dalam jaringan, melindungi dari hewan herbivora dan sebagai detoksifikasi logam (Nakata 2003).
Senyawa oksalat dalam tanaman biasanya berada dalam bentuk larut air dan tidak larut air. Oksalat larut air berada dalam bentuk asam oksalat, sodium oksalat dam kalium oksalat, sedangkan oksalat yang tidak larut air berada dalam bentuk garam kalsium oksalat, magnesium oksalat (terutama garam kalsium) (Noonan dan Savage 1999). Kalsium oksalat merupakan jenis garam yang terbentuk antara ion kalsium dan ion oksalat.
Secara umum terdapat lima jenis kalsium oksalat yang berada di dalam tanaman, yaitu berbentuk jarum (raphide), bentuk pensil (rectangular), bulat (druse), prisma dan parallelogram (rhomboid). Semua jenis kristal kalsium oksalat tersebut merupakan mineral yang relatif stabil dan sedikit larut dalam air (Webb 1999), tidak larut dalam keadaan netral atau alkali dan mudah dipecahkan oleh asam (Noonan dan Savage 1999).
2.4 Penurunan kadar Oksalat
Umbi yang termasuk ke dalam spesies Araceae terutama edible aroid
kulit tersebut disebabkan oleh senyawa yang terdapat pada permukaan kristal calsium oksalat jenis rafida. Kristal rafida ini hanya berfungsi sebagai pembawa sedangkan senyawa yang menyebabkan iritasi tersebut adalah jenis protein dengan bobot molekul 26 KDa (Paul et al. 1999).
Jenis oksalat lain yang terdapat dalam umbi araceae adalah oksalat larut air. oksalat larut air yang ada dalam bahan pangan tersebut jika masuk ke dalam tubuh manusia, maka dapat menghambat bioavailibilitas kalsium dalam tubuh karena akan membentuk kompleks yang tidak dapat dicerna. Kompleks ini akan mengendap di dalam ginjal dan membentuk batu ginjal (Noonan dan Savage 1999). Oleh sebab itu, kedua jenis oksalat, baik oksalat larut air maupun yang tidak larut air memberikan efek yang tidak baik bagi tubuh jika berada dalam konsentrasi yang cukup tinggi. Untuk perlu dilakukan proses penurunan kadar oksalat untuk dapat mengurangi efek negatif tersebut.
Beberapa cara dapat dilakukan untuk mengurangi kandungan oksalat dalam sampel. Sangketkit et al. (2001) melakukan proses penurunan kadar oksalat pada umbi yam New Zealand (Oxalis Tuberosa Mol.) dengan beberapa cara pemasakan konvensional, yaitu dengan perebusan, pengukusan dan pemanggangan. Hasilnya, terjadi penurunan kandungan total oksalat pada umbi yang direbus dan dikukus, namun terjadi kenaikan kandungan oksalat pada umbi yang dipanggang. Hasil yang sama juga terjadi pada proses penurunan kadar oksalat berbagai jenis varietas umbi talas oleh Catterwood et al. (2007). Hasilnya menunjukkan bahwa dengan proses perebusan, terjadi penurunan kandungan total oksalat dari 1714 ppm menjadi 506 ppm, sedangkan proses pemanggangan meningkatkan kandungan oksalat menjadi 2290 ppm.
Berbeda dengan proses perebusan, proses pemanggangan menyebabkan terjadinya peningkatan kandungan oksalat dalam sampel. Hingga saat ini, terdapat dua penjelasan ilmiah yang mungkin mengenai hal ini. Pertama, kulit permukaan umbi akan terkena dengan suhu tinggi selama proses pemanggangan yang akan menyebabkan terjadinya proses pemutusan prekursor oksalat yang ada pada kulit dan jaringan luar. Karena fungsi oksalat dalam tanaman adalah untuk melindungi dari pemangsa, maka kemungkinan besar jumlah oksalat di kulit luar lebih banyak dibandingkan di dalam. Selain itu, selama proses pemanggangan akan terjadi penguapan kandungan air dalam umbi sehingga kandungan oksalat dalam sampel akan terkonsentrasi (Sangketkit et al. 2001)
2.5 Cookies dan mie
Biskuit adalah sejenis makanan yang terbuat dari tepung terigu dengan penambahan bahan makanan lainnya, dengan proses pemanasan dan pencetakan (SNI 01-2973-1992). Biskuit terbagi menjadi biskuit keras, crackers, cookies, dan wafer. Cookies adalah sejenis biskuit dari adonan lunak, berlemak tinggi, renyah, dan bila dipatahkan penampang potongannya bertekstur kurang padat (Manley 2000).
Bahan-bahan yang digunakan dalam pembuatan cookies terbagi dalam dua kelompok, yaitu bahan pengikat dan bahan pelembut. Bahan-bahan yang berfungsi sebagai pengikat adalah tepung, susu, dan putih telur. Sedangkan bahan-bahan yang berfungsi sebagai pelembut adalah gula, lemak, baking powder, dan kuning telur (Matz dan Matz, 1978).
Penambahan tepung dilakukan pada bagian paling akhir. Metode ini baik untuk cookies karena menghasilkan adonan yang bersifat membatasi pengembangan gluten yang berlebihan (Matz dan Matz 1978). Sesuai dengan namanya, metode all in dilakukan dengan pencampuran seluruh bahan lalu diaduk sampai membentuk adonan. Adonan yang telah dicetak selanjutnya ditata dalam loyang yang telah diolesi dengan lemak lalu dipanggang dalam oven. Pengolesan lemak berfungsi untuk mencegah lengketnya cookies pada loyang setelah dipanggang. Adonan dipanggang dengan suhu ±176.7 ºC (350 ºF) selama ±10 menit. Suhu dan lama waktu pemanggangan mempengaruhi kadar air cookies. Matz dan Matz (1978) menerangkan bahwa semakin sedikit jumlah gula dan
lemak yang digunakan, suhu pemanggangan dapat dibuat lebih tinggi (177-204 ºC). Setelah dipanggang, cookies harus segera didinginkan untuk
mengurangi pengerasan akibat memadatnya gula dan lemak.
Mi kering didefinisikan sebagai produk makanan kering yang dibuat dari tepung terigu dengan penambahan bahan makanan lain dan bahan tambahan makanan yang diizinkan, berbentuk khas mi (SNI 01-2974-1996). Proses pengolahan mi kering sebenarnya hampir sama dengan mi instan. Pada mi kering terjadi proses pengeringan untuk mengurangi kadar air mi hingga 10-12 persen. Sedangkan proses pengolahan mi instan umumnya dengan digoreng dan dilengkapi oleh bahan tambahan seperti bumbu, cabe, kecap, minyak, dan sayuran kering sehingga mudah dihidangkan dengan segera Menurut Departemen Kesehatan RI (1992), dalam 100 gram mi kering terkandung 337 kkal energi, protein 7.9 g, lemak 11.8 g, karbohidrat 50.0 g, kalsium 49 mg, fosfor 47 mg, besi 2.8 mg, vitamin B1 0.01 mg, dan air 28.9 g.
2.6 Substitusi pati pada pembuatan cookies dan mie
Tepung terigu kini merupakan bahan makanan pokok penting kedua di Indonesia, setelah beras. dimana kebutuhannya terus meningkat dari tahun ke tahun. Saat ini konsumsi terigu penduduk Indonesia mencapai 17 kg/kapita/tahun. Pada saat ini seluruh kebutuhan tepung terigu dalam negeri dipenuhi dari impor dalam bentuk biji gandum yang kemudian diproses menjadi tepung terigu oleh industri penepungan. Ketergantungan yang sangat tinggi pada terigu impor ini akan mengganggu kemandirian pangan nasional.
Ketergantungan masyarakat Indonesia terhadap tepung terigu ini perlu dikurangi agar tidak mengganggu stabilitas ketahanan dan kemandirian pangan nasional. Salah satu upaya yang dapat dilakukan untuk mengatasi masalah ini adalah melalui diversifikasi pangan pokok berbasis bahan pangan lokal. Seperti sudah diketahui bahwa Indonesia memiliki komoditas pangan sumber karbohidrat yang sangat beragam, baik yang tergolong serealia seperti jagung, sorgum, hanjeli dan hermada, serta aneka umbi seperti ubikayu, ubijalar, talas, gadung, gembili, suweg, iles-iles, kentang, garut dan ganyong (Widowati 2009).
Komoditas yang sedang dikembangkan untuk dapat menggantikan terigu adalah tepung jagung. Sampai saat ini tepung dan pati jagung sudah digunakan untuk mensubstitusi tepung terigu dalam pembuatan mie. Budiyah (2004) melakukan pembuatan mi jagung instan dengan memanfaatkan pati jagung dan protein jagung (Corn Gluten Meal). Mi jagung memiliki beberapa keunggulan dibandingkan produk pangan lainnya. Menurut Juniawati (2003), mi jagung instan mengandung nilai gizi yang baik yaitu sekitar 360 kalori/kemasan atau lebih tinggi dibandingkan dengan nilai gizi pada nasi (178 kalori),. Namun, nilai gizi ini masih lebih rendah bila dibandingkan dengan mi terigu instan (471 kalori). Tingginya nilai gizi yang terdapat pada mi jagung instan menunjukkan bahwa produk tersebut dapat dijadikan sebagai bahan pangan alternatif pilihan pengganti nasi.
dimana granula pati yang kecil, seperti pati beras, membutuhkan air dalam jumlah yang banyak dalam proses pembuatan adonana. Karakteristik pemasakan dari mie tersebut dipengaruhi oleh kandungan amilosa dan straktur halus amilopektin, yang menyebabkan perbedaan di dalam penyerapan air dan waktu optimum pemasakan.
Selain diaplikasikan pada pembuatan mie, pati juga banyak diaplikasikan pada pembuatan cookies. Kue kering merupakan salah satu jenis makanan ringan yang diminati masyarakat. Konsumsi rata-rata kue kering di kota besar dan pedesaan di Indonesia adalah 0.40 kg/kapita/tahun.Salah satu pati yang sudah diaplikasikan dalam pembuatan cookies adalah pati garut. Pati garut merupakan pati yang diperoleh dari tanaman Maranta arundinacea L.Cookies pati garut yang dihasilkan memiliki nilai indeks glikemik yang lebih rendah dibandingkan dengan
cookies tepung terigu (Gustiar 2009).
Pada tahun 2006, Saguilan et al. Melakukan penelitian mengenai sustitusi pati resisten dari pati pisang dalam pembuatan cookies. Hasilnya menunjukkan bahwa cookies dari pati pisang memiliki tingkat kesukaan yang sama dengan
cookies tepung terigu. Hasil ini mengindikasikan bahwa pati pisang berpotensi untuk dijadikan sebagai ingredient dalam pembuatan produk roti yang mengandung karbohidrat dengan daya cerna yang rendah.
3. BAHAN DAN METODE
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan dari bulan Agustus 2010 hingga Februari 2011. Penelitian ini dilakukan di Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian Bogor, laboratorium SEAFAST Center dan laboratorium kimia PPSHB Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, IPB.
3.2 Bahan dan Alat
Bahan-bahan yang digunakan adalah umbi walur yang diperoleh dari Saradan, Madiun Jawa Timur, HCl teknis, NaCl teknis, NaOH teknis, soda kue, bahan pembuatan mie dan cookies (terigu berprotein tinggi dan bahan tambahan pangannya), serta bahan-bahan kimia untuk analisa.
Alat-alat yang digunakan pada penelitian ini adalah alat slicer (pengiris), alat pemarut, pengering tray drier, alat pengepres dan ayakan, Rapid Visco Analyzer (RVA), Texture Analyzer Brookfield Engineering© TC3, chromameter,
HPLC, Mikroskop polarisasi, SEM, oven pemanggang, mixer dan peralatan gelas untuk analisa.
3.3 Metodologi
Penelitian ini dibagi menjadi empat tahapan (Gambar 5), yaitu (1) tahap karakterisasi sifat fisikokimia umbi walur, (2) tahap penurunan kadar umbi walur; (3) tahap produksi dan karakterisasi sifat fisikokimia dan fungsional pati walur; (4) tahap aplikasi pati walur untuk pembuatan cookies dan mie.
3.3.1 Tahap Karakterisasi Sifat Fisikokimia Umbi Walur
Karakterisasi umbi walur dilakukan untuk mengetahui karakteristik umbi walur yang digunakan dalam penelitian ini. Analisis yang dilakukan pada tahapan ini adalah analisis proksimat yang meliputi analisis kadar air, kadar abu, kadar protein, kadar lemak dan kadar karbohidrat, analisis total pati, analisis kandungan amilosa, analisis mikrostruktur, meliputi analisis Scanning electron Microscop
Umbi Walur
Karakterisasi sifat fisikokimia
Reduksi oksalat
Penentuan kadar oksalat
Analisis proksimat, kadar amilosa, daya cerna pati Rendemen, warna, densitas kamba
Kelarutan, swelling power, kekuatan gel Pasting properties (RVA)
Karakterisasi Analisa tekstur Analisis sensori Analisis Proksimat
Karakterisasi Analisis pemasakan Analisa tekstur Analisis sensori Analisis Proksimat
Analisis Proksimat Kadar oksalat Analisis mikrostruktur
Produksi pati walur
Aplikasi pati walur
Pembuatan mie Pembuatan cookies
[image:30.612.99.506.73.473.2]Karakterisasi sifat fisikokimia
Gambar 5 Diagram alir yang meliputi empat tahapan penelitian.
3.3.2 Tahap Penurunan Kandungan Total Oksalat
Tahapan ini bertujuan untuk mengurangi kandungan oksalat dalam umbi walur yang menyebabkan iritasi pada bibir jika dikonsumsi. Proses penurunan kandungan oksalat dilakukan dengan dua tahapan penelitian, yaitu tahap optimasi pelarut dan tahapan optimasi lama perendaman. Pada tahap optimasi pelarut, sampel umbi walur yang telah dikupas dan diiris dengan ketebalan 2 mm lalu direndam dalam air dan dipanaskan selama 3 jam. Setelah 3 jam air perendaman dibuang dan dicuci dengan air. Setelah itu, irisan umbi lalu direndam dalam pelarut selama 5 menit. Pelarut yang dipilih adalah air, HCl 0.2 N, NaOH 0.2 N dan NaCl 1.7 N. Setelah itu, larutan dibuang dan direndam kembali dalam larutan
Tahap pertama
Tahap kedua
Tahap Ketiga
natrium bikarbonat 1% lalu diikuti dengan pencucian. Perbandingan antara umbi walur dan pelarut adalah 10 kg umbi walur dengan 10 L pelarut. Kandungan oksalat yang terkandung pada irisan umbi walur tersebut dianalisis dengan menggunakan metode Savage et al. (2000).
Setelah diperoleh pelarut yang paling optimal dalam menutunkan kandungan oksalat pada irisan umbi walur, lalu dilakukan proses perendaman yang paling optimal untuk menghasilkan nilai total oksalat yang paling rendah. Umbi walur yang telah diparut lalu direndam dalam pelarut terbaik selama 3 jam. Setiap 30 menit sekali diambil sebagian umbi walurnya untuk selanjutnya dicuci dan direndam dalam pelarut natrium bikarbonat 1% selama 5 menit lalu dicuci dengan air dan dianalisis kandungan oksalatnya dengan menggunakan metode Savage et al. (2000). Lama perendaman yang dipilih adalah yang menghasilkan total oksalat yang paing rendah.
Oksalat dalam umbi walur diturunkan kandungan oksalatnya dengan menggunakan metode kimia, yaitu dengan perendaman dalam larutan asam (pH<3), basa (pH>9) dan larutan garam selama 5 menit. Umbi walur yang telah dibersihkan dari kulit luarnya lalu dipotong hingga memiliki ukuran 2 mm. Larutan yang digunakan dalam tahapan ini adalah air, HCl 0.2 N, NaOH 0.2 N dan NaCl 1.7 Nlalu diikuti dengan perendaman dalam larutan natrium bikarbonat 1% selama 5 menit. Konsentrasi dan waktu yang dipilih merupakan hasil optimasi penurunan kadar oksalat pada talas Banten yang dilakukan oleh Mayasari (2010). Kandungan oksalat yang terkandung dalam umbi hasil perendaman tersebut dianalisis dengan metode kualitatif secara mikroskopis (polarisasi) dan metode kuantitatif dengan High Performance Liquid Chromatography (HPLC) (Savage et al. 2000).
3.3.3 Tahap Produksi dan Karakterisasi Pati Walur 3.3.3.1 Produksi tepung pati walur
Tahapan ini bertujuan untuk memproduksi pati walur dari umbi yang telah mengalami proses penurunan kadar oksalat. Bubur umbi walur yang sudah mengalami penurunan kandungan oksalatnya selanjutnya ditambahkan air dengan perbandingan 10 kg pati dalam 10 liter air. Larutan bubur umbi walur tersebut dimasukkan ke dalam kain saring dan dibungkus kemudian ditekan dengan menggunakan alat pressure untuk mengeluarkan pati hingga ampas bubur umbi walur menjadi kering. Ampas tersebut selanjutnya ditambahkan kembali dengan air seperti proses sebelumnya dan dilakukan proses yang sama untuk meningkatkan rendemen. Air hasil pengepresan tersebut selanjutnya dinetralkan dengan menggunakan NaOH 40% hingga mencapai pH 7 lalu diendapkan selama semalam. Setelah semalam, pati yang mengendap dikeringkan pada suhu 50 °C selama 8 jam pati tersebut kemudian dihancurkan dan disaring dengan menggunakan saringan berukuran 80 mesh. Diagram alur ekstraksi pati dapat dilihat pada Gambar 6.
3.4.3.2Karakteristik sifat fisikokimia tepung pati walur
Umbi walur
diparut
Pencucian dengan air (10 kg:10 L)
Pendiaman selama 1 jam
Pengepresan hingga ampas kering
Pengendapan selama semalam
Dekantasi
Pengeringan pada suhu 50 °C selama 8 jam menggunakan pengering tray drier
Penyaringan dengan saringan 80 mesh
Supernatan dibuang
Pati
Penetralan larutan dengan NaOH 40%
Perendaman dalam HCl 0.2 N selama 30 menit lalu dicuci dengan air bersih
Perendaman dalam Natrium bikarbonat 1% selama 5 menit lalu dicuci dengan air
Ampas dibuang
[image:33.612.108.503.77.602.2]
Gambar 6 Diagram alir ekstraksi pati.
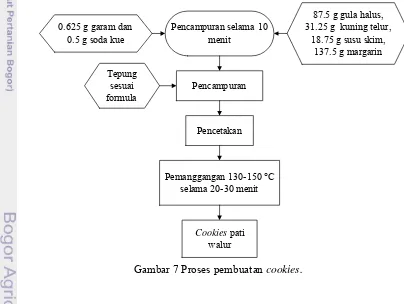
3.3.4 Pembuatan Cookies dan Mie Pati Walur 3.3.4.1 Proses produksi produk cookies (Gustiar 2009)
dengan menggunakan tepung komposit, yaitu campuran antara tepung terigu dan pati walur. Tepung komposit yang digunakan adalah campuran terigu dan pati walur dengan perbandingan 0, 25, 50, 75 dan 100%.
Proses pembuatan cookies dilakukan dengan menimbang sebanyak 87.5 g gula halus lalu ditambah dengan 137.5 g margarin, 18.75 susu skim, 31.25 g kuning telur, 0.625 g garam dan 0.5 g soda. Campuran tersebut kemudian diaduk dengan menggunakan mixer selama 10 menit. Selanjutnya, ke dalam adonan tersebut ditambahkan tepung komposit perlahan-lahan sambil diaduk hingga merata. Setelah tercampur, adonan tersebut dicetak dan dipanggang dalam oven selama 30 menit pada suhu 130-150 °C lalu dikemas. Diagram alir pembuatan
cookies dapat dilihat pada Gambar 7. Analisis organoleptik dilakukan terhadap
cookies yang dihasilkan untuk mengetahui tingkat kesukaan panelis terhadap produk cookies pati walur.
0.625 g garam dan 0.5 g soda kue
87.5 g gula halus, 31.25 g kuning telur ,
18.75 g susu skim, 137.5 g margarin
Pencampuran Pencampuran selama 10
menit
Tepung sesuai formula
Pencetakan
Pemanggangan 130-150 °C selama 20-30 menit
Cookies pati
[image:34.612.101.505.335.639.2]walur
Gambar 7 Proses pembuatan cookies.
3.3.4.2Analisis organoleptik
telah melewati proses pemanggangan. Untuk mengetahui tingkat kesukaan panelis, dilakukan analisis multivariate terhadap data hasil uji organoleptik. Jika berdasarkan analisis multivariate dinyatakan ada pengaruh nyata pada perlakuan maka akan dilanjutkan dengan uji lanjut Duncan.
Uji organoleptik yang digunakan pada tahapan ini adalah uji hedonik. Panelis yang digunakan adalah panelis tidak terlatih sebanyak 25 orang panelis. Skor penilaian yang digunakan dalam uji ini ada 7 tingkat, yaitu, skor 1 (sangat tidak suka), 2 (tidak suka), 3 (agak tidak suka), 4 (netral), 5 (agak suka), 6 (suka), dan 7 (sangat suka). Penilaian tingkat kesukaan didasarkan pada karakteristik produk meliputi warna, rasa, aroma, tekstur, keseluruhan dan after taste
(Lampiran 16).
3.3.4.3Karakterisasi produk cookies tepung pati walur
Karakterisasi produk cookies dilakukan untuk mengetahui karakteristik awal produk cookies, baik dari segi kimia maupun fisik. Analisis fisik yang dilakukan adalah analisis kekerasan produk cookies dengan menggunakan alat
texture analyzer. Analisis kimia yaitu analisis proksimat dilakukan terhadap produk cookies terpilih dari hasil uji organoleptik pada tahap formulasi.
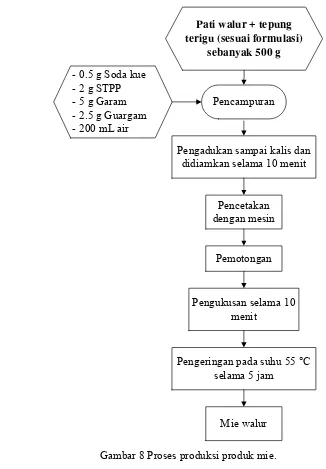
3.3.4.4 Proses pembuatan produk mie
Selain diaplikasikan dalam pembuatan produk cookies, pati walur juga diaplikasikan dalam pembuatan produk mie. Pembuatan produk mie dilakukan dengan menggunakan tepung komposit dengan komposisi pati walur sebesar 0, 10, 20, 30, 40 dan 60%.
dapat dilihat pada Gambar 8. Analisis organoleptik dilakukan terhadap mie yang dihasilkan untuk menentukan formula terbaik.
Pengadukan sampai kalis dan didiamkan selama 10 menit
Pencetakan dengan mesin
Pemotongan
Pengukusan selama 10 menit
Pengeringan pada suhu 55 °C selama 5 jam
- 0.5 g Soda kue - 2 g STPP - 5 g Garam - 2.5 g Guargam - 200 mL air
Pati walur + tepung terigu (sesuai formulasi)
sebanyak 500 g
Pencampuran
[image:36.612.131.457.113.582.2]Mie walur
Gambar 8 Proses produksi produk mie.
3.3.4.5 Uji Organoleptik
Produk mie yang diujikan adalah produk mie yang telah mengalami rehidrasi. Untuk mengetahui tingkat kesukaan panelis, dilakukan analisis
multivariate terhadap data hasil uji organoleptik. Jika berdasarkan analisis
Uji organoleptik yang digunakan pada tahapan ini adalah uji hedonik. Panelis yang digunakan adalah panelis tidak terlatih sebanyak 25 orang. Skor penilaian yang digunakan dalam uji ini ada 7 tingkat, yaitu, skor 1 (sangat tidak suka), 2 (tidak suka), 3 (agak tidak suka), 4 (netral), 5 (agak suka), 6 (suka), dan 7 (sangat suka). Penilaian tingkat kesukaan didasarkan pada karakteristik produk meliputi kelengketan, kekenyalan, rasa dan keseluruhan
3.3.4.6 Karakterisasi sifat fisik dan kimia produk mie
Karakterisasi produk mie dilakukan untuk mengetahui karakteristik awal, baik dari segi kimia maupun fisik. Analisis fisik yang dilakukan meliputi analisis karakteristik pemasakan dan analisis tekstur. Analisis kimia yaitu analisis proksimat dilakukan terhadap produk mie terpilih dari hasil uji organoleptik pada tahap formulasi.
3.4Analisis Data
Analisis statistik untuk penelitian tahap penurunan kandungan oksalat pada umbi walur menggunakan rancangan Anova Single Factor (RAL) dengan dua kali ulangan tiap-tiap perlakuan. Penelitian analisis organoleptik pada sampel
cookies dan mie menggunakan analisis multivariate dengan uji lanjut Duncan.
3.4.1 Rancangan Acak Lengkap (RAL) (Steel dan Torrie 1980)
Data yang diperoleh dari penelitian dianalisis dengan menggunakan
software microsoft excel 2003 dengan metode Rancangan Acak Lengkap atau
Anova Single Factor dengan 2 kali ulangan. Model rancangan yang digunakan adalah sebagai berikut :
Yij = µ + τi + εij
Keterangan:
Yij = Nilai pengamatan dari perlakuan ke-i (konsentrasi oksalat) dan ulangan ke-j µ = Nilai rataan umum populasi
τi = Pengaruh perlakuan ke-i (jenis pelarut dan waktu perendaman)
3.4.2 Analisis multivariate
Data yang diperoleh dari panelis dianalisis dengan menggunakan software
SPSS 16 dengan metode multivariate. Model rancangan yang digunakan adalah sebagai berikut :
Keterangan: n = Jumlah data
ni = Jumlah ulangan ke-i
Ri = Jumlah pangkat perlakuan ke-i
3.5 Prosedur analisis 3.5.1 Analisis proksimat 3.5.1.1 Kadar Air (AOAC 2005)
Cawan alumunium dikeringkan dalam oven selama 15 menit dan didinginkan dalam desikator selama 10 menit lalu ditimbang (A). Sampel ditimbang sebanyak ± 2 g dalam cawan (B). Cawan beserta isi dikeringkan dalam oven 100oC selama 6 jam. Cawan dipindahkan ke dalam desikator lalu didinginkan dan ditimbang sampai diperoleh berat konstan (C).
Perhitungan :
Kadar Air (% bb) = ( ) x100%
B A C B ⎥⎦ ⎤ ⎢⎣ ⎡ − −
3.5.1.2 Kadar Abu (AOAC 2005)
Cawan yang akan digunaan untuk pengabuan terlebih dahulu dikeringksn di dalam oven selama 15 menit lalu didinginkan dalam desikator dan ditimbang (A). Sebanyak ± 3 g sampel ditimbang di dalam cawan (B), kemudian dibakar dalam ruang asap sampai tidak mengeluarkan asap lagi. Pengabuan dilakukan di dalam tanur listrik pada suhu 400-600oC selama 4-6 jam sampai terbentuk abu berwarna putih atau memiliki berat yang tetap. Abu beserta cawan didinginkan dalam desikator dan kemudian ditimbang (C).
(
)
3(
1)
1 n n 12 H 2 + − ⎟⎟ ⎠ ⎞ ⎜⎜ ⎝ ⎛ + = ∑= n n
Perhitungan : Kadar Abu (% bb) = x100%
B A C−
3.5.1.3 Kadar Protein Metode Mikro Kjeldahl (AOAC 2005)
Analisis protein metode ini terdiri atas tiga tahap, yaitu destruksi, destilasi, dan titrasi. Sebanyak 2 gram sampel ditimbang, kemudian dimasukkan ke dalam labu kjeldahl 50 mL, lalu ditambahkan 7 g K2SO4, kjeltab 0.005 g jenis
HgO dan 15 mL H2SO4 pekat dan 10 mL H2O2 ditambahkan secara perlahan ke
dalam labu dan didiamkan 10 menit di ruang asam. Sampel didestruksi pada suhu 410 oC selama kurang lebih 2 jam atau sampai cairan berwarna hijau bening. Labu kjeldahl dicuci dengan akuades 50 hingga 75 mL, kemudian air tersebut dimasukkan ke dalam alat destilasi. Hasil destilasi ditampung dalam erlenmeyer 125 mL yang berisi 25 mL asam borat (H3BO3) 4% yang mengandung indikator bromcherosol green 0.1% dan methyl red 0.1% dengan perbandingan 2:1. Destilasi dilakukan dengan menambahkan 50 mL larutan NaOH-Na2S2O3 ke
dalam alat destilasi hingga tertampung 100-150 mL destilat di dalam erlenmeyer dengan hasil destilat berwarna hijau. Lalu destilat dititrasi dengan HCl 0.2 N sampai terjadi perubahan warna merah muda yang pertama kalinya. Volume titran dibaca dan dicatat. Larutan blanko dianalisis seperti contoh.
Kadar protein dihitung dengan rumus sebagai berikut : % 100 contoh
mg
14,007 HCl
N blanko) mL
-HCl mL ( N
% = × × x
% Protein = % N x faktor konversi* *) FK = 6.25
3.5.1.4 Kadar Lemak (AOAC 2005)
labu dipanaskan dalam oven pada suhu 105 oC. Setelah dikeringkan sampai berat tetap dan didinginkan dalam desikator kemudian labu beserta lemak ditimbang (C) dan dilakukan perhitungan kadar lemak.
Kadar Lemak (%) = x100%
B A C−
3.5.1.5Kadar Karbohidrat (by different)
Karbohidrat dihitung berdasar metode by difference dengan perhitungan : Kadar Karbohidrat (%) = 100% - (P + A + Ab + L)
Dimana : P = kadar protein (% bb) A = kadar air (% bb) Ab = kadar abu (% bb) L = kadar lemak (% bb)
3.5.1.6Analisis serat kasar (SNI 01-2891 1992)
Sebanyak 2-4 gram sampel dihilangkan lemaknya dengan cara ekstraksi soklet atau dengan cara mengaduk dan mengenaptuangkannya dalam pelarut organik. Sampel lalu dimasukkan ke dalam erlenmeyer 500 mL dan ditambahkan 50 mL H2SO4 1.25% dan dididihkan selama 30 menit dengan menggunakan
pendingin tegak. Selanjutnya, sebanyak 50 mL NaOH 3.25% ditambahkan ke dalam larutan dan dididihkan kembali selama 30 menit. Dalam keadaan panas, larutan tersebut disaring dengan menggunakan corong Buchner yang berisi kertas saring tak berabu yang telah dikeringkan dan diketahui bobotnya. Endapan yang terdapat pada kertas saring selanjutnya dicuci berturut-turut dengan larutan H2SO4
1.25% panas, air panas dan etanol 96%. Kertas saring beserta isinya lalu dimasukkan ke dalam cawan yang telah diketahui bobotnya dan dikeringkan pada suhu 105 °C lalu didinginkan dan ditimbang sampai bobotnya tetap.
Perhitungan : 100%
Ws Wo -Wi kasar serat
% = x
Keterangan : Wo = Berat kertas saring
3.5.2 Analisis mikrostruktur 3.5.2.5SEM
Sebanyak 2 mg sampel disimpan dalam cetakan logam. Granula pati kemudian terdistribusi pada permukaan cetakan tersebut dan terselimuti oleh emas-palladium (60:40). Selanjutnya, sampel yang telah dilapisi tersebut difoto dengan menggunakan alat Scanning Electron Microscope JSM-5000 dengan perbesaran 1000 kali.
3.5.2.6Mikroskop polarisasi
Tepung dibuat suspensi encer dengan melarutkan 1 sudip sampel dalam ±20 mL air. Diambil beberapa tetes suspensi ke atas sebuah gelas objek. Gelas penutup dipasang, lalu preparat diamati dengan menggunakan mikroskop polarisasi cahaya dengan perbesaran 400 kali dan gambar yang teramati dipotret dengan kamera dan foto granula pati yang dihasilkan dicetak pada film.
3.5.3 Kadar oksalat (Modifikasi Savage et al. 2000)
Sebanyak 5 g sampel umbi yang telah dihaluskan atau 10 g sampel tepung pati ditimbang lalu dilarutkan dalam 50 mL HCl 2 M. Campuran tersebut dimasukkan ke dalam water bath 80 °C selama 15 menit. Ekstrak yang diperoleh kemudian didinginkan lalu dimasukkan ke dalam labu takar 100 mL dan volumenya ditepatkan dengan menggunakan HCl 2 M. Setiap sampel dilakukan tiga kali ekstraksi. Oksalat larut air diekstraksi dengan metode yang sama dengan menggunakan 50 mL air deionisasi.
kurva standar asam oksalat (0-500 ppm). Semua sampel diekstraksi dan dianalisis secara triplo.
3.5.4 Analisis total pati (BSN 1992)
Metode yang digunakan untuk analisis total pati adalah berdasarkan SNI 01-2892-1992 (BSN 1992). Sebanyak 1 gram sampel ditambahkan dengan larutan HCl 3% sebanyak 200 mL lalu dipanaskan dengan mengunakan pendingin tegak selama 2.5 jam. Setelah dingin, sampel dinetralkan pH nya dengan menggunakan larutan NaOH 40% dan selanjutnya dimasukkan ke dalam labu takar 250 mL dan ditera dengan menggunakan akuades. Sebanyak 10 mL dari larutan tersebut dimasukkan ke dalam erlenmeyer asah dan ditambahkan 25 mL pereaksi luff schrool lalu dipanaskan kembali menggunakan pendingin tegak selama 10 menit dimulai dari gelembung pertama.
Setelah mencapai suhu ruang, ke dalam larutan tersebut ditambahkan 25 mL asam sulfat 25% dan diikuti dengan 20 mL larutan KI 20%. Selanjutnya, larutan harus langsung dititrasi dengan menggunakan larutan tiosulfat dengan pereksi kanji 0.5% hingga warna berubah menjadi putih susu. Prosedur analisis yang sama dilakukan terhadap blanko. Perhitungan kadar pati sampel ditentukan berdasarkan kadar glukosa yang terkuantifikasi pada titrasi sampel. Kadar glukosa dihitung berdasarkan volume dan normalitas larutan Na2S2O3 yang digunakan,
sebagai berikut:
Na2S2O3 yang digunakan = (Vb-Vs)x N Na2S2O3 x 10
Keterangan: Vb = volume Na2S2O3 yang digunakan untuk tirtasi blanko
Vs = volume Na2S2O3 yang digunakan untuk titrasi sampel
N Na2S2O3 = konsentrasi Na2S2O3 yang digunakan untuk titrasi
Jumlah (mg) gula yang terkandung untuk mL Na2S2O3 yang digunakan
ditentukan dengan daftar Luff Schrool (Tabel 1). Dari tabel tersebut dapat diketahui hubungan antara volume Na2S2O3 0.1N yang digunakan dengan jumLah
100 w1
Fp w
G= × ×
P = G x 0.90
Keterangan: G = Kadar glukosa sampel (%)
W =Glukosa yang terkandung untuk mL Na2S2O3 yang
dipergunakan (mg) (Tabel 1) w1 = Bobot sampel (mg)
fp = Faktor pengenceran P = Kadar pati (%)
Tabel 1 Penetapan Gula menurut Luff Schoorl Na2S2O3
0.1 N (mL)
Glukosa, fruktosa dan gula inversi (mg)
Na2S2O3
0.1 N (mL)
Glukosa, fruktosa dan gula inverse (mg)
1 2.4 13 33.0
2 4.8 14 35.7
3 7.2 15 38.5
4 9.7 16 41.3
5 12.2 17 44.2
6 14.7 18 47.1
7 17.2 19 50.0
8 19.8 20 53.0
9 22.4 21 56.0
10 25.0 22 59.1 11 27.6 23 62.2 12 30.3
3.5.5 Kandungan amilosa-amilopektin (Apriyantono et al. 1989) Pembuatan kurva standar amilosa
Sebanyak 40 mg amilosa murni dimasukkan ke dalam labu takar 100 mL, ditambahkan 1 mL etanol 95% dan 9 mL larutan NaOH 1 N ke dalam labu. Labu takar lalu dipanaskan ke dalam penangas air pada suhu 95 °C selama 10 menit. Setelah didinginkan, larutan gel pati ditambahkan air destilata sampai tanda tera sebagai larutan stok standar.
Ditambahkan 2 mL larutan iod (0.2 g I2 dan 2 g KI dilarutkan dalam 100 mL air
destilata) ke dalam setiap labu, lalu diukur absorbansinya dengan spektrofotometer pada panjang gelombang 625 nm. Kurva standar merupakan hubungan antara kadar amilosa dan absorbansi.
Analisis sampel
Sebanyak 100 mg sampel pati dimasukkan ke dalam labu takar 100 mL. Kemudian ditambahkan 1 mL etanol 95% dan 9 mL larutan NaOH 1 N ke dalam
labu. Labu takar lalu dipanaskan dalam penangas air pada suhu 95 °C selama 10 menit. Setelah didinginkan, larutan gel pati ditambahkan air destilata sampai
tanda tera dan dihomogenkan. Dipipet 5 mL larutan gel pati dipindahkan ke dalam labu takar 100 mL. Ke dalam labu takar tersebut kemudian ditambahkan 1.0 mL larutan asam asetat 1 N dan 2 mL larutan iod, lalu ditera dengan air destilata. Larutan dibiarkan selama 20 menit, lalu diukur absorbansinya dengan spektrofotometer pada panjang gelombang 625 nm. Kadar amilosa ditentukan berdasarkan persamaan kurva standar yang diperoleh.
W
100
f
V
C
(%)
amilosa
Kadar
=
×
×
×
Dengan : C = Konsentrasi amilosa (mg/mL) V = Volume akhir contoh (mL) F = Faktor pengenceran
W = Berat contoh (mg)
Kandungan amilosa dalam sampel dapat digunakan untuk memperkirakan kandungan amilopektin. Kandungan amilopektin dapat dihitung berdasarkan selisih antara total kandungan pati dengan kandungan amilosa.
3.5.6 Daya cerna pati (Metode in vitro) (Muchtadi et al. 1992)
7.0. Kemudian diinkubasikan dalam penangas air 37 ºC selama 15 menit. Ke dalam salah satu larutan tersebut ditambahkan 5 mL larutan enzim α-amilase dan diinkubasikan lagi pada suhu 37 ºC selama 15 menit. Sedangkan satu set suspensi lainnya tidak direaksikan dengan enzim α-amilase dan digunakan sebagai blanko sampel.
Ke dalam tabung reaksi lain ditempatkan 1 mL campuran reaksi. Kemudian ditambahkan 2 mL pereaksi dinitrosalisilat, dan dipanaskan dalam penangas air 100 ºC selama 10 menit. Setelah didinginkan, campuran reaksi diencerkan dengan menambahkan 10 mL air destilata. Warna oranye-merah yang terbentuk dari campuran reaksi diukur absorbansinya menggunakan spektrofotometer pada panjang gelombang 520 nm. Kadar maltosa dari campuran reaksi dihitung dengan menggunakan kurva standar maltosa murni yang diperoleh dengan cara mereaksikan larutan maltosa standar dengan pereaksi dinitrosalisilat menggunakan prosedur seperti diatas.
% 100 D -C
B -A cerna
Daya = ×
Ketarangan : A = Kadar maltosa sampel setelah reaksi enzim B = Kadar maltosa sampel sebelum reaksi enzim C = Kadar maltosa pati murni setelah reaksi enzim D = Kadar maltosa pati murni sebelum reaksi enzim
3.5.7 Analisis Kandungan Fosforus (Metode molibdovanadat AOAC 2005) Larutan standar fosfor dibuat dalam konsentrasi 2 mg/mL dengan melarutkan sebanyak 8.788 g KH2PO4 ke dalam satu L akuades. Lalu dibuat
menjadi kurva standar dengan konsentrasi 0.5, 0.8, 1.0 dan 1.5 mg/100 mL pelarut lain dengan.
Sebanyak 2 g sampel dimasukkan ke dalam cawan porselen dan dipanaskan selama 4 jam pada suhu 600 °C. Selanjutnya, sampel didinginkan dan ditambahkan 40 mL HCl 25% dan beberapa tetes HNO3 dan kemudian
Sebanyak 1 mL larutan standar maupun larutan sampel lalu ditambahkan dengan 20 mL pereaksi molibdovanadat dan didiamkan selama 10 menit. Larutan lalu diukur absorbansinya dengan spektrofotometer pada panjang gelombang 400 nm. Kadar fosfor ditentukan berdasarkan persamaan kurva standar yang diperoleh. W f V C (%) fosfor
Kadar = × ×
Dengan : C = Konsentrasi fosfor (mg/100 mL) V = Volume akhir contoh (mL) F = Faktor pengenceran
W = Berat contoh (mg)
3.5.8 Rendemen
Pengukuran rendemen pati dihitung berdasarkan perbandingan berat pati yang diperoleh terhadap berat umbi tanpa kulit (bk) yang dinyatakan dalam persen (%). % 100 (g) (bk) segar umbi Bobot (g) dihasilkan yang pati Bobot (%)
Rendemen = ×
3.5.9 Analisis derajat putih (Lanier et al. 1991)
Sampel ditempatkan pada wadah yang transparan. Pengukuran menghasilkan nilai L*, a*, b*, dan °H. L* menyatakan parameter kecerahan, a* menyatakan warna kromatik (hue) dan b* menyatakan intensitas warna.
]
*
b
*
a
L*)
[(100
-100
2 2 2 1/2(WI) putih
Derajat =
−
+ +3.5.10 Densitas kamba
3.5.11 Analisis kekuatan gel dengan Texture Analyzer Brookfield Engineering© TC3
Pati dibuat suspensi dengan konsentrasi padatan kering sebanyak 10%. Suspensi dipanaskan sampai mencapai suhu gelatinisasinya. Pasta pati dituang ke dalam tabung plastik (diameter 4 cm dan tinggi 5 cm sampai penuh). Tabung disimpan pada suhu 4 °C selama 24 jam. Pengukuran tekstur dilakukan untuk mengukur kekuatan gel dengan menggunakan Texture Analyzer pada kondisi berikut mode: Test mode and option force in compression, pre test speed: 2 mm/detik, test speed: 0.2 mm/detik, post test speed: 2 mm/detik, distance: 2.0 mm, tipe: auto, force: 5 g, diameter probe : 38,1 mm. Penentuan kekuatan gel didasarkan pada maksimum gaya (nilai puncak) dengan satuan gf (gram force). Kekuatan gel sampel dinyatakan sebagai nilai elastis modulus dengan menggunakan persamaan sebagai berikut :
l l A F l l A F Δ × = Δ = = / / G γ σ
Keterangan : F = Gaya yang diberikan oleh alat Texture analyzer (Poundforce) A = Luas permukaan kontak antara probe dengan sampel (m2) l = Tinggi sampel
∆l = Perubahan sampel yang terjadi
3.5.12 Profil gelatinisasi pati dengan Rapid Visco Analyzer (RVA)
Analisis profil gelatinisasi tepung dilakukan dengan menggunakan alat
Rapid Visco Analyzer (RVA). Sampel terlebih dahulu harus sudah diketahui kadar airnya untuk mengetahui jumlah sampel dan air yang akan digunakan dalam analisis. Berdasarkan data kadar air tersebut, diketahui sampel dan jumlah air yang digunakan, lalu ditimbang sebanyak sampel yang dibutuhkan dan dilarutkan dengan akuades. Sampel tersebut dimasukkan pada alat RVA dan dilakukan analisis.
selama 5 menit. Hasil pengukuran dengan alat ini diantaranya adalah suhu awal gelatinisasi, viskositas maksimum (peak viscosity), viskositas pada suhu 95 °C, viskositas setelah 95 °C dipertahankan, viskositas pada suhu 50 °C, dan viskositas setelah suhu 50 °C dipertahankan. Data yang diperoleh dari analisis ini adalah suhu gelatinisasi, peak viscosity (PV) atau viskositas maksimum,
breakdown viscosity (BDV), setback viscosity (SV), dan final viscosity (FV) atau viskositas akhir.
3.5.12 Kelarutan dan kemampuan mengembang (Nadiha et al. 2010)
Sebanak 0.4 gram sample tepung (basis kering) dimasukkan ke dalam tabung sentrifus dan ditambahkan dengan 40 mL air destilasi. Bubur tepung tersebut kemudian dipanaskan di dalam water bath pada suhu 80 °C selama 30 menit. Setelah didinginkan dan mencapai suhu ruangan, larutan tersebut kemudian disentrifuse dengan kecepatan 3000 gravitasi selama 15 menit. Supernatan dipindahkan secara hati-hati dan pati yang sudah mengembang kemudian ditimbang. Supernatan yang telah dipindahkan kemudian diuapkan selama semalam pada suhu 110 °C. Analisis dilakukan secara triplikat.
(g) kering pati Bobot
(g) basah sedimen Bobot
(b/b) mengembang
Kemampuan =
(g) kering pati Bobot
(g) kering supernatan Bobot
(%) Kelarutan =
3.5.13 Analisis Tekstur (Zoulias et al. 2002)
Tekstur dari sampel cookies dianalisis dengan menggunakan TexturePro
CT VI.2 Build 9 menggunakan sharp probe, panjang 6 cm dan tebal 0.1 mm. Alat tersebut di set dengan kecepatan 1 mm/s dan jarak 3 mm. Semua pengukuran dilakukan sebanyak enam kali dan hasil yang ditampilkan adalah nilai rata-rata dari keenam nilai tersebut.
3.5.14 Nilai energi cookies (Almatsier 2001)
Penentuan nilai energi makanan melalui perhitungan dapat dilakukan menurut komposisi karbohidrat, lemak protein, serta nilai energi makanan tersebut.
Energi = (4 kkal/g × kadar karbohidrat ) + (4 kkal/g × kadar protein) + (9 kkal/g × kadar lemak)
3.5.15 Karakteristik pemasakan, meliputi :
Analisis Waktu Optimum Pemasakan (AACC 1999)
Prinsip dari analisis ini adalah mengukur waktu hingga mie tidak membentuk garis putih ketika ditekan dengan dua potong kaca. Mie kering ditimbang sebanyak 5 g, kemudian air sebanyak 150 mL dididihkan pada gelas piala bertutup dan dibiarkan memdidih selama 3 menit. Sampel mie dimasukkan kedalam gelas piala dan ditutup kembali. Stop watch dinyalakan tepat pada saat sampel dimasukkan dalam air yang telah dididihkan. Setiap satu menit dilakukan pengambilan satu untaian mie dan dilakukan penekanan dengan dua buah kaca. Pemasakan dikatakan optimum bila sudah tidak terbentuk garis putih ketika mie ditekan dengan dua potong kaca.
Analisis kehilangan padatan selama pemasakan (AACC 1999)
100% awal
Berat
n dikeringka setelah
supernatan
KPAP= ×
100% awal
Berat
awal berat -rehidrasi setelah
Mi ×
= rption Water abso
3.5.16 Texture Profile Analysis (TPA) mie dengan Texture Analyzer Brookfield Engineering© TC3
Pengukuran tekstur mie dilakukan setelah mie direhidrasi sesuai dengan waktu optimum pemasakan, sehingga data karakteristik tekstur yang dihasilkan merupakan kondisi siap untuk dikonsumsi. Mie (sekitar 10 cm) sebanyak 50 g dimasukan ke dalam 700 mL air yang telah dididihkan selama 3 menit. Waktu pemasakan disesuaikan dengan waktu optimum pemasakan. Mie yang telah masak disiram dengan 100 mL air dingin sebanyak dua kali dan ditiriskan, kemudian dengan cepat dilakukan pengukuran tekstur.
Probe yang digunakan adalah berbentuk silinder dengan diameter 38.1 mm. Alat diset dengan pre test speed 2.0 mm/s, tes speed 0.1 mm/s, repture test distance 50%, force 4.5 g dan count 2. Sampel yang telah direhidrasi diletakkan pada probe tersebut, kemudian alat dijalankan. Hasil analisis TPA akan memperoleh nilai kekerasan dengan satuan gram force (gf), elastisitas dangan satuan gram second (gs), dan kelengketan dengan satuan gram force (gf). Hasil kurva menunjukkan hubungan antara gaya untuk mendeformasi waktu.
Kekerasan digambarkan sebagai gaya (gf) yang dibutuhkan untuk menggigit mie. Tingkat kekerasan diperoleh dari maksimum gaya (nilai puncak) pada tekanan pertama (Hardness 1). Elastisitas diartikan sebagai kemampuan sampel untuk dapat kembali untuk ke kondisi semula setelah diberikan tekanan pertama sehingga disebut juga kekenyalan. Penentuan tingkat elastisitas berdasarkan rasio antara jarak yang ditempuh oleh sampel pada tekanan kedua sehingga tercapai nilai gaya maksimum (L2) dengan jarak yang ditempuh oleh sampel pada tekanan pertama sehingga tercapai gaya maksimum (L1) atau (L2/L1). Kelengketan ditentukan berdasarkan nilai puncak di bawah kurva atau
4. HASIL DAN PEMBAHASAN
4.1 Karakterisasi Sifat Fisikokimia Umbi Walur 4.1.1 Analisis Proksimat
Penelitian mengenai umbi walur sangatlah terbatas. Hingga saat ini, belum banyak pengetahuan mengenai kandungan kimia yang terdapat pada umbi walur. Berdasarkan hasil analisis, diketahui bahwa umbi walur memiliki kandungan lemak, protein, abu dan karbohidrat berturut-turut sebesar 14.41; 6.42; 4.89; dan 74.28% bk. Hasil ini tidak terlalu berbeda dengan kandungan gizi yang terdapat pada umbi suweg menurut Das et al. (2009). Kandungan gizi tertinggi pada umbi walur adalah karbohidrat (Tabel 2). Meskipun kandungan karbohidrat pada umbi walur lebih rendah dibandingkan dengan umbi suweg dan singkong, namun hasil tersebut masih mengindikasikan bahwa seperti halnya umbi suweg dan singkong, umbi walur pun memiliki potensi untuk dimanfaatkan menjadi sumber bahan pangan alternatif.
Tabel 2 Perbandingan data proksimat umbi walur dan umbi Suweg
No. Komposisi kimia Walur Suweg Singkongc
1. Kadar air (% bb) 74.46 78.70 a 62.50 2. Kadar lemak (% bk) 14.41 0.47 a 0.80 3. Kadar protein (% bk) 6.42 5.63 a 3.20 4. Kadar abu (% bk) 4.89 7.51 a 0.3 5. Kadar karbohidrat (% bk) 74.28 86.38 a 92.53 6. Kadar pati (% bk) 65.72 39.36 b 75.00
a
Das et al. (2009); bRichana dan Titi (2004); cRukmana (1997)
4.1.2 Ukuran Granula Pati Walur
Pati terdiri atas butiran-butiran kecil yang disebut sebagai granula. Gambar 9a menunjukkan sifat birefringence dari pati, yaitu sifat granula pati yang dapat merefleksikan cahaya terpolarisasi sehingga di bawah mikroskop polarisasi membentuk bidang berwarna biru dan kuning. French (1984) menyatakan bahwa warna biru dan kuning pada permukaan granula pati disebabkan oleh adanya perbedaan indeks refraktif dalam granula pati. Indeks refraktif tersebut dipengaruhi oleh struktur molekular amilosa dalam pati. Bentuk heliks dari amilosa dapat menyerap sebagian cahaya yang melewati granula pati (Zhou et al.
1998).
[image:52.612.154.454.293.495.2](a) (b)
Gambar 9 Bentuk granula pati umbi walur mikroskop polarisasi (a); Scanning Electron Microscop (SEM) (b).
Sebaran, bentuk dan ukuran granula setiap jenis pati adalah berbeda-beda tergantung dari molekul penyusunnya, yaitu amilosa dan amilopektin. Penampakan mikroskopik dari granula pati seperti bentuk, ukuran, keseragaman dan letak hilium berbeda-beda untuk setiap jenis tanaman penghasil pati. Dengan demikian sifat fisik tersebut dapat digunakan sebagai variabel dalam identifikasi pati.
4.1.3 Kadar Amilosa dan Kekuatan Gel
[image:53.612.127.513.385.432.2]Tiap jenis pati memiliki sifat yang tidak sama tergantung dari panjang rantai karbon dan perbandingan antara molekul yang lurus (amilosa) serta yang bercabang (amilopektin). Kandungan amilosa pati walur adalah sebesar 22.42% (Tabel 3). Hasil ini menunjukkan bahwa pati walur termasuk ke dalam jenis pati normal. Menurut Hoover et al. (2010), jenis pati normal adalah jenis pati yang memiliki kandungan amilosa sebesar 15-30%.
Tabel 3 Perbandingan data karakteristik umbi walur dan tepung terigu
No. Komposisi kimia Walur