ABSTRAK
UJI APLIKASI JAMURBEAUVERIA BASSIANA (BALSAMO) VUILL. TERHADAP SYMPHYLID YANG HIDUP PADA TANAH
BERBAHAN ORGANIK DAN TANPA BAHAN ORGANIK DI LABORATORIUM
Oleh
Desye Rinche Natalia Simarmata
Desye Rinche Natalia Simarmata
perlakuan dimana symphylid hidup pada tanah yang berbahan organik maupun tanpa bahan organik sangat rendah. Mortalitas symphylid tertinggi pada kedua set percobaan terdapat dalam perlakuan aplikasiB. bassiana terhadap symphylid yang hidup pada tanah berbahan organik yaitu sebesar 10 % dan 6 %. Dengan demikian hasil penelitian ini belum dapat
membuktikan bahwaB. bassianasecara nyata mampu menginfeksi symphylid.
UJI APLIKASI JAMURBEAUVERIA BASSIANA(BALSAMO) VUILL.TERHADAP SYMPHYLIDYANG HIDUP PADA TANAH
BERBAHAN ORGANIK DAN TANPA BAHAN ORGANIK DI LABORATORIUM
Oleh
DESYE RINCHE NATALIA SIMARMATA
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA PERTANIAN
Pada
Jurusan Agroteknologi Fakultas Pertanian
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
UJI APLIKASI JAMURBEAUVERIA BASSIANA(BALSAMO) VUILL.TERHADAP SYMPHYLIDYANG HIDUP PADA TANAH
BERBAHAN ORGANIK DAN TANPA BAHAN ORGANIK DI LABORATORIUM
(Skripsi)
Oleh
DESYE RINCHE NATALIA SIMARMATA
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
iv
iv
DAFTAR GAMBAR
Gambar Halaman
1. Tanaman nanas yang terserang symphylid ………. 8
2. Symphylid dewasa ……….. 9
3. Telur symphylid ………. 10
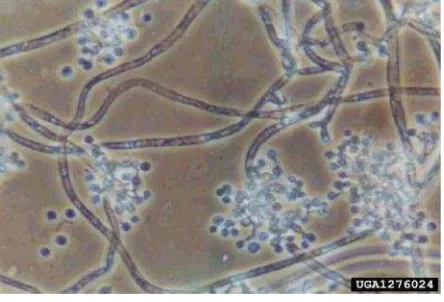
4. Konidia jamurB. bassiana ……… 12
5. Tata letak unit-unit percobaan pada metode residu pakan ………. 22
6. Tata letak unit-unit percobaan pada metode residu pada hidup symphylid ………... 23
7. Telur symphylid (a) dan symphylid yang mengalami kematian (b) ………... 29
DAFTAR ISI
Halaman
DAFTAR TABEL ...….. i
DAFTAR GAMBAR ...….. iv
I. PENDAHULUAN ………. 1
1.1 Latar Belakangdan Masalah ……… 1
1.2 Tujuan Penelitian ...….. 4
1.3 Kerangka Pemikiran ………. 4
1.4 Hipotesis ………... 6
II. TINJAUAN PUSTAKA ………. 7
2.1Symphylid ……….. 7
a. Taksonomi symphylid ……… 7
b. Gejala kerusakan ……… 8
c. Morfologi ……… 9
d. Siklus hidup ……… 10
e. Pengendalian symphylid ………. 10
2.2 Jamur EntomopatogenBeauveria bassiana (Baals.) (Vuill) ………..…. 11
a. Mekanisme infeksi jamurB. bassiana ……….. 12
b.Keamanan hayati ……….. 13
c. Perbanyakan jamur entomopatogen B. bassiana …………... 14
2.3Bahan Organik ………... 14
III. BAHAN DAN METODE ………... 15
3.1 Waktu dan Tempat Penelitian ………... 16
3.2 Bahan dan Alat ………. 16
3.3 Metode Penelitian ……….. 17
3.4.1 Persiapan symphylid percobaan ……….. 18
3.4.1.1 Pengambilan symphylid ……… 18
3.4.1.2 Rearing symphylid ……… 18
3.4.2 Perbanyakan jamurB. bassiana ……… 19
3.4.2.1 Pembuatan mediaPotato Dextrose Agar (PDA)19 ……….. 19
3.4.2.2 Pembuatan kultur murniB.bassiana. …………... 19
3.4.2.3 PerbanyakanB. bassianadengan menir jagung ……….... 20
3.4.3 PengujianB. bassianapada symphylid ……….. 20
3.4.3.1 Pembuatan suspensiB. bassiana ……… 20
3.4.2.2 Penyiapan unit percobaan ………... 21
a. Aplikasi dengan metode residu pakan ………. 21
b. Aplikasi dengan metode tanah media hidup symphylid ………... 22
3.5 Pengamatan ………. 24
3.6 Analisis Data ……….. 25
IV. HASIL DAN PEMBAHASAN ………. 26
4.1 Mortalitas Symphylid pada Pengujian AplikasiB. bassiana dengan Metode Residu Pakan ……… 26
4.2 Mortalitas Symphylid pada Pengujian Aplikasi B. bassianadengan Metode Residu Tanah Media Hidup Symphylid ………. 27
V. KESIMPULAN DAN SARAN ……… 31
5.1 Kesimpulan ………... 31
5.2 Saran ……… 31
PUSTAKA ACUAN ……….. … 32
i
DAFTAR TABEL
Tabel Halaman
1. Data hasil pengamatan mortalitas symphylid pada metode
residu pakan. ……….. 24 2.Data hasil pengamatan mortalitas symphylid pada metode
residu pada hidup symphylid. ………... 24 3. Persentase mortalitas symphylid selama 20 hari pengamatan
aplikasiB. bassianadengan metode residu pakan. ………... 26 4. Persentase mortalitas symphylid selama 20 hari pengamatan
aplikasiB. bassianadengan metode residu tanah media hidup
symphylid. ………. 28
5. Data Mortalitas symphylid (ekor) tanpa aplikasiB. bassiana
(Kontrol). ………... 36 6. Data mortalitas symphylid (ekor) aplikasiB. bassianadengan
metode residu pakan terhadap symphylid yang hidup pada tanah
berbahan organik. ………. 37 7. Hasil perhitungan mortalitas symphylid berdasarkan data
hasil pengamatan aplikasiB.bassianaterhadap symphylid
dengan metode residu pakan. ……… 38 8. Data awal hasil perhitungan mortalitas symphylid 1-5 hsa aplikasi
B. bassianadengan metode residu pakan. ……… 39 9. Data hasil perhitungan mortalitas symphylid 5 hsa aplikasi
B. bassianadengan metode residu pakan pada sidik ragam
taraf 5%. ……… 39 10. Data awal hasil perhitungan mortalitas symphylid 10 hsa
aplikasiB. bassianadengan metode residu pakan. ………... 40 11. Data hasil perhitungan mortalitas symphylid 10 hsa aplikasi
B. bassianadengan metode residu pakan pada sidik ragam
ii 12. Data awal hasil perhitungan mortalitas symphylid 15 hsa
aplikasiB. bassianadengan metode residu pakan. ……… 40 13. Data hasil perhitungan mortalitas symphylid 15 hsa aplikasi
B. bassianadengan metode residu pakan pada sidik ragam
taraf 5%. ………. 41 14. Data awal hasil perhitungan mortalitas symphylid 20 hsa
aplikasiB. bassianadengan metode residu pakan. ……… 41 15. Data hasil perhitungan mortalitas symphylid 20 hsa aplikasi
B. bassianadengan metode residu pakan pada sidik ragam
taraf 5%. ……… 41 16. Persentase mortalitas symphylid selama 20 hari pengamatan
aplikasiB. bassianadengan metode residu pakan. ……… 42 17. Data aplikasi mortalitas symphylid tanpaB. bassiana.
(Kontrol). ………... 43 18. Data mortalitas symphylid (ekor) aplikasiB. bassianadengan
metode residu pada tanah berbahan organik sebagai media hidup
symphylid. ………. 44
19. Data mortalitas symphylid (ekor) aplikasiB. bassianadengan metode residu pada tanah tanpa bahan organik sebagai media
hidup symphylid. ……….. 45 20. Hasil perhitungan mortalitas symphylid berdasarkan data hasil
pengamatan aplikasiB.bassianadengan metode residu tanah
media hidup symphylid. ……… 46 21. Data awal hasil perhitungan mortalitas symphylid 5 hsa aplikasi
B.bassianadengan metode residu tanah media hidup
Symphylid. ………. 46 22. Data hasil perhitungan mortalitas symphylid 5 hsa aplikasi
B. bassianadengan metode residu tanah media hidup symphylid
pada sidik ragam taraf 5%. ……….. 46 23. Data awal hasil perhitungan mortalitas symphylid 10 hsa aplikasi
B.bassianadengan metode residu tanah media hidup
Symphylid. ………... 47 24. Data hasil perhitungan mortalitas symphylid 10 hsa aplikasi
B. bassianadengan metode residu tanah media hidup symphylid
iii 25. Data awal hasil perhitungan mortalitas symphylid 15 hsa aplikasi
B.bassianadengan metode residu tanah media hidup
Symphylid. ……….. 47 26. Data hasil perhitungan mortalitas symphylid 15 hsa aplikasi
B. bassianadengan metode residu tanah media hidup symphylid
pada sidik ragam taraf 5%. ………... 48 27. Data awal hasil perhitungan mortalitas symphylid 1-20 hsa
aplikasiB.bassianadengan metode residu tanah media hidup
Symphylid. ……… 48 28. Data hasil perhitungan mortalitas symphylid 1-20 hsa aplikasi
B. bassianadengan metode residu tanah media hidup symphylid
pada sidik ragam taraf 5%. ……… 48 29. Persentase mortalitas symphylid selama 1-20 hari pengamatan
aplikasiB. bassianadengan metode residu tanah media hidup
`
Tuhan, berikanlah kepadaku hati yang tentram untuk
menerima apa yang tidak bisa aku ubah, keberanian untuk
mengubah apa yang masih bisa aku ubah, dan hikmat untuk
membedakan kedua-duanya
(Reinhold Niebuhr)
Tuhan gak pernah terlambat atau terlalu cepat, Tuhan
punya waktu yang tepat
Ketika aku memiliki keberanian menghadapi
suatu kegagalan besar dalam hidupku, aku tidak
perlu takut dan berhenti, karena keberhasilan
adalah milikku
Tunduk kepada proses, hidup dalam proses, pembentukan pasti mengalami proses untuk mencapai suatu terobosan,
I am History Maker
Dengan penuh rasa syukur kupersembahkan karya ini sebagai
tanda terimakasihku kepada
Kedua orangtuaku
Bapak Walsen Simarmata dan Mama Meri Sianipar, S. Pd.
sebagai wujud bakti, cinta dan terimakasihku, yang telah
mencurahkan seluruh kasih sayang, nasihat, kesabaran, perhatian,
motivasi, kerjakeras dengan tulus telah membesarkan, mendidik,
dan mendoakan. Tuhan Yesus Memberkati.
Kedua adikku tersayang,
Deka Anggie Pratama Simarmata
dan
Daniel Sapta Nuari Simarmata
.Keluarga besarku Op. Jonter Simarmata dan Op. Maju Sianipar
serta para sahabat yang telah memberikan doa dan dukungan serta
motivasi selama ini
RIWAYAT HIDUP
Penulis dilahirkan di Kelurahan Dayamurni, Kecamatan Tulang Bawang Tengah, Kabupaten Tulang Bawang Barat, pada tanggal 31 Desember 1990. Penulis
merupakan putri pertama dari tiga bersaudara pasangan Bapak Walsen Simarmata dan Ibu Meri Sianipar, S. Pd.
Penulis telah menyelesaikan pendidikan Sekolah Dasar Negeri 04 Panaragan Jaya Tulang Bawang Barat pada tahun 2003; Sekolah Menengah Pertama di SMP Negeri 02 Tulang Bawang Tengah pada tahun 2006; Sekolah Menengah Atas di SMA PGRI 01 Dayamurni Tulang Bawang Barat pada tahun 2009. Penulis terdaftar sebagai Mahasiswa Program Studi Agroteknologi Fakultas Pertanian, Universitas Lampung pada tahun 2009 melalui jalur Ujian Masuk Lokal (UML).
SANWACANA
Puji syukur Penulis sampaikan kepada Tuhan Yang Maha Esa yang telah memberikan anugerah, mencurahkan kasihNYA, melimpahkan berkat, karunia, kemurahan, ilmu serta memberikan kemudahan dan kelancaran kepada penulis untuk dapat menyelesaikan skripsi ini. Di dalam proses peulisan skripsi ini
penulis telah menerima bantuan dan bimbingan dari banyak pihak. Oleh karena itu penulis mengucapkan terima kasih kepada:
1. Ibu Ir. Lestari Wibowo, M. P., selaku pembimbing utama atas bimbingan, saran, motivasi, serta kesabaran yang diberikan selama penelitian dan penyusunan skripsi ini.
2. Bapak Dr. Ir. Afandi, M. P., selaku pembimbing kedua atas bimbingan, saran, motivasi, serta kesabaran yang diberikan selama penelitian dan penyusunan skripsi ini.
3. Bapak Prof. Dr. Ir. Hamim Sudarsono, M. Sc., selaku pembahas atas
bimbingan, saran, motivasi, serta kesabaran yang diberikan selama penelitian dan penyusunan skripsi ini.
4. Bapak Ir. Agus Muhammad Hariri, M. S., selaku dosen pembimbing
akademik atas bimbingan, saran, nasihat, dan dukungan yang selalu diberikan kepada penulis selama masa kuliah di Perguruan Tinggi Universitas Lampung. 5. Bapak Prof. Dr. Ir. Purnomo, M. S., selaku ketua bidang proteksi tanaman
6. Bapak Dr. Ir. Kuswanta Futas Hidayat, M. P., selaku Ketua Program Studi Agroteknologi, Fakultas Pertanian, Universitas Lampung.
7. Bapak Prof. Dr. Ir. Irwan Sukri Banuwa, M. Sc., selaku Dekan Fakultas Pertanian, Universitas Lampung.
8. Kedua orangtuaku Bapak Walsen Simarmata dan Mama Meri Sianipar, S. Pd., atas cinta, doa, dan dukungan yang tak terbatas.
9. Kedua adikku tersayang Deka Anggie Pratama Simarmata dan Daniel Sapta Nuari atas segala cinta, doa dan dukungannya.
10. Teman-teman seperjuanganku,“Konsentrasi Hama dan Penyakit Tanaman” AGT 2009 atas dukungan dan semangat serta pertemanannya selama ini. 11. Teman-teman, Candra Susanti, Siti Jarlina, Susi Susanti, Dina Marlinawati,
Eko Andrianto, Ika, Maya, Fransiskus, Icha, Septi, Desnidasari, Irma Banjarnahor, Eka, Wasis, Aldi, Maria dan Astri Ambun.
12. Penyemangatku, Dadang Riadi.
13. Mba Uum, Bapak Paryadi, Mas Mustofa, Mas Jein, dan Mas Iwan atas bantuannya.
Bandar Lampung, 10 Desember 2015
Penulis
I. PENDAHULUAN
1.1 Latar Belakang dan Masalah
Nanas (Ananas comusus) merupakan salah satu tanaman hortikultura yang buahnya banyak disukai oleh masyarakat di berbagai penjuru dunia. Nanas mendominasi perdagangan buah tropika dunia sehingga nanas juga sangat berperan dalam bidang ekonomi. Produksi buah nanas mencapai 20 % dari buah tropika dunia. Berdasarkan data dari Badan Statistik Nasional pada tahun 2012, hasil produksi nanas yaitu 178. 899 ton. Indonesia merupakan negara pengekspor buah nanas, baik dalam bentuk buah nanas olahan atau buah segar. Tanaman nanas ini sangat potensial untuk terus dikembangkan karena berperan sebagai komoditas ekspor (BPS, 2012).
2 terbesar di dunia dan menjadi produsen utama nanas olahan di Indonesia (Oviana, 2013).
Pemanfaatan lahan secara intensif untuk menanaman tanaman semusim sepanjang tahun dapat menurunkan kandungan bahan organik di dalam tanah. Karamaet al. (1990) menyatakan untuk mempertahankan kandungan bahan organik tanah perlu diimbangi dengan pemberian pupuk organik yang memadai. Tanpa bahan
organik, kesuburan tanah akan menurun meskipun pupuk anorganik diberikan dengan takaran tinggi. Pertanaman nanas membutuhkan tanah dengan aerasi dan drainase yang baik, serta mengandung humus. Nanas cukup toleran dengan pH rendah (tanah masam), sehingga pada kondisi tersebut masih mampu tumbuh subur dan berbuah baik. Derajat keasaman yang sesuai untuk tanaman ini berkisar antara 4,5-5,5 (Lisdiana dan Soemadi, 1997).
Selain itu, adanya organisme pengganggu tanaman (OPT) menjadi salah satu kendala dalam budidaya pertanaman nanas. Akhir-akhir ini PT GGP melakukan pemberian bahan organik yang tinggi untuk pertanaman nanas. Permasalahan muncul ketika terdapat kerusakan pada akar tanaman nanas dalam jumlah yang tinggi. Lisdiana dan Soemadi (1997) melaporkan tanaman nanas memiliki perakaran sedikit dan dangkal serta peka terhadap penggenangan. Kerusakan pada akar tanaman nanas ini disebabkan oleh symphylid.
3 Daun menjadi berwarna merah dan semakin lama tanaman akan menjadi kerdil dan mati. Hal ini menyebabkan kerugian besar bagi PT GGP, sehingga dilakukan pengendalian symphylid dengan fumigan dan pestisida kimia. Salah satu
alternatif untuk mengurangi penggunaan insektisida sintetik dalam mengendalikan populasi hama adalah mengunakan agensia hayati berupa jamur entomopatogen.
Beauveria bassianamerupakan jamur yang dapat menginfeksi serangga dan banyak ditemukan di dalam tanah. Mandalet al. (2003) menyatakan bahwa patogen serangga tidak mengakibatkan resistensi hama, dan aman bagi organisme bukan sasaran, termasuk mamalia. Selain itu, keefektifan jamur patogen dalam mengendalikan berbagai jenis serangga hama sudah tidak diragukan lagi. Di dalam tubuh inangnya jamur ini akan memperbanyak diri hingga seluruh jaringan serangga terinfeksi. Serangga yang telah terinfeksiB. bassianabiasanya akan berhenti makan, sehingga menjadi lemah, dan akhirnya mengalami kematian. Serangga yang mati tidak selalu disertai gejala pertumbuhan spora. Secara umum jamur entomopatogen membutuhkan lingkungan yang lembab untuk dapat
menginfeksi serangga.
Plate (1976) menyatakan bahwa mekanisme infeksi yang dilakukanB. bassiana dimulai dari melekatnya konidia pada kutikula serangga, kemudian berkecambah dan tumbuh di dalam tubuh inangnya. Symphylid juga merupakan hewan
4
1.2 Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui apakah jamur entomopatogenB. bassianayang diaplikasikan mampu menginfeksi symphylid yang hidup pada tanah berbahan organik maupun tanpa bahan organik.
1.3 Kerangka Pemikiran
Karamaet al. (1990) menyatakan untuk mempertahankan kandungan bahan organik tanah perlu diimbangi dengan pemberian pupuk organik yang memadai. Tanpa bahan organik, kesuburan tanah akan menurun meskipun pupuk anorganik diberikan dengan takaran tinggi. Permasalahan terjadi ketika pemberian bahan organik yang tinggi pada tanaman memicu munculnya hewan artropoda seperti symphylid. Flint (1990) menyatakan symphylid memakan bibit yang tumbuh, akar tanaman, rambut akar dan bahan organik yang membusuk. Indikasi
kerusakan yang ditimbulkan symphylid adalah tanaman kerdil dan tanaman sakit. Tingginya tingkat pembusukan bahan organik adalah daya tarik utama untuk hama ini.
5 Secara umum jamur entomopatogen membutuhkan lingkungan yang lembab untuk dapat menginfeksi serangga.
Jamur B. bassiana pada dasarnya mampu menginfeksi hewan artropoda dari kelas insekta terutama dari ordo Lepidoptera, Hemiptera, Homoptera, dan Coleoptera (Varela andMorales 1996; Hardaningsih dan Prayogo 2001; Prayogo et al.2002b). Hal tersebut dapat dibuktikan dalam beberapa penelitian dimana jamur patogen serangga mampu mengendalikan berbagai jenis serangga hama seperti hama perusak pucuk pada tanaman kelapa (Mandarina, 2008), ulat grayak (Surtikanti dan Yasin, 2009dalamNunilahwatiet al., 2012),wereng coklat (Rahayuningtias dan Julyasih, 2010), wereng hijau (Ladja, 2010), penggerek tongkol jagung (Khasanah, 2008), penggerek umbi kentang (Khairani, 2007) dan penggerek buah kopi (Marleni, 2013).
6
1.4 Hipotesis
Berdasarkan kerangka pemikiran yang telah diuraikan hipotesis pada penelitian ini adalah jamur entomopatogenB. bassianabersifat patogenik dan dapat
II. TINJAUAN PUSTAKA
2.1 Symphylid
a. Taksonomi symphylid
Symphylid merupakan bagian dari kelas Symphyla (Ghidiu, 2005). Symphyla merupakan bagian dari filum artropoda subfilum Miriapoda. Kelas Symphyla sendiri terdiri atas dua famili, yaitu Scutigerellidae dan Scolopendrellidae
(Scheller, 1961). Scheller dan Addis (2002) menyebutkan Symphyla memiliki 15 genus dan 500 spesies di dunia. Secara sederhana klasifikasi symphylid adalah sebagai berikut:
Filum : Artropoda Subfilum : Miriapoda Kelas : Symphyla
Ordo : Symphyla/ Cephalostigmata Famili : Scutigerellidae
Genus :Scutigerella&Hanseniella
Spesies :Scutigerellaspp. &Hanseniellaspp.
8
b. Gejala kerusakan
Symphylid merupakan salah satu hama yang merusak akar pada tanaman nanas. Selain itu, symphylid juga memakan tumbuhan lainnya seperti ganggang, jamur dan lumut. Namun, pada saat masa tanam, symphylid tertarik dengan biji dan akar yang sangat muda, dimana symphylid membutuhkan makan yang banyak dengan mengunyah akar yang lebih tua (Waterhouse, 1968). Symphylid dapat menurunkan produksi tanaman dan menyebabkan akar “sapu setan”. Kerusakan
akar pada tanaman akan mempengaruhi pertumbuhan dan hasil, terutama jika tanah kering. Apabila populasi symphylid meningkat pada waktu tanam, pertumbuhan tanaman muda akan terhambat karena rusaknya akar. Tanaman yang terserang symphylid memiliki sedikit akar dan mudah ditarik dari dalam tanah dan menyebabkan tanaman mati (Bartholomew, 2003).
9
Flint (1990) menyatakan symphylid memakan bibit yang tumbuh, akar tanaman, rambut akar dan bahan organik yang membusuk. Indikasi kerusakan yang ditimbulkan symphylid adalah tanaman kerdil dan tanaman sakit. Tingginya tingkat pembusukan bahan organik adalah daya tarik utama untuk serangga ini.
c. Morfologi
Symphylid berbentuk kecil, mirip dengan Miriapoda, tidak memiliki mata dan warna tubuh (Greenslade, 2002). Symphylid memiliki panjang tubuh antara 2-6 mm dan terlihat seperti lipan berwarna putih (Bartholomew, 2003).
Flint (1990) menyatakan bahwa symphylid memiliki 12 pasang kaki, 14 bagian tubuh, dan sepasang antena panjang berbentuk manik-manik. Symphylid yang belum dewasa lebih kecil dan memiliki 6 pasang kaki.
10
d. Siklus hidup
Symphylid meletakkan telur secara berkelompok antara 4-25 butir, pada kedalaman 9-12 inci di bawah permukaan tanah. Telur menetas dalam waktu sekitar 10 hari menjadi nimfa dengan 6 pasang kaki dan 6 segmen antennal. Seluruh siklus hidup berkisar 45-60 hari. Selama cuaca panas, symphylid bergerak ke dalam lapisan tanah. Symphylid sangat peka terhadap cahaya dan bergerak cepat di tanah, bersembunyi dengan cepat ketika diganggu (Flint, 1990).
Gambar 3. Telur symphylid (Sumber: Ralph Berry, 1973)
e. Pengendalian symphylid
11
2.2 Jamur EntomopatogenBeauveria bassiana (Bals.) (Vuill.)
Salah satu jamur entomopatogen yang sangat potensial dalam pengendalian beberapa spesies serangga hama yaituB. bassiana (Balsamo) Vuillemin. Gillespie (1988) menyatakan jamurB. bassianasebagai agensi hayati sangat efektif mengendalikan sejumlah spesies serangga hama termasuk kutu putih, rayap, dan beberapa jenis kumbang. Secara sederhana taksonomi jamurB. bassiana (Bals.) (Vuill.) menurut Hughes (1971) seperti berikut:
Filum : Ascomycota Kelas : Hypomycetes Ordo : Hypocreales Famili : Clavicipitaceae Genus : Beauveria
Species :Beauveria bassianaBalsamo Vuill.
B. bassianamerupakan cendawan tanah yang sangat umum di temukan di seluruh dunia. Cloyd (2003) melaporkan sampai saat ini telah dikenal lebih dari 750 spesies jamur entomopatogen dari sekitar 100 generasi jamur.
12
Gambar 4. Konidia jamurB. bassiana
(Sumber:http://www.forestryimages.org/browse/subthumb.cfm?sub=3482)
JamurB. bassianamemiliki spektrum yang luas dan dapat mengendalikan banyak spesies serangga hama tanaman. Jamur ini masuk ke dalam tubuh serangga melalui kulit diantara ruas-ruas tubuh. Penetrasi terjadi pada saat spora pada kutikula tumbuh. Hifa jamur mengeluarkan enzim kitinase, lipase, dan protemase yang mampu menguraikan komponen penyusun kutikula serangga. Di dalam tubuh serangga hifa berkembang dan masuk kedalam pembuluh darah (Mahr, 2003).
a. Mekanisme infeksi jamurB. bassiana
13 Plate (1976) menggungkapkan efektivitasB. bassianadalam menginfeksi
serangga hama tergantung pada spesies atau strain jamur, dan kepekaan stadia serangga pada tingkat kelembaban lingkungan, struktur tanah (untuk serangga dalam tanah), serta temperatur yang tepat.
Mekanisme infeksi dimulai dari melekatnya konidia pada kutikula serangga, kemudian berkecambah dan tumbuh di dalam tubuh inangnya (Plate, 1976). Spora yang jatuh pada permukaaan kutikula berkecambah dan untuk menembus lapisan kutikula, digunakan tabung penetrasi yang dibentuk pada ujung tabung kecambah. Setelah mencapai saluran pembuluh darah, jamur tumbuh dengan pesat sehingga nutrisi di dalam tubuh terserap, kemudian darah menjadi kental, dan akhirnya mati. JamurB. bassianamemproduksi toksin yang disebut
beauvericin. Toksin ini dapat menyebabkan gangguan pada fungsi hemolimfa dan
nukleus serangga sehingga mengakibatkan pembengkakan yang disertai pengerasan pada serangga yang terinfeksi (Kučera dan Samšiňáková, 1968).
Serangga inang utamaB. bassianayang dilaporkan oleh Plate (1976) yaitu kutu pengisap (aphid), kutu putih (whitefly), belalang, hama pengisap, lalat, kumbang, ulat, thrips, tungau, dan beberapa spesies uret.
b. Keamanan hayati
14 bassiacridin, bassianolide, beauverolides, tenellin, dan oosporein (Strasseret al., 2000; Veyet al., 2001; Quesada-Moraga and Vey, 2004).
Tingkat kepekaan serangga bukan sasaran terhadap infeksiB. bassiana diungkapkan Plate (1976) sangat ditentukan oleh virulensi dan patogenisitas jamur, serta spesies serangga inang. Selain itu, perbedaan fisiologis dan ekologis inang juga mempengaruhi infeksiB. bassiana. Misalnya, serangga bukan sasaran yang mudah terinfeksiB. bassianadi laboratorium tidak akan serta merta terinfeksi pada kondisi lapang.
c. Perbanyakan jamur entomopatogenB. bassiana
PerbanyakanB. bassianasebagian besar dilakukan pada media padat, seperti beras, gandum, atau jagung (Nelson and Glare, 1996; Junianto dan
Sulistyowati, 2002). Fungsi utama jamurB. bassiana adalah menginfeksi inang, maka konidia merupakan propagul jamur yang paling memungkinkan untuk diproduksi. Tiga jenis bahan media alami yang telah dicoba dalam perbanyakan B. bassianaskala besar di New Zealand adalah beras, gandum, dan barley. Beras merupakan media paling sesuai bagi perkembanganB. bassianadengan
produktivitas konidia tertinggi mencapai 4,38 x 109 konidia/g beras.
2.3 Bahan Organik
15 sehingga pada kondisi tersebut masih mampu tumbuh subur dan berbuah baik. Tanah harus ringan hingga sedang dengan tekstur setengah berat atau liat. Derajat keasaman yang sesuai untuk tanaman ini berkisar antara 4,5-5,5 (Lisdiana dan Soemadi, 1997).
III. BAHAN DAN METODE
3.1 Tempat dan Waktu Penelitian
Penelitan ini dilaksanakan di Laboratorium Hama dan Penyakit Tanaman, Fakultas Pertanian, Universitas Lampung. Symphylid sebagai hama uji dalam penelitian ini diperoleh dari kebun nanas milik PT Great Giant Pineapple (GGP) Kecamatan Terbanggi Besar Kabupaten Lampung Tengah. Penelitian ini dilaksanakan pada bulan Januari-April 2015.
3.2 Bahan dan Alat
Bahan-bahan yang digunakan pada penelitian ini yaitu media PDA (potato
dextrose agar), menir jagung, isolat jamurB. bassianayang diperoleh dari UPTD Balai Perlintanbun Tegineneng, Lampung, aqua destilata steril, tissue, alkohol 70 %, daun pepaya, dan tanah berbahan organik. Hama uji dalam penelitian ini yaitu symphylid yang diperoleh dari PT GGP Kecamatan Terbanggi Besar, Kabupaten Lampung Tengah.
17
autoklaf,laminar air flow(LAF), lemari pendingin, timbangan elektrik, kertas label, dan kaca pembesar (luv).
3.3 Metode Penelitian
Penelitian ini terdiri dari 2 set percobaan, yaitu aplikasiB. bassianaterhadap symphylid dengan metode residu pakan dan metode residu tanah pada media hidup symphylid. Masing-masing percobaan disusun dalam Rancangan Acak Lengkap (RAL) yang terdiri dari 3 perlakuan dan 10 ulangan sehingga terdapat 30 satuan percobaan. Perlakuan untuk metode residu pakan adalah sebagai berikut: KP : Tanpa aplikasiB. bassiana.
BP : AplikasiB. bassianadengan metode residu pakan terhadap symphylid yang hidup pada tanah berbahan organik.
TP :AplikasiB. bassianadengan metode residu pakan terhadap symphylid yang hidup pada tanah tanpa bahan organik.
AplikasiB. bassianadengan metode residu pada media hidup symphylid
dilakukan dengan cara melakukan penyemprotan suspensiB. bassianapada tanah tempat yang digunakan sebagai media hidup symphylid. Sebagai perlakuan untuk metode residu pada media hidup symphylid adalah sebagai berikut:
KM : Tanpa aplikasiB. bassiana.
BM :AplikasiB. bassianadengan metode residu pada tanah berbahan organik sebagai media hidup symphylid.
18
3.4 Pelaksanaan Penelitian
Penelitian ini dilakukan dengan 3 tahap. Pertama, persiapan symphylid sebagai serangga uji percobaan. Tahap ini meliputi kegiatan pengambilan symphylid secara manual danrearingsymphylid. Kedua, perbanyakan jamurB. bassiana yang meliputi pembuatan kultur murni dan perbanyakan dalam media jagung. Tahap terakhir yaitu pengujianB. bassianapada symphylid dengan metode residu pakan, penyiapan unit-unit percobaan dan pengamatan.
3.4.1 Persiapan Symphylid Percobaan
3.4.1.1 Pengambilan symphylid
Symphylid diperoleh dengan cara manual, yaitu menggali tanah kebun nanas pada lokasi kebun yang lembab dan pernah tergenang (perairan drainasenya yang kurang baik) sedalam 10-15 cm dengan menggunakan sekop kecil. Kegiatan ini dilakukan di perkebunan nanas milik PT GGP Lampung Tengah. Symphylid yang didapat kemudian dimasukkan ke dalam nampanrearing. Jumlah symphylid yang diperlukan untuk persiapan penelitian ini berkisar 300 ekor.
3.4.1.2 Rearingsymphylid
19
simpan atau dipelihara pada tempat yang relatif gelap. Kelembaban tanah di jaga dengan menyemprotkan air dengansprayer.
3.4.2 Perbanyakan JamurB. bassiana
3.4.2.1 Pembuatan mediaPotato Dextrose Agar(PDA)
Untuk membuat media ini bahan yang diperlukan yaitu 1laquades, 200g
kentang, 20g dextrose, dan 20gagar. Kentang dikupas hingga bersih, dicuci dan dipotong berbentuk kotak seperti dadu dengan ukuran 12 mm. Setelah itu,
kentang direbus ke dalam 1 liter air, selama kurang lebih 20 menit. Kentang dipisahkan dari larutannya, disaring supaya larutan kelihatan bersih. Air rebusan kentang tersebut dimasukkan ke dalam tabung erlenmeyer kemudian ditambahkan dextrosedan agar. Diaduk perlahan hingga homogen dan menjadi larutan PDA.
Setelah itu dilakukan sterilisasi, tabung erlenmeyer berisi larutan PDA ditutup dengan menggunakanalumunium foil, dikencangkan dengan karet gelang, dan dibungkus plastik tahan panas. Kemudian, semua bahan tersebut di autoklaf selama 2 jam. Media tersebut diangkat dan dibiarkan agak dingin. Selanjutnya, media yang telah jadi dituang ke masing-masing cawan petri dalam ruangan steril (Laminar Air Flow).
3.4.2.2 Pembuatan kultur murniB. bassiana
20
mempertahankan isolat murni. Isolasi dilakukan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Lampung dengan menggunakan media PDA kemudian dilakukan inkubasi selama ± 2 minggu.
3.4.2.3 PerbanyakanB. bassianadengan menir jagung
Menir jagung yang telah disiapkan dicuci sampai bersih, kemudian disiram dengan air mendidih. Setelah itu menir jagung dikukus hingga matang selama 30 menit, kemudian diangkat dan dikering anginkan. Setelah menir jagung dingin, sebanyak 100 g dimasukkan ke dalam kantong plastik tahan panas. Menir jagung tersebut disterilkan dengan autoklaf pada suhu 1200C, tekanan 1 atm selama 2 jam. Setelah di autoklaf , menir jagung diangkat dan dikering anginkan kembali. Selanjutnya,B. bassianadiinokulasi dan diinkubasi selama 2-3 minggu.
3.4.3 PengujianB. bassianapada symphylid
3.4.3.1 Pembuatan suspensiB. bassiana
Setelah 2 minggu masa inkubasi jamurB. bassiana pada menir jagung dilakukan pemanenan. Kemudian diambil menir jagung yang telah ditumbuhi jamurB. bassiana(formulasi basah) dengan menggunakan sendok, di timbang sebanyak 10 g. Diukur aquades sebanyak 100 ml menggunakan gelas ukur. Setelah itu aquades 100 ml dan menir jagung yang ditumbuhiB. bassianaditimbang kemudian dimasukkan ke dalam labu erlenmeyer diaduk hingga merata.
21
3.4.3.2 Penyiapan unit percobaan
Setiap unit percobaan terdiri dari toples kecil berukuran diameter 5 cm dengan tinggi 4 cm yang berisi 10 g tanah dan pakan berupa 0,3 g irisan daun pepaya. Setiap toples yang disediakan diinfestasikan 5 ekor symphylid.
a. Aplikasi dengan metode residu pakan
22
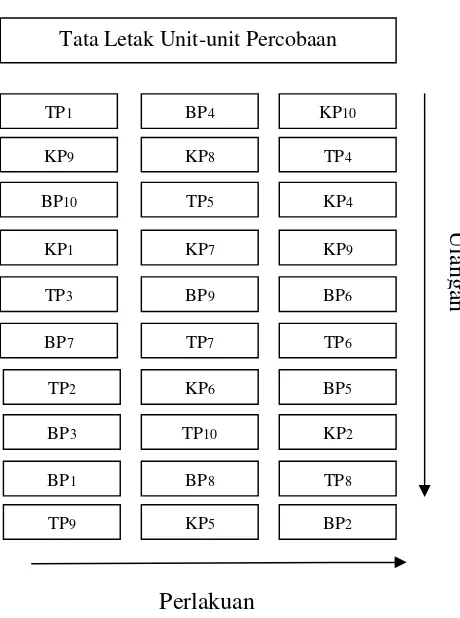
Gambar 5. Tata letak percobaan pada metode residu pakan di laboratorium. Keterangan:
KP : Tanpa aplikasiB. bassiana.
BP : AplikasiB. bassianadengan metode residu pakan terhadap symphylid yang hidup pada tanah berbahan organik.
TP : AplikasiB. bassianadengan metode residu pakan terhadap symphylid yang hidup pada tanah tanpa bahan organik.
b. Aplikasi dengan metode residu tanah media hidup symphylid
Selanjutnya, metode residu tanah pada media hidup symphylid diaplikasikan dengan 3 perlakuan yakni terdiri dari kontrol dengan tanpa penyemprotanB. bassianasebagai perlakuan pertama. Pada perlakuan kedua dan ketiga, di
U
Perlakuan
Tata Letak Unit-unit Percobaan
23
semprotkan 1cc (5 kali penyemprotan) suspensiB. bassianapada 20 g tanah baik tanah yang berbahan organik maupun tanpa bahan organik. Lalu diaduk hingga merata, dikeringangikan, kemudian symphylid diletakkan pada masing-masing perlakuan. Setiap perlakuan pada masing-masing metode percobaan diulang 10 kali dan disusun secara acak sebagai berikut:
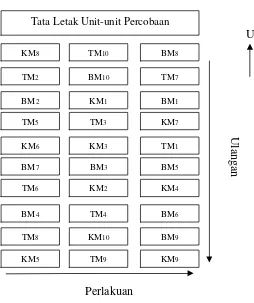
Gambar 6. Tata letak percobaan pada metode residu pada hidup Symphylid di laboratorium.
Keterangan:
KM : Tanpa aplikasiB. bassiana.
BM : AplikasiB. bassianadengan metode residu pada tanah berbahan organik sebagai media hidup symphylid.
TM : AplikasiB. bassianadengan metode residu pada tanah tanpa bahan organik sebagai media hidup symphylid.
U Tata Letak Unit-unit Percobaan
24
3.5 Pengamatan
Patogenitas ditentukan dengan mengamati mortalitas (kematian) symphylid. Indikasi kematian serangga uji dilakukan dengan cara mengamati symphylid di bawah mikroskop untuk mengetahui apakah pada tubuh symphylid tumbuh jamur B. bassiana. Untuk mendeteksi penyebab kematian symphylid akan diinkubasi
diatas media PDA. Pengamatan mortalitas dilakukan setiap hari. Data hasil pengamatan akan disajikan kedalam tabel seperti dibawah ini:
Tabel 1. Data hasil pengamatan mortalitas symphylid pada metode residu pakan
Perlakuan ∑ Mortalitas symphylid (ekor) pada pengamatan hari
ke-1 2 3 4 5 6 7 8 ... 20
KP BP TP
Tabel 2. Data hasil pengamatan mortalitas symphylid pada metode residu pada hidup symphylid
Perlakuan ∑ Mortalitas symphylid (ekor) pada pengamatanhari
ke-1 2 3 4 5 6 7 8 ... 20
KM BM TM
Menurut Rustamaet al.(2008), persentase mortalitas (kematian) serangga dapat dihitung menggunakan rumus seperti berikut:
= 100%
25
N = jumlah serangga yang diuji (ekor).
3.6 Analisis Data
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Aplikasi jamurB. bassianaterhadap symphylid hanya menyebabkan kematian tidak lebih dari 10 % dan mortalitas symphylid tidak berbeda nyata antar perlakuan. Berdasarkan percobaan yang telah dilakukan dapat disimpulkan bahwaB. bassianabelum terbukti mampu menginfeksi dan menyebabkan mortalitas symphylid.
5.2 Saran
PUSTAKA ACUAN
Barnett. H. L. 1960.Ilustrated Genera of Imperfecty Fungy. Published by Burgess Pub. Co, Minneapolis. Mishawaka, IN, U.S.A Second Edition P: 62. Bartholomew, D. P., R. E Paull and K. G. Rohrbach. 2003. The Pineapple: Botany,
production and Uses. Bartholomew, D. P., R. E Paull and K. G. Rohrbach (eds.). CABI Publishing, Wallingford, UK. Pp 1-301.
Biro Pusat Statistik (BPS). 2012. Produksi Nanas. http://bps.go.id. Diakses pada tanggal 20 Mei 2014.
Burger, H. D and N. W. Hussey. 1971. Microbial Control of Insects and Mites. Academic Press. New York.
Cloyd. 2003. Nursery, Greenhouse and Landscape: Naturalis-O, A new
Mycoinsecticida. htpp://www.Entomology.wisc.edu/mben /land210 html). Diakses 21 Januari 2003.
Dinata, A. 2006. Insektisida Yang Ramah Lingkungan. Diakses dari:
http://www.pikiranrakyat.com.cetak/044/15/cakrawala.penelitian. Tanggal 23 Agustus 2015.
Flint, M. L. 1990.Pests of the Garden and Small Farm. Pest Notes Publication 3332. Division of Agriculture and Natural Resources, University of California. Ghidiu, G. M. 2005.Garden Symphylans. Fact Sheet 234 NJ Agricultural Experiment
Station (NJAES), Rutger. The State University of New Jersey. USA. Gillespie, A. T. 1988. Use of fungi to control pests of agricultural importance, p.
37-60. In M. N. Burge (ed.), Fungi in biological control systems. Manchester University Press, Manchester, England.
32 Hughes, S. J. 1971. Phycomycetes, Basidiomycetes, and Ascomycetes as Fungi
Imperfecti. In: Taxonomy of Fungi Imperfecti (B. Kendrick, ed.), pp. 7-36. University of Toronto Press, Toronto.
Junianto dan Sulistyowati, 2002. Formulasi Agens HayatiBeauveria bassianadan Uji Lapangan Pengendalian Penggerek Buah Kopi (Hypothenemus hampei). Pusat Penelitian Kopi dan Kakao Indonesia, Jember. J. Pelita Perkebunan 18 (3) : 129-138.
Karama, A.S., A.R. Marzuki, dan I. Marwan. 1990. Penggunaan pupuk organik pada tanaman pangan. Prosiding Lokakarya Nasional Efisiensi Penggunaan Pupuk. Puslit Tanah dan Agroklimat. Bogor. 395-425 hlm.
Khairani, N. 2007. Uji efektifitasB. bassiana(Balsamao) dan DaunLantara camara L. Terhadap Hama Penggerek Umbi Kentang (Phthorimaea operculella Zell.) di Gudang. (Skripsi). Fakultas Pertanian. Universitas Sumatera Utara. Medan. 72 hlm.
Khasanah, N. 2008. Pengendalian Hama Penggerek Tongkol JagungHelicoverpa armigeraHubner. (Lepidotera: Noctuidae) denganBeauveria bassiana Strain Lokal Pada Pertanaman Jagung Manis di Kabupaten Donggala. Jurnal Agroland, 15 (2): 106-111.
Kučera, M. and A. Samšiňáková. 1968. Toxins of the entomophagous fungus
Beauveria bassiana.J. Invertebrate Pathology12: 316-320.
Ladja, F.T. 2010. Pengaruh Aplikasi CendawanBeauveria bassianadanVerticilum leucaniiTerhadap MortalitasNephotettix virescensSebagai Vector Virus Tungro.Prosiding Seminar Ilmiah dan Pertemuan Tahunan Pej dan Pfj Xx Komisariat Daerah Sulawesi Selatan. Sulawesi Selatan. 27 Mei 2010. P: 62-68.
Lisdiana dan W. Soemadi. 1997. Budidaya Nanas, Pengolahan dan Pemasaran. Aneka. Solo. 78p.
Mahr, S. 2003. The EntomopathogenBeauveria bassiana.University of Winconsin, Madison. http://www.entomology.wisc.edu/mbcn/kyf410.html. Diakses tanggal 18 Maret 2015.
33 Mandarina, D. 2008. Uji Efektifitas Beberapa Entomopatogen Pada Larva dan Imago
Brontispa longissimaGestro. (Coleoptera: Chrysomelidae) di Laboratorium. (Skripsi). Fakultas Pertanian. Universitas Sumatera Utara. Medan. 63 hlm. Marleni, N. 2013. Efikasi JamurBeauveria bassianaPada Penggerek Buah Kopi Dari
Sumber Jaya. (Skripsi). Fakultas Pertanian. Universitas Lampung. Bandar Lampung. 46 hlm.
Nelson, T. L and T. R. Glare. 1996. Large scale production of new zealand strains of Beauveria and Metarhizium. Proceedings 49th N. Z. Plant Protection Conf., p.
257-261.
Nunilahwati, H., S. Herlinda., C. Irsan., dan Y. Pujiastuti. 2012. Eksplorasi, Isolasi dan Seleksi Jamur Entomopatogen Plutella Xylostella(Lepidoptera:
Yponomeutidae) Pada Pertanaman Caisin (Brassica Chinensis) Di Sumatera Selatan. Universitas Sriwijaya. Palembang. J. HPT Tropika 12(1): 1-11. Oviana, T. 2013. Hubungan Kondisi Visual Tanaman terhadap Populasi Symphylid
dan GejalaWitches Broompada Akar Tanaman Nanas [Ananas comosus(L) Merr]. Laporan Praktik Umum. Universitas Lampung. Bandar Lampung. Plate, J. 1976. Fungi. Biological Control: A guide to natural enemies in North
America. Cornel University. 4pp.
Prayogo, Y. 2006. Upaya Mempertahankan Keefektifan Cendawan Entomopatogen Untuk Mengendalikan Hama Tanaman Pangan. Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian. Malang.J: Litbang Pertanian25 (2): 47-54.
Rahayuningtias, S dan K. S. M. Julyasih. 2010. Pengaruh Tingkat Kerapatan Spora JamurBeauveria bassiana(Bals) Vuill Terhadap Mortalitas Imago Wereng Coklat (Nilaparvata lugensStal) di Laboratorium.Prosiding Seminar Nasional HPTI. Surabaya, 14 April 2010. P: 87-90.
Robert, D. W. 1981. Toxins of Entomopathogenic Fungi.InH. D. Burger (ed.). Microbial Control of Pest and Plant Disease. 1970-1980. Firsted. London: Academic Press.
34 Scheller, U. 1961. Studies on The Symphylid Fauna of The Hawaiian Island.
Proccedings.Hawaiian Entomological Society17(3): 443-456.
Scheller U and J. Adis. 2002. Symphyla.InAdis J (Ed.): Amazonian Arachnida and Myrapoda. Pensoft Publishers, Sofia. Pp. 547-554.
Storey, K. G. and A. W. Gardner. 1968. Movement of an Aqueous Spray of
Beauveria bassianainto The Profile Four Georgia Soils.Environ Entomol 17: 135-139.
Strasser, H., A. Vey., and T. Butt. 2000. Are there any risks in using
entomopathogenic fungi for pest control, with particular reference to the bioactive metabolites of Metarhizium, Tolypocladium, and Beauveria species? Biocontrol Science and Technology 10:717-735.
Quesada-Moraga, E. and A. Vey. 2004. Bassiacridin, a protein toxic for locusts secreated by the enthomopathogenic fungusBeauveria bassiana. Mycological Research 108: 441-452.
Umble, J., R. Dufour., G. Fisher., J. Fisher., J., Leap., and M. V. Horn. 2006.
Symphylans: Soil Pest Management Options. ATTRA. National Center for Appropriate Technology (NCAT). US.
Umble, J. R. and J. R. Fisher. 2003. Influence of below-ground feeding by garden symphylans (Cephalostigmata: Scutigerellidae) on plant health.
Environmental Entomology32 (5): 1251-1261.
Utomo,C dan D. J. Pardede, 1990.Efikasi JamurBeauveria bassianaTerhadap Penggerek Batang KakaoZeuzera coffeaeNietn.
http://forester-untad.blogspot.co.id/2012/08/laporan-akhir-program-kreativitas.html. Bul Perkebunan. 21(4): 243-251.
Varela, A. and E. Morales. 1996. Characterization of someBeauveria bassiana isolates and their virulence toward the coffee berry borerHypothenemus hampei. J. Invertebr. Pathol. (67): 147−152.
Vey, A., R. E. Hoagland., and T. M. Butt. 2001. Toxic metabolites of fungal biocontrol agents. Fungi as Biocontrol Agents. Progress, Problem and Potensial (Butt T.M, C. Jackson, and N. Magan,eds), pp. 311-346. CABI Publishing, Oxford, UK.