Lampiran 2. Gambar Pohon dan Daun (Moringa oleifera Lam.)
Lampiran 2. (Lanjutan)
Gambar 2. Daun kelor
Lampiran 2. (Lanjutan)
Gambar 4. Makroskopik Daun Kelor Kering
Gambar 5 . A. Daun Kelor Kering yang Telah Menjadi Serbuk
B. Daun Kelor yang Telah Direbus
Lampiran 3. Bagan Alir Proses Destruksi Kering (Daun Kelor Kering)
Dibersihkan dari pengotor
Dicuci dengan akua demineralisata Ditiriskan
Dikeringkan di udara terbuka terhindar dari sinar matahari langsung selama 7 hari
Dihaluskan dengan blender Dihomogenkan
Ditimbang 10 gram di dalam krus porselen Ditambahkan 5 ml Asam Nitrat (1:1) Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit
Dilakukan selama 55 jam dan dibiarkan hingga dingin di dalam desikator
500g Daun Kelor
Sampel yang telah dihaluskan
Sampel yang telah mengarang
Lampiran 4. Bagan Alir Proses Destruksi Kering (Daun Kelor Rebus)
Dibersihkan dari pengotor
Dicuci dengan akua demineralisata Ditiriskan
Direbus selama 10 menit dalam 700 ml akua demineralisata yang telah mendidih
Ditiriskan
Dihaluskan dengan blender Dihomogenkan
Ditimbang 10 gram di dalam krus porselen Ditambahkan 5 ml Asam Nitrat (1:1) Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit
Dilakukan selama 48 jam dan dibiarkan hingga dingin di dalam desikator
500g Daun Kelor
Sampel yang telah dihaluskan
Sampel yang telah mengarang
Lampiran 5. Bagan Alir Pembuatan Larutan Sampel
1. Bagan Alir Pembuatan Larutan Sampel Daun Kelor Kering
Dilarutkan dalam 5 ml Asam Nitrat (1:1) Dimasukkan ke dalam labu tentukur 50 ml Dibilas krus porselen akua demineralisata
Dicukupkan dengan akua demineralisata hingga garis tanda
Disaring dengan kertas saring Whatman No.42 Dibuang 5 ml filtrat untuk menjenuhkan kertas saring
Dimasukkan ke dalam botol
Dilakukan analisis kualitatif
Dilakukan pengenceran dengan memipet 1 ml larutan sampel ke dalam labu tentukur 50 ml lalu dicukupkan hingga garis tanda
Dilakukan analisis kuantitatif dengan spektrofotometer serapan atom pada λ 279,5 nm (lampu katoda mangan) untuk mangan, dan λ 213,9 nm (lampu katoda zink) untuk zink
Sampel yang telah dekstruksi
Filtrat
Larutan sampel
Lampiran 5. (Lanjutan)
2. Bagan Alir Pembuatan Larutan Sampel Daun Kelor Kering
Dilarutkan dalam 5 ml Asam Nitrat (1:1) Dimasukkan ke dalam labu tentukur 50 ml Dibilas krus porselen akua demineralisata
Dicukupkan dengan akua demineralisata hingga garis tanda
Disaring dengan kertas saring Whatman No.42 Dibuang 5 ml filtrat untuk menjenuhkan kertas saring
Dimasukkan ke dalam botol
Dilakukan analisis kualitatif
Dilakukan pengenceran dengan memipet 5 ml larutan sampel ke dalam labu tentukur 50 ml lalu dicukupkan hingga garis tanda
Dilakukan analisis kuantitatif dengan spektrofotometer serapan atom pada λ 279,5 nm (lampu katoda mangan) untuk mangan
Dilakukan analisis kuantitatif laruitan sampel tanpa dilakukan pengenceran dengan spektrofotometer erapan atom pada λ 213,9 nm (lampu katoda zink) untuk zink Sampel yang telah
dekstruksi
Filtrat
Larutan sampel
Lampiran 6. Gambar Hasil Analisis Kualitatif Mangan dan Zink
Gambar 4. A. Hasil Analisis Kualitatif Daun Rebus dan Kering Kelor Mangan B. Hasil Analisis Kualitatif Daun Rebus dan Kering Kelor Zink
Gambar 5. Kristal Pakis Zink Perbesaran 1x40
Daun Kering Daun Kering
Daun Rebus Daun Rebus
Lampiran 7. Data Kalibrasi Mangan dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 0,0058
2. 0,2000 0,1299
3. 0,4000 0,2400
4. 0,8000 0,4555
5. 1,2000 0,6813
6. 1,6000 0,8989
No X Y XY X² Y²
1 0,0000 0,0058 0,0000 0,0000 0,00003364
2 0,2000 0,1299 0,0260 0,0400 0,01687401
3 0,4000 0,2400 0,0960 0,1600 0,0576000
4 0,8000 0,4555 0,3644 0,6400 0,20748025
5 1,2000 0,6813 0,8175 1,4400 0,46416969
6 1,6000 0,8989 1,4382 2,5600 0,80802121
∑X = 4,200 ∑Y = 2,4114
∑XY=
2,7422 ∑ X²= 4,8400
∑ Y² = 1,5541788
X= 0,7000 Y= 0,4019
� = ∑�� −((∑ �� ∑ �)/ �)
∑ �²−( (∑ �)² / � )
� = 2,7422−((4,200� 2,4114)/ 6) 4,8400−((4,200)2/ 6)
� = 0,5548
Y = ��̅+ �
b = Y– ��̅
= 0,4019 – (0,5548 x 0,7000) = 0,01354
Lampiran 7. (Lanjutan)
r = ∑XY − [
(∑X )(∑Y ) n ]
��∑X2 – (∑X)² / n � (∑Y2− (∑Y)² / n )
r = 2,7422 – �
(4,200 )(2,4114 )
6 �
��4,8400 −(4,200 )2
6 ��1,5541788 − (2,4114 )2
6 �
r =1,0542 1,05431
Lampiran8. Data Kalibrasi Zink dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 0,0011
2. 0,2000 0,0461
3. 0,4000 0,0922
4. 0,6000 0,1379
5. 0,8000 0,1841
6. 1,0000 0,2285
No X Y XY X² Y²
1 0,0000 0,0011 0,0000 0,0000 0,00000121
2 0,2000 0,0461 0,00915085 0,03940225 0,00212521 3 0,4000 0,0922 0,0369261 0,16040025 0,00850084 4 0,6000 0,1379 0,08282274 0,36072036 0,01901641 5 0,8000 0,1841 0,14781389 0,64464841 0,03389281 6 1,0000 0,2285 0,2279059 0,99480676 0,05221225
∑X = 3,0000
∑Y = 0,6899
∑XY= 0,50462409
∑ X²= 2,20001774
∑ Y² = 0,11574873
X= 0,5000 Y= 0,1150
� = ∑�� −((∑ �� ∑ �)/ �)
∑ �²−( (∑ �)² / � )
� = 0,50462409 −((3,0000� 0,6899)/ 6) 2,20001774−((3,0000)2/ 6)
� = 0,22835
Y = ��̅+ �
b = Y – ��̅
= 0,1150– (0,22835x0,5000) = 0,00075
Lampiran 8. (Lanjutan)
r = ∑XY − [
(∑X )(∑Y ) n ]
��∑X2– (∑X)² / n � (∑Y2− (∑Y)² / n )
r = 0,5046240 –�
(3,0000 )(0,6899 )
6 �
��2,20001774 −(3,0000 )�
6 ��0,11574873− (0,6899 )�
6 �
r = 0,1597 0,11597
Lampiran 9. Hasil Analisis Kadar Mangan dan Zink dalam Daun Kelor Kering 1. Hasil Analisis Kadar Mangan
2. Hasil Analisis Kadar Zink Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0123 0,3225 0,5770 13,9079
2 10,0526 0,3265 0,5641 14,0287
3 10,0322 0,3245 0,5606 13,9700
4 10,0438 0,3250 0,5615 13,9762
5 10,0247 0,3239 0,5594 13,9505
6 10,0261 0,3240 0,5597 13,9561
SD 0,03939
Kadar 13,9649 ±
0,0648
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0123 0,1099 0,4780 11,9353
2 10,0526 0,1399 0,4955 12,3226
3 10,0322 0,1130 0,4916 12,2505
4 10,0438 0,1131 0,4920 12,2463
5 10,0247 0,1124 0,4889 12,1923
6 10,0261 0,1127 0,4903 12,2255
SD 0,004791
Kadar 12,24744 ±
Lampiran 10. Hasil Analisis Kadar Mangan dan Zink dalam Daun Kelor Rebus 1. Hasil Analisis Kadar Mangan
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0348 0,2313 0,3923 0,97735
2 10,0458 0,2326 0,3948 0,98250
3 10,0376 0,2321 0,3939 0,98106
4 10,0322 0,2309 0,3918 0,97636
5 10,0303 0,2292 0,3887 0,9688
6 10,0298 0,2289 0,3882 0,9676
SD 0,0063
Kadar 0,9768 ±
0,0104
2. Hasil Analisis Kadar Zink
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0348 0,0528 0,2279 0,11355
2 10,0458 0,0538 0,2323 0,11562
3 10,0376 0,0528 0,2279 0,11352
4 10,0322 0,0524 0,2262 0,11274
5 10,0303 0,0521 0,2249 0,11211
6 10,0298 0,0517 0,2231 0,11122
SD 0,00099213
Kadar 0,112626 ±
Lampiran 11. Contoh Perhitungan Kadar Mangan dan Zink dalam Daun Kelor Kering
1. Contoh Perhitungan Kadar Mangan
Berat sampel yang ditimbang = 10,0123 gr Absorbansi (Y) = 0,3225
Persamaan garis regresi: Y = 0,5548 X + 0,01345 X = 0,3225− 0,01345
0,5548 = 0,5570 µg/ml Konsentrasi mangan = 0,5570 µg/ml
Kadar (µg/100g) =Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran Berat Sampel (gr )
= 0,5570µg/ml x 50 ml x 50 10,0123 gr
= 139,079 µg/gr = 13,9079 mg/100 gr
2. Contoh Perhitungan Kadar Zink
Berat sampel yang ditimbang = 10,0123 gr Absorbansi (Y) = 0,1099
Persamaan garis regresi: Y = 0,22835 X + 0,00075 X = 0,1099−0,00075
0,22835 = 0,4780 µg/ml Konsentrasi zink = 0,4780 µg/ml
Kadar (µg/100g) = Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran Berat Sampel (gr )
= 0,4780 µg/ml x 50 ml x 50 10,0123 gr
Lampiran 12. Contoh Perhitungan Kadar Mangan dan Zink dalam Daun Kelor Rebus
1. Contoh Perhitungan Kadar Mangan
Berat sampel yang ditimbang = 10,0348 gr Absorbansi (Y) = 0,2313
Persamaan garis regresi: Y = 0,5548 X + 0,01345 X = 0,2313− 0,01345
0,5548 = 0,3923 µg/ml Konsentrasi mangan = 0,3923 µg/ml
Kadar (µg/100g) =Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran Berat Sampel (gr )
= 0,3923µg/ml x 50 ml x 5 10,0348 gr
= 9,7735 µg/gr = 0,97735 mg/100 gr
2. Contoh Perhitungan Kadar Zink
Berat sampel yang ditimbang = 10,0348 gr Absorbansi (Y) = 0,0528
Persamaan garis regresi: Y = 0,22835 X + 0,00075 X = 0,0528−0,00075
0,22835 = 0,2279 µg/ml Konsentrasi zink = 0,2279 µg/ml
Kadar (µg/100g) = Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran Berat Sampel (gr )
= 0,2279 µg/ml x 50 ml x 1 10,0348 gr
Lampiran 13. Perhitungan Statistik Kadar Mangan dalam Sampel 1. Perhitungan Statistik Kadar Mangan dalam Daun Kelor Kering
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
1 13,9079 0,057 0,003249
2 14,0287 0,0638 0,00407044
3 13,9700 0,0051 0,00002601
4 13,9762 0,0113 0,00012769
5 13,9505 0,0144 0,00020736
6 13,9561 0,0088 0,00007744
∑ Xi= 83,7894 ∑ (Xi-X)² =
0,00775794
X= 13,9649
SD = �∑(Xi−X)²
�−1
= �0,00775794 mg /100 g 6−1
= 0,03939 mg/100 g
Pada interval kepercayaan 99% dengan nilai α = 0,01 dk = 5 maka diperoleh nilai t tabel: α/ 2 = 0,005, dk = 5 adalah 4,0321.
Data diterima jika t hitung < t tabel
t hitung = | ��−� |
�� / √�
t hitung 1 = |0,057|
0,03939 / √6 = 3,5446 t hitung 2 = |0,0638|
t hitung 3= |0,0051|
0,03939 / √6 = 0,3171 t hitung 4 = |0,0113|
0,03939 / √6 = 0,7027 t hitung 5 = |0,0144 |
0,03939/ √6 = 0,8955 t hitung 6 = |0,0088 |
0,03939/ √6 = 0,5472
Kadar mangan dalam daun kelor kering : µ = X ± (t (α / 2, dk) x SD / √�)
= 13,9649 mg/100g ± (4,0321x 0,03939 mg/100g / √6 )
= (13,9649 ± 0,0648) mg/100 g
Lampiran 13. Perhitungan Statistik Kadar Mangan dalam Sampel 2. Perhitungan Statistik Kadar Mangan dalam Daun Kelor Rebus
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
1 0,97735 0,000055 0,0000003025
2 0,98250 0,0057 0,00003249
3 0,98106 0,00426 0,0000181476
4 0,97636 0,00006 0,0000000036
5 0,9688 0,008 0,000064
6 0,9676 0,0092 0,00008464
∑ Xi= 5,8607 ∑ (Xi-X)² =
0,0001995837 X= 0,9768
SD = �∑(Xi−X)²
�−1
= �0,0001995837 mg /100 g 6−1
= 0,0063 mg/100 g
Pada interval kepercayaan 99% dengan nilai α = 0,01 dk = 5 maka diperoleh nilai t tabel: α/ 2 = 0,005, dk = 5 adalah 4,0321.
Data diterima jika t hitung < t tabel
t hitung = | ��−� |
�� / √�
t hitung 1 = |0,000055 |
0,0063 / √6 = 0,2138 t hitung 2 = |0,0057 |
0,0063 / √6 = 2,2162
t hitung 3 = |0,00426 |
0,0063 / √6 = 1,6563 t hitung 4 = |0,00006 |
0,0063 / √6 = 0,0233 t hitung 5 = |0,008|
0,0063 / √6 = 3,1104 t hitung 6 = |0,0092|
0,0063 / √6 = 3,5770
Kadar mangan dalam daun kelor rebus : µ = X ± (t (α / 2, dk) x SD / √�)
= 0,9768 mg/100g ± (4,0321 x 0,0063 mg/100g / √6)
= (0,9753 ± 0,0104) mg/100g
Lampiran 14. Perhitungan Statistik Kadar Zink dalam Sampel 2. Perhitungan Statistik Kadar Zink dalam Daun Kelor Kering
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
1 11,9353 0,2601 0,0676520
2 12,3226 0,1272 0,01617984
3 12,2505 0,0551 0,00303601
4 12,2463 0,0509 0,00259081
5 12,1923 0,0031 0,000961
6 12,2255 0,0301 0,0090601
∑ Xi= 73,1725 ∑ (Xi-X)² =
0,09037428
X= 12,1954
SD = �∑(Xi−X)²
�−1
= �0,0009037428 mg /100 g 6−1
= 0,1344 mg/100g
Pada interval kepercayaan 99% dengan nilai α = 0,01 dk = 5 maka diperoleh nilai t tabel: α/ 2 = 0,005, dk = 5, adalah 4,0321.
Data diterima jika t hitung < t tabel
t hitung = | ��−� |
�� / √�
t hitung 1 = |0,2601 |
0,01344 / √6 = 4,7404 t hitung 2 = |0,1272 |
0,01344 / √6 = 2,3182 t hitung 3 = |0,0551 |
Lampiran 14. (Lanjutan)
t hitung 4 = |0,0509|
0,01344 / √6 = 0,9276 t hitung 5 = |�,����|
�,����� / √� = 0,0564
t hitung 6 = |�,����|
�,����� / √� = 0,5485
Karena data 1 ditolak, maka dilakukan uji t ulang tanpa mengikutkan data 1
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
2 12,3226 0,07516 0,0056490256
3 12,2505 0,00306 0,0000093636
4 12,2463 0,00114 0,0000012996
5 12,1923 0,05514 0,0030404196
6 12,2255 0,02194 0,0004813636
∑ Xi= 61,2372 ∑ (Xi-X)² =
0,009181472
X= 12,24744
SD =�∑(Xi−X)²
�−1
=
�
�,�����������/�����−�
= 0,04791 mg/100g
Lampiran 14. (Lanjutan)
Data diterima jika t hitung < t tabel
t hitung = | Xi−X | SD / √n
t hitung 2 = |�,�����|
�,����� / √� = 3,5444
t hitung 3 = |0,00306 |
�,�����/ √� = 0,1443 t hitung 4 = |0,00114 |
�,����� / √5 = 0,0537
t hitung 5 = |�,�����|
�,����� / √� = 2,6003
t hitung 6 = |0,02194 |
�,�����/ √5 = 1,0346
Kadar zink dalam daun kelor kering: µ = X ± (t (α / 2, dk) x SD / √�)
= 12,24744 mg/100g ± (4,6041 x 0,04791 mg/100g / √5 )
= (12,24744 ± 0,0986) mg/100g
Lampiran 14. Perhitungan Statistik Kadar Zink dalam Sampel 2. Perhitungan Statistik Kadar Zink dalam Daun Kelor Rebus
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
1 0,11355 0,000425 0,000000180625
2 0,11562 0,002495 0,000006225025
3 0,11352 0,000395 0,000000156025
4 0,11274 0,000385 0,000000148225
5 0,11211 0,001015 0,000001030225
6 0,11121 0,001915 0,000003667225
∑ Xi= 0,67875 ∑ (Xi-X)² =
0,00001140735 X= 0,113125
SD =
�
∑(Xi−X)² �−1=
�
0,00001140735 mg /100 g6−1
= 0,00151045 mg/100g
Pada interval kepercayaan 99% dengan nilai α = 0,01 dk = 5 maka diperoleh nilai t tabel: α/ 2 = 0,005, dk = 5 adalah 4,0321.
Data diterima jika t hitung < t tabel
t hitung = | Xi−X |
SD / √n
t hitung 1 = |0,000425 |
0,00151045 / √6 = 0,6892
t hitung 2 = |0,002495 |
0,00151045 / √6 = 4,0461
t hitung 3 = |0,000395 |
Lampiran 14. (Lanjutan)
t hitung 4 = |0,000385 |
0,00151045 / √6 = 0,6243
t hitung 5 = |0,001015 |
0,00151045 / √6 = 1,6460
t hitung 6 = |0,001915 |
0,00151045 / √6 = 3,1055
Karena data 2 ditolak, maka dilakukan uji t ulang tanpa mengikutkan data 2
No Xi
Kadar (mg/100g)
(Xi-X) (mg/100g)
(Xi-X)² (mg/100g)
1 0,11355 0,000924 0,000000853776
3 0,11352 0,000894 0,000000799236
4 0,11274 0,000114 0,000000012996
5 0,11211 0,000516 0,000000266256
6 0,11121 0,001416 0,000002005056
∑ Xi= 0,56313 ∑ (Xi-X)² =
0,00000393732 X= 0,112626
SD =
�
∑(Xi−X)² �−1=
�
0,00000393732 mg /100 g5−1
= 0,00099213 mg/100g
Lampiran 14. (Lanjutan)
Data diterima jika t hitung < t tabel
t hitung = | ��−� | �� / √�
t hitung 1 = |0,000924 |
0,00099213 /√5 = 2,0825
t hitung 3 = |0,000894 |
0,00099213 /√5 = 2,0149
t hitung 4 = |0,000114 |
0,00099213 /√5 = 0,2569
t hitung 5 = |0,000516 |
0,00099213 /√5 = 1,1629
t hitung 6 = |0,001416 |
0,00099213 /√5 = 3,1914
Kadar zink dalam daun kelor rebus: µ = X ± (t (α / 2, dk) x SD / √�)
= 0,112626 mg/100g ± (4,6041 x 0,00099213 mg/100g / √5 )
= (0,112626 ± 0,00204) mg/100g
Lampiran 15. Hasil Analisis Kadar Mangan dan Zink Sebelum Penambahan Masing-Masing Larutan Baku pada Daun Kelor Kering
1. Hasil Analisis Kadar Mangan Sebelum Ditambahkan Larutan Standar Mangan
2. Hasil Analisis Kadar Zink Sebelum Ditambahkan Larutan Standar Zink Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0123 0,3225 0,5570 13,9079
2 10,0526 0,3265 0,5641 14,0287
3 10,0322 0,3245 0,5606 13,9700
4 10,0438 0,3250 0,5615 13,9762
5 10,0247 0,3239 0,5594 13,9505
6 10,0261 0,3240 0,5597 13,9561
∑ 60,1917 83,7894
Rata-rata 10,03195 13,9649
Sampel BeratSampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g)
1 10,0123 0,1099 0,4780 11,9353
2 10,0526 0,1399 0,4955 12,3226
3 10,0322 0,1130 0,4916 12,2505
4 10,0438 0,1131 0,4920 12,2463
5 10,0247 0,1124 0,4889 12,1923
6 10,0261 0,1127 0,4903 12,2255
∑ 60,1917 73,1725
Lampiran 16. Hasil Analisis Kadar Mangan dan Zink Sesudah Penambahan Masing-Masing Larutan Baku pada Daun Kelor Kering
1. Hasil Uji Recovery Mangan Setelah Ditambahkan 14 ml Larutan Standar Mangan (Konsentrasi 10 µg/ml)
2. Hasil Uji Recovery Zink Setelah Ditambahkan 12 ml Larutan Standar Zink (Konsentrasi 10 µg/ml)
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Recovery (%)
1 10,0123 0,3520 0,6102 15,2362 91,64
2 10,0526 0,3560 0,6174 15,3542 100,14
3 10,0322 0,3517 0,6096 15,1911 88,39
4 10,0438 0,3533 0,6125 15,2457 92,97
5 10,0247 0,3516 0,6094 15,1975 88,85
6 10,0261 0,3513 0,6089 15,1829 87,80
∑ 60,1917 549,79
Rata-rata 10,03195 91,63
Sampel BeratSampel (g) Absorbansi (A) Konsentrasi (µg/ml) Kadar (mg/100g) Recovery (%)
1 10,0123 0,1215 0,5288 13,2037 80,42
2 10,0526 0,1252 0,5449 13,5512 109,65
3 10,0322 0,1235 0,5375 13,3943 96,45
4 10,0438 0,1241 0,5401 13,4436 100,60
5 10,0247 0,1220 0,5309 13,2397 83,45
6 10,0261 0,1233 0,5367 13,3828 96,46
∑ 60,1917 567,03
Lampiran 17. Perhitungan Uji Perolehan Kembali Kadar Mangan dan Zink dalam Daun Kelor Kering
1. Perhitungan uji perolehan kembali kadar mangan Sampel 1
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3520 − 0,01345
0,5548 = 0,6102 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,6102 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,6102 µg/ml
10,0123 g x 50 ml x 50
= 152,362 µg/g
= 15,2362 mg/100g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 15,9853 mg/100g
Kadar rata-rata sebelum ditambahkan lautan baku (CA) = 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
= (15,2362 − 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 2
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3560 − 0,01345
0,5548 = 0,6174 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,6174 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,6174 µg/ml
10,0526 g x 50 ml x 50
= 153,542 µg/g
= 15,3542 mg/100g
Kadar sampel 2 setelah ditambah larutan baku (CF) = 15,3542 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA) = 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
=
10 µg/ml10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
=(15,3542− 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 3
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3517 − 0,01345
0,5548 = 0,6096 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,6096 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,6096 µg/ml
10,0322 g x 50 ml x 50
= 151,911 µg/g
= 15,1911 mg/100g
Kadar sampel 3 setelah ditambah larutan baku (CF) = 15,1911 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA)= 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
= (15,1911− 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 4
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3533 − 0,01345
0,5548 = 0,6125 µg/ml Konsentrasi setelah ditambahkan larutan baku = 0,6125 µg/ml Kadar sampel setelah ditambah larutan baru (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,60125 µg/ml
10,0438 g x 50 ml x 50
= 152,457 µg/g
= 15,2457 mg/100g
Kadar sampel 4 setelah ditambah larutan baku (CF) = 15,2457 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA) = 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
= (15,2547− 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 5
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3516 − 0,01345
0,5548 = 0,6094 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,6094 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,6094 µg/ml
10,0247 g x 50 ml x 50
= 151,975 µg/g
= 15,1975 mg/100g
Kadar sampel 5 setelah ditambah larutan baku (CF) = 15,1975 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA)= 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
= (15,1975− 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 6
Persamaan regresi : Y = 05548 X + 0,01345
X = 0,3513 − 0,01345
0,5548 = 0,6089 µg/ml Konsentrasi setelah ditambahkan larutan baku = 0,6089 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,6089 µg/ml
10,0261 g x 50 ml x 50
= 151,829µg/g
= 15,1829 mg/100g
Kadar sampel 6 setelah ditambah larutan baku (CF) = 15,1829 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA) = 13,9649 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 14 ml
= 13,8724 µg/g
= 1,38724 mg/100g
% Perolehan kembali mangan = CF−CA
�∗� x 100%
= (15,1829− 13,9649) mg /100 g
1,38724 mg /100 g x 100%
Lampiran 17. Perhitungan Uji Perolehan Kembali Mangan dan Zink dalam Daun Kelor Kering
2. Perhitungan Uji Perolehan Kembali Zink Sampel 1
Persamaan regresi : Y = 0,22835 X + 0,00075
X = 0,1215 − 0,00075
0,22835 = 0,5288 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5288 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5288 µg/ml
10,0123 g x 50 ml x 50
= 132,037µg/g
= 13,2037 mg/100g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 13,2037 mg/100g
Kadar rata-rata sampel sebelum ditambah lautan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907 µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
= (13,2037− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 2
Persamaan regresi : Y = 0,22835 X + 0,00075
X = 0,1252 − 0,00075
0,22835 = 0,5449 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5449 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5449 µg/ml
10,0526 g x 50 ml x 50
= 135,5120µg/g
= 13,5512 mg/100g
Kadar sampel 2 setelah ditambah larutan baku (CF) = 13,5512 mg/100g
Kadar rata-rata sebelum ditambah larutan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907 µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
=(13,5512− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 3
Persamaan regresi : Y = 0,22835 X + 0,00075 X = 0,1235 − 0,00075
0,22835 = 0,5375 µg/ml Konsentrasi setelah ditambahkan larutan baku = 0,5375 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5375 µg/ml
10,0322 g x 50 ml x 50
= 133,943 µg/g
= 13,3943 mg/100g
Kadar sampel 3 setelah ditambah larutan baku (CF) = 13,3943 mg/100g
Kadar rata-rata sebelum ditambahkan larutan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery= 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
= (13,3943− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 4
Persamaan regresi : Y = 0,22835 X + 0,00075
X = 0,1241 − 0,00075
0,22835 = 0,5401 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5401 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5401 µg/ml
10,0438 g x 50 ml x 50
= 134,436µg/g
= 13,4436 mg/100g
Kadar sampel 4 setelah ditambah larutan baku (CF) = 13,4436 mg/100g
Kadar rata-rata sebelum ditambahkan lautan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
= (13,4436− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 5
Persamaan regresi : Y = 0,22835 X + 0,00075 X = 0,1220 − 0,00075
0,22835 = 0,5309 µg/ml Konsentrasi setelah ditambahkan larutan baku = 0,5309 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5309 µg/ml
10,0247 g x 50 ml x 50
= 132,397 µg/g
= 13,2397 mg/100g
Kadar sampel 5 setelah ditambah larutan baku (CF) = 13,2397 mg/100g
Kadar rata-rata sebelum ditambahkan lautan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
= (13,2397− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 17. (Lanjutan) Sampel 6
Persamaan regresi : Y = 0,22835 X + 0,00075 X = 0,1233 − 0,00075
0,22835 = 0,5367 µg/ml Konsentrasi setelah ditambahkan larutan baku = 0,5375 µg/ml Kadar sampel setelah ditambah larutan baku (CF)
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5367 µg/ml
10,0322 g x 50 ml x 50
= 133,825 µg/g
= 13,3825 mg/100g
Kadar sampel 6 setelah ditambah larutan baku (CF) = 13,3825 mg/100g
Kadar rata-rata sebelum ditambahkan lautan baku (CA) = 12,2474 mg/100g
Berat sampel rata-rata uji recovery = 10,03195 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat sampel rata−rata x Volume (ml)
= 10 µg/ml
10,03195 g x 12 ml
= 11,8907 µg/g
= 1,18907 mg/100g
% Perolehan kembali zink = CF−CA
�∗� x 100%
= (13,3825− 12,2474 ) mg /100 g
1,18907 mg /100 g x 100%
Lampiran 18. Perhitungan Simpangan Baku Relatif (RSD) Kadar Mangan dan Zink
1. Perhitungan Simpangan Baku Relatif (RSD) Kadar Mangan
No. Persen perolehan kembali (Xi) (%)
(Xi - X) (%)
(Xi - X)2 (%)
1. 91,64 0,01 0,0001
2. 100,14 8,51 72,4201
3. 88,39 -3,24 10,4976
4. 92,97 1,34 1,7956
5. 88,85 -2,78 7,7284
6. 87,80 -3,83 14,6689
∑Xi = 549,79
∑(Xi - X)2
= 107,1107 X= 91,63
SD =
�
∑(Xi−X)² �−1SD =
�
107,1107 %6−1
SD = 4,628405773%
RSD = ��
� X 100%
RSD = 4,628405773 %
91,63% X 100%
Lampiran 18. (Lanjutan)
2. Perhitungan Simpangan Baku Relatif (RSD) Kadar Zink
No. Persen perolehan kembali (Xi) (%)
(Xi - X) (%)
(Xi - X)2 (%)
1. 80,42 -14,085 198,387225
2. 109,65 15,145 229,371025
3. 96,45 1,945 3,783025
4. 100,60 6,095 37,149025
5. 83,45 -11,055 122,213025
6. 96,46 1,955 3,822025
∑ Xi = 567,03 ∑(Xi - X)2
= 594,722575 X= 94,505
SD =
�
∑(Xi−X)² �−1SD =
�
594,722575 %6−1
SD = 10,90616867%
RSD = ��
� X 100%
RSD =10,90616867 %
94,505 % X 100%
Lampiran 19. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) 1. Perhitungan Batas Deteksi dan Batas Kuantitasi Mangan
Y = 0,5548 X + 0,01345 Slope = 0,5548
No
Konsentrasi (µg/ml)
X
Absorbansi
Y Yi Y-Yi (Y-Yi)
2
1 0,0000 0,0058 0,01345 -0,00765 0,0000585225 2 0,2000 0,1299 0,12441 0,00549 0,0000301401 3 0,4000 0,2400 0,23537 0,00463 0,0000214369
4 0,8000 0,4555 0,45729 0,00179 0,000003041
5 1,2000 0,6813 0,67921 0,00209 0,0000043681 6 1,6000 0,8989 0,90113 0,00223 0,0000049729
∑(Y-Yi)2
= 0,001226446
Simpangan Baku =
�
∑(Y−Yi )² �−2=
�
0,0012264464
= 0, 0055
Batas Deteksi = 3 X ���� �����
=3 X 0,001226446
0,5548
= 0,0297 µg/ml
Batas Kuantitasi = 10 X ��
� � �����
=10 X 0,001226446
0,5548
Lampiran 19. (Lanjutan)
2. Perhitungan Batas Deteksi dan Batas Kuantitasi Zink Y = 0,22835 X + 0,00075
Slope = 0,22835
No
Konsentrasi (µg/ml)
X
Absorbansi
Y Yi Y-Yi (Y-Yi)
2
1 0,0000 0,0011 0,00075 -0,0064 0,00004096
2 0,2000 0,0461 0,0464 -0,0004 0,0000009
3 0,4000 0,0922 0,0921 0,0001 0,0000001
4 0,6000 0,1379 0,1378 0,0001 0,0000001
5 0,8000 0,1841 0,1834 0,0007 0,0000049
6 1,0000 0,2285 0,2291 -0,0006 0,0000036
∑(Y-Yi)2
= 0,00004192
Simpangan Baku =
�
∑(Y−Yi )² �−2=
�
0,000041924
= 0,0032372
Batas Deteksi = 3 X ��
� � �����
= 3 X 0,0032372
0,22835
= 0,0425 µg/ml
Batas Kuantitasi = 10 X ��
� � �����
= 10 X 0,0032372
0,22835
Lampiran 21. Gambar Alat-Alat yang Digunakan
Gambar 1. Spektrofotometri Serapan Atom (HITACHI Zeeman AA-7000)
[image:47.595.116.486.378.592.2]Lampiran 21. (Lanjutan)
Gambar 3. PureLab UHQ (ELGA)
[image:48.595.180.446.433.717.2]Lampiran 21. (Lanjutan)
DAFTAR PUSTAKA
Almatsier, S. (2009). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia PustakaUtama. Hal. 228.
Bassett, J., Denny, R.C., Jeffrey, G.H., dan Mendham, J. (1991). Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Penerjemah: Pudjaatmaka, A., dan Setiono. (1994). Buku Ajar Vogel Kimia Analisis Kuantitatif Anorganik. Edisi Keempat. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 943.
Bender, D.A. (2008). Introduction to Nutrition and Metabolism. Edisi Keempat. Boca Raton: CRC Press. Hal. 387.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Hal. 650, 692.
Ditjen POMRI. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Hal. 1067.
Ermer, J., dan McB. Miller, J.H. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Fahey, J.W. (2005). Moringa oleifera: A Review of the Medical Evidence for Its Nutritional, Therapeutic, and Prophylactic Properties. Part 1.Trees for Life Journal. Hal. 2.
Gandjar, I.G., dan Rohman, A. (2008). Kimia Farmasi Analisis. Cetakan Ketiga.Yogyakarta: Pustaka Pelajar. Hal. 298, 305-306, 310-312, 319-322. Golden, M.H. (2009). Proposed Recommended Nutrient Densities for Moderately
Malnourished Children. Food and Nutrition Bulletin. 30(3): 298.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3). Hal. 117–119,12–122, 127–130.
Harris, D.C. (2007). Quantitative Chemical Analysis. Edisi Ketujuh. New York: W. H. Freeman and Company. Hal. 455.
Hernandez-Saavedra, N.Y., dan Ochoa, J.L. (1999). Copper-Zinc Superoxide Dismutase from the Marine Yeast Debaryomyces hansenii. Yeast. 15:657. Ilyas, M., Arshad, M.U., Saccd, F., dan Iqbal, M. (2015). Antioxidant Potential
and Nutitional Comparison of Moringa Leaf and Seed Powders and Their Tea Infusions. The Journal of Animal & Plant Sciences. 25(1): 228.
Kasolo, J.N., Bimenya, G.S., Ojok, L., dan Ogwal-okeng, J.W. (2011). Phytochemicals and Acute Toxicity of Moringa oleifera Roots in Mice. Journal of Pharmacognosy and Phytotherapy. 3(3).Hal. 38.
Khopkhar, S.M. (1985). Basic Concept of Analytical Chemistry. Terjemahan: Saptoraharjo, A. (1990). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Hal 275.
Krisnadi, A.D. (2015). Kelor Super Nutrisi. Edisi Revisi. Blora: Kelorina.com. Hal.12-13.
Kurniasih. (2013). Khasiat dan Manfaat Daun Kelor. Yogyakarta: Pustaka Baru Press. Hal. 35 – 36, 39, 59 – 62, 146.
Linder, M.C. (1985). Nutritional Biochemistry and Metabolism. Penerjemah: Parakkasi, A. (1992). Biokimia Nutrisi dan Metabolisme: dengan Pemakaian secara Klinis. Jakarta: UI Press. Hal 279-281.
Luthfiyah, F. (2012). Potensi Gizi Daun Kelor (Moringa oleifera) Nusa Tenggara Barat. Media Bina Ilmiah. 6(2): 43.
Moyo, B., Masika, P.J., Hugo, A., dan Muchenje, V. (2011). Nutritional Characterization of Moringa (Moringa oleifera Lam.) Leaves. African Journal of Biotechnology. 10(60): 12925.
Poedjiadi, A. (1994). Dasar-Dasar Biokimia. Edisi Revisi. Jakarta: Universitas Indonesia. Hal. 419.
Roloff, A., Weisgerber, H., Lang, U.M., dan Stimm, B. (2009). Moringa oleifera. Enzyklopädie der Holzgewächse, Handbuch und Atlas der Dendrologie. Hal. 2, 6.
Rosmarkam, A,. dan Yuwono, N.W. (2002). Ilmu Kesuburan Tanah. Yogyakarta: Kanisius. Hal. 31.
Sharma, A.D., Bhullar, A., Rakhra, G., dan Mamik, S. (2014). Analysis of Hydrophilic Antioxidant Enzymes in Invasive Alien Species Parthenium hysterophrus Under High Temperature Abiotic Stress Like Conditions. Journal of Stress Physiology & Biochemistry,10(2): 235.
Sikorsi, Z.E. (2002). Food Components and Their Role in Food Quality. Dalam: Sikorsi, Z.E. (2002). Chemical and Functional Properties of Food Components Series. Edisi Kedua. New York: CRC Press. Hal. 4.
Stosh, S.J., dan Hartman, M.J. (2015). Review of Safety and Efficacy of Moringa oleifera. Phytotherapy Research. 29: 796.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 227-228.
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Balai Riset Industri dan Standarisasi Medan Sumatera Utara, laboratorium penelitian, dan laboratorium Kimia Farmasi Kualitatif Fakultas Farmasi USU. Penelitian dilakukan pada bulan Oktober 2015 – Februari 2016.
3.2 Jenis Penelitian
Jenis penelitian yang dilakukan adalah penelitian eksperimental yaitu penelitian yang dimaksudkan untuk mencari pengaruh perlakuan tertentu, yaitu pengeringan dan perebusan dari daun kelor (Moringa oleifera Lam) terhadap yang lain yaitu kandungan mangan dan zink pada daun kelor dalam kondisi yang terkontrol.
3.3 Alat
Spektrofotometer Serapan Atom (Hitachi Zeeman AA-7000) lengkap dengan lampu katoda Mn dan Zn, Tanur (Stuart), PureLab UHQ (ELGA), Kertas Whatmann no.42, Neraca analitik (BOECO), Krus porselen, Hot plate (FISONS),
Blender (National), Mikroskop, spatula, dan alat-alat gelas.
3.4 Bahan
Semua bahan yang digunakan dalam penelitian ini mempunyai kualitas pro analisis produksi E. Merck yaitu larutan baku Mn(NO3)2 1000 ppm, larutan
kalium sulfida 1% (b/v) (Laboratorium Kimia Analisis Kualitatif), dan akua demineralisata (Laboratorium Penelitian Fak. Famasi USU)
3.5 Metode Pengambilan Sampel
Pengambilan sampel daun kelor dilakukan secara puporsif yaitu tanpa membandingkan dengan daun kelor yang sama dari daerah lain. Sampel yang digunakan adalah daun kelor yang berasal dari Desa Bintang Meriah, Kecamatan Batang Kuis, Kabupaten Deli Serdang, Provinsi Sumatera Utara pada bulan Oktober 2015.
3.6 Identifikasi Sampel
Identifikasi tumbuhan dilakukan oleh Herbarium Bogoriense, Bidang Botani, Pusat Penelitian dan Pengembangan Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bogor, Jalan Raya Jakarta–Bogor Km.46, Cibinong.
3.7 Pembuatan Pereaksi
3.7.1 Larutan Asam Nitrat (1:1)
Asam Nitrat 65% sebanyak 500 ml diencerkan dengan air suling hingga 500 ml (Ditjen POM, 1979).
3.7.2 Larutan Kalium Sulfida 1% (b/v)
Kalium Sulfida sebanyak 1 g dilarutkan dengan air suling hingga 100 ml (Ditjen POM, 1979)
3.7.3 Larutan K2Hg(CNS)4 1,3% (b/v)
3.8 Prosedur Penelitian 3.8.1 Penyiapan Sampel
Daun kelor segar sebanyak 1 kg, dibersihkan dari pengotoran, dicuci bersih dengan akua demineralisata, ditiriskan. Selanjutnya dibagi menjadi 2 bagian, masing-masing sebanyak 500 g. Bagian pertama dibiarkan kering dengan cara diangin-anginkan di udara terbuka terhindar dari sinar matahari langsung hingga kering selama 7 hari, lalu dihaluskan dengan blender dan dihomogenkan. Bagian kedua direbus dalam 700 ml akua demineralisata mendidih selama 10 menit, ditiriskan, lalu dihaluskan dengan blender, dan dihomogenkan.
3.8.2 Proses Destruksi Kering
Sampel yang telah dihaluskan, lalu ditimbang sebanyak 10 gram dalam krus porselin, ditambah 5 ml HNO3 (1:1), dilakukan 6 kali pengulangan,
selanjutnya diarangkan di atas hot plate, lalu diabukan di dalam tanur mula-mula pada temperatur 100oC dan secara perlahan-lahan dinaikkan interval 25oC setiap 5 menit sampai temperatur menjadi 500oC dan pengabuan dilakukan selama 55 jam (dihitung saat suhu sudah 500°C), lalu suhu tanur diturunkan ± 29°C, krus porselin dikeluarkan. Kemudian dibiarkan dingin di dalam desikator (Isaac, 1990 dengan modifikasi).
Pada sampel daun rebus dilakukan proses destruksi yang sama namun lama pengabuan berbeda yaitu 48 jam (dihitung saat suhu sudah 500°C).
3.8.3 Pembuatan Larutan Sampel
Sampel hasil dekstruksi yang di dalam krus porselin dilarutkan dengan 5 ml HNO3 (1:1), dibiarkan hingga selururhnya melarut lalu dituangkan ke dalam
labu tentukur 50 ml, lalu krus porselen dibilas dengan akua demineralisata, lalu dituangkan juga ke dalam labu tentukur, dicukupkan volumenya dengan akua demineralisata hingga garis tanda. Kemudian disaring dengan kertas saring Whatmann no. 42 dimana 5 ml filtrat pertama dibuang untuk menjenuhkan kertas
saring, selanjutnya filtrat ditampung ke dalam botol (Isaac, 1990). Larutan ini digunakan untuk analisis kualitatif dan kuantitatif. Bagan alir pembuatan larutan sampel dapat dilihat pada Lampiran 5 halaman 47.
3.9 Analisis Kualitatif 3.9.1 Mangan
3.9.1.1 Reaksi Warna dengan Larutan Kalium Sulfida
Larutan sampel 1 ml dimasukkan ke dalam tabung reaksi, ditambahkan 3 tetes larutan kalium sulfida. Jika terdapat mangan maka akan dihasilkan endapan merah muda (Vogel, 1979).
3.9.2 Zink
3.9.2.1 Reaksi Pengendapan dengan Larutan K2Hg(CNS)4
Larutan sampel dimasukkan ke dalam tabung reaksi, ditambahkan 2 ml larutan K2Hg(CNS)4 terbentuk endapan putih dimana endapan membentuk
3.10 Analisis Kuantitatif
3.10.1 Pembuatan Kurva Kalibrasi Mangan
Larutan baku mangan (1000 µg/ml) dipipet sebanyak 2 ml, dimasukkan ke dalam labu tentukur 100 ml, dan dicukupkan dengan akua demineralisata sampai garis tanda (konsentrasi 20 µg/ml) disebut Larutan Induk Baku 1 mangan.
Larutan induk baku 1 mangan (LIB 1 mangan) dipipet 25 ml dimasukkan ke dalam labu tentukur 50 ml, lalu di cukupkan dengan akua demineralisata sampai garis tanda (konsentrasi 10 µg/ml) disebut Larutan Induk Baku 2 mangan (LIB 2 mangan).
Larutan untuk kurva kalibrasi mangan dibuat dengan memipet 1; 2; 4; 6; dan 8 ml dari LIB 2 mangan (konsentrasi 10 µg/ml) , masing-masing dimasukkan ke dalam labu tentukur 50 ml, dan dicukupkan dengan akua demineralisata sampai garis tanda (larutan ini mengandung 0,2 µg/ml; 0,4 µg/ml; 0,8 µg/ml; 1 ,2 µg/ml; dan 1,6 µg/ml), lalu diukur pada panjang gelombang 279,5 nm (lampu katoda mangan), dengan nyala udara-asetilen.
3.10.2 Pembuatan Kurva Kalibrasi Zink
Larutan baku zink (1000 µg/ml) dipipet sebanyak 2 ml, dimasukkan ke dalam labu tentukur 100 ml, dicukupkan dengan akua demineralisata sampai garis tanda (konsentrasi 20 µg/ml) disebut Larutan Induk Baku 1 zink.
Larutan untuk kurva kalibrasi zink dibuat dengan memipet 1; 2; 3; 4 dan 5 ml dari LIB 2 zink (konsentrasi 10 µg/ml), masing-masing dimasukkan ke dalam labu tentukur 50 ml, dan dicukupkan dengan akua demineralisata sampai garis tanda (larutan ini masing-masing mengandung 0,2 µg/ml; 0,4 µg/ml; 0,6 µg/ml; 0,8 µg/ml; dan 1,0 µg/ml), lalu diukur pada panjang gelombang 213,9 nm (lampu katoda zink), dengan nyala udara-asetilen.
3.11 Penetapan Kadar Mineral dalam Sampel 3.11.1 Penetapan Kadar Mangan
Larutan sampel daun kelor kering hasil destruksi sebanyak 1 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Larutan sampel daun kelor rebus hasil destruksi sebanyak 5 ml dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan dengan akua demineralisata hingga garis tanda.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 279,5 nm dengan nyala udara-asetilen dan dilakukan 6 kali pengulangan. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku mangan. Konsentrasi mangan dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
3.11.2 Penetapan Kadar Zink
Larutan sampel daun kelor rebus hasil destruksi telah masuk ke dalam rentang kurva kalibrasi sehingga tidak perlu dilakukan pengenceran.
Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 213,9 nm dengan nyala udara-asetilen dan dilakukan 6 kali pengulangan. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku zink. Konsentrasi zink dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
3.11.3 Perhitungan Kadar Mineral dalam Sampel
Kadar mangan dan zink dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar mineral (µg/g) = Konsentrasi (µg/ml ) x Volu me (ml ) x Faktor Pengenceran Berat Sampel (g)
3.12 Analisis Data Secara Statistik 3.12.1 Penolakan Hasil Pengamatan
Sampel kadar mangan dan zink yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik.
Menurut Sudjana (2005), standar deviasi dapat dihitung menggunakan rumus sebagai berikut:
SD = �∑(��−�)2
�−1
Keterangan: Xi = kadar sampel (mg/100 g)
Untuk mencari t hitung digunakan rumus: t hitung = | Xi−X |
SD / √n
penolakan hasil pengamatan dapat disimpulkan apabila nilai t hitung lebih besar dari t tabel (t hitung > t kritis) yang dapat dilihat pada tabel distribusi T pada Lampiran 22 pada halaman 76. Untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 99%, α = 0.01, dk = n-1, dapat digunakan rumus:
μ = X� ± t(∝/2,dk ) x SD √n
Keterangan: X = kadar rata-rata sampel (mg/100 g) SD = standar deviasi (mg/100 g)
dk = derajat kebebasan (dk = n-1) α = interval kepercayaan
n = jumlah pengulangan
3.13 Analisis Validasi Metode
3.13.1 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel yang sudah ditambahkan larutan standar dengan konsentrasi tertentu, kemudian dihitung berapa jumlah analit yang ditambahkan (Ermer dan McB. Miller, 2005).
Daun kering kelor ditimbang sebanyak 10 gram di dalam krus porselen, lalu ditambahkan 14 ml LIB 2 mangan (konsentrasi 10 µg/ml) dan 12 ml LIB 2 zink (konsentrasi 10 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
Persen Perolehan Kembali = CF − CA
CA∗ x 100 %
Keterangan:
CA = kadar logam dalam sampel sebelum penambahan baku (mg/100g)
CF = kadar logam dalam sampel setelah penambahan baku (mg/100g)
C*A = kadar larutan baku yang ditambahkan (mg/100g)
3.13.2 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut:
RSD = ×100% X
Keterangan: X = kadar rata-rata sampel (%) SD = standar deviasi (%)
RSD = relative standard deviation (%)
3.13.3 Penentuan Batas Deteksi dan Batas Kuantitasi
Menurut Harmita (2004), batas deteksi (Limit of Detection, LOD) merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sebaliknya batas kuantitasi (Limit of Quantitation, LOQ) merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku Residual (Sy/x) = �∑(�−��)2
�−2
Batas Deteksi (µg/ml) = 3���/�
�����
Batas Kuantitasi (µg/ml) = 10 ���/�
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Herbarium Bogoriense, Bidang Botani, Pusat Penelitian dan Pengembangan Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor, Jalan Raya Jakarta–Bogor Km.46, Cibinong. Disebutkan bahwa tumbuhan yang digunakan adalah daun tumbuhan kelor (Moringa oleifera Lam.), suku Moringaceae. Surat hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1 halaman 41.
4.2 Identifikasi Sampel yang Digunakan
Sampel yang digunakan adalah daun kelor segar yang memiliki ciri-ciri berbentuk bulat telur dengan ukuran kecil-kecil bersusun majemuk dalam satu tangkai, bagian atas daun warna hijau tua dengan permukaan licin sedangkan bagian bawah daun berwarna hijau keputihan, panjang dan lebar rata rata daun kelor adalah 2,6 cm dan 1,6 cm. Daun kelor memiliki tangkai pendek dengan tulang daun menyirip, juga tidak memiliki bau dan rasa yang khas. Pada penelitian ini sampel yang digunakan adalah seluruh daun kelor dari 1 tangkai pada tanpa memasukkan daun kelor yang memiliki warna kuning, sebab daun kelor memiliki tekstur lembut walaupun daun tersebut tua. Hasil identifikasi tumbuhan dapat dilihat di Lampiran 2 halaman 42.
4.3 Analisis Kualitatif
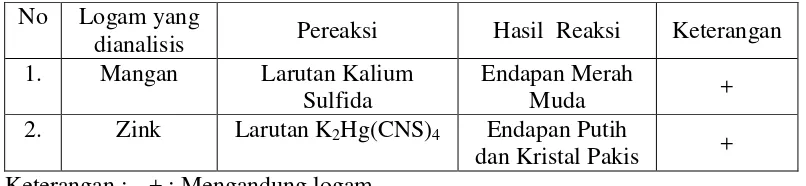
dapat dilihat pada Lampiran 6 halaman 49 dan hasil analisis kualitatif dapat dilihat pada Tabel 4.1.
Tabel 4.1 Hasil Analisis Kualitatif No Logam yang
dianalisis Pereaksi Hasil Reaksi Keterangan 1. Mangan Larutan Kalium
Sulfida
Endapan Merah
Muda +
2. Zink Larutan K2Hg(CNS)4 Endapan Putih
dan Kristal Pakis + Keterangan : + : Mengandung logam
Dari Tabel 4.1 diatas menunjukkan bahwa larutan sampel yang diperiksa terdapat ion mangan dan ion zink. Sampel dikatakan positif terdapat ion mangan karena menghasilkan endapan merah muda dengan penambahan larutan kalium sulfida dan terdapat ion zink apabila ditambahkan K2Hg(CNS)4 menghasilkan
emdapan putih dengan bentuk kristal pakis (Vogel, 1979).
Hasil absorbansi dengan spektrofotometri serapan atom menunjukkan adanya absorbansi pada λ 279,5 nm untuk logam mangan dan λ 213,9 nm untuk
logam zink. Hal ini turut membuktikan bahwa sampel mengandung logam mangan dan zink.
4.4 Analisis Kuantitatif
4.4.1 Kurva Kalibrasi Mangan dan Zink
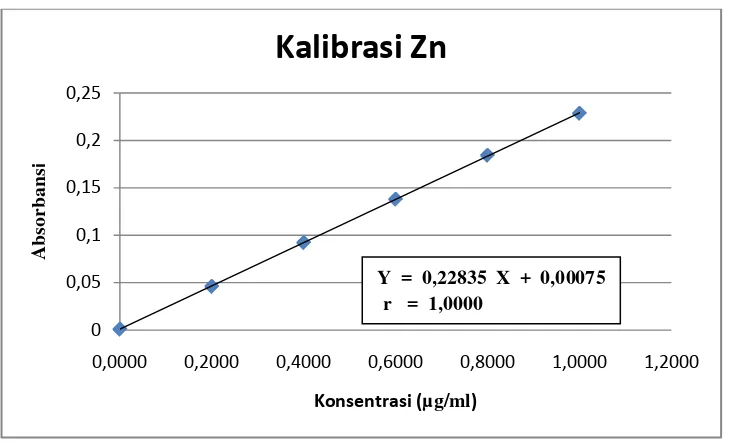
Kurva kalibrasi dengan spektrofotometri serapan atom dibuat dalan berbagai konsentrasi dengan konsentrasi yang meningkat. Dari pengukuran kurva kalibrasi diperoleh masing-masing persamaan regresi yaitu Y = 0,5548 X + 0,01354 untuk mangan dan Y = 0,22835 X + 0,00075 untuk zink.
Gambar 4.1 Kurva Kalibrasi Larutan Baku Mangan
Gambar 4.2 Kurva Kalibrasi Larutan Baku Zink
Berdasarkan kurva diatas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) mangan sebesar 0,9999 dan zink sebesar 1,0000. Nilai r ≥ 0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (Konsentrasi) dan Y (Absorbansi) (Ermer dan McB. Miller, 2005).
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1
0,0000 0,5000 1,0000 1,5000 2,0000
A
bs
or
ban
si
Konsentasi (µg/ml)
Kalibrasi Mn
0 0,05 0,1 0,15 0,2 0,250,0000 0,2000 0,4000 0,6000 0,8000 1,0000 1,2000
A bs o r ba ns i
Konsentrasi (µg/ml)
Kalibrasi Zn
Y = 0,22835 X + 0,00075 r = 1,0000
[image:65.595.131.496.366.588.2]Data hasil pengukuran absorbansi larutan baku dan perhitungan persamaan garis regresi mangan dan zink dapat dilihat pada Lampiran 7 dan 8 halaman 50 sampai 53.
4.4.2 Analisis Kadar Mangan dan Zink pada Daun Kelor Kering dan Daun Kelor Rebus
Penentuan kadar mangan dan zink dilakukan secara spektrofotometri serapan atom. Konsentrasi mangan dan zink dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku masing-masing mineral. Agar konsentrasi mineral mangan dan zink dalam sampel berada pada rentang kurva kalibrasi maka masing-masing sampel diencerkan terlebih dahulu dengan faktor pengenceran yang berbeda-beda.
Konsentrasi mangan dan zink pada sampel daun kelor kering melebihi dari rentang kurva kalibrasi, maka masing-masing sampel harus diencerkan lagi (faktor pengenceran = 50). Pada sampel daun rebus, konsentrasi mangan melebihi rentang kurva kalibrasi sehingga harus dilakukan pengenceran (faktor pengenceran = 5), namun pada zink, konsentasi telah berada dalam rentang kurva kalibrasi sehingga tidak perlu dilakukan pengenceran (faktor pengenceran = 1). Data dan contoh perhitungan dapat dilihat pada Lampiran 11 sampai dengan Lampiran 12, halaman 56-57.
Analisis kemudian dilanjutkan dengan perhitungan statistik (hasil perhitungan dapat dilihat pada Lampiran 13 sampai dengan lampiran 14, halaman 58-67).
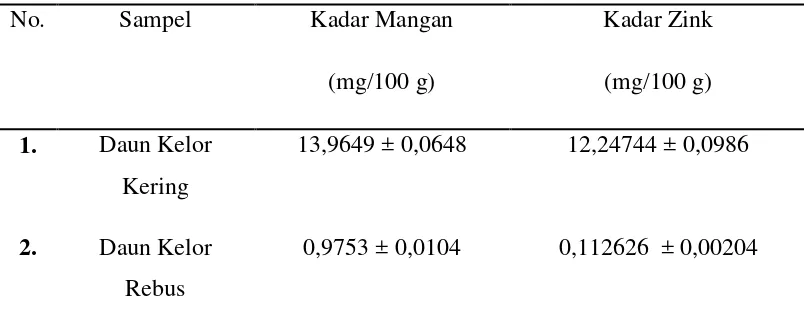
Tabel 4.2 Hasil Analisis Kadar Mangan dan Zink dalam Sampel
No. Sampel Kadar Mangan
(mg/100 g)
Kadar Zink (mg/100 g) 1. Daun Kelor
Kering
13,9649 ± 0,0648 12,24744 ± 0,0986
2. Daun Kelor Rebus
0,9753 ± 0,0104 0,112626 ± 0,00204
Pada Tabel 4.2 di atas menunjukkan kadar mangan dan zink pada daun kering kelor adalah (13,9649 ± 0,0648) mg/100 g dan (12,24744 ± 0,0986) mg/100 g, sedangkan kadar mangan dan zink pada daun kelor rebus adalah (0,9753 ± 0,0104) mg/100 g dan (0,112626 ± 0,00204) mg/100 g.
Berdasarkan Tabel 4.2 diatas dapat diketahui bahwa kadar mangan pada daun kelor kering lebih besar dibandingkan di daun rebus kelor, menurut Sikorsi, (2002), komposisi makanan dapat berubah akibat pengaruh enzim mikroba, bentuk aktif dari oksidasi, pemanasan, penambahan zat, dan proses dalam kondisi pH rendah atau tinggi. Perubahan komposisi pada sampel daun kelor ini diakibatkan oleh adanya pemanasan.
halnya zink, mangan ternyata di dalam tumbuhan berikatan dengan superoxide dismutase atau SOD membentuk kompleks Mn-SOD yang merupakan enzim antioksidan yang penting di dalam mitokondria. Superoxide dismutase merupakan senyawa yang bersifat hidrofil (Sharma, dkk., 2014) sehingga dengan adanya pemanasan pada proses perebusan yang dilakukan pada sampel akan terjadi peluruhan senyawa yang dalam hal ini SOD berikatan dengan mineral Mn dan Cu-Zn.
Kadar mangan dan zink yang diperoleh pada penelitian ini memiliki hasil yang lebih besar dibandingkan yang dilakukan oleh Ilyas, dkk., (2015). Berdasarkan penelitian yang dilakukan Ilyas, dkk., (2015) kadar mangan dalam daun kelor kering (8,009 ± 0.21 mg/100 g) dan kadar zink pada daun kelor kering (7,009 ± 0.13 mg/100 g). Kandungan hara dalam tanaman berbeda-beda tergantung pada jenis hara, jenis tanaman, kesuburan tanah atau jenis tanah dan pengelolaan tanaman (Rosmarkam dan Yuwono, 2002). Daun kelor yang digunakan pada penelitian Ilyas, dkk., (2015) tidak diperoleh dari daerah Indonesia yang tidak diketahui jenis dan kesuburan tanahnya, sedangkan daun kelor pada penelitian ini diperoleh dari daerah di Indonesia tepatnya di Desa Bintang Meriah, Kecamatan Batang Kuis, Kabupaten Deli Serdang, Provinsi Sumatera Utara yang tanahnya subur sehingga ketersediaan unsur haranya baik.
4.4.3 Uji Perolehan Kembali (Recovery)
Perhitungan persen recovery mangan dan zink dalam sampel dapat dilihat pada Lampiran 17 pada halaman 70 sampai 81. Persen recovery mangan dan zink dalam sampel dapat dilihat pada Tabel 4.3.
Tabel 4.3 Persen Uji Perolehan Kembali (recovery) Kadar Mangan dan Zink
No. Logam yang Dianalisis
Rata-Rata Recovery (%)
Syarat Rentang Recovery (%)
1. Mangan 91,63
80 – 120
2. Zink 94,505
Berdasarkan Tabel 4.3 diatas, diketahui bahwa nilai rata-rata recovery untuk logam mangan dan zink adalah 91,63% dan 94,51%. Nilai rata-rata hasil uji perolehan kembali (recovery) tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar mangan dan zink dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80 – 120% (Ermer dan McB. Miller, 2005).
4.4.4 Simpangan Baku Relatif
[image:69.595.112.518.644.725.2]Perhitungan simpangan baku relatif mangan dan zink dalam sampel dapat dilihat pada Lampiran 18 pada halaman 82 sampai 83. Simpangan baku relatif mangan dan zink dalam sampel dapat dilihat pada Tabel 4.4 berikut
Tabel 4.4 Simpangan Baku Relatif Mangan dan Zink dalam Sampel
No. Logam yang Dianalisis Simpangan Baku (%) Simpangan Baku Relatif (%) Syarat Simpangan Baku Relatif(%)
1. Mangan 4,63 5,05
16
Berdasarkan Tabel 4.4 diatas, nilai simpangan baku dan simpangan baku relatif dari logam mangan adalah 4,63% dan 5,05%, dan nilai simpangan baku dan simpangan baku relatif dari logam zink adalah 10,91% dan 11,54%.
Nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per
million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per
billion (ppb) RSD-nya adalah tidak lebih dari 32% (Harmita, 2004). Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki ketelitian yang baik karena memenuhi syarat.
4.4.5 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi mangan dan zink diperoleh batas deteksi (Limit of Detection, LOD) dan batas kuantitasi (Limit of Quantitation, LOQ) masing-masing dapat dilihat pada Tabel 4.5 berikut:
Tabel 4.5 Batas Deteksi dan Batas Kuantitasi Mangan dan Zink No. Logam yang
Dianalisis Batas Deteksi (µg/ml) Batas Kuantitasi (µg/ml)
1. Mangan 0,0297 0,0991
2. Zink 0,0425 0,1418
Berdasarkan Tabel 4.5 diatas, batas deteksi dan kuantitasi mangan adalah 0,0425 µg/ml dan 0,1418 µg/ml, dan batas deteksi dan kuantitasi zink adalah 0,0297 µg/ml dan 0,0991 µg/ml. Konsentrasi mangan dan zink yang diperoleh
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
1. Hasil analisis kualitatif menunjukkan adanya mineral mangan dan zink di dalam daun kelor kering dan daun kelor rebus.
2. Hasil penetapan kadar mangan dan zink secara spektrofotometri serapan atom, beturut-turut pada daun kering sebesar (13,9649 ± 0,0648) mg/100 g dan (12,24744 ± 0,0986) mg/100 g, pada daun rebus sebesar (0,9753 ± 0,0104) mg/100 g dan (0,112626 ± 0,00204) mg/100 g.
5.2Saran
1. Kadar mineral di serbuk daun juga cukup tinggi disarankan dapat menjadi sumber mineral alternatif untuk dikonsumsi masyarakat.
2. Disarankan kepada masyarakat untuk mengkonsumsi sayuran daun kelor rebus untuk sumber mineral dan nutrisi.
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel 2.1.1 Kelor
Menurut Kasolo, dkk., (2011), sistematika tumbuhan kelor adalah sebagai berikut:
Kingdom : Plantae
Divisio : Magnoliophyta Kelas : Magnoliopsida Ordo : Brassicales Kelas : Moringaceae Genus : Moringa
Spesies : Moringa oleifera Lam
Moringa (Moringa oleifera Lam) merupakan tanaman asli sub-Himalaya, namun tanaman ini juga tumbuh secara luas pada daerah pada iklim tropis dan subtropis meliputi Afrika, Amerika selatan dan tengah, Mexico, Hawaii, juga melewati Asia dan tenggara Asia seperti India, Pakistan, Bangladesh, Afganistan. Tanaman ini dikenal sebagai drumstick berdasarkan penampilan dari bentuk polong yang belum masak, juga dikenal sebagai pohon ben oil karena kandungan derivat minyak dari biji kelor. Selain itu kelor dibeberapa regional dikenal sebagai Benzolive, Horseradish, Marango, Mloge, Mulangay, Saijihan, dan Sajna
Kelor merupakan tanaman yang sangat cepat tumbuh, dapat bertahan dan terus menghasilkan ketika kering dan panas, juga tumbuh secara optimal pada lahan kering di seluruh bagian tropis. Selain itu, tanaman ini dapat tumbuh hingga 10 atau 12 m tingginya.. Tanaman ini batangnya berkayu, tegak, berwarna putih kotor, namun batang kayunya lunak atau mudah patah (Roloff, dkk., 2008).
Daun kelor merupakan daun majemuk dimana tangkai daunnya memiliki cabang kedua namun biasanya sampai percabangan ketiga yang memiliki panjang hingga 45 cm. Daun kelor memiliki panjang 1,2 hingga 2,0 cm dan lebar 0,6 hingga 1,0 cm. Bagian permukaan atas helai daun kelor berwarna hijau dan sedangkan bagian permukaan bawah berwarna lebih pucat, juga kedua permukaan halus. Daun kelor berbentuk bulat menyerupai telur, daunnya yang tipis dan lemas membentuk pangkal daun membulat dan ujung yang tumpul (Roloff, dkk., 2008).
2.1.2 Kandungan
Daun kelor yang telah dikarakterisasi diketahui mengandung kaya akan vitamin seperti tiamin dan riboflavin, mineral, asam amino, dan asam lemak. Sebagai tambahan, daun kelor diketahui mengandung berbagai macam senyawa antioksidan, seperti asam askorbat, flavonoid, fenol, dan karotenoid (Stosh dan Hartman, 2015). Menurut Fahey, (2005), daun kelor mengandung lebih banyak vitamin A dibanding wortel, lebih banyak zat besi dibanding bayam, lebih banyak kalium dibanding pisang, serta kualitas protein dari daun kelor dapat menyaingi susu dan telur, hal inilah salah satu alasan mengapa kelor dikatakan mengandung kaya akan nutrisi, sedangkan pada bijinya mengandung 19-47% minyak yang dikenal sebagai ben oil, yang kaya akan palmitat, stearat, dan asam oleat (Roloff, dkk., 2008).
2.1.3 Manfaat
2.2 Mineral
Mineral merupakan bagian tubuh dan memegang peran penti