Penyisihan ammonium secara kimiawi menggunakan magnesium
(studi kasus: TPA Benowo)
Ika Mayang Sari2, Warmadewanthi1
Jurusan Teknik Lingkungan, Institut Teknologi Sepuluh Nopember, Surabaya
1
warma@its.ac.id;2kadika_wontreal@yahoo.co.id
ABSTRAK
Penelitian ini menggunakan lindi artificial dengan karakteristik yang sama dari lindi TPA Benowo dan lindi TPA Benowo. Penelitian ini dilakukan dengan 4 variabel, diantaranya waktu reaksi, pH, dosis magnesium dan tipe magnesium. Penelitian ini menggunakan 2 tipe magnesium yaitu MgO dan MgSO4. Tujuan dari penelitian ini adalah untuk menyisihkan kandungan ammonium pada lindi
dengan pengolahan kimiawi yaitu menggunakan magnesium.
Hasil penelitian menunjukkan kondisi optimum terjadi pada menit ke-20 dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1,5:1:1 dan pH optimum untuk penyisihan ammonium dan
pospat pada pH 9. Removal efisiensi ammonium dan pospat yang dicapai pada penelitian menggunakan lindi artificial masing-masing sebesar 99,33% dan 96,69 Removal efisiensi ammonium dan pospat yang dicapai pada penelitian menggunakan lindi TPA Benowo masing-masing sebesar 97,83% dan 69,05%.
1. PENDAHULUAN
Penimbunan sampah pada landfill di kota besar sering menemukan masalah karena tidak mengikuti kaidah penimbunan sampah di sanitary landfill. Salah satu masalah pada proses penimbunan sampah adalah timbulan dan pengolahan lindi.
Lindi didefenisikan sebagai cairan yang telah mengalami perkolasi melalui tumpukan sampah. Lindi mengandung materi tersuspensi, bahan-bahan terlarut, dan terekstraksi dari sampah, dan beberapa dari kandungan lindi tersebut sangat berbahaya (Tchobanoglous, Theisen, Vigil, 1993). Karakteristik lindi sangat tergantung dari komposisi sampah yang tertimbun di dalam landfill. Secara umum, lindi mengandung ammonia-nitrogen (NH4-N) yang tinggi dan ratio BOD/COD yang
tinggi sehingga menyulitkan dalam pengolahan biologis (Kim et al., 2007). Konsentrasi NH4-N
yang tinggi di dalam lindi akan sangat menganggu proses pengolahan secara anaerobik, karena senyawa ini menghambat kinerja dari bakteri methan dalam proses methanasi (Wiszniowski et al., 2006). Azis et al., (2004) menyatakan diperlukan pre-treatment untuk menghilangkan NH4-N
sebelum dilakukan pengolahan lindi secara biologis.
Salah satu alternatif untuk mengurangi konsentrasi NH4-N dapat dilakukan pengolahan secara
kimiawi. Pengolahan yang sering dilakukan adalah memisahkan senyawa ini dengan membentuk endapan magnesium ammonium pospat (MgNH4PO4.6H2O) atau dikenal sebagai mineral struvite.
Beberapa peneliti juga sudah meneliti pengurangan NH4-N dalam lindi dengan pengolahan kimiawi
dengan pembentukan mineral magnesium ammonium pospat (MAP) (Kim et al., 2007; Li et al., 1999). Warmadewanthi dan Liu (2009) juga melakukan penelitian mengenai pemisahan pospat, flour, dan ammonium dari air buangan semiconductor dengan pembentukan mineral MAP,
2. METODE PENELITIAN dan BAHAN-BAHAN yang DIGUNAKAN
2.1.Karakteristik Lindi
Penelitian ini menggunakan lindi artificial dengan karakteristik yang sama dari lindi TPA Benowo . Penggunaan lindi artificial untuk menentukan apakah terjadi penyisihan ammonium dengan penambahan magnesium. Selain lindi artificial, penelitian ini juga menggunakan lindi TPA Benowo.Karakteristik lindi artificial dapat dilihat pada Tabel 1, sedangkan karakteristik lindi TPA Benowo dapat dilihat pada Tabel 2.
Tabel 1 Karakteristik Lindi Artificial
No. Parameter Satuan Nilai
1. NH4-N mg/L 1510
2. PO4-P mg/L 75,20
Sumber: hasil analisis laboraturium
Tabel 2 Karakteristik Lindi TPA Benowo
No. Parameter Satuan Nilai
1. NH4-N mg/L 1747,5
2. PO4-P mg/L 76,20
3. Cl mg/L 22200
4. SO4 mg/L 2357,58
5. PV mg/L KMnO4 6636
Sumber: hasil analisa laboratorium
2.2. Bahan-bahan yang Digunakan
Bahan-bahan yang digunakan pada penelitian ini yaitu yaitu magnesium oxyde (MgO),
magnesium sulphate (MgSO4), ammonium chloride (NH4Cl), natrium dihydrogenphosphate
2.3.Pelaksanaan Penelitian
Dalam penelitian ini digunakan 4 variabel yaitu:
1. Keefektifan magnesium; garam magnesium yang digunakan yaitu MgO dan MgSO4
2. Waktu reaksi; untuk menentukan waktu optimum dengan range pengadukan antara 0 – 1 jam 3. pH; range pH yang dipakai antara 7-10
4. Dosis penambahan magnesium; dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] yaitu:
ü 1:1:1 ü 1,5:1:1 ü 2:1:1
Parameter yang akan dianalisa adalah ammonium [NH4-N] dan pospat [PO4-P]. Analisa [NH4
-N] dan [PO4-P] menggunakan metode spektrofotometri.
Penelitian dilakukan di Laboratorium Ekotoksikologi, Jurusan Teknik Lingkungan Institut Teknologi Sepuluh Nopember Surabaya. Pada penelitian ini, magnesium yang dipakai (MgO dan MgSO4) ditambahkan kedalam 1000 mL lindi artifisial dan diaduk menggunakan jar-test apparatus
dengan kecepatan pengadukan (mixing speed) sebesar 200 rpm dan range waktu pengadukan antara 0 – 60 menit. Berdasarkan literatur, Burns et al. (2003) menemukan waktu reaksi optimum untuk pengendapan mineral MAP pada rentang waktu 10 – 40 menit. Sodium hydroxide (NaOH) 6 M ditambahkan untuk meningkatkan pH. Pengambilan sampel diambil setiap 10 menit. Penelitian dilakukan dalam skala laboratorium menggunakan batch system.
Parameter yang diuji pada penelitian ini adalah Ammonium (NH4-N) dan Pospat (PO4-P).
Analisa Ammonium (NH4-N) menggunakan metode Nessler dimana pada sampel yang diambil
ditambahkan 1 mL reagen Nessler dan 1,25 mL Garam Signette kemudian diukur menggunakan spektrofotometer pada panjang gelombang 410 nm. Analisa Pospat (PO4-P) menggunakan metode
Molybdate dan 3 tetes larutan SnCl2 kemudian diukur menggunakan spektrofotometer pada panjang
gelombang 650 nm.
3. HASIL PENELITIAN
Efek pH dengan Variasi Penambahan MgO dan MgSO4
pH merupakan salah satu parameter yang digunakan dalam penelitian ini karena aktivitas ion NH4 dan PO4 dipengaruhi oleh pH. NH4 akan tervolatilisasi menjadi NH3 pada pH lebih besar dari 9
(Wang et al., 2005; Uludag-Demirer, Demirer, Chen, 2005). Chimenos et al. (2006) mengatakan apabila pH lebih kecil dari 7 tidak akan terbentuk kristal mineral MAP tetapi membentuk kristal lain yaitu newberyite (MgHPO4.3H2O). Pada pH lebih kecil dari 7, kemungkinan terbentuknya
mineral MAP terlalu kecil (Jaffer et al., 2002; Stratfull, Schrimshaw, Lester, 2001). Wang et al. (2005) mengungkapkan bahwa dengan peningkatan pH lebih besar dari 10 maka sudah dipastikan akan membentuk lapisan endapan yang tidak dapat diidentifikasikan (amorphous). Warmadewanthi dan Liu (2009) mengatakan removal efisiensi dari ammonium menurun seiring dengan peningkatan pH dari 10-12 dikarenakan adanya persaingan antara ion hydroxyl [OH-] dengan ion-ion PO4, selain
itu juga, pada pH diatas 10, tidak hanya mineral MAP yang terbentuk, tetapi juga mineral-mineral lain juga terbentuk seperti mineral Brucite (Mg(OH)2) yang lebih dominan pada pH 11-12 dan
Bobierrite (Mg3(PO4)2.8H2O). Warmadewanthi dan Liu (2009) juga mengatakan bahwa solubilitas
dari pospat menurun dengan signifikan dengan adanya peningkatan pH pada range 7 sampai 10. Oleh karena itu, range pH yang digunakan pada penelitian ini antara pH 7 sampai pH 10. Pada penelitian ini digunakan variasi jenis magnesium yaitu MgO dan MgSO4. Hasil penelitian efek dari
pH untuk penyisihan ammonium dengan menggunakan MgO dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 dapat dilihat pada Gambar 1.
0 10 20 30 40 50 60 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 Konsentra si Ammoni um (mg/L) Waktu (menit) pH 7 pH 8 pH 9 pH 10 [Mg]:[NH4+ ]:[PO4 3-] = 1:1:1 menggunakan MgO
Gambar 1 Grafik pengaruh dari pH untuk penyisihan ammonium dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 menggunakan MgO
Berdasarkan Gambar 1 di atas, removal efisiensi untuk pH 7 sebesar 97,93%, removal efsiensi untuk pH 8 sebesar 96,66%, removal efisiensi untuk pH 9 sebesar 99,44% dan removal efisiensi untuk pH 10 sebesar 98,36%. Pada penelitian ini, pH optimum yang dicapai pada pH 9 dengan peningkatan removal efisiensi yang signifikan sebesar 2,78% dari pH 8 ke pH 9 yaitu dari 96,66% menjadi 99,44%. Pada penelitian ini, terjadi penurunan removal efisiensi dari pH 9 ke pH 10 dari 99,44% menjadi 98,36%. Penelitian yang dilakukan oleh Stratful et al. (2004) menggunakan limbah
artificial memiliki karakteristik sama dengan effluent anaerobic digester. Penelitian ini memperoleh
hasil yang sama seperti penjelasan di atas bahwa terjadi penurunan removal efisiensi dari pH 9 ke pH 10, penurunan ini disebabkan adanya proses volatilisasi ammonium menjadi ammonia.
Grafik di atas dapat memberikan informasi bahwa pada perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 waktu reaksi optimum pada pH optimum yaitu pH 9 terjadi pada menit
ke-20, sedangkan untuk pH 7, pH 8, dan pH 10, waktu reaksi yang dibutuhkan untuk penyisihan ammonium selama 50 menit.
Selain ammonium, penelitian ini juga menganalisis kandungan pospat yang terdapat dalam lindi. Hal ini dikarenakan, mineral MAP tidak hanya terdiri dari ion ammonium, tetapi juga mengandung
ion pospat. Prosedur penyisihan pospat sama dengan prosedur penyisihan ammonium yaitu dengan menambahkan magnesium ke dalam lindi artificial. Magnesium yang digunakan pada penelitian ini yaitu MgO. Hasil penelitian efek dari pH untuk penyisihan pospat dengan menggunakan MgO dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 dapat dilihat pada Gambar 2.
0 10 20 30 40 50 60 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 Konsen trasi Pospat (mg/L) Waktu (menit) pH 7 pH 8 pH 9 pH 10 [Mg]:[NH4 + ]:[PO4 3-] = 1:1:1 menggunakan MgO
Gambar 2 Grafik pengaruh dari pH untuk penyisihan pospat dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 menggunakan MgO
Hasil penelitian pada Gambar 2 menunjukkan bahwa waktu reaksi optimum untuk penyisihan pospat pada pH optimum yaitu pH 10 terjadi pada menit ke-20. Berdasarkan teori, seiring dengan peningkatan pH, maka removal efisiensi yang dihasilkan juga semakin baik (Zhang, Ding, Ren, 2008). Removal efisiensi untuk pH 7 sebesar 96,49%, pH 8 removal efisiensi mencapai sebesar 96,48%. Removal efisiensi untuk pH 9 sebesar 96,74% dan pH 10 memiliki removal efisiensi sebesar 97,9%. Removal efisiensi meningkat dari 96,48% menjadi 97,9%. Pada penelitian ini pH optimum untuk menyisihkan pospat yaitu pada pH 10 dengan removal efisiensi sebesar 987,9% .
Warmadewanthi dan Liu (2009) menyatakan seiring peningkatan pH, maka removal efisiensi untuk penyisihan semakin baik, namun, tidak hanya mineral MAP yang kemungkinan terbentuk tetapi mineral lain juga terbentuk yaitu mineral Bobierrite (Mg3(PO4)2.8H2O) dan Brucite
Li, Zhao, Hao (1999) melakukan penyisihan ammonium dari lindi yang dikumpulkan di landfill WENT, Hongkong, dengan menggunakan pengendapan bahan kimia. Penelitiannya menggunakan 3 kombinasi bahan kimia yaitu MgCl2.6H2O + Na2HPO4.12H2O, MgO + 85% H3PO4,
Ca(H2PO4)2.H2O + MgSO4.7H2O. MgSO4.7H2O, dapat meminimisasi salinitas setelah pengendapan,
namun kurang efisien untuk penyisihan ammonium (NH4+-N) jika dibandingkan dengan MgO. Oleh
karena lindi TPA Benowo mengandung salinitas yang cukup tinggi, maka penelitian ini juga menggunakan MgSO4. Hasil penelitian efek dari pH untuk penyisihan ammonium menggunakan
MgSO4 dapat dilihat pada Gambar 3.
0 10 20 30 40 50 60 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 Konsen tr asi Amm onium ( mg/L) Waktu (menit) pH 7 pH 8 pH 9 pH 10 [Mg]:[NH4+ ]:[PO4 3-] = 1:1:1 menggunakan MgSO4
Gambar 3 Grafik pengaruh dari pH untuk penyisihan ammonium dengan perbandingan molar rasio [Mg2+]:[NH4
+
]:[PO4
3-] 1:1:1 menggunakan MgSO4
Removal efisiensi ammonium pada penelitian dapat dilihat pada Gambar 4.3. Removal efisiensi ammonium pada pH 7 sebesar 98,05%, pH 8 removal efisiensi ammonium sebesar 98,94%, sedangkan untuk pH 9, removal efisiensi ammonium mencapai 97,45%, dan removal efisiensi ammonium pada pH 10 sebesar 97,99%. Pada penelitian ini, pH optimum yang dicapai adalah pH 8 dikarenakan removal efisiensi mencapai 98,94%.
Berdasarkan grafik di atas, dapat diketahui bahwa waktu reaksi optimum pada pH optimum yaitu pada pH 8 terjadi pada menit ke-50, jika dibandingkan dengan menggunakan MgO, waktu reaksi yang diperlukan lebih lama.
Variasi penambahan MgSO4 ini juga melakukan analisis kandungan pospat. Prosedur yang
digunakan sama dengan prosedur yang dilakukan untuk analisis penyisihan ammonium yaitu dengan penambahan magnesium ke dalam lindi artificial. Hasil penelitian efek dari pH untuk penyisihan kandungan pospat menggunakan MgSO4 dapat dilihat pada Gambar 4.
0 10 20 30 40 50 60 0 10 20 30 40 50 60 70 80 1400 1450 1500 1550 1600 1650 1700 Konsentrasi Pospat (m g/L ) Waktu (menit) pH 7 pH 8 pH 9 pH 10 [Mg]:[NH4+ ]:[PO4 3-] = 1:1:1 menggunakan MgSO4
Gambar 4 Grafik pengaruh dari pH untuk penyisihan pospat dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 menggunakan MgSO4
Removal efisiensi pospat dapat diketahui dari Gambar 4 pH 7 removal efisiensi mencapai sebesar 96,13%, removal efisiensi pospat untuk pH 8 sebesar 94,55%, sedangkan pH 9 removal efisiensi mencapai sebesar 96,83% dan removal efisiensi untuk pH 10 sebesar 97,57%. Dapat disimpulkan bahwa pH optimum pada penelitian ini terjadi pada pH 10 karena removal efisiensi pospat sebesar 97,57%. Hasil penelitian yang didapat sesuai dengan teori yang dikemukakan oleh Warmadewanthi dan Liu (2009) yaitu seiring peningkatan pH, maka removal efisiensi untuk penyisihan semakin baik, namun, tidak hanya mineral MAP yang kemungkinan terbentuk tetapi mineral lain juga terbentuk yaitu mineral Bobierrite (Mg3(PO4)2.8H2O).
Waktu reaksi optimum pada pH optimum yaitu pada pH 10 pada penelitian ini (Gambar 4) terjadi pada menit ke-50.
Kondisi optimum pada penelitian untuk penyisihan ammonium dengan variasi penambahan MgO maupun MgSO4 dapat dilihat pada Gambar 5, sedangkan untuk penyisihan pospat dapat
dilihat pada Gambar 6.
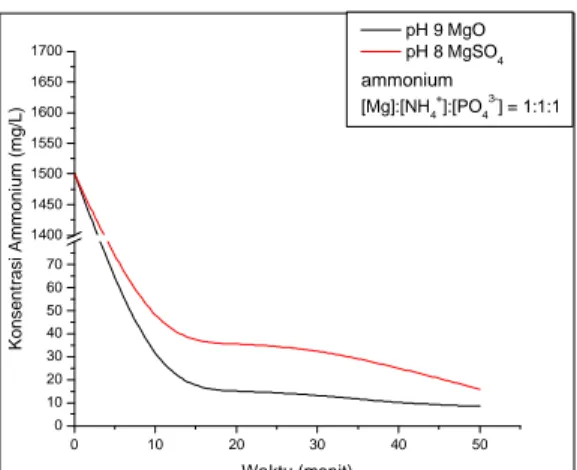
0 10 20 30 40 50 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 Konsent rasi Ammoni um (mg/L) Waktu (menit) pH 9 MgO pH 8 MgSO4 ammonium [Mg]:[NH4 + ]:[PO4 3-] = 1:1:1
Gambar 5 Perbandingan antara pH optimum untuk penyisihan ammonium dengan variasi penambahan MgO dan MgSO4
Hasil penelitian penyisihan ammonium dengan variasi penambahan MgO, pH optimum terjadi pada pH 9 dengan removal efisiensi sebesar 99,44%, sedangkan penyisihan ammonium dengan variasi penambahan MgSO4, pH optimum terjadi pada pH 8 dengan removal efisiensi sebesar
98,94%. Perbedaan pH optimum disebabkan solubilitas senyawa MgO dan MgSO4 yang
ditambahkan ke dalam lindi artificial.
Berdasarkan grafik di atas, dapat dilihat bahwa penyisihan ammonium dengan variasi penambahan MgO removal efisiensi mencapai lebih besar dibandingkan dengan variasi penambahan MgSO4 yaitu sebesar 99,44%. Waktu reaksi optimum pada pH 9 MgO terjadi pada
menit ke-20 dan pada pH 8 MgSO4 terjadi pada menit ke-50. Ini dapat diartikan bahwa keefektifan
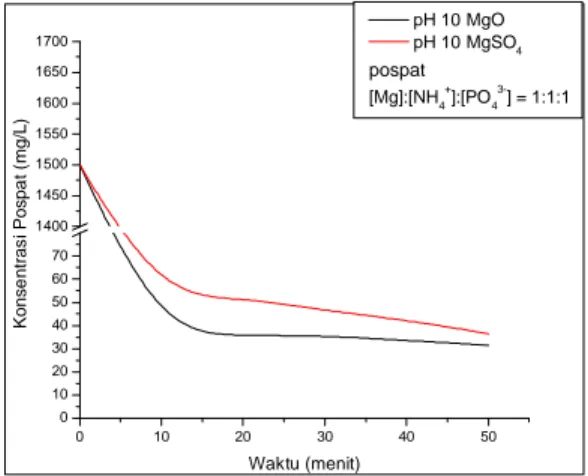
0 10 20 30 40 50 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 Konse ntras i Pospa t (mg/L) Waktu (menit) pH 10 MgO pH 10 MgSO4 pospat [Mg]:[NH4+]:[PO43-] = 1:1:1
Gambar 6 Perbandingan antara pH optimum untuk penyisihan pospat dengan variasi penambahan MgO dan MgSO4
Hasil penelitian penyisihan pospat dengan variasi penambahan MgO, pH optimum terjadi pada pH 10 dengan removal efisiensi sebesar 97,9%, sedangkan penyisihan pospat dengan variasi penambahan MgSO4, pH optimum terjadi pada pH 10 dengan removal efisiensi sebesar 97,57%.
Berdasarkan grafik di atas, dapat dilihat bahwa waktu reaksi optimum pada pH 10 MgO terjadi pada menit ke-20, sedangkan waktu reaksi pada pH 10 MgSO4 terjadi pada menit ke-50. Ini dapat
diartikan bahwa keefektifan MgO untuk penyisihan pospat dari lindi efektif.
Tujuan utama dari penelitian ini adalah untuk penyisihan kadar ammonium yang terdapat dalam lindi, maka kondisi optimum yang digunakan untuk menginvestigasi lindi TPA Benowo adalah pH 9 dengan penambahan variasi penambahan MgO. Pada kondisi tersebut, penyisihan pospat juga dapat berlangsung dibuktikan dengan removal efisiensi pospat lebih besar dari 95% yaitu sebesar 96,74%.
Efek dosis dengan Variasi Penambahan MgO dan MgSO4
Variasi dosis magnesium yang ditambahkan merupakan parameter lain yang digunakan pada penelitian ini. Warmadewanthi dan Liu (2009) mengatakan bahwa seiring dengan peningkatan
molar rasio, maka removal efisiensi juga meningkat. Penambahan dosis magnesium dilakukan pada range pH yang sudah ditentukan yaitu pH 7 sampai pH 10.
Berdasarkan yang sudah dijelaskan, pH optimum untuk penyisihan ammonium menggunakan MgO terjadi pada pH 9. Hasil penambahan dosis Magnesium pada pH 9 menggunakan MgO dapat dilihat pada Tabel 3.
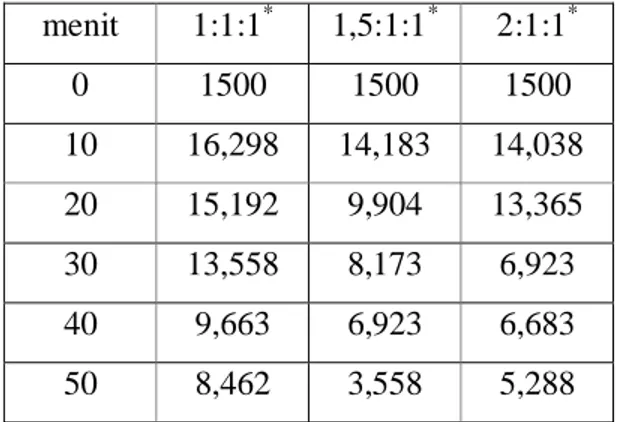
Tabel 3 Hasil Penambahan Dosis Magnesium untuk Penyisihan Ammonium pada pH 9 Menggunakan MgO menit 1:1:1* 1,5:1:1* 2:1:1* 0 1500 1500 1500 10 16,298 14,183 14,038 20 15,192 9,904 13,365 30 13,558 8,173 6,923 40 9,663 6,923 6,683 50 8,462 3,558 5,288
Sumber: hasil analisis laboratorium
Keterangan: * = Perbandingan Molar Rasio [Mg2+]:[NH4+]:[PO43-] (dalam mg/L)
Berdasarkan yang sudah dijelaskan, pH optimum untuk penyisihan pospat menggunakan MgO terjadi pada pH 10. Hasil penambahan dosis Magnesium pada pH 10 menggunakan MgO dapat dilihat pada Tabel 4.
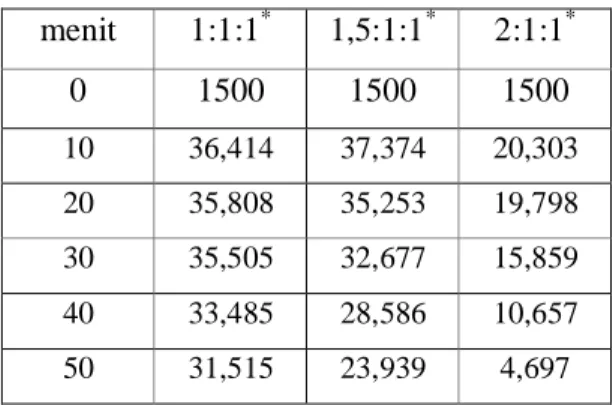
Tabel 4 Hasil Penambahan Dosis Magnesium untuk Penyisihan Pospat pada pH 10 Menggunakan MgO menit 1:1:1* 1,5:1:1* 2:1:1* 0 1500 1500 1500 10 36,414 37,374 20,303 20 35,808 35,253 19,798 30 35,505 32,677 15,859 40 33,485 28,586 10,657 50 31,515 23,939 4,697
Sumber: hasil analisis laboratorium
Keterangan: * = Perbandingan Molar Rasio [Mg2+]:[NH4+]:[PO43-] (dalam mg/L)
Terkait penjelasan pada efek pH, kondisi optimum untuk penyisihan ammonium pada penelitian menggunakan lindi arificial terjadi pada pH 9 dengan variasi penambahan MgO, sehingga pH untuk penyisihan ammonium menggunakan MgSO4 terjadi pada pH 9. Hasil penambahan dosis
Magnesium pada pH 9 menggunakan MgSO4 dapat dilihat pada Tabel 5.
Tabel 5 Hasil Penambahan Dosis Magnesium untuk Penyisihan Ammonium pada pH 9 Menggunakan MgSO4 menit 1:1:1* 1,5:1:1* 2:1:1* 10 64,231 57,356 40,962 20 60,433 55,673 39,327 30 59,279 51,010 38,942 40 55,000 44,856 37,260 50 38,269 39,327 36,490 60 64,231 57,356 40,962
Sumber: hasil analisis laboratorium
Keterangan: * = Perbandingan Molar Rasio [Mg2+]:[NH4+]:[PO43-] (dalam mg/L)
Terkait penjelasan pada efek pH, kondisi optimum untuk penyisihan ammonium pada penelitian menggunakan lindi arificial terjadi pada pH 9 dengan variasi penambahan MgO, sehingga pH untuk
penyisihan pospat menggunakan MgSO4 terjadi pada pH 10. Hasil penambahan dosis Magnesium
pada pH 10 menggunakan MgO dapat dilihat pada Tabel 6.
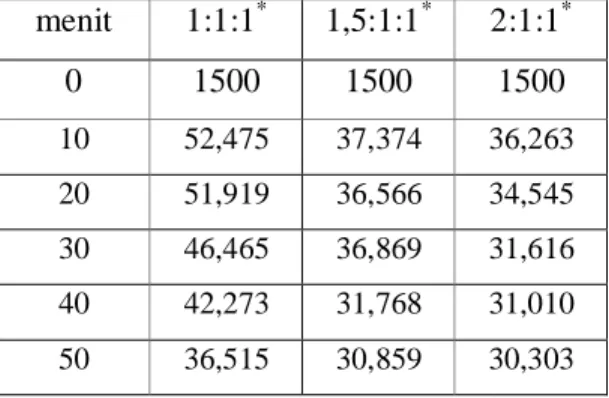
Tabel 6 Hasil Penambahan Dosis Magnesium untuk Penyisihan Pospat pada pH 10 Menggunakan MgSO4 menit 1:1:1* 1,5:1:1* 2:1:1* 0 1500 1500 1500 10 52,475 37,374 36,263 20 51,919 36,566 34,545 30 46,465 36,869 31,616 40 42,273 31,768 31,010 50 36,515 30,859 30,303
Sumber: hasil analisis laboratorium
Keterangan: * = Perbandingan Molar Rasio [Mg2+]:[NH4+]:[PO43-] (dalam mg/L)
Berdasarkan Tabel 3 di atas, terjadi peningkatan removal efisiensi dari perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1:1:1 ke perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 2:1:1 yaitu
dari 98,99% menjadi 99,41%. Berdasarkan Tabel 5 di atas, terjadi peningkatan removal efisiensi seiring dengan peningkatan penambahan dosis magnesium dari 95,97% menjadi 97,38%. Berdasarkan Tabel 4 di atas, terjadi peningkatan removal efisiensi dari 97,61% menjadi 98,68%. Berdasarkan Tabel 6 di atas, terjadi peningkatan removal efisiensi seiring dengan peningkatan penambahan dosis magnesium dari 96,54% menjadi 97,70%.
Waktu Reaksi dengan Variasi Penambahan MgO dan MgSO4 pada pH Optimum
Perbandingan waktu reaksi untuk pH 9 dengan variasi penambahan MgO dan untuk pH 9 dengan variasi penambahan MgSO4 dapat dilihat pada Tabel 7 dibawah.
Tabel 7 Perbandingan Waktu Reaksi untuk Penyisihan Ammonium pada pH 9 dengan Variasi Penambahan MgO dan MgSO4
Perbandingan [Mg2+]:[NH4+]:[PO43] MgO (menit) MgSO4 (menit) 1:1:1 20 50 1,5:1:1 20 50 2:1:1 50 20
Sumber: hasil analisis laboratorium
Berdasarkan tabel di atas, dapat dilihat bahwa waktu reaksi untuk pH 9 dengan variasi penambahan MgO lebih cepat dibandingkan dengan variasi penambahan MgSO4. Ini dapat
disimpulkan bahwa MgO lebih efektif untuk penyisihan ammonium dibandingkan MgSO4.
Perbandingan waktu reaksi untuk pH 10 dengan variasi penambahan MgO dan untuk pH 9 dengan variasi penambahan MgSO4 dapat dilihat pada Tabel 8 dibawah.
Tabel 8 Perbandingan Waktu Reaksi untuk Penyisihan Pospat pada pH 10 dengan Variasi Penambahan MgO dan MgSO4
Perbandingan [Mg2+]:[NH4+]:[PO43] MgO (menit) MgSO4 (menit) 1:1:1 20 50 1,5:1:1 20 20 2:1:1 50 20
Sumber: hasil analisis laboratorium
Berdasarkan tabel di atas, dapat dilihat bahwa waktu reaksi untuk pH 10 dengan variasi penambahan MgO lebih cepat dibandingkan dengan variasi penambahan MgSO4. Ini dapat
Hasil Penelitian pada Lindi TPA Benowo
Kondisi optimum untuk menginvestigasi lindi TPA Benowo adalah waktu reaksi optimum terjadi pada menit ke-20 dengan perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1,5:1:1 dan pH
optimum untuk penyisihan ammonium dan pospat pada pH 9.
Hasil penelitian penyisihan ammonium dan pospat pada Lindi TPA Benowo, Surabaya, dapat dilihat pada Gambar 7 dan Gambar 8 di bawah.
0 10 20 30 40 50 0 10 20 30 40 50 60 70 1400 1450 1500 1550 1600 1650 1700 1750 1800 1850 1900 Konsentrasi Ammonium ( mg/L) Waktu (menit) pH 9 menggunakan MgO [Mg2+]:[NH4+]:[PO43-] = 1.5:1:1
Gambar 7 Grafik penyisihan ammonium pada Lindi TPA Benowo, Surabaya
Berdasarkan grafik di atas, dapat disimpulkan bahwa dengan penambahan magnesium yaitu MgO ke dalam lindi terjadi penyisihan ammonium sebesar 97,83%. Jika dibandingkan dengan penggunaan lindi artificial, removal efisiensi untuk penyisihan ammonium menggunakan lindi TPA Benowo lebih kecil dikarenakan banyaknya material-material yang berbahaya yang terdapat di dalam lindi. Removal efisiensi yang dicapai dengan menggunakan lindi artificial adalah 99,33%.
0 10 20 30 40 50 0 10 20 30 40 50 60 70 80 Konsentrasi Pospat (mg/L) Waktu (menit) pH 9 menggunakan MgO [Mg2+]:[NH4+]:[PO43-] = 1.5:1:1
Gambar 8 Grafik penyisihan pospat pada Lindi TPA Benowo, Surabaya
Berdasarkan grafik diatas, dapat disimpulkan bahwa dengan penambahan magnesium yaitu MgO ke dalam lindi terjadi penyisihan pospat sebesar 69,05%. Ini dibuktikan dengan pengurangan kandungan pospat yang terdapat pada lindi yaitu dari 76,20 mg/L menjadi 23,59 mg/L.
4. KESIMPULAN dan SARAN
Kesimpulan
Kesimpulan yang dapat ditarik dari penelitian yang dilakukan sebagai berikut:
1. Magnesium yang lebih efektif penggunaannya pada penelitian ini untuk penyisihan ammonium dan pospat adalah MgO dikarenakan removal efisiensi ammonium dan pospat yang dihasilkan lebih baik.
2. Penambahan dosis magnesium optimum terjadi pada perbandingan molar rasio [Mg2+]:[NH4+]:[PO43-] 1.5:1:1 pada pH 9. Waktu reaksi pada pH optimum terjadi pada menit
ke-20.
3. Pada lindi artificial removal efisiensi penyisihan ammonium mencapai 99,33% dan removal efisiensi penyisihan pospat mencapai 96,69%.
4. Pada lindi TPA Benowo, Surabaya, removal efisiensi penyisihan ammonium mencapai 97,83% dan removal efisiensi penyisihan pospat mencapai 69,05%.
Saran
Saran untuk studi penyisihan ammonium dengan penambahan magnesium adalah: 1. Perlu dilakukan studi yang sama dengan variasi kecepatan pengadukan (mixing speed). 2. Perlu dilakukan studi analisis kemurnian dari endapan yang terbentuk.
3. Perlu dilakukan studi yang sama untuk menganalisa salinitas yang terdapat dalam lindi TPA Benowo.
5. REFERENSI
1. Burns, R., Moody, L., Walker, F., and Raman, D. (2001). Laboratory and in-situ reductions of soluble phosphorus in swine waste slurries. Environmental Technology, 22, hal.1273–1278. 2. Chimenos, J.M., Fernández, A.I., Hernández, A., Haurie, L., Espiell, F., Ayora, C. (2006).
Optimization of phosphate removal in anodizing aluminium wastewater. Water Research, 40, hal.137-143.
3. Jaffer, Y., Clark, T.A., Pearce, P., Parsons, P.A. (2002). Potential phosphorus recovery by struvite formation. Water Research, 36, hal.1836-1842.
4. Kim, D., Ryu, H.D., Kim, M.S., kim, J., Lee, S.I. (2007). Enhanching struvite precipitation potential for ammonia nitrogen removal in municipal landfill leachate. Journal of Hazardous
Materials, 146, hal.81-85.
5. Li, X.Z., Zhao, Q.L., Hao, X.D. (1999). Ammonium removal from landfill leachate by chemical precipitation. Waste Management, 19, hal.409-415.
6. Stratful, I., Scrimshaw, M.D., Lester, J.N. (2001). Conditions influence the precipitation of magnesium ammonium phosphate. Water Research, 35, hal.4191-4199.
7.
Stratful, I., Scrimshaw, M.D., Lester, J.N. (2004). Removal of struvite to prevent problems associated with its accumulation in wastewater treatment works. Water Environmental Research,76, hal.437–443.
8. Tchobanoglous, G., Hilary, T., Samuel, A.V. (1993). Integrated solid waste management: Engineering principles and managemet issues. McGraw-Hill, Inc, Singapore.
9. Uludag-Demirer, S., Demirer, G.N., Chen, S. (2005). Ammonia removal from anaerobically digested diary manure by struvite precipitation. Process Biochemistry, 40, hal.3667-3674.
10.Wang, J., Burken, J.G., Zhang, X.J., Surampalli, R. (2005). Engineering struvite precipitation: Impact of component-ion molar rations and pH. Journal of Environmental Engineering, 131, hal. 1443-1440.
11.Warmadewanthi, Liu, J.C. (2009). Recovery of phosphate and ammonium as struvite from semiconductor wastewater. Separation Purification Technology, 64, hal.368-373.
12.Wiszniowski, J., Robert, D., Surmacz-Gorska, J., Miksch, K., Weber, J.V. (2006). Landfill leachate treatment methods. Environmental Chemical Letter: a review, 4, hal.51-61.
![Gambar 1 Grafik pengaruh dari pH untuk penyisihan ammonium dengan perbandingan molar rasio [Mg 2+ ]:[NH 4 +](https://thumb-ap.123doks.com/thumbv2/123dok/4550405.3306374/6.918.332.623.135.373/gambar-grafik-pengaruh-untuk-penyisihan-ammonium-perbandingan-molar.webp)
![Gambar 2 Grafik pengaruh dari pH untuk penyisihan pospat dengan perbandingan molar rasio [Mg 2+ ]:[NH 4 +](https://thumb-ap.123doks.com/thumbv2/123dok/4550405.3306374/7.918.333.623.289.523/gambar-grafik-pengaruh-untuk-penyisihan-pospat-perbandingan-molar.webp)
![Gambar 3 Grafik pengaruh dari pH untuk penyisihan ammonium dengan perbandingan molar rasio [Mg 2+ ]:[NH 4](https://thumb-ap.123doks.com/thumbv2/123dok/4550405.3306374/8.918.330.623.447.685/gambar-grafik-pengaruh-untuk-penyisihan-ammonium-perbandingan-molar.webp)
![Gambar 4 Grafik pengaruh dari pH untuk penyisihan pospat dengan perbandingan molar rasio [Mg 2+ ]:[NH 4 +](https://thumb-ap.123doks.com/thumbv2/123dok/4550405.3306374/9.918.334.624.407.633/gambar-grafik-pengaruh-untuk-penyisihan-pospat-perbandingan-molar.webp)