Selection method of curcuminoid extraction to determine the quality of
Temulawak rhizome (Curcuma xanthorrhiza
Roxb
.)
Budhi Santoso*, Syofi Rosmalawati*, Prasetyawan Yunianto**, Anis Herliyati M*, dan Suparjo*
*Balai Pengkajian Bioteknologi, BPPT, **Pusat Teknologi Farmasi dan Medika, BPPT
Kawasan Puspiptek Serpong, Tangerang Selatan 15314, Banten
ABSTRAK
Telah dilakukan ekstraksi kurkuminoid dari rimpang Curcuma xanthorrhiza dengan berbagai perlakuan. Be-berapa parameter ekstraksi seperti ukuran serbuk rimpang, jenis pelarut, suhu, dan lama ekstraksi telah di-tentukan oleh peneliti dengan berbagai konsentrasi kurkuminoid. Sedangkan metode ekstraksi yang cepat dan standar yang diperlukan dalam menentukan kualitas dari rimpang C. xanthorrhiza diperlukan untuk standarisasi bahan baku obat tradisional. Secara umum, penggunaan rimpang Curcuma dalam industri jamu tradisional, ekstraksi dengan air melalui proses perebusan sangat umum digunakan. Penelitian ini dilakukan ekstraksi rimpang Curcuma dengan beberapa jenis pelarut yaitu air, metanol, etil asetat, butanol, dan heksana dengan metode ekstraksi direbus, partisi dan pengocok horisontal. Tingkat senyawa kurkuminoid pada anali-sis HPLC menunjukkan bahwa ekstraksi dengan pelarut etil asetat dengan metode shaker horisontal meng-hasilkan kandungan kurkuminoid tertinggi dibandingkan dengan metode dan pelarut lain. Metode ekstraksi dengan pengocok horisontal selama 60 menit dengan menggunakan heksana dapat digunakan untuk menen-tukan kualitas rimpang Curcuma dengan cepat dan efisien. Hasil analisis HPLC terhadap kadar kurkuminoid dari ekstrak Curcuma dengan metode mendidih sangat rendah, hal itu mungkin karena perubahan kurkumin menjadi senyawa lain seperti asam vanilat dan asam ferulat.
Kata kunci: ekstraksi, temulawak, kurkuminoid, asam vanillin, dan asam ferulat.
ABSTRACT
xanthorrhiza rhizome for the standarization of traditional pharmaceutical raw materials. In general, the use of Curcuma rhizome in traditional herbal medicine industry, extraction with water through the boiling process is very common. This research was conducted on the extraction of Curcuma rhizome with several types of solvents, namely water, methanol, ethyl acetate, butanol, and hexane with extraction method were boiled, partition, and horizontal shaker. The levels of curcuminoid compound on HPLC analysis showed that the ethyl acetat solvent extraction with the horizontal shaker had highest curcuminoid content compare to other methods and solvents. Extraction method by horizontal shaker for 60 minutes using hexane could be used to determine the quality of Curcuma rhizome quickly and efficiently. The results of HPLC analysis of curcuminoid level from Curcuma extract by boiling method was very low, this was possible because of changes in the curcumin into other compounds such as vanillic acid, and ferulic acid.
Key words: extraction, temulawak, curcuminoid, vanillin acid, and ferulic acid.
PENDAHULUAN
Khasiat temulawak sebagai obat telah teruji baik secara empiris maupun klinis. Temulawak telah banyak diteliti mempunyai khasiat sebagai obat beberapa jenis penyakit infeksi maupun kanker. Beberapa aktivitas biologis rimpang temulawak diketahui sebagai antiokidan dan mengatasi inflamasi (Seung dkk., 2005), sebagai immunostimulan (Elfahmi dan Elin, 2009; Ah-Jin dkk., 2007), antikanker, anti jamur candida dan anti bakteri patogen mulut (Park dkk., 2003; Rukayadi dkk., 2006), sebagai komponen pengatur haid dan mengatasi
keputihan (Nurendah dkk., 1996; Sugita, 2008),
sebagai bahan kosmetik (Dzulkarnain dan Wahjoedi, 1996), dan membantu dalam recovery
penyakit (Sembiring dkk., 2006).
Rimpang temulawak banyak digunakan sebagai bahan baku utama obat-obatan karena kandungan senyawa aktifnya. Senyawa utama yang diketahui mempunyai efek sebagai obat diantaranya kurkumin dan xantorizol. Kandungan utama rimpang temulawak terdiri
dari senyawa pati 48-54%, kurkuminoid ±3%,
dan senyawa atsiri 3-12%. Sementara itu senyawa kurkuminoid terdiri atas tiga (3) senyawa utama yaitu, kurkumin ±77%, demetoksikurkumin
±18%, dan bisdemetoksikurkumin ±5%
(Rukayadi dkk., 2006).
Berbagai perlakuan ekstraksi kurkumin dari rimpang temulawak telah dilakukan oleh beberapa peneliti. Metode dua kali ekstraksi dengan parameter ukuran (mesh) rimpang, perbandingan pelarut, perbandingan temperatur, dan lama waktu ekstraksi dapat menghasilkan konsentrasi kurkuminoid yang berbeda-beda
berkisar antara 15-32% w/v (Darusman dkk., 2009; Sugita dkk., 2008; Syafitri dkk., 2008). Metode ekstraksi kunyit atau tumeric
dengan dua kali ekstraksi untuk determinasi kurkuminoid yaitu dengan metode Soxhlet ekstraktor menggunakan heksan selama 30 menit dan kemudian diekstraksi ulang dengan metanol selama 120 menit dinilai cukup efektif (Jayaprakasha dkk., 2002).
turmeric oleoresin (CRTO) menggunakan kolom silika gel yang dielusidasi dengan larutan heksan kemudian menggunakan larutan benzene and etil asetat sebagai solven dalam tiga perbandingan
konsentrasi yaitu, 82:18 v/v ; 70:30 v/v ; 58:42 v/v. Hasil analisis HPLC dari empat aksesi Salem,
Mysore, Erode, dan Balasore menunjukkan bahwa senyawa kurkuminoid tertinggi dicapai oleh
aksesi Salem 9,18% disusul kemudian
masing-masing oleh aksesi Erode 9,11%, Balasore 7,10%, dan Mysore 2,34%. Sedangkan untuk senyawa kurkumin yang tertinggi dicapai oleh Balasore 5,65%, Salem 4,14%, Erode 4,00%, dan Mysore 1,06%. Senyawa demetoksikurkumin
masing-masing adalah Erode 3,36%, Salem 2,88%, Mysore 0,86%, dan 0,83%; dan
bisdemetoksi-kurkumin Salem 2,16%, Erode 1,75%, Balasore 0,62%, dan Mysore 0,42%.
Ekstraksi serbuk temulawak dengan ukuran 40 dan 60 mesh yang diekstrak selama
4, 6, dan 8 jam menggunakan pelarut alkohol 70
%, dibiarkan selama 24 jam, selanjutnya ekstrak disaring dan diuapkan sehingga dihasilkan ekstrak kental. Hasil analisis kurkumin menggunakan HPLC, menunjukkan bahwa kadar kurkumin yang terdapat dalam ekstrak kental
berkisar antara 1,34-2,88%. Kadar kurkumin
tertinggi dihasilkan pada kehalusan serbuk 40 mesh dan ekstraksi selama 4 jam (Sembiring dkk., 2006).
Pada umumnya, pemanfaatan rimpang temulawak di industri jamu tradisional, dilakukan ekstraksi dengan menggunakan air melalui proses perebusan (digodog). Sementara itu, proses pemanasan dapat merubah struktur dan komponen bioaktif pada kurkumin, kapsaisin dan
piperin dari kunyit (Curcuma longa), red pepper (Capsicum annuum) dan black pepper (Piper nigrum) (Suresh dkk., 2009). Hasil penelitian Suresh (2009) membuktikan bahwa pemanasan dapat merubah struktur kimia kurkumin menjadi senyawa-senyawa lain yaitu asam ferulat, vanillin, dan asam vanilat. Analisis profil kandungan senyawa kurkumin dari ekstrak temulawak yang direbus perlu dilakukan untuk mengetahui apakah terjadi penurunan atau perubahan dari senyawa kurkumin.
Determinasi dan kuantifikasi kurkminoid (kurkumin, demetoksikurkumin, dan bisdemetoksikurkumin) menggunakan HPLC telah dilakukan oleh beberapa peneliti, namun masih menghasilkan konsentrasi yang berbeda-beda. Beberapa faktor yang dapat mempengaruhi diantaranya sumber tanaman, metode ekstraksi dan analisis, serta keragaman genetiknya.
Sementara itu, kebutuhan metoda ekstraksi yang cepat dan baku diperlukan dalam menentukan kualitas rimpang temulawak untuk standarisasi bahan baku obat. Untuk mengetahui kandungan senyawa aktif kurkuminoid dari rimpang temulawak diperlukan metode analisis kimia yang efektif dan efisien, sehingga dapat menentukan kandungan kurkuminoid dan xanthorrhizol lebih cepat dan akurat. Pada penelitian ini telah dilakukan ekstraksi rimpang temulawak dengan beberapa jenis pelarut yaitu air dengan cara direbus; metanol, etil asetat, butanol dan heksan dengan metode ekstraksi
METODE PENELITIAN
Penelitian dilaksanakan di Laboratorium Balai Pengkajian Bioteknologi (Biotek), Badan Pengkajian dan Penerapan Teknologi (BPPT), dari bulan April-Juli 2010. Rimpang temulawak yang digunakan merupakan aksesi temulawak Bogor. Pelarut yang digunakan terdiri dari heksan (teknis), etil asetat (teknis), butanol (teknis), metanol (teknis), air, acetonitril HPLC grade (Merck), asam format (Merck), standar HPLC kurkuminoid (Supelco), dan standar HPLC kurkumin (Sigma). Sedangkan peralatan yang digunakan adalah pisau, baki pengering, oven, blender, ayakan, tabung sentrifus PPCO 500 ml, tabung konsentrator, horizontal shaker, sentrifus Beckman, botol sampel 500 ml, kertas saring,
rotary evaporator, konsentrator, HPLC Alliance 2695 (Waters) with Photodiode Array Detector
2996 (Waters) dengan kolom Symmetry C18 5
µm, 4,6 mm x 250 mm (Waters), HPLC (Waters),
kolom Eurospher C-18 5 µm, 4,6 mm x 250 mm,
detector UV-Vis 254 nm.
Pembuatan simplisia
Rimpang temulawak dicuci dengan air dan ditiriskan. Rimpang diiris tipis menggunakan pisau atau irisan untuk membuat kripik. Irisan rimpang ditimbang dan ditempatkan pada baki pengeringan dalam oven suhu 40oC dan
dikeringkan sampai diperoleh berat konstan menjadi simplisia kering. Rendemen kering simplisia temulawak diukur dengan menghitung selisih matematis perbedaan berat basah dan berat kering dibandingkan dengan berat basahnya. Simplisia yang sudah kering digiling dengan menggunakan blender dan diayak dengan ayakan mesh 24 (±700 µm). Kadar air
serbuk temulawak diukur menggunakan alat
Moisture Analyzer-AND seri MS-70.
Ekstraksi dengan cara partisi
Serbuk temulawak sebanyak 10 g dimasukkan ke dalam tabung erlenmeyer kemudian ditambahkan pelarut metanol sebanyak 500 ml dan dimaserasi dengan
menggunakan rotary shaker selama 24 jam.
Selanjutnya disentrifus dengan kecepatan 6.000 rpm selama 15 menit kemudian supernatan dipisahkan dan dievaporasi sampai dihasilkan ekstrak kering. Ekstrak tersebut ditambahkan air dan etil asetat masing-masing sebanyak 250 ml serta dipisahkan menggunakan corong pisah sehingga diperoleh fraksi etil asetat dan fraksi air. Fraksi etil asetat dievaporasi sampai diperoleh ekstrak etil asetat kering, kemudian ditambahkan pelarut metanol dan heksan masing-masing sebanyak 250 ml serta dilakukan pemisahan. Masing-masing fraksi dievaporasi sehingga diperoleh ekstrak kering metanol (etil asetat) dan ekstrak kering heksan. Sementara ekstrak air tersebut di atas ditambahkan pelarut butanol sebanyak 250 ml dan dipisahkan menjadi fraksi butanol dan fraksi air. Fraksi butanol dievaporasi sehingga diperoleh ekstrak kering butanol.
Ekstraksi kurkuminoid dengan beberapa pelarut dengan horizontal shaker
Kemudian dipisahkan supernatan dan pelet dengan menampung supernatan pada botol sampel 500 ml berwarna coklat. Ekstraksi pelet dilakukan ulangan seperti pada tahap sebelumnya. Hasil ekstraksi digabungkan dan kemudian dievaporasi dengan menggunakan
rotary evaporator (rotavapor) pada suhu 45oC
sampai masing-masing pelarutnya menjadi 5 ml dan dipindahkan ke dalam tabung konsentrator serta dilakukan konsentrasi pada konsentrator sampai dihasilkan kristal kurkuminoid. Kristal kompleks kurkuminoid kemudian dipindahkan ke dalam tabung sentrifus dan ditimbang berat kristal serta disimpan dalam lemari es sebagai sediaan injeksi HPLC.
Ekstraksi kurkuminoid dengan cara direbus
Serbuk temulawak masing-masing sebanyak 5 g dimasukkan ke dalam beaker glass
500 ml kemudian ditambahkan air sebanyak 250 ml dan dididihkan di atas hotplate stirer sampai dengan sisa air dalam beaker glass tinggal 125 ml. Ekstrak rebusan selanjutnya disaring dengan kertas saring, disentrifus dan supernatannya ditampung untuk dianalisa kadar senyawa kurkuminoid dengan HPLC.
Analisa HPLC
HPLC yang digunakan yaitu HPLC Alliance 2695 (Waters) with Photodiode Array Detector
2996 (Waters) dengan column Symmetry C18
5 µm, 4,6 mm x 250 mm (Waters). Elusi secara
isokratik dengan eluen H2O: asam format:
asetonitril, dengan perbandingan 49,95%:
0,05%: 50%, dan flow rate: 1,2 ml/min,
pada suhu kamar dan deteksi pada panjang gelombang UV 425 nm. Standar kurkuminoid yang digunakan dari Sigma Aldrich cat. No.
C7727, kadar kurkumin 10 ppm, dengan volume injeksi sebanyak 10 µl. HPLC (Waters), kolom
yang digunakan Eurospher C-18, 250 x 0.46
mm, detector UV-Vis 254 nm, fase gerak dengan eluen TFa 0,1% : HCN secara gradien, kecepatan
gerak 1 ml/min, volume injeksi 10 µl, standar kurkuminoid yang digunakan dari Sigma 80%
(kurkumin max. 70%, demetoksikurkumin 19%, dan bisdemetoksikur-kumin 5%).
HASIL DAN PEMBAHASAN
Analisis kualitatif ekstrak temulawak Bogor dilakukan menggunakan TLC. Hasil analisis TLC, pelarut etil asetat dan air dengan cara direbus dapat mengekstrak ketiga senyawa kurkuminoid yaitu kurkumin, demetoksikurkumin, dan bisdemetoksikurkumin. Sementara itu pelarut heksan dan butanol hanya dapat mengekstraksi senyawa kurkumin dan demetoksikurkumin seperti terlihat pada Gambar 1 Pelarut etil asetat menghasilkan spot yang paling tebal dibanding dengan pelarut heksan, air dan butanol. Pada dasarnya butanol juga merupakan pelarut semi polar yang cukup baik, ada kemungkinan konsentrasi bisdemetoksikurkumin yang terambil terlalu kecil sehingga tidak terdeteksi dalam analisis TLC.
pelarut heksan hanya dapat mengekstraksi 2 senyawa kurkuminoid yaitu demetoksikurkumin dan kurkumin. Hal ini dapat dilihat pada Tabel 2, dimana meskipun pelarut heksan dapat mendeteksi senyawa kurkumin tetapi dalam jumlah kecil dan hanya mendeteksi senyawa demetoksikurkumin dalam jumlah yang sangat kecil serta tidak dapat mendeteksi adanya senyawa bisdemetoksikurkumin.
Gambar 1. Analisis TLC ekstrak temulawak Bogor yang diekstrak dengan air, heksan, etil asetat, dan butanol
(a)
(b)
(c)
(d)
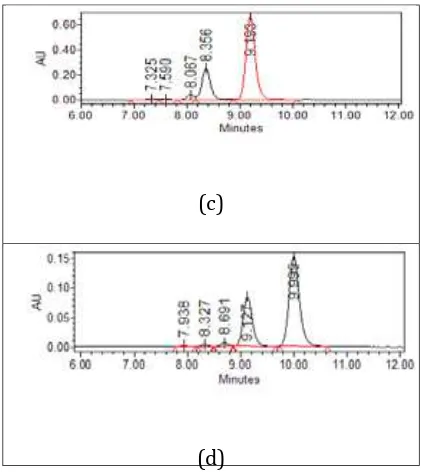
Gambar 2. Kromatogram HPLC sampel temulawak aksesi Bogor yang diekstrak dengan menggunakan beberapa jenis pelarut etil asetat (a), butanol (b), metanol (c), dan air dengan cara direbus (d)
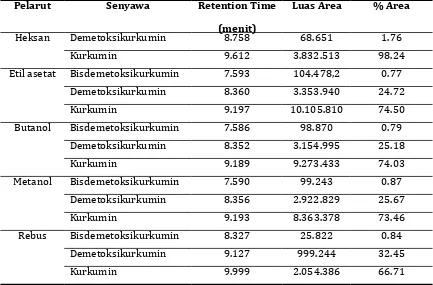
Tabel 1. Analisis senyawa kurkuminoid dari temulawak asal Bogor yang diekstrak dengan beberapa jenis pelarut
Pelarut Senyawa Retention Time
(menit)
Luas Area % Area
Heksan Demetoksikurkumin 8.758 68.651 1.76
Kurkumin 9.612 3.832.513 98.24
Etil asetat Bisdemetoksikurkumin 7.593 104.478,2 0.77 Demetoksikurkumin 8.360 3.353.940 24.72
Kurkumin 9.197 10.105.810 74.50
Butanol Bisdemetoksikurkumin 7.586 98.870 0.79 Demetoksikurkumin 8.352 3.154.995 25.18
Kurkumin 9.189 9.273.433 74.03
Metanol Bisdemetoksikurkumin 7.590 99.243 0.87 Demetoksikurkumin 8.356 2.922.829 25.67
Kurkumin 9.193 8.363.378 73.46
Rebus Bisdemetoksikurkumin 8.327 25.822 0.84 Demetoksikurkumin 9.127 999.244 32.45
Kurkumin 9.999 2.054.386 66.71
Perebusan temulawak dengan air dapat mengekstrak ketiga senyawa kurkuminoid namun konsentrasinya paling rendah dibanding ketiga pelarut lainnya, dapat dilihat pada Tabel 1. Pada Gambar 2d menunjukkan adanya 2
peak yang merupakan kromatogram peak dari senyawa demetoksi kurkumin dan kurkumin.
Hasil analisis ekstrak temulawak dengan beberapa pelarut dengan cara partisi, menunjukkan bahwa pelarut etil asetat dan butanol dapat mengekstrak kurkuminoid lebih tinggi dibanding pelarut yang lainnya. Pelarut butanol dapat mengekstrak senyawa kurkuminoid lebih tinggi dibanding pelarut etil asetat. Sedangkan pada ekstraksi dengan
Tabel 2. Persentase (w/w) komposisi kurkuminoid berdasarkan jenis pelarut dan cara ekstraksi aksesi Bogor dengan HPLC*
Ekstrak
Sampel
Kurkumin Demetoksi
kurkumin
Bisdemetoksi-kurkumin
Total
Kurkuminoid
Heksan 0,212 0,004 0,000 0,216
Etil asetat 5,591 1,856 0,058 7,505
Butanol 5,131 1,746 0,055 6,932
Metanol 4,627 1,617 0,055 6,299
Rebus 0,568 0,276 0,007 0,851
*Rata-rata dari injeksi duplo
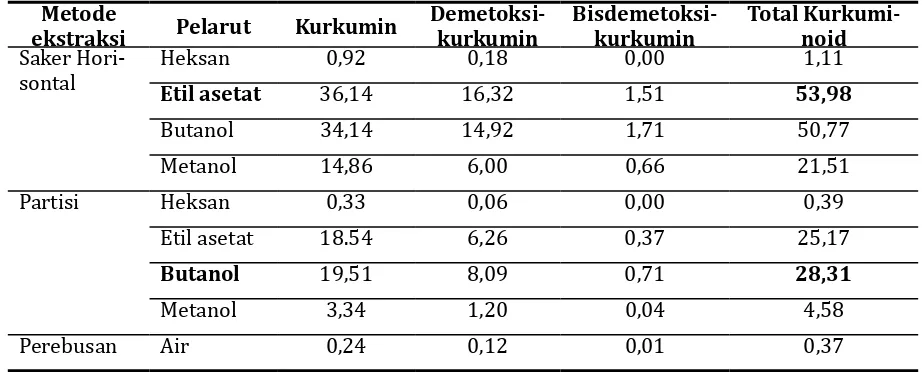
Tabel 3. Persentase (w/v) komposisi kurkuminoid berdasarkan ekstraksi saker horisontal, partisi, dan pere -busan dari temulawak aksesi Bogor dengan HPLC*
Metode
ekstraksi Pelarut Kurkumin
Demetoksi-kurkumin
Bisdemetoksi-kurkumin
Total Kurkumi-noid
Saker Hori-sontal
Heksan 0,92 0,18 0,00 1,11
Etil asetat 36,14 16,32 1,51 53,98
Butanol 34,14 14,92 1,71 50,77
Metanol 14,86 6,00 0,66 21,51
Partisi Heksan 0,33 0,06 0,00 0,39
Etil asetat 18.54 6,26 0,37 25,17
Butanol 19,51 8,09 0,71 28,31
Metanol 3,34 1,20 0,04 4,58
Perebusan Air 0,24 0,12 0,01 0,37
*Rata-rata dari injeksi duplo
Kadar kurkumin hasil analisa HPLC dalam sampel temulawak asal Bogor berkisar
5% (w/v) sampel kering dalam bentuk serbuk
kering temulawak. Sementara itu kadar kurkumin yang diperoleh dengan cara perebusan
mempunyai kadar 0.5% (w/v). Suresh (2009)
dengan mengunakan sampel Curcuma longa
membuktikan bahwa pemanasan dapat merubah struktur kimia kurkumin menjadi senyawa-senyawa lain seperti misalnya ferulic acid,
vanillin, dan vanillic acid.
Sehubungan dengan hal itu maka dilakukan profiling HPLC ekstrak temulawak (Curcuma xanthorriza) yang telah mengalami
proses perebusan dengan air. Profiling
senyawa ekstrak temulawak hasil perebusan menggunakan HPLC dapat dilihat pada Gambar 5. Selanjutnya juga dilakukan profiling dari ketiga standar vanillic acid, vanillin, ferulic acid
Gambar 3. Profil kromatogram temulawak dengan ekstraksi direbus
Gambar 4. Profil standar vanillic acid (1), vanillin (2), ferulic acid (3) dan total kurkuminoid (4)
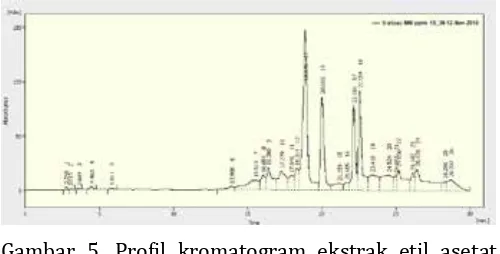
Gambar 5. Profil kromatogram ekstrak etil asetat temulawak 500 ppm
Sebagai pembanding digunakan profil dari ekstrak hasil maserasi etil asetat temulawak (Gambar 5). Setelah diperoleh profil yang terbaik dari masing-masing sampel, maka kemudian dilakukan profil gabungan pada ekstrak temulawak hasil rebusan untuk melihat apakah ada perubahan munculnya senyawa
vanillin, vanillic acid atau ferulic acid. Profiling
gabungan ekstrak hasil rebusan dilakukan pada
konsentrasi 19.800 ppm, karena kadarnya yang
sangat rendah, agar mudah untuk dibandingkan dengan standar vanillin 200 ppm, dan ekstrak etil asetat 500 ppm.
Gambar 6. Profil gabungan hasil perbandingan ketiga profil standar (vanillic acid, vanillin dan ferulic acid) dengan ekstrak temulawak seduh dan etil asetat
Dari hasil perbandingan ketiga profil standar (vanillic acid, vanillin dan ferulic acid) dengan ekstrak temulawak seduh dan etil asetat (Gambar 6), tampak bahwa pada ekstrak etil asetat tidak terdapat perubahan atau munculnya ketiga senyawa (vanillic acid, vanillin dan ferulic acid). Sedangkan jika dibandingkan antara ekstrak seduhan dengan ekstrak etil asetat terdapat perbedaan yaitu adanya puncak pada waktu retensi 2,7 menit di ekstrak seduhan, dimana pada ekstrak etil asetat tidak ada, meskipun belum diketahui jelas senyawa apa puncak tersebut. Demikian halnya puncak pada menit
4,63 dan 5,8 pada ekstrak seduhan, meskipun
merubah senyawa aktif dari temulawak sehingga hasil pada analisis HPLC senyawa kurkuminoid ekstrak rebusan temulawak sangat rendah.
KESIMPULAN
Metode ekstraksi dengan cara horizontal shaker selama 60 menit menggunakan pelarut etil asetat untuk senyawa Kurkuminoid dapat digunakan untuk menentukan kualitas rimpang temulawak secara cepat dan efisien. Pelarut etil asetat merupakan pelarut yang dapat mengekstrak ketiga senyawa kurkuminoid dengan hasil yang paling tinggi dibanding ketiga pelarut lainnya pada ekstraksi dengan cara maserasi beberapa jenis pelarut. Hasil analisis kadar senyawa kurkuminoid pada HPLC ekstrak temulawak dengan cara perebusan sangat rendah, hal ini dimungkinkan karena adanya perubahan senyawa kurkumin menjadi senyawa lain seperti vanillin acid dan ferulic acid. Penelitian lebih lanjut guna mengetahui efek perebusan temulawak dan adanya degradasi senyawa kurkumin menjadi beberapa senyawa lain perlu dilakukan.
TERIMA KASIH
Penelitian ini disponsori oleh Kementrian Riset dan Teknologi melalui program bidang riset terapan, Insentif Riset SiNas.
DAFTAR PUSTAKA
Darusman, LK., Djauhary EPK., Priosoeryanto BP., Nurcholis W., Rohaeti E., Rahminiwati M., Utami Dyah S., and Rafi M. 2009. Efficacy and Standarization of Temulawak (Curcuma xanthorrhiza Roxb.). Proceeding.
Indonesian Temulawak Expert Meeting, Jakarta, Indonesia. Monday 29 th, 2009 Dzulkarnain, B. dan Wahjoedi B. 1996. Informasi
Ilmiah Kegunaan Kosmetika Tradisional.
Majalah Cermin Dunia Kedokteran, 108:
21-26
Elfahmi dan Yulinah E. 2009. Phytochemistry of Curcuma xanthorrhiza. Proceeding.
Indonesian Temulawak Expert Meeting, Jakarta, Indonesia. Monday 29 th, 2009 Jayaprakasha GK., Rao LJM., and Sakariah
KK. 2002. Improved HPLC Method for The Determination of Kurkumin, Demetoksikurkumin, and Bisdemetoksi-kurkumin. Journal of Agricultural and Food Chemistry. 50: 3668-3672
Kim Ah-Jin, Yeon-O Kim, Jae Seok Shim, and Jae-Kwan Hwang. 2007. Immunostimulating Activity of Crude Polysaccharide Extract Isolated from Curcuma xanthorrhiza Roxb.
Bioscience, Biotechnol. Biochem, 71(6):
1428-1438.
Seung LC., Jin D-Q., Mok H., Oh SJ., Lee JU., Hwang JK., Ha I. and Han J-S. 2005. Antioxidant and Anti inflammatory Activities of Xanthorrhizol in Hippocampal Neurous & Primary Cultured Microglia. Journal of Neuroscience Research, 82: 831-836
Nurendah P., Praswanto S., Dzulkarnain B., dan Sundari D. 1996. Informasi Penelitian komponen Jamur Pengatur Haid. Majalah Cermin Dunia Kedokteran, 108: 11-17
Park J-H., Kim M-J., Park K-K., Kim H-O., Hwang J-K., and Chung W-Y. 2003. Journal of Korean Association of Cancer Prevention, 8(2):
Yaya R., Yong D., and Hwang J-K. 2006. Journal of Antimicrobial Chemotheraphy, 57: 1231-1234
Sembiring BB., Ma’mun Edi IG. 2006. Pengaruh kehalusan bahan dan lama ekstraksi terhadap mutu ekstrak temulawak (Curcuma xanthorrhiza Roxb.). Bul. Littro,
XVII(2): 53-58.
Sugita P., Bambang S., Imam P., Kamilah HA.
2008. Curcumin content improvement of
ethanol extract of temulawak (Curcuma xanthorrhiza Roxb.) using liquid-liquid extraction. Proceeding. The first International Symposium on Temulawak (Curcuma xanthorrhiza Roxb.), Bogor. Mei
27-28, 2008
Suresh, D., K.N. Gurudutt, Krishnapura Srinivasan. 2009. Euro. Food. Res. Technol, 228: 807-812
Syafitri UD., Darusman LK. and Supriadi D. 2008. Extraction optimization of temulawak (Curcuma xanthorrhiza Roxb.) curcuminoids.
Oral presentation on The first International Symposium on Temulawak, Bogor. Mei