LAPORAN TETAP PRAKTIKUM
KIMIA TERAPAN
Disusun oleh :
1. Alvin Prayoga (061540411906) 2. Anggy Permatasari (061540411907) 3. Idham Satriawan (061540411913) 4. M. Qurais Akbar (061540411914) 5. M. Adhi Pranata (061540411916) 6. Saidina Ali (061540412259) 7. Tia Hanifah A (061540412260) 8. Tri Kurniawan (061540412261) 9. Yossy Karlina (061540412262)
Instruktur : Lety Trisnaliani, S.T, M.T
Judul Percobaan : Analisis Air (Penentuan Kesadahan/ Ion Ca2+) Jurusan : Teknik Kimia Prodi S1 Terapan Teknik Energi
Kelas/Kelompok : 1 EGD/ 1
ANALISIS AIR (PENENTUAN KESADAHAN/ION Ca
2+)
I. TUJUAN PERCOBAAN
Mampu melakukan penentuan kesadahan pada sampel air dengan metoda titrasi kompleks.
II. PERINCIAN KERJA
Standardisasi larutan EDTA
Penentuan kesadahan ( ion Ca2+)
III. ALAT –ALAT YANG DIGUNAKAN
Labu ukur 250ml, 500 ml 2
Erlenmeyer 250 ml 6
Buret 50 ml 2
Gelas kimia 100 ml 4
Larutan buffer pH 10
V. GAMBAR ALAT (TERLAMPIR)
VI. DASAR TEORI
Kesadahan dalam air terutama disebabkan oleh ion-ion Ca2+ dan Mg2+, juga oleh Mn2+, Fe2+, dan semua kation bermuatan dua. Air yang kesadahannya tinggi biasanya terdapat paada air tanah di daerah yang bersifat kapur, di mana Ca2+ dan Mg2+ berasal.
Air sadah mengakibatkan konsumsi sabun lebih tinggi, karena adanya hubungan kimiawi antara ion kesadahan dengan dengan molekul sabun menyebabkan sifat sabun/deterjen hilang. Kelebihan ion Ca2+ serta ion CO32-(salah satu ion alkalinity) mengakibatkan terbentuknya kerak pada dinding pipa yang disebabkan oleh endapan kalsium karbonat CaCO3. Kerak ini akan mengurangi penampang basah dari pipa dan menyulitkan pemanasan air dalam ketel.
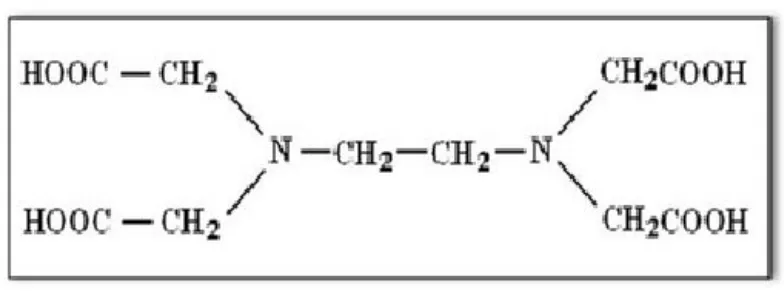
Kesadahan air dapat ditentukan dengan titrasi langsung dengan titran asam etilen diamin tetra asetat (EDTA) dengan menggunakan indicator Eriochrome Black T atau Calmagite. Sebelumnya EDTA distandardisasi dengan larutan standar kalsium, biasanya standar primer yang digunakan adalah CaCO3.
Etilen Diamin Tetra Asetat:
logam dengan pertolongan kedua nitrogen dan empat gugus karboksil. Misalnya dengan ion kobalt,membentuk kompleks EDTA oktahidrat.
Pada titrasi ini indicator yang digunakan adalah indicator metalokromik yang merupakan senyawa organic berwarna, yang membentuk kelat dengan ion logam. Khelatnya mempunyai warna yang berbeda dengan warna indicator bebasnya.
Struktur Eriochrome Black T :
VII. PROSEDUR PERCOBAAN 7.1 Pembuatan larutan EDTA
Menimbang 1 gram dinatrium dihidrogen EDTA dihidrat dan 0,025 gram MgCl2.6H2O
Memasukkan ke dalam gelas kimia 100 ml,melarutkan dalam air
Memindahkan ke dalam labu ukur 250 ml,menambahkan air sampai 250 ml. Menghomogenkan.
7.2 Pembuatan larutan buffer
Melarutkan 3,375 amonium klorida dalam 28,5 ml amonium hidroksida pekat Mengencerkan sampai 50 ml dalam gelas ukur 50 ml. pH larutan sedikit lebih
besar dari 10.
7.3 Pembuatan larutan baku CaCO3
Menambahkan setetes demi setetes HCl 1:1 sampai berhenti bergelegak dan larutan menjadi jernih
Mengencerkan sampai garis tanda, mengocok sampai homogen.
7.4 Standardisasi larutan natrium EDTA
Memipet 25 ml larutan kalsium karbonat ke dalam erlenmeyer 250 ml Menambahkan 5 ml larutan buffer
Menambahkan 5 tetes indiaktor eriochrom black T
Menitrasi dengan larutan EDTA, hingga warna merah anggur berubah menjadi biru. warna merah harus lenyap sama sekali
7.5 Penentuan kesadahan
Memipet 25 ml air sampel dalam Erlenmeyer 250 ml Menambahkan 1 ml buffer
Menambahkan 5 tetes indicator
VIII. DATA PENGAMATAN
8.1 Standardisasi Larutan EDTA No
. gram analit (CaCO3) Volume titran (EDTA) Perubahan warna
1 0,2 gr 17,5 ml
25 ml 1 ml Merah anggur
menjadi biru Normalitas EDTA secara teori
= 0,0214 mek/ml
Normalitas EDTA secara prakek Volume Rata-rata Titran : 17,5 ml
1) mg CaCOBE CaCO33 = Volume EDTA x N.EDTA
0,2gr x1000mggr x25025mlml
100,09mg/mol
2mek/mol
= 17,5 ml x N EDTA
N EDTA=875,787520ml mek/ml
N EDTA=0,022mek/ml
% Kesalahan = N.teori – N.praktek x 100 N.teori
= 0,02 14 N – 0,0 22 N x 100 0,0214 N
= 2,8 %
9.2 Penentuan kesadahan a) Sampel 1
Percobaan 1,2 & 3 ; V.EDTA Rata-rata = 1 ml
mg CaCO3 = V EDTA X N EDTA X BE CaCO3
= 1 ml X 0,022 mek/ml X 100,09mg/mol
2mek/mol
= 1 ml X 0,022 mek/ml X 50,045 mg/mek
= 1,10099 miligram
mg CaCO3/ liter atau (ppm) = 1000ml/liter . mg contoh
= 1000
mg CaCO3/ liter atau (ppm) = 1,651485 miligram X 1000ml/liter
X. PERTANYAAN
1. Apakah yang dimaksud deengan kompleksometri?
Kompleksometri adalah jenis titrasi dimana titran dan titrat saling mengkompleks. Jadi membentuk hasil berupa kompleks. Titrasi kompleksometri adalah salah satu metode kuantutatif dengan memanfaatkan reaksi kompleks antara ligan dengan ion logam utamanya, yang umum adalah EDTA.
2. Jelaskan istilah-istilah berikut:
a. Kompleks inert
Suatu kompleks yang mengalami subtitusi ngugus ligan yang sangat lambat disebut juga non labil.
b. Kelat logam
Cincicn heterositik yang terbentuk oleh interajsi suatu ion logam dengan dua atau lebih gugus fungsional dalam logam
c. Penopengan
Pengguanaan suatu reagensia utnuk membentuk suatu kompleks stabil dengan sebuah ion yang tanpa pembentukan itu ion akan menyangga reaksi yang diingnkan.
d. Ligan heksidentat
Ligan yang mengadung enam buah atom donor pasangan elektro yang emlalui kedua atom N dan empat atom O.
e. Bilangan koordinasi
Banyakanya ikatan yang dibentuk oleh suatu atom sentral dalam suatu kompleks.
Diketahui: gr sampel= 0,2428 gram Volume sampel = 250 ml Volume alikot = 50 ml Volume EDTA =42,74 ml Berat moilekul=100,09 gr/mol Ditanya: Molekul EDTA =…?
Jawab:
Gr CaCO3 = gram alikot V CaCO3 V alikot 0,2428 gram = gram alikot
250 ml 50 ml
Gram alikot = 0,04856 gram
Gram alikot = V EDTA X M EDTA BM CaCO3
0,04856 gr = 0,04272 liter X M EDTA 100,09 gr/mol
XI. ANALISIS DATA
Pada percobaan ini dapat dianalisis bahwa untuk menentukan kesadahan pada suatu sampel perlu melakukan bebarapa tahapan. Awalnya kami melakukan standarisasi larutan EDTA dengan larutan std primer CaCO3. Kemudian melakukan penentuan kesadahan.
Pada percobaan standarisasi, CaCO3 bertindak sebagai analit sedangkan larutan EDTA sebagai titran. Pertama kita membuat larutan EDTA untuk sebagai titran, kita menimbang 2 gram EDTA dan MgCl2 6H2O 0,05 gr masukkan kedalam gelas kimia , setelah itu pindahkan ke dalam labu ukur 500 ml. tambahkan air sampai tanda batas 500 ml serta homogenkan. Setelah itu kita membuat larutan buffer dengan menimbang 6,75 gram ammonium kloria serta menambahkan 57 ml ammonia pekat di lemari asam , kemudian masukkan ke dalam labu ukr 100 ml, setelah itu tambahkan aquadest smpai tanda batas. Setelah larutan EDTA dan Buffer dibuat , kita membuat larutan baku CaCO3 pertama kita menimbang CaCO3 sebanyak 0,2 gram yang murni telah dikeringkan didalam oven 100oC, kemudian masukkan ke dalam labu ukur tambahkan 50 ml aquadest, tambahkan setetes demi tetes 1 : 1 sampai larutan menjadi jernih. Kemudian encerkan sampai tanda batas serta homogenkan.
Setelah larutan diatas telah dibuat semua , kita menstandarisasi larutan CaCO3. Larutan CaCO3 dipipet sebanyak 25 ml kemudian menambahkan 2,5 ml larutan buffer dan menambahkan 3 tetes indicator EBT. Kemudiam melakukan titrasi dari titran ke analit. Saat proses titrasi, terjadi perubahan warna yang semula berwarna merah anggur menjadi biru. Perubahan warna tersebut terjadi pada volume rata-rata 20,5 ml. Titrasi ini dilakukan sebanyak 3 kali. Normalitas EDTA yang didapat dari hasil standardisasi yaitu 0,022 mek/ml dengan persen kesalahan 2,8%. Kesalahan tersebut dapat terjadi karena beberapa hal, yaitu :
- Alat yang digunakan kurang bersih
- Zat yang digunakan telah terkontaminasi
- Ketidaktepatan dalam pengukuran dan penimbangan
- Ketidaktepatan dalam pembuatan larutan
- Ketidaktelitian dalam menitrasi
erlenmeyer kemudian menambahkan 1ml larutan buffer dan 5 tetes indicator EBT, dilakukan 3 kali percobaan setiap sampel. Kemudian melakukan titrasi dari titrannya yaitu larutan EDTA ke analitnya yaitu sampel yang diuji tersebut. Volume rata-rata yang didapat dari hasil titrasi sampel 1 yaitu 1 ml, sehingga didapatkan Kesadahan pada sample 1 sebesar 44,0396 mg/liter atau ppm. Sedangkan sampel 2 didapat volume rata-rata sebesar 1,5 ml , sehingga didapatkan Kesadahan pada sample 2 sebesar 66,0594 mg/liter atau ppm dan sampel 3 didapat volume rata-rata sebesar 1ml, sehingga didapatkan Kesadahan pada sample 3 sebesar 44,0396 mg/liter atau ppm.
XII. KESIMPULAN
Kesadahan dalam air terutama disebabkan oleh ion-ion Ca2+ dan Mg2+, juga oleh Mn2+, Fe2+, dan semua kation bermuatan dua.
Kesadahan air dapat ditentukan dengan titrasi langsung dengan titran asam
etilen diamin tetra asetat (EDTA) dengan menggunakan indicator Eriochrome Black T
Adapun hasil dari percobaan didapat sebagai berikut :
Pada standardisasi larutan EDTA
- Volume titran = 17,5 ml
- Normalitas EDTA = 0,022 N dengan persen kesalahan 2,8 % Penentuan kesadahan
- Sampel 1 , Volume titran = 1 ml kesadahan = 44,0396 mg/liter atau ppm
- Sampel 2, Volume titran = 1,5 ml kesadahan = 66,0594 mg/liter atau ppm
- Sampel 3, Volume titran = 1 ml
XII. DAFTAR PUSTAKA
Jobsheet Penuntun Praktikum Kimia Terapan. 2015. “Titrasi Asam Basa”. Politeknik Negeri Sriwijaya
GAMBAR ALAT (LAMPIRAN)
Buret Erlenmeyer Labu ukur
Neraca Analitik Corong Botol Aquades
Spatula Pipet Tetes Pengaduk
Gelas kimia
Bola Karet
Pipet Ukur