Tekanan Uap Air di bawah 100°c Panas Molar dari Penguapan (M-4)
Riska Tri Handayani(140310150041)*, Nuraini Nafisah (140310150081)
Selasa , 15.00 – 17.00 WIB 30 April 2018
Asisten : Intan Oktaviani
Abstrak
Dalam kehidupan seharihari ketika sering menemui perubahan wujud zat salah satu contohnya adalah perubahan wujud zat cair menjadi uap atau yang disebut dengan penguapan. Proses penguapan dipengaruhi oleh temperatur dan tekanan sebagaimana pada persamaan claussiusclapeyron yang menghubungakan tekanan dan temperatur untuk menyelidiki tekanan uap air dibawah 100°c. Oleh karena itu pada percobaan ini bertujuan untuk menyelidiki tekanan uap air pada 4085°c serta menentukan nilai ratarata untuk penguapan panas dengan melakukan demineralisasi air setelah itu dimasukan ke dalam labu 3 leher lalu memanaskannya kembal sehingga didapat data temperatur dan tekanan yang nilainya memiliki hubungan yang sebanding yaitu semakin besar temperatur maka tekanan juga akan semakin besar sesuai persamaan gas ideal bahwa P v = nRT. Selain itu didapatkan pula panas molar sebesar 15324,27 Joule, panas molar ini merupakan panas yang dibutuhkan zat untuk mengubah fasa cair menjadi fasa uap. Dan nilai KSR yang didapat adalah 62,8%, kesalahan ini dapat disebabka oleh air yang belum terdemineralisasi sempurna sehingga mempengaruhi proses penguapan.
Kata kunci: penguapan, claussiusclapeyron, tekanan, temperatur
I. Pendahuluan
Dalam kehidupan seharihari kita sering menemukan perubahan wujud zat seperti perubahan wujud zat cair menjadi gas atau uap. Perubahan wujud zat ini dipengaruhi oleh fasa yang merupakan bagian dari sistem dengan komposisi kimia dan fisika yang sama. Proses perubahan zat cair juga dipengaruhi oleh perubahan tekanan dan temperatur sebagaimana pada persamaanclaussiusclapeyron yang menghubungakan tekanan dan temperatur untuk menyelidiki tekanan uap air dibawah 100°c. Oleh karena itu pada percobaan ini bertujuan untuk menyelidiki tekanan uap air pada 4085°c serta menentukan nilai ratarata untuk penguapan panas.
Tekanan merupakan suatu istilah yang digunakan untuk mengukur kekuatan dari suatu zat cair atau gas. Semakin tinggi tekanan disuatu tempat maka temperatur pada tempat tersebut juga akan semakin besar. Terdapat 2 jenis tekanan yaitu tekanan hidrostatis dan tekanan udara[2]. Tekanan hidrostatis
merupakan tekanan yang zat cair pada keadaan diam yang dapat dinyatakan dengan persamaan :
P = � g h (1)
Sedangkan tekanan udara adalah tekanan yang menggerakan massa udara dalam setiap satuan luas tertentu yang dapat dinyatakan dalam persamaan:]
P =
F
A
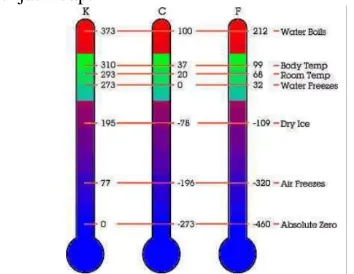
(2)Temperatur merupakan ukuran mengenai panas dinginnya suatu zat/ benda. Temperatur dapat mengubah sifat zat contohnya mengubah zat cair menjadi uap.
Gambar 1. Nilai temperatur untuk berbagai kondisi
Proses perubahan wujud zat yang lain dapat diketahui dari diagram fasa sebagai berikut:
Gambar 2. Diagram P-T[3]
Hubungan tekanan dan temperatur pada percobaan ini dapat diungkapkan dalam persamaan claussius-clapeyron. Bila dua fasa dalam sistem satu komponen berada dalam kesetimbangan, kedua fasa tersebut mempunyai energi Gibbs molar yang sama. Pada sistem yang memiliki fasa α dan β,[1]
Gα = Gβ (3)
Jika tekanan dan suhu diubah dengan tetap menjaga kesetimbangan, maka
dGα = dGβ (4) entalpi penguapan, sublimasi,peleburan maupun transisi antara dua padat.[1]
ΔH
sublimasi=
ΔH
peleburan+
ΔH
penguapan (10) Untuk peristiwa penguapan dan sublimasi, Clausius menunjukkan bahwa persamaan Clapeyron dapat disederhanakan dengan mengandaikan uapnya mengikuti hukum gas ideal dan mengabaikan volumecairan (Vl) yang jauh lebih kecil dari volume uap (Vg). [1] clapeyron, dapat juga diungkapkan dalam persamaan :
ln
P
=
λ
RT
(18)Dimana
P
=
P
0−
P
read+
P
awal (19)III. Metode Penelitian
Alat dan bahan
Alat- alat percobaan dalam percobaan ini adalah
Gambar 3.Susunan alat percobaan tekanan uap air di bawah 100 °C panas molar dari penguapan
Metode eksperimen
IV. Data dan Analisis
Rumus yang digunakan
Menghitung P (tekanan)
P = P0 – Ppembaca – Pawal (20)
Menghitung panas molar (λ)
λ = m. R (21)
dengan m adalah at (gradien) dari grafik temperatur terhadap tekanan.
Menghitung KSR
KSR =
|
λlit
λ
−
λ
lit
|
x 100%(22)
Data percobaan
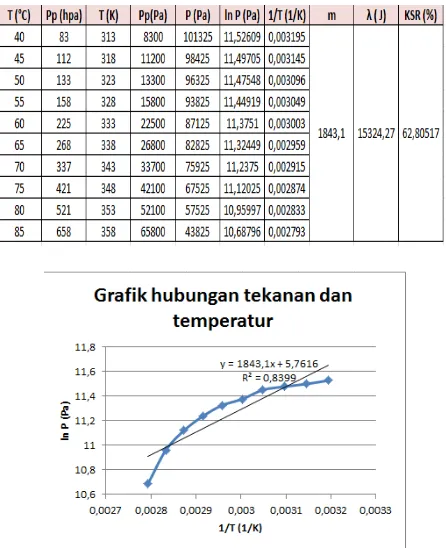
Tabel 1. Hasil pengamatan tekanan, temperatur dan panas molar
Gambar 4. Grafik ln P terhadap 1/T
Keterangan:
P
= Tekanan (Pa) T = Temperatur (K)λ = Panas molar (J)
Contoh perhitungan (diambil contoh data pertama tabel 1):
1. Menghitung
P
:Dengan persamaan (20) didapat
P
=
101325
Pa
2. MenghitunglnP
Ln P = ln (101325) = 11,52609 Pa
3. Mengitung 1/T
1/T = (1 /313) = 0,003195 1/K
4. Menghitung KSR
Dengan persamaan (22) didapatkan KSR = 62,80517%
Analisis Data
manometer dan termometer. Selain itu, dihubungkan pula dengan pompa vakum untuk mengurangi uap air karena uap air ini akan terus meningkat.
Pada percobaan akan didapatkan nilai tekanan dan temperatur yang berbanding lurus artinya bahwa semakin besar temperatur air yang dipanaskan maka tekanannya akan meningkat karena ketika air dipanaskan maka air akan mencapai titik didihnya kemudian akan berubah fasa menjadi uap/gas. Hal ini sesuai dengan persamaan gas ideal bahwa Pv = n RT, terlihat bahwa semakin besar temperatur maka tekanan juga akan semakin besar. Selain itu, berdasarkan hubungan claussiusclapeyron bahwa tekanan beberapa zat akan meningkat secara linier dengan meningkatnya temperatur yang diungkapkan
dalam persamaan
ln
P
=
λ
RT
sehingga untukgrafik hubungan ln P terhadap 1/T akan berbanding lurus. Dengan adanya kenaikan temperatur, tekanan uap akan melebihi tekanan atmosferik dan akan mengangkat cairan dalam bentuk uap sehingga untuk menentukan tekanan dapat dihitung dengan persamaan (20) . Dan nilai λ merupakan panas molar yaitu panas yang dibutuhkan zat untuk menaikan temperatur zat dalam kelvin sehingga dengan adanya panas molar ini maka zat cair akan berubah fasa dari cair ke fasa uap. Dan didapatkan nilai panas molarnya sebesar 15324,27 J. Jika proses ini terjadi pada kondisi vakum (tekanan 1 atm) maka air akan menguap pada suhu 100°c, sedangkan jika tidak berada dalam kondisi vakum ( tekanannya tidak 1 atm) maka air dapat menguap dibawah suhu 100°c karena pada percobaan labu labu disimpan/dinaikkan sehingga berada diatas permukaan air. Hal inilah yang menyebabkan air akan lebih cepat menguap meskipun suhunya belum mencapai 100°c. Pada percobaan ini didapatkan nilai KSR = 62,80157%. Kesalahan ini dapat disebabkan oleh air yang belum terdemineralisasi sempurna sehingga air masih memiliki kandungan mineral lain yang dapat mempengaruhi proses penguapan air.
V. Simpulan
1. Tekanan uap air pada temperatur 40°c - 85°c didapatkan bahwa nilai tekanan akan semakin besar dengan naiknya temperatur sesuai persamaan gas ideal bahwa PV = n RT
2. Berdasarkan persamaan claussius-clapeyron bahwa tekanan beberapa zat akan meingkat secara linear dengan meningkatnya temperatur. Sehingga nilai ln P akan berbanding lurus dengan 1/T sesuai
persamaan
ln
P
=
λ
RT
3. Nilai rata-rata penguapan panas pada percobaan ini adalah 15324,27 Joule atau 15,32427 KJ. Nilai rata-rata penguapan panas ini digunakan untuk mengubah fasa zat cair menjadi fasa uap.
Daftar Pustaka
[1] Fitriani. 2005. Kesetimbangan Fasa.
https://thekicker96.wordpress.com/kesetimba ngan-fasa/. ( diakses 28 April 2018 12:44 WIB)
[2] Tekanan uap air . 2014.
http://www.ilmukimia.org/2014/11/tekanan uapairlarutan.html (diakses 28 April 2018 11.30)
[3] Perubahan wujud zat. 2013.
![Gambar 2. Diagram P-T[3]](https://thumb-ap.123doks.com/thumbv2/123dok/3942827.1886247/2.595.325.487.651.770/gambar-diagram-p-t.webp)