i
PEMBUATAN DAN EVALUASI GEL ANTI-AGEING EKSTRAK TEMPE DENGAN GLISERIN SEBAGAI CHEMICAL PENETRATION ENHANCER
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Olivia Christie Anjalicca NIM : 108114040
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
PEMBUATAN DAN EVALUASI GEL ANTI-AGEING EKSTRAK TEMPE DENGAN GLISERIN SEBAGAI CHEMICAL PENETRATION ENHANCER
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Olivia Christie Anjalicca NIM : 108114040
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
v
HALAMAN PERSEMBAHAN
Ikutilah kata hatimu dan bersikap tegaslah karena apa yang kamu pilih dan ambil akan menentukan jalanmu untuk ke depannya...
Semuanya ini proses untuk mendapatkan yang terbaik dan semuanya akan indah pada waktunya...
Bermimpilah, targetkanlah, usahalah untuk mencapai semuanya itu karena semuanya pasti akan ada jalannya...
Kupersembahkan untuk :
Keluargaku, Mamah, Papah, Vina, Ivan, Edwin
viii PRAKATA
Puji syukur dan terima kasih penulis panjatkan kepada Tuhan Yesus
Kristus atas semua rahmat, kasih dan penyertaan-Nya sehingga penulis dapat
menyelesaikan skripsi “Pembuatan dan Evaluasi Gel Anti-Ageing Ekstrak Tempe dengan Gliserin sebagai Chemical Penetration Enhancer” sebagai salah satu
syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi,
Universitas Sanata Dharma, Yogyakarta.
Selama perkuliahan, penelitian hingga proses penyusunan skripsi, penulis
telah mendapatkan bantuandari berbagai pihak yang berupa dukungan sarana,
bimbingan, nasihat, kritik dan saran. Pada kesempatan ini, penulis ingin
mengucapkan terimakasih kepada :
1. Aris Widayati, M.Si., Apt., Ph.D., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma.
2. Dr. Sri Hartati Yuliani, M.Si., Apt., selaku dosen pembimbing atas segala
kesabaran untuk selalu mendukung, memotivasi, membimbing, dan memberi
masukan kepada penulis dalam penyusunan skripsi ini.
3. Enade Perdana Istyastono, Ph.D., Apt., selaku dosen penguji atas
ketersediaannya meluangkan waktu untuk menjadi dosen penguji, serta kritik
dan saran yang diberikan kepada penulis.
4. Florentinus Dika Octa Riswanto, M.Sc., selaku dosen penguji atas
ketersediaannya meluangkan waktu untuk menjadi dosen penguji sekaligus
memberikan kritik dan saran kepada penulis.
5. Prof. Dr. Sri Noegrohati, Apt., atas diskusi, masukan dan saran dalam
penyusunan skripsi.
6. Phebe Hendra, M.Si., selaku dosen pembimbing akademik yang telah
memberikan kritik dan saran kepada penulis.
7. Semua dosen Fakultas Farmasi yang telah membagikan ilmunya kepada
penulis selama penulis melaksanakan kuliah di Fakultas Farmasi Universitas
ix
8. Segenap laboran dan karyawan, Pak Musrifin, Pak Parlan, Mas Bimo, Mas
Agung, Pak Wagiran, Pak Parjiman, Pak Heru, Mas Kayat, Mas Darto atas
bantuan dan kerjasamanya selama penulis melakukan penelitian.
9. Papi, Mami, Vina, Ivan, dan Edwin atas dukungan, kasih sayang, cinta dan
semangatnya.
10. Hendy atas dukungan, semangat, kasih sayang, cinta dan kebersamaannya.
11. Sita sebagai teman satu tim atas bantuan, kerjasama, canda tawa, keluh kesah
dan dukungan selama penyusunan skripsi.
12. Juli, Liana, Angel, Yudhytha, Reri, Cilla Tuing, Cilla Ciun, Lulu, Ve, Odil,
Didit, Fanny, Monic, Aries teman-teman Farmasi A 2010 dan FST 2010.
Terimakasih telah menjadi teman yang luar biasa, bekerjasama, berbagi duka
serta dukungan yang telah diberikan selama ini dan segala pengalaman yang
tak terlupakan selama masa kuliah.
13. Mba Tyas, Mba Asti, Nadia, keluarga Wisma Surya terimakasih telah
menjadi teman yang luar biasa selama di kos, berbagi canda tawa serta
dukungan yang telah diberikan selama bersama-sama di kos Wisma Surya.
14. Seluruh pihak yang tidak dapat penulis sebutkan satu persatu yang telah
banyak memberikan andil hingga terselesaikannya skripsi ini.
Penulis menyadari bahwa penyusunan skripsi ini masih banyak
kekurangannya mengingat keterbatasan kemampuan dan pengalaman yang
dimiliki. Oleh sebab itu kritik dan saran yang membangun sangat diperlukan oleh
penulis demi kesempurnaan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi
perkembangan ilmu pengetahuan.
Yogyakarta,
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN... v
PERNYATAAN KEASLIAN KARYA ... vi
LEMBAR PERSETUJUAN PUBLIKASI ... vii
PRAKATA ... viii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
INTISARI ... xviii
ABSTRACT ... xix
BAB I PENDAHULUAN ... 1
A. Latar Belakang ... 1
xi
2. Keaslian Penelitian ... 4
3. Manfaat Penelitian ... 4
B. Tujuan Penelitian ... 5
BAB II PENELAAHAN PUSTAKA... 6
A. Isoflavon dan Tempe ... 6
I. Kromatografi Cair Kinerja Tinggi (KCKT) ... 18
J. Landasan teori ... 20
K. Hipotesis ... 21
BAB III METODOLOGI PENELITIAN... 22
A. Jenis dan Rancangan Penelitian ... 22
B. Variabel Penelitian ... 22
C. Definisi Operasional ... 22
D. Alat dan Bahan Penelitian ... 23
1. Alat penelitian ... 23
2. Bahan penelitian ... 24
xii
1. Ekstraksi isoflavon dari tempe ... 24
2. Pembuatan larutan baku genistein yang digunakan untuk penentuan panjang gelombang pengamatan ... 25
3. Penetapan panjang gelombang maksimum ... 25
4. Pembuatan larutan baku genistein ... 26
5. Penetapan kadar ekstrak tempe ... 26
6. Pemilihan formula ... 27
7. Pembuatan sediaan gel anti-ageing ekstrak tempe ... 28
8. Uji sifat fisis sediaan gel anti-ageing ekstrak tempe ... 28
a. Uji Daya Sebar ... 28
b. Uji pH ... 29
c. Uji Viskositas ... 29
9. Uji iritasi primer dengan metode Draize Test ... 29
10.Uji penetrasi sediaan gel dengan metode Franz Diffusion Cell 30 11.Analisis hasil ... 31
a. Indeks Iritasi Primer ... 31
b. Jumlah Kumulatif Genistein ... 31
BAB IV HASIL DAN PEMBAHASAN ... 33
A. Ekstraksi Isoflavon dari Tempe ... 33
B. Penetapan Kadar Ekstrak Isoflavon Tempe ... 34
a. Penetapan Panjang Gelombang Maksimal ... 34
b. Pembuatan Kurva Baku Genistein ... 35
xiii
C. Pembuatan dan Uji Sifat Fisi Sediaan Gel Anti-ageing Ekstrak
Isoflavon Tempe ... 37
1. pH ... 38
2. Daya sebar ... 38
3. Viskositas ... 39
D. Uji Iritasi Primer dengan Metode Draize Test ... 40
E. Uji Penetrasi Sediaan Gel dengan Metode Franz Diffusion Cell ... 41
BAB V KESIMPULAN DAN SARAN ... 45
A. Kesimpulan ... 45
B. Saran ... 45
DAFTAR PUSTAKA ... 46
LAMPIRAN ... 50
xiv
DAFTAR TABEL
Halaman
Tabel I. Formula gel standar dan modifikasi ... 27
Tabel II. Formula gel yang digunakan ... 28
Tabel III. Evaluasi Reaksi Iritasi Kulit ... 29
Tabel IV. Kriteria iritasi ... 30
Tabel V. Data uji sifat fisik, Q3jam, dan Fluks... 40
xv
DAFTAR GAMBAR
Halaman
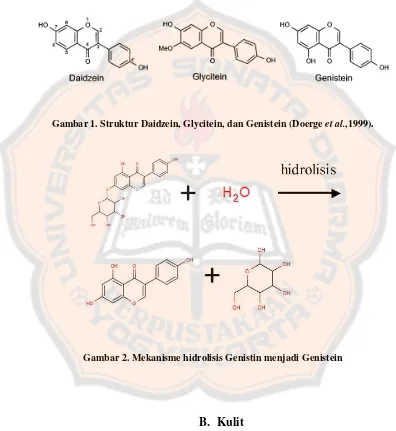
Gambar 1. Struktur Daidzein, Glycitein, dan Genistein ... 7
Gambar 2. Mekanisme hidrolisis Genistin menjadi Genistein... 7
Gambar 3. Struktur kulit ... 8
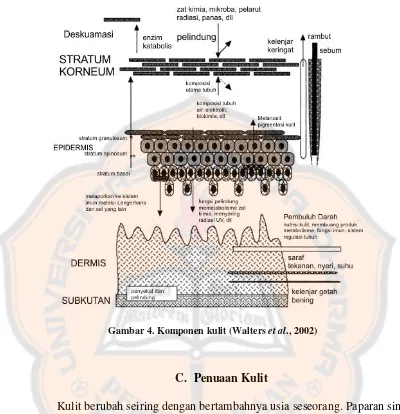
Gambar 4. Komponen kulit ... 10
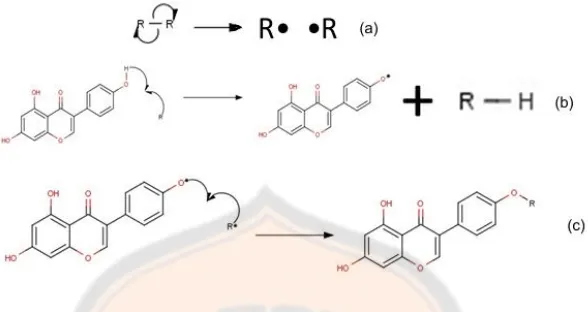
Gambar 5. Mekanisme penangkapan radikal bebas oleh Genistein, (a) tahap inisiasi, (b) tahap elongasi, (c) tahap terminasi ... 12
Gambar 6. Struktur Gliserin ... 16
Gambar 7. Diagram blok sistem KCKT secara umum ... 19
Gambar 8. Spektra genistein dengan pelarut etanol ... 34
Gambar 9. Spektra genistein dengan pelarut buffer ... 34
Gambar 10. Kurva hubungan antara konsentrasi baku genistein dengan AUC menggunakan pelarut etanol ... 35
Gambar 11. Kurva hubungan antara konsentrasi baku genistein dengan AUC menggunakan pelarut buffer ... 36
Gambar 12. Gambar sediaan gel anti-ageing ekstrak tempe ... 37
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Penimbangan Ekstraksi ... 51
Lampiran 2.Data Penimbangan Ekstrak Bobot Tetap ... 51
Lampiran 3. Spektra panjang gelombang pengamatan genistein ... 52
Lampiran 4. Data penimbangan baku dan perhitungan kadar larutan baku
genistein ... 53
Lampiran 5. Kromatogram dan data penentuan kurva baku genistein
dengan pelarut etanol ... 54
Lampiran 6.Persamaan dan gambar kurva baku genistein dengan
pelarut etanol ... 56
Lampiran 7. Kromatogram dan data penentuan kurva baku genistein
dengan pelarut buffer ... 57
Lampiran 8.Persamaan dan gambar kurva baku genistein dengan pelarut
buffer ... 59
Lampiran 9. Data penimbangan, kromatogram dan perhitungan kadar
sampel ... 59
Lampiran 10. Data hasil pengukuran uji sifat fisik sediaan gel ... 62
xvii
Lampiran 12. Ethical Clearance ... 65
Lampiran 13. Kromatogram sampel dalam sediaan dengan uji Franz Cell
Diffusion ... 66
Lampiran 14. Kadar genistein setelah uji Franz Cell Diffusion pada
setiap formula ... 70
Lampiran 15. Foto gel anti-ageing ekstrak tempe ... 72
xviii INTISARI
Salah satu penyebab penuaan dini adalah radikal bebas. Isoflavon merupakan salah satu antioksidan yang dapat mencegah adanya radikal bebas. Isoflavon yang digunakan dalam penelitian ini berasal dari ekstrak tempe.
Chemical penetration enhancer dapat membantu masuknya isoflavon ke dalam kulit. Penelitian mengenai Pembuatan dan Evaluasi Gel Anti-Ageing Ekstrak Tempe dengan Gliserin sebagai Chemical Penetration Enhancer Chemical penetration enhancer bertujuan untuk mengetahui pengaruh penetrasi ekstrak isoflavon tempe dengan chemical penetration enhancer gliserin dengan konsentrasi FI 0%, FII 5%, FIII 10%, dan FIV 20%.
Penelitian ini merupakan penelitian eksperimental murni. Evaluasi sediaan gel ekstrak isoflavon tempe ini dilihat berdasarkan parameter jumlah kumulatif dan fluks dengan menggunakan metode Franz Diffusion Cell secara in vitro.
Hasil penelitian menunjukkan bahwa FI mempunyai jumlah kumulatif dan fluks yang lebih tinggi daripada FII, FIII, dan FIV. Jumlah kumulatif FI, FII, FIII, dan FIV berturut-turut adalah 1,885±0,065; 0,953±0,028; 0,660±0,026; dan 0,572±0,015 µg/cm2. Nilai fluks FI, FII, FIII, dan FIV berturut-turut adalah 0,628; 0,318; 0,220; 0,191 µg/cm2/jam. Gliserin sebagai chemical penetration enhancer
berpengaruh menurunkan penetrasi dengan meningkatnya konsentrasi.
Kata kunci: Tempe, ekstrak tempe, isoflavon, chemical penetration enhancer, gliserin, gel
xix ABSTRACT
One of the causes of aging is free radicals. Isoflavone is one of antioxidants which can scavenge free radical. Sources of isoflavones used in this study is derived from tempe extract. Chemical penetration enhancers are subtances which can help isoflavone penetrates into the skin. Research about Formulation and Evaluation of Gel Anti-Ageing of Extract Tempe with glycerin as Chemical Penetration Enhancer ait to observe the effect of penetration of isoflavone tempe extract by using chemical penetration enhancer glycerin at concentration F1 0%, FII 5%, FIII 10%, and FIV 20%.
This research was a purely experimental study. Evaluation of this research was looking for the response of cumulative amount and flux by testing Franz Diffusion Cell in vitro.
The result shown that FI has cumulative amount and flux was higher than FII, FIII, and FIV. The cumulaltive amount of FI, FII, FIII, and FIV were 1,885±0,065; 0,953±0,028; 0,660±0,026; and 0,572±0,015 µg/cm2. Flux of FI, FII, FIII, and FIV were 0,628; 0,318; 0,220; 0,191 µg/cm2/hours. Glycerin as chemical penetration enhancer showed effect toward decrease penetration of isoflavone by increased a concentration of glycerin.
1 BAB I
PENDAHULUAN
A. LATAR BELAKANG
Penuaan merupakan proses alami yang terjadi pada setiap orang yang
da-pat dilihat di kulit. Meningkatnya usia, fungsi kulit ikut menurun, kulit akan
kehi-langan elastisitas sehingga mulai kendur dan berkeriput (Wahyono, 2011).
Pe-nuaan juga bisa disebabkan oleh faktor eksternal seperti sinar matahari, polusi
udara, maupun nutrisi yang tidak seimbang. Radiasi sinar UV matahari
menye-babkan foto oksidasi yang terjadi akibat pelepasan reactive oxygen species (ROS).
Meningkatnya ROS sebagai akibat radikal bebas dapat menyebabkan naiknya
peroksidasi lipid. Lipid yang seharusnya menjaga kulit agar tetap segar, berubah
menjadi lipid peroksida karena bereaksi dengan radikal bebas sehingga
memper-cepat penuaan (Wahyono, 2011).
Radikal bebas merupakan molekul yang mengandung satu atau lebih
elektron tidak berpasangan pada orbital luarnya. Adanya elektron yang tidak
ber-pasangan menyebabkan senyawa tersebut sangat reaktif mencari ber-pasangan dengan
menempel pada sel yang berpasangan. Radikal bebas bersumber dari polusi, asap
rokok, sinar ultraviolet dimana akan menyebabkan penuaan dini seperti kerutan
pada kulit, kulit kusam, dan kendur (Rohmatussolihat, 2009). Oleh karena itu
un-tuk mencegah radikal bebas dapat digunakan antioksidan. Antioksidan dapat
menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif
memben-tuk radikal bebas tak reaktif yang relatif stabil sehingga reaksi oksidasi berhenti
(Hudson, 1990). Berdasarkan mekanisme kerjanya, maka dapat dikembangkan
sediaan cosmeceuticals untuk menghambat penuaan dini yang disebabkan oleh
radikal bebas.
Isoflavon adalah salah satu senyawa yang berpotensi sebagai antioksidan.
Isoflavon termasuk dalam golongan senyawa flavonoid dan merupakan senyawa
polifenol. Kandungan isoflavon ini banyak terdapat di dalam kedelai dan produk
olahannya (Hernawati, 2010). Isoflavon pada kedelai berbentuk glikosida yang
terdiri dari 64% genistin, 24% daidzin, dan 13% glisitin; dan bentuk aglikon.
Ben-tuk glikosida terdapat pada makanan kedelai yang tidak difermentasi, sedangkan
yang difermentasi misalnya tempe, isoflavonnya dalam bentuk bebas (aglikon).
Ketika bentuk glikosida didegradasi menjadi senyawa aglikon maka akan lebih
mudah diserap oleh tubuh (Astuti, 2008).
Isoflavon aglikon dapat dibuat dalam bentuk sediaan gel, lotion, dan
cream. Pada penelitian kali ini, isoflavon akan dibuat dalam bentuk sediaan gel
hidrofilik. Bentuk sediaan gel mempunyai beberapa kelebihan yaitu dapat
mem-berikan rasa dingin di kulit dengan adanya kandungan air yang cukup tinggi
se-hingga nyaman digunakan, mudah dipakai, menyebar dengan baik dan
memberi-kan kenyamanan pada penggunanya (Mitsui, 1997). Menurut penelitian Nan et al.
larut di dalam eter, kloroform dan petroleum eter. Genistein termasuk dalam
isoflavon dimana sebagian larut dalam air sehingga bisa dibuat jadi gel.
Chemical penetration enhancer diperlukan untuk meningkatkan
ma-suknya zat aktif (isoflavon) ke dalam stratum corneum sehingga dapat mencapai
lapisan dermis untuk mencegah penuaan kulit dengan menangkap radikal bebas.
Zat peningkat penetrasi dapat bekerja melalui tiga mekanisme, yaitu: dengan cara
mempengaruhi struktur stratum corneum, berinteraksi dengan protein intraseluler,
dan memperbaiki partisi obat, coenhancer atau cosolvent ke dalam stratum
corneum (Swarbrick dan Boylan, 1986).
Bahan-bahan yang dapat digunakan sebagai peningkat penetrasi antara
lain: air, sulfoksida, azone, pyrrolidones, asam-asam lemak, alkohol dan glikol,
surfaktan, urea, minyak atsiri, terpen dan fosfolipid (Sukmawati dan Suprapto,
2010). Pada penelitian ini digunakan zat peningkat penetrasi yaitu gliserin.
Glis-erin dapat digunakan sebagai chemical penetration enhancer pada konsentrasi
0,1-20% (Stinchcomb dan Banks, 2010). Kecepatan penetrasi obat dengan
meng-gunakan chemical penetration enhancer gliserin ke dalam kulit dapat dilakukan
secara in vitro menggunakan Franz Diffusion Cell.
1. Perumusan Masalah :
Bagaimana pengaruh gliserin sebagai chemical penetration enhancer
2. Keaslian Penelitian
Penelitian pengembangan isoflavon dalam pembuatan gel telah dilakukan
oleh Lulu (2010) dalam penelitiannya yang berjudul “Optimasi Formula Gel
Anti-Ageing Ekstrak Etil Asetat Isoflavon dengan Carbopol 940 Sebagai
Gelling Agent dan Propilen Glikol Sebagai Humektan : Aplikasi Desain
Faktorial”. Dalam penelitian tersebut digunakan isoflavon yang berasal dari
ekstrak etil asetat tempe serta dilakukan optimasi formula gel.
Berdasarkan penelitian diatas, “Pembuatan dan Evaluasi Gel Anti-Ageing
Ekstrak Tempe dengan Gliserin sebagai Chemical Penetration Enhancer”
belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat teoretis
Menambah pengetahuan terutama dalam bidang farmasi mengenai
penetrasi genistein ke dalam kulit pada sediaan gel dengan penetration
enhancer gliserin.
b. Manfaat metodologis
Menambah informasi ilmu pengetahuan kefarmasian mengenai upaya
pengembangan dan aplikasi formula gel ekstrak bahan alam dan
penggunaan chemical penetration enhancer dalam formulasi gel ekstrak
c. Manfaat praktis
Memberikan informasi kepada masyarakat maupun penelitian lebih
lanjut mengenai chemical penetration enhacer dalam sediaan gel
anti-ageing ekstrak tempe.
B. TUJUAN PENELITIAN 1.Tujuan umum
Membuat sediaan gel anti-ageing ekstrak tempe.
2. Tujuan khusus
Mengetahui pengaruh gliserin sebagai chemical penetration enhancer
6 BAB II
PENELAAHAN PUSTAKA
A. Isoflavon dan Tempe
Isoflavon merupakan senyawa yang termasuk dalam golongan flavonoid
yang merupakan senyawa polifenolik. Senyawa isoflavon banyak ditemukan pada
tanaman kacang-kacangan (Leguminosa) dan produk olahannya (Astuti, 2008).
Salah satu tanaman kacang-kacangan yang mengandung isoflavon yaitu kedelai
dan salah satu produk olahan yang mengandung isoflavon yaitu tempe
(Hernawati, 2010). Tempe merupakan makanan tradisional yang dibuat dengan
cara memfermentasikan kedelai tanpa kulit dengan jamur Rhizopus, sampai
kedelai tertutup dengan miselium putih jamur dan mempunyai aroma khas jamur
(Pramesti, 2007).
Isoflavon pada kedelai terdiri dari aglikon (genistein, glisitein, dan
daidzein), glikosida (daidzin, genistin, dan glisitin) (Pramesti, 2007). Kandungan
isoflavon dalam 100 g kedelai berkisar 0,1-0,5 g (Cho et al., 2009). Di dalam
kedelai, isoflavon yang banyak ditemukan sebagai β-glukosida yang dapat
terhidrolisis menjadi bentuk aglikon menjadi daidzein, genistein, glisitein
(Carrao-Panizzi et al., 2002). Bentuk aglikon dari isoflavon lebih aktif daripada glikosida
dimana pengaruh itu sebanding dengan peningkatan jumlah gugus hidroksil pada
molekulnya (Pramesti, 2007).
Genistin dan daidzin akan terhidrolisis menjadi bentuk aglikonnya
fermentasi akibat aktivitas enzim β-glukosidase. Rhizopus oryzae dan Rhizopus
oligosporus diketahui memproduksi enzim β-glukosidase yang menghidrolisis
isoflavon glikosida menjadi isoflavon aglikon sehingga menyebabkan senyawa
isoflavon aglikon lebih banyak pada tempe (Pramesti, 2007).
Gambar 1. Struktur Daidzein, Glycitein, dan Genistein (Doerge et al.,1999).
Gambar 2. Mekanisme hidrolisis Genistin menjadi Genistein
B. Kulit
Kulit merupakan organ terbesar pada tubuh dimana bobot kulit dapat
mencapai 10% bobot individu dengan luas permukaan kulit pada orang dewasa
protektif ini menjadikan tubuh terhindar dari masuknya zat-zat asing (bakteri,
virus, debu) yang dapat membahayakan tubuh (Nugroho, 2013). Menurut Walters
et al. (2002), secara anatomi kulit terdiri dari empat lapisan jaringan yaitu stratum
korneum, epidermis, dermis, dan subkutan (lapisan lemak dibawah kulit).
Stratum korneum merupakan lapisan terluar kulit sebagai hasil
pembelahan sel epidermis ke arah keluar yang membentuk lapisan-lapisan terluar
epidermis (Nugroho, 2013) yang selnya telah kehilangan air, tidak berinti dan
mati (Walters et al., 2002). Sel-sel ini akan mengalami keratinisasi menjadi
struktur yang disebut korneosit (Nugroho, 2013).
Gambar 3. Struktur kulit (Walters et al., 2002)
Stratum korneum erat hubungannya dengan kosmetik karena dapat
mencerminkan kondisi kulit. Lapisan ini berperan pada tahap penembusan
sehingga menentukan konsentrasi senyawa aktif pada sel target. Membran
dan biologis disebabkan oleh adanya jembatan disulfida (menyusun serat keratin
α) dan ikatan kovalen antarmolekul. Ketebalan stratum korneum dapat dirangsang
oleh paparan ulang senyawa kimia atau fisika. Respon ini melindungi epidermis
dari rangsangan luar (Mitsui, 1997; Alache, Devissaguet, dan Hermann, 1993).
Epidermis merupakan bagian kulit di bawah stratum korneum yang
tersusun atas lapisan-lapisan sel seluler dan tipis dengan kandungan air yang
mulai berkurang jika dibandingkan dengan jumlah air yang ada di dermis.
Semakin ke atas kandungan air semakin menurun dan akhirnya sama sekali hilang
di bagian stratum korneum (Nugroho, 2013). Tebal epidermis secara keseluruhan
yaitu 74,9-96,4 µm (Sandby-Moller et al., 2003). Menurut umur lapisan selnya,
lapisan epidermis dapat dibedakan menjadi stratum germinativum yang
merupakan lapisan terdalam (usia termuda), stratum spinosum, stratum
granulosum, dan stratum korneum di lapisan terluar (Barry, 1983).
Dermis merupakan bagian di bawah epidermis berupa lapisan-lapisan sel
aselular yang menjadi tempat sistem pembuluh darah, saraf, folikel rambut,
kelenjar minyak, dan kelenjar keringat (Nugroho, 2013). Dermis mempunyai tebal
sekitar 0,1-0,5 cm dan terdiri dari 70% kolagen dan jaringan elastin (Walters et
al., 2002). Dermis dihubungkan dengan epidermis oleh papilla. Dermis tersusun
dari materi nonselular yang mendukung keberadaan organ-organ pembuluh darah,
pembuluh limfa, urat-urat saraf, dan komponen retikuloendotelia (Nugroho,
2013). Jaringan lemak subkutan terletak di bawah dermis yang berperan penting
dalam menyerap panas, meredam tekanan atau beban yang menimpa kulit
Gambar 4. Komponen kulit (Walters et al., 2002)
C. Penuaan Kulit
Kulit berubah seiring dengan bertambahnya usia seseorang. Paparan sinar
matahari dipercaya mempercepat proses perubahan kulit. Penuaan kulit dapat
dipercepat lagi dengan adanya radikal bebas. Tanda-tanda penuaan kulit yang
dapat terlihat yaitu kulit terlihat kasar, kering, kendur dan kehilangan
elastisitasnya, terdapat noda hitam, keriput, timbul lipatan pada leher dan garis
kerutan pada wajah (Tortora et al., 1990).
Faktor yang dapat menyebabkan penuaan kulit salah satunya adalah
terluarnya memiliki elektron yang tidak berpasangan sehingga elektron tersebut
menjadi reaktif dan tidak stabil. Elektron akan mencari pasangan elektron yang
lain dengan cara menariknya dari molekul lain. Pada kulit, radikal bebas akan
merusak lemak dan membran sel sehingga menyebabkan kulit kehilangan
kekencangan dan timbul keriput (Tortora et al., 1990).
Senyawa bioaktif isoflavon yang mengandung gugus fenolik mempunyai
kemampuan sebagai antioksidan dan mencegah kerusakan akibat radikal bebas
melalui dua mekanisme, yaitu mendonorkan ion hidrogen dan bertindak sebagai
scavenger radikal bebas secara langsung. Isoflavon mempunyai kemampuan
untuk mencegah peroksidasi lipid karena berperan sebagai akseptor radikal bebas
sehingga dapat menghambat reaksi rantai radikal bebas pada oksidasi lipid dan
radikal bebas dapat diredam (Astuti, 2008).
Senyawa flavonoid dapat mendonorkan hidrogen pada radikal bebas
sehingga menghasilkan radikal stabil berenergi rendah yang berasal dari senyawa
flavonoid yang kehilangan atom hidrogen. Radikal antioksidan yang terbentuk
menjadi lebih stabil melalui proses resonansi struktur cincin aromatiknya
sehingga tidak mudah untuk terlibat pada reaksi radikal lain (Astuti, 2008).
Mekanisme penangkapan radikal bebas oleh genistein di dalam lapisan
dermis meliputi tahap inisiasi, elongasi, dan terminasi. Tahap inisiasi merupakan
tahap pembentukan radial, tahap elongasi merupakan tahap penyerangan radial,
Gambar 5. Mekanisme penangkapan radikal bebas oleh Genistein, (a) tahap inisiasi, (b)
tahap elongasi, (c) tahap terminasi
D. Gel
Gel merupakan sediaan semisolid yang mengandung larutan bahan aktif
tunggal maupun campuran dengan pembawa senyawa hidrofilik atau hidrofobik
(Dirjen POM, 1995). Beberapa gel mempunyai tampilan jernih karena adanya
tampilan dari air dan lainnya keruh yang disebabkan bahan-bahannya tidak
terdis-persi molekular atau membentuk agregat. Gel harus memiliki clarity dan kilau
untuk menarik konsumen. (Allen dan Loyd, 2002).
Gel dikategorikan menjadi gel inorganik, organik, hidrogel, dan
organo-gel. Gel inorganik mempunyai sistem dua fase, sedangkan gel organik mempunyai
sistem satu fase. Hidrogel mengandung bahan yang terdispersi seperti koloid atau
terlarut pada air. Pada konsentrasi tinggi, koloid hidrofilik membentuk gel
semi-solid yang disebut jelly (Allen dan Loyd, 2002).
Hidrogel komposisi utamanya tersusun dari 85-95% air atau campuran
mendinginkan (Buchmann dan Stephan, 2001). Humektan yang ditambahkan
membuat sediaan ini menjadi lunak, memberikan kelembutan, daya sebar yang
cukup, dan menghindari kemungkinan terjadinya pengeringan. Keuntungan gel
tipe ini yaitu tidak berlemak, membentuk lapisan film tembus pandang elastis
setelah kering dengan daya lekat tinggi, tidak menyumbat por-pori, dan mudah
dicuci dengan air (Voight, 1994).
E. Sifat Fisik Gel
Sifat umum yang diinginkan dari sediaan gel yaitu dapat diterima oleh
konsumen seperti mudah dikeluarkan dari wadah, sensasi dingin ketika kontak
dengan kulit, kemampuan melekat pada tempat aplikasi selama waktu tertentu,
residu yang tidak meninggalkan rasa lengket setelah diaplikasikan, dan efikasi
klinis yang terkait pelepasan obat dan absoprsi. Hal ini terkait dengan daya sebar,
dan viskositas sediaan sehingga perlu diperhatikan (Garg et al., 2002).
Daya sebar berhubungan dengan sudut kontak tiap tetes cairan atau
preparasi semisolid yang berhubungan langsung dengan koefisien friksi. Faktor
yang mempengaruhi daya sebar adalah formulanya kaku atau tidak, kecepatan dan
lama tekanan yang menghasilkan kelengketan, temperatur pada tempat aksi.
Kecepatan penyebaran bergantung pada viskositas formula, kecepatan evaporasi
pelarut, dan kecepatan peningkatan viskositas karena evaporasi (Garg et al.,
2002).
Viskositas adalah pernyataan tahanan dari suatu cairan untuk mengalir.
Semakin tinggi viskositas maka semakin besar tahanannya (Martin et al., 1993).
akan menurunkan daya sebar (Garg et al., 2002). Gel pada penggunaan topikal
sebaiknya tidak terlalu lengket karena dapat menimbulkan rasa tidak nyaman.
Konsentrasi gelling agent yang terlalu tinggi dengan bobot molekul yang terlalu
besar akan menghasilkan gel yang sulit diaplikasikan (Zatz et al.,1996).
F. Penetration Enhancer
Penetration enhancer adalah senyawa-senyawa kimia tunggal maupun
kombinasi yang mempunyai kemampuan meningkatkan permeabilitas (Nugroho,
2013) dan mengurangi impermeabilitas kulit secara temporal (sementara)
se-hingga dapat lebih mudah dilewati oleh bahan obat (Sinha dan Kaur, 2000).
Ideal-nya, bahan yang digunakan sebagai penetration enhancer haruslah inert secara
farmakologi, tidak toksik, tidak mengiritasi, tidak menyebabkan alergi (tidak
ber-sifat alergenik), tidak berbau, tidak berwarna, tidak berasa, murah, serta
kompati-bel dengan zat aktif maupun eksipien yang digunakan (Sinha dan Kaur, 2000).
Selain itu, penetration enhancer harus dapat membalikkan barrier pertahanan
stratum korneum kepada struktur awal ketika konsentrasi enhancer telah habis
tanpa menyebabkan kematian sel (Pathan et al., 2009).
Mekanisme umum penetration enhancer yaitu dengan mengacaukan
struktur lipid dari stratum korneum kemudian berinteraksi dengan protein
interse-luler dan terakhir meningkatkan partisi obat/zat aktif, coenhancer atau pelarut ke
Beberapa senyawa yang bertindak sebagai penetration enhancer, yaitu:
a. Golongan alkohol dan glikol
Alkohol rantai pendek (C2-C5) dan senyawa golongan glikol
dapat meningkatkan absorpsi, khususnya absorpsi molekul polar.
Senyawa ini meningkatkan absorpsi dengan cara meningkatkan
fluiditas dari lapisan lipid pada stratum korneum dengan berinteraksi
dengan protein pada stratum korneum (Rosen, 2005).
b. Asam lemak dan esternya
Sejumlah besar asam lemak sudah secara luas diteliti untuk
meningkatkan penetrasi sediaan trasndermal. Asam lemak tidak
jenuh dilaporkan lebih aktif daripada asam lemak yang jenuh.
Mekanisme aksi dari asam lemak adalah meningkatkan kelarutan
dari obat, meningkatkan partisi obat, meningkatkan penetrasi pelarut
dan mengubah struktur barrier kulit (Rosen, 2005).
c. Terpene
Terpene diketahui dapat meningkatkan permeasi perkutan dari
obat hidrofilik maupun yang bersifat hidrofob. Terpene yang bersifat
polar ternyata diketahui dapat meningkatkan permeasi dari senyawa
polar dan sebaliknya (Rosen, 2005).
d. Amina dan amida
Senyawa yang termasuk golongan ini meliputi urea dan
derivatnya, asam amino dan esternya, amida, seperti azone dan
enhancer dan merupakan salah satu senyawa yang banyak diteliti
karena dapat meningkatkan permeasi dari obat dalam spektrum luas
(Rosen, 2005).
G. Gliserin
Gliserin merupakan cairan higroskopis yang tidak berwarna, tidak
berbau, rasa manis. Gliserin dapat digunakan dalam formulasi seperti oral,
optalmik, topikal maupun parenteral. Fungsi gliserin dapat digunakan sebagai
humektan dan emolient dalam sediaan topikal. Dalam sediaan krim, emulsi,
parenteral dapat berfungsi sebagai solvent maupun co-solvent. Sedangkan di
dalam sediaan larutan oral dapat berfungsi sebagai pemanis, pengawet. Selain itu
gliserin juga dapat digunakan sebagai plasticizer. Penggunaan yang berbeda
fungsi ini dapat digunakan sesuai dengan konsentrasi yang diperbolehkan (Rowe
et al., 2009).
Gliserin merupakan bahan yang sudah terdaftar dalam Food and Drug
Assosiation (FDA), dan aman digunakan dalam konsentrasi 0,2-65,7%
(Smolinske, 1992). Gliserin juga bisa digunakan sebagai penetration enhancer
dengan konsentrasi 0,1-20% (Stinchcomb dan Banks, 2010).
Gliserin bersifat sebagai penetration enhancer dan juga sebagai
humektan yang kuat dan aman bagi kulit karena mempunyai kemampuan
menyerap air yang hampir sama dengan natural moisturizing factor (NMF) yang
merupakan pengikat alami dalam kulit (Pius, 2012). Gliserin termasuk dalam
golongan glikol yang dapat memfasilitasi masuknya senyawa aktif dengan
membentuk celah yang disebut microchannel pada stratum korneum dan
memungkinkan senyawa aktif yang lebih polar berpenetrasi ke dalam kulit
(Dayan, 2005).
Humektan dapat membantu menjerat air dari udara yang kemudian dapat
berpenetrasi ke dalam kulit, bila kelembaban relatif rendah. Tetapi humektan
dapat juga menarik air dari bagian epidermis dan dermis yang dapat menyebabkan
kulit menjadi kering. Mekanisme humektan yang menarik air untuk penetrasi ke
dalam kulit, akan mengakibatkan pengembangan stratum korneum yang
memberikan persepsi kulit halus dengan sedikit kerut (Johnson, 2002).
H. Draize Test
Draize test merupakan model uji in vivo yang biasa digunakan dalam uji
iritasi dengan menggunakan kelinci albino. Uji ini menggunakan sistem scoring
untuk menunjukkan index iritasi primer yang didapatkan dari perhitungan eritema
dan edema yang dihasilkan (Maibach, 2001).
Kelinci albino yang sudah dicukur bulunya diaplikasikan sediaan atau
senyawa yang akan diukur indeks iritasi primernya pada waktu tertentu. Iritasi
tertentu. Iritasi ini dapat terjadi jika suatu zat menempel pada kulit dan
menyebabkan zat tersebut terpenetrasi masuk ke dalam kulit dan mengakibatkan
dilatasi pembuluh darah pada daerah yang terkena. Jika zat tersebut mengiritasi
maka akan menyebabkan iritasi pada kulit yang terkena zat tersebut dan
sebaliknya (Irsan, dkk., 2013).
Hasil eritema maupun edema diukur dengan menggunakan sistem
scoring yang kemudian dihitung dengan rumus untuk mengetahui indeks iritasi
primer yang didapatkan (Irsan, dkk., 2013).
I. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi Cair Kinerja Tinggi (KCKT) merupakan salah satu metode
kromatografi cair yang dilengkapi dengan sistem pompa bertekanan tinggi untuk
mengalirkan fase gerak dan detektor yang sensitif sehingga pemisahan dapat
berlangsung dengan cepat dan memiliki efisiensi yang tinggi. Salah satu
keunggulan KCKT dibandingkan dengan kromatografi gas yaitu dapat untuk
menganalisis senyawa yang tidak menguap atau tidak tahan panas tanpa peruraian
atau tanpa perlunya derivat yang menguap (Dirjen POM, 1995).
Instrumen KCKT terdiri dari delapan komponen pokok, yaitu wadah fase
gerak, sistem penghantaran fase gerak, alat untuk memasukkan sampel, kolom,
detektor, wadah penampung buangan fase gerak, tabung penghubung, dan suatu
perekam/komputer (Rohman, 2007).
Fase gerak biasanya terdiri dari campuran pelarut yang dapat bercampur
oleh polaritas keseluruhan pelarut, polaritas fase diam, dan sifat komponen
sampel. Fase normal dimana fase diam lebih polar daripada fase gerak,
kemampuan elusi meningkat dengan meningkatkan polaritas pelarut, sedangkan
untuk fase terbalik dimana fase diam kurang polar daripada fase gerak,
kemampuan elusi menurun dengan meningkatnya polaritas pelarut (Rohman,
2007).
Fase diam yang digunakan berupa silika yang dimodifikasi secara
kimiawi, silika yang tidak dimodifikasi, atau polimer-polimer stiren dan divinil
benzen. Permukaan silika adalah polar dan sedikit asam karena adanya residu
gugus silanol (SiOH). Oktadesil silika (ODS/C18) merupakan fase diam yang
paling banyak digunakan karena mampu memisahkan senyawa-senyawa dengan
kepolaran rendah, sedang, maupun tinggi (Rohman, 2007).
Gambar 7. Diagram blok sistem KCKT secara umum (Rohman, 2007)
Penelitian mengenai genistein dengan menggunakan KCKT telah
dilakukan oleh Orhan et al. (2011) dengan penelitian analisis kandungan genistein
menggunakan fase diam C18, fase gerak metanol : air (70:30) dengan panjang
gelombang 261 dan kecepatan alir 0,7ml/menit.
J. Landasan Teori
Penuaan kulit merupakan hal yang terjadi pada manusia dikarenakan
bertambahnya usia, faktor radikal bebas, dan makanan. Isoflavon mempunyai
daya antioksidan yang dapat menghambat penuaan kulit. Tempe merupakan salah
satu sumber yang mengandung isoflavon, yang digunakan sebagai bahan aktif
dalam sediaan anti-ageing untuk menghambat penuaan kulit di dermis (Astuti,
2008).
Sediaan anti-ageing merupakan sediaan cosmeuticals yang dalam
penelitian ini, akan dibuat dalam formulasi gel karena mempunyai sifat fisik dan
stabilitas yang dapat diterima oleh masyarakat, mempunyai konsistensi yang
lembut, serta memberikan rasa nyaman pada kulit saat penggunaan maupun
pembersihannya yang mudah dicuci dengan air.
Dalam sediaan gel ini diformulasikan pula penetration enhancer yang
berfungsi untuk membawa bahan aktif serta meningkatkan penetrasi isoflavon,
khususnya genistein ke dalam lapisan kulit untuk mencegah penuaan kulit di
dermis. Penetration enhancer yang digunakan dalam formulasi sediaan ini adalah
gliserin. Dalam penelitian ini akan dilihat kemampuan penetration enhacer
gliserin dengan empat konsentrasi yang berbeda untuk mengetahui pengaruhnya
dalam membawa dan meningkatkan bahan aktif ke dalam lapisan kulit tanpa
Gliserin bersifat sebagai penetration enhancer dan juga sebagai
humektan yang mempunyai kemampuan menarik air untuk penetrasi ke dalam
kulit, akan mengakibatkan pengembangan stratum korneum (Johnson, 2002).
Gliserin termasuk dalam golongan glikol yang dapat memfasilitasi masuknya
senyawa aktif dengan membentuk celah yang disebut microchannel pada stratum
korneum dan memungkinkan senyawa aktif yang lebih polar berpenetrasi ke
dalam kulit (Dayan, 2005).
Salah satu isoflavon yaitu genistein yang mempunyai sifat semipolar
yang diformulasikan ke dalam gel dengan penetration enhancer gliserin
diharapkan dapat berpenetrasi ke dalam lapisan kulit dengan metode Franz
Diffusion Cell dan perlu dilakukan penetapan kadar untuk mengetahui kadar
genistein yang terpenetrasi.
Penetapan kadar genistein dilakukan dengan metode KCKT fase terbalik
detektor UV, karena KCKT memiliki sensitivitas dan selektivitas yang baik untuk
analisis senyawa dalam campuran dengan kadar yang kecil serta genistein
memiliki gugus kromofor yang dapat memberikan serapan pada daerah panjang
gelombang UV.
K. Hipotesis
Gliserin dapat berfungsi sebagai chemical penetration enhancer terhadap
22 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan rancangan eksperimental murni.
B. Variabel Penelitian
1. Variabel bebas
Kadar gliserin yang digunakan sebagai chemical penetration enhancer.
2. Variabel tergantung
Sifat fisik gel anti-ageing ekstrak isoflavon tempe yang meliputi daya
sebar, viskositas gel dan pH sediaan serta kecepatan penetrasi zat aktif ke
dalam kulit.
3. Variable pengacau terkendali
Kecepatan putar dan waktu pengadukan dalam proses pembuatan sediaan
gel, wadah penyimpanan, lama penyimpanan.
4. Variable pengacau tak terkendali
Kelembaban, suhu ruangan saat pembuatan dan penyimpanan gel,
kondisi patologis hewan uji, subyektifitas penulis dalam pengamatan.
C. Definisi Operasional
1. Ekstrak tempe adalah cairan kental yang diperoleh dari hasil ekstraksi tempe
2. Gel anti-ageing ekstrak tempe adalah sediaan semi padat yang dibuat dari
ekstrak tempe sesuai formula yang telah ditentukan.
3. Chemical penetration enhancer adalah substansi atau senyawa yang dapat
memfasilitasi absorpsi penetrasi melalui kulit dengan mengurangi
impermeabilitas dari kulit secara sementara, dalam hal ini adalah gliserin.
4. Sifat fisik gel anti-ageing adalah parameter untuk mengetahui kualitas fisik gel
anti-ageing, dalam penelitian ini meliputi parameter daya sebar, pH, dan
viskositas.
5. Draize Test adalah uji iritasi yang dilakukan pada hewan uji untuk mengetahui
apakah sediaan gel anti-ageing ekstrak kedelai menyebabkan iritasi atau tidak.
Hewan uji yang digunakan adalah kelinci albino.
6. Franz Cell Diffusion adalah suatu alat uji yang digunakan untuk mengukur
jumlah obat yang terpenetrasi melalui kulit secara in vitro.
D. Alat dan Bahan Penelitian 1. Alat penelitian
Alat yang digunakan pada penelitian ini adalah alat-alat gelas (Iwaki
TE-32 Pirex Japan Unmderli), alat maserasi (Innova 2100 platform shaker),
Vaccum Rotary Evaporator (Janke-Kulken), mixer, blender, neraca analitik
Mettler-Todelo AB204, Horizontal Double Plate, indikator pH universal
Merck, pHmeter, Viskometer Rion VT-04, alat vakum, seperangkat alat KCKT
dengan detektor ultraviolet (UV) merek Shimadzu LC-2010C, kolom C18
B115Y620), seperangkat komputer (merek Dell B6RDZ1S Connexant system
RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet D2566
HP-024-000 625730), UV/Vis Spectrophotometer SP-3000plus merek OPTIMA dengan
deterktor silicon photo diode, millipore, alat ultrasonicator Refsch., Tipe :
T460 (Schwing.1 PXE, FTZ-Nr. C-066/83, HF-Frequ.:35 kHz), mikropipet,
dan kertas saring Whatman 0,45 μm.
2. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah tempe yang diperoleh
dari SUPERINDO, Seturan, aquadest, gliserin, propilenglikol, carbopol 940,
triethanolamin, metil paraben, natrium klorida dan ethanol kualitas farmasetis;
ethanol, metanol p.a. (E. Merck), aquabidest hasil penyulingan di laboratorium
Kimia Analisis Instrumental Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta, dan baku pembanding genistein.
E. Tata Cara Penelitian 1. Ekstraksi isoflavon dari tempe
Tempe segar yang didapatkan dari SUPERINDO merek MUCHLAR,
Seturan dipotong-potong kecil kemudian diblender hingga halus. Kemudian
tempe yang sudah halus ditimbang sebanyak 150,0 gram ditambah petrolium
eter (PE) sebanyak 300,0 mL (1:2), kemudian di maserasi selama sehari (±24
jam). Kemudian PE dibuang dan ditambahkan etanol sebanyak 300,0 mL
kemudian di maserasi selama 3 hari. Hasil maserasi disaring sehingga
menggunakan rotary evaporator hingga didapatkan ekstrak kental tempe.
Ekstrak kental ini dimasukkan ke dalam oven dengan suhu 50°C selama 1 jam kemudian dikeluarkan dan ditimbang bobotnya. Kemudian dilakukan hal yang
sama hingga didapatkan bobot tetap.
2. Pembuatan larutan baku genistein yang digunakan untuk penentuan panjang gelombang pengamatan
Sejumlah lebih kurang 1,0 mg genistein ditimbang seksama dan
dilarutkan dalam 1,0 mL etanol sehingga didapatkan konsentrasi sebesar
1000,0 µg/mL, kemudian dibuat larutan intermediet dengan mengambil
sebanyak 0,5 mL dimasukkan ke dalam labu takar 5,0 mL kemudian
diencerkan dengan etanol hingga tanda batas sehingga didapatkan konsentrasi
sebesar 100,0 µg/mL. Larutan seri untuk pengamatan panjang gelombang
menggunakan 2 konsentrasi yaitu 5,0 dan 10,0 µg/mL. Larutan seri dibuat dari
larutan intermediet dengan mengambil masing-masing sejumlah 250,0 dan
500,0 µ L dimasukkan ke dalam labu 5,0 mL kemudian diencerkan dengan
etanol hingga tanda batas sehingga didapatkan konsentrasi sebesar 5 µg/mL,
10 µg/mL.
3. Penetapan panjang gelombang maksimum
Masing-masing konsentrasi 5, 10 µg/mL larutan seri baku genistein
spektrofotometer UV-Vis. Spektrum yang dihasilkan akan menunjukkan
panjang gelombang maksimum yang akan digunakan pada sistem KCKT.
4. Pembuatan larutan baku genistein
Sejumlah lebih kurang 1,0 mg genistein ditimbang seksama dan
dilarutkan dalam 1,0 mL etanol sehingga didapatkan konsentrasi sebesar
1000,0 µg/mL, kemudian dibuat larutan intermediet dengan mengambil
sebanyak 0,5 mL dimasukkan ke dalam labu takar 5,0 mL kemudian
diencerkan dengan etanol hingga tanda batas sehingga didapatkan konsentrasi
sebesar 100,0 µg/mL.
Pembuatan seri larutan baku dibuat dari larutan intermediet dengan
mengambil masing-masing sejumlah 5,0; 25,0; 50,0; 250,0; 500,0 µL
dimasukkan ke dalam labu ukur 5,0 mL secara beruturan dari volume kecil
hingga besar kemudian diencerkan dengan etanol hingga tanda batas sehingga
didapatkan konsentrasi sebesar 0,1; 0,5; 1,0; 5,0; dan 10,0 µg/mL. Larutan
disaring dengan millipore dan didegassing dengan ultrasonicator selama 15
menit kemudian diinjeksikan ke dalam sistem KCKT fase terbalik.
5. Penetapan kadar ekstrak tempe
Ekstrak tempe di timbang sebanyak 1,0 g kemudian dilarutkan ke dalam
15,0 mL aquadest dan 15,0 mL etil asetat kemudian dilakukan ekstraksi
cair-cair. Fase atas larutan diambil (larutan A), kemudian fase bawah ditambahkan
hingga dua kali. Fase atas disatukan dengan larutan A. Larutan A kemudian
diuapkan hingga didapatkan bobot tetap.
Ekstrak yang telah bobot tetap dilarutkan dengan etanol secukupnya
kemudian dimasukkan ke dalam labu takar 100,0 mL dan diencerkan dengan
etanol hingga tanda batas. Larutan stok sampel diambil sebanyak 1 mL
dimasukkan ke dalam labu takar 10,0 mL kemudian diencerkan dengan etanol
hingga tanda batas. Larutan disaring dengan di milipore dan didegassing
dengan ultrasonicator selama 15 menit, kemudian diinjeksikan ke dalam
sistem KCKT fase terbalik detektor UV dengan fase diam C18, fase gerak
metanol : air (70:30) dengan kecepatan alir fase gerak 0,7 mL/min sebanyak
20,0 µ L.
6. Pemilihan formula
Formula yang digunakan mengacu pada International Journals of
Pharmaceutical Compounding dengan judul Gel Compounding. Formula yang
digunakan adalah sebagai berikut :
Tabel I. Formula gel standar dan modifikasi
Formula Standar Formula Modifikasi R/ Carbopol 0,5 g R/ Carbopol 1%
Formula yang digunakan:
Tabel II. Formula gel yang digunakan
Bahan F1 F2 F3 F4
7. Pembuatan sedian gel anti ageing ekstrak tempe
Campur gliserin dan ekstrak tempe menggunakan mixer skala kecepatan
1 hingga homogen, kemudian tambahkan propilenglikol campur homogen.
Carbopol 940 ditambahkan ke dalam campuran kemudian mixer selama 2
menit, kemudian ditambahkan sisa aquadest, metil paraben ke dalam campuran
dan mixer hingga homogen. TEA ditambahkan ke dalam campuran dan
dicampur homogen menggunakan mixer skala kecepatan satu selama 2 menit.
Sediaan gel ditambahkan pewangi apel sebanyak 5 tetes dan dimixer homogen.
8. Uji sifat fisis sediaan gel anti-ageing ekstrak tempe
a. Uji Daya Sebar. Uji daya sebar dilakukan 48 jam setelah pembuatan
dengan cara gel ditimbang seberat 1 gram dan diletakkan di tengah kaca
bulat berskala, kemudian ditutup dengan kaca bulat yang lain. Diatas gel
diberi beban dengan berat total 125 gram kemudian didiamkan selama 1
b. Uji pH. Uji pH dilakukan sesaat setelah pembuatan gel menggunakan
indikator pH universal.
c. Uji Viskositas. Uji viskositas dilakukan dengan menggunakan alat
viskosmeter dengan cara gel dimasukkan ke dalam wadah dan dipasang
pada portable viscotester. Viskositas gel diketahui dengan mengamati
gerakan jarum penunjuk viskositas. Uji ini dilakukan 48 jam setelah
pembuatan gel.
9. Uji iritasi primer dengan metode Draize Test
Evaluasi iritasi primer dilakukan dengan menggunakan hewan uji kelinci
albino sebanyak 2 kelinci setiap formula. Dibuat area dengan ukuran 2,54 x
Tabel III. Evaluasi Reaksi Iritasi Kulit (Buchman dan Stephan, 2001)
Jenis Iritasi Skor Eritema Tanpa eritema 0
Eritema hampir tidak tampak 1 Eritema berbatas jelas 2 Eritema moderat sampai berat 3 Eritema berat (merah bit) sampai sedikit membentuk kerak 4
Edema Tanpa edema 0
Edema hampir tidak tampak 1 Edema berbatas jelas 2 Edema moderat (tepi naik ±1 cm) 3 Edema berat (tepi naik lebih dari 1 mm dan meluas keluar
daerah pejanan)
Tabel IV. Kriteria iritasi (Buchman dan Stephan, 2001)
Indeks Iritas Kriteria Iritasi Senyawa Kimia 0 Tidak mengiritasi <2 Kurang merangsang 2-5 Iritasi moderat
>5 Iritasi berat
10. Uji penetrasi sediaan gel dengan metode Franz Diffusion Cell
Uji penetrasi menggunakan membran abdomen kulit mencit jantan galur
Swiss usia 2-3 bulan. Mencit dibius dengan eter kemudian bulu pada bagian
abdominal dicukur dan disayat serta lemak-lemak pada bagian subkutan yang
menempel dihilangkan secara hati-hati. Sayatan direndam dalam larutan Na
fisiologis steril dan disimpan pada suhu 4°C. Kompartemen reseptor diisi dengan larutan dapat fosfat pH 7,4 sekitar 27,0 mL yang dijaga suhunya sekitar
37±0,5°C dan diaduk dengan pengaduk magnetik stirer dengan kecepatan 300rpm.
Kulit abdomen diletakkan diantara kompartemen donor dan
kompartemen reseptor dengan sisi dermal berhubungan langsung dengan
medium reseptor. Sampel ditimbang seksama sebanyak ±1,0 gram kemudian
diaplikasikan pada permukaan kulit. Kemudian sampel diambil pada jam
ke-0,5; 1; 2; dan 3 sebanyak 600,0 µ L dari kompartemen reseptor dengan
menggunakan syriringe dan larutan dapar fosfat pH 7,4 segera ditambahkan
sejumlah volume yang sama dengan volume yang diambil. Kemudian sampel
disaring dengan menggunakan milipore dan diinjekkan ke dalam sistem KCKT
11. Analisis Hasil
a. Indeks Iritasi Primer
Indeks iritasi primer untuk sediaan juga dihitung dengan rumus sebagai
berikut :
Jumlah kumulatif genistein yang terpenetrasi per luas area difusi
(µg/cm2) dapat dihitung dengan rumus :
Q kumulatif = 𝐶𝑛.𝑉 +( 𝐶.
𝑛 −1 𝑖=1 𝑆) A
Keterangan :
Q = Jumlah kumulatif isoflavon yang terpenetrasi per luas area difusi(µg/cm2)
Cn = Konsentrasi isoflavon µg/mL pada sampling menit ke-n V = Volume sel difusi Franz
𝐶
𝑛−1
𝑖=1 = Jumlah konsentrasi isoflavon (µg/mL) pada sampling pertama
hingga sebelum menit ke-n S = Volume sampling (mL) A = Luas area membran (cm2)
Kemudian dilakukan perhitungan fluks (kecepatan penetrasi tiap satuan
waktu) obat berdasarkan hukum Fick I :
𝐽= M
S × t
Keterangan :
J = Fluks (µ g cm-2 jam-1)
M = Jumlah kumulatif genistein yang melalui membran (µg) S = Luas area difusi (cm2)
Kemudian dibuat grafik kumulatif genistein yang terpenetrasi (µ g) per
33 BAB IV
HASIL DAN PEMBAHASAN
A. Ektraksi Isoflavon dari Tempe
Penelitian ini menggunakan tempe yang didapatkan dari SUPERINDO,
Seturan dengan merek MUCHLAR sebanyak 3 kg untuk meminimalkan faktor
pengacau. Tempe yang digunakan dipotong-potong terlebih dahulu kemudian di
blender sampai halus untuk memperluas area kontak dengan cairan penyari
se-hingga proses maserasi lebih baik. Tempe yang digunakan untuk maserasi
sebanyak 2655,80 g.
Tempe dimaserasi menggunakan petroleum eter (PE) untuk menarik
senyawa non polar seperti protein, lemak, dan pengotor non polar lainnya yang
terdapat pada tempe. Kemudian PE dibuang dan dilakukan remaserasi
mengguna-kan etanol untuk menarik flavonoid dari tempe. Selanjutnya dilakumengguna-kan pemekatan
hingga bobot tetap untuk menghilangkan kandungan etanol di dalam ekstrak.
Hasil pemekatan berupa cairan kental berwarna coklat kehitaman berbau khas
sebanyak 69,6132 g.
Ekstrak tempe sebanyak 3,1884 g diekstraksi cair-cair menggunakan etil
asetat dan akuades sehingga didapatkan fraksi isoflavon. Proses ini dilakukan
untuk menarik aglikon isoflavon (Robinson dan Trevor, 1991). Selanjutnya fraksi
etil asetat dipekatkan untuk menghilangkan etil asetat sehingga didapatkan cairan
B. Penetapan Kadar Ekstrak Isoflavon Tempe
a. Penetapan panjang gelombang maksimal
Penetapan panjang gelombang maksimal (λmaks) bertujuan untuk mencari
panjang gelombang yang dapat memberikan serapan secara maksimal. Penetapan
λmaks dilakukan dengan menggunakan larutan baku genistein dengan konsentrasi
5,035 µg/mL dan 10,07 µ g/mL. Penetapan panjang gelombang dilakukan dengan
menggunakan dua pelarut yaitu etanol dan buffer fosfat pH 7,4. Penetapan
panjang gelombang menggunakan pelarut etanol digunakan untuk penetapan
kadar ekstrak isoflavon tempe. Sedangkan penetapan panjang gelombang
menggunakan pelarut buffer digunakan untuk penetapan kadar sediaan dari sel
difusi Franz. Hal ini disebabkan karena adanya perbedaan pelarut maka panjang
gelombang yang dihasilkan pun berbeda.
Gambar 8. Spektra baku genistein dengan pelarut etanol
Gambar 9. Spektra baku genistein dengan pelarut buffer fosfat pH 7,4
261 nm
Dari hasil scanning panjang gelombang maksimal (Gambar 6 dan 7 )
diketahui bahwa λmaks genistein dengan pelarut etanol adalah 261 nm dan dengan
pelarut buffer fosfat pH 7,4 adalah 269 nm.
b. Pembuatan kurva baku genistein
Kurva baku genistein dibuat dengan menggunakan senyawa standar
genistein yang bertujuan untuk memperoleh persamaan regresi linear yang
selan-jutnya digunakan untuk menghitung kadar genistein dalam ekstrak isoflavon
tempe. Penggunaan genistein sebagai standar karena genistein merupakan salah
satu senyawa isoflavon yang terdapat di dalam tempe (Pramesti, 2007).
Pengu-kuran seri baku genistein dilakukan pada panjang gelombang 261 nm dan 269 nm
dengan menggunakan 5 seri konsentransi, yaitu 0,1007 µg/mL; 0,5035 µ g/mL;
1,007 µg/mL; 5,035 µ g/mL dan 10,07 µg/mL.
Gambar 11. Kurva hubungan antara konsentrasi baku genistein dengan AUC menggunakan pelarut buffer fosfat pH 7,4
Berdasarkan pengukuran tersebut, diperoleh persamaan kurva baku
genistein dengan pelarut etanol yaitu y = 214780,720x – 16242,695 dengan nilai r
sebesar 0,99950 yang akan digunakan dalam penetapan kadar isoflavon dalam
ekstrak isoflavon tempe dan diperoleh persamaan kurva baku genistein dengan
pelarut buffer fosfat pH 7,4 yaitu y = 172800,318x – 12453,734 dengan nilai r
sebesar 0,9991 yang akan digunakan dalam penetapan kadar isoflavon dengan
menggunakan sel difusi Franz.
c. Penetapan kadar isoflavon ekstrak tempe
Penetapan kadar isoflavon tempe dilakukan untuk mengetahui isoflavon
di dalam ekstrak tempe. Ekstrak tempe yang telah dilakukan LLE (Liquid-Liquid
Extraction) kemudian dilarutkan ke dalam etanol p.a di dalam labu ukur 100,0
mL. Larutan uji diperoleh dengan mengambil sebanyak 1,0 mL larutan stok yang
kemudian diencerkan ke dalam labu 10,0 mL. Larutan uji inilah yang akan diukur
dengan KCKT pada panjang gelombang 261 nm. Isoflavon yang dimaksudkan
dalam penelitian ini adalah semua kandungan isoflavon yang ada di dalam ekstrak
kering tempe yang terhitung terhadap genistein karena senyawa baku yang
digunakan adalah genistein. Dari hasil penetapan kadar genistein dalam ekstrak
tempe diperoleh kadar sebesar 0,4506 % b/b.
C. Pembuatan dan Uji Sifat Fisis Sediaan Gel Anti-ageing Esktrak Isoflavon Tempe
Formula yang digunakan dalam penelitian ini yaitu carbopol 940 sebagai
basis gel hidrofilik, TEA (Trietanolamin) sebagai pembasa atau netralisasi
carbopol, gliserin sebagai chemical penetration enhancer, propilenglikol sebagai
humektan, akuades sebagai pelarut, parfum, pengawet, dan ekstrak isoflavon
tempe sebagai zat aktif. Carbopol 940 bersifat asam seingga dibutuhkan TEA
untuk menaikkan pH karena kulit manusia mempunyai pH pada range 5,5-7. Hal
ini untuk menghindari iritasi kulit apabila pH terlalu asam atau basa. Selain itu,
pada pH netral, pada carbopol 940 terjadi proses tolak menolak antar ion pada
gugus karboksil sehingga membuat gel menjadi lebih rigit (kaku) dan
mengembang (Barry, 1983).
Uji sifat fisis sediaan gel anti-ageing ekstrak isoflavon tempe dilakukan
untuk mengetahui sediaan gel yang dihasilkan telah memiliki sifat fisis yang baik
yaitu dapat diterima oleh masyarakat (acceptable). Sifat fisis yang diamati dalam
penelitian ini adalah daya sebar, viskositas, dan pH. Uji sifat fisis sediaan,
khususnya daya sebar dan viskositas dilakukan 48 jam setelah pembuatan gel
di-mana waktu 48 jam dianggap sudah tidak ada lagi pengaruh gaya atau energi yang
diberikan dalam proses pembuatan sediaan yang dapat mempengaruhi hasil
pen-gujian.
1. pH
Uji pH dilakukan untuk mengetahui pH tiap formula yang dibuat, sesaat
setelah pembuatan gel dengan menggunakan pH universal. Hasil uji pH menurut
Tabel V, didapatkan bahwa semua sediaan mempunyai pH 6 yang masuk ke
dalam range pH yang dingiinkan yaitu pH dengan range 5,5-7.
2. Daya sebar
Pengujian daya sebar sediaan gel bertujuan untuk mengetahui
kemampuan sediaan gel menyebar dan merata pada area yang diinginkan di
per-mukaan kulit saat diaplikasikan. Daya sebar berbanding terbalik dengan
viskositas, semakin kecil viskositas suatu sediaan semisolid maka kemampuan
menyebarnya pada permukaan kulit akan semakin besar, begitu juga sebaliknya
(Garg et al, 2002). Daya sebar yang optimum untuk sediaan semistiff adalah
Pengujian daya sebar dilakukan dengan menimbang 1 g sediaan
ke-mudian ditimpa dengan kaca bundar dengan total berat 125 g, ditunggu selama
satu menit, setelah itu diukur daya sebarnya. Berdasarkan data daya sebar pada
Tabel V, semua sediaan masuk ke dalam range daya sebar yaitu 3-5 cm sehingga
termasuk dalam sediaan semistiff. Daya sebar adalah karakteristik yang berguna
untuk memperhitungkan kemudahan saat digunakan, pengeluaran dari wadah
serta mempengaruhi penerimaan konsumen (Garg et al., 2002). Dilihat secara
vis-ual, sediaan gel ini tidak terlalu cair dan tidak terlalu kental sehingga dapat
diap-likasikan di kulit dengan mudah dan dapat menyebar rata di kulit.
3. Viskositas
Pengujian viskositas dilakukan untuk mengetahui tingkat kekentalan gel.
Viskositas dapat diartikan sebagai tahanan untuk mengalir. Viskositas berbanding
terbalik dengan kemampuan alir dimana semakin besar viskositas maka
kemam-puan untuk mengalir akan semakin kecil, begitu pula sebaliknya (Martin et. al,
1993). Pengujian viskositas dalam penelitian ini dilakukan 48 jam setelah
pem-buatan karena setelah 48 jam sediaan dianggap sudah melewati suatu fase yang
tidak ada lagi energi mekanik (shearing) yang digunakan saat proses
pencampu-ran sehingga viskositas yang terukur dianggap viskositas sistem gel yang
se-benarnya, sehingga diharapkan struktur kerangka tiga dimensi gel telah tertata
dengan baik. Pengukuran viskositas sediaan gel dilakukan menggunakan
vis-cotester Rion seri VT dengan menggunakan rotor nomor 2. Berdasarkan data
200-300 dPas, sehingga dapat dikatakan bahwa gel yang dibuat tidak terlalu
ken-tal maupun tidak terlalu encer.
Tabel V. Data Uji Sifat Fisik, Q3jam, dan Fluks
Formula pH Viskositas (d.Pas)
D. Uji Iritasi Primer dengan Metode Draize Test
Uji iritasi primer sediaan gel anti-ageing ekstrak tempe dilakukan untuk
mengetahui efek dari sediaan dalam mengiritasi kulit. Sediaan yang mengiritasi
kulit cenderung tidak dapat digunakan selama periode waktu tertentu karena
adanya kecenderungan pemakai untuk menghentikan penggunaan bila terjadi
reaksi iritasi. Sifat mengiritasi dapat berasal dari gesekan mekanis, pH sediaan,
maupun sifat kimia dari bahan yang terkandung di dalam formula.
Penelitian ini menggunakan kelinci albino sebagai hewan percobaan
karena tidak memiliki pigmen sehingga lebih mudah dalam pengamatan efek
iri-tasi. Iritasi yang timbul ditandai dengan adanya eritema dan edema pada area kulit
yang telah diberi gel.
Tabel VI. Hasil indeks iritasi primer
Kelinci Indeks iritasi primer Kriteria
Hasil uji iritasi primer gel anti-ageing ekstrak tempe menunjukkan
bahwa pada semua formula memberikan nilai indeks iritasi primer 0. Hasil ini
menunjukkan bahwa keempat formula tidak mengiritasi pada kulit sehingga aman
digunakan.
E. Uji Penetrasi Sediaan Gel dengan Metode Franz Diffusion Cell
Uji penetrasi bertujuan untuk mengetahui banyaknya zat aktif (isoflavon)
yang dapat menembus ke dalam kulit. Uji penetrasi ini dilakukan secara in vitro
dengan metode Franz diffusion cell. Uji penetrasi ini juga bertujuan untuk
menge-tahui pengaruh gliserin sebagai chemical penetration enhancer dalam
mening-katkan penetrasi obat melalui membran kulit mencit dari sediaan gel.
Membran yang digunakan yaitu kulit bagian abdomen mencit jantan
galur Swiss yang berumur 2-3 bulan dengan luas membran 4,867 cm2. Kulit men-cit yang digunakan dalam uji ini mudah didapatkan dan mempunyai permeabilitas
yang mirip dengan permeabilitas kulit manusia. Preparasi kulit mencit awalnya
dicukur kemudian dihilangkan lemak subkutannya agar tidak mengganggu uji
penetrasi. Setelah itu kulit dikondisikan dalam larutan Na fisiologis 0,9% selama
maksimal 24 jam. Ketika kulit akan digunakan, kulit dikondisikan pada medium
reseptor yaitu buffer fosfat pH 7,4 : etanol (7:3). Buffer fosfat pH 7,4 digunakan
sebagai cairan reseptor karena simulasi kondisi pH cairan biologis manusia.
Membran dipastikan telah kontak dengan cairan kompartemen reseptor
agar sediaan yang diaplikasikan dapat berpenetrasi menembus kulit menuju cairan
antara membran dengan cairan yang dapat menghalangi penetrasi zat aktif ke
kompartemen reseptor. Pada kompartemen perlu dilakukan pengadukan
meng-gunakan magnetik stirer yang berfungsi untuk homogenisasi.
Setiap formula gel masing-masing diuji in vitro dengan menggunakan sel
difusi selama 3 jam dengan 4 kali pencuplikan yaitu pada jam ke 0,5; 1; 2; dan 3.
Lama pengujian selama 3 jam ini diasumsikan seperti lama menempelnya gel di
kulit setelah diaplikasikan serta dengan waktu 3 jam ini, isoflavon dapat masuk ke
dalam kulit. Sampel yang diambil sebanyak 0,6 mL dari kompartemen, kemudian
segera tambahkan 0,6 mL cairan kompartemen baru ke dalam sel difusi untuk
menjaga volume cairan tetap konstan selama percobaan berlangsung. Pengukuran
sampel dilakukan menggunakan KCKT dengan fase gerak metanol : air (70:30)
dengan flow rate 0,7 ml/menit (Orhan, et al., 2011) pada panjang gelombang
269 nm.
Uji penetrasi secara in vitro memiliki dua parameter yaitu jumlah
kumu-latif zat yang terpenetrasi dan fluks (laju penetrasi). Hasil kumukumu-latif penetrasi
ek-strak isoflavon tempe melalui membran kulit mencit selama 3 jam dari sediaan
gel dapat dilihat pada tabel V. Berdasarkan data pada tabel V didapatkan bahwa
jumlah isoflavon yang terpenetrasi terbanyak yaitu pada sediaan formula 1 dengan
konsentrasi gliserin 0. Hal ini disebabkan karena dengan penambahan gliserin
yang semakin banyak maka viskositas sediaan pun bertambah, kecuali pada
formula 2 dan 3, sehingga dimungkinkan zat aktif (ekstrak tempe) tidak dapat
Fluks diperoleh pada keadaan steady state dengan mengikuti kaidah
hu-kum Fick. Jumlah hu-kumulatif obat terpenetrasi melalui membran mencit diplotkan
terhadap waktu dan dibuat persamaan regresi linear sehingga dapat ditentukan
nilai fluks isoflavon tempe. Fluks ditentukan dari kemiringan grafik tersebut pada
keadaan steady state dimana terlihat sebagai satu garis mendatar pada kurva fluks
yang diplotkan terhadap satuan waktu. Nilai fluks yang diperoleh dapat dilihat
pada Tabel V.
Berdasarkan Tabel V didapatkan bahwa formula 1 memiliki nilai fluks
lebih tinggi daripada formula yang lainnya selama 3 jam percobaan. Hal ini berarti
bahwa formula 1 memiliki kecepatan penetrasi obat yang lebih tinggi.
Gambar 13. Kurva hubungan antara waktu dengan jumlah kumulatif
Jumlah terpenetrasi yang lebih tinggi pada formula 1 yang tidak
men-gandung gliserin memiliki nilai viskositas yang lebih rendah dan mempunyai