UJI POTENSI ANTIBAKTERI EKSTRAK ETANOL UMBI BINAHONG (Anredera cordifolia (Tenore) Steen)
TERHADAP Staphylococcus aureus ATCC 25923 dan Pseudomonas aeruginosa ATCC 27853
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh:
Martina Herlianawati NIM : 038114009
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
Setiap masalah yang terjadi
adalah
proses, tantangan, dan pilihan
untuk tidak menyerah pada keadaan.
Kita yang harus mengendalikan keadaan,
dan bukan keadaan
yang mengendalikan kita.
Jadi, jalani dengan maksimal
karena
Tuhan
punya cara sendiri
untuk melihat dan menilainya
.Le Gra,
Karyaku ini ada untuk:
My Lord Jesus and My Holy Marry, Papa, Mama, Sisca, Seluruh Sahabat dan Kerabat,
serta Almamaterku
INTISARI
Binahong Anredera cordifolia (Tenore) Steen, secara empiris digunakan masyarakat untuk menyembuhkan beberapa penyakit salah satu diantaranya adalah untuk mengobati infeksi pada luka. Penyebab yang paling umum pada infeksi kulit yang terluka adalah Staphylococcus aureus dan Pseudomonas aeruginosa. Oleh karena itu perlu dilakukan penelitian untuk mengetahui potensi ekstrak etanol umbi binahong terhadap Staphylococcus aureus dan Pseudomonas aeruginosa. Selain itu perlu diketahui pula kandungan kimia dalam umbi binahong yang berperan sebagai senyawa antibakteri. Maka dilakukan uji tabung dari serbuk umbi binahong dan ui KLT dari ekstrak etanol.
Penelitian ini termasuk penelitian eksperimental murni rancangan acak lengkap pola satu arah. Subyek uji dalam penelitian ini adalah Staphylococcus aureus ATCC 25923 yang merupakan bakteri gram positif dan Pseudomonas aeruginosa ATCC 27853 yang merupakan bakteri gram negatif. Penentuan aktivitas antibakteri umbi binahong dilakukan dengan metode difusi paperdisk. Sedangkan penentuan Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) ekstrak umbi binahong dilakukan dengan metode dilusi padat. Uji kandungan kimia terhadap serbuk umbi binahong dilakukan dengan uji tabung dan uji kandungan kimia ekstrak etanol umbi binahong dilakukan dengan metode Kromatografi Lapis Tipis (KLT). Analisis hasil KLT dilakukan secara deskriptif komparatif.
Hasil penelitian dengan metode difusi menunjukkan bahwa ekstrak etanol umbi binahong tidak memiliki potensi antibakteri. Berdasarkan uji tabung, serbuk umbi binahong diketahui mengandung flavonoid, alkaloid, polifenol, tanin, dan saponin. Untuk uji KLT, diketahui bahwa ekstrak etanol umbi binahong mengandung flavonoid, polifenol, tanin dan saponin.
Kata kunci : potensi antibakteri, umbi binahong, Staphylococcus aureus, Pseudomonas aeruginosa, uji tabung, uji KLT
ABSTRACT
Binahong Anredera cordifolia (Tenore) Steen empirically are used to threat some illness, one of them is to threat wound infection. Usually, wound infection ware caused by Staphylococcus aureus and Pseudomonas aeruginosa. So it was needed to research the potency of ethanolic extract of binahong’s tubers against Staphylococcus aureus and Pseudomonas aeruginos. Beside that, the tubes test and the TLC test were needed to know the chemical contents of binahong tubers which can be used as a antibacterial agent.
This research was a pure experimental research with the one way pattern of complete-random research design. The subject in this research were
Staphylococcus aureus ATCC 25923 which is positive gram bacterial and
Pseudomonas aeruginosa ATCC 27853 which is negative gram bacterial. Antibacterial activity was determined by diffusion method using paperdisk. Whereas, the Minimum Inhibitory Consentration (MIC) and Minimum Bacterisidal Consentration (MBC) of ethanolic extract of binahong’s tubers were conducted by solid dilution method. The identification of chemical contents of powders of binahong’s tubers was conducted by tubes test and the ethanolic extract of binahong’s tuber was conducted by TLC test. The result of TLC test was analysed using comparative-descriptive analysing method.
The result showed that the ethanolic extract of binahong’s tuber has not antibacterial activities against Staphylococcus aureus and Pseudomonas aeruginosa. Based on the tube test, the powder of binahong’s tubers maybe contain flavonoid, alkaloid, polyphenol, tannin, and saponin. The TLC result showed that the ethanolic extract of binahong’tuber contents of flavonoid, polyphenol, tannin, and saponin.
Keyword : Antibacterial potency, binahong’s tubers, Staphylococcus aureus Pseudomonas aeruginosa, tubes test, TLC test
KATA PENGANTAR
Kasih dan karunia-Nya yang berlimpah, membuat penulis tak henti-hentinya mengucap puji dan syukur atas terselesaikannya skripsi dengan judul UJI POTENSI ANTIBAKTERI EKSTRAK ETANOL UMBI BINAHONG
(Anredera cordifolia (Tenore) Steen) TERHADAP Staphylococcus aureus
ATCC 25923 dan Pseudomonas aeruginosa ATCC 27853ini.
Penyusunan skripsi ini merupakan syarat untuk mendapatkan gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Semua yang tertuang dalam skripsi ini diperoleh dengan kerja keras dan tidak lain karena peran, bantuan, bimbingan, motivasi, dukungan, dan doa dari beberapa pihak, dan karenanya, penulis ingin mengucapkan terimakasih kepada:
1. Ibu Rita Suhadi, M.Si., Apt selaku Dekan Fakultas Farmasi Sanata Dharma,
2. Ibu Erna Tri Wulandari, M.Si., selaku dosen pembimbing yang sudah meluangkan waktu dan perhatian, serta banyak membantu selama diskusi, bimbingan, dan revisi,
3. Bapak Ign. Y. Kristio Budiasmoro, M.Si, selaku dosen penguji atas diskusi dan masukan kepada penulis,
4. Bapak Yohanes Dwiatmaka, M.Si, selaku dosen penguji atas diskusi dan masukan kepada penulis,
5. Papa dan mama tercinta, Fx. Untung Puryanto dan Tarsicia Sri Setyani atas kesabaran dan kepercayaan yang mungkin sedikit terkikis, tulusnya
doa dan cinta, dukungan moral dan material, serta semangat yang mengiringi langkah penulis,
6. Satu-satunya adik ‘kecil’ku Fransisca Kurnianingsih, atas telinga, hati, dan pikiran yang selalu menjadi jawaban atas segala keluh kesahku,
7. Nella, seorang sahabat, tempat curhat, mbak, dan teman se‘binahong’ atas seluruh moment yang terjadi dan segala pengalaman yang membuat kita lebih kaya dalam memaknai hidup.
8. Mas Wahyu, Meta, Mas Alfren dan Budhe, Pakdhe terimakasih banyak atas perhatian, waktu, dan tenaga yang tersita untukku.
9. Mas Sarwanto, Mas Wagiran, Mas Sigit, dan Mas Andre, laboran sekaligus teman dalam canda dan kerjasama selama penelitian
10.Sahabat-sahabat hatiku, Johan, Wati, Ratih, Totok, Bambang, Ana, Tusti, Tica, Ceu Sri, Bernan, Mas Wondo, Bayu, dan Top-X, atas senyum, canda, tawa, tangis, perhatian, dan semangat yang pernah, masih dan selalu ada buat aku. You make me standing still with everything you do, Thanks a lot guys…
11.Teman-teman baikku, Otong, Surya, Evelyn, Beni, Rinto, Punto, Sutaman, Kris, Helmi, De Eya, Nice, De Esti, Agnes, dik Henong, mb Dinta, mb Devi, Vivi, Dewi&albert, Rosalia Guruh, Vian, Sakundita, Yohana, Netly, Bangun, mb Obe, abang Franky, pakdhe Muji, Ci’ Mey, Mba Endar, Jeng Fitri, dan Pak Ciek Hendro, atasdetik, menit, hari, bulan, dan tahun yang menyertai kebersamaan kita. Without you all,I’m nothing.
12.Every single guy in : The 10th generation of VL, Wisma Rosari, Farmasi 2003, Kelompok Praktikum A, Tim layat kelas A, kelp. KKN Ceporan angkatan XXXIII, asisten mikro 2006/2007, dan Skripsi Lantai 3 atas untaian cerita yang mengisi hari-hariku,
13.Dan semua pihak yang langsung ataupun tidak langsung sudah membantu dalam penyusunan skripsi ini.
Penulis menyadari bahwa skripsi ini jauh dari sempurna, untuk itu penulis dengan rendah hati mohon maaf apabila terdapat kesalahan dalam penulisan, dan untuk itu, penulis menerima segala kritik maupun saran yang membangun.
Akhirnya penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan pada umumnya dan semua orang yang membaca skripsi ini pada khususnya.
Tuhan memberkati.
Yogyakarta, Juni 2007 Penulis,
Martina Herlianawati
DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
INTISARI ... vi
DAFTAR LAMPIRAN ... xviii
BAB I. PENGANTAR ... 1
A. Binahong Anredera cordifolia (Tenore) Steen ... 6
1. Deskripsi ... 6
2. Ekologi dan penyebaran ... 7
3. Kandungan Kimia ... 7
4. Kegunaan ... 7
B. Penyarian ... 8
C. Ekstrak Etanol ... 9
D. Sterilisasi ... 10
E. Bakteri Uji ... 11
1. Staphylococcus aureus ... 11
2. Pseudomonas aeruginosa ... 12
F. Amoksisilin ... 12
G. Metode Pengujian Potensi Antibakteri ... 13
H. Kromatografi Lapis Tipis ... 16
I. Flavonoid ... 18
J. Akaloid ... 19
K. Senyawa Polifenol ... 20
L. Tanin ... 21
M. Saponin ... 22
N. Keterangan Empiris ... 23
BAB III. METODOLOGI PENELITIAN ... 24
A. Jenis dan Rancangan Penelitian ... 24
B. Variabel dan Definisi Operasional ... 24
1. Variabel Penelitian ... 24
2. Definisi Operasional ... 25
C. Bahan dan Alat Penelitian ... 26
1. Bahan ... 26
2. Alat ... 27
D. Jalannya Penelitian ... 27
1. Determinasi Tanaman Binahong ... 27
2. Pengumpulan Bahan ... 28
3. Penyerbukan Bahan ... 28
4. Pembuatan Ekstrak Etanol dengan Metode Maserasi ... 28
5. Skrining Fitokimia ... 28
a. Uji Tabung ... 29
b. Uji kualitatif secara Kromatografi Lapis Tipis ... 31
6. Uji Potensi Antibakteri Ekstrak Etanol Umbi Binahong terhadap Staphylococcus aureus dan Pseudomonas aeruginosa ... 34
E. Analisis Data ... 36
BAB IV. HASIL DAN PEMBAHASAN ... 37
A. Determinasi ... 37
B. Pengumpulan dan Penyerbukan Bahan ... 37
C. Pembuatan Ekstrak dengan Metode Maserasi ... 38
D. Skrining Fitokimia ... 41
1. Uji Tabung ... 41
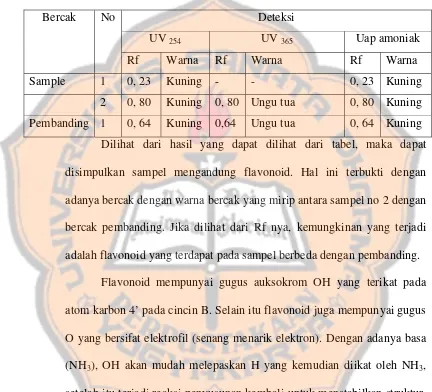
2. Uji Kualitatif secara Kromatografi Lapis Tipis ... 46
E. Uji potensi antibakteri ekstrak etanol umbi binahong terhadap
Staphylococcus aureus ATCC 25923 dan Pseudomonas aeruginosa
ATCC 27853 ... 53
BAB V. KESIMPULAN DAN SARAN ... 58
A. Kesimpulan ... 58
B. Saran ... 58
DAFTAR PUSTAKA ... 59
LAMPIRAN ... 62
BIOGRAFI PENULIS ... 79
DAFTAR TABEL
Tabel I Pembuatan Variasi Konsentrasi Uji ... 35 Tabel II Hasil pengamatan uji tabung terhadap serbuk
umbi binahong ... 41 Tabel III Nilai Rf dan warna bercak pada uji KLT dengan fase
diam silika gel GF 254 dan fase gerak butanol : asam asetat : air (4:1:5 ) dan pembanding rutin 0,05%
untuk analisis flavonoid ... 47 Tabel IV Nilai Rf dan warna bercak pada uji KLT dengan fase diam
silika gel GF 254, fase gerak etil asetat : methanol : air (70:20:10)dan pembanding skopolamin untuk analisis
alkaloid……….. 49 Tabel V Nilai Rf dan warna bercak pada uji KLT dengan fase diam
silika gel GF 254, fase gerak toluen, etil asetat, metanol (70:20:10) dan pembanding eugenol untuk analisis
senyawa fenolik……… ... 50 Tabel VI Nilai Rf dan warna bercak pada uji KLT dengan fase diam
silika gel GF 254, fase gerak etil asetat : metanol : air (100 : 13,5 : 10) dan pembanding asam tanat untuk
analisis tanin………... 51 Tabel VII Nilai Rf dan warna bercak pada uji KLT dengan fase diam
silika gel GF 254, fase gerak toluen : etil asetat (93:7) dan
pembanding Glycyrrhiza Radix untuk analisis saponin………. 52
Tabel VIII Diameter zona hambat ekstrak etanol umbi binahong
terhadap Staphylococcus aureus ATCC 25923……… 55 Tabel IX Diameter zona hambat ekstrak etanol umbi binahong
terhadap Pseudomonas aeruginosa ATCC 27853……… 56
DAFTAR GAMBAR
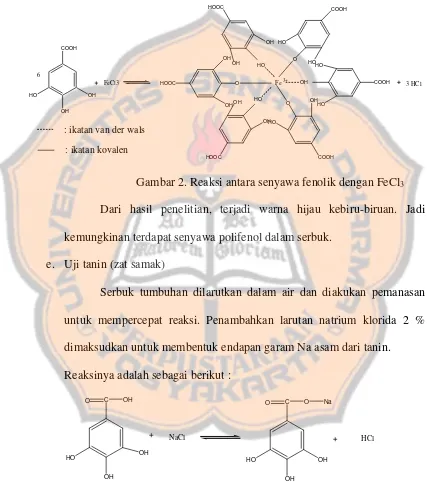
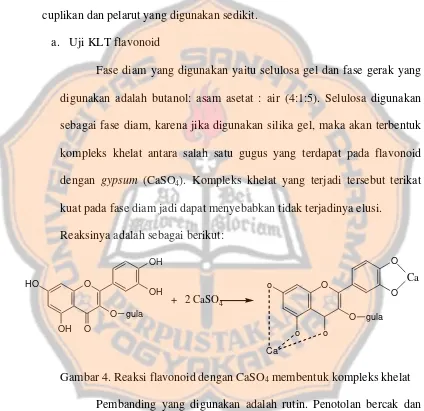
Gambar 1. Kerangka Flavonoid ………. 18 Gambar 2. Reaksi antara Senyawa Fenolik dengan FeCl3……... 44 Gambar 3. Reaksi antara NaCl dengan Senyawa fenolik ……….. 44 Gambar 4. Reaksi flavonoid dengan CaSO4 membentuk
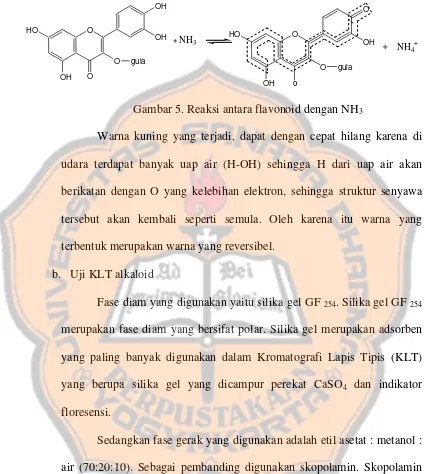
kompleks khelat……… 46 Gambar 5. Reaksi antara Flavonoid dengan NH3 ………. 48
DAFTAR LAMPIRAN
Lampiran 1. Surat Keterangan Selesai Melakukan Determinasi dari
BalaiPenelitian Tanaman Obat... 62 Lampiran 2. Determinasi Tanaman Binahong (Anredera cordifolia
(Tenore) Steen)... 63 Lampiran 3. Foto Tanaman Binahong (Anredera cordifolia (Tenore)
Steen) dan foto serbuk umbi binahong... 64 Lampiran 4. Foto Hasil Uji Pendahuluan Serbuk Umbi Binahong
Dengan UjiTabung ... 65 Lampiran 5. Foto Hasil Uji Alkaloid Serbuk Umbi Binahong
Dengan UjiTabung ... 66 Lampiran 6. Foto Hasil Uji Antrakinon Serbuk Umbi Binahong
Dengan Uji Tabung ... 67 Lampiran 7. Foto Hasil Uji Polifenol Serbuk Umbi Binahong
Dengan UjiTabung ... 68 Lampiran 8. Foto Hasil Uji Tanin Serbuk Umbi Binahong
Dengan Uji Tabung ... 69 Lampiran 9. Foto Hasil Uji Saponin Serbuk Umbi Binahong
Dengan Uji Tabung ... 70 Lampiran 10. Foto Hasil KLT Ekstrak Etanol Umbi Binahong dengan
Deteksi UV 254, UV 365, dan uap amoniak pada
Analisis Flavonoid ... 71
Lampiran 11. Foto Hasil KLT Ekstrak Etanol Umbi Binahong dengan Deteksi UV 254, UV 365, pereaksi Dragendorf pada
Analisis Alkaloid ... 72 Lampiran 12. Foto Hasil KLT Ekstrak Etanol Umbi Binahong dengan
Deteksi UV 254, UV 365, dan pereaksi FeCl3 pada Analisis Polifenol ... 73 Lampiran 13. Foto Hasil KLT Ekstrak Etanol Umbi Binahong dengan
Deteksi UV 254, UV 365, dan pereaksi FeCl3 pada Analisis Tanin ... 74 Lampiran 14. Foto Hasil KLT Ekstrak Etanol Umbi Binahong dengan
Deteksi UV 254, UV 365, dan pereaksi Anisaldehid Asam
Sulfat pada Analisis Saponin ... 75 Lampiran 15. Foto Hasil Uji Potensi Antibakteri Ekstrak Etanol Umbi
Binahong terhadap Staphylococcus aureus ATCC 25923
Dengan Metode Difusi Paperdisk ... 76 Lampiran 16. Foto Hasil Uji Potensi Antibakteri Ekstrak Etanol Umbi
Binahong terhadap Pseudomonas aeruginosa ATCC 27853 Dengan Metode Difusi Paperdisk ... 77 Lampiran 17. Foto Kontrol Pertumbuhan Staphylococcus aureus
ATCC 25923 dan Kontrol pertumbuhan Pseudomonas
aeruginosa ATCC 27853 ... 78
BAB I
PENGANTAR
A. Latar Belakang Masalah
Tumbuhan obat dan obat tradisional (OT) merupakan aset nasional yang perlu terus digali, diteliti, dikembangkan dan dioptimalkan pemanfaatannya. Untuk itu perlu dilakukan penelitian dan pengembangan tanaman obat dan obat tradisional dalam sistem pelayanan kesehatan formal (Sumaryono, 2000). Penggunaan obat tradisional memiliki kelebihan antara lain yaitu bahannya mudah didapat, murah dan dapat diramu sendiri. Karena alasan itulah masyarakat berusaha memanfaatkan alam sekitar untuk memenuhi kebutuhan obat ketika menderita sakit.
Binahong (Anredera cordifolia (Tenore) Steen merupakan tanaman yang mudah didapatkan. Binahong sangat mudah tumbuh di beberapa kondisi secara vegetatif, mempunyai karakteristik agresif dan sulit dikendalikan. Hal ini dikarenakan umbi sebagai alat reproduksi secara vegetatif tumbuh di dalam maupun di atas tanah (Vivian et al, 2005).
Dalam kehidupan sehari-hari, masyarakat mengenal binahong sebagai tanaman yang dapat digunakan untuk mengobati beberapa penyakit. Namun penggunaan binahong tersebut belum dibuktikan sampai tahap uji klinik. Penelitian yang pernah dilakukan, mengemukakan bahwa ekstrak kloroform dari herba binahong Anredera cordifolia (Tenore) Steen dapat menghambat
pertumbuhan beberapa bakteri (Meyer, 2004). Sedangkan dalam masyarakat, penggunaannya hanya secara empiris yaitu berupa perasan, rebusan, seduhan, dimakan secara langsung, maupun dioleskan pada daerah yang akan diobati. Binahong dipercaya dapat menyembuhkan beberapa penyakit antara lain sebagai obat antiinflamasi, anti-ulcer, obat untuk menyembuhkan luka dan juga dapat sebagai liver-protective. Selain itu juga digunakan untuk mengobati infeksi pada luka (Anonim, 2006a).
Infeksi pada luka itu sendiri terjadi karena fungsi kulit sebagai pertahanan (barrier) hilang. Hilangnya pertahanan kulit dan terkelupasnya lapisan jaringan di bawah kulit yang basah dan kaya akan nutrien merupakan hal yang ideal untuk kolonisasi bakteri pada area kulit yang terluka atau terbakar. Penyebab yang paling umum pada infeksi kulit yang terluka adalah Pseudomonas aeruginosa dan
Staphylococcus aureus (Naim, 2006). P. aeruginosa merupakan bakteri gram negatif sedangkan S. aureus merupakan gram positif (Jawetz, Melnick, dan Adelberg, 1996).
Seperti telah disebutkan di atas, pada penelitian sebelumnya digunakan kloroform untuk menyari senyawa yang terdapat dalam herba binahong. Kloroform merupakan penyari yang bersifat non polar, sehingga senyawa-senyawa yang tersari dimungkinkan hanya senyawa-senyawa-senyawa-senyawa yang bersifat non polar. Untuk itu dalam penelitian ini, digunakan etanol yang bersifat semi polar. Dengan demikian senyawa-senyawa yang tersari tidak hanya yang bersifat non polar tetapi juga yang bersifat polar.
Pada penelitian sebelumnya, bahan yang digunakan berupa herba binahong. Untuk iu perlu diketahui bagian mana dari herba binahong tersebut yang dapat menghambat pertumbuhan bakteri. Oleh karena itu, penulis melakukan penelitian mengenai ekstrak etanol umbi binahong, terutama potensinya sebagai antibakteri terhadap S. aureus dan P. Aeruginosa, sehingga dapat diketahui khasiat dari umbi binahong sebagai obat menyembuhkan infeksi pada luka.
1. Permasalahan
Ditinjau dari latar belakang yang ada, maka permasalahan yang ingin diangkat dalam penelitian ini adalah:
1. Apakah ekstrak etanol umbi binahong berpotensi sebagai antibakteri terhadap S. aureus dan P. aeruginosa?
2. Berapa besar Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) dari ekstrak etanol umbi binahong terhadap S. aureus dan P. aeruginosa ?
3. Kandungan kimia apa sajakah yang terdapat di dalam umbi binahong yang bermanfaat sebagai antibakteri?
2. Manfaat penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan sumbangan ilmiah terutama mengenai tanaman obat baru yang dapat dikembangkan menjadi obat tradisional dan fitofarmaka.
b. Manfaat praktis
Penelitian ini diharapkan dapat menjadi sumbangan yang berharga untuk mendalami pengobatan penyakit infeksi yang disebabkan oleh S. aureus
dan P. aeruginosa dengan menggunakan tanaman yang berpotensi digunakan sebagai obat.
3. Keaslian penelitian
Sejauh penelusuran pustaka dan pengamatan peneliti, pernah dilakukan penelitian mengenai potensi antibakteri ekstrak kloroform dari herba Anredera cordifolia (Tenore) Steen terhadap Bacillus cereus, Bacillus pulmilus, Bacillus subtilis, Staphylococcus aureus, Enterobacter cloacae, Escherichia coli,
Klebsiella pneumoniae, Pseudomonas aeruginosa, Serratia marcescens, dan
Enterobacter aerogenes (Meyer, 2004). Bahan yang digunakan dalam penelitian tersebut adalah herba dari binahong, maka perlu dilakukan penelitian mengenai potensi antibakteri dari salah satu organ tanaman binahong terhadap bakteri penyebab infeksi pada luka dalam hal ini yaitu umbinya.
B. Tujuan penelitian Penelitian ini bertujuan untuk:
1. Mengetahui ada tidaknya potensi antibakteri ekstrak etanol umbi binahong terhadap S. aureus dan P. aeruginosa.
2. Mengetahui Konsentrasi Hambat Minimum dan Konsentrasi Bunuh Minimum ekstrak etanol umbi binahong pada pertumbuhan S. aureus dan
P. aeruginosa.
3. Mengetahui kandungan kimia yang terdapat di dalam umbi binahong yang bermanfaat sebagai senyawa antibakteri secara kualitatif melalui uji tabung dan uji Kromatografi Lapis Tipis.
BAB II
TINJAUAN PUSTAKA
A. Anredera cordifolia (Tenore) Steen
1. Deskripsi
Binahong merupakan tumbuhan yang termasuk dalam familia
Basellaceae, genus Anredera, dengan nama spesies Anredera cordifolia
(Tenore) Steen. Sinonim dari Anredera cordifolia (Tenore) Steen adalah
Boussingaultia baselloides Auct.non H.B.K, Boussingaultia gracillis Miers,
Boussingaultia pseudobasselloides (Vivian, 2005).
Di beberapa negara binahong dikenal sebagai ‘uala hupe, anredera,
enredarera del mosquito, filikafa, Gulf madeiravine, hearthleaf madeiravine,
lamb’s tails, Madeira vine, mignonette vine, parra de Madeira (Vivian, 2005).
Habitus; herba, menjalar, panjang mencapai lima meter. Batang; lunak,
warna merah tua kehijauan, permukaan halus dan licin, pada bagian aksiler
daun, tumbuh umbi tunggal maupun berkelompok. Daun; tunggal, tata letak
daun tersebar, permukaan daun halus dan licin, daging daun tebal, warna hijau
muda, pertulangannya menyirip, helaian daun bentuk jantung, ujung runcing,
tepi rata – bergelombang, pangkal berbelah, panjang helaian 2-10 cm, lebar
1-7 cm, panjang tangkai daun kurang lebih 1 cm. Bunga; majemuk, bentuk
tandan atau malai bercabang, panjang perbungaan 10 -35 cm, daun kelopak
pada bagaian basal berlekatan dengan daun mahkota, putih – krem, bentuk
oval – memanjang, panjang 1- 2 mm, lebar 1 mm, ujung membulat, daun
mahkota pada bagain basal berlekatan, putih – krem, bentuk oval – membulat,
panjang 2-3 mm, lebar 1-2 mm, benang sari; berdaging, tangkai sari pada
bagian basal berlekatan, panjang 2-4 mm, putik; satu panjang 1-2 mm. Akar;
tunggang (Backer, 1968)
2. Ekologi dan Penyebaran
Binahong hidup liar di hutan, ladang, dan padang rumput. Tumbuh
tersebar di berbagai kawasan di dunia termasuk di antaranya di Afrika,
Australia dan wilayah Pasifik, Eropa, dan Amerika. Tumbuhan ini sangat
mudah tumbuh di beberapa kondisi secara vegetatif, mempunyai karakteristik
agresif dan sulit dikendalikan. Hal ini dikarenakan umbi sebagai alat
reproduksi secara vegetatif tumbuh di dalam maupun di atas tanah (Vivian,
2005).
3. Kandungan Kimia
Binahong mengandung asam askorbat dan fenol dalam jumlah kecil
(Sato, Nagata, dan Engle, 2005). Basellaceae lainnya yaitu Anredera diffusa
mengandung asam oleanolic yang berperan dalam proses penyembuhkan luka
(Moura-Letts dan Marcalo,2006). Selain itu, terdapat pula serat, karbohidrat,
air, protein, abu, flavonoid, dan lendir pada Anredera baselloides (Anonim,
2006b).
4. Kegunaan
Secara empiris binahong digunakan untuk menyembuhkan beberapa
penyakit antara lain sebagai obat antiinflamasi, anti-ulcer, menyembuhkan
luka dan juga dapat sebagai liver-protective. Selain itu juga digunakan untuk
mengobati infeksi pada luka (Anonim, 2006a). Ada pula penelitian yang
mengemukakan bahwa ekstrak kloroform dari herba (Anredera cordifolia
(Tenore) Steen dapat menghambat pertumbuhan beberapa bakteri (Meyer,
2004).
B. Penyarian
Penyarian adalah kegiatan penarikan zat yang dapat larut dari bahan yang
tidak dapat larut dengan pelarut cair. Faktor yang mempengaruhi kecepatan
penyarian adalah kecepatan difusi zat yang larut melalui lapisan-lapisan batas
antara cairan penyari dengan bahan yang mengandung zat tersebut. Zat aktif yang
terdapat dalam berbagai simplisia dapat digolongkan ke dalam alkaloida,
glikosida, flavonoid dan lain-lain. (Anonim, 1986). Cara penyarian dapat
dibedakan menjadi :
1. Infundasi
Infundasi adalah proses penyarian (menyari simplisia dengan air
pada suhu 90oC selama 15 menit) yang umumnya digunakan untuk
menyari zat kandungan aktif yang larut dalam air dari bahan-bahan nabati
(Anonim, 1986).
2. Maserasi
Maserasi dilakukan dengan cara merendam serbuk simplisia dalam
cairan penyari. Cairan penyari akan menembus dinding sel dan masuk ke
dalam rongga sel yang mengandung zat aktif. Zat aktif akan larut dan
karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel
dengan yang di luar sel, maka larutan yang terpekat didesak keluar.
Peristiwa tersebut berulang sehingga terjadi keseimbangan konsentrasi
antara larutan di luar sel dan di dalam sel (Anonim,1986).
3. Perkolasi
Perkolasi adalah cara penyarian yang dilakukan dengan
mengalirkan cairan penyari melalui serbuk simplisia. Prinsip perkolasi
adalah sebagai berikut : serbuk simplisia ditempatkan dalam suatu bejana
silinder, yang bagian bawahnya diberi sekat berpori. Cairan penyari
dialirkan dari atas ke bawah melalui serbuk tersebut, cairan penyari akan
melarutkan zat aktif sel-sel yang dilalui sampai mencapai keadaan jenuh.
Gerak ke bawah disebabkan oleh kekuatan gaya beratnya sendiri dan
cairan diatasnya, dikurangi daya kapiler yang cenderung untuk menahan
(Anonim, 1986).
C. Ekstrak etanol
Tahap awal pemisahan suatu senyawa dari suatu tumbuhan dapat disebut
sebagai ekstraksi. Faktor yang perlu dipertimbangkan dalam pemilihan metode
ekstraksi antara lain kesesuaian antara senyawa kimia yang terkandung dalam
bahan dengan sifat pelarut yang digunakan (Houghton dan Raman, 1998).
Dalam buku Farmakope Indonesia Edisi IV, disebutkan bahwa ekstrak
adalah sediaan kental yang diperoleh dengan mengekstraksi senyawa aktif dari
simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan masa serbuk yang
tersisa diperlakukan sedemikian sehingga memenuhi baku yang telah ditetapkan
(Anonim, 2000a).
Pelarut yang sering digunakan untuk ekstraksi adalah etanol. Etanol
(C2H5OH) merupakan cairan yang mudah menguap, jernih, dan tidak berwarna.
Sebagai pelarut, etanol mempunyai kelebihan antara lain mempunyai toksisitas
rendah dibanding metanol, lebih stabil dan lebih murah. Etanol bersifat semipolar,
maka dapat digunakan untuk mengekstrasi senyawa-senyawa yang bersifat polar
dan non polar (Houghton dan Raman, 1998).
D. Sterilisasi
Sterilisasi ialah suatu proses untuk mematikan semua mikroorganisme
yang terdapat pada atau di dalam suatu benda. Pemilihan metode sterilisasi
didasarkan pada sifat bahan yang akan disterilkan (Pelczer dan Chan, 1986 )
Cara umum yang sering digunakan untuk sterilisasi, antara lain:
1. Sterilisasi dengan panas
Cara ini paling banyak digunakan. Dapat digunakan untuk
sterilisasi baik alat maupun media. Sterilisasi dengan panas dapat
dibedakan menjadi tiga jenis, yaitu: dengan udara panas kering, panas
lembab, dan pemijaran (Pelczer dan Chan, 1986 ). Untuk sterilisasi
dengan udara panas kering, rentang suhu yang khas yang dapat
diterima di dalam bejana sterilisasi kosong adalah lebih kurang 15
menit, jika alat sterilisasi beroperasi pada suhu tidak kurang dari 250oC
sedangkan untuk proses satu siklus autoklaf yang ditetapkan dalam
Farmakope Indonesia untuk media atau pereaksi adalah selama 15
menit pada suhu 121oC (Anonim, 1994).
2. Sterilisasi dengan penyaringan
Sterilisasi ini digunakan untuk bahan-bahan yang sangat peka
terhadap pemanasan (serum, antibiotika, toksin) atau bahan yang
relatif tidak tahan terhadap pemanasan tinggi (medium yang
mengandung senyawa gula). Untuk keperluan ini dibutuhkan alat filter
atau saringan bakteri.
3. Sterilisasi dengan bahan kimia
Bahan yang mudah rusak apabila disterilkan pada suhu tinggi,
dapat disterilkan secara kimia dengan menggunakan gas radiasi. Bahan
kimia yang digunakan untuk sterilisasi gas antara lain etilanoksida,
asam parasetat, formaldehid, dan glutaraldehide alkalin (Suriawinata,
1986).
E. Bakteriuji
1. Staphylococcus aureus
S. aureus termasuk dalam familia Micrococcaceae adalah bakteri
dengan sel-sel berbentuk bola dengan garis tengah sekitar 1µm dan tersusun
dalam kelompok-kelompok tak beraturan. Pada biakan cairan tampak juga
kokus tunggal, berpasangan, atau berbentuk rantai. Kokus muda bersifat gram
positif kuat, sedangkan pada biakan yang lebih tua, banyak sel menjadi gram
negatif. S aureus tidak bergerak dan tidak membentuk spora. Oleh obat-obatan
seperti penisilin S. aureus dilisiskan. S. aureus tumbuh paling cepat pada suhu
37ºC. S. aureus membentuk koloni berwarna abu-abu sampai kuning emas
(Jawetz, et al, 1996).
Bakteri ini menyebabkan penyakit pada hampir semua jaringan tubuh
yang terutama adalah abses. S. aureus merupakan flora normal pada rongga
hidung bagian depan, perineum, saluran pencernaan, atau kulit ( Jawetz, et al,
1996).
2. Pseudomonas aeruginosa
P. aeruginosa termasuk dalam familia Pseudomonadaceae berbentuk
batang, bergerak, dan merupakan bakteri gram negatif aerob yang
menghasilkan pigmen yang larut dalam air dan berdifusi melalui pembenihan
buatan, tidak meragikan laktosa, dan membentuk koloni bulat halus dengan
berfloresensi kehijau-hijauan dan bau aromatis (Jawetz, et al, 1996).
P. aeruginosa menyebabkan infeksi pada luka kulit seperti luka bakar,
dan membentuk nanah yang berwarna biru hijau, meningitis. Bakteri ini juga
dapat menginfeksi saluran kemih atau saluran pernafasan (Jawetz, et al, 1996).
F. Amoksisilin
Amoksisilin merupakan suatu antibiotik golongan beta laktam derivat
penisilin dengan spektrum luas. Amoksisilin mempunyai aktivitas bekterisida
terhadap bakteri gram positif maupun gram negatif dengan mekanisme
menghambat pembentukan atau sintesis dinding sel mikroba (Surini, 2006).
Amoksisilin ditemukan tahun 1972 merupakan antibiotik yang umum
dipakai karena cukup manjur dalam membunuh bakteri (Hendriyana, 2004).
Amoksisilin mempunyai aktivitas yang sama dengan ampisilin. Bedanya,
amoksisilin diserap di gastro intestinal lebih efektif dibandingkan ampisilin.
Ampisilin merupakan antibakteri yang mempunyai spektrum penghambatan yang
lebih luas dibanding dengan penisilin. Ampisilin dapat menghambat tidak hanya
pneumococci, meningococco, gonococci dan streptococci yang lain, tetapi juga
dapat menghambat beberapa bakteri bacillus (Harvey et all, 2003).
Untuk masing-masing antibiotik dan jenis kumannya, mempunyai
diameter yang berbeda-beda untuk dinilai sebagai antibiotik yang sensitif (poten
dalam terapi). Untuk Stapylococcus akan memberikan makna resisten terhadap
ampisilin jika diameter zona hambat yang terjadi sama atau kurang dari 20 mm
dan dinyatakan sensitif apabila diameter zona hambat yang terjadi lebih dari 29
mm. Sedangkan untuk Pseudomonas dikatakan resisten apabila diameter zona
hambatnya kurang dari atau sama dengan 11 mm dan dikatakan sensitif apabila
diameter zona hambatnya lebih dari 14 mm (Anonim, 1993).
G. Metode Pengujian Potensi Antibakteri
Bahan antibakteri secara umum diartikan sebagai bahan yang mengganggu
pertumbuhan dan metabolisme bakteri. Obat yang digunakan untuk membasmi
bakteri, penyebab infeksi pada manusia, ditentukan harus memiliki sifat toksisitas
selektif setinggi mungkin (Anonim, 1995).
Berdasarkan sifat toksisitas selektif, ada antibakteri yang bersifat
menghambat pertumbuhan bakteri, dikenal sebagai aktivitas bakteriostatik dan
ada yang bersifat membunuh bakteri, dikenal sebagai aktivitas bakterisid. Kadar
minimal yang diperlukan untuk menghambat pertumbuhan bakteri atau
membunuhnya, masing–masing dikenal sebagai Kadar Hambat Minimal (KHM)
dan Kadar Bunuh Minimal (KBM) (Anonim, 1995).
Metode pengujian potensi antibakteri dapat dibedakan menjadi 2 yaitu:
1. Metode difusi
Metode ini mengukur aktivitas mikroba berdasarkan pengamatan luas
daerah hambat pertumbuhan mikroba karena obat berdifusi dari titik awal
pemberian ke daerah difusi. Mikroba ditanam pada media yang sesuai dan di
atasnya diletakkan kertas cakram yang mengandung bahan obat atau dibuat
sumuran dengan diameter tertentu yang diisi larutan bahan obat dengan kadar
tertentu (Hugo & Russel, 1987).
Metode difusi ada tiga macam yaitu:
a. Cara Kirby Bauer
Metode ini dilakukan dengan cara mengoleskan suspensi bakteri
dengan konsentrasi tertentu, umumnya 108 Colony Forming Unit (CFU)
per ml permukaan media hingga rata. Kertas yang mengandung antibiotika
diletakkan di atas media lalu diinkubasikan pada 37ºC selama 18-24 jam,
setelah itu baca hasilnya. Potensi antibakteri ditentukan dengan mengukur
diameter zona hambatan yang terbentuk. Pada zona hambatan akan terlihat
adanya pertumbuhan yang kurang subur jika dibandingkan dengan daerah
di luar pengaruh antibiotik tersebut (Hugo dan Russel, 1987).
b. Cara sumuran
Penyiapan dilakukan seperti cara Kirby Bauer. Pada agar yang
telah diolesi bakteri uji dibuat sumuran dengan garis tengah tertentu dan
tegak lurus terhadap permukaan media. Kemudian ke dalam sumuran ini
diberi larutan uji dan diinkubasi pada 37ºC selama 24-28 jam, hasilnya
dibaca seperti cara Kirby Bauer (Hugo dan Russel, 1987).
c. Cara Pour Plate
Mula-mula satu mata ose suspensi bakteri dicampur dengan 4 ml
agar 1,5% pada temperature 50ºC. Setelah suspensi mikrobia homogen,
tuangkan di atas media agar dan dibiarkan membeku, kemudian di atasnya
diletakan disk dan diinkubasi pada suhu 37ºC selama 18-24 jam, hasilnya
dibaca dengan mengukur diameter hambat (Hugo dan Russel, 1987).
2. Metode dilusi
Ada dua macam metode dilusi yaitu:
a. Cara pengenceran serial dalam tabung (dilusi cair)
Pada cara ini zat antibakteri yang akan diuji aktivitasnya
diencerkan secara serial dengan metode pengenceran kelipatan dua di
dalam medium cair dan selanjutnya diinokulasikan dengan mikroba uji.
Setelah diinkubasi pada suhu 37ºC selama 18-24 jam untuk bakteri dan
fungi, aktivitas zat antibakteri ditentukan sebagai Konsentrasi Hambat
Minimum, yaitu konsentrasi terendah yang masih dapat menghambat
pertumbuhan mikroba (Hugo dan Russel, 1987).
b. Cara penapisan lempeng agar (dilusi padat)
Pada cara ini zat yang akan ditentukan aktivitas antibakterinya
diencerkan secara serial dengan metode pengenceran berkelipatan dua di
dalam medium agar bersuhu 40-50ºC kemudian dituangkan ke dalam
cawan petri. Setelah lempeng agar membeku, ditanamkan inokulum
mikroba dan kemudian diinkubasi pada suhu 37ºC dalam jangka waktu
yang sesuai dengan pertumbuhan mikroba yang diuji, aktivitas zat
antibakteri ditentukan sebagai Konsentrasi Bunuh Minimum yaitu
konsentrasi terendah yang masih dapat membunuh mikroba (Hugo dan
Russel, 1987).
H. KromatografiLapis Tipis
Kromatografi adalah cara pemisahan berbagai senyawa yang ada dalam
sediaan dengan jalan penyarian berfraksi, penyerapan, dan pertukaran ion, pada
zat berpori dengan menggunakan cairan atau gas yang mengalir (Stahl, 1985).
1. Kromatografi Lapis Tipis
Kromatografi Lapis Tipis merupakan salah satu metode kromatografi
cair yang paling sederhana. Kromatografi cair dapat dikembangkan dengan
pelarut tunggal atau bisa juga dengan campuran dua pelarut atau lebih (Stahl,
1985).
Absorban yang sering digunakan yaitu silika gel. Silika gel adalah
bahan yang berpori dan amorf. Struktur dasar dari silika gel terbentuk selama
pembentukan gel asam polisiklik dari asam monosiklik (Stahl, 1985).
Pada metode ini, setelah pengembangan, harus dilakukan
pembandingan antara bentuk bercak, daerah bercak, resolusi, bercak-bercak
yang lain yang terdapat dalam lempeng. Nilai Rf dapat digunakan sebagai
nilai yang menggambarkan jarak elusi. Nilai Rf dapat dihitung dengan
menggunakan rumus:
Kelebihan KLT antara lain yaitu pemisahan senyawa yang amat
berbeda seperti senyawa organik ataupun anorganik dapat dilakukan dengan
alat yang harganya tidak terlalu mahal. Jumlah cuplikan dengan konsentrasi
rendah dapat ditangani yaitu sekitar 0,1μg – 5mg. Pemakaian pelarut dan
jumlah cuplikan yang diperlukan sedikit, sedangkan penotolan cuplikan
berganda dimungkinkan. Selain itu juga dapat memisahkan campuran yang
mengandung sampai empat komponen yang berbeda (Stahl, 1985).
Kekurangan teknik ini yaitu pada pembuatan fase diam pada lempeng
yang membutuhkan tambahan waktu, kecuali bila sudah tersedia lempeng
yang diproduksi secara komersial (Sulasmono, 1995).
2. Fase gerak
Fase gerak merupakan medium angkut yang terdiri dari satu atau
beberapa pelarut (Stahl, 1985). Dalam beberapa kasus, penggunaan pelarut
tunggal sudah memberikan hasil yang memuaskan. Akan tetapi pada sebagian
besar kasus, satu pelarut tidak dapat mengembangkan fase diam cukup jauh.
Karena itu harus dicampur antara pelarut untuk memperoleh kepolaran yang
diinginkan (Gritter, 1991).
3. Pengembangan dan Deteksi
Lempeng yang telah ditotoli ditaruh di dalam bejana kecil yang berisi
pelarut yang tingginya beberapa cm. Tinggi pelarut di dalam bejana harus di
bawah tempat penotolan lempeng. Bejana ditutup dan pelarut dibiarkan
merambat naik sampai 10-15 cm (Gritter, 1991).
Pengembangan memerlukan waktu sekitar 5 menit, bergantung pada
penyerap dan pelarut. Pengembangan lempeng biasanya dilakukan dalam
bejana kaca yang dapat menampung beberapa lempeng. Bejana dijaga tetap
jenuh dengan pelarut pengembang dengan bantuan sehelai kertas saring yang
tercelup ke dalam pengembang. Keefisienan pemisahan dapat ditingkatkan
dengan cara pengembangan berganda (Gritter, 1991).
I. Flavonoid
Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3-C6
yaitu kerangka karbonnya terdiri atas 2 gugus C6 (cincin benzene tersubtitusi)
yang disambungkan oleh rantai alifatik dengan 3 karbon. Kerangka flavonoid
tersebut dapat digambarkan sebagai
C
Gambar 1. Kerangka flavonoid
Flavonoid umumnya terdapat dalam tumbuhan, terikat pada gula sebagai
glikosida dan aglikon flavonoid yang manapun mungkin saja terdapat dalam satu
tumbuhan dalam beberapa bentuk kombinasi glikosida (Robinson, 1991).
Ada beberapa fase gerak yang biasa digunakan untuk menghasilkan
pemisahan yang baik pada lempeng selulosa. Butanol : Asam asetat : Air
(40:50:10) fase atas, merupakan fase gerak yang sering digunakan. Aglikon dari
flavonoid mempunyai nilai Rf yang tinggi dan waktu elusi yang lama (Stahl,
1969).
Pada UV 254 nm, semua flavonoid menyebabkan pemadaman fluoresensi,
dimana terlihat sebagai warna biru gelap pada lempeng KLT. Pada UV 365 nm,
tergantung pada strukturnya, flavonoid berfluoresensi kuning, biru, atau hijau
(Wagner, 1984).
J. Alkaloid
Alkaloid adalah senyawa organik yang berasal dari alam yang
mengandung satu atau lebih atom nitrogen, berada dalam distribusi terbatas dan
dalam dosis yang rendah memiliki efek farmakologi. Di alam, alkaloid terdapat
dalam bentuk bebas, sebagai garam dan N-Oksida. Alkaloid biasanya berupa zat
padat, tetapi ada pula yang berupa zat cair, seperti ephedrine dan spartein.
Alkaloid berasa pahit dan sukar larut dalam air, tetapi mudah larut dalam
kloroform, eter, dan pelarut organik lain yang relatif non polar. Sebaliknya bila
berupa garam, alkaloid akan mudah larut dalam air, tetapi tidak larut dalam
pelarut organik (Samuelson, 2002).
Pemisahan alkaloid secara KLT dapat menggunakan fase diam silika gel,
alumina, selulosa atau kieselguhr. Pemisahan yang baik diperoleh jika silika gel
sudah diaktifkan. Banyak alkaloid dapat dideteksi secara visibel. Sebagian besar
alkaloid juga memiliki bercak yang berfloresensi di bawah sinar UV 365. Reagent
yang biasanya dipakai untuk mendeteksi adalah reagen Dragendorf (Stahl, 1969).
Dengan penyemprotan reagen Dragendorff, menunjukkan warna cokelat atau
orange (visibel) yang tidak stabil (Wagner, 1984).
K. Senyawa polifenol
Senyawa fenolik dapat digolongkan menjadi senyawa fenol sederhana,
fenol asam karboksilat, α-Pyrones, Lichens, Lignan, chromones, flavonoid, dan
Quinone. Pemisahan senyawa fenolik dapat dilakukan dengan metode KLT
menggunakan fase diam silika gel. Pemilihan fase geraknya tergantung tingkat
polaritas campuran yang akan dipisahkan. Contoh fase gerak yang sering
digunakan adalah benzene : kloroform (50: 50), kloroform : methanol (97:3), dan
lain-lain (Stahl, 1969)
Aktivitas fisiologis senyawa fenolik tumbuhan banyak dan beragam.
Beberapa senyawa fenolik bersifat racun terhadap hewan pemangsa tumbuhan
(herbivora) dan beberapa bersifat racun serangga. Senyawa fenolik lain
mempunyai aktivitas antiinflamasi, karena senyawa ini menghambat sintesis
prostaglandin (Robinson, 1991).
Hanya antosianin dan beberapa derivat quinon yang dapat dideteksi secara
langsung dengan sinar tampak pada lempeng silika gel. Senyawa fenolik lainnya,
merupakan senyawa yang tidak berwarna dan harus diwarnai. Dengan FeCl3
bercak akan terlihat berwarna kuning tua sampai ungu tergantung jenis
polifenolnya. Biasanya bercak yang terjadi berwarna biru kehijauan (Stahl, 1969).
L. Tanin
Tanin merupakan senyawa yang sangat kompleks, biasanya terdapat
sebagai campuran polifenol yang sangat sulit dikristalkan. Tanin dengan air
membentuk larutan koloidal, mempunyai reaksi asam dan rasanya sangat sepat.
Makin murni tanin, makin kurang kelarutannya dalam air dan makin mudah
diperoleh dalam bentuk kristal. Tanin larut pula dalam pelarut organik yang polar,
setidak-tidaknya sampai batas tertentu, tetapi tidak larut dalam pelarut organik
non polar seperti benzene dan kloroform. Larutan tanin dalam air dapat
diendapkan dengan penambahan asam mineral atau garam (Robinson,1991).
Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae
teradapat khusus dalam jaringan kayu. Terdapat dua jenis tanin, yaitu tanin
terhidrolisis dan tanin terkondensasi. Tanin terhidrolisis dapat dihidrolisis oleh
asam atau enzim seperti tannase. Tanin jenis ini terbentuk dari beberapa molekul
asam fenolik seperti asam galat dan asam heksahidroksidipenik yang disatukan
oleh ikatan ester dengan molekul glukosa. Sedangkan tanin terkondendasi tidak
terhidrolisis menjadi molekul yang lebih sederhana dan tidak mengandung gugus
gula. Tanin terkondensasi akan berubah warna menjadi cairan tidak larut berwarna
merah ketika bereaksi dengan asam atau enzim terkondensasi, sedangkan tanin
terhidrolisis akan membentuk warna biru ketika bereaksi dengan garam besi
(Trease dan Evans, 2002).
Tanin merupakan senyawa asam karboksilat fenol yang dapat dipisahkan
menggunakan fase diam silica gel dan fase gerak toluene: etil formate: asam
format (50:40:10) (Stahl, 1969).
Beberapa tanin terbukti mempunyai aktivitas antioksidan, menghambat
pertumbuhan tumor, tanin juga dapat meracuni hati (Robinson,1991). Tanin juga
berfungsi sebagai anthelmintik, anti HIV, antibakteri, antikanker, dan anti
karsinogenik (Duke, 1992).
M.Saponin
Saponin tersebar luas di berbagai jenis tumbuhan. Keberadaan saponin
sangat mudah ditandai dengan pembentukkan larutan koloidal dengan air apabila
digojok menimbulkan buih yang stabil. Saponin merupakan senyawa berasa pahit
menusuk dan menyebabkan bersin dan sering mengakibatkan iritasi pada selaput
lendir (Gunawan, 2004). Beberapa saponin bekerja sebagai senyawa antimikroba.
(Robinson, 1991).
Adanya saponin dapat ditunjukkan dengan beberapa cara antara lain
dengan indeks buih. Indeks buih menunjukkan angka pengenceran dari bahan
yang diperiksa. Reaksi identifikasi ini akan memberikan lapisan buih setinggi 1
cm bila larutan sampel ditambah air digojok dalam gelas ukur selama 15 detik dan
selanjutnya dibiarkan selama 15 menit (Gunawan, 2004).
Pengujian KLT untuk saponin menggunakan fase gerak contohnya
kloroform : methanol : air (65: 35 : 10) untuk memisahkan campuran glikosida
terpenoid yang netral. Dengan fase diam yang sering digunakan adalah silika gel
(Wagner, Bladt, dan Zgainski, 1984).
N. Keterangan Empiris
Binahong digunakan masyarakat secara empiris untuk mengobati beberapa
penyakit antara lain yaitu sebagai obat antiinflamasi, anti-ulcer, penyembuh luka
dan juga dapat sebagai liver-protective. Selain itu binahong juga dapat mengobati
infeksi mikroba, salah satunya adalah penyakit infeksi pada luka (Anonim, 2005).
Luka pada kulit dapat disebabkan oleh infeksi Staphylococcus aureus dan
Pseudomonas aeruginosa (Naim, 2006).
Staphylococcus aureus merupakan bakteri yang menyebabkan penyakit
pada hampir semua jaringan tubuh yang terutama adalah abses. Staphylococcus
aureus merupakan flora normal pada rongga hidung bagian depan, perineum,
saluran pencernaan, atau kulit. Sedangkan Pseudomonas aeruginosa merupakan
bakteri menyebabkan infeksi pada luka kulit seperti luka bakar, dan membentuk
nanah yang berwarna biru hijau, meningitis. Bakteri ini juga dapat menginfeksi
saluran kemih atau saluran pernafasan (Jawetz, et al, 1996).
Penelitian ini bersifat eksploratif, belum ada informasi yang menyatakan
secara langsung dalam sistem pelayanan kesehatan formal mengenai manfaat dari
tumbuhan ini. Untuk itu penelitian dilakukan berdasarkan penggunaan binahong
secara empiris oleh masyarakat.
BAB III
METODOLOGI PENELITIAN
A. Jenis danRancanganPenelitian
Penelitian ini termasuk jenis penelitian eksperimental yang bersifat
eksploratif dengan perlakuan pemberian konsentrasi ekstrak etanol umbi binahong
yang berbeda terhadap S. aureus dan P. aeruginosa. Analisis yang dilakukan
merupakan rancangan acak lengkap pola satu arah. Penelitian dilakukan di
Laboratorium Farmakognosi Fitokimia dan Laboratorium Mikrobiologi Fakultas
Farmasi Universitas Sanata Dharma.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel Penelitian
a. Variabel bebas yaitu ekstrak etanol umbi binahong dengan konsentrasi
100%, 75%, 50% dan 25%.
b. Variabel tergantungnya adalah diameter zona hambat pertumbuhan S.
aureus dan P. aeruginosa.
c. Variabel terkendali antara lain waktu inkubasi (24 jam), suhu inkubasi
(37ºC), jenis bakteri uji, volume suspensi bakteri uji yang diinokulasikan
dalam media (0,2 ml), konsentrasi suspensi bakteri uji setara dengan
larutan standar Mc. Farland II (6x108 CFU/ml), volume larutan uji yang
diinokulasikan dalam paperdisk (20µl), dan tempat tumbuh binahong di
d. Variabel tak terkendali antara lain suhu pengeringan bahan di bawah
matahari.
2. Definisi operasional
a. Potensi antibakteri adalah kemampuan ekstrak etanol umbi binahong yang
dapat membunuh atau menghambat pertumbuhan bakteri bakteri S. aureus
ATCC 25923 dan P. aeruginosa ATCC 27853 yang dapat dilihat dari zona
jernih yang menggambarkan zona hambat pertumbuhan bakteri,
dibandingkan dengan DMSO sebagai pelarut.
b. Ekstrak etanol umbi binahong merupakan hasil maserasi dari 175g umbi
batang dari tanaman binahong dengan menggunakan pelarut etanol pa
70% sebanyak 1312,5ml dimana pergantian cairan penyari dilakukan
setiap 24 jam sekali dengan jumlah yang sama dan diperoleh ekstrak
kental sebanyak 14,23 gram.
c. Staphylococcus aureus ATCC 25923 merupakan stock strain bakteri gram
positif, berbentuk coccus dengan diameter 0,5 -1,5 µm, nonmotil,
mengalami metabolisme secara respirasi dan fermentasi, menunjukkan
reaksi positif untuk uji katalase, dan negatif untuk reaksi oksidasi,
diperoleh dari Dinas Kesehatan Propinsi D.I Yogyakarta dengan nomor
contoh uji S. 34.4, asal contoh uji : Komersial Oxoid tahun 2004.
d. Pseudomonas aeruginosa ATCC 27853 merupakan stock strain bakteri
positif untuk uji katalase, diperoleh dari Dinas Kesehatan Propinsi D.I
Yogyakarta dengan nomor contoh uji P.10.4. asal contoh uji : Komersial
Oxoid tahun 2004.
e. Zona hambat adalah daerah di sekitar paperdisk yang tidak ditemukan
adanya pertumbuhan bakteri S. aureus ATCC 25923 dan P. aeruginosa
ATCC 27853 dan yang terdapat pertumbuhan bakteri dalam jumlah sedikit
yang berupa zona jernih.
C. Bahan dan Alat Penelitian
1. Bahan
Bahan yang digunakan dalam penelitian adalah umbi binahong yang
diperoleh dari Balai Penelitian Tanaman Obat di Tawangmangu, nutrien
agar (oxoid) , DMSO sebagai kontrol negatif, aquadest steril, amoksisilin
injeksi kering (Danoxilin® 1000 mg) sebagai kontrol positif, bakteri
Staphylocuccus aureus ATCC 25923 dan Pseudomonas aeruginosa ATCC
27853yang diperoleh dari Dinas Kesehatan Propinsi D.I Yogyakarta. Fase
diam : lempeng KLT silika Gel GF 254, dan selulosa, fase gerak toluene:
etil asetat (93:7), etil asetat: metanol: air (70:20:10), toluene: etil asetat :
metanol (70:20:10), n-Butanol: Asam asetat: Air (4: 1: 5), etil asetat :
metanol : air (100 : 13,5 : 10), pembanding rutin, skopolamin, eugenol,
asam tanat, Glycyrrhiza Radix, deteksi uap amoniak, dragendroff LP,
2. Alat
Alat-alat yang digunakan dalam penelitian ini antara lain:
a. Alat untuk preparasi sampel uji: Alat-alat gelas (Pyrex), Paltform
Shaker (Innova 2001, New BrunswickScientific), Rotary evaporator
(janke dan Kunkel, Ika- Labotechnik, RV 05-ST), Waterbath
(Memmert, Tipe BE 400, GmbH+ CoKG-D91126, Swahaban FRG
Germany),
b. Alat- alat untuk pengujian potensi antimikroba : Vortek (Stuart
Scientic), Micro Safety Cabinet, Mikropipet 10μl Nichiryo Model 5000
DG, Jarum Ose, spreader, Bunsen, Almari es (Sharp), Timbangan
analitik (Metter Toledo AB 204).
c. Alat untuk KLT : Bejana pengembangan KLT/ Chamber, lampu UV
dengan panjang gelombang 365nm dan 254 nm mikropipet 5µl, alat
semprot, kertas saring.
D. JalannyaPenelitian
1. Determinasi tanaman binahong
Tanaman binahong dideterminasi oleh Balai Penelitian Tanaman Obat
(BPTO) Tawangangmangu dengan menggunakan pustaka acuan C. A. Backer
2. Pengumpulan bahan
Umbi binahong diperoleh dari Balai Penelitian Tanaman Obat
Tawangangmangu. Umbi yang diperoleh berupa umbi batang yang sudah
dikeringkan.
3. Pembuatan Serbuk
Pembuatan serbuk dilakukan dengan menggunakan blender. Kemudian
serbuk yang telah diperoleh, diayak dengan menggunakan pengayak 12/50,
sehingga diperoleh serbuk dengan derajad halus yang homogen.
4. Pembuatan ekstrak etanol dengan metode maserasi
Sebanyak 175 g serbuk umbi binahong, diletakkan ke dalam 7
erlenmeyer terpisah, kemudian direndam dengan 187,5 ml pada tiap
erlenmeyer selama 3 hari (serbuk : cairan penyari = 10:75) dan cairan penyari
diganti setiap hari dengan jumlah yang sama. Proses perendaman juga disertai
dengan penggojogan dengan shaker. Setelah itu, hasil maserasi (maserat)
disaring dan kemudian diuapkan dengan menggunakan rotary evaporator.
Untuk menghilangkan seluruh pelarut yang masih terdapat di dalam ekstrak,
hasil penguapan dari rotary evaporator diuapkan kembali di atas waterbath.
Hasil penyaringan ditempatkan dalam cawan porselin yang telah ditara
sebelumnya.
5. Skrining Fitokimia
a. Uji Tabung
Uji tabung serbuk umbi binahong meliputi uji pendahuluan, uji
alkaloida, uji antrakinon, uji polifenol, uji tanin, uji kardenolida, dan uji
saponin.
1) Uji pendahuluan
Serbuk tumbuhan (2g) ditambah air (10 ml), dipanaskan selama 30
menit di atas air mendidih. Larutan disaring menggunakan kapas. Lalu
ditambahkan larutan kalium hidroksida (beberapa tetes).
2) Uji alkaloida
Serbuk tumbuhan (2g) dipanaskan dalam tabung reaksi besar
dengan asam klorida 1% (10ml) selama 30 menit dalam penangas air
mendidih. Suspensi disaring dengan kapas ke dalam tabung reaksi A1 dan
tabung reaksi A2 sama banyak. Larutan A1 ditambah pereaksi Dragendorf
(3 tetes) dan larutan A2 ditambah pereaksi mayer (3 tetes).
3) Uji antrakinon
Serbuk tumbuhan (300 mg) dididihkan selama 2 menit dengan
kalium hidroksida 0,5 N (10 ml) dan larutan hidrogen peroksida (1 ml).
Setelah dingin, suspensi disaring melalui kapas. Filtrat (5 ml) ditambah
asam asetat glacial (10 tetes) sampai pH 5, lalu ditambahkan toluene (10
ml). Lapisan atas (5 ml) dipisahkan dengan pipet dan dimasukkan ke
4) Uji polifenol
Serbuk tumbuhan (2 g) dipanaskan dengan air (10 ml) selama 10
menit dalam penangas air mendidih. Disaring panas-panas, setelah dingin
ditambah 3 tetes pereaksi besi (III) klorida.
5) Uji tanin (zat samak)
Serbuk tumbuhan (2 g) dipanaskan dengan air (10 ml) selama 30
menit di atas tangas air. Disaring, filtrat (5 ml) ditambahkan larutan
natrium klorida 2 % (1 ml), bila terjadi suspensi atau endapan disaring
melalui kertas saring, kemudian filtrat ditambahkan 5ml larutan gelatin 1%
6) Uji saponin
a) Tambahkan air (10 ml) ke dalam tabung reaksi yang berisi serbuk
tumbuhan (100 mg), tutup dan kocok kuat-kuat selama 30 detik.
Biarkan tabung dalam kondisi tegak selama 30 menit.
b) Uji lain dilakukan dengan menggunakan pipa kapiler (diameter 1
mm, panjang 12,5 cm). Larutan hasil pemanasan serbuk tumbuhan
(2 g) dengan air (10 ml) selama 30 menit di atas tangas air, setelah
disaring, filtrat dimasukkan ke dalam pipa kapiler penuh-penuh.
Kapiler diletakkan dalam posisi tegak vertikal, kemudian cairan
dibiarkan mengalir bebas. Sebagai pembanding, dikerjakan hal
b. Uji kualitatif secara Kromatografi Lapis Tipis Ekstrak Etanol Umbi
Binahong
a. Pembuatan Larutan Uji untuk KLT dari Ekstrak Etanol Umbi
Binahong
Ekstrak etanol umbi binahong yang digunakan untuk uji KLT
adalah ekstrak etanol dengan konsentrasi 10%. Pembuatannya dilakukan
dengan cara ekstrak etanol umbi binahong ditimbang sebanyak 0,5 g,
kemudian dilarutkan dengan 5 ml etanol p.a 70%.
b. Pembuatan Fase Diam
Fase diam yang digunakan dalam uji KLT untuk senyawa saponin,
alkaloid, tanin dan senyawa fenolik adalah silika gel GF 254 sedangkan
untuk flavonoid digunakan selulosa. Fase diam selulosa yang digunakan
merupakan selulosa p.a, yang berupa lembaran kertas mika yang dilapisi
dengan selulosa.
Untuk silika gel GF 254, dibuat dengan perhitungan : dibutuhkan
1,5 g silika gel GF untuk tiap lempeng. Jadi penimbangan silika gel GF
disesuaikan dengan jumlah lempeng yang akan dibuat. Kemudian serbuk
silika gel yang sudah ditimbang tersebut, dilarutkan dengan 3 ml aquadest
untuk tiap gramnya (jumlah aquadest yang digunakan juga menyesuaikan
c. Penjenuhan Fase Gerak di dalam Bejana
Bejana kromatografi yang akan digunakan, dilapisi dengan kertas
saring yang telah dipotong dengan ukuran yang sesuai di bagian dalamnya.
Fase gerak yang digunakan dimasukkan ke dalam bejana. Kemudian
bejana ditutup rapat dan dibiarkan hingga seluruh isi bejana jenuh dengan
uap fase gerak yang ditandai dengan seluruh permukaan kertas saring pada
dinding bagian dalam bejana telah terbasahi oleh fase gerak.
1) Uji KLT flavonoid
Fase diam yang digunakan yaitu selulosa dan fase gerak yang
digunakan adalah butanol: asam asetat : air (4:1:5). Pembanding yang
digunakan adalah rutin. Sampel dan pembanding ditotolkan pada lempeng
KLT kemudian dielusi pada batas tertentu (10 cm). Setelah itu dideteksi
dengan UV 254 nm, UV 365 nm dan dengan uap amonia.
2) Uji KLT alkaloid
Fase diam yang digunakan adalah silika gel GF 254 dan fase gerak
yang digunakan adalah etil asetat: methanol: air (70:20:10). Sebagai
pembanding digunakan skopolamin. Sampel dan pembanding ditotolkan
bersama-sama pada lempeng KLT, kemudian dielusi pada batas tertentu
(10 cm). Setelah itu dideteksi dibawah sinar UV 254 nm dan UV 365 nm,
kemudian dideteksi dengan pereaksi semprot Dragendorff
3) Uji KLT senyawa fenolik
yang digunakan adalah toluene: etil asetat: metanol (70:20:10).
Pembanding yang digunakan yaitu Eugenol. Sampel dan pembanding
ditotolkan pada lempeng KLT, kemudian dielusi pada batas tertentu (10
cm) dan dikeringkan. Deteksi dilakukan dibawah sinar UV 254 nm dan
pereaksi semprot FeCl3.
4) UjiKLTtanin
Uji KLT tanin menggunakan fase diam silika gel GF 254 dan fase
gerak etil asetat : metanol : air (100 : 13,5 : 10). Sampel dan pembanding
yang berupa asam tanat 1% ditotolkan pada lempeng KLT kemudian
dielusi pada batas tertentu (10 cm). Setelah itu dideteksi dengan UV 254
nm, UV 365 nm dan FeCl3.
5) Uji KLT saponin
Fase diam yang digunakan adalah silika gel GF 254. Fase gerak
yang digunakan adalah toluen : etil asetat (93 : 7). Ekstrak etanol umbi
binahong 10% dan pembanding yaitu Glycyrrhiza Radix 1% ditotolkan
pada lempeng silika gel GF 254 menggunakan mikropipet berukuran 5µl,
kemudian dielusi pada batas tertentu (10 cm). Setelah elusi selesai, bercak
dideteksi dengan pereaksi anisaldehid - asam sulfat dan diamati secara
6. Uji potensi antibakteri ekstrak etanol umbi binahong terhadap
Staphylococcus aureus dan Pseudomonas aeruginosa
a. Penyiapan stok bakteri uji
Diambil dua ose kultur dari kultur bakteri stok menggunakan jarum
ose steril. Diinokulasikan pada 5 ml Nutrian Agar miring dan diinkubasi
selama 24 jam pada suhu 37ºC di inkubator.
b. Pembuatansuspensi Bakteri uji
Pembuatan suspensi bakteri dilakukan dengan mengambil 1-2 ose
bakteri dari stok yang telah dibuat sebelumnya, diinokulasikan pada 3 ml
media Nutrien Broth. Suspensi tersebut diinkubasikan selama 24 jam pada
suhu 37ºC. Kemudian divortex, dan disetarakan kekeruhannya dengan
larutan standard Mc. Farland II (6x108 CFU/ml) menggunakan Nutrien
Broth.
c. Pembuatanvariasi konsentrasi larutan uji
Larutan uji yang digunakan untuk uji potensi antibakteri, merupakan
ekstrak etanol yang dibuat dalam berbagai konsentrasi yaitu 25%, 50%,
75%, 100%. Ekstrak etanol dengan konsentrasi 100% (stok larutan uji)
dibuat dengan cara: ekstrak kental (hasil penyarian) yang diperoleh
ditimbang sejumlah 10g yang kemudian dilarutkan ke dalam 10 ml
Dari stok larutan uji tersebut, dapat dibuat variasi konsentrasi larutan
uji sebagai berikut:
Tabel I. Pembuatan Variasi Konsentrasi Uji Konsentrasi
larutan uji (%)
Volume yang diambil dari stok larutan uji
(ml)
d. Pembiakan suspensi bakteri uji secara spread platting
Media NA sebanyak 20 ml dituang ke dalam cawan petri, dan
didiamkan sampai memadat. Suspensi bakteri sebanyak 0,2 ml
dipindahkan ke dalam media yang sudah memadat lalu diratakan
menggunakan spreader.
e. Metode difusi
Setelah pembiakan secara spread platting, siapkan paperdisk yang
telah dijenuhkan dengan amoksisilin sebagai kontrol positif, DMSO
sebagai kontrol negatif, ekstrak etanol umbi binahong dengan konsentrasi
25%, 50%, 75%, dan 100% Petri-petri tersebut diinkubasikan selama 24
jam pada suhu 37ºC kemudian diamati ada tidaknya zona hambat di sekitar
paperdisk. Zona hambat yang terbentuk diukur dengan penggaris. Pada uji
potensi antibakteri ini dilakukan replikasi sebanyak 3 kali.
f. Metodedilusi padat
Pada uji potensi antibakteri pada metode difusi, didapatkan
tersebut, dibuat rentang konsentrasi yang lebih rendah sebanyak 5 variasi
konsentrasi untuk mengetahui KHM dari masing-masing ekstrak.
Pengujian dimulai dengan membuat suspensi bakteri yang disetarakan
kekeruhannya dengan standard Mc. Farland II (6x108 CFU/ml). Dari
suspensi tersebut, diambil 0,5 ml, ditambah dengan larutan uji sebanyak
0,5 ml dengan kadar tertentu dan dicampur rata dengan 20 ml NA yang
dicairkan. Setelah itu dituang dalam cawan petri dan diinkubasi selama 24
jam pada suhu 37ºC. Diamati banyak sedikit atau ada tidaknya
pertumbuhan bakteri uji pada berbagai variasi konsentrasi dengan diberi
tanda.
E. Analisis Data
Analisis uji antibakteri dengan metode difusi paperdisk dilakukan
dengan mengukur diameter zona hambat yang dapat dilihat dari zona
jernih di sekitar paperdisk Analisis hasil KLT bersifat deskriptif dan
komparatif, dilakukan dengan menghitung harga Rf dan mengamati bercak
yang timbul dari ekstrak etanol dan membandingkannya dengan standar
BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi
Determinasi tanaman dilakukan di Balai Penelitian Tanaman Obat (BPTO) Tawangmangu. Diidentifikasi di BPTO menurut acuan C. A. Backer (1968). Identifikasi tanaman ini bertujuan untuk memastikan bahwa tanaman yang digunakan adalah binahong (Anredera cordifolia (Tenore) Steen). Dari hasil determinasi tersebut, tanaman binahong yang digunakan dalam penelitian ini diketahui memiliki nama ilmiah Anredera cordifolia (Tenore) Steen (Lampiran 1 dan lampiran 2).
Bagian tanaman yang digunakan yaitu umbinya. Menurut Tjitrosoepomo (1985), umbi merupakan metamorfosis (penjelmaan, perubahan bentuk) dari batang dan akar. Umbi biasanya merupakan suatu bagian yang membengkak, bangun bulat, seperti kerucut atau tidak beraturan, merupakan tempat penimbunan makanan, dapat merupakan metamorfosis dari batang, dapat pula merupakan metamorfosis dari akar. Dalam penelitian ini umbi yang dimaksud adalah umbi batang yaitu metamorfosis dari batang.
B. Pengumpulan Bahan dan Pembuatan Serbuk
dilakukan untuk mengurangi kadar air dari bahan. Air merupakan media yang baik untuk pertumbuhan mikroba, dengan demikian pengeringan dapat mencegah terjadinya pembusukan. Selain itu, juga dapat untuk menghentikan reaksi-reaksi enzimatik yang terjadi pada bahan tersebut.
Penyerbukan dilakukan dengan menggunakan blender. Penyerbukan ini bertujuan untuk memperkecil ukuran partikel bahan dan meningkatnya luas permukaan bahan. Dengan meningkatnya luas permukaan bahan, maka kontak antara cairan penyari dengan bahan semakin besar, sehingga serbuk akan semakin mudah terbasahi oleh penyari. Dengan demikian diharapkan penyarian akan lebih efektif dan mempermudah penarikan senyawa dari serbuk oleh penyari.
Serbuk yang diperoleh kemudian diayak dengan ayakan nomor 12/50. Nomor pengayak menunjukkan jumlah lubang tiap-tiap 2,54 cm, dihitung searah dengan panjang kawat. Jadi derajat halus serbuk dengan pengayak nomor 12/50 adalah 4,7/19,7. Hasil ini mendekati derajat halus serbuk simplisia pada umumnya yaitu 4/18. Derajat halus serbuk dapat dinyatakan dengan satu nomor atau dua nomor. Jika derajat halus dinyatakan dengan dua nomor, berarti semua serbuk dapat melalui pengayak dengan nomor terendah dan tidak lebih dari 40% melalui pengayak nomor tertinggi (Anief, 2000). Dalam hal ini, berarti semua serbuk dapat melalui pengayak nomor 12 dan tidak lebih dari 40% dapat melalui pengayak nomor 50.
C. Pembuatan Ekstrak Etanol dengan Metode Maserasi
ditentukan. Mekanisme metode maserasi yaitu cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif. Zat aktif akan larut dan karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan yang di luar sel, maka larutan yang terpekat didesak keluar. Peristiwa tersebut berulang sehingga terjadi keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel (Anonim,1986).
Menurut Anonim (1986), maserasi pada umumnya dilakukan dengan cara 10 bagian simplisia dengan derajat halus yang cocok dimasukkan ke dalam bejana, kemudian dituangi dengan 75 bagian cairan penyari, ditutup dan dibiarkan selama 5 hari, sambil berulang-ulang kali diaduk.
Dalam penelitian ini, serbuk yang digunakan sebanyak 175g dibagi ke dalam 7 Erlenmeyer (tiap Erlenmeyer berisi 25 gram serbuk), kemudian direndam dengan 187,5 ml etanol pa 70% pada tiap erlenmeyer. Perbandingan serbuk dan cairan penyari 10:75. Pengadukan dilakukan dengan cara digojok menggunakan mesin pengaduk yang berputar-putar terus menerus (shaker). Ini merupakan salah satu modifikasi dari maserasi. Proses penggojokkan itu sendiri hanya dilakukan selama 3 hari. Hal ini dilakukan karena pada hari ke-3 cairan penyari yang digunakan sudah jernih. Dengan demikian diasumsikan sebagian besar senyawa sudah tersari. Untuk menghindari terjadinya penjenuhan cairan penyari, maka cairan penyari yang digunakan yaitu etanol diganti setiap 24 jam sekali, sehingga etanol yang digunakan tetap baru.
mekanik). Proses pengadukan tersebut akan meningkatkan kelarutan senyawa yang terdapat dalam serbuk, sehingga dimungkinkan senyawa yang tersari akan lebih banyak. Selain itu, penggojogan akan meratakan konsentrasi di luar sel, sehingga perbedaan konsentrasi di dalam dan di luar sel yang sebesar-besarnya terjaga. Modifikasi lain yang dapat dilakukan yaitu remaserasi dimana dilakukan pergantian cairan penyari setelah dilakukan penyaringan pada maserat sebelumnya. Keuntungan lain dari maserasi adalah secara metodologis, keterulangan proses lebih terjamin. Hal ini dikarenakan perbandingan jumlah pelarut dengan jumlah serbuk dan lama waktu penyarian proses maserasi dapat ditentukan.
Setelah itu, hasil maserasi (maserat) disaring dan kemudian diuapkan dengan menggunakan rotary evaporator. Supaya hasil maserat lebih pekat, maka harus diuapkan lagi di atas waterbath, dan kemudian disimpan di dalam oven pada suhu 30oC. Penguapan ini bertujuan untuk menguapkan cairan penyari, sehingga didapatkan ekstrak kental. Proses penguapan ini dilakukan bertahap di
rotary evaporator kemudian dilanjutkan di atas waterbath untuk alasan teknis. Maksudnya tidak mungkin penguapan hanya dilakukan di rotary evaporator sampai menjadi kental. Jadi sebelum benar-benar kental, ekstrak harus dipindahkan ke dalam cawan porselin yang sudah ditara dan diuapkan di atas