Adsorpsi Zat Warna Pembuatan Larutan Zat Warna
Larutan stok zat warna 1000 mg/L dibuat dengan melarutkan 1000 mg serbuk Cibacron Red dalam air suling dan diencerkan hingga 1 liter. Kemudian dibuat kurva standar dari larutan hasil pengenceran larutan stok ini dengan konsentrasi 5, 10, 20, 30, 40, dan 50 mg/l (Lampiran 2).
Penentuan Panjang Gelombang Maksimum
Panjang gelombang maksimum diukur
dengan spektrofotometer Spectronic 20D+
pada rentang panjang gelombang 515-525 nm dengan larutan Cibacron Red 5 mg/L.
Penentuan Waktu Optimum Adsorpsi
Sebanyak 1 g adsorben dimasukkan ke dalam 50 mL larutan Cibacron Red 50 mg/L, kemudian larutan digojok dengan alat gojok. Adsorpsi dilakukan dengan variasi waktu adsorpsi 0, 30, 60, 90, 120, dan 150 menit. Campuran disaring dan absorbansi filtrat diukur pada panjang gelombang maksimum. Waktu optimum ditentukan dengan menghitung efisiensi dan kapasitas adsorpsi maksimum.
Penentuan Bobot Optimum Adsorben
Variasi bobot adsorben yang digunakan adalah 0.5, 1.0, 1.5, 2.0, dan 2.5 g. Masing-masing dimasukkan ke dalam 50 mL larutan Cibacron Red 50 mg/L, kemudian digojok dengan alat gojok selama waktu optimum. Campuran disaring dan absorbans filtrat diukur pada panjang gelombang maksimum. Setelah itu, dihitung efisiensi adsorpsi dan kapasitas adsorpsi menggunakan rumus sebagai berikut:
Persentase adsorpsi dapat dihitung dengan mengunakan persamaan: Keterangan: Q = kapasitas adsorpsi (mg/g) V = volume larutan (L) Co = konsentrasi awal (mg/L) C = konsentrasi akhir (mg/L) m = bobot adsorben (g)
Penentuan Nisbah Optimum Adsorben
Adsorben dengan nisbah tertentu ditimbang sebanyak 1,0 g dan dimasukkan ke dalam Erlenmeyer yang berisi 50 mL larutan Cibacron Red 50 mg/L. Campuran digojok selama 60 menit, disaring dan diambil filtratnya, kemudian diukur dengan
spektrofotometer Spectronic 20D+ pada
panjang gelombang maksimum.
Penentuan Isoterm Adsorpsi (Victoria 2009)
Erlenmeyer yang berisi 1,0 g adsorben dengan nisbah optimum ditambah dengan 50 mL zat warna pada berbagai konsentrasi, yaitu 20, 40, 60, 80, dan 100 mg/L, lalu digojok selama 120 menit. Setelah itu, disaring dan diambil filtratnya untuk diukur dengan
spektrofotometer Spectronic 20D+ pada
panjang gelombang 516 nm. Persamaan regresi linear menggunakan persamaan Langmuir dan Freundlich dibuat untuk menentukan jenis isoterm yang sesuai. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Penentuan Waktu Optimum dan Pengaruh Bobot Adsorben Arang Aktif
Metode penentuan waktu optimum dan pengaruh bobot adsorben arang aktif dilakukan dengan merujuk pada metode penentuan waktu optimum dan bobot optimum adsorben ATA.
HASIL DAN PEMBAHASAN
Aktivasi Ampas Tebu, Kaolin, danBentonit
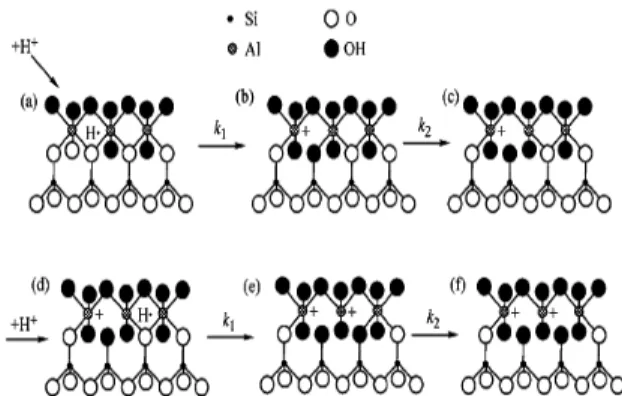
Aktivasi ampas tebu dengan H3PO4 30%
dan NaOH 0,1 N bertujuan menghilangkan senyawa-senyawa selain polisakarida yang larut dalam asam dan basa, agar tidak ikut berperan dalam mekanisme adsorpsi zat
warna. Aktivasi kaolin menggunakan H2SO4
30% bertujuan melarutkan
komponen-komponen seperti Fe2O3, Al2O3, CaO, dan
MgO yang mengisi ruang antarlapisan kaolin, sehingga menambah luas permukaan
adsorben. Ion-ion Ca2+ dan Mg2+ yang berada
pada permukaan kristal adsorben secara berangsur-angsur juga akan digantikan oleh
ion H+ dari H
2SO4 (Gambar 4). Begitu juga
halnya dalam aktivasi bentonit. Kation logam
seperti Na+, Ca2+, dan Mg2+ dalam struktur
bentonit digantikan dengan H+ dari H
2SO4 (Gambar 5). m C) o V(C Q % o C C) o (C 100 (%) adsorpsi Efisiensi
Gambar 4 Skema interaksi proton dengan struktur kaolin (Dudkin et al. 2004).
Gambar 5 Skema interaksi proton dengan struktur bentonit (Darma 2010).
Adsorpsi Cibacron Red
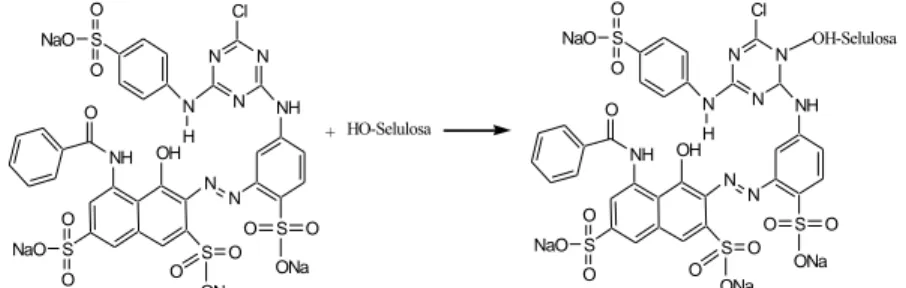
Penjerapan zat warna oleh ampas tebu berlangsung melalui reaksi antara gugus-OH selulosa dalam ampas tebu dan gugus-gugus
tertentu pada zat warna tekstil. Zat warna reaktif dapat mewarnai serat selulosa dalam kondisi tertentu dan membentuk senyawa dengan ikatan kovalen (Gambar 6) atau ikatan hidrogen (Gambar 7). S O O NaO N H N N N NH Cl S N O O ONa N S O ONa NH O S O O NaO O OH S O O NaO N H N N N NH O-Selulosa S N O O ONa N S O ONa NH O S O O NaO O OH HCl + HO-Selulosa +
S O O NaO N H N N N NH Cl S N O O ONa N S O ONa NH O S O O NaO O OH S O O NaO N H N N N NH Cl S N O O ONa N S O ONa NH O S O O NaO O OH + HO-Selulosa OH-Selulosa
Gambar 7 Mekanisme reaksi pembentukan ikatan hidrogen antara selulosa dan Cibacron Red.
Seleksi Adsorben
Adsorben yang digunakan pada tahap seleksi adalah campuran bentonit-ampas tebu, campuran kaolin-ampas tebu, dan ampas tebu. Adsorben campuran dari kaolin, bentonit dan ampas tebu dibuat dengan nisbah 75:25, 50:50, dan 25:75 dan 100:0. Pengaruh perlakuan adsorben dan nisbahnya terhadap kapasitas dan efisiensi adsorpsi dapat dilihat pada Gambar 8 dan 9.
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60 1,80 A1 A2 A3 B1 B2 B3 C1 C2 C3 D1 D2 D3 E1 E2 E3 F1 F2 F3 Campuran adsorben K ap as it as a d so rp si ( m g /g) 0,00 10,00 20,00 30,00 40,00 50,00 60,00 70,00 80,00 E fi si en s i ad so rp si ( % )
Kapasitas adsorpsi Efisiensi adsorpsi (%)
Gambar 8 Seleksi campuran adsorben nisbah 25:75 (1); 50:50 (2); dan 75:25 (3). A (ATAK), B (ATBK), C (ATABA), D (ATBBA), E (ATAB), dan F (ATBB).
0,00 10,00 20,00 30,00 40,00 50,00 60,00 70,00 80,00 90,00 G H I J K L M Adsorben E fi s ie ns i pe nj e ra p a n (% ) 0,00 0,50 1,00 1,50 2,00 2,50 K a pa s ita s pe nj e ra pa n (m g/ g )
Efisiensi adsorpsi Kapasitas adsorpsi
Gambar 9 Perlakuan optimum adsorpsi
Cibacron Red dengan
nisbah 100:0. G (ATB), H (ATA), I (AT), J (KA), K (K), L (BA), dan M (B).
Hasil penelitian menunjukkan bahwa kapasitas dan efisiensi adsorpsi terbesar dihasilkan oleh adsorben H yang terbuat dari ampas tebu dengan aktivasi asam (ATA). Pada nisbah optimum tersebut diperoleh kapasitas adsorpsi sebesar 1.94 mg/g dan efisiensi adsorpsi sebesar 77.59%. Data selengkapnya dapat dilihat pada Lampiran 3. Adsorben lainnya, yaitu ampas tebu (AT) dan ampas tebu teraktivasi basa (ATB) tidak mengadsorpsi. Hal ini menunjukkan bahwa pencucian basa tidak sesuai untuk perlakuan awal adsorben ampas tebu. Perlakuan tersebut menyebabkan ampas tebu semakin bermuatan negatif sehingga kurang untuk mengadsorpsi zat warna reaktif Cibacron Red yang bermuatan negatif.
Optimalisasi Adsorpsi Cibacron Red pada Ampas Tebu Teraktivasi Asam (ATA)
Adsorben ATA ditentukan kondisi optimum adsorpsinya terhadap zat warna reaktif Cibacron Red dengan mengukur dua parameter, yaitu waktu adsorpsi dan bobot adsorben. Setelah itu, jenis isoterm adsorpsinys ditentukan. Setiap adsorben memiliki karakteristik yang berbeda sehingga kondisi yang dibutuhkan untuk adsorpsi juga berbeda.
Waktu Adsorpsi
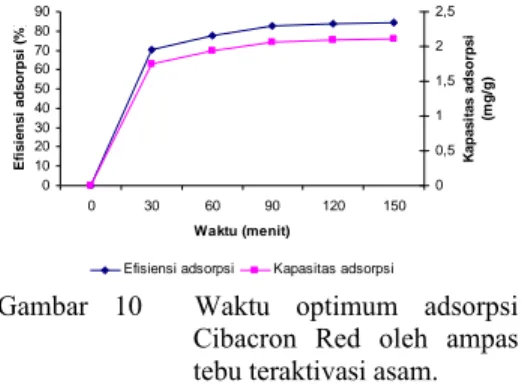
Efisiensi dan kapasitas adsorpsi meningkat dengan bertambah lamanya waktu adsorpsi (Gambar 10). Larutan Cibacron Red yang diadsorpsi berkonsentrasi 50 mg/L. Konsentrasi larutan cibacron red menurun dari 50 mg/L menjadi 7.99 mg/L. Waktu optimum adsorpsi yang diperoleh adalah 120 menit dengan kapasitas adsorpsi 2.10 mg/g, artinya setiap 1 g adsorben mampu mengadsorpsi 2.10 mg ion Cibacron Red dalam waktu 120 menit dengan efisiensi adsorpsi 84%. Setelah 120 menit, kapasitas dan efisiensi adsorpsi
cenderung tetap. Data selengkapnya dapat dilihat pada Lampiran 4. Hal ini menunjukkan bahwa adsorben telah jenuh oleh zat warna Cibacron Red. Jika proses dilanjutkan, maka kemungkinan tidak ada lagi zat warna yang diadsorpsi oleh adsorben, sampai akhirnya terjadi pelepasan kembali atau desorpsi.
0 10 20 30 40 50 60 70 80 90 0 30 60 90 120 150 Waktu (menit) E fi si en si ad so rp si ( % ) 0 0,5 1 1,5 2 2,5 K a p asi tas ad s o rp si (m g/ g)
Efisiensi adsorpsi Kapasitas adsorpsi
Gambar 10 Waktu optimum adsorpsi
Cibacron Red oleh ampas tebu teraktivasi asam.
Bobot Adsorben
Bobot adsorben berpengaruh terhadap kapasitas dan efisiensi adsorpsi larutan Cibacron Red dengan konsentrasi 50 mg/L (Gambar 11). 0,00 20,00 40,00 60,00 80,00 100,00 120,00 0,5 1,0 1,5 2,0 2,5 Bobot adsorben (g) E fi si en si ad so rp si ( % ) 0,00 0,50 1,00 1,50 2,00 2,50 K a p asi tas ad s o rp si (m g/ g)
Efisiensi adsorpsi Kapasitas adsorpsi
Gambar 11 Pengaruh bobot adsorben ampas tebu teraktivasi asam terhadap adsorpsi Cibacron Red.
Data pada Lampiran 5 menunjukkan bahwa nilai kapasitas adsorpsi tidak sejalan dengan efisiensi adsorpsi. Sebagai contoh, pada kondisi waktu dan konsentrasi yang sama, kenaikan bobot adsorben menurunkan kapasitas adsorpsi, tetapi meningkatkan efisiensi adsorpsi. Kapasitas adsorpsi menunjukkan banyaknya adsorbat yang diadsorpsi per satuan bobot adsorben. Karena itu, nilainya dipengaruhi oleh besarnya bobot adsorben. Jika bobot adsorben dinaikkan, sedangkan waktu adsorpsi dan konsentrasi adsorbat tetap, peningkatan jumlah tapak aktif akan meningkatkan penyebaran adsorbat, sehingga dibutuhkan waktu lebih lama untuk mencapai kesetimbangan. Disisi lain efisiensi adsorpsi menyatakan banyaknya konsentrasi zat warna yang diadsorpsi oleh adsorben.
Karena itu nilainya hanya ditentukan oleh perubahan konsentrasi zat warna setelah diadsorpsi oleh adsorben. Semakin banyak adsorben yang digunakan, semakin banyak warna yang diadsorpsi. Hal ini memperkuat penelitian Diapati (2009) dan Victoria (2010) yang menyatakan bahwa peningkatan bobot adsorben akan menurukan kapasitas adsorpsi dan meningkatkan efisiensi adsorpsi.
Hasil penelitian menunjukkan bahwa efisiensi adsorpsi Cibacron Red meningkat dari 41.17% sampai 99.52% dengan variasi bobot dari 0.5 g sampai 2.5 g. Sebaliknya kapasitas adsorpsi menurun dari 2.06 mg/g menjadi 1.00 mg/g. Saat bobot 0.5 gram hampir seluruh permukaan adsorben telah terikat dengan adsorbat, sementara pada bobot 2.5 gram masih banyak tapak aktif yang belum berikatan dengan adsorbat.
Optimalisasi Adsorpsi Cibacron Red pada Arang Aktif
Waktu Adsorpsi
Data hasil penelitian pada Lampiran 7, yang diringkaskan pada Gambar 12, menunjukkan bahwa konsentrasi larutan cibacron red menurun dari 50 mg/L menjadi 16,13 mg/L. Waktu optimum adsorpsi adalah 90 menit dengan kapasitas adsorpsi 1,69 mg/g, artinya setiap 1 g adsorben mampu mengadsorpsi 1.69 mg ion Cibacron Red dalam waktu 90 menit dengan efisiensi adsorpsi 66.34%. Kapasitas dan efisiensi adsorpsi meningkat seiring dengan meningkatnya waktu adsorpsi. Tetapi menurun setelah melewati 90 menit. Hal ini sesuai dengan hasil penelitian Raghuvanshi et al. (2004) yang menyatakan bahwa efisiensi adsorpsi berbanding lurus dengan waktu sampai titik tertentu, kemudian menurun setelah melewati titik tersebut. Hal ini menunjukkan bahwa adsorben telah jenuh oleh zat warna Cibacron Red. Jika proses dilanjutkan, maka kemungkinan tidak ada lagi zat warna yang diadsorpsi oleh adsorben, sampai akhirnya terjadi pelepasan kembali atau desorpsi.
0,00 10,00 20,00 30,00 40,00 50,00 60,00 70,00 80,00 0 30 60 90 120 150 Waktu (menit) E fi si en si ad so rp si ( % ) 0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60 1,80 K a p asi tas ad s o rp si (m g/ g)
Efisiensi adsorpsi Kapasitas adsorpsi
Gambar 12 Waktu optimum adsorpsi Cibacron Red oleh arang aktif.
Bobot Adsorben
Bobot adsorben berpengaruh terhadap kapasitas dan efisiensi adsorpsi larutan Cibacron Red 50 mg/L oleh arang aktif (Gambar 13, Lampiran 8). Pada kondisi waktu dan konsentrasi yang sama, kenaikan bobot adsorben menurunkan kapasitas adsorpsi, tetapi meningkatkan efisiensi adsorpsi. Penambahan bobot adsorben pada volume dan konsentrasi zat warna yang tetap dapat meningkatkan kemampuan mengadsorpsi zat warna, namun kurang efektif. Hasil penelitian menunjukkan bahwa efisiensi adsorpsi cibacron red yang meningkat dari 46.84% sampai 81.25% dengan variasi bobot dari 0.5 g sampai 2.5 g. Penambahan jumlah adsorben akan menurunkan kapasitas adsorpsi spesifik dari 2.33 mg/g menjadi 0.81 mg/g. Hal ini disebabkan karena saat bobot 0.5 gram hampir seluruh permukaan adsorben telah terikat dengan adsorbat, sedangkan pada bobot 2.5 gram masih banyak tapak aktif yang belum berikatan dengan adsorbat.
0,00 10,00 20,00 30,00 40,00 50,00 60,00 70,00 80,00 90,00 0,50 1,00 1,50 2,00 2,50 bobot adsorben (g) E fis ie n s i a d s o rp s i ( % ) 0,00 0,50 1,00 1,50 2,00 2,50 Kap as it as a d so rp si ( % )
Efisiensi adsorpsi Kapasitas adsorpsi
Gambar 13 Pengaruh bobot adsorben arang aktif terhadap adsorpsi Cibacron Red.
Perbandingan Adsorpsi Cibacron Red pada Adsorben Ampas Tebu Teraktivasi
Asam dan Arang Aktif
Kinerja ATA dievaluasi dengan membandingkan kemampuan adsorpsinya dengan adsorben komersial, yaitu arang aktif. Hasil penelitian menunjukkan bahwa nilai kapasitas dan efisiensi adsorpsi Cibacron Red lebih besar diperoleh dengan menggunakan adsorben ATA (Tabel 1)
Tabel 1 Kapasitas dan Efisiensi adsorpsi Cibacron Red dengan adsorben ampas tebu teraktivasi asam (ATA) dan arang aktif (AA)
Adsorben EP (%) Q (mg/g)
ATA 84.00 2.10
AA 67.64 1.69
Gambar 14 Larutan Cibacron Red setelah diadsorpsi oleh adsorben ampas tebu teraktivasi asam (ATA).
Gambar 15 Larutan Cibacron Red setelah diadsorpsi oleh adsoben arang aktif (AA).
Gambar 14 dan 15 menujukkan perbedaan warna larutan Cibacron Red setelah diadsorpsi oleh ampas tebu teraktivasi asam dan arang aktif. Terlihat bahwa larutan Cibacron Red hasil adsorpsi dengan arang aktif lebih sedikit pekat daripada yang diadsorpsi oleh ATA. Gambar 16 menunjukkan bahwa kapasitas dan efisiensi
adsorpsi adsorben ampas tebu teraktivasi asam (ATA) lebih tinggi daripada arang aktif (AA) berturut-turut sebesar 2.10 mg/g dan 1.69 mg/g dan 84.02% dan 67.64%. Hal ini menunjukkan bahwa modifikasi asam pada adsorben dapat meningkatkan luas permukaan dan pori dari adsorben sehingga dapat digunakan sebagai adsorben alternatif dalam penjerapan larutan Cibacron Red. Hal ini sesuai dengan penelitian sebelumnya yang dilakukan oleh Raghuvanshi et al. (2004) dan Azhar et al. (2005) yang menyatakan bahwa modifikasi adsorben ampas tebu menggunakan asam dapat meningkatkan efisiensi adsorpsi terhadap zat warna.
0 10 20 30 40 50 60 70 80 90 ATA AA Adsorben E fi si en si ad so rp si ( % ) 0 0,5 1 1,5 2 2,5 K a p asi tas ad s o rp si (m g/ g)
Efisiensi adsorpsi Kapasitas Adsorpsi
Gambar 16 Efisiensi dan kapasitas adsorpsi ampas tebu teraktivasi asam (ATA) dan arang aktif (AA).
Isoterm Adsorpsi
Isoterm adsorpsi menunjukkan hubungan kesetimbangan antara konsentrasi adsorbat dalam fluida dan pada permukaan adsorben pada suhu tetap. Telah banyak adsorpsi yang dikembangkan untuk mendeskripsikan interaksi antara adsorben dan adsorbat. Tipe isoterm Freundlich dan Langmuir pada umumnya dianut oleh adsorpsi fase padat-cair (Atkins 1990). Lampiran 6 dan 7 menunjukkan hasil penentuan jenis isoterm adsorpsi ATA dan arang aktif.
Nilai linearitas (Gambar 17 dan 18) yang diperoleh dari kedua persamaan tersebut menunjukkan bahwa adsorben ampas tebu teraktivasi asam (ATA) mengikuti jenis isoterm Freundlich dan Langmuir. Hal ini dikarenakan nilai linearitas dari kedua persamaan tersebut yang tidak berbeda nyata. Hasil tersebut menunjukkan bahwa jenis ikatan yang terjadi antara adsorbat dan adsorben adalah fisisorpsi dan kimisorpsi. Freundlich mengasumsikan adsorpsi fase padat-cair berlangsung secara adsorpsi multilayer. Dalam fisisorpsi, ikatan antara adsorbat maupun ikatan antar adsorbat dengan adsorben bersifat lemah karena hanya
melibatkan interaksi Van der Waals. Sedangkan pada jenis adsorpsi kimisorpsi menunjukkan terbentuknya ikatan antara adsorbat dan adsorben yang berupa ikatan kovalen dan ikatan hydrogen sebagaimana yang telah ditunjukkan pada Gambar 6 dan 7.
0 0,5 1 1,5 2 -1 -0,5 0 0,5 1 1,5 2 Log C Log x /m
Gambar 17 Isoterm Freundlich adsorpsi zat warna Cibacron Red oleh ampas tebu teraktivasi asam (ATA).
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0 5 10 15 20 25 30 35 40 45 C (mg/l) C/ x /m ( g /l )
Gambar 18 Isoterm Langmuir adsorpsi zat warna Cibacron Red oleh ampas tebu teraktivasi asam (ATA). Sedangkan jenis isoterm dari arang aktif adalah Freundlich (Gambar 19 dan 20). Sementara itu, Cibacron Red dapat dijerap dengan baik oleh adsorben arang aktif akan tetapi pola penjerapannya kurang baik. Hal ini terlihat dari kelinieran kurva yang rendah (Lampiran 9). 0,0000 0,5000 1,0000 1,5000 2,0000 0,9000 1,0000 1,1000 1,2000 1,3000 1,4000 1,5000 1,6000 1,7000 Log C Log x /m
Gambar 19 Isoterm Freundlich adsorpsi zat warna Cibacron Red oleh arang aktif (AA). y = 1.3915 + 0.2469 x r = 0,9989 y = 0.0490 + 0.0159x r = 0.9924 y = 0.3784 + 0.126x r = 0,9083
0,0000 0,1000 0,2000 0,3000 0,4000 0,5000 0,6000 0,7000 0,8000 5,0000 10,0000 15,0000 20,0000 25,0000 30,0000 35,0000 40,000045,0000 C (mg/l) C/ x /m ( g /l )
Gambar 20 Isoterm Langmuir adsorpsi zat warna Cibacron Red oleh arang aktif (AA).
Bentuk logaritma dari persamaan Freundlich .
c
n
k
m
x
log
1
log
log
Nilai x/m menunjukkan massa adsorbat yang dijerap pergram adsorben, c menunjukkan konsentrasi kesetimbangan adsorbat dalam larutan setelah diadsorpsi (mg/l), dan n dan k menunujukkan konstanta empiris. Persamaan di atas menunjukkan jumlah zat warna yang dijerap oleh ampas tebu (log x/m) berbanding terbalik dengan nilai konstanta n dan berbanding lurus dengan konstanta k. Artinya jumlah zat warna yang dijerap akan semakin besar jika nilai konstanta n kecil dan nilai konstanta k besar. Nilai konstanta n, k, α, dan β dapat dihitung dari persamaan isoterm adsorpsi Freundlich dan Langmuir untuk Cibacron Red (Tabel 2 dan 3).
Tabel 2 Nilai konstanta n dan k dari persamaan Freundlich untuk ampas tebu teraktivasi asam (ATA) dan arang aktif (AA)
Adsorbat n k R
ATA 4.0502 24.6320 99.89
AA 7.9365 2.3900 90.83
Bentuk logaritma dari persamaan Langmuir:
c
m
x
c
1
1
/
Nilai x/m menunjukkan massa adsorbat yang dijerap pergram adsorben, c menunjukkan konsentrasi kesetimbangan adsorbat dalam larutan setelah diadsorpsi (mg/l), dan α dan β menunujukkan konstanta empiris.
Tabel 3 Nilai konstanta α dan β dari persamaan Langmuir untuk ampas tebu teraktivasi asam (ATA) dan arang aktif (AA)
Adsorbat α β R
ATA 62.8931 0.3245 99.24
AA 23.0952 0.0090 36.98
Nilai n dan k pada isoterm Freundlich tergantung pada suhu, adsorben, dan unsur-unsur yang dijerap. Nilai n menggambarkan intensitas dari adsorpsi, sedangkan nilai k menunjukkan kapasitas adsorpsi dari adsorben. Nilai α menggambarkan jumlah yang dijerap atau kapasitas adsorpsi untuk membentuk lapisan sempurna pada permukaan adsorben. Nilai β merupakan konstanta yang bertambah dengan kenaikan ukuran molekuler yang menunjukkan kekuatan ikatan molekul adsorbat pada permukaan adsorben.
Berdasarkan data penelitian Victoria (2010) yang menggunakan campuran limbah padat tapioka dan kaolin sebagai bahan dasar pembuatan adsorben memberikan hasil yang baik untuk penjerapan zat warna biru metilena. Hal ini dikarenakan kaolin dan limbah tapioka yang telah diaktivasi pada adsorben campuran tersebut menyebabkan sifat permukaan adsorben tersebut semakin bermuatan positif. Sehingga sangat baik digunakan untuk menjerap zat warna reaktif biru metilena yang bermuatan positif. Namun dalam penelitian ini memberikan hasil yang kurang baik untuk campuran kaolin-ampas tebu dan bentonit-ampas tebu. Seharusnya dengan bahan dasar yang sama-sama berbasis selulosa dapat memberikan hasil yang baik seperti penelitian sebelumnya yang menggunakan campuran limbah padat tapioka dan kaolin. Hal ini menunjukkan bahwa campuran kaolin-ampas tebu dan bentonit-ampas tebu kurang baik digunakan sebagai menjerap zat warna bermuatan negatif seperti Cibacron Red.
SIMPULAN DAN SARAN
SimpulanAdsorben dari ampas tebu teraktivasi asam menunjukkan dapat digunakan sebagai adsorben untuk zat warna Cibacron Red. Pengunaan adsorben dari campuran kaolin-amas tebu dan bentonit-ampas tebu dinilai kurang baik digunakan sebagai adsorben
y = 0.4654 + 0.0042x