BAB I PENDAHULUAN
A. Latar Belakang Masalah
Buah mengkudu (Morinda citrifolia L.) atau dikenal dengan Noni merupakan buah yang sering digunakan sebagai obat tradisional, salah satunya untuk terapi penyakit kardiovaskular sebagai antihiperkolesterol (Sasnan dkk., 2014). Efek antihiperkolesterol dari ekstrak mengkudu dibuktikan dari penelitian Sisca (2012) yang menunjukkan bahwa dosis 50 mg ekstrak etanol buah mengkudu yang diberikan setiap hari secara per oral selama 4 minggu pada tikus hiperkolesterol dapat menurunkan kolesterol total, trigliserida, LDL, dan rasio LDL/HDL. Penelitian Sasnan dkk. (2014) juga membuktikan bahwa ekstrak mengkudu dapat menurunkan kolesterol total sebesar 13,8% dan kadar LDL sebesar 15,5% pada pasien hiperkolesterolemia setelah diberikan dua kapsul ekstrak mengkudu dosis 500 mg yang dikonsumsi 3 kali sehari selama 2 minggu.
Buah mengkudu kaya akan flavonoid yang bermanfaat sebagai penghambat biosintesis lipid (Nandhasri dkk., 2005; Ramamoorthy dan Bono, 2007). Senyawa flavonoid terutama rutin dan kuersetin memiliki aktivitas antioksidan yang kuat dan mampu menghambat biosintesis kolesterol pada tikus hingga 50% (Glaser dkk., 2002). Namun, flavonoid rutin dan kuersetin diketahui memiliki kelarutan dalam air yang rendah yaitu 0,125 g/L dan 1,53-12,5 mg/L (Pedriali dkk., 2008; Pool dkk., 2013) sehingga berpengaruh pada terhambatnya proses absorpsi senyawa ke dalam tubuh. Absorpsi oral rutin dan kuersetin hanya sekitar 20% pada manusia (Hollman dkk., 1997). Kuersetin juga memberikan
bioavailabilitas yang rendah yaitu sekitar 16,2% pada tikus (Khaled dkk., 2003). Kelarutan dan absorpsi flavonoid rutin dan kuersetin yang rendah akan membuat efek antihiperkolesterolnya tidak maksimal.
Peningkatan kelarutan senyawa flavonoid rutin dan kuersetin dalam ekstrak mengkudu dapat dilakukan dengan formulasi berbasis lipid.
Self-Nanoemulsifying Drug Delivery System (SNEDDS) merupakan salah satu metode
formulasi berbasis lipid yang terdiri dari minyak, surfaktan, dan kosurfaktan yang akan membentuk nanoemulsi secara spontan ketika dimasukkan dalam media air disertai agitasi ringan (Nazzal dkk., 2002). Sediaan SNEDDS memiliki tetesan emulsi yang berukuran kurang dari 100 nm sehingga dapat meningkatkan absorpsi dan bioavailabilitas obat yang kelarutannya rendah dalam air (Singh dkk., 2009; Joshi dkk., 2013). Peningkatan absorpsi dan bioavailabilitas oral obat melalui formulasi SNEDDS juga dapat menurunkan dosis pemberian (Kumar dkk., 2010). Ekstrak etanolik buah mengkudu diformulasikan menjadi SNEDDS sebagai upaya untuk meningkatkan absorpsi dan bioavailabilitas dari flavonoid rutin dan kuersetin dalam ekstrak etanolik buah mengkudu sehingga diharapkan efek farmakologinya lebih maksimal.
Formulasi ekstrak etanolik buah mengkudu menjadi SNEDDS pada penelitian ini dilakukan menggunakan fase minyak berupa minyak nabati. Minyak nabati dipilih dalam formulasi SNEDDS karena aman dikonsumsi, mudah diperoleh, dan mengandung asam lemak dan vitamin larut lemak yang bermanfaat sebagai antioksidan (Jannin dkk., 2007). Komponen minyak nabati, surfaktan, dan kosurfaktan yang digunakan dalam formulasi SNEDDS ditentukan dengan
melakukan proses skrining terhadap kemampuan setiap komponen dalam melarutkan ekstrak paling banyak. Hasil formulasi SNEDDS dianalisis melalui karakterisasi kejernihan, waktu emulsifikasi dalam Artificial Gastric Fluid (AGF), stabilitas dalam Artificial Gastric Fluid (AGF) dan Artificial Intestinal Fluid (AIF), serta ukuran dan distribusi tetesan emulsi menggunakan Particle Size
Analyzer (PSA).
B. Rumusan Masalah
1. Apakah ekstrak etanolik buah mengkudu bersama minyak nabati, surfaktan, dan kosurfaktan terpilih dapat diformulasikan menjadi SNEDDS yang homogen?
2. Apakah formula optimum SNEDDS ekstrak etanolik buah mengkudu mampu membentuk emulsi secara spontan, jernih, stabil dalam AGF dan AIF, serta menghasilkan distribusi tetesan emulsi seragam dengan ukuran tetesan kurang dari 100 nm?
C. Tujuan Penelitian
1. Mengetahui komposisi minyak nabati, surfaktan, dan kosurfaktan terpilih yang dapat menghasilkan SNEDDS ekstrak etanolik buah mengkudu yang homogen.
2. Mengetahui formula optimum SNEDDS ekstrak etanolik buah mengkudu yang mampu membentuk emulsi secara spontan, jernih, stabil dalam AGF dan AIF, serta menghasilkan distribusi tetesan emulsi seragam dengan ukuran tetesan kurang dari 100 nm.
D. Manfaat Penelitian
Penelitian ini diharapkan dapat bermanfaat bagi perkembangan ilmu pengetahuan di bidang farmasi khususnya tentang sistem penghantaran obat berbasis nanoteknologi berupa sediaan SNEDDS. Selain itu, bagi industri farmasi diharapkan penelitian ini dapat dikembangkan menjadi suatu produk yang memanfaatkan bahan obat tradisional sehingga dapat menjadi pilihan alternatif bagi pengobatan pasien.
E. Tinjauan Pustaka 1. Buah Mengkudu (Morinda citrifolia L.)
Gambar 1. Buah Mengkudu
Klasifikasi tanaman:
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae
Bangsa : Rubiales Suku : Rubiaceae Marga : Morinda
Spesies : Morinda citrifolia L.
(BPOM RI, 2008)
Morinda citrifolia L. memiliki nama yang berbeda di setiap negara antara
lain Noni di Hawaii, Indian mulberry di India, Ba Ji Tian di China, Nonu atau Nono di Tahiti, Cheese fruit di Australia, Mengkudu atau Pace di Indonesia dan Malaysia (Wang dkk., 2002). Buah mengkudu berbentuk bongkol, permukaan tidak teratur, berdaging, panjang 3-10 cm dan bisa mencapai 20 cm. Buah mengkudu muda berwarna hijau, menjelang masak berwarna putih kekuningan, dan setelah masak berwarna putih transparan, lunak, dan berbau busuk (McClatchey, 2002). Buah mengkudu mengandung berbagai macam senyawa antara lain iridoid, kumarin (skopoletin), flavonoid (rutin, kuersetin, kaempferol), terpenoid, alkaloid (prokseronin, seronin), polisakarida, asam lemak (asam linoleat, asam kaproat, asam kaprilat, asam ursolat), antrakuinon (nordamnakantal, morindon, rubiadin), lignan, dan fitosterol (Potterat dan Hamburger, 2007; Wang dkk., 2002).
Buah mengkudu banyak dimanfaatkan sebagai bahan obat tradisional. Buah mengkudu dilaporkan memiliki efek terapetik yang luas. Beberapa penelitian telah membuktikan bahwa buah mengkudu dapat memberikan efek antiinflamasi (Mckoy dkk., 2002), hipoglikemik dan hepatoprotektif (Nayak dkk.,
2011), hipolipidemik (Hadijah dkk., 2008; Sasnan dkk., 2014), antihipertensi (Palu dkk., 2008), dan aktivitas antioksidan (Ikeda dkk., 2009).
Buah mengkudu mengandung antioksidan yang memiliki potensi besar untuk menghambat radikal bebas. Mengkudu kaya akan flavonoid yang dapat menghambat biosintesis lipid dengan cara menghambat enzim HMG Co-A reduktase (Ramamoorthy dan Bono, 2007; Palu dkk., 2012). Dosis 250, 500, dan 1000 mg/kg BB ekstrak air buah mengkudu dapat menurunkan kadar trigliserida dalam plasma tikus diabetes (Hadijah dkk., 2008). Ekstrak etanolik buah mengkudu dapat menurunkan kolesterol total sebesar 13,8% dan kadar LDL sebesar 15,5% pada pasien hiperkolesterolemia setelah diberikan dua kapsul ekstrak mengkudu dosis 500 mg yang dikonsumsi 3 kali sehari selama 2 minggu (Sasnan dkk., 2014).
Buah mengkudu banyak diformulasikan dalam bentuk sediaan jus, tablet, dan kapsul. Bentuk tablet dan kapsul ekstrak mengkudu telah mampu menutupi bau tidak enak dari buah mengkudu (Hertiani dkk., 2011). Buah mengkudu pernah diformulasikan menjadi tablet effervescent dengan bahan pemanis sukrosa dan aspartam (Hertiani dkk., 2011). Puspitasari (2007) juga pernah memformulasikan sari buah mengkudu menjadi sediaan granul effervescent. Formulasi tersebut bertujuan untuk mempermudah konsumsi buah mengkudu sebagai suplemen tambahan.
2. Self-Nanoemulsifying Drug Delivery System (SNEDDS)
Self-Nanoemulsifying Drug Delivery System (SNEDDS) merupakan salah
formulasi senyawa dengan kelarutan dalam air rendah (Kalepu dkk., 2013). Sediaan SNEDDS terdiri dari campuran isotropik antara obat, minyak, surfaktan, dan satu atau lebih kosurfaktan yang ketika kontak dalam media air seperti cairan lambung disertai agitasi ringan akan membentuk nanoemulsi minyak dalam air (o/w) (Nazzal dkk., 2002). Emulsi yang terbentuk berukuran kurang dari 100 nm. Ukuran droplet yang mencapai nanometer dapat meningkatkan absorpsi oral sehingga dapat meningkatkan bioavailabilitas obat (Joshi dkk., 2013). Sediaan SNEDDS juga memiliki keunggulan lain yaitu stabilitas penyimpanannya lebih baik dibandingkan emulsi, dapat memperkecil dosis, serta dapat melindungi obat yang sensitif terhadap pengaruh lingkungan lambung (Kumar dkk., 2010).
Sediaan SNEDDS dibagi menjadi 5 grade berdasarkan penilaian tampilan visual dan waktu emulsifikasi (Heshmati dkk., 2013), yaitu: Grade A menghasilkan tampilan visual emulsi yang jernih dengan waktu emulsifikasi kurang dari 1 menit. Grade B menghasilkan tampilan visual sedikit jernih dan putih kebiruan dengan waktu emulsifikasi kurang dari 2 menit. Grade C menghasilkan emulsi dengan tampilan visual putih (seperti susu) dengan waktu emulsifikasi kurang dari 3 menit. Grade D menghasilkan emulsi dengan tampilan visual keruh dan ada sedikit lapisan minyak dengan waktu emulsifikasi lebih dari 3 menit. Grade E menghasilkan emulsi dengan tampilan tetesan minyak yang besar pada permukaan dengan waktu emulsifikasi lebih dari 3 menit.
Formula SNEDDS yang optimal dipengaruhi oleh rasio komponen minyak, surfaktan, dan kosurfaktan, sifat fisikokimia obat dan komponen, serta pH dan suhu saat emulsifikasi terjadi (Date dkk., 2010). Pemilihan dan optimasi
komponen SNEDDS sangat penting dilakukan karena komposisi dari komponen SNEDDS akan mempengaruhi karakteristik nanoemulsi seperti, ukuran tetesan,
polydispersity index, waktu emulsifikasi, dan pelepasan obat secara in vitro
(Sakthi dkk., 2013). Komponen utama SNEDDS adalah: a. Minyak
Minyak merupakan komponen penting dalam formulasi SNEDDS karena minyak berfungsi sebagai media pembawa obat dan akan memfasilitasi terjadinya emulsifikasi. Sifat fisikokimia minyak seperti berat molekul, polaritas, dan viskositas dapat mempengaruhi spontanitas terbentuknya nanoemulsi, ukuran tetesan nanoemulsi, dan kelarutan obat (Date dkk., 2010). Minyak yang dipilih untuk formulasi SNEDDS adalah minyak yang dapat melarutkan obat secara maksimal dan mampu membentuk emulsi berukuran nanometer dalam waktu singkat (Date dkk., 2010).
Modifikasi panjang dan pendeknya rantai trigliserida serta tingkat kejenuhan rantai trigliserida pada minyak merupakan faktor penentu keberhasilan formulasi SNEDDS (Singh dkk., 2009). Trigliserida diklasifikasikan menjadi tiga, yaitu rantai pendek (<5 atom C), medium (6-12 atom C), dan panjang (>12 atom C) (Sarpal dkk., 2010). Minyak dengan trigliserida rantai panjang lebih sulit teremulsi dibandingkan minyak dengan trigliserida rantai medium dan rantai pendek (Anton dan Vandamee, 2009).
Minyak nabati adalah salah satu jenis minyak yang dapat digunakan untuk formulasi SNEDDS. Minyak nabati dipilih karena aman dikonsumsi dan mudah diperoleh. Minyak nabati terdiri dari trigliserida (90-95%), asam lemak bebas,
fosfolipid, dan non saponifiable product seperti pigmen dan sterol atau vitamin larut lemak seperti tokoferol dan karotenoid yang bermanfaat sebagai antioksidan alami sehingga mencegah minyak dari ketengikan (Jannin dkk., 2007). Minyak nabati yang umum digunakan dalam formulasi SNEDDS yaitu minyak zaitun, minyak jagung, minyak kedelai, dan Virgin Coconut Oil (VCO) (Patel dkk., 2010).
Virgin Coconut Oil (VCO) merupakan minyak nabati terpilih yang
digunakan dalam formulasi SNEDDS pada penelitian ini. Minyak VCO tersusun atas 92% asam lemak jenuh (90% rantai medium dan 10% rantai panjang), 6% asam lemak monounsaturated, dan 2% asam lemak polyunsaturated (Harini dan Astirin, 2009). Asam lemak rantai medium dalam VCO terdiri dari asam laurat, asam miristat, dan asam palmitat (Syah, 2005). Kandungan asam lemak tertinggi dalam VCO adalah asam laurat (C12H24O2) sebesar 45-55% (Harini dan Astirin, 2009). Asam laurat adalah asam lemak rantai medium dengan atom C-12 yang dapat diabsorpsi dengan mudah serta mempunyai kemampuan meningkatkan laju metabolisme dan penyerapan nutrisi dalam tubuh (Santos dkk., 2005; Harini dan Astirin, 2009). Asam lemak rantai medium tidak memasuki siklus kolesterol dan tidak disimpan sebagai lemak di dalam tubuh sehingga tidak menyebabkan obesitas (Dayrit, 2003). Minyak VCO juga terbukti dapat menurunkan total kolesterol dan kadar LDL serta meningkatkan kadar HDL dalam darah pada tikus hiperkolesterol (Harini dan Astirin, 2009). Minyak VCO pernah digunakan sebagai fase minyak dalam formulasi SNEDDS ketoprofen oleh Zein (2014) dengan komposisi 0,833 mL VCO, 3,565 mL tween 80, 0,605 mL PEG 400 yang
mampu membentuk nanoemulsi dengan ukuran diameter tetesan sebesar 2,8 ± 0,7 nm dan nilai PI sebesar 0,402.
Gambar 2. Struktur asam laurat
b. Surfaktan
Surfaktan atau surface active agent adalah suatu molekul yang memiliki dua bagian dalam struktur kimianya, yaitu bagian hidrofilik dan hidrofobik (Attwood dan Florence, 2008). Surfaktan juga dapat berperan dalam melarutkan obat. Surfaktan yang berasal dari alam lebih aman digunakan dibanding surfaktan sintetis, namun surfaktan alami memiliki kemampuan self-emulsification yang kurang baik sehingga jarang digunakan dalam formulasi SNEDDS (Singh dkk., 2009).
Karakteristik surfaktan seperti HLB, viskositas, dan afinitas terhadap fase minyak memiliki pengaruh pada proses emulsifikasi dan ukuran tetesan nanoemulsi (Date dkk., 2010). Surfaktan yang digunakan untuk formulasi SNEDDS adalah surfaktan dengan nilai HLB lebih dari 10 (Kommuru dkk., 2001). Semakin tinggi nilai HLB, surfaktan semakin besifat hidrofilik dan dapat dengan mudah membentuk emulsi minyak dalam air (o/w) (Attwood dan Florence, 2008). Surfaktan non-ionik lebih sering digunakan daripada surfaktan ionik karena sifatnya yang kurang terpengaruh oleh pH, aman, dan biokompatibel untuk penggunaan melalui rute oral (Azeem dkk., 2009; Patel dkk., 2011).
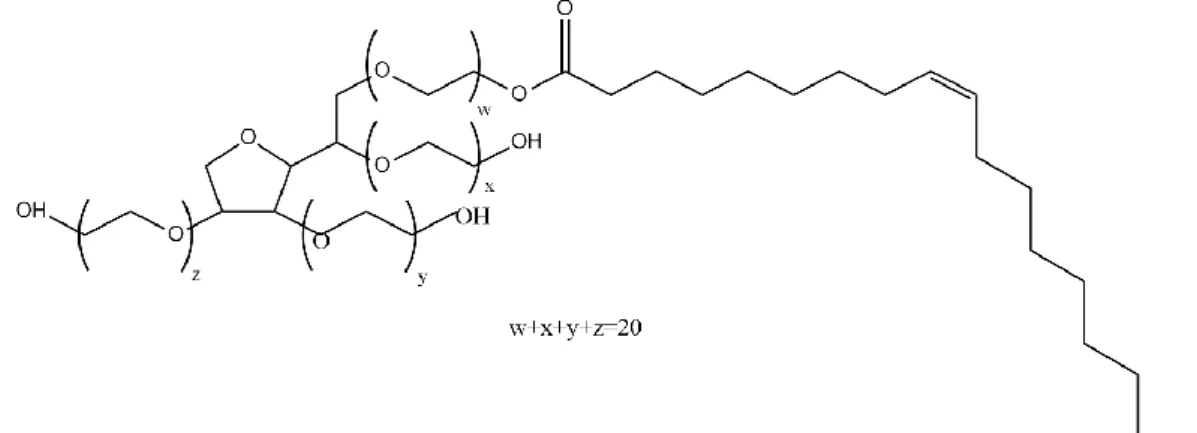
Surfaktan yang terpilih pada penelitian ini adalah tween 80. Tween 80 atau polioksietilen-20-sorbitan monooleat merupakan surfaktan non-ionik hidrofilik dengan nilai HLB 15 (Rowe dkk., 2009) sehingga cocok digunakan dalam formulasi SNEDDS. Tween 80 terdiri dari 70% asam oleat dan beberapa asam lemak seperti asam palmitat (Shah dkk., 1994). Tween 80 biasa dimanfaatkan sebagai emulgator, peningkat kelarutan, dan peningkat penetrasi (Rowe dkk., 2009; Akhtar dkk., 2011). Batas aman konsumsi tween 80 adalah 25 mg/kg BB per hari (Rowe dkk., 2009). Fathoroni (2014) berhasil memformulasikan SNEDDS simvastatin menggunakan surfaktan tween 80, kosurfaktan PEG 400, dan minyak zaitun dengan komposisi 80%:10%:10% yang menghasilkan rata-rata ukuran nanoemulsi sebesar 26,166 ± 7,52 nm, waktu emulsifikasi kurang dari 1 menit, serta stabil dalam media akuades, AGF, dan AIF.
Gambar 3. Struktur Tween 80
c. Kosurfaktan
Kosurfaktan adalah molekul ampifilik lemah yang berfungsi untuk mendukung agregasi dari surfaktan dalam pembuatan emulsi (Chennamsetty dkk.,
2005). Kosurfaktan ditambahkan pada formula SNEDDS untuk meningkatkan disolusi, absorpsi obat, drug loading, mempercepat waktu emulsifikasi, dan mengatur ukuran tetesan emulsi (Han dkk., 2011; Makadia dkk., 2013). Penambahan kosurfaktan pada formulasi nanoemulsi berpengaruh pada penurunan tegangan antarmuka dan mencegah terjadinya koalesen (Parmar dkk., 2011). Kosurfaktan yang sering digunakan seperti span, propilen glikol, polietilen glikol, dan polioksietilen dapat membantu melarutkan surfaktan hidrofil maupun obat lipofil ke dalam basis minyak (Kumar dkk., 2010). Struktur dan panjang rantai hidrofobik pada kosurfaktan mempengaruhi pembentukan nanoemulsi. Semakin panjang rantai, pembentukan nanoemulsi semakin baik (Parmar dkk., 2011).
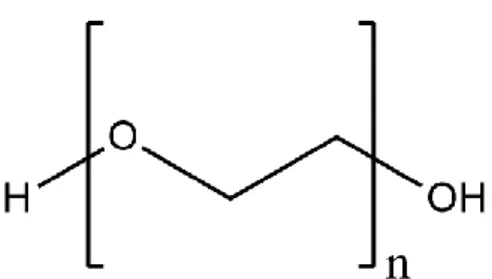
Kosurfaktan yang digunakan pada penelitian ini adalah polietilen glikol 400 atau PEG 400. Kosurfaktan PEG 400 termasuk bahan toksik dan non-iritan sehingga aman digunakan. Berat molekul PEG 400 berkisar antara 380-420 g/mol (Rowe dkk., 2009). Kosurfaktan PEG 400 berwujud cairan kental, tidak berwarna, dan transparan. Kosurfaktan PEG 400 memiliki nilai HLB yang tinggi yaitu 11,6 sehingga dapat membantu surfaktan dalam meningkatkan pembentukan nanoemulsi secara spontan. Batas aman konsumsi PEG 400 adalah 10 mg/kg BB per hari (Rowe dkk., 2009). Penelitian Zein (2014) berhasil membuat formulasi SNEDDS ketoprofen menggunakan kosurfaktan PEG 400, surfaktan tween 80, dan minyak nabati sebagai fase minyak yang dapat membentuk nanoemulsi dengan waktu emulsifikasi 44,43 ± 0,232 detik dalam AGF dengan ukuran tetesan nanoemulsi sebesar 2,8 ± 0,7 nm.
Gambar 4. Struktur PEG 400
F. Landasan Teori
Sediaan SNEDDS merupakan sistem penghantaran obat berbasis lipid yang terdiri dari obat, minyak, surfaktan, dan satu atau lebih kosurfaktan yang ketika kontak dalam media air seperti cairan lambung disertai agitasi ringan akan membentuk nanoemulsi minyak dalam air (o/w) (Nazzal dkk., 2002). Emulsi yang terbentuk berukuran kurang dari 100 nm sehingga dapat meningkatkan absorpsi oral dan bioavailabilitas obat (Joshi dkk., 2013). Keberhasilan formulasi SNEDDS dapat dikarakterisasi melalui beberapa parameter yaitu, kejernihan, waktu emulsifikasi, stabilitas dalam AGF dan AIF, serta ukuran diameter tetesan emulsi.
Komponen minyak yang dipilih untuk formulasi SNEDDS adalah minyak yang dapat melarutkan obat paling banyak dan menghasilkan emulsi berukuran nanometer dalam waktu singkat. Minyak nabati dipilih dalam penelitian ini karena aman dikonsumsi, mudah diperoleh, dan mengandung asam lemak dan vitamin larut lemak yang bermanfaat sebagai antioksidan alami (Jannin dkk., 2007). Fathoroni (2014) telah memformulasikan simvastatin menggunakan minyak nabati sebagai fase minyak dengan komposisi 10% minyak zaitun, 80% tween 80, dan 10% PEG 400 yang menghasilkan nanoemulsi dalam waktu kurang dari 1 menit dengan ukuran 26,166 ± 7,522 nm serta stabil dalam akuades, AGF, dan
AIF. Formulasi SNEDDS dengan minyak nabati juga pernah dilakukan oleh Pramudita (2014) yang menggunakan ketoprofen, VCO sebagai fase minyak, surfaktan tween 80 dan tween 20, serta kosurfaktan PEG 400. Penelitian tersebut menghasilkan nanoemulsi jernih dengan nilai transmitan lebih dari 99,0% dengan waktu emulsifikasi dalam AGF 4,27 menit, stabil dalam AGF dan AIF, serta memiliki ukuran tetesan nanoemulsi sebesar 2,1 ± 0,6 nm dengan distribusi ukuran tetesan yang seragam.
Bahan obat tradisional dapat diformulasikan menjadi SNEDDS. Beberapa penelitian terbukti berhasil memformulasikan ekstrak tanaman menjadi sediaan SNEDDS. Penelitian Li dkk. (2011) berhasil memformulasikan ekstrak daun
Diospyros kaki dalam sediaan SNEDDS dengan komposisi Cremophor EL,
Transcutol P, Labrafil M 1944 CS (56:34:10 w/w) yang secara signifikan dapat meningkatkan bioavailabilitas senyawa aktif yaitu flavonoid kuersetin dan kaempferol sebesar 1,5 dan 1,6 kali lebih tinggi dibanding ekstrak dalam sediaan tablet. Hafizah (2014) juga berhasil membuat formulasi SNEDDS dari kombinasi ekstrak Curcuma xanthorrhiza Roxb. dan daun Gynura procumbens menggunakan minyak nabati yaitu VCO, surfaktan tween 80, dan kosurfaktan PEG 400. Penelitian tersebut menghasilkan sistem SNEDDS homogen dengan kemampuan melarutkan 40 mg kombinasi ekstrak tiap mL, waktu emulsifikasi selama 58,14 ± 2,65 detik dalam AGF, nilai transmitan 97,57 ± 0,76%, dan diameter nanoemulsi sebesar 4,0 ± 0,0 nm. Berdasarkan penelitian-penelitian tersebut, ekstrak tanaman dan minyak nabati baik rantai panjang maupun rantai
medium dapat diformulasikan menjadi SNEDDS yang homogen dan menghasilkan emulsi secara spontan berukuran nanometer.
G. Hipotesis Hipotesis pada penelitian ini adalah:
1. Komposisi minyak nabati, surfaktan, dan kosurfaktan terpilih dapat menghasilkan SNEDDS ekstrak etanolik buah mengkudu yang homogen. 2. Formula optimum SNEDDS ekstrak etanolik buah mengkudu mampu
membentuk emulsi secara spontan, jernih, stabil dalam AGF dan AIF, serta menghasilkan distribusi tetesan emulsi seragam dengan ukuran tetesan kurang dari 100 nm.