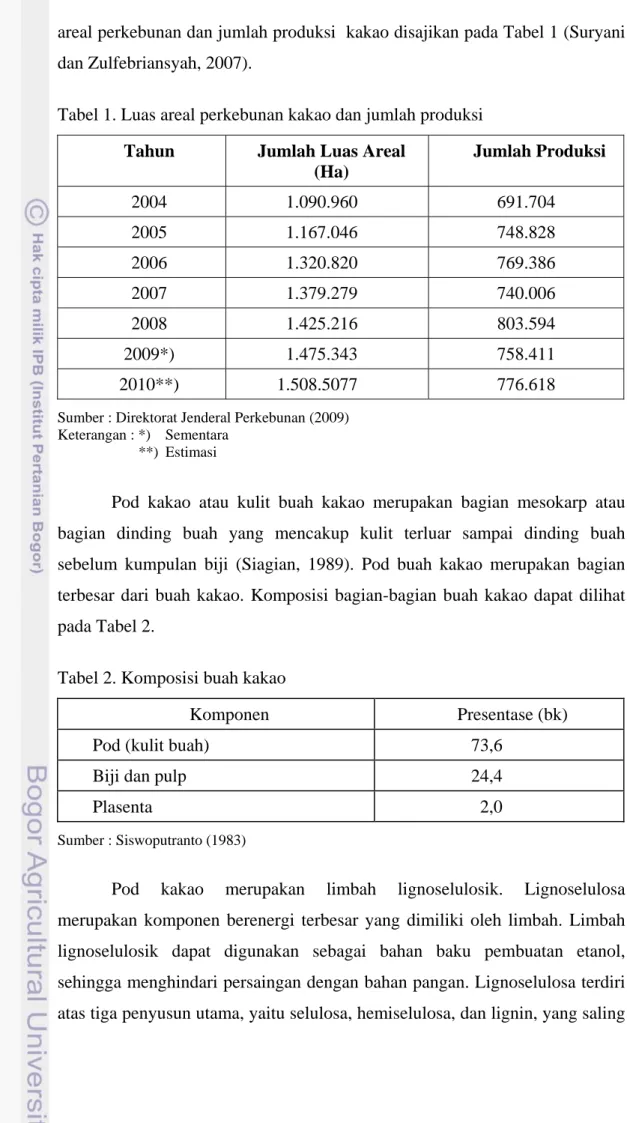
Pod (kulit buah) Biji dan pulp
Plasenta II. TINJAUAN PUSTAKA
KAKAO (Theobroma cacao) Tanam
A.
an kakao (Theobroma cacao) merupakan tanaman tropis yang berasal
yak ditanam di daerah Sulawesi Selatan, Lampung, Sumate
dari hutan tropis Amerika Selatan. Oleh bangsa Maya buah tanaman tersebut disebut ka-ka-wa dan dalam bahsa Nahuat disebut xocoat. Kemudian oleh Linnaeus, tanaman tersebut diberi nama Theobroma yang berarti makanan dewa-dewa (food of gods). Kakao (Theobroma cacao) merupakan tanaman perkebunan yang diharapkan buahnya. Pada umumnya bagian buah kakao yang dimanfaatkan adalah biji kakao. Bagian-bagian lain dari buah kakao seperti pod dan plasenta merupakan limbah yang belum banyak dimanfaatkan (Anonim, 2009).
Gambar 1. Bagian-bagian buah kakao (Anonim, 2009)
Kakao ban
ra Utara, Nusa Tenggara Timur, dan Papua. Komoditi ini merupakan salah satu sumber devisa negara, sehingga keberadaan perkebunan dan produktivitasnya terus ditingkatkan. Sejak tahun 1980 Pemerintah memberikan prioritas terhadap produksi kakao sebagai salah satu mata dagangan yang dikembangkan secara cepat. Produksinya sebagian besar diekspor, khususnya ke negara-negara Belanda, Jerman Barat, Amerika Serikat, dan Singapura. Saat ini produksi kakao Indonesia menempati urutan terbesar kedua setelah Pantai Gading dan sudah bisa melampaui Ghana. Luas
areal perkebunan dan jumlah produksi kakao disajikan pada Tabel 1 (Suryani dan Zulfebriansyah, 2007).
Tabel 1. Luas areal perkebunan kakao dan jumlah produksi Tahun Jumlah Luas Areal
(Ha) Jumlah Produksi 2004 1.090.960 691.704 2005 1.167.046 748.828 2006 1.320.820 769.386 2007 1.379.279 740.006 2008 1.425.216 803.594 2009*) 1.475.343 758.411 2010**) 1.508.5077 776.618 Sumber : Dire Keterangan : *
ktorat Jenderal Perkebunan (2009) ) Sementara
erupakan bagian
Tabel 2. Kom
Komponen Presentase (bk)
**) Estimasi
Pod kakao atau kulit buah kakao merupakan bagian mesokarp atau bagian dinding buah yang mencakup kulit terluar sampai dinding buah sebelum kumpulan biji (Siagian, 1989). Pod buah kakao m
terbesar dari buah kakao. Komposisi bagian-bagian buah kakao dapat dilihat pada Tabel 2.
posisi buah kakao
Pod (kulit buah) 73,6
Biji dan pulp 24,4
Plasenta 2,0 Sumber : Siswoputranto (1983)
Pod kakao merupakan limbah lignoselulosik. Lignoselulosa merupakan komponen berenergi terbesar yang dimiliki oleh limbah. Limbah lignoselulosik dapat digunakan sebagai bahan baku pembuatan etanol, sehingga menghindari persaingan dengan bahan pangan. Lignoselulosa terdiri atas tiga penyusun utama, yaitu selulosa, hemiselulosa, dan lignin, yang saling
terikat erat membentuk satu kesatuan. Komposisi kimia pod kakao disajikan ada Tabel 3.
abel 3. Komposisi kimia pod kakao
No Komponen Persentase (bk) p T 1 Kadar air 12.96 2 Kadar abu 11.10 3 Kadar lemak 1.11 4 Kadar protein 8.75 5 Kadar karbohidrat 16.27 6 Kadar lignin 20.11 7 Kadar selulosa 31.25 8 Kadar hemiselulosa 48.64 Sumber : Ashadi (1988) LIGNOSELULOSA
Lignoselulosa merupakan komponen berenergi terbesar yang dimiliki oleh biomassa dan dapat digunakan sebagai bahan baku pembuatan etanol sehingga menghindari persaingan dengan bahan pangan. Lignoselulosa memiliki tiga penyusun utama, yaitu selulosa, hemiselulosa, dan lignin yang saling terikat erat membentuk satu kesatuan (Sun dan Cheng, 2002).
B.
1. Selulosa
elimpah pada hamp struktu umbuhan biasanya selulosa berasosiasi dengan polisakarida lain seperti hemiselulosa dan lignin memb kerangka utam sel tumbuhan (Holtzapple, 1993). Selulo rupakan polisakarida yang terdiri atas satu glukosa yang terikat dengan ikatan sidik. Isolasi selul butuhkan perlakuan kimia yang intensif. Residu glukosa tersusun dengan posisi
ikata dan selanjutnya pengulangan
Selulosa merupakan jenis polisakarida yang paling m ir setiap r tumbuhan. Pada t
entuk a dinding
sa me an-satuan
β-1.4-gliko osa mem n 180oβ antara satu dengan yang lain
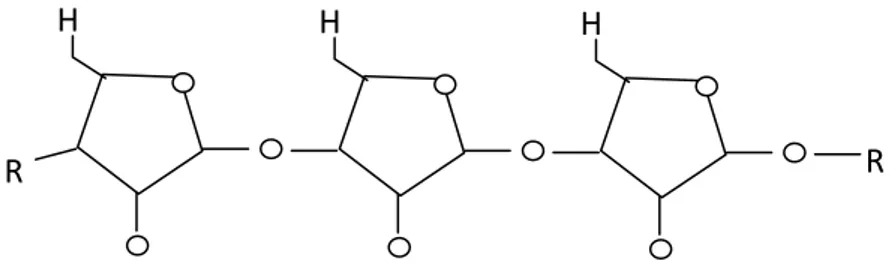
unnit dari ranttai selulosaa membentuuk unit sellobiosa (O’Sullivan, 11997). Strruktur seluloosa dapat diilihat pada GGambar 2.
–
Gambar 2. Sttruktur kimiia selulosa ((Girindra, 1990)
O me Gugus OH ini dapa embentu s fungsional at
l dari rantaii selulosa addalah guguss hidroxil.
sel sel uju dis 19 sat Pa po sel 27 me me sem et me Hi bag k i lulosa deng lulosa menj ungnya. Uju stabilkan ol 93). Molek tu dengan anjang mole limer yang lulosa terga 000 unit g enggunakan enghasilkan mpurna aka al., 1982) enjadi etano Mikro drolisis selu gian berkri berinterak katan hidro gan air. G jadi hidrofil ung –C1 m eh ikatan hi kul selulosa lainnya m ekul selulos g disebut d antung pada glukan. Selu n asam ata n monomer an menghasi . Selanjutn ol. ofibril terdi ulosa akan istal. Pada
ksi satu sam ogen. Ikatan Gugus –OH lik. Rantai memiliki sif idrogen yan a merupakan membentuk sa ditentuka dengan dera jenis tanam ulosa dapat au enzim. selulosa ya ilkan disaka nya glukosa iri dari ba lebih muda kenyataann ma lain deng n –H juga H selulosa selulosa m fat pereduk ng kuat dise n mikrofibr rantai polim an oleh jum ajat polimer man dan um t dihidrolisi Hidrolisis aitu glukosa arida dari se a yang dih agian berk ah terjadi p nya selulos gan gugus – G – Gugus O, –N, d terjadi ant a tara gugus an –S, –OH menyebabbkan permuukaan memiliki guggus –H di kkedua
ksi. Struktur epanjang ran
ril dari gluk mer yang mlah unit g r rantai sel ntai (Holtza kosa yang te sangat pan glukan di d lulosa apple, erikat njang. dalam risasi. Deraajat polimeerisasi mumnya dalaam kisaran 2
2000-is menjadi se glukosa dee mpurna a, sedangkan elulosa yait hasilkan dap kristal dan pada bagian sa terdiri d a selulosa n hidrolisis tu sel ngan akan tidak obiosa pat a (Fan diferme bag entasi ian a n amo amorf. rf dar dari 1 ripada 5% bbagian
amo merupakan bagian berkristal ( t al., 1978).
isis selulosa lebih sulit untuk dilakukan. Susunan bagian berkristal lebih teratur dan rapat. Bagian ini sukar bereaksi dengan pereaksi tertentu. Pada bagian tersebut pengikatan antar molekul selulosa
2. Hemiselulosa
miselulosa merupakan suatu polisakarida lain yang terdapat dalam tanam
asam. Hemiselulosa merupakan polisakarida yang mempunyai berat
menghasilkan D-glukosa, sedangkan hasil hidrolisis hemiselulosa akan menghasilkan D-xilosa dan monosakarida lainnya (Winarno, 1984). Menurut Janes (1969), monomer gula penyusun hemiselulosa terdiri dari monomer gula berkarbon lima (pentosa) dan enam (heksosa), misalnya xilosa, arabinosa, manosa, glukosa, galaktosa, dan sejumlah kecil ramnosa, asam glukoroat, asam metal glukoronat, dan asam galaturonat. Kandungan hemiselulosa di
dalam biom 7% (berat
kering biomassa). Hemiselulosa lebih mudah dihidrolisis daripada selulos
rf dan 85% lainnya Tsao e
Akibatnya hidrol
terutama terjadi karena ikatan hidrogen. Ikatan kimia hidrogen antara molekul selulosa yang berdekatan berfungsi untuk memperkuat struktur mikrofibril. Sebagai akibatnya bagian berkristal ini tidak larut dalam air dan bersifat sangat stabil (Whistler et al., 1985).
He
an dan tergolong senyawa organik. Casey (1952) menyatakan bahwa hemiselulosa bersifat non-kristalin, tidak bersifat serat, dan mudah mengembang karena itu hemiselulosa sangat berpengaruh terhadap bentuk jalinan antar serat pada saat pembentukan lembaran. Hemiselulosa lebih mudah larut dalam pelarut alkali dan lebih mudah dihidrolisis dengan
molekul lebih kecil daripada selulosa.
Perbedaan hemiselulosa dengan selulosa yaitu hemiselulosa mudah larut dalam alkali tapi sukar larut dalam asam, sedang selulosa adalah sebaliknya. Hemiselulosa juga bukan merupakan serat-serat panjang seperti selulosa. Hasil hidrolisis selulosa akan
assa lignoselulosa berkisar antara 11% hinga 3
H H H
R daripada gula heksosa (Perez et al., 2002). Rumus bangun hemiselulosa dapat dilihat pada Gambar 3.
R
traksi. Rata-rata derajat polimerisasi dari hemiselulosa bervari
3.
bobot molekul kira-kira 11.000 yang dibentuk oleh tiga dimensi polimerisasi. Lignin merupakan ek yang tersusun dari unit fenil propana yang terikat di dalam s
Gambar 3 . Struktur polimer hemiselulosa. (Frassoldati et al., 2005)
Hemiselulosa umumnya dikelompokkan berdasarkan residu gula utama yang menyususun rangkanya, seperti xilan, mannan, galaktan, dan glukan, dengan xilan dan mannan adalah gugus utama dari hemiselulosa. Hemiselulosa umumnya dilaporkan berasosiasi secara kimia atau terikat silang dengan polisakarida, protein, atau lignin. Xilan kemungkinan sebagai wilayah ikatan utama antara lignin dan karbohirat lain. Hemiselulosa lebih mudah larut daripada selulosa dan dapat diisolasi dari kayu dengan eks
asi antara 70 dan 200 tergantung pada jenis kayu (Achmadi, 1989).
Lignin
Lignin merupakan salah satu dari tiga komponen dasar biomassa. Lignin merupakan bahan organik bukan karbohidrat yang berbentuk amorf dan tersusun atas satuan-satuan fenol (Chang et al., 1981). Jaringan polimer fenolik pada lignin berfungsi merekatkan serat selulosa dan hemiselulosa sehingga menjadi sangat kuat (Sun dan Cheng, 2002).
Lignin adalah komplek polimer hidrokarbon dengan komponen senyawa alifatik dan aromatik. Brown (1979) mengatakan bahwa lignin merupakan polimer aromatik kompleks dengan
molekul kompl
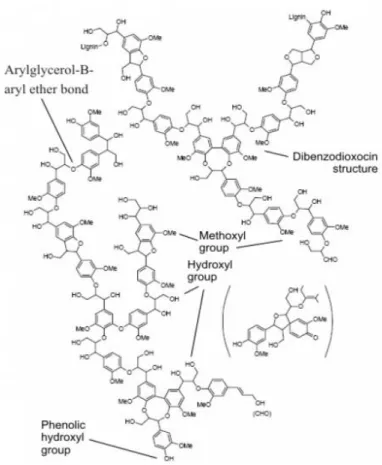
Gambar 4. Struktur kimia lignin (Brunov, 1998)
Lignin adalah material yang paling kuat di dalam biomassa. Lignin sangat resisten terhadap degradasi, baik secara biologi, enzimatis, maupun kimia. Karena kandungan karbon yang relatif tinggi dibandingkan dengan selulosa dan hemiselulosa, lignin memiliki kandungan energi yang tinggi (Palonen, 2004). Lignin ditemukan secara alami sebagai bagian integral dari dinding sel tanaman, terbenam di dalam polimer matrik dari selulosa dan hemiselulosa. Komposisi lignin di alam sangat bervariasi tergantung pada spesies tanaman.
emiliki struktur yang bermacam-macam. Lignin seperti terdiri dari daerah amorf dan bentuk-bentuk terstruktur seperti partikel
tab
i-dimensional lignin sangat dipengaruhi oleh matrik polisakarida. Simulasi dinamik m
Lignin m
ung dan globul. Ada indikasi pula bahwa struktur kimia dan tr
enunjukkan bahwa gugus hidroksil dan metoksil di dalam prekusor lignin dan oligomer mungkin berinteraksi dengan mikrofibril selulosa sejalan dengan fakta bahwa lignin memiliki karakteristik hidrofobik (Faix et al., 1985).
Lignin mempunyai sifat fisik dan kimia yang berbeda dengan selulosa. Menurut Pasaribu (1987), lignin mudah dioksidasi oleh larutan alkali dan bahan-bahan oksidator, tahan terhadap hidrolisis oleh asam-asam mineral, mudah larut dalam larutan sulfit pada keadaan basa dan lignin yang telah dihalogenasi dengan klor akan mudah larut dalam alkali. Struktur kimia lignin mengalami perubahan di bawah kondisi suhu yang an asam. Pada reaksi dengan temperatur tinggi mengakibatkan lignin t
tinggi lignin
C. ET
massa lignoselulosa dapat dikelompokkan menjadi dua kelompok besar, yaitu platform biokimia (biochemical platform) atau gula (sugar platform) dan platform termokimia (thermochemical
platform). Platform biokimia meliputi proses hidrolisis selulosa dan
hemiselulosa menjadi monomer gula penyususnnya, fermentasi gula menjadi ethanol, destilasi dan dehidrasi untuk menghasilkan ethanol fuel grade. Platform termokimia secara umum meliputi dua tahapan utama, yaitu gasifikasi dan dilanjutkan dengan konversi gas yang dihasilkan menjadi etanol (Hamelinck et al., 2005). Secara sederhana proses koversi biomassa lignoselulosa dapat digambarkan seperti pada Gambar 5.
tinggi d
erpecah menjadi partikel yang lebih kecil dan terlepas dari selulosa (Taherzadeh, 2008).
Polimer lignin dapat dikonversi ke monomernya tanpa mengalami perubahan dalam bentuk dasarnya. Lignin pada umumnya tahan terhadap hidrolisis karena adanya ikatan eter dan ikatan karbon. Pada suhu
akan mengalami perubahan struktur dengan membentuk asam format, metanol, asam asetat, aseton, vanilin dan sebagainya, sedangkan bagian yang lainnya mengalami kondensasi (Brown, 1979).
ANOL
Gambar 5. Proses produksi etanol dari biomassa lignoselulosa (Hamelinck et
al., 2005)
Secara umum proses pembuatan bioetanol melalui tiga tahapan yaitu tahap persiapan bahan baku, tahap fermentasi dan tahap pemurnian. Pada
tahap persiapan ersi terlebih
dahulu menjadi larutan gula sebelum yang sudah dalam
Sherrington, 1992). Ferm sub
kegiatan katalis biokim jenis m
has
adalah fermentasi gula, baik yang berupa glukosa, sukrosa, maupun fruktosa oleh ragi (yeast
Pad
bioetano
etanol dengan m suh
stoikiom
Biomassa Pretreatment Hidrolisis Fermentasi Purifikasi
Pembangkit Tenaga
Limbah Padat Uap Panas
Etanol Limbah Cair
Energi Listrik
bahan baku yang berupa padatan harus dikonv
difermentasi menjadi etanol. Bahan baku bentuk larutan bisa langsung difermentasi (Gaman dan
entasi adalah suatu proses perubahan kimia pada strat organik, baik karbohidrat, protein, lemak atau lainnya melalui
ia yang dikenal sebagai enzim yang dihasilkan oleh ikroba spesifik (Prescott dan Dunn, 1959). Bioetanol diperoleh dari il fermentasi bahan yang mengandung gula. Tahap inti produksi bioetanol
) terutama Saccharomyces sp. atau bakteri Zymomonas mobilis. a proses ini gula akan dikonversi menjadi etanol dan gas karbondioksida.
Tahap fermentasi merupakan tahap kedua dalam proses produksi l. Pada tahap ini terjadi pemecahan gula-gula sederhana menjadi elibatkan enzim dan ragi. Fermentasi dilakukan pada kisaran u 27-32°C. Pada tahap ini akan dihasilkan gas CO2 dengan perbandingan etri yang sama dengan etanol yang dihasilkan yaitu 1 : 1. Setelah
melalui pro dal cer kar (M men ferm
diti ahan glukosa menjadi etanol dan aldehid yang perlu dibersihkan per etan (wa seh iasanya hanya mencapai 8 sampai 10% saja, sehingga untuk memperoleh etanol yang
nol 95% diperlukan proses lainnya, yaitu proses distilasi. Proses distilas
D.
menghasilkan gula sederhana. Hidrolisis meliputi proses pemecahan polisakarida di dalam biomassa lignoselulosa, yaitu selulosa dan hemiselulosa menjadi monomer gula penyusunnya. Hidrolisis sempurna selulosa menghasilkan glukosa, sedangkan hemiselulosa menghasilkan beberapa monomer gula pentosa (C5)
ses pemurnian, gas CO2 dapat digunakan sebagai bahan baku gas am pembuatan minuman berkarbonat (Prescott dan Dunn, 1959).
Produksi etanol dari substrat gula oleh khamir Saccharomyces
evisiae merupakan proses fermentasi dengan kinetika sangat sederhana
ena hanya melibatkan satu fase pertumbuhan dan produksi angunwidjaja, 1994). Pada fase tersebut glukosa diubah secara simultan
jadi biomasa, etanol dan CO2. Etanol yang dihasilkan dari proses entasi biasanya masih mengandung gas-gas antara lain CO2 yang mbulkan dari pengub
. Gas CO2 pada hasil fermentasi tersebut biasanya mencapai 35 sen volume, sehingga untuk memperoleh etanol yang berkualitas baik, ol tersebut harus dibersihkan dari gas tersebut. Proses pembersihan
shing) CO2 dilakukan dengan menyaring etanol yang terikat oleh CO2, ingga dapat diperoleh etanol yang bersih dari gas CO2.
Kadar etanol yang dihasilkan dari proses fermentasi, b
berkadar eta
i dilaksanakan melalui dua tingkat, yaitu tingkat pertama dengan beer
column dan tingkat kedua dengan rectifying column. Destilasi sederhana tidak
dapat dilakukan karena etanol-air erupakan campuran azeotrop yang susah disahkan karena mempunyai sifat yang menyerupai. Sehingga diperlukan teknik khusus, salah satu alternatifnya yaitu dengan menggunakan teknologi membran (Hamelinck et al., 2005).
HIDROLISIS ASAM
Hidrolisis adalah salah satu tahapan dalam pembuatan etanol berbahan baku limbah lignoselulosa. Hidrolisis bertujuan untuk
dan heksosa (C6). Secara umum teknik hidrolisis dibagi menjadi dua, yaitu hidrolisis berbasis asam dan hidrolisis dengan enzim.
Asam merupakan katalis yang tidak spesifik dan dapat menghidrolisis selulosa seperti halnya pati. Ikatan glikosidik pada selulosa bersifat rentan terhadap hidrolisis yang dikatalis oleh asam. Rendemen glukosa yang tinggi dapat dihasilkan dari hidrolisis asam jika dicapai kondisi yang optimum. Pada metode hidrolisis asam, biomassa lignoselulosa dipaparkan dengan asam pada suhu dan tekanan tertentu selama waktu tertentu. Hidrolisis menghasilkan monomer gula dari polimer selulosa dan hemiselulosa (Sun dan Cheng, 2002).
Beberapa asam yang umum digunakan untuk hidrolisis asam antara lain adalah asam sulfat (H2SO4), asam perklorat, dan HCl. Asam sulfat
Menurut Rohajatien (1989), hidrolis dengan menggunakan asam sulfat mampu
hidrolis
diperoleh kembali (recovery). Akan tetapi asam kuat bersifat korosif sehingga merupakan asam yang paling banyak dimanfaatkan untuk hidrolisis asam.
is
menghasilkan rendemen yang lebih besar dibandingkan dengan menggunakan asam jenis lain (HCl). Hidrolisis asam dapat dikelompokkan menjadi hidrolisis asam pekat dan hidrolisis asam encer (Taherzadeh dan Karimi, 2007). Menurut Grethlein (1978), hidrolisis asam dapat dilakukan dengan menggunakan asam pekat H2SO4 72% atau HCL 42% pada suhu ruang. Selain itu juga dapat dilakukan dengan larutan asam 1% pada suhu 100-120°C selama 3 jam atau lebih.
Hidrolisis asam pekat merupakan teknik yang sudah dikembangkan cukup lama. Braconnot di tahun 1819 pertama kali menemukan bahwa selulosa dapat dikonversi menjadi gula (Taherzadeh dan Karimi, 2007). Hidrolisis asam pekat menghasilkan gula yang tinggi (90% dari hasil teoritik) dibandingkan dengan hidrolisis asam encer, dan dengan demikian akan menghasilkan etanol yang lebih tinggi (Hamelinck et al., 2005). Kecepatan
is oleh asam pada konsentrasi tinggi tidak tergantung pada struktur kristal selulosa, sehingga lebih dari 90% glukosa dapat dihasilkan. Kosaric et
al. (1983) menambahkan bahwa hidrolisis selulosa dengan konsentrasi tinggi
jarang diterapkan secara komersial karena harga asam kuat cukup mahal. Hidrolisis asam konsentrasi tinggi akan lebih ekonomis jika asam dapat
memerlukan biaya tambahan untuk perawatan alat-alat produksi (Kosaric et
al., 1983). Hidrolisis menggunakan asam pekat akan mempercepat proses
hidrolis
t adalah (1) tahap yang m
empengaruhi proses degradasi selulosa menjadi glukosa dan juga memepengaruhi degradasi glukosa sebagai produk.
elebihi waktu optimum akan mendegradasi glukosa menjad
akan terbentuk produk samping berupa hidroksimetil furfural (HMF) akibat is tetapi akan menurunan hasil hidrolisis karena glukosa mudah sekali diuraikan (Hamelinck et al., 2005).
Hidrolisis asam encer juga dikenal dengan hidrolisis asam dua tahap (two stage acid hydrolysis) dan merupakan metode hidrolisis yang banyak dikembangkan dan diteliti saat ini. Hidrolisis asam encer pertama kali dipatenkan oleh H.K. Moore pada tahun 1919. Pada penggunaan asam encer proses hidrolisis akan berlangsung lambat karena adanya daya tahan dari kristal selulosa, tetapi dapat mengurangi penguraian glukosa oleh asam (Hamelinck et al., 2005).
Menurut Tsao et al. (1978), hidrolisis asam biasanya dilakukan dalam dua tahap untuk meminimumkan hasil samping yang tidak diinginkan. Purwadi (2006) menyebutkan bahwa kedua tahap tersebu
elibatkan asam encer, yaitu asam sulfat 1% pada 80-120°C selama 30-240 menit dan (2) tahap yang menggunakan asam lebih keras, yaitu 5 sampai 20% asam sulfat dan suhu yang lebih tinggi mendekati 180°C. Hasil hidrolisis yang ideal dapat diperoleh jika gula yang dihasilkan segera dipisahkan dari medium hidrolisisnya. Komponen terlarut yang utama pada hasil hidrolisis akhir adalah glukosa, xilosa, selobiosa, furfuraldehid, hidroksimetil furfural, dan asam-asam organik seperti asam format, asam levulinat, dan asam asetat (Grethlein, 1975).
Lama waktu hidrolisis m
Waktu hidrolisis yang m
i komponen-komponen yang lebih sederhana yang biasanya bersifat racun terhadap mikroorganisme (Tewari, 1988).
Penggunan konsentrasi asam yang semakin tinggi mengakibatkan gula pereduksi yang dihasilkan semakin berkurang. Hal ini disebabkan terjadinya penguraian monosakarida yang dihasilkan menjadi senyawa lain yang tidak diinginkan. Pada hidrolisis selulosa dengan asam untuk menghasilkan gula,
penguraian glukosa pada suasana asam. HMF ini akan terus bereaksi membentuk asam-asam organik seperti levulinat dan asam format pada suasana
dekstro
enyatakan komponen gula di dalam gula cair yang m
asam dan suhu tinggi. Menurut Taherzadeh dan Karimi (2007), beberapa senyawa inhibitor yang dapat terbentuk selama proses hidrolisis asam adalah furfural, 5-hidroksimetilfurfural, asam levulinik, asam asetat, asam format, asam uronat, asam 4-hidroksibenzoik, asam vanilik, vanillin, fenol, cinnamaldehid, formaldehida, dan beberapa senyawa lain.
Rohajatien (1989) melakukan penelitian tentang pengaruh konsentrasi asam dan waktu hidrolisis terhadap kandungan gula pereduksi, ekuivalen
sa dan total padatan kering gula sederhana yang dihasilkan dari hidrolisis pod kakao. Nilai konsentrasi asam sulfat dan asam klorida yang digunakan adalah 5, 10, dan 15%. Hidrolisis dilakukan selama 10, 20, 30, 40, dan 50 menit pada suhu 121°C. Hasil penelitian menunjukan bahwa rata-rata kadar gula pereduksi tertinggi dicapai pada hidrolisis dengan larutan HCl 15% selama 30 menit (1,83% (b/v)) dan hidrolisis dengan H2SO4 15% selama 10 menit (1,95% (b/v)).
Hidrolisis asam sepenuhnya terjadi secara acak dan sebagian gula yang dihasilkan merupakan gula perduksi sehingga pengukuran gula pereduksi tersebut dapat dijadikan alat pengontrol kualitas hasil (Tjokroadikoesoemo, 1986). Kadar gula pereduksi m
emiliki struktur aldehid atau hidroksil keton bebas seperti maltosa, laktosa, glukosa, dan lain-lain. Pengukuran gula pereduksi hidrolisat dilakukan dengan menggunakan metode DNS. Menurut Apriyantono et al. (1989), metode DNS tidak spesifik dan akan mengukur seluruh senyawa pereduksi. Jika glukosa digunakan sebagai standar, maka untuk menentukan selobiosa nilai yang diperoleh 15% lebih rendah dari yang sebenarnya, sedangkan untuk silosa 15% lebih tinggi. Konsentrasi gula fermentasi diperoleh dengan menjumlahkan kandungan glukosa, selobiosa dan silosa yang terdapat pada hidrolisat.
E.
m yang dihasilkan oleh mikroba spesifik (Presco
dibagi menjadi dua tipe yaitu fermentasi aerob dan anaerob
an bahwa suhu optimum untuk fermentasi antara 25-30 oC dan ka
ai substrat gula, tergantung spesies
FERMENTASI
Fermentasi adalah suatu proses perubahan kimia pada substrat organik, baik karbohidrat, protein, lemak, atau sejenisnya melalui kegiatan katalis biokimia yang dikenal sebagai enzi
tt dan Dunn, 1981). Secara biokimia, fermentasi juga dapat diartikan sebagai pembentukan energi melalui senyawa organik. Secara sederhana proses fermentasi alkohol dari bahan baku yang mengandung gula atau glukosa terlihat pada reaksi berikut :
C6 H12O6 Æ 2 C2H5OH + 2 CO2 + 2 ATP + 5 Kkal Proses fermentasi
. Fermentasi aerob akan menghasilkan asam laktat dan pada proses anaerob akan dihasilkan etanol. Fermentasi menurut jenis medianya dapat dibedakan menjadi dua, yaitu fermentasi media padat dan fermentasi media cair. Fermentasi media padat adalah fermentasi yang substratnya tidak larut dan tidak mengandung air bebas, tetapi cukup mengandung air untuk keperluan mikroba. Fermentasi media cair adalah proses fermentasi yang substratnya larut atau tersuspensi dalam media cair. Fermentasi media padat umumnya berlangsung pada media dengan kadar air berkisar antara 60-80% (Gaman dan Sherrington, 1992).
Fermentasi etanol memakan waktu 30-72 jam. Frazier dan Westhoff (1978) menambahk
dar gula antara 10-18%. Jika konsentrasi gula terlalu tinggi, aktivitas khamir dapat terhambat dan waktu fermentasi menjadi lebih lama serta tidak semua gula dapat terfermentasi (Paturau, 1969)
Mikroorganisme yang sering digunakan untuk proses fermentasi yaitu khamir. Khamir mampu mengkonsumsi berbag
yang digunakan. Secara umum, mikroorganisme ini dapat tumbuh dan memfermentasi gula menjadi etanol secara efisien pada suhu 28-35 oC. Walaupun laju awal produksi etanol meningkat pada suhu lebih tinggi, produktifitas keseluruhan menurun karena efek penghambatan etanol meningkat (Ratledge, 1991).
Faktor lingkungan seperti suhu, pH, kebutuhan nutrient dan kofaktor perlu diperhatikan dalam kehidupan khamir. Sejumlah kecil oksigen harus disediakan pada proses fermentasi oleh khamir karena oksigen merupakan komponen yang diperlukan dalam biosintesis beberapa asam lemak tidak jenuh. Untuk kebutuhan oksigen dalam proses fermentasi biasanya diberikan tekanan oksigen 0.05-0.10 mm Hg. Jika tekanan oksigen yang diberikan lebih besar dari dari nilai tersebut maka konversi akan cenderung ke pertum
arah
-6 dan 3-6. Perubahan pH dapat mempengaruhi pemben
Gambar 6. Kurva pertumbuhan kultur mikroba (Fardiaz, 1988)
buhan sel. Kebutuhan relatif nutrien sebanding dengan komponen utama sel khamir, yaitu mencakup karbon, oksigen, nitrogen dan hidrogen. Pada jumlah lebih rendah, fosfor, sulfur, potasium dan magnesium juga harus tersedia untuk sintesis komponen-komponen mineral. Beberapa mineral seperti Mn, Co, Cu dan Zn serta faktor pertumbuhan organik seperti asam amino, asam nukleat dan vitamin diperlukan dalam jumlah besar untuk pertumbuhan khamir (Oura, 1983).
Menurut Prescott dan Dunn (1959), pH pertumbuhan khamir yang baik antara pH 3.5
tukan hasil samping fermentasi. Pada pH tinggi maka konsentrasi gliserin akan naik dan juga berkorelasi positif antara pH dan pembentukan asam piruvat. Pada pH tinggi maka fase lag akan berkurang dan aktivitas fermentasi akan naik. Pertumbuhan mikroba di dalam suatu kultur mempunyai kurva seperti terlihat pada Gambar 6.
Fase Logaritmi Fase Statis Fase Kematian Fase Adaptas Jumlah Sel Hidup Waktu
Pada proses fermentasi terdapat dua parameter yang mengendalikan pertum
at menghalangi proses fermentasi lebih
lanjut, jika t scott dan
Dunn, 1981). Selama proses fermentasi akan timbul panas. Bila tidak dilakuk
a yang merupakan hasil aktivitas fermentasi sel kh
1. Gl
buhan dan metabolisme khamir, yaitu konsentrasi gula dan etanol. Secara kinetik glukosa berperan ganda, pada konsentrasi rendah (kurang dari 1 g/l) merupakan substrat pembatas, sedangkan pada konsentrasi tinggi (lebih dari 300 g/l) akan menjadi penghambat (Mangunwidjaja, 1994). Pada permulaan proses fermentasi, khamir memerlukan oksigen untuk pertumbuhannya. Setelah terjadi akumulasi CO2, reaksi berubah menjadi anaerob. Etanol yang terbentuk dap
kadar e anol tersebut mencapai 13-15% volume (Pre
an pendinginan, suhu akan terus meningkat dan akan menghambat proses fermentasi (Oura, 1983).
Faktor-faktor yang dapat mempengaruhi jumlah etanol yang dihasilkan dari fermentasi adalah mikroorganisme dan media yang digunakan, adanya komponen media yang dapat menghambat pertumbuhan serta kemampuan fermentasi mikroorganisme dan kondisi selama fermentasi (Astuty, 1991). Selain itu hal-hal yang perlu diperhatikan selama fermentasi adalah pemilihan khamir, konsentrasi gula, keasaman, ada tidaknya oksigen dan suhu dari perasan buah.
Etanol dihasilkan dari gul
amir. Etanol pada proses fermentasi alkoholik terbentuk melalui beberapa jalur metabolisme bergantung jenis mikroorganisme yang terlibat. Untuk Saccharomyces serta sejumlah khamir lainnya, etanol terbentuk melalui jalur Embden Meyerhof Parnas (EMP), reaksinya sebagai berikut (Rizani, 2000):
ukosa difosforilasi oleh ATP mula-mula menjadi D-glukosa-6 fosfat, kemudian mengalami isomerasi berubah menjadi D-frukstoda-6 fosfat dan difosforilasi lagi oleh ATP menjadi D-fruktosa-1, 6 difosfat.
2. D-fruktosa-1, 6 difosfat dipecah menjadi satu molekul D-gliseraldehid-3 fosfat dan satu molekul aseton fosfat.
3. Dihidroksi aseton fosfat disederhanakan menjadi L-gliserol-3 fosfat oleh NADH2.
4. AT
mentasi etanol meliputi dua tahap utama Fermen
P melepaskan satu molekul fosfat yang diterima oleh gliseraldehid-3 fosfat yang kemudian menjadi D-1, 3 difosfogliserat dan ADP.
5. D-1, 3 difosfogliserat melepaskan energi fosfat yang tinggi ke ADP untuk membentuk D-3 fosfogliserat dan ATP.
6. D-3 fosfogliserat berada dalam keseimbangan dengan D-2 fosfogliserat. 7. D-2 fosfogliserat membebaskam air untuk menghasilkan fosfoenol
piruvat.
8. ADP menggeser rantai fosfat yang kaya energi dari fosfoenolpiruvat untuk menghasilkan piruvat dan ATP.
9. Piruvat didekarboksilasi menghasilkan asetaldehid dan CO2.
10. Akhirnya asetaldehid menerima hidrohen dari NADH2 menghasilkan etanol.
Menurut Fardiaz (1992), fer
tasi diawali dengan pemecahan rantai karbon dari glukosa dan pelepasan paling sedikit dua pasang atom hidrogen melalui jalur EMP menghasilkan senyawa karbon lainnya yang lebih teroksidasi daripada glukosa. Senyawa yang teroksidasi tersebut direduksi kembali oleh atom hidrogen yang dilepaskan dalam tahap pertama, membentuk senyawa-senyawa hasil fermentasi yaitu etanol.