KOROSI ELEKTROKIMIAWI
(KOR)
Koordinator LabTK
Dr. Pramujo Widiatmoko
PROGRAM STUDI TEKNIK KIMIA
FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI BANDUNG
2016
KOR – 2016/PW 2
Kontributor:
Dr. Isdiriayani Nurdin, Dr. Hary Devianto, Dr. Ardiyan Harimawan, Robby Sukma Dharmawan, Jeffrey Pradipta W
KOR – 2016/PW i
DAFTAR ISI
DAFTAR ISI ... i
DAFTAR GAMBAR ... ii
DAFTAR TABEL ... iii
BAB I PENDAHULUAN ... 1
BAB II TUJUAN DAN SASARAN PERCOBAAN... 2
2.1. Tujuan Percobaan... 2
2.2. Sasaran Percobaan ... 2
BAB III RANCANGAN PERCOBAAN ... 3
3.1. Perangkat dan Alat Ukur ... 3
3.2. Bahan/Zat Kimia ... 3
3.3. Kondisi Percobaan ... 3
3.3.1. Variabel yang Dibuat Tetap ... 3
3.3.2. Variabel yang Divariasikan... 4
3.3.3. Variabel Terikat ... 4
3.4. Rangkaian Alat... 4
BAB IV PROSEDUR KERJA ... 5
4.1. Persiapan ... 5
4.4. Percobaan Inti ... 6
DAFTAR PUSTAKA ... 7
LAMPIRAN
LAMPIRAN A TABEL DATA MENTAH LAMPIRAN B PROSEDUR PERHITUNGAN LAMPIRAN C SPESIFIKASI LITERATUR
KOR – 2016/PW ii
DAFTAR GAMBAR
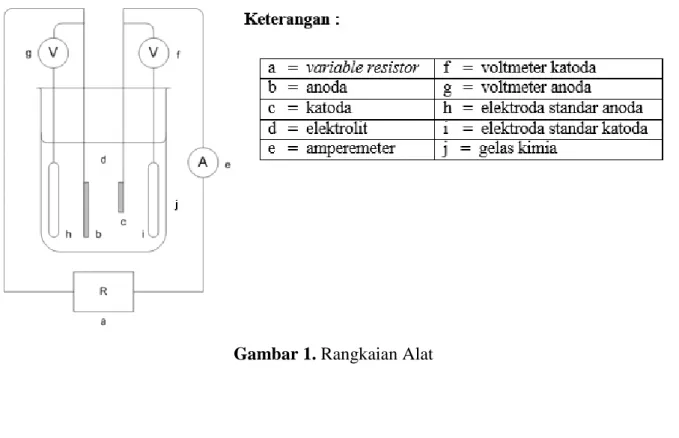
Gambar 1. Rangkaian Alat ... 4 Gambar 2. Diagram Alir Percobaan ... 6 Gambar 3. Hasil percobaan (a) Fe-Zn (b) Fe-Cr ... 10
KOR – 2016/PW iii
DAFTAR TABEL
Tabel 1. Tabel Data Pengamatan... 9 Tabel 2. Potensial Standar Beberapa Logam ... 11
KOR – 2016/PW 1
BAB I
PENDAHULUAN
Korosi merupakan peristiwa kerusakan material akibat interaksi dengan lingkungannya. Peristiwa korosi dapat terjadi pada peralatan industri yang terbuat dari logam dan terpapar berbagai lingkungan agresif. Korosi di pabrik kimia dapat menyebabkan kerugian yang besar, mulai dari kerusakan peralatan, proses produksi terhenti selama perbaikan peralatan yang terkorosi, kebocoran bahan baku/produk antara/produk akhir yang berpotensi bahaya bagi lingkungan maupun para pekerja pabrik yang bersangkutan. Oleh sebab itu, proses korosi perlu dipelajari agar dapat ditentukan cara yang tepat untuk mengendalikannya.
Secara alami, logam di lingkungan oksidatif cenderung teroksidasi. Kecenderungan tersebut dinyatakan sebagai potensial kesetimbangan standar reaksi reduksi/oksidasi kation-logam. Perbandingan kemudahan/kecenderungan teroksidasi/terkorosi berbagai logam dinyatakan dalam deret potensial standar (electromotive force, emf-series).
Ada beberapa metoda pengendalian korosi yang dapat diterapkan pada peralatan pabrik yang terbuat dari logam. Metoda pengendalian korosi yang menggunakan dasar ilmu elektrokimia adalah proteksi katodik, proteksi anodik dan penambahan inhibitor. Prinsip kerja proteksi katodik dan proteksi anodik adalah perubahan potensial logam untuk mengurangi laju korosi yang sebanding dengan arus listrik yang mengalir. Sedangkan penambahan inhibitor bertujuan untuk mengurangi luas permukaan aktif anoda ataupun katoda.
KOR – 2016/PW 2
BAB II
TUJUAN DAN SASARAN PERCOBAAN
2.1. Tujuan Percobaan
Praktikum ini dilakukan dengan tujuan untuk memahami proses korosi elektrokimiawi logam beserta metode pengendaliannya.
2.2. Sasaran Percobaan
Dari praktikum ini diharapkan dapat diidentifikasi:
1. Diagram potensial – arus (diagram Evans) dari pasangan elektroda tertentu dalam larutan tertentu, serta penentuan fungsi masing-masing logam sebagai katoda atau anoda
2. Proses pengendali korosi yang bersangkutan (kendali anodik, katodik, atau campuran) 3. Pengaruh variasi luas permukaan katoda atau anoda dan variasi konsentrasi elektrolit
KOR – 2016/PW 3
BAB III
RANCANGAN PERCOBAAN
3.1. Perangkat dan Alat Ukur
Perangkat dan alat ukur yang digunakan untuk melaksanakan percobaan ini adalah: a. Gelas kimia 500 mL
b. Elektroda pelat baja karbon, aluminium, tembaga, dan stainless steel masing-masing dengan luas permukaan 0,25 (0,5 x 0,5) cm2 dan 25 (5 x 5) cm2
c. Tahanan variabel 0 – 10 k d. Amperemeter
e. Voltmeter f. Kabel tembaga
g. Elektroda standar Cu/CuSO4 jenuh h. Labu Takar 1000 mL
i. Pipet ukur 5-10 mL (sesuai kebutuhan) j. Corong
3.2. Bahan/Zat Kimia
Berikut adalah bahan dan zat kimia yang diperlukan: a. H2SO4 Pekat 98% b. Padatan KOH/NaOH c. Aqua dm d. CuSO4 e. Isolator Tape 3.3. Kondisi Percobaan
Kondisi percobaan terdiri dari variabel percobaan yang dibuat tetap dan variabel percobaan yang diubah.
3.3.1. Variabel yang Dibuat Tetap
a. Tekanan udara ruang (660 – 700 mmHg) b. Temperatur ruang (23 – 28 oC)
KOR – 2016/PW 4
c. Volume elektrolit (250 mL) d. Jarak antar elektroda (1 cm) e. Jenis elektroda dan elektrolit
3.3.2. Variabel yang Divariasikan
a. Jenis dan konsentrasi elektrolit (larutan H2SO4 dan larutan NaOH dengan berbagai macam variasi konsentrasi)
b. Pasangan jenis elektroda (baja karbon, aluminium, tembaga, stainless steel) c. Perbandingan luas permukaan elektroda (luas anoda/luas katoda : 1/1, 1/25, 25/1)
3.3.3. Variabel Terikat
a. Arus
b. Beda potensial elektroda (katoda dan anoda)
3.4. Rangkaian Alat
Rangkaian alat yang digunakan dalam percobaan ini dapat dilihat pada Gambar 1. Rangkaian tersebut berupa rangkaian intensiostatik dengan variasi tahanan.
KOR – 2016/PW 5
BAB IV
PROSEDUR KERJA
Langkah kerja praktikum modul korosi elektrokimiawi terdiri dari dua langkah utama, yaitu : 1. Persiapan
a. Penyiapan Elektroda
b. Pembuatan Larutan Elektrolit c. Perangkaian Alat
2. Percobaan Inti
Meliputi pembuatan diagram Evans dan analisis.
4.1. Persiapan
a. Penyiapan Elektroda
Dua buah elektroda (sesuai dengan penugasan) beserta elektroda standar Cu dibersihkan dengan menggunakan kertas abrasif mulai dari grade terendah hingga 1200 CW di bawah alir mengalir. Kemudian elektroda tersebut dicuci dengan aqua dm dan dikeringkan sebelum digunakan dalam percobaan.
b. Pembuatan Larutan Elektrolit
Langkah pembuatan elektrolit bergantung pada jenis elektrolit yang digunakan (sesuai penugasan).
i. Larutan H2SO4
Larutan H2SO4 dibuat dengan mengambil sejumlah volume H2SO4 dengan menggunakan pipet ukur dan filler. Larutan tersebut kemudian dimasukkan ke dalam sejumlah air dalam gelas kimia 500 mL. Larutan H2SO4 dimasukkan ke dalam aqua dm secara perlahan. Kemudian masukkan larutan ke dalam labu takar dan tambahkan aqua dm hingga larutan mencapai tanda batas.
INGAT : Masukkan H2SO4 ke dalam air, bukan sebaliknya!
ii. Larutan KOH/NaOH
Padatan KOH/NaOH ditimbang sesuai dengan kebutuhan. Padatan tersebut kemudian dimasukkan ke dalam gelas kimia berisi sejumlah air. Larutan KOH dimasukkan ke dalam labu takar dan ditambah aquua dm hingga larutan mencapai tanda batas.
KOR – 2016/PW 6
c. Perangkaian Alat
Alat dirangkai seperti rangkaian alat yang diperlihatkan dalam Gambar 1.
4.4. Percobaan Inti
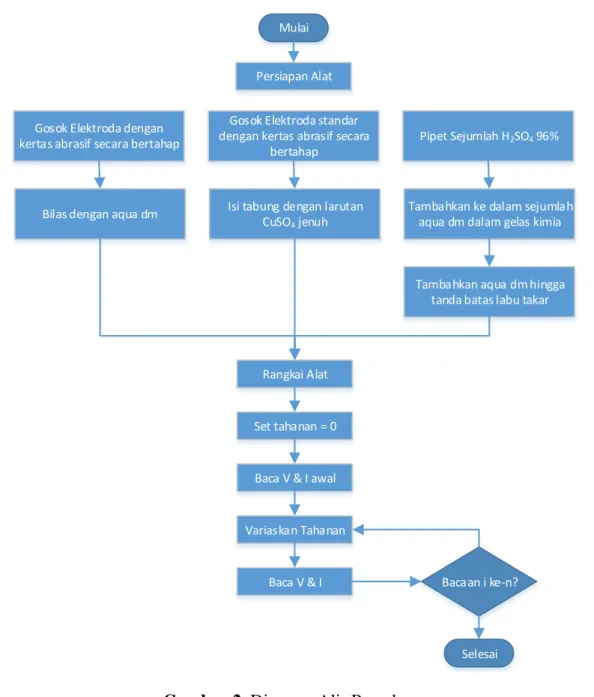
Catat tegangan sel dan arus listrik ketika tahanan variabel diset sama dengan nol. Setelah itu, arus dikecilkan dengan cara memperbesar tahanan variabel sedikit demi sedikit. Lakukan perubahan tahanan sel beberapa kali hingga arus tidak lagi terbaca oleh amperemeter. Catat arus dan tegangan sel setiap kali mengubah tahanan. Setelah itu, alurkan hasil percobaan sebagai diagram Evans. Diagram alir percobaan diperlihatkan pada Gambar 2.
Mulai
Persiapan Alat
Gosok Elektroda dengan kertas abrasif secara bertahap
Gosok Elektroda standar dengan kertas abrasif secara
bertahap
Pipet Sejumlah H2SO4 96%
Bilas dengan aqua dm Isi tabung dengan larutan CuSO4 jenuh
Tambahkan ke dalam sejumlah aqua dm dalam gelas kimia
Tambahkan aqua dm hingga tanda batas labu takar
Rangkai Alat
Set tahanan = 0
Baca V & I awal
Variaskan Tahanan
Baca V & I
Selesai Bacaan i ke-n?
KOR – 2016/PW 7
DAFTAR PUSTAKA
Jean Besson et Jacques Guitton, 1972, Manipulations d’electrochimie, introduction a la
theorie et a la pratique de la cinetique electrochimique, Paris: MASSON & CIE.
Jones, D.A., 1992, Principles and Prevention of CORROSION, Macmillan Publishing Company.
KOR – 2016/PW 8
KOR – 2016/PW 9
LAMPIRAN A
TABEL DATA MENTAH
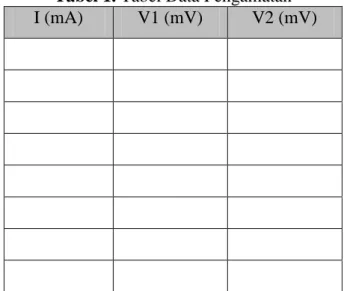
Contoh dari tabel pengamatan yang digunakan selama percobaan adalah sebagai berikut.
CONTOH
Run ke :
Elektroda 1 (luas) :
Elektroda 2 (luas) :
Jenis & Konsentrasi Elektrolit :
Tabel 1. Tabel Data Pengamatan
KOR – 2016/PW 10
LAMPIRAN B
PROSEDUR PERHITUNGAN
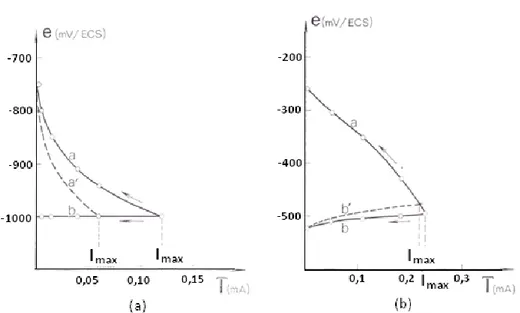
Gambar 6 menunjukkan diagram Evans yang diperoleh dari percobaan. Dalam kedua kasus dengan pasangan elektroda Fe-Zn dan Fe-Cr, korosi terkendali oleh reaksi katodik. Perhatikan bahwa pada kasus Fe – Cr, arus maksimum 0,23 mA terpusat pada anoda Fe seluas 0,03 cm2 sehingga menghasilkan korosi sumuran dalam yang mengkhawatirkan. Sebaliknya, dengan pasangan Fe – Zn, arus sebesar 0,12 mA terbagi pada anoda Zn seluas 25 cm2. Korosi yang terjadi pada pasangan elektroda ini adalah korosi merata. Oleh karena itu, pengurangan tebal elektroda akibat korosi berjalan sangat lambat.
Gambar 3. Hasil percobaan (a) Fe-Zn (b) Fe-Cr
Pada kondisi percobaan dengan penutupan 50% luas permukaan katodik ataupun anodik, terjadi perubahan laju korosi yang ditandai dengan turunnya arus. Hasilnya dapat dilihat pada Gambar 6 dengan garis putus-putus.
Dari diagram Evans hasil percobaan dapat diketahui: a. Tipe reaksi korosi : kendali katodik / kendali anodik
b. Logam yang berfungsi sebagai katoda dan yang berfungsi sebagai anoda
c. Laju korosi maksimum, dihitung dari ianodik max (= Imax/luas anoda) menggunakan rumus Faraday ( )
KOR – 2016/PW 11
LAMPIRAN C
SPESIFIKASI LITERATUR
C.1. Deret Potensial Standar
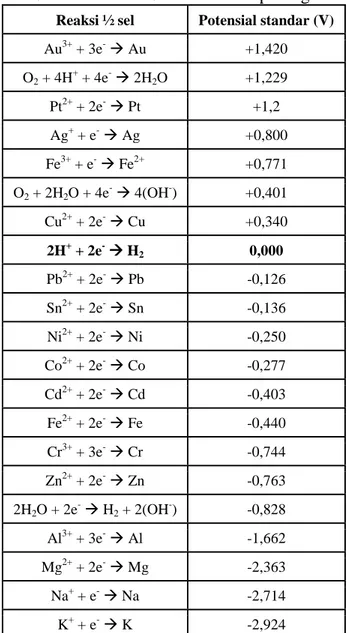
Tabel 2. Potensial Standar Beberapa Logam
Reaksi ½ sel Potensial standar (V)
Au3+ + 3e- Au +1,420 O2 + 4H+ + 4e- 2H2O +1,229 Pt2+ + 2e- Pt +1,2 Ag+ + e- Ag +0,800 Fe3+ + e- Fe2+ +0,771 O2 + 2H2O + 4e- 4(OH-) +0,401 Cu2+ + 2e- Cu +0,340 2H+ + 2e- H2 0,000 Pb2+ + 2e- Pb -0,126 Sn2+ + 2e- Sn -0,136 Ni2+ + 2e- Ni -0,250 Co2+ + 2e- Co -0,277 Cd2+ + 2e- Cd -0,403 Fe2+ + 2e- Fe -0,440 Cr3+ + 3e- Cr -0,744 Zn2+ + 2e- Zn -0,763 2H2O + 2e- H2 + 2(OH-) -0,828 Al3+ + 3e- Al -1,662 Mg2+ + 2e- Mg -2,363 Na+ + e- Na -2,714 K+ + e- K -2,924
C.2. Konduktivitas Elektrik Logam
KOR – 2016/PW 12
LAMPIRAN D
LEMBAR KENDALI KESELAMATAN KERJA
No Bahan Sifat Bahan Tindakan Penanggulangan
1 Asam sulfat (H2SO4) Sangat korosif Berbahaya apabila terhirup Berbahaya apabila kontak dengan kulit Apabila kontak dengan kulit akan menyebabkan luka bakar Dapat menyebabkan iritasi pernafasan Sangat beracun Berbahaya pada lingkungan akuatik Titikdidih 270°C
Wujud cairan tak berwarna Berat molekul 98,08 g/mol Bau : Berkarakter sedikit Kelarutan di dalam air : Larut, menimbulkan panas ( reaksi eksotermis )
Terhirup :
Segera berobat. Bilas dengan air secepatnya. Apabila sulit untuk bernafas segera beri oksigen. Jangan
menggunakan pernafasan dari mulut ke mulut.
Tertelan :
Tidak perlu dimuntahkan. Apabila korban dalam keadaan sadar berikan 2 – 4 gelas susu atau air. Segera bawa ke dokter.
Terkena Kulit :
Apabila terkena kulit atau rambut segera basuh dengan sabun dan air selama 15 menit. Kemudian cari pengobatan
Terkena mata :
Apabila terkena mata basuh dengan air mengalir kurang lebih selama 30 menit, jangan biarkan korban mengusap dan merapatkan mata.
Kerjakan di dalam lemari asam 2 Tembaga (II) Sulfat (CuSO4) Tidak berbau Menyebabkan iritasi kulit, mata, saluran pernafasan dan pencernaan, serta kerusakan organ-organ dalam Titikdidih 150°C Wujud padatan Berat molekul 249,69 g/mol
Jika terhirup, segera pergi ke ruang terbuka
Terkena mata: Periksa dan lepaskan jika ada lensa kontak. Dalam kasus kontak, segera basuh mata dengan air mengalir sekurang-kurangnya 15 menit. Air dingin dapat digunakan. Dapatkan perawatan medis.
Terkena Kulit: Dalam kasus kontak, segera siram kulit dengan banyak air. Tutup kulit yang teriritasi dengan suatu emolien.
KOR – 2016/PW 13
Bersihkan sepatu yang terkena bahan sebelum digunakan kembali.
Dapatkan perawatan medis.
3 Air Berat molekul
18,02 g/mol Titik didih 100°C Massa jenis 1 gr/cm3 Specific gravity : 1 pH : 7 Titikdidih : 100 o C Titikleleh : 0 oC Tidak terbakar Tidak berbau Tidakberwarna
Segera lap dengan kain kering jika bahan tumpah
Kecelakaan yang mungkin terjadi Penanggulangan
Praktikan tergelincir tumpahan bahan Tangani bahan-bahan dengan hati-hati khususnya untuk Asam sulfat (H2SO4), dan panggil pengurus laboratorium jika tidak mengerti untuk membersihkannya.
Perlengkapan keselamatan kerja
Sarung tangan Jaslab Masker Goggle
Prosedur Keselamatan Kerja
1. Pengecekan Alat dan Bahan
Pastikan alat berada dalam kondisi baik dan tidak rusak
Pastikan bahan-bahan yang diambil benar dan tertutup rapat 2. Percobaan
Pastikan rangkaian yang disusun sudah sesuai dengan percobaan
Segera lap jika bahan tumpah 3. Pasca Percobaan
Pastikan semua peralatan telah dimatikan dan kabel listrik dicabut
Pastikan meja dan lantai bersih dari tumpahan bahan