15 BAB III
METODE PENELITIAN A. Tempat dan Waktu
Penelitian dilakukan di Laboratorium Mirobiologi Universitas Semarang digunakan untuk pengaktifan stater, pembuatan larutan gula merah (gula tebu, kelapa, aren dan siwalan) dan pembuatan soygurt. Laboratorium Uji Indrawi Universitas Semarang digunakan untuk pengujian organoleptik kesukaan aroma soygurt dan Laboratorium Kimia CV. Chem-mix Pratama, Bantul digunakan untuk pengujian total gula, total gula reduksi dan total asam asetat. Penelitian dilakukan pada bulan Januari 2019 sampai dengan Febuari 2019
B. Bahan dan Alat
Bahan dan peralatan yang digunakan untuk pembuatan soygurt adalah susu nabati kedelai dimana kedelainya didapatkan dari Desa Nambuhan, Kabupaten Grobogan, Jawa Tengah, yogurt plain (starter yogurt komersial) yang berisi bakteri Lactobacillus bulgaricus dan Streptococcus thermophilus, susu bubuk skim dan gula merah ( gula tebu, gula kelapa, gula aren dan gula siwalan).
Alat yang digunakan untuk pembuatan soygurt yaitu Waterbath merk memert, panci stainless steel, kompor, kotak plastik berpenutup, cup, sendok pengaduk, saringan, beker gelas, timbangan analitik, thermometer dan inkubator.
Bahan dan peralatan untuk pengujian total gula terdiri dari HCl 25%. NaOH 50%, Indikator Phenolphthalein (PP), aquades, larutan luff, larutan KI 30%, larutan Tiosulfat 0,1%, indicator kanji, spektrofotometer, labu takar 100 ml, Erlenmeyer 500 ml, dan pipet volume. Bahan dan peralatan untuk penentuan total
asam (asetat) antara lain larutan NaOH 0,1%, indicator fenolftalein (pp) 1%, dan peralatan titrasi. Bahan dan peralatan untuk penentuan kadar gula reduksi terdiri dari larutan glukosa standard, reagensia nelson, neraca analitik, pipet ukur 1 ml dan 10 ml, beaker glass 500 ml, Erlenmeyer, tabung reaksi, propipet, labu takar 100 ml, waterbath, penjepit, vortex, dan spektrofotometer. Bahan dan peralatan untuk penentuan kesukaan aroma yoghurt terdiri dari kertas kuisioner dan alat tulis.
C. Rancangan Percobaan
Rancangan percobaan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) satu faktor dan diulang sebanyak 4 kali. Adapun kode perlakuan adalah sebagai berikut:
P1 = Kontrol (tanpa penambahan gula merah) P2 = Penambahan Gula siwalan
P3 = Penambahan Gula kelapa P4 = Penambahan Gula aren P5 = Penambahan Gula tebu Variabel yang diamati meliputi: 1. Total gula (Somogyi, 1952)
2. Total gula reduksi (metode nelson-somogyi; Sudarmadji, 1952) 3. Total asam titrasin (Total Asam Asetat) (Legowo, 2005)
D. Prosedur Penelitian
1. Prosedur Pembuatan Subkultur Stater
Pembuatan subkultur stater untuk mengaktifkan BAL (Bakteri Asam Laktat) yang ada didalam stater komersial (yogurt plain) menurut Cahyanti (2008) dengan modifikasi adalah sebagai berikut :
a. Susu bubuk skim 9 g ditambahkan kedalam susu kedelai sampai 100 ml. b. Larutan susu skim 100 ml dicampur dengan stater (yogurt plain) 100 ml
perbandingan (1 : 1), kemudian dihomogenkan hingga rata.
c. Diinkubasi pada suhu 37 0C, selama 24 jam sehingga menjadi subkultur aktif yaitu jumlah BAL mencapai 106 CFU/ml.
Diagram alir pembuatan subkultur starter dapat dilihat pada Gambar 1: Larutan susu skim
(9 g susu skim ditambahkan susu kedelai sampai 100 ml)
Gambar 1. Diagram alir pembuatan subkultur starter (Cahyanti, 2008: dengan modifikasi)
2. Prosedur Pembuatan Susu Kedelai
Proses pembuatan susu kedelai dilakukan dengan beberapa tahap menurut (Nizori, A., dkk. 2007) dengan modifikasi yaitu sebagai berikut:
homogenisasi (1 : 1)
Inkubasi (T:37o C, t:24 Jam) Starter Yogurt Plain
(100 ml)
Subkultur (200 ml)
1. Kacang kedelai varietas Malabar dengan kualitas baik direndam dengan menggunakan 8000 ml air selama 12 jam.
2. Kacang kedelai yang telah direndam, dilakukan perebusan selama 15 menit dalam air mendidih sebanyak 16.000 ml.
3. Setelah perebusan, kacang kedelai dicuci untuk memisahkan kedelai dengan kotoran dan kulit ari.
4. Kacang kedelai yang telah bersih, kemudian dihancurkan menggunakan blender selama 5 menit dengan penambahan aquades 1:1.
5. Setelah proses penghancuran,kemudian dilakukan penyaringan sebanyak dua kali menggunakan saringan biasa dan kain mori untuk memisahkan sari kedelai dengan ampas.
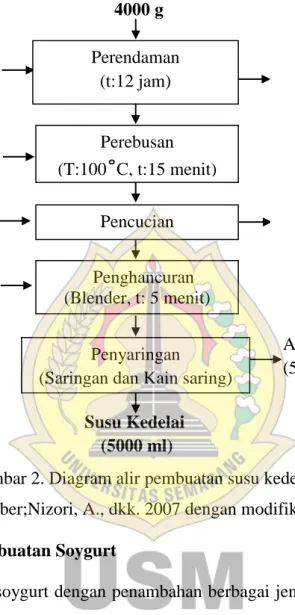
Diagaram alir pembuatan susu kedelai dapat dilihat pada gambar 2.
Gambar 2. Diagram alir pembuatan susu kedelai (Sumber;Nizori, A., dkk. 2007 dengan modifikasi) 3. Prosedur Pembuatan Soygurt
Pembuatan soygurt dengan penambahan berbagai jenis gula merah (gula siwalan, gula kelapa, gula aren, gula tebu) menurut (Susilorini dan Sawitri, 2008) dengan modifikasi yaitu sebagai berikut:
a. Susu kedelai masing-masing 1000 ml dimasukkan kedalam 5 gelas ukur . b. Dimasukkan masing-masing 50 gram gula, gula kelapa, gula aren dan gula
tebu pada 4 gelas ukur yang berisi 1000 ml susu kedela, kecuali P1 karena sebagai kontrol. Air 4000 ml Air mengalir Ampas kedelai (500 g) Perendaman (t:12 jam) Pencucian Perebusan (T:100˚C, t:15 menit) Penghancuran (Blender, t: 5 menit) Penyaringan
(Saringan dan Kain saring) Susu Kedelai
(5000 ml)
Air Kotor, Kulit ari Air 8000 ml
Kedelai jenis malabar 4000 g
Aquades 1:1 Air 16000 ml
Air rendaman
c. Susu kedelai di pasteurisasi pada suhu 80˚C selama 15 menit dalam waterbath.
d. Susu kedelai dilakukan tempering hinga mencapai 40˚C.
e. Masukkan 50 ml subkultur dari yogurt plain yang telah diaktifkan dan 125 gram susu skim kedalam susu yang sudah di pasteurisasi lalu dihomogenkan.
f. Masukkan kedalam cup plastik berpenutup yang sudah diberi label sesuai perlakuan dan ulangan.
g. Fermentasi pada inkubator pada suhu 40˚C selama 24 jam.
h. Dilakukan uji kadar total gula, total gula reduksi, total asam asetat, dan kesukaan aroma soygurt.
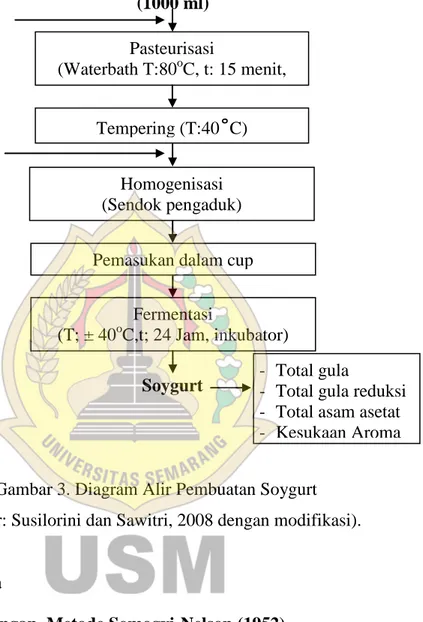
Diagram alir pembuatan Soygurt dapat dilihat pada Gambar 3. Susu Kedelai
(1000 ml)
(sumber: Susilorini dan Sawitri, 2008 dengan modifikasi).
E. Prosedur Analisa
1. Total Gula dengan Metode Somogyi-Nelson (1952)
Terhadap 1 ml sampel filtrat hasil fermentasi ditambah 1 ml reagen Nelson C, kemudian dipanaskan selama 20 menit pada suhu 100oC. selanjutnya didinginkan dan ditambah 1 ml reagen Arsenomolibdat, dikocok dan diencerkan dengan air destilasi hingga volumenya menjadi 10 ml. Absorbansinya dibaca dengan spektrofotometer dengan panjang Susu skim
(125 g), Subkultur (50 ml)
Gambar 3. Diagram Alir Pembuatan Soygurt Homogenisasi (Sendok pengaduk) Pasteurisasi (Waterbath T:80oC, t: 15 menit, waterbath) Tempering (T:40˚C) Gula siwalan,gula kelapa,gula aren, gula tebu (50 g)
Pemasukan dalam cup
Fermentasi
(T; ± 40oC,t; 24 Jam, inkubator)
Soygurt - Total gula - Total gula reduksi - Total asam asetat - Kesukaan Aroma
gelombang 520 nm, sebagai blanko digunakan air destilasi pengganti sampel.
Pembuatan reagen dalam analisis gula dengan metode Somogyi-Nelson
a. Reagen Nelson A
Reagen Nelson A terdiri dari Na2CO3. Anhidrat 12,5 gr, KNa. Tartrat 12,5 gr, NaHCO3 10 gr dan Na2SO4 100 gr dilarutkan dalam aquadest hingga tepat 500ml.
b. Reagen Nelson B
Pereaksi ini terdiri dari CuSO4.5 H2O sebanyak 15 gr dilarutkan dalam 100 ml air demineral dan ditambahkan 1-2 tetes H2SO4 pekat.
c. Larutan stoc C
Larutan stoc C dibuat dengan A : B dengan perbandingan 25 : 1 (dibuat pada saat akan digunakan).
d. Larutan arsenomolibdat
Pereaksi arsenomolibdat dibuat dengan cara (NH4)2MoO4 25 gr, H2SO4 pekat 21 ml dan aquadest 400 ml dicampur dengan (Na2HAsO4. 7H2O) yang dilarutkan dalam 25 ml air. Kemudian diaduk dan diinkubasi pada 37oC selama 24 – 28 jam, dan disimpan dalam botol coklat dan didalam lemari pendingin.
e. Larutan stok glukosa standard.
Glukosa standard 1% dalam (W/v) dalam asam benzoate jenuh diencerkan sehingga diperoleh larutan glukosa standard dengan
kosentrasi masing – masing 50, 150 dan 300 µg/ml.
f. Larutan xylose standar dibuat dengan kosentrasi 1000 µM dan untuk deret Standar dibuat melalui pengenceran sehingga diperoleh 100, 200, 300, 400 dan 500 µM.
Perhitungan total gula sebagai berikut:
1. Total Asam Laktat (Hadiwiyoto, 1994)
2. Total Gula Reduksi menurut Nelson-Somogyi (Sudarmadji, 1984) Prinsip analisis kadar gula reduksi dengan metode Nelson-Somogyi
adalahgula reduksi akan mereduksi kuprioksida menjadi
kuprooksida.Kuprooksida yang terbentuk direaksikan dengan
arsenomolibdat sehingga terbentuk molibdenum yang berwarna biru. Metode ini dapat digunakan untuk mengukur kadar gula reduksi dengan menggunakan pereaksi tembaga arseno molibdat. Kupri mula – mula direduksi menjadi bentuk kupro dengan pemanasan larutan gula.kupro yang terbentuk selanjutnya dilarutkan dengan arseno molibdat menjadi molibdenum berwarna biru yang menunjukkan ukuran konsentrasi gula dan membandingkannya dengan larutan standar sehingga konsentrasi gula dalam sampel dapat ditentukan.Reaksi warna yang terbentuk dapat menentukan konsentrasi gula dalam sampel dengan mengukur absorbansinya (Sudarmadji, 1984).Prosedur pengukuran adalah sebagai berikut:
Penyiapan Kurva Standar :
Total Gula = Bobot sakar (mg) x Fp x 0.95 x 100 % Bobot contoh (mg)
a. Membuat larutan glukosa standar (10 mg glukose anhidrat/100ml). b. Dari larutan glukosa standar tersebut dilakukan 6 pengenceran
sehingga diperoleh larutan glukosa dengan konsentrasi : 2,4,6,8, 10 mg/100ml.
c. Menyiapkan 7 tabung reaksi yang bersih, masing – masing diisi dengan 1 ml larutan glukosa standar tesebut diatas. Satu tabung diisi 1 ml air suling sebagai blanko.
d. Menambahkan ke dalam masing – masing tabung diatas 1 ml reagensia Nelson, dan panaskan semua tabung pada penangas air mendidih selama 20 menit.
e. Mengambil semua tabung dan segera mendinginkan bersama – sama dalam gelas piala yang berisi air dingin sehingga suhu tabung mencapai 25°C.
f. Setelah dingin, menambahkan 1 ml reagensia Arsenomolibdat, gojog sampai semua endapan Cu2O yang ada larut kembali.
g. Setelah semua endapan Cu2O larut sempurna, menambahkan 7 ml air suling, gojog sampai homogen.
h. Menera “Optical Density” (OD) masing – masing larutan tersebut pada panjang gelombang 540 nm.
i. Membuat kurva standar yang menunjukkan hubungan antara konsentrasi glukosa dan OD.
a. Menyiapkan larutan sampel yang mempunyai kadar gula reduksi 2 – 8 mg/ 100 ml. Perlu diperhatikan, bahwa larutan sampel ini harus jernih, karena itu bila dijumpai larutan sampel yang keruh atau berwarna maka perlu dilakukan penjernihan terlebih dahulu dengan menggunakan Pb-asetat atau bubur Alumunium hidroksida
b. Memipet 1 ml larutan sampel yang jernih tersebut ke dalam tabung reaksi yang bersih.
c. Menambahkan 1 ml reagensia Nelson, dan selanjutnya diperlakukan seperti pada penyiapan kurva standar diatas.
d. Jumlah gula reduksi dapat ditentukan berdasarkan OD larutan sampel dan kurva standar larutan glukosa.
Perhitungan gula reduksi sebagai berikut :
3. Total Asam Asetat (Legowo, 2005)
Kadar total asam asetat ditentukan dengan cara titrasi (Legowo, 2005) menggunakan NaOH 0,1 N dan indikator fenolptalein. Larutan NaOH sangat bersifat higroskopis, sehingga larutan dibuat sesaat sebelum titrasi, dan dikalibrasi terlebih dahulu dengan cara titrasi menggunakan larutan standar primer asam oksalat 0,1 N.Total asam asetat yogurt diukur dengan metode titrasi asam-basa. Prosedur pengukuran adalah sebagai berikut:
a. Ditimbang 10-15 g contoh dan ditambahkan 200 ml air suling panas sambil diaduk-aduk, kemudian didinginkan sampai suhu kamar.
b. Larutan contoh dimasukkan kedalam labu ukur 250 ml, dihimpitkan sampai tanda tera, kemudian dikocok dan disaring.
c. 100 ml filtrat dipipet dan dimasukkan kedalam Erlenmeyer 250 ml, dan diberi 1-3 tetes indikator PP 0,1%.
d. Dititrasi dengan larutan NaOH 0,1N sampai titik akhir.
e. Bila pada waktu penambahan alkali terbentuk warna kecoklatan yang akan mengganggu titik akhir, ditambahkan air panas dan indikator lebih banyak dari yang seharusnya.
f. Dicatat volume larutan NaOH 0,1N yang digunakan untuk titrasi. g. Dihitung % keasaman (dihitung sebagai asam asetat) dengan rumus:
Keterangan:
V1 = volume larutan NaOH 0,1 N yang digunakan untuk titrasi (ml) N = normalitas larutan NaOH 0,1 N
B = bobot setara asam asetat = 60,052 mg/ mmol V2 = volume sampel (ml)
4. Kesukaan Aroma (Rahayu, 2001)
Uji organoleptik ditentukan menggunakan metode pengujian hedonik (Rahayu, 2001).Pengujian organoleptik (aroma) soygurt dengan berbagai gula merah yang digunakan menggunakan skala numerik untuk menilai sifat produk yang disajikan menggunakan metode uji hedonik. Pengujian
dilakukan dengan cara 20 panelis yang semi-terlatih diberi kertas kuisioner dan mencium aroma soygurt. Skala numerik dan hedonik meliputi : 1= Amat sangat tidak suka, 2 = sangat tidak suka, 3= tidak suka, 4= netral, 5= suka, 6= sangat suka, 7= amat sangat suka. Penilaian kesukaan aroma soygurt dapat dilihat pada Tabel 4.
Tabel 4. Skala kesukaan aroma soygurt
Skala Numerik Skala Hedonik
7 Amat Sangat Suka
6 Sangat Suka
5 Suka
4 Netral
3 Tidak Suka
2 Sangat Tidak Suka
1 Amat Sangat Tidak Suka
Pengujian hedonik dilakukan pada kondisi ruangan yang bersih, sirkulasi udara yang baik, tempat dan peralatan yang sama, sehingga persepsi terhadap produk yang diuji adalah sama. Panelis memberikan penilaian pada kuesioner yang telah disediakan.Kuisioner yang digunakan untuk uji kesukaan aroma.
5. Analisis Data
Model linier yang menyatakan nilai hasil pengamatan sesuai rancangan percobaan yang digunakan adalah:
Yij = µ + i + ij Keterangan : i : 1,2,3,4,5 j : 1,2,3,4
µ : nilai tengah umum i : pengaruh perlakuan ke-i
ij : pengaruh acak pada perlakuan ke-i dan ulangan ke-j.
Hipotesis penelitian yang diuji adalah H0: µ1=µ2=µ3=µ4=µ5=µ, yang berarti perbedaan jenis gula merah tidak mengakibatkan perbedaan rata-rata populasi total gula, total gula reduksi, total asam asetat, dan tingkat kesukaan aroma pada soygurt.Sedangkan hipotesis alternatef penelitian yang diuji adalah H1: µ1≠µ2≠µ3≠µ4≠µ5≠µ, yang berarti paling sedikit ada satu nilai µ yang berbeda satu dengan yang lain, yang berarti perbedaan berbagai gula merah mengakibatkan perbedaan rata-rata populasi total gula, total gula reduksi, total asam asetat, tingkat kesukaan aroma pada soygurt.
Data yang diperoleh dianalisis statistik menggunakan sidik ragam.Apabila terdapat perbedaan antar perlakuan, yang berarti ada pengaruh perlakuan jenis gula merah terhadap hasil pengamatan pada taraf signifikasi 5%, maka dilanjutkan dengan uji Dunnet untuk mengetahui tingkat perbedaan antar perlakuan terhadap kontrol. Data dianalisis menggunakan program SPSS Statistik Versi 23.