PENETAPAN KADAR DAIDZEIN DALAM WOUND HEALING PATCH DENGAN METODE REVERSE PHASE HIGH PERFORMANCE LIQUID
CHROMATOGRAPHY
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Maria Euphrasia Yolanda Mane NIM : 148114161
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENETAPAN KADAR DAIDZEIN DALAM WOUND HEALING PATCH DENGAN METODE REVERSE PHASE HIGH PERFORMANCE LIQUID
CHROMATOGRAPHY
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Maria Euphrasia Yolanda Mane NIM : 148114161
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi PRAKATA
Puji syukur penulis haturkan kepada Tuhan atas segala berkat dan penyertaan-Nya sehingga skripsi yang berjudul “Penetapan Kadar Daidzein dalam
Wound Healing Patch dengan Metode Reverse Phase High Performance Liquid
Chromatography” yang disusun untuk memenuhi persyaratan dalam memperoleh gelar Sarjana Strata Satu Program Studi Farmasi (S. Farm.) dapat diselesaikan dengan baik. Skripsi ini merupakan bagian dari penelitian Dr. Sri Hartati Yuliani, Apt. Yang berjudul “Pengembangan Sediaan Penyembuh Luka bagi Penderita Diabetes dengan Bahan Aktif Ekstrak Tempe” berdasarkan SK No: 020d/LPPM USD/ IV/ 2017. Penulis menyadari banyak pihak yang telah berperan dan berkontribusi dalam proses pembuatan skripsi ini dari awal hingga akhir, maka dengan rasa syukur penulis mengucapkan terimakasih kepada:
1. Ibu Aris Widayati, M.Si., Ph.D., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Bapak Florentinus Dika Octa Riswanto, M.Sc. selaku Dosen Pembimbing Utama yang telah sabar membimbing dan memotivasi dalam proses penyusunan skripsi.
3. Ibu Dr. Sri Hartati Yuliani, M.Si., Apt. dan Ibu Dr. Christine Patramurti, M.Si., Apt. selaku Dosen Penguji atas arahan, kritik, dan saran yang telah diberikan kepada penulis
4. Michael Rahardja Gani, M.Farm, Apt. Selaku dosen pendamping laboratorium atas motivasi dan saran dalam proses pembuatan skripsi. 5. Dr. Dewi Setyaningsih, M.Sc, Apt. selaku Kepala Penanggung Jawab
Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam penggunaan fasilitas laboratorium untuk kepentingan penelitian ini.
6. Mas Bimo , Mas Agung, Pak Wagiran, Mas Purwanto dan Mas Kethul selaku laboran dan karyawan Laboratorium Fakultas Farmasi yang telah banyak membantu penulis pada masa penelitian.
7. Bapak Fransiskus Mane dan mama Yustina Theresia Rona, dan adik Antonia Paulina Bao atas segala semangat, doa, kasih, dan pengorbanannya
vii
dalam membantu menyelesaikan skripsi ini.
8. Teman-teman seperjuangan skripsi Leona Wong dan Gloria Elan Deovita, serta Sary, Tinni, dan Nita atas segala kerjasama dan kebersamaan selama penyusunan skripsi ini dari awal hingga akhir.
9. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari masih terdapat banyak kekurangan dalam skripsi ini, namun begitu diharapkan hasil skripsi ini dapat bermanfaat bagi semua pihak terutama di bidang ilmu farmasi.
Yogyakarta, 12 Januari 2018 Penulis
viii DAFTAR ISI
Halaman Sampul ... i
Halaman Persetujuan Pembimbing ... ii
Halaman Pengesahan ... iii
PERNYATAAN KEASLIAN KARYA ... iiiv
PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... ix DAFTAR GAMBAR ... x ABSTRAK ... xii ABSTRACT ... xiii PENDAHULUAN... 1 METODE PENELITIAN ... 2
HASIL DAN PEMBAHASAN ... 5
KESIMPULAN DAN SARAN ... 10
UCAPAN TERIMA KASIH ... 10
DAFTAR PUSTAKA ... 11
LAMPIRAN ... 13
ix
DAFTAR TABEL
Tabel I. Data pengukuran keseragaman bobot patch ... 6 Tabel II. Data pengukuran kurva baku daidzein ... 8 Tabel III. Data pengukuran kadar daidzein dalam sampel ... 9
x
DAFTAR GAMBAR
xi
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis daidzein ... 13
Lampiran 2. Data penimbangan bobot sampel wound healing patch ... 14
Lampiran 3. Kromatogram patch tanpa ekstrak tempe ... 15
Lampiran 4. Kromatogram baku daidzein ... 16
Lampiran 5. Kromatogram sampel ... 17
Lampiran 6. Perhitungan kadar daidzein dalam wound healing patch ... 22
xii ABSTRAK
Daidzein merupakan bentuk aglikon dari isoflavon yang banyak terdapat dalam tempe dan dapat berfungsi sebagai penyembuh luka. Daidzein dapat diperoleh dari ekstrak etanol tempe. Ekstrak etanol tempe dapat dibuat dalam sediaan patch sebagai matriks pembawa untuk mendukung pemanfaatannya sebagai penyembuh luka. Untuk menjamin khasiat, mutu dan keamanan maka perlu dilakukan penetapan kadar daidzein dalam wound healing patch dengan metode yang telah teroptimasi dan tervalidasi.
Penelitian ini bertujuan untuk menetapkan kadar senyawa daidzein dalam
wound healing patch ekstrak tempe, sehingga mendukung pemanfaatannya dalam
bidang kesehatan. Dengan demikian penelitian ini juga turut memberikan informasi terkait kandungan senyawa daidzein yang mampu terekstraksi dan terukur kadarnya dengan metode ini. Daidzein dianalisis dengan metode Reverse Phase High
Performance Liquid Chromatography (HPLC) dengan fase diam berupa kolom C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm) dan fase gerak campuran metanol dan akuabidestilata 70:30 v/v dengan kecepatan alir 0,8 mL/menit menggunakan detektor UV pada panjang gelombang 248 nm.
Kadar daidzein dalam wound healing patch ekstrak tempe yang diambil dari sepuluh sampel dinyatakan sebanyak 1,3109 ± 0,0509 (%b/b) dengan simpangan baku relatif sebesar 3,8809%.
Kata kunci: daidzein, penetapan kadar, reverse phase HPLC, wound healing
xiii ABSTRACT
Daidzein, an aglycone form of isoflavone widely presented in tempeh, has a benefit as wound healing agent. Daidzein can be obtained from the ethanol extract of tempeh. Ethanol extract of tempeh can be prepared in a patch as a carrier matrix to support its benefit as a wound healing agent. Since it was important to ensure its efficacy, quality and safety, it was necessary to determine daidzein levels in wound healing patch using an optimized and validated method.
This study aimed to determine concentration of daidzein in the wound healing patch, to support its benefit in health. This study also provides information related to the content of daidzein compounds that can be extracted and measured with this method. Daidzein was analyzed using Reverse Phase High Performance Liquid Chromatography (HPLC) method with the stationary phase of C18 type Luna Phenomenex® (dimension 250 x 4.6 mm, 5 μm particle size) and mobile phase of methanol : redistilled water 70:30 v/v with a flow rate 0.8 mL/min using a UV detector at wavelength 248 nm.
Concentration of daidzein in ten samples wound healing patch were 1,3109 ± 0,0509 (%w/w) with the RSD value of 3,8809%.
Key words : content determination, daidzein, reverse phase HPLC, wound healing patch.
1 PENDAHULUAN
Kedelai (Glycine max L.) sudah dikonsumsi mulai dari ribuan tahun yang lalu dan merupakan salah satu sumber protein penting di negara-negara Asia (Luthria et al. 2007). Kedelai memiliki berbagai komponen fungsional seperti karbohidrat, asam amino, dan isoflavonoid (Yang et al. 2010). Konsumsi kedelai tahunan secara global telah meningkat 114-170 juta ton selama dekade terakhir (Luthria et al. 2007).
Produk olahan kedelai contohnya tempe banyak dikonsumsi di negara-negara Asia terutama di Indonesia (Yang et al. 2010). Tempe dihasilkan melalui proses fermentasi kedelai oleh jamur Rhizopus (Astuti 2000). Dengan adanya fermentasi, dapat meningkatkan jumlah isoflavon aglikon salah satunya senyawa daidzein (Bavia et al. 2012).
Daidzein merupakan salah satu dari tiga isoflavon dominan yang ditemukan pada kedelai (Rostagno et al. 2009) dan dapat dimanfaatkan sebagai antikanker (He and Chen 2013) mengobati penyakit kardiovaskular, osteoporosis (Wong et al. 2008) serta sebagai antioksidan dan antiinflamasi (Yu et al. 2016). Selain itu, daidzein juga memiliki manfaat sebagai wound healing dengan meningkatkan ketebalan lapisan kolagen luka pada tikus betina (Uyar et al. 2014) dan penebalan lapisan epidermis pada wanita yang telah menopause jika dikonsumsi selama 6 bulan (Accorsi-Neto et al. 2009).
Seiring dengan kemajuan teknologi formulasi sediaan farmasi, maka dikembangkan sediaan wound healing patch (Gani 2013) yang berasal dari selulosa bakteri. Selulosa bakteri merupakan media yang dapat digunakan sebagai penutup luka (Mohite et al. 2014). Dengan penambahan ekstrak tempe, selulosa bakteri dapat dimanfaatkan sebagai penyembuh luka. Oleh karena itu sediaan wound
healing patch oleh Gani (2013) dimodifikasi dengan penambahan ekstrak etanol
tempe (Yuliani et al. 2016).
Penelitian ini bertujuan untuk mengetahui kadar daidzein dalam wound
healing patch ekstrak tempe menggunakan metode reverse phase HPLC yang telah
dioptimasi dan divalidasi serta mendukung pemanfaatannya dalam bidang kesehatan salah satunya sebagai penyembuh luka (Uyar et al. 2014). Pemilihan
2
metode ini karena dapat memisahkan campuran senyawa sehingga sekaligus mengidentifikasi, mengukur dan memurnikan masing-masing komponen campuran (Boligon and Linde 2014). Selain itu juga analisis menggunakan reverse phase HPLC dengan detektor UV, dapat sekaligus mendeteksi beberapa senyawa yang terbaca di panjang gelombang tersebut, sehingga analisis dapat dilakukan simultan serta hanya menggunakan volume sedikit untuk menganalisa, karena memiliki sensitivitas yang tinggi (Siddiqui 2017).
Penetapan kadar senyawa daidzein setelah optimasi dan validasi penting dilakukan untuk mendukung pemanfaatan wound healing patch ekstrak tempe dalam bidang kesehatan sebagai kontrol kualitas sediaan.
METODE PENELITIAN Alat dan bahan penelitian
Alat yang digunakan dalam penelitian ini adalah HPLC dengan detektor ultraviolet, Shimadzu LC-2010C HT, kolom C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm), komputer (merek Hp 3CR3160M7C), ultrasonikator Refsch, Tipe : T460 (Schwing 1 PXE, FTZ-Nr. C-066/83, HF-Frequ:35 kHz), timbangan semimicro SCALTEC (max 60/210 g, min 0,001 g), timbangan analitik OHAUS Pioneer (max 410 g, min 0,001 g), water
purification system Easy Pure II RF, timbangan ultramicro merek RADWAG® seri UYA 2.3 Y (max : 2,1 g, min 0,01 mg), mikropipet (Socorex), alat vakum GAST,
rotary shaker (Orbital shaker Optima S-762), waterbath, rotary evaporator (Buchi Rotavapor R-210), penyaring Whatman 0,45 µm, millipore, corong pisah dan
alat-alat gelas (Pyrex).
Bahan yang digunakan dalam penelitian ini adalah reference standard daidzein dengan kemurnian ≥ 98% (Aldrich), metanol gradient grade for LC (E.Merck), etanol technical grade, etil asetat technical grade, akuabidestilata hasil penyulingan di Laboratorium Kimia Analisis Instrumental Universitas Sanata Dharma, wound healing patch selulosa bakteri acetobacter xylinum yang dibuat menggunakan media ketela rambat (Gani 2013) dengan modifikasi penambahan ekstrak tempe (Yuliani et al. 2016).
3 Sistem Kromatografi
Sistem kromatografi yang digunakan untuk analisis penetapan kadar daidzein dalam wound healing patch ekstrak tempe merupakan sistem yang telah dioptimasi dan divalidasi dengan fase gerak metanol : akuabidestilata (70:30 v/v), kecepatan alir 0,8 mL/menit, deteksi pada panjang gelombang UV 248 nm, volume injeksi 10 µL, dengan kolom C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm).
Preparasi sampel
Wound healing patch ekstrak tempe berukuran seluas 4cm2 ditimbang kemudian dimasukkan ke dalam labu erlenmeyer. Sampel ditambahkan akuadestilata dan etanol sebanyak 50 mL dengan perbandingan (50:50) v/v (Wong 2018) lalu dimaserasi selama 24 jam pada suhu kamar dengan kecepatan 120 rpm (Mohite et al. 2014). Setelah 24 jam, larutan hasil maserasi diambil dan dilakukan penguapan etanol menggunakan rotary evaporator dengan suhu 50°C. Setelah etanol diuapkan, ditambahkan etil asetat sebanyak 25 mL lalu digojog dan dimasukkan corong pisah. Dilakukan ekstraksi cair-cair kemudian fraksi etil asetat diambil, sedangkan akuadestilata diekstraksi lagi dengan etil asetat 25 mL. Setelah tiga kali ekstraksi cair-cair, fraksi etil asetat yang didapat dicampur, kemudian diuapkan menggunakan waterbath pada suhu 50°C sampai kering.
Pembuatan fase gerak untuk HPLC
Fase gerak berupa metanol sebanyak 500 mL disaring menggunakan penyaring Whatman 0,45 µm dibantu dengan pompa vakum lalu didegassing selama 10 menit menggunakan ultrasonikator. Akuabidestilata sebanyak 500 mL disaring menggunakan penyaring Whatman 0,45 dibantu dengan pompa vakum, kemudian didegassing selama 10 menit menggunakan ultrasonikator.
Analisis Kualitatif Senyawa daidzein
Pelarut metanol, baku daidzein dan sampel hasil preparasi kemudian dimasukkan ke dalam tray lalu dilakukan penginjekan sebanyak 10 µL pada HPLC yang
4
digunakan yaitu kolom Phenomenex® C18, 250 x 4.6 mm dengan fase gerak metanol-akuabidestilata (70:30), laju alir 0,8 mL/min dan dideteksi pada panjang gelombang 248 nm
Pembuatan Larutan stok baku daidzein 200,0 µg/mL dan intermediet baku daidzein 20,0 µg/mL
Sebanyak 0,20 mg baku daidzein ditimbang seksama kurang lebih dan dilarutkan dalam metanol hingga 1,0 mL sehingga diperoleh konsentrasi 200,0 µg/mL. Kemudian diambil sebanyak 100 µL dari larutan stok 200,0 µg/mL lalu dilarutkan dalam metanol hingga 1,0 mL sehingga diperoleh konsentrasi 20,0 µg/mL.
Pembuatan kurva linieritas daidzein
Dibuat larutan seri baku 0,6; 1,2; 1,8; 2,4; 3,0; dan 3,6 µg/mL dengan mengambil masing-masing secara berurut 30; 60; 90; 120; 150; 180 µL dan ditambahkan metanol p.a hingga 1000 µL. Larutan seri baku daidzein masing-masing konsentrasi diinjeksikan sebanyak 10 µL pada reverse phase HPLC dan dideteksi pada panjang gelombang 248 nm. Diamati puncak kromatogram yang muncul dan AUC (area under curve) masing-masing puncak.
Pembuatan larutan sampel
Sampel kering hasil fraksi etil asetat dilarutkan menggunakan metanol p.a dan dipindahkan ke labu ukur 10 mL dan ditambahkan metanol hingga batas tanda. Setelah itu diambil sebanyak 0,1 mL dan dipindahkan ke mikrotube dan ditambahkan metanol p.a hingga 1,0 mL. Sampel kemudian disaring menggunakan
milipore dengan pori 0,2 µL lalu dipindahkan ke vial HPLC dan dilakukan degassing selama 10 menit.
Injeksi larutan sampel
Sampel hasil degassing tersebut kemudian dimasukkan ke dalam tray lalu dilakukan penginjekan sebanyak 10 µL pada reverse phase HPLC. Kondisi HPLC
5
yang digunakan yaitu kolom Phenomenex® C18, 250 x 4.6 mm dengan fase gerak metanol-akuabidestilata (70:30), laju alir 0,8 mL/min dan dideteksi pada panjang gelombang 248 nm. Penginjekan dilakukan replikasi sebanyak enam kali tiap sampel. Diamati puncak kromatogram yang muncul dan nilai AUC (Area Under
Curve) dari masing-masing puncak.
Analisis Hasil
Analisis kualilatif daidzein dengan cara membandingkan waktu retensi (tR) sampel terhadap baku. Analisis kuantitatif senyawa daidzein dengan penetapan kadar senyawa daidzein berdasarkan AUC (area under curve) dari baku. Dengan metode regresi linier, nilai konsentrasi (µg/mL) terhadap AUC diplotkan dari masing-masing seri larutan baku sehingga didapatkan persamaan y=bx+a (y = nilai AUC, x = konsentrasi senyawa, a = intersep, b = slope) dengan kriteria penerimaan yaitu koefisien korelasi (r) mendekati 1.
Nilai AUC sampel dimasukkan ke dalam persamaan regresi sebagai nilai y sehingga didapat kadar daidzein yang terukur dalam sampel. Hasil penetapan kadar
wound healing patch ekstrak tempe kemudian dihitung standar deviasi (SD) dan
standar deviasi relatif (RSD) untuk mengetahui metode hasil optimasi dan validasi dapat diaplikasikan untuk menetapkan kadar daidzein dalam ekstrak tempe yang diformulasi pada sediaan wound healing patch ekstrak tempe.
HASIL DAN PEMBAHASAN
Penetapan kadar daidzein dalam wound healing patch ekstrak tempe dapat dianalisis menggunakan metode reverse phase HPLC yang telah dioptimasi dan divalidasi (Deovita 2018, Wong 2018).
Pada tahap optimasi diperoleh kondisi optimum yaitu kolom C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm) fase gerak metanol : akuabidestilata dengan perbandingan 70:30 (v/v), kecepatan alir 0,8 mL/menit, detektor UV pada panjang gelombang maksimum 248 nm (Wong 2018).
Pada tahap validasi metode diperoleh bahwa metode reverse phase HPLC memenuhi parameter validasi meliputi selektivitas yang dilihat dari nilai resolusi
6
sebesar 1,929, linieritas dengan nilai koefisien korelasi (r) = 0,9982 dengan persamaan kurva baku y=22567,5x + 13048,4, nilai LOD sebesar 0,1733 dan LOQ 0,577. Nilai persen recovery metode yaitu 90-106% dan akurasi sebesar 2,0-4,9% serta persen recovery ekstraksi sebesar 83-89% (Deovita 2018).
Daidzein yang dianalisis dan ditetapkan kadarnya terdapat dalam matriks
wound healing patch yang dibuat berdasarkan metode Gani (2013) dengan
modifikasi penambahan ekstrak tempe dari Yuliani (2016). Sampel yang diperoleh terdiri dari sepuluh sampel wound healing patch ekstrak tempe. Kriteria yang harus dipenuhi yaitu representatif, yakni dapat mencerminkan populasi yang diwakilinya, dengan sepuluh patch dan dilakukan enam kali replikasi pengukuran diharapkan mampu memenuhi persyaratan tersebut.
Tabel I. Data Pengukuran Keseragaman Bobot Patch
Sampel Bobot patch (g) Rata-rata bobot patch (g) SD RSD (%) A 0,02289 0,02227 0,00049 2,19 B 0,02241 C 0,02314 D 0,02243 E 0,02182 F 0,02175 G 0,02173 H 0,02222 I 0,02189 J 0,02246
Keseragaman bobot dilakukan pada sepuluh sampel sebagai tahap awal identifikasi keseragaman kandungan daidzein pada wound healing patch ekstrak tempe. Dari hasil tersebut diketahui bahwa sampel satu dan lainnya berada pada rentang dengan nilai rata-rata (0,02227 ± 0,00049). Data penimbangan sepuluh sampel yang telah dilakukan, diketahui bahwa simpangan baku relatif yang dihasilkan sebesar 2,19%. Menurut Farmakope Indonesia V, keseragaman bobot sediaan patch dikatakan baik apabila bobot masing-masing sediaan patch memiliki
7
simpangan baku relatif ≤ 2%. Hal ini menunjukan bahwa dari sepuluh sampel
wound healing patch ekstrak tempe belum memiliki keseragaman bobot yang baik.
Uji kualitatif dilakukan untuk memastikan waktu retensi daidzein dengan melihat kromatogram yang dihasilkan oleh pelarut, baku daidzein dan sampel. Berdasarkan gambar 1 diketahui bahwa waktu retensi daidzein berada pada menit 5,25 dilihat dari adanya puncak baku daidzein pada gambar 1 (B) dan sampel pada gambar 1 (C).
Gambar 1. Gambaran kromatogram pelarut metanol (A), baku daidzein (B), sampel (C). Peak: Dz, Daidzein. Kolom C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm,
ukuran partikel 5 µm). Fase gerak metanol:akuabidestilata (70:30). Flow rate 0,8 mL/menit. Deteksi pada 248 nm.
Pembuatan kurva baku, bertujuan untuk memperoleh persamaan regresi linier yang selanjutnya akan digunakan untuk menghitung kadar daidzein dalam sampel wound healing patch ekstrak tempe. Persamaan regresi linier yang diperoleh
(A)
(B)
(C)
Dz
8
menyatakan hubungan linier antara konsentrasi (jumlah) analit pada beberapa seri baku dengan respon area under curve (AUC). Parameter yang dilihat untuk menentukan linieritas adalah koefisien korelasi (r) yang menyatakan korelasi antara jumlah analit dengan AUC yang dihasilkan.
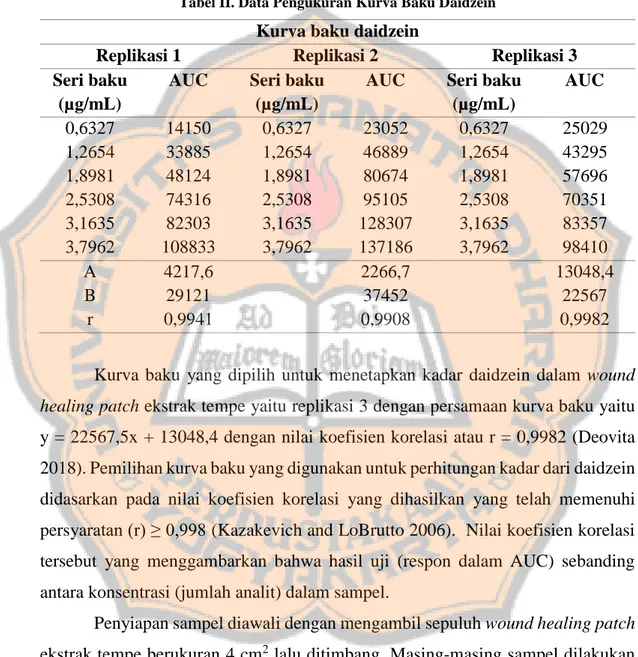
Tabel II. Data Pengukuran Kurva Baku Daidzein
Kurva baku daidzein
Replikasi 1 Replikasi 2 Replikasi 3
Seri baku (µg/mL)
AUC Seri baku (µg/mL)
AUC Seri baku (µg/mL) AUC 0,6327 1,2654 1,8981 2,5308 3,1635 3,7962 14150 33885 48124 74316 82303 108833 0,6327 1,2654 1,8981 2,5308 3,1635 3,7962 23052 46889 80674 95105 128307 137186 0,6327 1,2654 1,8981 2,5308 3,1635 3,7962 25029 43295 57696 70351 83357 98410 A B r 4217,6 29121 0,9941 2266,7 37452 0,9908 13048,4 22567 0,9982
Kurva baku yang dipilih untuk menetapkan kadar daidzein dalam wound
healing patch ekstrak tempe yaitu replikasi 3 dengan persamaan kurva baku yaitu
y = 22567,5x + 13048,4 dengan nilai koefisien korelasi atau r = 0,9982 (Deovita 2018). Pemilihan kurva baku yang digunakan untuk perhitungan kadar dari daidzein didasarkan pada nilai koefisien korelasi yang dihasilkan yang telah memenuhi persyaratan (r) ≥ 0,998 (Kazakevich and LoBrutto 2006). Nilai koefisien korelasi tersebut yang menggambarkan bahwa hasil uji (respon dalam AUC) sebanding antara konsentrasi (jumlah analit) dalam sampel.
Penyiapan sampel diawali dengan mengambil sepuluh wound healing patch ekstrak tempe berukuran 4 cm2 lalu ditimbang. Masing-masing sampel dilakukan proses ekstraksi dengan maserasi. Metode ekstraksi maserasi dipilih untuk mengekstrak isoflavon karena merupakan teknik sederhana dan mudah dalam pengaplikasiannya (Yatsu et al. 2016). Pelarut yang digunakan untuk maserasi merupakan hasil optimasi metode ekstraksi dengan kandungan daidzein terekstraksi paling banyak pada perbandingan etanol : akuadestilata 50:50 (v/v), kecepatan 120
9
rpm selama 24 jam pada suhu ruang (Wong 2018). Pemilihan pelarut tersebut berdasarkan pertimbangan bahwa senyawa aglikon banyak terlarut dalam etanol (Zhang et al. 2007) dan penggunaan akuadestilata dengan tujuan mengembangkan
wound healing patch ekstrak tempe sehingga daidzein yang terdapat dalam matriks
dapat keluar lalu terlarut di dalam etanol.
Ekstrak cair yang didapatkan kemudian dilakukan penguapan etanol menggunakan rotary evaporator berdasarkan prinsip pemisahan larutan berdasarkan perbedaan titik didih. Untuk memisahkan pelarut etanol : akuadestilata, digunakan suhu 50ºC. Adanya vakum menyumbangkan tekanan sehingga dapat mempercepat penguapan etanol.
Analit daidzein kemudian diambil dengan cara menambahkan etil asetat sebanding dengan jumlah akuadestilata yang terdapat dalam labu evaporasi. Digunakan etil asetat karena diketahui kelarutan senyawa daidzein lebih tinggi pada etil asetat dibandingkan pada air (Nan et al. 2014). Kemudian campuran akuadestilata dan etil asetat dimasukkan ke corong pisah, dilakukan ekstraksi cair-cair. Dilakukan tiga kali ekstraksi cair-cair agar senyawa daidzein dapat terekstraksi secara optimal. Diambil fraksi etil asetat kemudian dilakukan pengeringan. Sebelum diujikan, sampel dilarutkan dengan metanol karena daidzein memiliki kelaruan yang baik dalam metanol (Nan et al. 2014).
Tabel III. Data Pengukuran Kadar Rata-rata Daidzein dalam Sampel Wound healing patch ekstrak tempe
Sampel rata-rata kadar daidzein dalam patch (% b/b) X SD RSD (%) A 1,2918 1,3109 0,0509 3,88 B 1,3100 C 1,2550 D 1,2620 E 1,2820 F 1,3616 G 1,3340 H 1,3030 I 1,4240 J 1,2860
10
Penetapan kadar daidzein pada sepuluh sampel dengan masing-masing sampel replikasi enam kali menghasilkan kadar rata-rata sebesar (1,3109 ± 0,0509) (%b/b) dengan simpangan baku relatif sebesar 3,88%. Berdasarkan Farmakope Indonesia IV diketahui bahwa keseragaman kandungan sediaan transdermal diketahui memenuhi syarat jika simpangan baku relatif kurang dari atau sama dengan 6% (Dirjen POM 1995)
Pada hasil penetapan kadar diketahui bahwa simpangan baku relatif kurang dari 6%. Hal ini membuktikan bahwa metode yang dikembangkan memiliki keterulangan yang baik sehingga kadar daidzein yang diperoleh dapat diterima. Meskipun demikian, metode ekstraksi yang dilakukan masih perlu dikembangkan untuk mendapatkan jumlah daidzein yang lebih optimal (Deovita 2018).
KESIMPULAN DAN SARAN
Dari hasil penelitian yang diperoleh, dapat disimpulkan bahwa rata-rata kadar daidzein dalam sampel wound healing patch ekstrak tempe sebanyak (1,3109 ± 0,0509) (%b/b) dengan simpangan baku relatif sebesar 3,88%. Hasil ini sesuai dengan syarat dari Farmakope Indonesia IV bahwa sediaan transdermal dengan pengukuran sepuluh sampel nilai RSD yang dipersyaratkan ≤ 6%. Meskipun demikian perlu adanya optimasi proses perendaman, ekstraksi dan
wound healing patch ekstrak tempe untuk memperoleh kadar daidzein optimum
yang terukur.
UCAPAN TERIMA KASIH
Penelitian ini didanai penelitian PTUPT Ristek Dikti dengan nomor kontrak 020d/LPPM USD/ IV/ 2017.
11 DAFTAR PUSTAKA
Accorsi-Neto, A., Haidar, M., Simões, R., Simões, M., Soares-Jr, J., and Baracat, E., 2009. Effects of isoflavones on the skin of postmenopausal women: a pilot study. Clinics, 64 (6), 505–510.
Astuti, M., 2000. Tempe, a nutritious and healthy food from Indonesia. Asia Pacific
Journal of Clinical Nutrition, 9 (4), 322–325.
Bavia, A.C.F., Silva, C.E. da, Ferreira, M.P., Leite, R.S., Mandarino, J.M.G., and Carrão-panizzi, M.C., 2012. Chemical composition of tempeh from soybean cultivars specially developed for human consumption. Ciênc. Tecnol.
Aliment., Campinas, 32 (3), 613–620.
Boligon, A.A. and Linde, M.A., 2014. Importance of HPLC in Analysis of Plants Extracts. Austin Chromatography, 1 (3), 2–3.
Deovita, G.E., 2018. Validasi Metode Analisis Daidzein dalam Wound Healing
Patch Secara Reverse Phase High Performance Liquid Chromatography.
Sanata Dharma.
Direktorat Jendral Pengawasan Obat dan Makanan, 1995. Farmakope Indonesia. IV. Jakarta: Departemen Kesehatan Republik Indonesia.
Direktorat Jendral Pengawasan Obat dan Makanan, 2014. Farmakope Indonesia. V. Jakarta: Departemen Kesehatan Republik Indonesia.
Gani, M.R., 2013. Pengaruh Pemberian Sediaan Biomaterial Selulosa Bakteri
Acetobacter xylinum dari Limbah Ketela Rambat (Ipomoea batatas Poir) dengan Penambahan Chitosan Sebagai Material Penutup Luka Pada Tikus Galur Wistar Jantan. Universitas Sanata Dharma.
He, F.J. and Chen, J.Q., 2013. Consumption of soybean, soy foods, soy isoflavones and breast cancer incidence: Differences between Chinese women and women in Western countries and possible mechanisms. Food Science and Human
Wellness, 2 (3), 146–161.
Kazakevich, Y. and LoBrutto, R., 2006. HPLC for Pharmaceutical Scientists. HPLC for Pharmaceutical Scientists. New Jersey: John Wiley & Sons, Inc. Luthria, D.L., Biswas, R., and Natarajan, S., 2007. Comparison of extraction
solvents and techniques used for the assay of isoflavones from soybean. Food
Chemistry, 105 (1), 325–333.
Mohite, B.K., Suryawanshi, R.K., and Patil, S. V., 2014. Study on the Drug Loading and Release Potential of Bacterial Cellulose. Cellulose Chemistry and
Technology, 50 (2), 219–223.
Nan, G., Shi, J., Huang, Y., Sun, J., Lv, J., Yang, G., and Li, Y., 2014. Dissociation Constants and Solubilities of Daidzein and Genistein in Different Solvents.
Journal of Chemical & Engineering Data, 59 (4), 1304–1311.
Rostagno, M.A., Villares, A., Guillamón, E., García-lafuente, A., and Martínez, J.A., 2009. Sample preparation for the analysis of isoflavones from soybeans and soy foods. Journal of Chromatography A, 1216, 2–29.
Siddiqui, M.R., 2017. Analytical techniques in pharmaceutical analysis : A review.
Arabian Journal of Chemistry, 10, S1409–S1421.
Uyar, B., Sivrikoz, O., Ozdemir, U., Dasbasi, T., and Sacar, H., 2014. Histological investigation of the effect of soybean (Glycine max) extracts on the collagen layer and estrogen receptors in the skin of female rats. Clinics, 69 (12), 854–
12 861.
Wong, L., 2018. Optimasi Metode Analisis Daidzein dalam Wound Healing Patch
Secara Reverse Phase High Performance Liquid Chromatography. Sanata
Dharma.
Wong, M.C.Y., Emery, P.W., Preedy, V.R., and Wiseman, H., 2008. Review Health benefits of isoflavones in functional foods ? Proteomic and metabonomic advances. Inflammopharmacology, 16, 235–239.
Yang, H.J., Park, S., Pak, V., Chung, K.R., and Kwon, D.Y., 2010. Fermented
Soybean Products and Their Bioactive Compounds. Soybean and Health.
Korea: InTech.
Yatsu, F.K.J., Koester, L.S., and Bassani, V.L., 2016. Isoflavone-aglycone fraction from Glycine max : a promising raw material for isoflavone-based pharmaceutical or nutraceutical products. Revista Brasileira de Farmacognosia, 26 (2), 259–267.
Yu, J., Bi, X., Yu, B., and Chen, D., 2016. Isoflavones: Anti-inflammatory benefit and possible caveats. Nutrients, 8 (6), 1–16.
Yuliani, S.H., Istyastono, E.P., and Riswanto, F.D.O., 2016. The Cytotoxic Activity on T47D Breast Cancer Cell of Genistein-Standardized Ethanolic Extract of Tempeh - A Fermented Product of Soybean ( Glycine max ). Oriental Journal
of Chemistry, 32 (3), 1619–1624.
Zhang, E.J., Ng, K.M., and Luo, K.Q., 2007. Extraction and Purification of Isoflavones from Soybeans and Characterization of Their Estrogenic Activities. Journal of Agricultural and Food chemistry, 55, 6940–6950.
13 LAMPIRAN
14
Lampiran 2. Data Penimbangan Bobot Sampel Wound healing patch ekstrak tempe Sampel Bobot cawan (g) Bobot cawan + patch (g) Bobot Patch (g) Rata-rata (g) SD RSD (%) A 10,55449 10,57738 0,02289 0,022274 0,000487 2,18606 B 10,55537 10,57778 0,02314 C 16,53291 16,55605 0,02314 D 14,29649 14,31892 0,02243 E 13,23405 13,25587 0,02182 F 10,55509 10,57684 0,02175 G 16,53394 16,55567 0,02173 H 14,29736 14,31958 0,02222 I 16,53405 16,55594 0,02189 J 16,53384 16,55630 0,02246
15
Lampiran 3. Kromatogram Patch Tanpa Ekstrak Tempe Parameter HPLC
Kolom : C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm)
Fase gerak : metanol : akuabidestilata (70:30 v/v) Kecepatan : 0,8 mL/menit
Detektor UV : 248 nm Volume injeksi : 10 µL
16 Lampiran 4. Kromatogram Baku Daidzein Parameter HPLC
Kolom : C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm)
Fase gerak : metanol : akuabidestilata (70:30 v/v) Kecepatan : 0,8 mL/menit
Detektor UV : 248 nm Volume injeksi : 10 µL
17 Lampiran 5. Kromatogram Sampel Parameter HPLC
Kolom : C18 tipe Luna merek Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm)
Fase gerak : metanol : akuabidestilata (70:30 v/v) Kecepatan : 0,8 mL/menit
Detektor UV : 248 nm Volume injeksi : 10 µL Kromatogram sampel A
18 Kromatogram sampel C
19 Kromatogram sampel E
20 Kromatogram sampel G
21 Kromatogram sampel I
22
Lampiran 6. Perhitungan Kadar Daidzein Dalam Wound healing patch ekstrak tempe Kadar daidzein = 𝑘𝑎𝑑𝑎𝑟 𝑡𝑒𝑟𝑢𝑘𝑢𝑟 𝑥 𝑓𝑎𝑘𝑡𝑜𝑟 𝑝𝑒𝑛𝑔𝑒𝑛𝑐𝑒𝑟𝑎𝑛 𝑥 𝑣𝑜𝑙𝑢𝑚𝑒 𝑎𝑘ℎ𝑖𝑟 (𝑚𝐿) 𝑏𝑜𝑏𝑜𝑡 𝑝𝑎𝑡𝑐ℎ (𝑔) 𝑥100% y = bx + a y = 22567,5x + 13048,4 Sampel A 𝑥 =81492 − 13048,5 22567,5 = 3,03284 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =3,03284 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02289 𝑔 = 13249,6 µ𝑔 𝑔 ⁄ = 0,0132496 𝑔⁄ 𝑥100 = 1,32496 % 𝑏/𝑏 𝑔 Sampel B 𝑥 =82763 − 13048,5 22567,5 = 3,08916 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =3,08916 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02241 𝑔 = 13784,7 µ𝑔 𝑔 ⁄ = 0,0137847 𝑔⁄ 𝑥100 = 1,37847 % 𝑏/𝑏 𝑔 Sampel C 𝑥 =81714 − 13048,5 22567,5 = 3,04268 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =3,04268 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02314 𝑔 = 13149,0 µ𝑔 𝑔 ⁄ = 0,0131490 𝑔⁄ 𝑥100 = 1,31490 % 𝑏/𝑏 𝑔 Sampel D 𝑥 =78947 − 13048,5 22567,5 = 2,92007 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,92007 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02243 𝑔 = 13018,6 µ𝑔 𝑔 ⁄ = 0,0130186 𝑔⁄ 𝑥100 = 1,30186 % 𝑏/𝑏 𝑔 Sampel E 𝑥 =77937 − 13048,5 22567,5 = 2,87531 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,87531 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02182 𝑔 = 13177,4 µ𝑔 𝑔 ⁄ = 0,0131774 𝑔⁄ 𝑥100 = 1,31774 % 𝑏/𝑏 𝑔
23 Sampel F 𝑥 =80442 − 13048,5 22567,5 = 2,98631 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,98631 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02175 𝑔 = 13730,2 µ𝑔 𝑔 ⁄ = 0,0137302 𝑔⁄ 𝑥100 = 1,37302 % 𝑏/𝑏 𝑔 Sampel G 𝑥 =80526 − 13048,5 22567,5 = 2,99003 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,99003 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02173 𝑔 = 13759,9 µ𝑔 𝑔 ⁄ = 0,0137599 𝑔⁄ 𝑥100 = 1,37599 % 𝑏/𝑏 𝑔 Sampel H 𝑥 =80206 − 13048,5 22567,5 = 2,97585 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,97585 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02222 𝑔 = 13392,7 µ𝑔 𝑔 ⁄ = 0,0133927 𝑔⁄ 𝑥100 = 1,33927 % 𝑏/𝑏 𝑔 Sampel I 𝑥 =82662 − 13048,5 22567,5 = 3,08291 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =3,08291 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02189 𝑔 = 14083,6 µ𝑔 𝑔 ⁄ = 0,0140836 𝑔⁄ 𝑥100 = 1,40836 % 𝑏/𝑏 𝑔 Sampel J 𝑥 =79822 − 13048,5 22567,5 = 2,95884 µ𝑔 𝑚𝐿 ⁄ 𝑘𝑎𝑑𝑎𝑟 𝑑𝑎𝑖𝑑𝑧𝑒𝑖𝑛 =2,95884 µ𝑔 𝑚𝐿 ⁄ 𝑥 10 𝑥 10 𝑚𝐿 0,02246 𝑔 = 13173,8 µ𝑔 𝑔 ⁄ = 0,0131738 𝑔⁄ 𝑥100 = 1,31738 % 𝑏/𝑏 𝑔
24
Lampiran 7. Data Pengukuran Replikasi Sampel Wound healing patch ekstrak tempe
Sampel AUC Kons (µg/mL) Dalam 1 mL Dalam 10 mL Bobot daidzein (mg) Kons daidzein dalam patch (% b/b) Rata-rata SD RSD (%) A 75546 2,769363 27,694 276,936 0,277 1,210 1,2918 0,070 5,432 78725 2,910229 29,102 291,023 0,291 1,271 81492 3,032839 30,328 303,284 0,303 1,325 82825 3,091907 30,919 309,191 0,309 1,351 84182 3,152037 31,520 315,204 0,315 1,377 75898 2,784961 27,850 278,496 0,278 1,217 B 82763 3,089159 30,892 308,916 0,309 1,378 1,310 0,067 5,120 83571 3,124963 31,250 312,496 0,312 1,394 79861 2,960567 29,606 296,057 0,296 1,321 75965 2,78793 27,879 278,793 0,279 1,244 75520 2,768211 27,682 276,821 0,277 1,235 78053 2,880452 28,805 288,045 0,288 1,285 C 74337 2,71579 27,158 271,579 0,272 1,174 1,255 0,068 5,399 75712 2,776719 27,767 277,672 0,278 1,200 80742 2,999606 29,996 299,961 0,300 1,296 81714 3,042676 30,427 304,268 0,304 1,315 76370 2,805876 28,059 280,588 0,281 1,213 82704 3,086545 30,865 308,654 0,309 1,334 D 77977 2,877084 28,771 287,708 0,288 1,283 1,262 0,045 3,542 78886 2,917363 29,174 291,736 0,292 1,301 77390 2,851073 28,511 285,107 0,285 1,271 74946 2,742776 27,428 274,278 0,274 1,223 78947 2,920066 29,201 292,007 0,292 1,302 73401 2,674315 26,743 267,431 0,267 1,192 E 77686 2,86419 28,642 286,419 0,286 1,313 1,282 0,041 3,200 77937 2,875312 28,753 287,531 0,288 1,318 77870 2,872343 28,723 287,234 0,287 1,316 72873 2,650918 26,509 265,092 0,265 1,215 75199 2,753987 27,540 275,399 0,275 1,262 75623 2,772775 27,728 277,278 0,277 1,271
25 F 80442 2,986312 29,863 298,631 0,299 1,373 1,3616 0,077 5,635 83525 3,122925 31,229 312,292 0,312 1,436 72661 2,641524 26,415 264,152 0,264 1,214 81746 3,044094 30,441 304,409 0,304 1,400 79737 2,955073 29,551 295,507 0,296 1,359 81180 3,019014 30,190 301,901 0,302 1,388 80442 2,986312 29,863 298,631 0,299 1,373 G 76124 2,794975 27,950 279,498 0,279 1,286 1,334 0,067 5,005 77506 2,856214 28,562 285,621 0,286 1,314 80526 2,990034 29,900 299,003 0,299 1,376 79829 2,959149 29,591 295,915 0,296 1,362 82879 3,094299 30,943 309,430 0,309 1,424 73819 2,692837 26,928 269,284 0,269 1,239 H 79343 2,937614 29,376 293,761 0,294 1,322 1,303 0,036 2,732 78980 2,921529 29,215 292,153 0,292 1,315 78189 2,886478 28,865 288,648 0,289 1,299 78470 2,89893 28,989 289,893 0,290 1,305 75025 2,746277 27,463 274,628 0,275 1,236 80206 2,975855 29,759 297,585 0,298 1,339 I 83382 3,116588 31,166 311,659 0,312 1,424 1,424 0,017 1,210 82622 3,082911 30,829 308,291 0,308 1,408 84972 3,187043 31,870 318,704 0,319 1,456 82759 3,088982 30,890 308,898 0,309 1,411 83593 3,125938 31,259 312,594 0,313 1,428 83089 3,103605 31,036 310,360 0,310 1,418 J 80188 2,975057 29,751 297,506 0,298 1,325 1,286 0,042 3,253 76841 2,826746 28,267 282,675 0,283 1,259 79822 2,958839 29,588 295,884 0,296 1,317 74737 2,733515 27,335 273,352 0,273 1,217 78192 2,886611 28,866 288,661 0,289 1,285 79641 2,950819 29,508 295,082 0,295 1,314 Rata-rata 1,31094 SD 0,050876 RSD (%) 3,880851
26
BIOGRAFI PENULIS
Penulis skripsi dengan judul “Penetapan Kadar Daidzein dalam Wound Healing Patch dengan Metode Reverse
Phase High Performance Liquid Chromatography”
memiliki nama lengkap Maria Euphrasia Yolanda Mane. Penulis lahir di Bandung pada tanggal 15 Februari 1996, merupakan anak dari pasangan Fransiskus Mane dan Yustina Theresia Rona. Penulis mengawali pendidikannya di TK Santa Agnes (2000-2002), kemudian melanjutkan pendidikan di Sekolah Dasar Katolik Santa Ursula Ende (2002-2008), Sekolah Menengah Pertama Katolik Santa Ursula Ende (2008-2011), dan Sekolah Menengah Atas Katolik Syuradikara Ende (2011-2014). Penulis kemudian melanjutkan pendidikan sarjana di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada tahun 2014. Selama menjadi mahasiswa di Fakultas Farmasi Universitas Sanata Dharma, penulis aktif dalam kegiatan kepanitiaan yaitu sebagai anggota divisi Humas Pharmacy Performance (2016) dan divisi Humas Lomba Cerdas Cermat Kimia (2016) serta anggota divisi konsumsi seminar Jurnalistik (2016). Selain aktif dalam kegiatan kepanitiaan, penulis juga aktif sebagai tim Media Farmasi periode 2015/2016. Penulis juga pernah menjadi asisten praktikum Kimia Dasar periode 2016 dan asisten praktikum Kimia Analisis periode 2017.