BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Kacang Kedelai
Tanaman kedelai adalah tanaman yang merupakan salah satu sumber potensi pangan
yang tidak asing lagi bagi masyarakat Indonesia. Kedelai merupakan sumber protein yang paling
murah di dunia sebab berbagai varietas kedelai yang ada di Indonesia mempunyai kadar protein
30,53 - 44 %. Kedelai atau Glycine max (L) Merr termasuk familia Leguminoceae, sub famili
Papilionaceae, genus Glycine max, berasal dari jenis kedelai liar yang disebut Glycine unriensis
( Samsudin, 1985 ). Menurut Ketaren (1986), secara fisik setiap kedelai berbeda dalam hal
warna, ukuran dan komposisi kimianya. Perbedaan secara fisik dan kimia tersebut dipengaruhi
oleh varietas dan kondisi dimana kedelai tersebut dibudidayakan. Biji kedelai tersusun atas tiga
komponen utama, yaitu kulit biji, daging (kotiledon), dan hipokotil dengan perbandingan 8:90:2.
Sedangkan komposisi kimia kedelai adalah 40,5% protein, 20,5% lemak, 22,2% karbohidrat,
4,3% serat kasar, 4,5% abu, dan 6,6% air (Snyder dan Kwon, 1987).
Klasifikasi tanaman kedelai (Snyder dan Kwon, 2000) :
Kingdom : Plantae
Divisio : Spermatophyta
Sub Divisio : Angiospermae
Classis : Dicotyledoneae
Ordo : Rosales
Famili : Leguminosae
Genus : Glycine
Spesies : Glycine max (L.) Meril
Kedelai merupakan sumber gizi yang sangat penting. Menurut Astuti (2003) dalam Anonim
(2009), komposisi gizi kedelai bervariasi tergantung varietas yang dikembangkan dan juga warna
kulit maupun kotiledonnya. Kandungan protein dalam kedelai kuning bervariasi antara 31-48%
Gambar 2.1.Tanaman dan Biji Kedelai(Anonim,2009)
Kedelai dan produk turunannya, sebagai makanan fungsional, juga merupakan sumber
antioksidan yang unggul. Zat aktif pada kedelai yang memiliki aktivitas fisiologis terkuat sebagai
antioksidan adalah flavonoid. Isoflavon termasuk salah satu golongan flavonoid dalam tempe.
Kedelai utuh ataupun produk olahannya semuanya mengandung isoflavon-isoflavon tersebut.
Kedelai atau produk olahannya sangat bermanfaat untuk meningkatkan kapasitas antioksidan
alami yang tersedia di dalam tubuh. Studi laboratorium membuktikan bahwa asupan isoflavon
akan memacu peningkatan kadar superoksida dismutase (SOD) di dalam darah sehingga
aktivitasnya sebagai antioksidan enzimatis meningkat. SOD mampu mengubah radikal
superoksida yang reaktif menjadi molekul yang lemah. Kinerja ini sangat menguntungkan karena
radikal bebas superoksida merupakan radikal bebas ganas yang memiliki dampak luas sebagai
penyebab berbagai macam penyakit (anonim, 2013). Kedelai memiliki kandungan 8 asam amino
essensial yaitu isoleusin,leusin, lisin, treosin, valin, metionin, fenilalanin, dan triptofan dengan
asam amino pembatas metionin dan sistein. Kandungan asam amino yang cukup tinggi pada
kedelai ada pada lisin dan treonin.
Minyak sayur (minyak kedelai, minyak kacang, minyak biji bunga matahari) memiliki
lemak tak jenuh ganda (PUFA) yang banyak mengandung asam linoleat dan arakhidonat yang
sangat bermanfaat bagi tubuh, tetapi memiliki potensi penyebab kanker jika minyak tersebut
teroksidasi. Oleh karena itu, jika sering mengkonsumsi makanan gorengan maka produk
gorengan yang dikonsumsi sebaiknya mengandung isoflavon, yaitu olahan kedelai, seperti tahu,
tempe, sari kedelai, miso, dan sebagainya. Jadi peningkatan risiko terhadap kanker dari asam
ini sangat dipengaruhi oleh isoflavon kedelai dalam menghambat radikal bebas penyebab stres
oksidatif. Penurunan stres oksidatif memberi pengaruh positif pada penurunan risiko terhadap
kanker.
Antosianin kulit kedelai mampu menghambat oksidasi LDL kolesterol yang merupakan
awal terbentuknya plak dalam pembuluh darah yang akan memicu berkembangnya penyakit
tekanan darah tinggi dan berkembangnya penyakit jantung koroner.
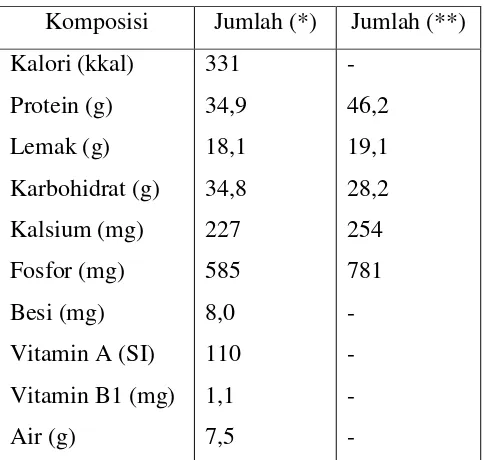
Tabel 2.1. Komposisi kimiawi kedelai kering per 100 gr dapat dilihat pada table di bawah ini:
Sumber : * Direktorat Gizi Depkes RI. (1972) dalam Koswara (1992)** Sutomo (2008).
Dari Tabel di atas dapat diketahui bahwa kandungan protein dan lemak kedelai menurut
Sutomo (2008) lebih tinggi daripada menurut Koswara (1992).
Selain keunggulan tersebut, ternyata kedelai juga mempunyai kelemahan-kelemahan.
Kedelai mengandung senyawa anti gizi seperti antitripsin, asam fitat dan oligosakarida penyebab
flatulensi (gas dalam perut). Kedelai mentah mengandung enzim-enzim dan senyawa-senyawa
yang dapat mengganggu pencernaan serta menyebabkan rasa pahit dan bau langu. Bau langu
membuat kedelai sulit untuk dikembangkan menjadi produk makanan kecuali tempe
Antitripsin adalah salah satu jenis protein yang menghambat kerja enzim tripsin didalam
tubuh. Senyawa ini secara alami banyak terdapat dalam kacang-kacangan terutama kacang
kedelai. Asam fitat merupakan sumber utama unsur fosfor dalam kacang-kacangan. Tetapi,
senyawa ini tidak dapat dicerna sehingga posfor dalam asam fitat tidak dapat digunakan tubuh.
Asam fitat termasuk kedalam senyawa anti gizi karena dapat mengkelat (mengikat) elemen
mineral terutama seng, kalsium, magnesium dan besi sehingga akan mengurangi ketersediaan
mineral- mineral tersebut secara biologis. Oligosakarida adalah jenis karbohidrat yang
merupakan polimer dari dua smapai sepuluh monosakarida. Oligosakarida yang mengandung
ikatan alfa-galaktrosida berhubungan dengan timbulnya flatulensi, yaitu menumpuknya gas-gas
dalam perut.
2.2. Tempe
Tempe adalah produk fermentasi yang amat dikenal oleh masyarakat Indonesia terutama
di Jawa (Kasmidjo,1990). Tempe terbuat dari kedelai rebus yang difermentasi oleh jamur
Rhizopus. Selama fermentasi, biji-biji kedelai terperangkap dalam rajutan miselia jamur membentuk padatan yang kompak berwarna putih (Steinkraus, 1960). Di Indonesia, tempe
dikonsumsi oleh hampir semua tingkatan masyarakat hampir di seluruh Indonesia terutama di
Jawa dan Bali. Penyajian kedelai menjadi tempe adalah unik dibandingkan dengan berbagai
bentuk penyajian sebagai pangan yang lain. Keunikan tersebut ialah karena sebagai tempe,
kedelai dikonsumsi utuh, berbeda dengan tahu atau susu kedelai misalnya, yang dikonsumsi
hanya sebagai ekstrak protein saja (Kasmidjo, 1990).
Tempe merupakan makanan hasil fermentasi tradisional berbahan baku kedelai dengan
bantuan jamur Rhizopus oligosporus. Mempunyai ciri-ciri berwarna putih, tekstur kompak dan flavor spesifik. Warna putih disebabkan adanya miselia jamur yang tumbuh pada permukaan biji
kedelai. Tekstur yang kompak juga disebabkan oleh miselia-miselia jamur yang menghubungkan
antara biji-biji kedelai tersebut. Terjadinya degradasi komponen-komponen dalam kedelai dapat
menyebabkan terbentuknya flavor spesifik setelah fermentasi (Kasmidjo, 1990). Cahyadi (2006),
melaporkan bahwa dalam tempe, kadar nitrogen kadarnya sedikit bertambah, kadar abu
Ragi umumnya digunakan dalam industri makanan untuk membuat makanan dan
minuman hasil fermentasi seperti acar, tempe, roti dan bir. Mikroorganisme yang digunakan di
dalam ragi terdiri atas kapang golongan Rhizopus (Rahman dkk., 2011).Secara tradisional
masyarakat Indonesia membuat ragi tempe dengan menggunakantempe yang sudah jadi. Tempe
tersebut diiris tipis-tipis, dikeringkan dengan oven pada suhu 400C-450C atau dijemur sampai
kering, digiling menjadi bubuk halus dan hasilnya digunakan sebagai ragi bubuk. Ragi tempe
memegang peranan penting dalam pembuatan tempe karena dapat mempengaruhi kualitas tempe
yang dihasilkan. Jenis kapang yang memegang peranan utama dalam pembuatan tempe adalah
Rhizopus oligosporus dan R.oryzae, sedangkan jenis kapang lain yang juga terdapat adalah R. stoloniferus dan R. Arrhizus (Suprapti, 2003).
Salah satu faktor yang penting dalam terjadinya perubahan selama perendaman adalah
terbebasnya senyawa-senyawa isoflavon dalam bentuk bebas (aglikon), dan teristimewa hadirnya
Faktor-II (6,7,4’ tri-hidroksi isoflavon), yang terdapat pada tempe tetapi tidak terdapat pada
kedelai, ternyata berpotensi tinggi (dibandingkan dengan isoflavon lainnya) sebagai antioksidan
(Gyorgy, 1964).
Enzim adalah katalis hayati substansi organik yang dihasilkan sel-sel hidup dalam jumlah yang
kecil. Namun dalam jumlah yang sedikitpun, enzim mampu mempercepat berlangsungnya suatu
reaksi kimia. Sintesis enzim oleh rhizopus sp, merupakan aspek yang sangat penting dalam fermentasi kedelai menjadi tempe. Selama masa inkubasi, molekul-molekul besar dan komples,
seperti protein, karbohidrat dan lemak dipecah menjadi komponen-komponen kecil.
Salah satu spesies kapang rhizopus oligosporus memegang peranan penting, karena aktivitas protease dan lipasenya tinggi. Rasa kembung yang biasa diderita setelah mengkonsumsi
kedelai tidak dirasakan oleh konsumen tempe. Manfaat lain yang dapat diperoleh melalui
fermentasi tempe lebih dinikmati cita rasanya dibandingkan dengan kedelai rebus. Berbagai
perubahan yang menguntungkan tersebut disebabkan oleh serangkaian enzimatis yang antara
lain melibatkan protease, karbohidrase, dan lipase.
Enzim β-glikosidase berperan dalam pemecahan isoflovon glukosida dalam kedelai menjadi aglikonnya selama fermentasi berlangsung. (Wade, 1992) menuliskan bahwa kemampuan khusus yang dimiliki β-glikosidase memutuskan ikatan β-1,4 glikosidik seperti yang terdapat pada isoflavon glikosida. (Ebata dkk 1972) menyatakan bahwa salah satu kapang
penghasil β- glukosidase adalah rhizopus sp. Fakta ini berhasil dideteksi keberadaan genistein setelah genistein dan di campur dengan “crude enzim” dari fraksi cair pertumbuhan rhizopus oligosporus. Selanjutnya (Wuryani 1992) juga melaporkan kemampuan rhizopus oligosporus
dan rhizopus oryzae dalam memecah ikatan glikosidik pada berbagai senyawa isoflavon yang terkonjugasi dengan gula menjadi turunannya yang berbentuk aglikon. Besarnya perubahan yang
terjadi sangat dipengaruhi oleh enzim yang dihasilkan kapang. Dalam upaya menghasilkan
makanan fungsional yang akan senyawa aktif isoflavon aglin diperlukan rhizopus sp.
2.3. Flavonoid
Flavonoid termasuk senyawa fenolik alam yang potensial sebagai antioksidan dan
mempunyai bioaktifitas sebagai obat. Flavonoid dalam tubuh manusia berfungsi sebagai
antioksidan sehingga sangat baik untuk pencegahan kanker. Ada beberapa jenis senyawa
flavonoid salah satunya isoflavon. Isoflavon merupakan isomer dari flavon dimana pada senyawa
Gambar 2.3 Struktur Senyawa Flavonoida
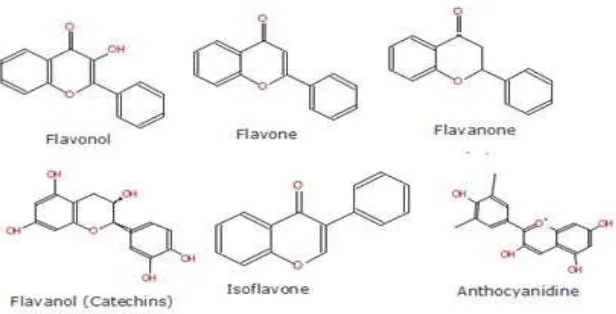
Beberapa jenis favonoida :
Gambar 2.4 Beberapa jenis struktur senyawa flavonoida
Isoflavon merupakan senyawa flavonoid yang merupakan salah satu anggota senyawa
fitoestrogen.Isoflavon merupakan salah satu kelompok fitoestrogen yaitu komponen bahan alam
yang banyak terdapat dalam kedelai maupun produk olahannya.Winarsi (2003) melaporkan
bahwa senyawa fitoestrogen dalam kedelai, dapat berperan sebagai antioksidan yang mampu
mencegah terjadinya reaksi oksidasi yang ditunjukkan melalui peningkatan status antioksidan
enzimatis. Bila terjadi reaksi oksidasi, maka isoflavon mampu menangkap senyawa radikal dan
mengubahnya menjadi senyawa stabil yang tidak berbahaya, isoflavon tidak akan menimbulkan
bahaya bagi orang yang mengkomsumsinya. Namun demikian direkomendasikan oleh Nagata
(1998) untuk mengkomsumsi isoflavon kedelai sebanyak 50- 100 mg / hari, bahkan sampai 150
mg / hari masih dapat ditoleransi. Kandungan isoflavon tertinggi terdapat pada produk kedelai
yang difermentasi, seperti tempe. Di dalam 1 gram protein kedelai, kira-kira mengandung 3,5 mg
isoflavon. Oleh sebab itu dengan mengetahui kandungan protein tempe atau olahan kedelai
2.4. Radikal Bebas
Radikal bebas adalah atom atau molekul yang tidak stabil dan sangat reaktif karena mengandung
satu atau lebih elektron tidak berpasangan pada orbital terluarnya. Untuk mencapai kestabilan
atom atau molekul, radikal bebas akan bereaksi dengan molekul disekitarnya untuk memperoleh
pasangan elektron. Reaksi ini akan berlangsung terus-menerus dalam tubuh dan bila tidak
dihentikan akan menimbulkan berbagai penyakit seperti kanker, jantung, katarak, penuaan dini,
serta penyakit degeneratif lainnya. Oleh karena itu tubuh memerlukan suatu substansi penting
yaitu antioksidan yang mampu menangkap radikal bebas tersebut sehingga tidak dapat
menginduksi suatu penyakit (Kikuzaki, 2002; Sibuea, 2003).
Radikal bebas tersebut dapat mengoksidasi asam nukleat, protein, lemak, bahkan DNA
sel dan menginisiasi timbulnya penyakit degeneratif (Leong dan Shui, 2001). Di dalam tubuh
kita terdapat senyawa yang disebut antioksidan yaitu senyawa yang dapat menetralkan radikal
bebas, seperti: enzim SOD (Superoksida Dismutase), gluthatione, dan katalase. Antioksidan juga
dapat diperoleh dari asupan makanan yang banyak mengandung vitamin C, vitamin E dan
betakaroten serta senyawa fenolik. Bahan pangan yang dapat menjadi sumber antioksidan alami,
seperti rempah-rempah, coklat, biji-bijian, buah-buahan, sayur-sayuran seperti buah tomat,
pepaya, jeruk dan sebagainya (Prakash, 2001; Trevor, 1995).
Keseimbangan antara kandungan antioksidan dan radikal bebas di dalam tubuh
merupakan salah satu faktor yang mempengaruhi kesehatan tubuh. Apabila jumlah radikal bebas
terus bertambah sedangkan antioksidan endogen jumlahnya tetap, maka kelebihan radikal bebas
tidak dapat dinetralkan. Akibatnya radikal bebas akan bereaksi dengan komponen sel dan
menimbulkan kerusakan sel (Arnelia 2002). Radikal bebas adalahmerupakan atom atau gugus
atom apa saja yang memiliki satu atau lebih elektron tak berpasangan. Karena jumlah elektron
ganjil, maka tidak semua elektron dapat berpasangan sehingga bersifat sangat reaktif. Jika
jumlahnya sedikit, radikal bebas dapat dinetralkan oleh sistem enzimatik tubuh, namun jika
berlebih akan memicu efek patologis Radikal bebas merupakan merupakan agen pengoksidasi
kuat yang dapat merusak sistem pertahanan tubuh dengan akibat kerusakan sel dan penuaan dini
biologi, Protein lipida dan DNA dari sel manusia yang sehat lah merupakan sumber pasangan
elektron yang baik(Kosasih, 2004).
Dampak reaktifitas senyawa radikal bebas bermacam-macam, mulai dari kerusakan sel
atau jaringan, penyakit autoimun, penyakit degeneratif seperti kanker, asterosklerosis, penyakit
jantung koroner (PJK), dan diabetes mellitus.Pembentukan radika bebas dan reaksi oksidasi pada
biomolekul akan berlangsung sepanjang hidup. Radikal bebas yang sangat berbahaya dalam
makhluk hidup anatar lain adalag golongan hidroksil (OH-) , superoksida (O-2), nitrogen
monooksida (NO), peroksidal (RO-2) , peroksinitrit (ONOO-), asam hipoklorit (HOCl), hidrogen
peroksida (H2O2) (Silalahi, 2006).
2.5. Antioksidan
2.5.1. Pengertian Antioksidan
Antioksidan merupakan senyawa pemberi elektron (elektron donor) atau reduktan. Senyawa ini
memiliki berat molekul kecil, tetapi mampu mengaktivasi berkembangnya reaksi oksidasi,
dengan cara mencegah terbentuknya radikal.Antioksidan dapat diperoleh,
1. Dari luar tubuh (eksogen) dengan cara melalui makanan dan miuman
yangmengandungvitamin C, E atau betakaroten.
2. Dari dalam tubuh (endogen) yakni dengan enzim superoksidan dismutasi (SOD),
gluthatione, perxidasi dan katalase yang diperoduksi oleh tunuh sebagai antioksidan (
Kosasih, 2004).
Tubuh manusia tidak mempunyai cadangan antioksidan dalam jumlah berlebih, sehingga
jika terjadi paparan radikal berlebih maka tubuh membutuhkan antioksidan eksogen. Adanya
kekhawatiran akan kemungkinan efek samping yang belum diketahui dari antioksidan sintetik
menyebabkan antioksidan alami alternatif yang sangat dibutuhkan (Sunarni, 2005). Senyawa
antioksidan memengang peranan penting dalam pertahanan tubuh terhadap perubahan buruk
yang disebabkan radikal bebas. Radikal bebas diketahui dapat menginduksi penyakit kanker,
arteriosklerosis dan penuaan, disebabkan oleh kerusakan jaringan karena oksidasi.
Berkaitan dengan fungsinya, senyawa antioksidan diklasifikasikan dalam tiga tipe antioksidan,
yaitu :
1. Antioksidan Primer
Termasuk:
•SOD (Superoxide Dismutase) •GPX (Glutathion Perokxide)
•Metalbinding protein seperti Ferrtin atau Ceruloplasmin.
Antioksidan primer ini bekerja untuk mencegah terbentuknya senyawa radikal bebas yang ada
menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi.
Contoh antioksidan ini adalah enzim SOD yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas.
2. Antioksidan Sekunder
Antioksidan ini berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai.
Contoh: antioksidan sekunder: vitamin E, vitamin C, betakaroten, asam urat, bilirubin dan
albumin.
3. Antioksidan Tersier
Antioksidan jenis ini memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal
bebas.Contoh enzim yang memperbaiki DNA pada inti sel adalah mentionin sulfoksidan reduktase.Adanya enzim-enzim perbaikan DNA ini berguna untuk mencegah penyakit misalnya kanker (Kosasih, 2004).
Antioksidan digunakan untuk melindungi komponen makanan yang bersifat tidak jenuh
(memiliki ikatan rangkap), terutama lemak dan minyak. Mekanisme kerja antioksidan secara
umum adalah menghambat oksidasi lemak. Tahapannya menurut Counsell dan Hornig (1981)
adalah
I. Inisiasi
RH + initiator R• II. Propagasi
R• + RH ROOH + R•
III. Terminasi
R• + R• RR
ROO• + R• ROOH + R•
Antioksidan sintetik adalah antioksidan yang diperoleh dari hasil sintesis reaksi kimia. Senyawa
fenol sintetis seperti Butil hidroksianisol (BHA) dan Butil hidroksitoluen (BHT) bukan
antioksidan yang baik, sebab pada pemaparan yang lama dapat menyebabkan efek negatif
terhadap kesehatan serta meningkatkan terjadinya karsinogenesis (Rohman , 2007). Antioksidan alami adalah antioksidan hasil ekstraksi bahan alam. Antioksidan alami seperti α - tokoferol dan asam askorbat, memiliki efek samping merugikan yang lebih kecil, tetapi aktivitasnya lebih
tinggi daripada antioksidan sintetik .
Beberapa contoh antioksidan sintetik yang diijinkan penggunaanya untuk makanan dan
penggunaannya telah sering digunakan, yaitu butil hidroksi anisol (BHA), butil hidroksi toluen
(BHT), propil galat (PG), tert-butil hidoksi quinon (TBHQ) dan tokoferol. Antioksidan -
antioksidan tersebut merupakan antioksidan alami yang telah diproduksi secara sintetis untuk
tujuan komersial. Senyawa antioksidan yang diisolasi dari sumber alami dan ditambahkan ke
makanan sebagai bahan tambahan pangan (Pratt dkk, 1992).
Senyawa antioksidan yang diisolasi dari sumber alami adalah yang berasal dari tumbuhan
yaitu tokoferol, vitamin C, betakaroten, flavonoid,dan senyawa fenolik. Isolasi antioksidan alami
telah dilakukan dari tumbuhan yang dapat dimakan, tetapi tidak selalu dari bagian yang dapat
dimakan. Antioksidan alami tersebar di beberapa bagian tanaman, seperti pada kayu, kulit kayu,
akar, daun, buah, bunga, biji dan serbuk sari (Pratt dkk, 1992).
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik atau polifenolik
yang dapat berupa golongan flavonoid, turunan asam sinamat, kumarin, tokoferol dan asam-asam
flavonol, isoflavon, kateksin, flavonol dan kalkon. Sementara turunan asam sinamat meliputi
asam kafeat, asam ferulat, asam klorogenat, dan lain-lain.
Komponen fenolik merupakan kelompok molekul yang besar dan beragam, yang terdiri
dari golongan aromatik pada metabolit sekunder tumbuh-tumbuhan.Fenolik dapat
diklasifikasikan ke dalam komponen yang tidak larut seperti lignin dan komponen yang larut
seperti asam fenolik, phenylpropanoids, flavonoid dan kuinon.Setiap tumbuh-tumbuhan
memiliki struktur komponen fenolik yang berbeda.Ada komponen fenolik yang memliki gugus –
OH banyak dan ada pula komponen fenolik yang memiliki gugus –OH yang sedikit. Gugus –OH
berperan dalam proses transfer elektron untuk menstabilkan dan meredam radikal bebas
(Harborne dan Williams 2000).
2.6. Metode Pengukuran Aktivitas Antioksidan
Pengukuran aktivitas antioksidan dilakukan dengan tiga metode yaitu:
1. Metode DPPH (1,1-diphenyl-2-picryl-hydrazil)
Pengukuran aktivitas antioksidan dapat dilakukan dengan beberapa cara. Salah satu metode
pengukan yang sering digunakan adalah metode DPPH. DPPH adalah ( 1,1-diphenyl-1-picryl-hydrazil) yang merupakan suatu radikal bebas yang stabil karena mekanisme delokalisasi elektron bebas oleh molekulnya, sehingga molekul ini tidak mengalami reaksi dimerisasi yang
sering terjadi pada sebahagian besar radikal bebas lainnya. Delokalisasi juga memberi efek
warna ungu yang dalam panjang gelombang 515 nm dalam pelarut etanol (Hirota dkk, 2003).Zat
ini berperan sebagai penangkap elektron atau penengkap radikal hidrogen bebas.Hasilnya adalah
molekul yang bersifat stabil. Jika suatu senyawa antioksidan direaksikan dengan zat ini maka
senyawa antioksidan tersebut akan menetralkan radikal bebas dari DPPH (Bintang, 2002).
Berikut ini dapat dilihat resonansi DPPH dan reaksi DPPH dengan atom H netral yang berasal
N N NO2 +
2.5.Struktur kestabilan radikal bebas DPPH (Ionita, 2003)
Pengukuran aktivitas antioksidan dilakukan dengan inkubasi DPPH dengan ekstrak
antioksidan selama 30 menit sehingga menghasilkan larutan ungu yang lebih pudar kemudian
dilakukan pengukuran panjang gelombang 515 nm. Aktivitas antioksidan diperoleh dari nilai
absorbansi yang selanjutnya akan digunakan untuk menghitung persentase inhibis 50% (IC50)
yang menyatakan konsentrasi senyawa antioksidan yang menyebabkan 50% dari DPPH
kehilangan karakter radikal bebasnya. Semakin tinggi kadar senyawa antioksidan dalam sampel
maka akan semakin rendah nilai IC50 (Mosquera, 2007).
Ketika larutan DPPH dicampurkan dengan bahan yang dapat memberi sebuah atom
hidrogen, molekul DPPH akan tereduksi sehingga intensitas warna ungu akan berkurang
(Molyneux,2004)
2. Metode FRAP (Ferric Reducting Antioxidant Power)
Metode FRAP (Benzie & Stain, 1996) mengunakan Fe (TPTZ)23+ kompleks besi-ligan
2,4,6-tripiridil-triazin sebagai pereaksi. Kompleks biru Fe (TPTZ)23+ akan berfungsi sebagai zat
pengoksidasi dan akan mengalami reduksi menjadi Fe (TPTZ)22+ yang berwarna kuning dengan
reaksi sebagai berikut:
Fe (TPTZ)23+ + AROH Fe (TPTZ)22+ + H+ + AR = O
3. Metode Cuprac ( Cupric Ion Reducting Antioxidant Capacity)
Metode Cuprac (Apak et al, 2007) menggunakan bis (neokuproin) tembaga (II) Cu(Nc)22+
sebagai pereaksi kromogenik. Pereaksi Cu(Nc)22+ yang berwarna kuning dengan reaksi :
Pada uji antioksidan dari ekstrak kacang kedelai dan tempe dengan metode DPPH diperlukan
pengukuran absorbansi dari ekstrak sampel tersebut dengan menggunakan spektrofotometri
UV-Vis . Metode spektrofotometri adalah metode analisis kuantitatif suatu analit dalam sampel yang
didasarkan pada adanya interaksi analit dengan energy radiasi berupa foton yang menyebabkan
eksitasi electron (transisi electron) pada analit. Misalkan analit penyerap foton adalah M dan
analit yang mengalami eksitasi electron adalah M*.
M + E —› M*
Analit dalam keadaan eksitasi (bertahan sekitar 10-8 – 10-9 detik ) akan mengalami relaksasi
secara fluoresensi atau fosforensi sebagai akibat dari reaksi fitokimia dalam analit dan segera
kembali ke keadaan dasar ( ground state) sambil melepaskan sejumlah kalor.
M* + E —› M + Kalor
Sesuai dengan persamaan Planck ( E=h.v = h. c / λ), setiap analit yang dapat menyerap / mengemisi foton memiliki panjang gelombang (λ) tertentu.
Interaksi foton dengan sesuai analit akan menghasilkan warna-warna pada cahaya tampak
oleh mata dengan panjang gelombang 4000 nm hingga 700 nm. Warna yang dihasilkan pada
cahaya tampak tersebut, merupakan pasangan dari setiap dua warna ( warna dan warna
komplementer) spectrum.
Tabel 2.2 Warna yang dihasilkan pada Cahaya Tampak
λ(nm) Warna Warna komplementer
a. Sumber Energi Radiasi
Sumber energi radiasi berisi material yang dapat tereksitasi ke tingkat energy yang lebih tinggi
oleh pengaruh voltase arus listrik yang tinggi. Bila material kembali ke tingkat energi yang lebih
rendah (keadaan dasar), akan mengemisikan sejumlah foton yang sesuai dengan perbedaan
energy keadaan tereksitasi dengan keadaan dasar. Sumber radiasi yang cocok dalam hal
pengukuran serapan adalah sumber radiasi yang memiliki spectra kontiniu, intensitas sama pada
rentangan panjang gelombang. Sumber radiasi pada daerah UV (180-350) nm dapat digunakan ;
lampu deuterium, lampu hydrogen dan lampu pengawa muatan xenon. Pada daerah tampak,
lampu yang biasa digunakan adalah lampu filament yang menghasilkan spectra kontiniu antara
350-2500 nm.
b. Monokromator
Untuk memecahkan radiasi polikromatik tersebut menjadi monokromatik digunakan filter dan
monokromator, agar panjang gelombang sesuai dengan panjang gelombang sample yang
diamati. Filter tersebut dari bahan khusus yang membolehkan transmitansi radiasi pada batas
panjang gelombang yang diamati, dengan lebar pita efektif berkisar: 20-25 nm. Monokromator
terdiri dari ; celahmasuk radiasi polikromatik, lensa/cermin ( pengumpul radiasi ),
prisma/grating ( pemecah panjang gelombang ), lensa/cermin ( penyatu radiasi ) dan celah keluar. Lehercelah masuk/ celah keluar akan mempengaruhi lebar pita radiasi. Celah yang sempit
akan menghasilkan pita yang sempit, akan tetapi intensitas yang mencapai detector akan
menurun. Minimum lebar pita sempit, akan tetapi akan intensitas yang mencapai detector akan
menurun. Minimum lebar pita sangat ditentukan oleh sensitivitas detector.
c. Kontainer Sampel ( kuvet )
Kontainer sampel ( kuvet ) dibentuk dari material yang dapat melewatkan energy radiasi pada
panjang gelombang daerah kerja. Kuvet yang terbuat dari kuartz atau silica biasanya digunakan
pada daerah kerja UV (< 350 nm ), kuvet gelas silikat dapat digunakan pada daerah kerja antara
350-2000 nm, sedang kuvet yang terbuat dari plastic dapat digunakan pada daerah tampak.
Untuk daerah kerja kuvet dan tampak, kuvet yang biasa digunakan adalah kuvet dengan panjang
celah ( ketebalan medium larutan ) yang akan dianalisis 1 cm. pada saat kuvet akan dipakai harus
kuvet dapat dilakukan dengan menggunakan kain halus dan tidak boleh dimasukan kedalam oven
sebab menyebabkan perubahan pada perubahan pada panjang kuvet. Kalibrasi kuvet dengan
larutan blanko harus dilakukan sebelum analisis larutan sampel.
d. Detektor
Detektor dapat menyerap energy foton baik yang berasal dari arus listrik maupun perubahan
panas. Sinyal yang ditunjukkan oleh detector yang diakibatkan oleh arus listrik atau perubahan
panas tanpa sampel tersebut : bisingan ( noise ). Sinyal yang dihasilkan dianggap sebagai sinyal
latar (background signal). Detector fotolistrik dibedakan atas : tabung foton ( phototube) dan sel
photovoltaic. Arus pada tabung foton kira-kira 10-11 A, perlu digandakan untuk dapat dibaca.
Agar sinyal elektronik dari detector dapat diukur, sinyal perlu digandakan beberapa kali dengan
menggunakan amplifier. Guna penyimpanan data, biasanya detector dilengkapi dengan
komputer.
e. Sistem pembacaan ( Readout )
Proses penterjemahan sinyal elektronik yang dihasilkan dari detector radiasi menjadi bentuk data
eksperimen dilakukan didalam system pembacaan yang terdiri dari: amplifier ammeter,